نمک چیست؟ – خواص + انواع نمک – به زبان ساده
«نمک» (Salt) در شیمی ترکیبی یونی است که از رسوبات سنگی و آب دریا استخراج میشود. نمک خوراکی یا سدیم کلرید رایجترین نوع نمک در میان انواع نمک است. نمکها یکی فراوردهای واکنش خنثیسازی اسیدها و بازها هستند. با مطالعه این مطلب خواهید آموخت که نمک چیست و چگونه تشکیل میشود. برای آشنایی بیشتر انواع نمک و کابردهای آن نیز در ادامه آورده شده است.


نمک چیست ؟
بدون دانستن دانش شیمی نیز بسیاری از مردم میتوانند تعریف خوبی از نمک داشته باشند. شیمیِ نمک نشان میدهد که این ماده از ترکیبات یونی است. یونها توسط پیوندهای یونی به یکدیگر متصل شدهاند. نمک خوراکی یا سدیم کلرید شناخته شدهترین نوع نمک است که کاربردهای زیادی در آشپزی و همچنین صنعت دارد که در پوسته زمین به فراوانی یافت میشود. در زیر برخی دیگر از نمکها پرکاربرد به همراه ویژگی و موارد استفاده آنها، فهرست شده است.
- پتاسیم دیکرومات : ترکیبی بسیار سمی، قابل اشتعال و سرطانزا است و بیشتر برای ساخت محلولهای تمیزکننده قوی استفاده میشود.
- کلسیم کلرید : جذب کننده بسیار خوب آب است و در زمستان برای یخزدایی جادهها استفاده میشود.
- مس سولفات : جذب کننده بسیار خوب آب است و در کودها و غذاهای فرآوری شده به کار میرود.
- سدیم بیسولفات : برای کاهش pH محلولها استفاده میشود.
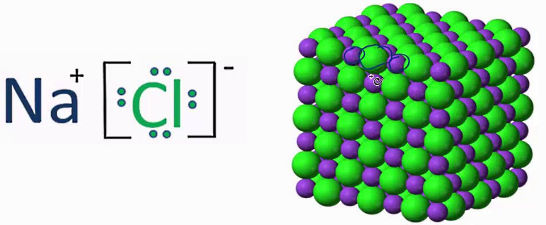
نمک از یون ساخته میشود. یون، اتم یا گروهی از اتمهای باردار هستند که به دو دسته کاتیون و آنیون تقسیم میشوند.
- آنیونها: به یونهایی گفته میشود که با جذب الکترون در لایه بیرونی بار منفی دارند. نافلزاتی مانند کلر و بیشتر هالوژنها میل به جذب الکترون دارند.
- کاتیونها: به یونهایی گفته میشود که با از دست دادن الکترون بار مثبت دارند. فلزاتی سدیم، منیزیم و کلسیم میل به از دست دادن الکترون دارند و در دسته کاتیونها قرار میگیرند.
یونهای میتواند ترکیبات معدنی مانند کلرید یا ترکیباتی آلی مانند استات باشند. همچنین میتواند از یونهای تک اتمی مثل فلورید یا یونهای چند اتمی مانند سولفات ساخته شوند.
برای تعیین فرمول شیمیایی نمکها باید کاتیون و آنیون مشخص شود. برای مثال را در نظر بگیرد. مولکول نمک از کاتیون سدیم و آنیون کلرید تشکیل شده است.
نمکها معمولاً انحلالپذیری خوبی در حلالهای قطبی مانند آب دارند و بهطور کامل در آنها تفکیک میشوند. کاتیونها توسط بخش منفی مولکول آب یعنی اکسیژن جذب شده و آنیونها به سمت بخش مثبت آب یا هیدروژنها کشیده میشوند.
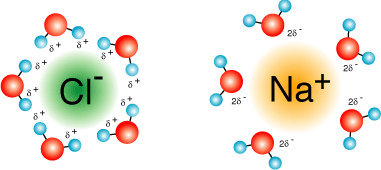
در دنیای کانیشناسی و زمینشناسی، سدیم کلرید یا نمک خوراکی با نام «هالیت» (Halite) شناخته میشود.
واکنشهای شیمیایی تولید نمک چیست ؟
واکنشهای شیمیایی گوناگونی وجود دارند که نمک از فراوردههای آن است. برخی از این واکنشها عبارتند از:
- واکنش اسید و باز
- واکنش با اکسیدهای فلزی
- واکنشهای رسوبی
- واکنش با کربنات فلزات
خنثی سازی اسید و باز
نمک بهطور کلی در نتیجه واکنش اسید و باز تشکیل میشود که به واکنشهای «خنثیسازی» (Neutralization) مشهور هستند. در واقع وقتی اسید و باز با هم واکنش میدهند موجب خنثی شدن یکدیگر میشوند. محصول خنثی شدن نیز نمک و آب است.
- محلولهای اسیدی حاوی یونهای هیدروژن هستند.
- محلولهای بازی حاوی یونهای هیدروکسید هستند.
که معادله شیمیایی یونها به صورت زیر رخ میدهد.
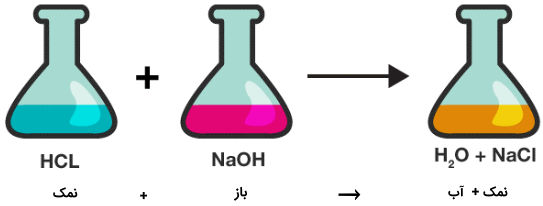
نمکها ترکیبات یونی بوده که از نظر بار الکتریکی بدون بار یا خنثی هستند. باید توجه داشت که نمکهای بدون بار یا خنثی زمانی تشکیل میشوند که واکنش بین اسید و باز قوی یا اسید و باز ضعیف باشد. برای مثال از واکنش اسید قوی و باز قوی ساخته میشود.
و واکنش استیک اسید با آمونیوم هیدروکسید که اسید و باز ضعیف هستند به صورت زیر انجام میشود و محصول این واکنش، آمونیوم استات که نمکی بدون بار است.
یونهای دوقطبی مانند متابولیتها، پپتیدها و پروتئینها در ساختار خود همزمان آنیون و کاتیون دارند ولی در دسته نمکها قرار نمیگیرند. از کاربردهای خنثیسازی اسید و باز را در کارکرد داروهای ضداسید معده میتوان مشاهده کرد. این داروها با اسید اضافی معده واکنش میدهند و آن را خنثی میکنند. نوع نمکی که در طی واکنش خنثیسازی تولید میشود به اسید و باز مورد استفاده بستگی دارد.
- نمکهای کلرید: در نتیجه خنثیسازی هیدروکلریک اسید تولید میشوند.

- نمکهای نیترات: در نتیجه خنثیسازی نیتریک اسیدها تولید میشوند.

- نمکهای سولفات: در نتیجه خنثیسازی سولفوریک اسید تولید میشوند.

اکسید فلزها
نمکها را همچنین میتوان از اکسید فلزها تولید کرد. در این واکنشها، اکسیدهای فلزی نقش بازی دارند و با اسیدها برای تولید نمک و آب واکنش میدهند. معادله واکنش اسید و اکسید فلز به صورت زیر است.

مثال:
در این واکنش اکسید فلز مس با هیدروکلریک اسید واکنش میدهد که محصول آن مس کلرید به همراه آب است.
واکنشهای رسوبی
برخی از نمکهای نامحلول مانند باریم سولفات از واکنش بین دو محلول تهیه میشوند. نمونهای از معادله واکنشهای رسوبی به صورت زیر است.
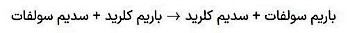
از واکنشهای رسوبی برای حذف برخی یونهای از محلول در روشهای تصفیه آب آشامیدنی و پساب استفاده میشود.

کربنات فلز
بیشتر کربناتهای فلزی ترکیباتی خنثی هستند. این ترکیبها میتواند با خنثیسازی اسیدها موجب تشکیل نمکها شوند. معادله واکنش اسید و کربنات فلز به صورت زیر است.
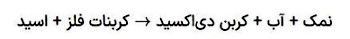
خنثیسازی اسیدها توسط کربناتهای فلزی افزون بر نمک و آب، کربن دیاکسید نیز تولید میکند. در طبیعت سنگهای معدنی مانند سنگ آهک که از کربنات فلز کلسیم تشکیل شدهاند در اثر بارانهای اسیدی تجزیه شده و آسیب میبینند.
خواص نمک چیست ؟
همه نمکها ویژگیهای مشترکی دارند. برخی از این ویژگیها که در بیشتر نمکها وجود دارد عبارتند از:
- پیوند یونی
- نقطه ذوب بالا
- رسانایی الکتریکی در حالت مذاب یا محلول
- ساختار بلوری
رنگ نمک
نمکها به شکل جامد، معمولاً شفاف یا بیرنگ هستند. در بسیاری از نمکها شفافیت یا کدری به اندازه تکبلورهایِ ترکیب مرتبط است. به دلیل بازتاب نور از کریستالیت (Crystallite)، بلورهای بزرگ معمولاً شفاف و دانههای پودر یا پلیکریستالی کدر هستند. نمکها رنگهای گوناگونی دارند که برخی در زیر آورده شدهاند.
| نمک | فرمول | رنگ |
|---|---|---|
| سدیم کرومات | زرد | |
| پتاسیم دیکرومات | نارنجی | |
| کبالت(II) نیترات | قرمز | |
| مس(II) سولفات | آبی | |
| پتاسیم پرمنگنات | بنفش | |
| نیکل(II) کلرید | سبز | |
| سدیم کلرید | بیرنگ | |
| منیزیم سولفات هفت آبه | سفید |
طعم و بوی نمک
نمکها همچنین طعم و مزههای متفاوتی دارند و پنج مزه اصلی را شامل میشوند.
- شور: سدیم کلرید
- شیرین: سرب(II) استات
- ترش: پتاسیم بیتارترات با فرمول
- تلخ: منیزیم سولفات
- «اومامی» (Umami): مونوسدیم گلوتامات
نمکهای قوی که از واکنش اسید و بازهای قوی تشکیل می شوند و فراریت کمی دارند، ترکیبات بیبویی هستد. در مقابل نمکهای ضعیف بو و رایحه دارند.
انحلال پذیری نمک ها
بهطور معمول ترکیبات یونی انحلالپذیری بالایی در محلوهای آبی یا قطبی دارند. این ترکیبات پس از حل شدن، به آنیون و کاتیونهای سازنده نمک تجزیه میشوند. میزان انحلالپذیری نمکها توسط «انرژی شبکه» (Lattice Energy) و برهمکنش یونها با حلال در بلورهای نمک مشخص میشود.
در زیر برخی از نمکها که انحلالپذیری مشابهی دارند فهرست شدهاند.
- نمکهای سدیم، پتاسیم و آمونیوم در آب حل میشوند. آمونیوم هگزاکلروپلاتینات با فرمول شیمیایی و پتاسیم کبالتینیتریت با فرمول جزو مواردی هستند که از این قاعده پیروی نمیکنند.
- بسیاری از نیتراتها و سولفاتها به جز باریم سولفات، کلسیم سولفات و سرب(II) سولفات
- کربناتهای فلزی نامحلول هستند. سدیم کربنات، پتاسیم کربنات و آمونیوم کربنات با فرمول شیمیایی کربناتهای فلزی محلول در آب هستند.
رسانایی نمک ها
نمکها ترکیباتی نارسانا و عایق الکتریکی هستند. اما به صورت محلول و مذاب توانایی رسانایی الکتریسیته دارند و میتوان از آنها برای الکترولیت استفاده کرد.
نقطه ذوب چیست؟
نمکها به دلیل ساختار بلوری و انرژی شبکه بالا نقطه ذوب بالایی دارند. نمکهای مذاب انرژی شبکه پایینی دارند و در دمای اتاق به صورت مایع هستند.

نام گذاری نمک ها
مانند نامگذاری ترکیبات یونی، نمکها به صورت زیر نامگذاری میشوند، اما معمولاً به نام کاتیونهای سازنده شناخته میشوند.
نام کاتیون + نام آنیون
در جدول زیر برخی از کاتیونها و آنیونهای نمکساز رایج فهرست شدهاند.
| کاتیونهای نمکساز | |
|---|---|
| کاتیون | یون |
| آمونیوم | |
| کلسیم | |
| آهن | و |
| منیزیم | |
| پتاسیم | |
| پیریدینیم | |
| سدیم | |
| مس | |
| آنیونهای نمکساز | |
| آنیون | یون |
| استات | |
| کربنات | |
| کلرید | |
| سیانید | |
| فلورید | |
| نیتریت | |
| اکسید | |
| فسفات | |
| سولفات | |
تولید نمک
نمک که به صورت خوراکی مصرف میکنیم یا نمکی که برای یخزدایی در فصل سرد روی سطح جاده پاشیده میشود از راههای مختلفی تولید میشوند. از مهمترین راههای تولید نمک استفاده از ذخایر نمک زیرزمینی به صورت معدن سنگ نمک و «استخراج محلولی» (Solution Mining) است.

سنگ نمک چیست؟
نمک از معدنهای سنگ نمک با حفر زمین توسط ماشینها و سپس انفجار و خرد کردن سنگهای نمک به دست میآید. بیشترین مصرف این نوع نمک برای یخزدایی به کار میرود.
استخراج محلولی
استخراج محلولی از رایجترین فرایندهای تولید نمک خوراکی و صنعتی است. در این روش آب به داخل بسترهای زیرزمینی معادن نمک هدایت میشود. پس از حل شدن نمک، «آب نمک» (Brine) به سطح پمپ شده و برای پالایش فرستاده میشود. در مرحله تصفیه کلسیم، منیزیم و سایر ناخالصیها حذف میشوند. سپس محلول آب نمک به مخازن بزرگی منتقل میشوند و با عمل تبخیر و حذف آب، نمک تولید میشود.
تبخیر آب نمک چیست؟
در برخی از کشورها نیز از گرمای خورشید برای تبخیر آب دریا و تولید نمک استفاده میکنند. این روش تولید نمک، با هدایت آب دریا به حوضچههای کوچک و پس از زمانی کافی برای تبخیر آب توسط گرمای خورشید انجام میشود. این روش با نام تولید نمک خورشیدی نیز معروف است.

آب نمک چیست ؟
«آب شور» (Saline Water) یا آب نمک، آبی با غلظت بالایی از نمکهای محلول مانند سدیم کلرید است. میزان نمک حل شده در آب یا غلظت آب شور بر حسب قسمت در میلیون بیان میشود. آبهای شور بر حسب به سه دسته تقسیم میشوند.
- آب شیرین - کمتر از
- آب اندکی شور - از تا
- آب نسبتاً شور - از تا
- آب بسیار شور - از تا
غلظت نمک در آب اقیانوسها حدود است. این مقدار برابر با ۳۵ گرم نمک در هر لیتر آب است. رسانندگی گرمایی یا انتقال گرما با افزایش شوری آب کاهش و با افزایش دما افزایش مییابد.
شورسنج
«شورسنج یا نمکسنج» (Salinometer) دستگاهی برای اندازهگیری میزان شوری یا نمک حل شده در محلول است. به دلیل تأثیر شوری بر رسانایی الکتریکی در این دستگاه از الکترومتر یا «هیدرومتر یا آبسنج» (Hydrometer) برای سنجش شوری آب استفاده شده است. از شورسنجها در ژنراتورهای آب شیرین به منظور سنجش کیفیت آب استفاده میکنند. در بسیاری از کشتیها به آب تقطیر شده با کیفیت بسیار بالا برای مصرف «دیگهای بخار» (Boilers) نیاز است که با استفاده از دستگاه نمکسنج، آلودگی نمکی تشخیص داده میشود.
فواید و مضرات نمک چیست؟
مصرف خارج از تعادل نمک، مصرف کم یا زیاد آن بر سلامتی تأثیر میگذارد. از نمک برای طعم دهی و نگهداری غذا استفاده میشود. مقدار کم یون سدیم و کلرید برای بیشتر موجودات زنده ضروری هستند. سیستم عصبی و کارکرد سلولی و اندامی بدن به یونهای سدیم نیاز دارد. نمک همچنین نقش مهمی در حفظ تعادل مایعات بدن دارد. کاهش سطح سدیم در بدن موجب فعال شدن سیستم رنین-آنژیوتانسین-آلدوسترون (Renin–Angiotensin System) در بدن میشود. این سیستم وظیفه تنظیم فشارخون و تعادل آب را برعهده دارد.
پیشنهاد سازمان بهداشت جهانی (WHO) برای حداکثر میزان نمک مصرفی در روز برای بزرگسالان ۵ گرم یا کمتر از یک قاشق چایخوری است. مصرف زیاد سدیم و دریافت پتاسیم کم (کمتر از ۳٫۵ گرم) میتواند با فشار خون بالا، افزایش خطر بیماری قلبی، سکته مغزی و بیماری کلیوی همراه باشد. هایپرناترمی و هیپوناترمی دو بیماری مرتبط با مصرف سدیم است.
- «هایپرناترمی» (Hypernatremia) که ناشی از بالا بودن میزان سدیم در خون است، باعث تشنگی، سرگیجه و اسپاسم یا گرفتگی ناگهانی و غیرارادی عضلانی میشود.
- «هیپوناترمی» (Hyponatremia) به دلیل میزان کم سدیم در خون اتفاق میافتد. این بیماری موجب بزرگ شدن سلولهای مغز میشود که میتواند تهوع، استفراغ، خستگی، اسپاسم و سردرد به همراه داشته باشد.
کاربرد نمک چیست ؟
نمکها از پرکاربردترین مواد در صنعت هستند. مصرف بالای این ترکیب در صنایع گوناگون موجب افزایش تقاضای زیاد آن در بازار شده است.
کاربرد نمک در صنعت
نمک کاربردهای فراوانی در تولید شیشه، پلی استر، پلاستیک، چرم و صنایع شیمیایی دارد. نمک برای ثبیت رنگ پارچه و در ساخت کاغذ، لاستیک، آلیاژ برنج، سفیدکننده و فولاد کاربرد دارد. برای تمیزکردن چاههای گاز و نفت از نمک استفاده میشود. برخی از زمینهها که نمک استفاده فراوانی دارد عبارتند از:
- یخزدایی: یخ زدایی جادهها، پیادهروها از کاربردهای استفاده از نمک صنعتی است. برف و یخبندان از مهمترین عاملهای مؤثر بر ایمنی جادهها هستند. نمک یکی از بهترین مواد شناخته شده برای محافظت از جادهها در روزهای برفی و یخبندان است. نمک پاشی موجب کاهش نقطه انجماد آب میشود و فرایند تشکیل یخ را به تأخیر میاندازد یا مانع تشکیل یخ میشود.

- صنعت نفت و گاز: در صنعت نفت و گاز برای افزایش ایمنی و کارایی از نمک در دکل حفاری نفت استفاده میشود. همچنین نمک ماده افزودنی به گل حفاری است. افزودن نمک موجب افزایش چگالی خاک میشود و فرایند حفاری با ایمنی بیشتری صورت میگیرد. همچنین نمک نقش روانکننده و خنککننده مته حفاری را دارد. از دیگر کاربردهای نمک در این صنعت برای لختهکنندگی، رقیقکنندگی و تثبیت کننده است.

- صنایع شیمیایی: برای تولید برخی مواد شیمیایی در این صنعت نمک صنعتی کاربرد فراوانی دارد. نمک در تولید سود سوزآور (سدیم هیدروکسید)، خاکستر سودا (سدیم کربنات) استفاده میشود. همچنین نمک برای تولید محصولاتی مانند سدیم سولفات، سدیم کربنات، هیدروکلریک اسید، سدیم بی کربنات، سدیم مایع، سدیم فلزی، و سدیم نیترات کاربرد دارد. با استفاده از فرایند الکترولیز از نمک برای تولید کلر استفاده میکنند.

- صنعت انرژی: در فرایند تولید انرژی خورشیدی برای انجام برخی از واکنشها، نمکهای صنعتی کاربرد دارد.
- صنایع فلزات: فرآوری فلزات و ساخت آلومینیوم ثانویه
- صنعت نساجی: برای تثبیت و استاندارد رنگ
- لاستیکسازی: برای جداسازی لاستیک از لاتکس، از نمک استفاده میشود.
- صنعت داروسازی: تهیه محلولهای نمکی و تولید کپسول
- صنعت صابون: ماده افزودنی به عنوان «فیلر» (Filler) در شویندهها و حلالها، که موجب جداسازی راحت مواد شیمیایی میشود.
- صنعت رنگدانه: ماده افزودنی به عنوان «فیلر» (Filler) و عامل آسیاب
- تصفیه آب: حذف کلسیم و منیزیم و از بین بردن سختی آب
کاربرد نمک در صنایع غذایی
هزاران سال است که نمک برای حفظ غذا و بهبود طعم و مزه استفاده میشود. همچنین به عنوان کنترلکننده رنگ، قوام دهنده و عامل کنترل تخمیر استفاده میشود.
سدیم، به شکل نمک معمولی، یکی از اجزای معدنی ضروری یک رژیم غذایی سالم است که به بدن در انجام عملکردهای حیاتی کمک میکند. یک رژیم غذایی متعادل سرشار از مواد معدنی و ویتامینها است و بسیاری از غذاها منابع طبیعی سدیم هستند. درصد نمکی که ما از غذاهای مختلف مصرف میکنیم به عادات غذایی فردی ما بستگی دارد، اما معمولاً حدود ۲۰ درصد نمکی که مصرف میکنیم از غذاهایی است که بهطور طبیعی حاوی نمک هستند.

- چاشنی و طعمدهنده: از اولین کاربردهای نمک افزایش طعم خوراکیها بودهاست. باعث خوشطعم شدن غذاهای کربوهیدراتی مانند نان، ماکارونی میشود به نشان دادن طعم طبیعی در سایر غذاها کمک میکند.
- نگهدارنده غذا: نمک قرنها برای نگهداری گوشت، ماهی، محصولات لبنی و بسیاری از مواد غذایی کاربرد داشته است. این نگهدارنده طبیعی با حذف آب باکتریها از رشد آنها جلوگیری میکند و مانع فاسد شدن خوراکیها میشود. نمک همچنین به فرایند تبرید یا سرمایش که از عاملهای مهم در بهداشت مواد غذایی است نیز کمک میکند.
- کنترل کننده رنگ: رنگ غذاهایی مانند گوشتهای فرآوری شده، ژامبون، بیکن و هاتداگ توسط نمکها با شکر و نیترات یا نیتریت کنترل میشود. نمک موجب کاهش تخریب قندها در فرایند تخمیر میشود و کاراملی شدن و همچنین رنگ طلایی نان را افزایش میدهد.
- قوامدهنده: نمک با تقویت گلوتن خمیر موجب استحکام و یکنواختی بافت آن میشود. نمک همچنین بافتی صاف و سفت به گوشتهای فرآوری شده و موجب تردی آنها میشود. این ماده شیمیایی در صنعت تولید پنیر موجب سفت شدن و یکنواختی آن میشود.
- کنترل تخمیر: در صنایع تولید غذا از نمک برای جلوگیری و کنترل رشد باکتریها و کپکها و تخمیرهای ناخواسته استفاده میشود. نمکها همچنین برای کنترل سرعت تخمیر اسید لاکتیک کاربرد دارند.
انواع نمک چیست ؟
نمکها از نظر ترکیب شیمیایی یا کاربرد به انواع گوناگونی دارند.
نمک اسیدی
به نمکهایی که هنگام حل شدن در آب، یون هیدرونیوم آزاد میکنند «نمکهای اسیدی» (Acid Salts) میگویند. نمکهای اسیدی فراورده واکنش خنثیسازی جزئی اسید دو یا چند پروتونی هستند. محلول نمکهای اسید از رسانایی الکتریکی بالاتری از حلال خالص دارد. از نمکهای اسیدی در صنایع غذایی برای خمیرمایه استفاده میشوند. برخی از این نمکهای اسیدی عبارتند از:
- پتاسیم بیتارترات
- مونوکلسیم فسفات
- سدیم آلومینیوم فسفات
- دیسدیم فسفات : در بازدارندههای خوردگی و مواد جرمگیریکننده کاربرد دارد.
- مونوسدیم فسفات : در خوراک دام، خمیردندان، مواد سفیدکننده و شیر تبخیری استفاده میشود. همچنین برای پاکسازی روده پیش از «کولونوسکوپی» (Colonoscopy) کاربرد دارد.
نمک بازی
به نمکهایی که هنگام حل شدن در آب، یون هیدروکسید آزاد میکنند «نمکهای بازی یا قلیایی» (Basic Salts) میگویند. نمکهای قلیایی فراورده واکنش باز قوی و اسید ضعیف هستند. این نوع از نمک مانند نمکهای اسیدی ترکیباتی خنثی نیستند و خاصیت بازی یا قلیایی دارند. «آبکافت یا هیدرولیز» (Hydrolysis) باز مزدوج نمک بازی هنگام حل شدن در آب با آزاد کردن یون هیدروکسید محلول بازی تشکیل میدهند.
نمکهای قلیایی محصول عناصر گروه فلزهای قلیایی و قلیایی خاکی هستند. ولی نمکهای بازی به هر نمکی میگویند که آبکافت شده و محلول بازی تولید کند. برای مثال، سدیم کربنات نمکی بازی است. کربنات نمک که از اسید ضعیف کربنیک اسید آمده است هیدرولیز شده و محلولی بازی تشکیل میدهد. ولی کلرید در سدیم کلرید که از اسید قوی هیدروکلریک اسید آمده است هیدرولیز نمیشود.
نمکهای بازی در پودرهای شوینده ماشین ظرفشویی استفاده میشوند. برخی از نمکهای بازی عبارتند از:
- سدیم کربنات
- سدیم استات
- پتاسیم سیانید
- سدیم سولفید
- سدیم بیکربنات
- سدیم هیدروکسید
- سرب سفید یا سفیداب سرب

نمک مضاعف
«نمک مضاعف» (Double salt) از تبلور دو نمک با نسب مولی یکسان ساخته میشود. در ترکیب نمک مضاعف بیش از یک کاتیون یا آنیون متفاوت وجود دارد. بسیاری از کمپلکس شیمیایی میتواند نمک مضاعف تولید کنند. نمکهای مضاعف هنگام حل شدن در آب بهشکل مخلوطی از دو نمک جدا هستند.
برخی از نمکهای مضاعف عبارتند از:
- زاجها با فرمول عمومی
- «نمکهای توتونز» (Tutton's salt) با فرمول عمومی
- پتاسیم سدیم تارترات
- آمونیوم آهن (II) سولفات
- بروملیت
- فلوروکربناتهای حاوی فلورید

نمک مذاب
نمک مذاب (Molten Salt) ترکیبی معدنی، غیرقابل اشتعال و غیرسمی که در شرایط استاندارد به شکل جامد است. این ترکیب با افزایش دما از جامد به مایع تغییر حالت میدهد. برخی از نمکهای مذاب که در دما و فشار معمولی به حالت مایع هستند به عنوان مایع یونی نامیده میشوند. برخی از کاربردهای نمکهای مذاب عبارتند از:
- مخلوط یوتکتیک (Eutectic) سدیم نیترات (۶۰٪) و پتاسیم نیترات (۴۰٪) برای استفاده در دمای ۲۶۰ تا ۵۵۰ درجه سلسیوس
- استفاده از مخلوط نمک کلرید مذاب در رآکتور نمک گداخته برای عملیات حرارتی بازپخت (Annealing) و مارتپخت (Martempering) کردن فولاد
استفاده از مخلوط نمک سیانور و کلرید برای اصلاح سطح آلیاژها - کرایولیت از نمکهای فلورید در نقش حلال آلومینیم اکسید در «فرایند هال–هرولت» (Hall-Héroult process) برای تولید آلومینیم استفاده میشود.
- استفاده از نمکهای فلورید، کلرید و هیدروکسید در نقش حلال برای پردازش حرارتی سوخت هستهای
- استفاده از نمکهای فلورید، کلرید و نیترات برای انتقال حرارت و ذخیرهسازی حرارتی در نیروگاههای برق خورشیدی متمرکز

نمک اپسوم
نمک اپسوم یا نمکهای حمام به شکل پودر به آب اضافه میشوند تا موجب بهبود نظافت شوند. این ترکیبات برای شبیهسازی خواص معدنی چشمههای آب گرم ساخته شدهاند. برخی از آنها حاوی گلیسیرین هستند و نقش نرمکننده یا مرطوبکننده را دارند. معمولاً از ترکیبات زیر برای نمک حمام استفاده میشوند. برخی از نمکهای فسفات به دلیل ویژگی شویندگی این ترکیبات به نرم شدن و پاکسازی سلولهای مرده پوست کمک میکنند. نمکهای حمام باعث رسوبزدایی و نرم شدن آب و عملکرد بهتر صابون و مواد شوینده میشوند. آب با غلظت بالای نمک، چگالی بیشتری دارد و حس سبکی و شناوری را در وان حمام ایجاد میکند. از این ترکیبات همچنین برای درمان «آرتریت یا التهاب مفصل» (Arthritis) استفاده میشود.
موادی که اغلب به عنوان نمک حمام برچسب گذاری میشوند عبارتند از
- منیزیم سولفات که به نمک اپسوم نیز شناخته میشود.
- سدیم کلرید
- سدیم هیدروژنکربنات یا جوش شیرین
- سدیم هگزامتافسفات
- تری سدیم هیدروژن دی کربنات ()
- بوره یا بوراکس که از نمکهای بوریک اسید است.
نمک خوراکی چیست ؟
نمک خوراکی معمولا اشاره به سدیم کلرید دارد. این ماده ترکیبی از دو عنصر شیمیایی سدیم و کلر است. نمک خوراکی انواع گوناگونی مانند نمک دریا، نمک تصفیه شده و نمک یددار دارد. نمکهای خوراکی بهطور معمول از راه استخراج سنگ نمک یا تبخیر آب دریا تولید میشوند.

سدیم کلرید
سدیم کلرید به شکل بلورهای سفید رنگ است ولی به دلیل وجود برخی عناصر دیگر مانند منیزیم رنگهای صورتی و خاکستری نیز دارد. نمک تعادل مایعات بدن را حفظ می کند و برای بقای موجودات زنده لازم است. استفاده از نمک برای طعم دادن به غذا از کاربردهای رایج آن است. طعم شور همراه با تلخی دارد. سدیم کلرید از مهمترین و قدیمیترین طعمدهندههای مورد استفاده توسط انسان است.
«همفری دیوی» (Humphry Davy) دانشمند انگلیسی در سال ۱۸۰۷ توانست ترکیب شیمیایی نمک را به اجزای سازنده آن یعنی سدیم و کلر تجزیه کند. این کار موجب شد تا عنصرهای سدیم و کلر در صنایع تولیدی مورد استفاده قرار گیرند. به دلیل خواص کلر و سدیم و همچنین ترکیبات آنها، نمک به یکی از مواد پرکاربرد در صنعت تبدیل شده است.

برخی از ترکیبات کلر که از اهمیت تجاری بالایی دارند عبارتند از:
- هیدروکلریک اسید: در ساخت استفاده میشود.
- هیدروکربنهای کلردار: در خشکشویی کاربرد دارد.
- کلسیم هیپوکلریت: با فرمول شیمیایی برای ضدعفونی کردن آب و برای سفید کردن خمیر چوب و پارچه استفاده میشود.
ترکیبات مهم سدیم عبارتند از:
- سدیم کربنات : برای کاهش سختی آب استفاده میشود.
- سدیم سولفات : مورد استفاده در پودرهای لباسشویی
- جوش شیرین : مورد استفاده در خمیر نان و کیک
- سدیم فسفات : در مواد شوینده، خمیردندان و برای کاهش سختی آب استفاده میشود.
- سدیم هیدروکسید : در خمیر چوب برای ساخت کاغذ استفاده میشود.
الکترولیز نمک چیست؟
الکترولیز یا برقکافت از روشهای جداسازی عناصر توسط جریان الکتریکی مستقیم است. الکترولیز سدیم کلرید از فرایندهای ردوکس بسیار مهم در صنایع شیمیایی است. سدیم کلرید به شکل محلول یا مذاب الکترولیز میشود. با عبور جریان الکتریکی از محلول غلیظ در الکترود منفی، گاز هیدروژن و در الکترود مثبت، گاز کلر و محلول سدیم هیدروکسید تشکیل میشوند. این فرایند سه فراورده مهم زیر را تولید میکند.
- گاز کلر : یونهای کلرید از محلول نمک به صورت گاز تشکیل میشوند.
- گاز هیدروژن : یونهای هیدروژن از آب گرفته میشوند.
- سدیم هیدروکسید : یونهای سدیم از محلول نمک و یونهای هیدروکسید از آب موجب تشکیل سدیم هیدروکسیدمی شوند.
از ترکیب این فراوردهها محصولات بیشتری نیز تولید میکنند. از ترکیب سدیم هیدروکسید و کلر برای تشکیل محلول سدیم هیپوکلریت استفاده میشود. سدیم هیپوکلریت سفیدکننده و ضدعفونی کننده است. همنچنین سدیم کلرات تحت شرایطی دیگر از ترکیب سدیم هیدروکسید و کلر تولید میشود. این ماده برای محلول علفکش کاربرد دارد. از واکنش سوختن گاز کلر در هیدروژن، هیدروژن کلرید تشکیل میشود. با حل کردن این گاز در آب، هیدروکلریک اسید تولید میکنند. اسید تولید شده از این روش خلوص بالایی دارد و در صنایع غذایی و دارویی به کار میرود.
سدیم نمک چیست؟
سدیم با عدد اتمی ۱۱ از عناصر گروه یک جدول تناوبی است. سدیم فلزی نرم، واکنشپذیر و رنگی نقرهای دارد. این فلز ششمین عنصر فراوان در پوسته زمین است. نمکهای سدیم انحلالپذیری خوبی در آب دارند. سدیم هیدروکسید یا سود سوزآور از شناخته شدهترین ترکیبات سدیم است که در تولید صابون کاربرد دارد. این فلز همچنین از عنصرهای ضروری برای موجودات زنده بهشمار میرود و یونهای آن از اجزای اصلی «مایعات برونسلولی» (Extracellular Fluid) هستند.

کلر نمک چیست؟
کلر با عدد اتمی ۱۷ از عنصرهای شیمیایی و عضو گروه هالوژنها بهشمار میآید. کلر در شرایط بهصورت گاز و به رنگ زرد مایل به سبز است. گاز کلر واکنشپذیری بسیار بالایی دارد و پس از فلوئور و اکسیژن بیشترین الکترونگاتیوی را دارد.
کلر در بدن به شکل هیدروکلریک اسید در معده به هضم غذا کمک میکند. همچنین این عنصر در سیستم ایمنی از بدن انسان در برابر عفونت محافظت میکند. کلر اولین ماده ضدعفونی کننده برای مقابله با شیوع بیماریها بود و برای ضدعفونی کردن آب آشامیدنی و جلوگیری از انتقال وبا و حصبه استفاده شد. به دلیل واکنشپذیری کلر در تولید بسیار از محصولات کاربرد دارد. تاکنون بیش از ۲۰۰۰ ترکیب آلی کلردار شناخته شدهاند و نزدیک به ۸۵ درصد از داروها حاوی کلر هستند. برخی از این داروها برای درمان بیماریهای قلبی، سرطان خون، التهاب مفاصل و آلرژی کاربرد دارند.
نمک دریا چیست ؟
نمک دریا که ترکیب اصلی آن سدیم کلرید است با تبخیر آب دریا به دست میآید. این نمک مانند نمک خوراکی در پخت و پز، نگهداری عذا و همچنین در لوازم آرایشی و بهداشتی کاربرد دارد. نمکهای دریایی ترکیب شیمیایی متفاوتی دارند و حدود ۰٫۲ تا ۱۰ درصد شامل یونهای کلسیم، پتاسیم و منیزیم کلرید و سولفات و دیگر عناصر موجود در آب طبیعی دریا هستند.

برخی از یونهای موجود در آب دریا که میتواند در نمکهای دریایی وجود داشته باشد در جدول زیر فهرست شده است.
| غلظت برخی از یونها در آب دریا | ||
|---|---|---|
| یون | فرمول | میلی گرم در لیتر |
| کلرید | ۱۸۹۸۰ | |
| سدیم | ۱۰۵۵۶ | |
| سولفات | ۲۶۴۹ | |
| منیزیم | ۱۲۶۲ | |
| کلسیم | ۴۰۰ | |
| پتاسیم | ۳۸۰ | |
| بی کربنات | ۱۴۰ | |
| برمید | - | ۶۵ |
نمک کوشر
نمک کوشر (Kosher Salt) شباهت زیادی به نمک سدیم کلرید دارد. بلورهای نمک کوشر درشت و طعمی نزدیک به دارد. از بیشتر این نمک برای پخت و طعمدار کردن گوشت استفاده میشود.

نمک پولکی
نمک پولکی (Flake Salt) به شکل ورقه و تکه کوچک کوچک است که از دریا به دست میآید. این نوع نمک طعمی شبیه به نمک خوراکی ولی با چسپندگی بیشتر دارد. انحلالپذیری آن در آب بیشتر است. این نوع نمک به صورت تجاری با فشردهسازی نمک معمولی نیز ساخته میشود.

نمک صورتی هیمالیا
«نمک صورتی هیمالیا» (Himalayan Pink Salt) حاوی مقادیر کمی آهن اکسید با ترکیب اصلی است. منابع اصلی این نمک در پنجاب کشور پاکستان است. طعمی سبکتر از نمک معمولی و شیرینتر دارد. بیشتر در غذاهای سرخکردنی و فروشویی سبزیجات استفاده میشود.

نمک صورتی آند
«نمک صورتی آند» (Andean Pink Salt) از چشمههای آبشور در کوههای آند کشورهای پرو و بولیوی برداشت میشود. این نمک حاوی ترکیبات معدنی کمیاب بسیاری است. ترکیب اصلی آن آهن اکسید با است که از نظر طعم و عطر به نمک صورتی هیمالیا شبیه است.

گل نمک چیست؟
«گل نمک یا فلور دی سل» (Fleur De Sel) بیشتر از سواحل فرانسه و بخشهایی از آمریکای شمالی از بالای حوضچههای آب شور که تبلور سریعتری دارند برداشت میشود. رنگی سفید مایل به خاکستری دارد که گاهی به دلیل وجود ریزجلبکهای آب شور رنگ صورتی کمرنگ میگیرد. این نمک کمتر برای برای پخت و پز مناسب است و قیمت بسیار بالایی دارد.

نمک خاکستری
«نمک خاکستری یا سل گریس» (Sel Gris) از پایین حوضچههای آب شور برداشت میشود و از نظر مواد معدنی غنیتر گل نمک و رنگی خاکستری دارد. از نمک خاکستری به شکل پودر و دانه ریز برای پخت و پز و از بلورهای درشت آن روی گوشت و ماهی استفاده میکنند. طعم این نمک بین گل نمک و نمک دریایی است.
نمک قرمز هاوایی
«نمک قرمز هاوایی» (Hawaiian Red Salt) حاوی خاک رس آتشفشانی است. نسبت به نمک معمولی سدیم و شوری کمتری دارد و مصرف درمانی دارد.

نمک سیاه هیمالیا
نمک سیاه هیمالیا یا «کالا نمک» (Kala Namak) از معدنهای نمک در پاکستان استخراج میشود. این نمک حاوی ماده معدنی گریژیت است که موجب ایجاد رنگ ارغوانی تیره آن شده است. به دلیل وجود گوگرد بوی تند و طعمی نزدیک به تخم مرغ دارد و در «گیاهخواری» (Vegetarianism) جایگزینی برای آن است. در آشپزی هندی به فراوانی از نمک سیاه استفاده میشود.

نمک سیاه قبرسی
«نمک پولکی سیاه قبرسی» (Cyprus Black Flake Salt) با تبخیر آب دریا و افزودن زغال فعال به دست میآید و بهطور طبیعی مانند نمک سیاه هیمالیا سیاهرنگ نیست. طعمی شبیه به نمک دریایی و درصد سدیم کمتری دارد. به دلیل بزرگ بودن ورقههای نمک بیشتر برای تزیین غذا و همچنین روی سالاد، ماهی استفاده میشود.

نمک آبی ایرانی
«نمک آبی ایرانی» (Persian Blue Salt) از منابع نمک سمنان در ایران استخراج میشود. رنگ آبی آن به دلیل وجود سیلویت (KCl) از کانیهای پتاسیم است. از این نمک که طعم گیرا و شیرینی دارد برای دسرها، غذاهای گوشتی و دریایی استفاده میشود. درصد پتاسیم در این نمک نسبتاً بالا است و حاوی منیزیم، آهن و کلسیم است. این نمک همچنین از کمیبابترین انواع نمک است.

نمک زدایی چیست ؟
«نمکزدایی» (Desalination) فرایندی شیمیایی است که در آن ترکیبات معدنی از آب شور حذف میشود. در این فرایند مواد معدنی و نمک را از آب حذف میکنند. از کاربردهای نمکزدایی در کشاورزی برای نمکزدایی خاک و تولید آب آشامیدنی مناسب برای مصرف و آبیاری است. همچنین، فرایند حذف نمک در بسیاری از کشتیهای دریایی و زیردریاییها برای تهیه آب مصرفی به کار میرود. به دلیل کمبود آب شیرین در سالهای اخیر توجه بیشتری به تولید آب از آب دریا شده است.
تولید آب از طریق این فرایند به دلیل مصرف انرژی زیاد نسبت به آب شیرین بهدست آمده از آبهای سطحی یا زیرزمینی و بازیافت آب هزینه بیشتری دارد. نمکزدایی به وسیله انرژی گرمایی و مکانیکی به روشهای گوناگونی انجام میشود. در زیر برخی از روشهای نمکزدایی آب فهرست شده است.
روشهای نمکزدایی از آب
- تقطیر
- «تقطیر ناگهانی چندمرحلهای» (Multi-stage Flash Distillation | MSF)
- «تقطیر اثر چندگانه» (Multiple-effect Distillation | MED)
- «تراکم بخار» (Vapor-Compression | VC)
- تبادل یونی
- فرایند غشایی
- «برگشت الکترودیالیزی» (Electrodialysis reversal | EDR)
- اسمز معکوس
- «نانوفیلتراسیون» (Nanofiltration | NF)
- «تقطیر غشایی» (Membrane Distillation | MD)
- اسمز مستقیم
- نمکزدایی
- نمکزدایی زمینگرمایی
- نمکزدایی خورشیدی
- «آبشیرینکن خورشیدی–رطوبتزدا» (Solar Humidification–Dehumidification | HDH)
- «رطوبتزایی اثر چندگانه» (Multiple-effect Humidification | MEH)
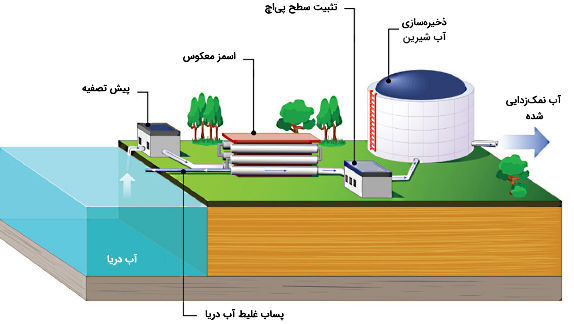
بهطور کلی روشهای نمکزدایی را میتوان به روشهای مبتنی بر غشاء و حرارت تقسیم کرد. روش تقطیر و اسمز معکوس از رایجترین فرآیندهای نمکزدایی هستند. روشهای اسمز معکوس و تقطیر ناگهانی چندمرحلهای در بین روشهای دیگر بالاترین بازده را از نظر ظرفیت نمکزدایی بیشتر دارند.
سوالات متداول
برخی از پرسشهای رایج درباره اینکه نمک چیست در این بخش پاسخ داده شده است.
نام دیگر نمک خوراکی چیست ؟
نمک سفید، نمک تصفیه شده از دیگر نامهای نمک خوراکی هستند. در شیمی این نمک، سدیم کلرید نام دارد.
آیا نمک ترکیب است؟
نمکها دستکم از دو عنصر تشکیل میشوند، و در دسته ترکیبات قرار میگیرند.
نمک فلزی چیست ؟
یکی از راههای تشکیل نمک جایگزین شدن فلز با هیدروژن اسید است که از واکنش ترکیبات فلزی مانند اکسیدها با اسید رخ میدهد.
نمک معدنی چیست ؟
نمک تصفیه شده یا نمک سفید تنها حاوی دو عنصر سدیم و کلر است. بهطور طبیعی نمک استخراج شده شامل طیف گستردهای از مواد معدنی دیگر مانند کلسیم، گوگرد، پتاسیم و منیزیم است. نمک دریا از منابع نمک معدنی است. نمک یددار نیز با افزودن پتاسیم یدید ، سدیم آلومینوسیلیکات و منیزیم کربنات به نمک سفید تولید میشود.
آزمون مطلب نمک
۱. ساختار مولکولی و ترکیب یونی نمکها چگونه تعریف میشود و چه تفاوتی با سایر ترکیبات شیمیایی دارند؟
نمکها ترکیبات آلی با زنجیره بلند اتم کربن و هیدروژن هستند که معمولا در آب نامحلولاند.
نمکها مولکولهایی با پیوند کووالانسی قویاند که اغلب نقطه ذوب پایینی دارند.
نمکها ترکیب یونی با پیوند یونی بین کاتیون و آنیون هستند که در آب به سادگی تفکیک میشوند.
نمکها تنها از یک نوع اتم ساخته میشوند و ساختار مولکولی ساده دارند.
تعریف نمک بر اساس ساختار یونی و پیوند یونی بین یونهای کاتیون و آنیون است که سبب میشود این ترکیبات در آب به راحتی تفکیک یا dissociate شوند. این ویژگی آنها را از ترکیبات آلی با زنجیره اتم کربن و هیدروژن یا مولکولهایی با پیوند کووالانسی قوی که نقطه ذوب پایینی دارند متمایز میکند. برخلاف ترکیباتی که فقط از یک نوع اتم ساخته شدهاند، نمکها حداقل از دو یون مختلف تشکیل شدهاند و ویژگیهای فیزیکی و شیمیایی خاص خود را دارند.
۲. کدام عامل بیشترین تاثیر را بر رنگ و انحلالپذیری نمکها دارد؟
روش تهیه و استخراج نمک
شکل بلوری نهایی نمک
دمای محیط هنگام تبلور
نوع و بار یونی کاتیون و آنیون
ترکیب و بار یونی کاتیون و آنیون تعیینکننده اصلی رنگ و انحلالپذیری نمکها هستند، زیرا یونهای تشکیلدهنده ویژگیهای ظاهری و شیمیایی نمک را شکل میدهند. «روش تهیه و استخراج»، «دمای محیط» و «شکل بلوری» بیشتر بر خلوص یا ظاهر فیزیکی و نه ویژگیهای شیمیایی پایه مانند رنگ و انحلالپذیری تاثیر دارند.
۳. کدام یک از یونهای زیر از متداولترین یونها در ترکیب نمکهای صنعتی و خوراکی محسوب میشود؟
لیتیم (Li+) و یدید (I-) بیشتر در نمکهای تجاری یافت میشوند
سدیم (Na+) و کلرید (Cl-) معمولترین یونها هستند
آهن (Fe2+) و فسفات (PO4 3-) به طور معمول نمک خوراکی میسازند
آلومینیوم (Al3+) و سیانید (CN-) اغلب در نمکهای رایج مشاهده میشوند
یونهای «سدیم (Na+) و کلرید (Cl-)» در ترکیب نمکهای صنعتی و خوراکی مانند سدیم کلرید کاربرد دارند و رایجترین یونها میباشند. دیگر یونهای مطرحشده مانند «لیتیم و یدید»، «آهن و فسفات» یا «آلومینیوم و سیانید» معمولا در نمکهای رایج صنعتی و خوراکی استفاده نمیشوند و یا کاربرد آنها بسیار محدود است.
۴. در واکنش میان اسید و باز (neutralization)، چه نوع محصولات و پیوندی حاصل میشود و این فرآیند چه تفاوتی با واکنش اسید و اکسید فلز دارد؟
نمک و آب با پیوند یونی حاصل میشود، در حالی که واکنش اسید و اکسید فلز نیز نمک و آب با همان پیوند تولید میکند
در واکنش اسید و باز فقط آب تولید میشود و پیوندها کووالانسی هستند، اما با اکسید فلز نمک و آب ایجاد میشود
واکنش اسید و باز نمک و آب با پیوند یونی میدهد، اما واکنش اسید و اکسید فلز مسیر مشابه اما با واکنشپذیری متفاوت دارد
در هر دو واکنش فقط آب و دیاکسید کربن (CO2) ایجاد میشود و نوع پیوند کاتیونی است
در واکنش اسید و باز، محصول اصلی نمک و آب با پیوند یونی است. واکنش اسید و اکسید فلز هم محصولش نمک و آب است، اما تفاوت اصلی آن در ماده شرکتکننده یعنی اکسید فلز به جای باز میباشد، هرچند مسیر هر دو مشابه است و ساختار یونی در نمک تولیدی حفظ میشود. متن مشخص نکرده که فقط آب یا دیاکسید کربن بهتنهایی تشکیل شوند؛ همچنین هیچ اشارهای به پیوند کووالانسی یا پیوند کاتیونی نشده و بر تولید نمک یونی و آب تاکید شده است.
۵. برای حذف یونهای خاص از آب، کدام نوع واکنش شیمیایی تولید نمک موثرترین روش محسوب میشود؟
واکنش اسید و باز برای تولید نمک محلول
واکنش اکسید فلز با اسید برای تهیه نمک
واکنش رسوبی جهت جداسازی نمک نامحلول
واکنش اسید با کربناتهای فلزی برای آزاد شدن گاز کربن دی اکسید
هنگامی که هدف حذف یونهای خاص از آب است، واکنش رسوبی بهترین راهکار محسوب میشود. در این روش، با شرکت دادن یونهای نامطلوب، نمک نامحلول ایجاد شده و به صورت رسوب از آب جدا میگردد. سایر روشها مانند «واکنش اسید و باز» یا واکنش اکسید فلز با اسید بیشتر به تولید نمکهای محلول مربوطند که خود در محلول باقی میمانند، نه اینکه یونها را حذف کنند. واکنش با کربناتهای فلزی نیز صرفا منجر به تولید گاز و نمک میشود و تمرکز آن بر حذف یونها از آب نیست.
۶. جدول نامگذاری یونها چه کمکی به تعیین ساختار نمک دارد؟
با آن میتوان نام و فرمول شیمیایی نمک را براساس کاتیون و آنیون مشخص کرد.
جدول بیشتر راهنمای انتخاب روش استخراج نمکهای صنعتی است.
از این جدول برای تعیین نقطه ذوب و ویژگی ظاهری نمک استفاده میشود.
این جدول فقط ترکیبات آلی نمک را مشخص میکند و کاربردی برای نمکهای معمولی ندارد.
استفاده از جدول نامگذاری یونها سبب میشود بتوان نام و فرمول شیمیایی هر نمک را دقیقا براساس شناسایی کاتیون و آنیون تشکیلدهنده پیدا کرد. این جدول فقط ساختار شیمیایی ترکیبات یونی را ارائه میدهد و جزئیاتی از ویژگی فیزیکی، نقطه ذوب یا روش تولید نمک ارائه نمیکند. جدول مختص نامگذاری ترکیبات یونهای نمک است و ربطی به روش استخراج یا طبقهبندی نمکهای آلی ندارد.
۷. در روش استخراج محلولی برای استخراج نمک چه مراحلی طی میشود و این روش چه تفاوتی با تبخیر آب شور دارد؟
در هر دو روش آب به نمک اضافه و پس از حلشدن، نمک با دستگاه جدا میشود.
در استخراج محلولی، نمک همراه گل و لای بالا میآید و بعد فیلتر میشود؛ در تبخیر، نمک ساییده میشود.
در هر دو روش، نمک از سنگ خردشده به دست میآید اما نحوه جداسازی متفاوت است.
در استخراج محلولی آب به لایههای زیرزمینی هدایت و نمک حلشده به سطح آورده میشود، اما در تبخیر، آب شور را از سطح تبخیر میکنند.
در روش استخراج محلولی آب را به لایههای زیرزمینی میرسانند تا نمک در آن حل شود و محلول نمکی به سطح منتقل میشود. این فرآیند محلول را برای جداسازی و تصفیه به بالا میآورد. درحالیکه در روش تبخیر آب شور، آب را روی سطح (مثلا آب دریا) رها میگذارند تا با انرژی خورشیدی تبخیر شود و نمک جامد باقی بماند.
۸. برای سنجش میزان شوری آب، کدام ابزار به شکل الکترونیکی عمل میکند و در صنایع کاربرد بیشتری دارد؟
شورسنج الکترونیکی برای اندازهگیری شوری استفاده میشود.
پیاچمتر (pH meter) میزان اسیدی بودن آب را نشان میدهد.
ترمومتر برای سنجش دمای آب به کار میرود.
آبسنج تنها چگالی آب را میسنجد.
استفاده از شورسنج الکترونیکی برای سنجش شوری آب دقیقتر و تخصصیتر است و این ابزار در صنایع دریایی و نیروگاهها بهکار میرود.
۹. از نظر ساختار شیمیایی و کاربرد صنعتی، چه تفاوتی میان نمکهای اسیدی، بازی و مضاعف وجود دارد؟
نمکهای اسیدی، بازی و مضاعف همگی برای کنترل رنگ در صنایع نساجی استفاده میشوند.
نمکهای اسیدی و مضاعف فقط در ساخت شیشه و پلاستیک نقش دارند، اما نمک بازی برای داروسازی مهم است.
همه این نمکها فقط یک نوع کاتیون و آنیون دارند و اغلب فقط در صنایع غذایی کاربرد دارند.
نمکهای اسیدی در خمیرمایه و نمکهای بازی در شویندهها و نمکهای مضاعف در کودهای معدنی استفاده میشوند.
نمکهای اسیدی غالبا در خمیرمایه به کار میروند، نمکهای بازی برای ساخت شویندهها و آلیاژسازی مناسباند و نمکهای مضاعف جایگاه مهمی در تهیه آلومینیوم و کودهای معدنی دارند. استفاده هر گروه براساس ویژگی شیمیایی و ساختار یونهای آن مشخص میشود.
۱۰. دلیل اصلی استفاده کارخانهها از الکترولیز سدیم کلرید برای تولید هیدروکسید سدیم چیست و چه فرآوردههای دیگری حاصل این واکنش هستند؟
الکترولیز باعث افزایش خلوص نمک و حذف یونهای مضر میشود.
این روش علاوه بر هیدروکسید سدیم، گاز کلر و گاز هیدروژن نیز تولید میکند.
این واکنش فقط هیدروکسید سدیم تولید میکند و دوستدار محیط زیست است.
از الکترولیز برای تهیه فقط گاز کلر در صنایع دارویی بهره میبرند.
الکترولیز سدیم کلرید روشی است که همزمان سه ماده کلیدی یعنی هیدروکسید سدیم، گاز کلر و گاز هیدروژن تولید میشود که هر سه در صنایع مختلف اهمیت بسیار دارد.
۱۱. نمک چرا برای سلامت سیستم عصبی و تعادل آب بدن اهمیت دارد؟
کمک به عملکرد عضلات و تنظیم انتقال عصبی
تحریک ترشح هورمون انسولین و کنترل قند خون
افزایش میزان اکسیژن خون و جذب آهن
تنظیم سرعت متابولیسم و تولید انرژی
عبارت «کمک به عملکرد عضلات و تنظیم انتقال عصبی» درست است زیرا طبق مطلب، یونهای سدیم و کلرید حاصل از نمک نقش کلیدی در عملکرد سیستم عصبی، کارکرد اندامها و تعادل آب بدن دارند. این یونها مسئول حفظ پیامرسانی عصبی و فعالیت صحیح عضلات هستند.
۱۲. کدام ویژگی فیزیکی نمک باعث شده است که در صنایع غذایی و داروسازی نقش کلیدی ایفا کند؟
انحلالپذیری بالا و بیبو بودن در آب
رنگهای متنوع و ظاهر بلوری
بیبو بودن و داشتن ساختار فلزی
نقطه ذوب بالا و کریستالی بودن
«انحلالپذیری بالا و بیبو بودن در آب» باعث شده نمک مادهای مناسب برای کاربردهای گسترده در صنایع غذایی و داروسازی باشد. نمک به راحتی در آب حل میشود، طعمدهنده خوراک است و بیبو بودن آن موجب میشود بر عطر محصولات تاثیر منفی نگذارد.
۱۳. انواع نمکهای خوراکی و غیرخوراکی معمولا براساس کدام ویژگی تقسیمبندی میشوند و هر دسته چه تفاوتی دارد؟
بر اساس ترکیب شیمیایی و منبع استخراج، هر گروه ویژگی فیزیکی و کاربرد خاص دارد.
صرفا بر اساس اندازه دانه، همه نمکها در ترکیب شیمیایی یکساناند.
بر اساس طعم و رنگ، هر گروه فقط از نظر ظاهری متفاوت است.
براساس میزان انحلالپذیری در آب، برخی فقط برای مصارف صنعتیاند.
دستهبندی نمکهای خوراکی و غیرخوراکی عمدتا بر اساس ترکیب شیمیایی، منبع استخراج و ویژگیهای فیزیکی انجام میشود. مانند نمک دریا، صورتی هیمالیا یا انواع معدنی که از نظر ترکیب یونی و محل استخراج باهم فرق دارند و کاربردهای مختلفی مثلا در آشپزی، بهداشت یا تزیین غذا دارند.













عالی بود ممنون
این مطالب را در برنامه فرادرس پیدا نمیکنم
آیا توی برنامه هم مطالب هستش یا فقط وبینار ها و ویدیو های آموزشی هست ؟
با سلام؛
در اپلکیشین فرادرس، دورههای ویدیویی فرادرس را میتوانید پیدا کنید. محتوای متنی از طریق وبسایت مجله فرادرس، در دسترس است.
با تشکر از همراهی شما با مجله فرادرس