اتم چیست؟ – به زبان ساده
اتمها یکی از ذرات تشکیلدهنده مواد هستند. در طی سالیان متمادی ۱۱۸ عنصر کشف شدهاند. این عنصرها در جدولی به نام جدول تناوبی نمایش داده میشوند. تمام اجسامی که در اطراف خود مشاهده میکنیم از اتم ساخته شدهاند. اما اتمِ تنها، بسیار کوچک است و در حالت عادی با چشم دیده نمیشود. در این مطلب از مجله فرادرس سعی میکنیم به پرسش اتم چیست به زبان ساده پاسخ دهیم و در مورد مدلهای اتمی مختلف، ساختار اتم، ذرات درون اتمی و هر آنچه به آن مربوط میشود صحبت کنیم.
- میآموزید اتم چیست، از چه اجزایی تشکیل شده است و نقش آن چیست.
- با خواص اتم، عدد اتمی و جرمی و دستهبندی عناصر آشنا میشوید.
- میتوانید مفهوم ایزوتوپ و انواع آن را درک کنید.
- ذرات زیر اتمی مانند الکترون، پروتون، نوترون و پوزیترون را میشناسید.
- با مدلهای اتمی مختلف از مدل تامسون تا مدل کوانتومی آشنا میشوید.
- میتوانید مفهوم پیوند، مولکول و ترکیب شیمیایی و انواع ان ها را درک کنید.

اتم چیست ؟
اتم کوچکترین واحد تشکیلدهنده ماده است و ویژگیهای آن ماده را دارد. این ذرات بسیار کوچک هستند. ماده چیزی است که بتوان آن را به صورت فیزیکی لمس کرد. هر چیزی در جهان (به جز انرژی) از ماده، و در نتیجه از اتم ساخته شده است. این ذرات به صورت مستقل وجود ندارند، بلکه با پیوستن به یکدیگر، مولکولها و یونها را تشکیل میدهند. این مولکولها و یونهای تشکیل شده نیز با پیوستن به یکدیگر موادی را تشکیل میدهند که در زندگی روزانه مشاهده و لمس میکنیم.
برای درک بهتر این مفهوم به غذای مصرفی روزانه خود دقت کنید. این غذای پخته شده از مواد گوناگونی مانند نمک، برنج، گوشت و ادویهجات تشکیل شده است. مواد گوناگون نیز مانند غذا از اتمهای مختلفی تشکیل شدهاند.
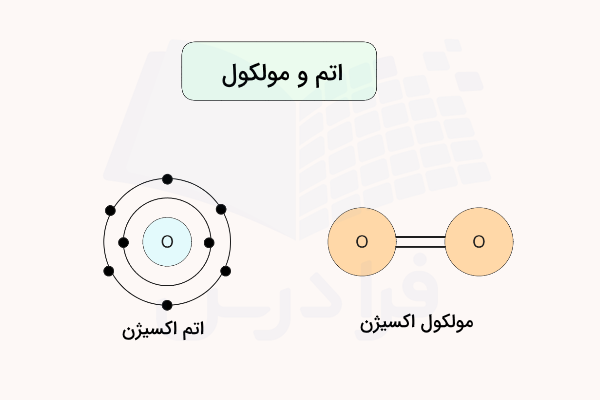
مولکول و اتم
اتمها به قدری کوچک هستند که دیده نمیشوند. بنابراین، برای پی بردن به ساختار و رفتار آنها، آزمایشهای مختلفی با تعداد زیادی از این ذرات، طراحی و انجام شدهاند. دانشمندان با استفاده از نتایج بهدست آمده از این آزمایشها، در تلاش هستند بهترین مدل برای اتم را بهدست آورند. این مدل بهدست آمده باید به مدل اتمها در دنیای واقعی بسیار نزدیک باشد.
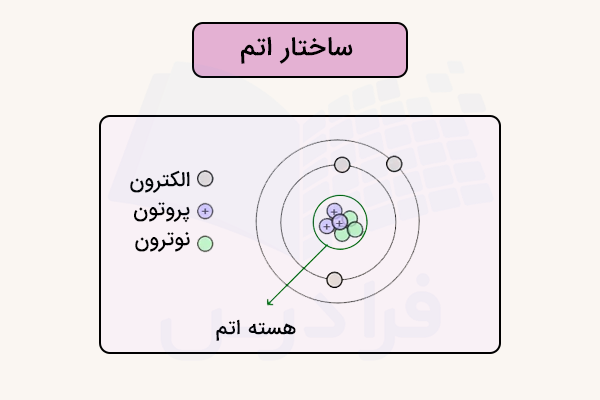
گفتیم این ذرات به صورت مستقل در جهان وجود ندارند و از قرار گرفتن کنار هم و پیوستن به یکدیگر ساختارهای مختلفی را تشکیل میدهند. در سادهترین حالت، مولکول تشکیل خواهد شد. آیا میدانید مولکول چیست؟ مولکولها از دو یا بیشتر از دو اتم تشکیل شدهاند که با استفاده از پیوندهای شیمیایی در کنار یکدیگر قرار گرفتهاند. این ذرات ممکن است با استفاده از دایره توصیف شوند. در مرکز این دایره، هسته قرار دارد. هسته از ذراتی به نام پروتونها و نوترونها تشکیل شده است.
تعریف اتم در شیمی چیست ؟
اتم کوچکترین ذره تشکیلدهنده عنصر است که ممکن است به صورت مستقل وجود داشته یا نداشته باشد، اما در واکنشهای شیمیایی همیشه شرکت میکند. این ذرات به صورت کوچکترین واحد تشکیلدهنده عنصر با خواص مشابه آن، تعریف میشود. اتم نیز از ذرات زیراتمی ساخته شده است که نمیتوانند ساخته یا تخریب شوند. اتمهای یک عنصر مشخص، یکسان هستند و عنصرهای مختلف، اتمهای مختلفی دارند. به عنوان مثال، عنصر کربن را در نظر بگیرید. این عنصر از اتمهای کربن ساخته شده است و تمام آنها یکسان هستند. اکنون دو عنصر نیتروژن و کربن را در نظر بگیرید. هر کدام از دو عنصر نیتروژن و کربن به ترتیب از اتمهای نیتروژن و کربن تشکیل شدهاند، اما اتمهای تشکیلدهنده هر یک از این دو عنصر با یکدیگر متفاوت هستند.
واکنش شیمیایی هنگامی رخ میدهد که اتمها در عنصری بازآرایی شوند. این ذرات از سه نوع ذره بنیادی تشکیل شدهاند:
- پروتون
- نوترون
- الکترون
وزن نوترونها و پروتونها تقریبا مشابه یکدیگر است، اما از وزن الکترون در مقابل وزن این دو ذره میتوان چشمپوشی کرد. بار الکتریکی پروتون مثبت، بار الکتریکی الکترون منفی و بار الکتریکی نوترون خنثی است. در اتم، تعداد الکترونها و پروتونها با یکدیگر برابر و بنابراین در حالت کلی اتم از نظر با الکتریکی خنثی است. گفتیم اگر اتم را دایرهای کوچک در نظر بگیریم، هسته در مرکز آن قرار میگیرد. هسته این ذرات از پروتونها و نوترونها تشکیل شده است. در نتیجه، بار الکتریکی آن مثبت خواهد بود. الکترونها ناحیهای از فضا را در اطراف هسته اشغال میکنند. از این رو، بیشتر جرم اتم داخل هسته متمرکز شده است.
به مرکز اتم، هسته گفته میشود. وزن این ذرات به طور تقریبی برابر وزن هسته است، زیرا میتوان از جرم الکترونهای اطراف هسته در مقابل جرم هسته، صرفنظر کرد. نوترون از نظر بار الکتریکی خنثی و جرم آن برابر یک واحد است. همچنین، پروتون بار الکتریکی مثبت دارد و جرم آن همانند نوترون، برابر یک واحد تعریف میشود. در ادامه عدد اتمی و عدد جرمی را تعریف خواهیم کرد.
عدد اتمی و عدد جرمی چیست ؟
عدد اتمی (Z) یک عنصر با استفاده از تعداد پروتونهای داخل آن، تعیین میشود. با استفاده از عدد اتمی میتوان یک عنصر را از عنصر دیگر تشخیص داد. عدد جرمی (A) عنصر به صورت تعداد پروتونها و نوترونهای تشکیل دهنده آن عنصر، تعریف میشود. جمع عدد جرمی و عدد اتمی یک اتم برابر با تعداد کل ذرات زیراتمی داخل آن اتم است. عدد جرمی، جرم هسته اتم بر حسب واحد وزن اتمی (Atomic Mass Unit | amu) را مشخص میکند.
در جدول تناوبی، عنصرها به گونهای قرار گرفتهاند که عدد اتمی و عدد جرمی آنها افزایش مییابد. برای درک بهتر مفاهیم عدد اتمی و عدد جرمی باید به ساختار این ذرات توجه کنیم. در مطالب بالا گفتیم که اتم از سه ذره بنیادی پروتون، الکترون و نوترون تشکیل شده است. به تصویر زیر دقت کنید. در طی سالهای گذشته تاکنون، مدلهای مختلفی برای این ذرات پیشنهاد شده است که در مورد آنها در ادامه صحبت خواهیم کرد. در یکی از این مدلهای اتمی، الکترونها در مدارها یا لایههایی به دور هسته قرار گرفتهاند. به تعداد الکترونها در بیرونیترین لایه، الکترونهای ظرفیت گفته میشود. به طور مشابه، تعداد پروتونها و نوترونها تعیینکننده عدد اتمی و عدد جرمی این ذرات هستند.
ویژگیهای عدد اتمی عبارت هستند از:
- عدد اتمی برابر تعداد پروتونهای داخل هسته این ذرات است.
- عدد اتمی با Z نشان داده میشود.
- اتمهای یک عنصر مشخص دارای تعداد پروتونهای یکسان، و در نتیجه عدد اتمی برابر هستند.
- اتمهای عنصرهای متفاوت، عددهای اتمی متفاوتی دارند.
- به اتمهای کربن توجه کنید. عدد اتمی آنها برابر ۶ است. اما اتمهای اکسیژن ۸ پروتون در هسته خود دارند. بنابراین عدد اتمی آنها برابر ۸ است.
در ادامه به ویژگیهای عدد جرمی توجه کنید:
- عدد جرمی اتم برابر جمع تعداد پروتونها و نوترونهای آن است.
- عدد جرمی با حرف انگلیسی A نمایش داده میشود.
- از آنجایی که پروتونهای و نوترونها در هسته این ذرات قرار گرفتهاند، به آنها نوکلئون گفته میشود.
- اتم کربن را در نظر بگیرید. گفتیم عدد اتمی آن برابر ۶ است. آیا میدانید عدد جرمی آن چه مقدار است؟ عدد جرمی برابر با جمع تعداد پروتونها و نوترونهای داخل اتم کربن و مقدار آن برابر ۱۲ است.
- در حالیکه تعداد پروتونها در تمام اتمهای عنصر ثابت باقی میماند، تعداد نوترونهای آن میتواند تغییر کند. بنابراین، اتمهای داخل عنصر میتوانند عددهای جرمی متفاوتی داشته باشند که به آنها ایزوتوپ گفته میشود.
- به طور تقریبی میتوان از جرم الکترون صرفنظر کرد. در نتیجه، جرم اتمی این ذرات برابر عدد جرمی آن است.
اکنون میتوانید تفاوتهای عددهای اتمی و جرمی را به راحتی بیان کنید. جدول زیر نحوه یافتن ظرفیت، عدد اتمی و عدد جرمی در اتم را بیان میکند.
| کمیت | نحوه یافتن |
| ظرفیت | تعداد الکترونهای بیرونیترین لایه |
| عدد اتمی | تعداد پروتونها |
| عدد جرمی | جمع تعداد پروتونها و نوترونها |
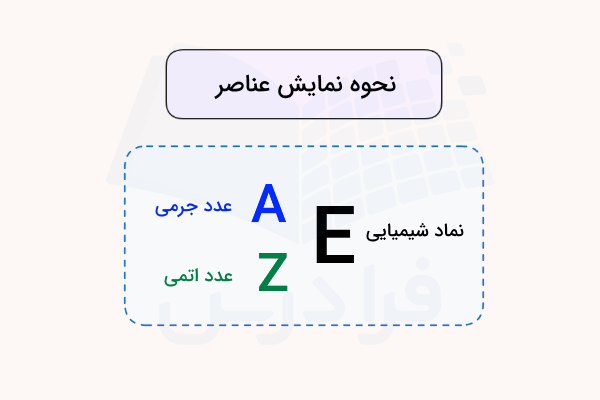
نماد اتم چیست ؟
برای نوشتن نماد اتمی مشخص، به دانستههای زیر نیاز داریم:
- نماد عنصر موردنظر
- عدد جرمی
- عدد اتمی
برای بهدست آوردن عدد اتمی یا عدد جرمی، به تعداد کل پروتونها و نوترونهای آن عنصر نگاه میکنیم. به عنوان مثال، عنصر کربن به صورت زیر نوشته میشود:
نحوه محاسبه تعداد نوترون های اتم چیست ؟
اگر تعداد پروتونها و عدد جرمی عنصری را بدانیم، به سادگی با کم کردن عدد اتمی از عدد جرمی، تعداد نوترونهای آن عنصر را بهدست میآوریم.
مثال محاسبه تعداد نوترون ها
اتمی دارای عدد اتمی ۹ و عدد جرمی ۱۹ است.
- تعداد پروتونهای این اتم را بهدست آورید.
- تعداد نوترونهای آن را محاسبه کنید.
- تعداد الکترونهایی که به دور هسته اتم میچرخند را بهدست آورید.
پاسخ: برای حل این مثال، به تعریف عدد جرمی و عدد اتمی توجه میکنیم.
قسمت ۱: عدد اتمی این عنصر برابر ۹ است، در نتیجه تعداد پروتونهای آن نیز برابر ۹ خواهد بود. در تعریف عدد اتمی داشتیم:
عدد اتمی = تعداد پروتونهای موجود در اتم
قسمت ۲: تعداد نوترونها در این اتم برابر ۱۰ است. برای بهدست آوردن تعداد نوترونها، عدد اتمی را از عدد جرمی کم میکنیم:
تعداد نوترونها = (پروتونها + نوترونها) - پروتونها
قسمت ۳: تعداد الکترونها در این اتم برابر ۹ است. زیرا، در یک اتم همواره تعداد الکترونها و پروتونها با یکدیگر برابر هستند.
مثال تعیین دسته بندی عناصر و به دست آوردن تعداد الکترون ها، پروتون ها و نوترون ها
اتمهای زیر را در نظر بگیرید. با مراجعه به جدول تناوبی، تعداد الکترونها، پروتونها و نوترونهای آنها را به همراه دستهبندی هر یک از این عناصر بنویسید.
- جیوه
- پلاتین
- برم
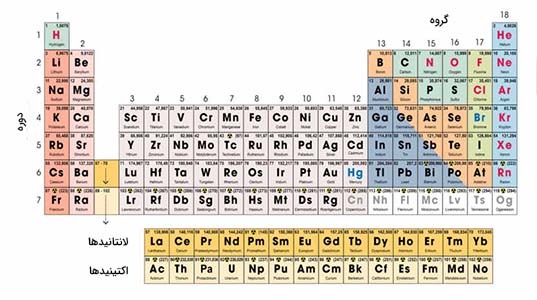
پاسخ: برای پاسخ به این پرسش، به جدول تناوبی فوق مراجعه میکنیم.
قسمت ۱: جیوه با نماد Hg نشان داده میشود و در گروه فلزات واسطه قرار دارد. این عنصر ۸۰ الکترون، ۸۰ پروتون و ۱۲۱ نوترون دارد.
قسمت ۲: پلاتین با نماد Pt نشان داده میشود و در گروه فلزات واسطه قرار دارد. این عنصر ۷۸ الکترون، ۷۸ پروتون و ۱۱۷ نوترون دارد.
قسمت ۳: برم با نماد Br نشان داده میشود و در گروه هالوژنها قرار دارد. این عنصر ۳۵ الکترون، ۳۵ پروتون و ۴۵ نوترون دارد.
مثال تعیین عنصر و به دست آوردن تعداد الکترون ها، پروتون ها و نوترون ها
با توجه به عبارتهای زیر، نام عنصر موردنظر را مشخص نمایید.
- کدام عنصر ۲۵ پروتون دارد؟
- کدام عنصر صفر نوترون دارد؟
- کدام عنصر ۸۳ الکترون دارد؟
پاسخ: برای پاسخ به این مثال میتوان به جدول تناوبی مثال قبل مراجعه کرد:
- منگنز
- هیدروژن
- بیسموت
مثال تعیین تعداد ذرات زیراتمی
برای هر یک از عنصرهای داده شده در ادامه، تعداد ذرات زیراتمی را مشخص کنید.
- Zn-67
- رادیوم
- کاتیون آلومینیوم
- آنیون فسفر
پاسخ: قبل از پاسخ به این مثال، به اختصار در مورد یون، آنیون و کاتیون صحبت خواهیم کرد. در مطالب فوق عنوان شد که اتمهای عنصرها در حالت عادی از نظر بار الکتریکی خنثی و در آنها تعداد الکترونها با پروتونها برابر هستند. هنگامی که این ذرات یا گروهی از اتمها یک یا بیشتر از یک بار الکتریکی منفی یا مثبت داشته باشند، به آنها یون گفته میشود. به یونهای بار مثبت، کاتیون، و به یونهای بار منفی، آنیون، میگوییم.
پس از آشنایی با تعریف آنیون و کاتیون، مثال داده شده را حل میکنیم:
- در این قسمت تعداد الکترونها، پروتونها و نوترونهای عنصرِ روی خواسته شده است. تعداد پروتونهای این عنصر برابر ۳۰ است. از آنجایی که اتم این عنصر از نظر بار الکتریکی خنثی است، تعداد الکترونهای آن با تعداد پروتونهای آن یکسان و برابر ۳۰ است. همچنین، تعداد نوترونهای آن برابر عدد ۳۷ است.

- اتم رادیوم نیز از نظر بار الکتریکی خنثی است و تعداد الکترونها و پروتونهای آن با یکدیگر برابر و مساوی ۸۸ هستند. همچنین، این اتم ۱۳۸ نوترون دارد.

- در این قسمت باید تعداد ذرات زیراتمی برای کاتیونِ آلومینیوم را بهدست آوریم. گفتیم به اتم باردار یون و اگر بار آن مثبت باشد، کاتیون میگوییم. آلومینیوم در گروه سوم و اصلی جدول تناوبی قرار دارد. تعداد الکترونهای لایه ظرفیت یا بیرونیترین لایه آن برابر ۳ است. این عنصر با از دست دادن سه الکترون آخرین لایه به کاتیون آلومینیوم تبدیل میشود.تعداد پروتونهای اتم کاتیون آلومینیوم برابر ۱۳ است. آیا تعداد الکترونهای آن نیز برابر ۱۳ خواهد بود؟ خیر، زیرا این اتم ۳ الکترون از دست داده است. در نتیجه، تعداد الکترونهای آن از تعداد پروتونها کمتر و برابر ۱۰ است. کاتیون یا آنیون بودن یک اتم بر تعداد نوترونهای آن تاثیری نخواهد داشت، بنابراین، کاتیون آلومینیوم ۱۴ نوترون دارد. در کاتیون این ذرات، تعداد الکترونها از تعداد پروتونها کمتر است.
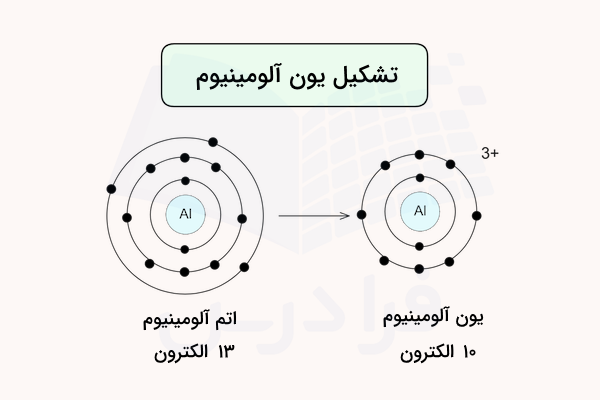
تشکیل یون آلومینیوم - در این قسمت از مثال فوق، تعداد ذرات زیراتمی را برای آنیون فسفر محاسبه میکنیم. فسفر در گروه پنجم و اصلی جدول تناوبی قرار دارد و با به دست آوردن ۳ الکترون، لایه ظرفیت خود را کامل میکند. بنابراین، این اتم با بهدست آوردن سه الکترون به آنیون فسفر تبدیل خواهد شد. از این رو، تعداد پروتونهای این اتم برابر ۱۵ و تعداد الکترونهای آن بیشتر از تعداد پروتونها و برابر ۱۸ خواهد بود. آنیون فسفر ۱۶ نوترون دارد.
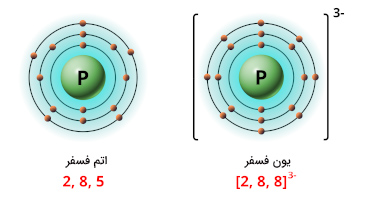
اکنون میتوانیم به پرسش اتم چیست به سادگی و به زبان ساده پاسخ دهیم. همچنین، با مفاهیم عدد اتمی و عدد جرمی و نحوه محاسبه الکترونها، پروتونها و الکترونهای این ذرات آشنا شدیم. در ادامه، در مورد ایزوتوپهای اتم و تعریف آن آشنا خواهیم شد.
ایزوتوپ چیست ؟
ایزوتوپها اعضای خانواده یک عنصر هستند که در آنها تعداد پروتونها یکسان ولی تعداد نوترونها متفاوت است. به بیان دیگر، ایزوتوپها عنصرهای متفاوتی هستند که به دلیل تفاوت در تعداد کل نوترونهای هسته، اعداد نوکلئونی متفاوتی دارند. ایزوتوپهای این ذرات دارای دو ویژگی اصلی به صورت زیر هستند:
- تعداد پروتونهای یکسان
- تعداد نوترونهای متفاوت
همانطور که میدانیم، تعداد پروتونهای داخل هسته عدد اتمی عنصر در جدول تناوبی را مشخص میکند. به عنوان مثال، کربن ۶ پروتون دارد و عدد اتمی آن برابر ۶ است. در حالت طبیعی، عنصر کربن دارای ۳ ایزوتوپ است:
- کربن ۱۲ که ۶ نوترون دارد.
- کربن ۱۳ که ۷ نوترون دارد.
- کربن ۱۴ که ۸ نوترون دارد.
در همه ایزوتوپهای کربن، تعداد پروتونها یکسان و برابر ۶ است. ذکر این نکته مهم است که مشخصات ایزوتوپ با اضافه شدن تنها یک نوترون، به طور قابلملاحظهای تغییر خواهد کرد. ایزوتوپ کربن ۱۲، پایدار است و هرگز دچار تجزیه رادیواکتیوی نخواهد شد. اما، ایزوتوپ کربن ۱۴ ناپایدار است و نصف این ماده پس از گذشت مدت زمان ۵۳۷۰ سال، واپاشی خواهد شد.
نمایش ایزوتوپ
ایزوتوپها مشخصات منحصربهفردی دارند. از این ویژگیها برای کاربردهای تشخیصی و درمان استفاده میشود.
در حالت کلی، ایزوتوپها به دو شکل نمایش داده میشوند:
- نام عنصر موردنظر را همراه با خط تیره (-) و عدد جرمی آن مینویسیم. به عنوان مثال، اورانیوم - ۲۳۵ و اورانیوم - ۲۳۹ دو ایزوتوپ متفاوت عنصر اورانیوم هستند.
- نشانهگذاری AZE (نوشتن نام عنصر به همراه عدد اتمی و عدد جرمی) دنبال شود. به عنوان مثال، ایزوتوپ اورانیوم - ۲۳۵ به صورت و اورانیوم - ۲۳۹ به صورت نوشته میشوند.
تصویر زیر نشاندهنده ایزوتوپهای پایدار اتم هیدروژن است.
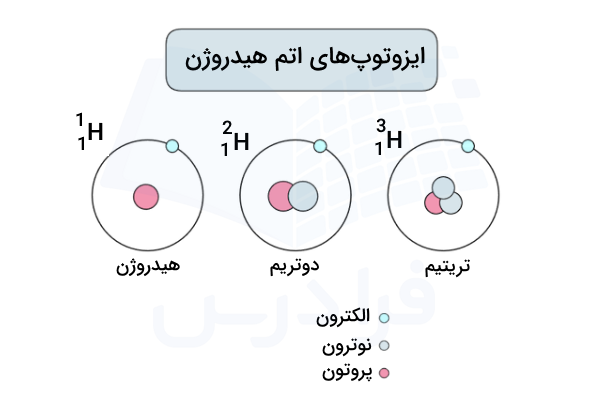
در مطالب فوق در مورد نحوه بهدست آوردن تعداد نوترونهای این ذرات صحبت کردیم. به عنوان مثال به ایزوتوپ کربن - ۱۲ توجه کنید. عدد اتمی کربن برابر ۶ است. بنابراین، تعداد کل نوترونهای در این ایزوتوپ برابر ۶ خواهد بود.
برخی از ایزوتوپها پایدار هستند و برخی از آنها بعد از گذشت مدت زمان مشخصی واپاشی میشوند. این ایزوتوپها رادیواکتیو و به رادیوایزوتوپها معروف هستند. کربن - ۱۴، تریتیوم (هیدروژن - ۳)، کلر - ۳۶، اورانیوم - ۲۳۵ و اورانیوم - ۲۳۹ مثالهایی از رادیوایزوتوپها هستند. نیمه عمر برخی از ایزوتوپها بسیار طولانی است (در حدود صدها تا میلیونها سال). به این ایزوتوپها، هستهها یا ایزوتوپهای پایدار گفته میشود. کربن - ۱۲، کربن - ۱۳، اکسیژن - ۱۶، اکسیژن - ۱۷، و اکسیژن - ۱۸ مثالهایی از هستههای پایدار هستند. هستههای اولیه به هستههایی گفته میشود که از آغاز تشکیل منظومه شمسی به وجود آمدهاند. از میان ۳۳۹ ایزوتوپ موجود بر روی زمین، تعداد ۲۸۶ ایزوتوپ به عنوان ایزوتوپهای اولیه شناخته شدهاند.
ویژگی های ایزوتوپ
نکات مهمی در مورد ایزوتوپها وجود دارند که به صورت زیر خلاصه شدهاند:
- تمام عنصرها ایزوتوپ دارند.
- دو نوع ایزوتوپ پایدار و ناپایدار (رادیواکتیو) وجود دارند.
- ۲۵۴ ایزوتوپ پایدار شناخته شده وجود دارند.
- تمام ایزوتوپهای مصنوعی که در آزمایشگاه ساخته شدهاند ناپایدار و رادیواکتیو هستند.
- برخی از عنصرها تنها میتوانند به شکل ناپایدار وجود داشته باشند (مانند اورانیوم).
- هیدروژن تنها عنصری است که ایزوتوپهای آن اسمهای منحصربهفرد دارند: دوتریوم برای هیدروژن با یک نوترون و تریتیوم برای هیدروژن با دو نوترون.
تاکنون به پرسش اتم چیست به زبان ساده پاسخ دادیم و در مورد ذرات زیراتمی داخل آن صحبت کردیم. در ادامه، کمی در مورد این ذرات زیراتمی خواهیم داد.
ذرات زیر اتمی در اتم چیست ؟
میدانیم اتم نوعی از سه ذره زیراتمی شامل پروتونها، نوترونها و الکترونها ساخته شده است. ذرات دیگری نیز مانند آلفا و بتا در اتم وجود دارند. بر طبق مدل بور (در ادامه در مورد نظریههای اتمی صحبت خواهد شد)، سه ذره اصلی تشکیلدهنده اتم به شکل زیر در عنصر هلیوم نشان داده شدهاند. بیشتر جرم اتم در هسته آن قرار دارد. هسته از پروتونها و نوترونها تشکیل شده است. در نتیجه، تمام بار مثبت اتم در هسته آن قرار گرفته است. الکترونها با بار منفی در بیرون هسته قرار دارند.

جدول زیر مشخصات این سه ذره زیراتمی مانند بار الکتریکی، جرم، بار اتمی، جرم اتمی و اسپین را نشان داده است.
| مشخصات | پروتون | نوترون | الکترون |
| بار الکتریکی بر حسب کولن | خنثی | ||
| بار اتمی | 1+ | 0 | 1- |
| جرم بر حسب گرم | |||
| جرم اتمی بر حسب Au | 1/0073 | 1/0078 | 0/00054858 |
| اسپین |
پروتون چیست ؟
پروتونها در سال 1919 توسط «ارنست رادرفورد» (Ernest Rutherford) در آزمایش ورقه طلا کشف شدند. او در این آزمایش ذرات آلفا (هستههای هلیوم) را به ورقهای از جنس طلا تاباند. پس از برخورد ذرات آلفا، ذرات آلفای مثبت آشکار شدند. رادرفورد با انجام این آزمایش به این نتیجه رسید که پروتونها در هسته وجود دارند و بار الکتریکی آنها مثبت است. تعداد پروتونهای در اتم تعیینکننده عدد اتمی آن اتم خواهد بود.
الکترون چیست ؟
الکترونها در سال ۱۸۹۷ میلادی توسط «سر جان جوزف تامسون» (Sir John Joseph Thomson) کشف شدند. تامسون پس از انجام آزمایشهای بسیار مانند پرتوهای کاتدی، نسبت جرم بار الکتریکی پرتوهای کاتدی را بهدست آورد. او اثبات کرد پرتوهای کاتدی ذرات بنیادی با بار منفی هستند. بعدها، این پرتوهای کاتدی به عنوان الکترونها شناخته شدند. «رابرت میلیکان» (Robert Milikan) با استفاده از آزمایش قطره روغن، مقدار بار الکتریکی الکترون را محاسبه کرد.
الکترونها در ابر الکترونی قرار گرفتهاند. این ابر در ناحیه اطراف هسته اتم قرار گرفته است. احتمال یافتن الکترون در ناحیههای نزدیک به هسته بیشتر است. الکترونها به صورت نشان داده میشوند. بار الکتریکی این ذرات منفی و از نظر اندازه برابر اندازه بار الکتریکی پروتونها، اما، جرم آنها در مقایسه با پروتون و نوترون، بسیار کمتر است. بنابراین، در بیشتر موارد از جرم الکترون چشمپوشی میشود. اگر در اتمی تعداد پروتونها با تعداد الکترونها برابر نباشد، اتم از نظر الکتریکی خنثی نیست و به یون تبدیل میشود.
نوترون چیست ؟
نوترونها در سال ۱۹۳۲ میلادی توسط «جیمز چادویک» (James Chadwick) کشف شدند. نوترونها به همراه پروتونها در هسته اتم قرار دارند و بیشتر جرم اتم را تشکیل میدهند. تعداد نوترونها از تفاضل تعداد پروتونها و عدد جرمی بهدست میآید. همچنین، تعداد نوترونها در عنصر، ایزوتوپ اتم و پایداری آن را تعیین میکند. به طور معمول، تعداد نوترونها با تعداد پروتونها برابر نیست.
در اتم علاوه بر ذرات زیراتمی الکترون، نوترون و پروتون، ذرات دیگری نیز وجود دارند. بسیاری از این ذرات از طریق تجزیه رادیواکتیو خارج میشوند. به این نکته توجه داشته باشید که در بسیاری از شکلهای تجزیه رادیواکتیو، پرتوهای گاما منتشر میشوند که به عنوان ذره در نظر گرفته نخواهند شد.
ذرات آلفا چیست ؟
ذرات آلفا به صورت ، یا تنها نشان داده میشوند. این ذرات، هستههای هلیوم با دو پروتون و دو نوترون هستند. اسپین کلی ذره آلفا برابر صفر است. واپاشی آلفا فرایندی است که در طی آن، اتم ذرات آلفا را منتشر میکند و به عنصر جدیدی تبدیل میشود. این فرایند تنها در عناصری با هستههای رادیواکتیو بزرگ رخ میدهد. کوچکترین عنصری که ذرات آلفا منتشر میکند، عنصر شماره ۵۲ یعنی تلوریم است.
در حالت کلی، ذرات آلفا آسیبرسان نیستند. این ذرات به سادگی با استفاده از یک ورقه یا پوست فرد میایستند.

ذرات بتا چیست ؟
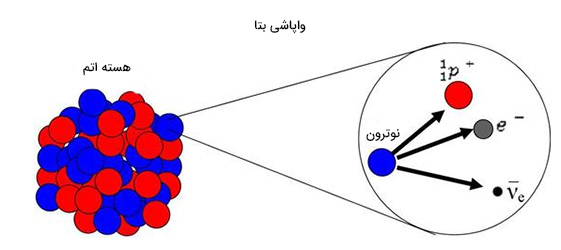
ذرات بتا، الکترونها یا پوزیترونهای آزاد با انرژی و سرعت بالا هستند. در نتیجه، یکی از نوترونها به پروتون، الکترون و ضد نوترینو واپاشیده میشود. پروتون، داخل هسته باقی میماند، اما الکترون و ضد نوترینو منتشر خواهند شد. به این الکترون، ذره بتا گفته میشود:
در فرایند واپاشی بتای فوق:
- n نشاندهنده نوترون
- نشاندهنده پروتون
- نشاندهنده الکترون یا ذره بتا
- نشاندهنده ضد نوترینو
هستند.
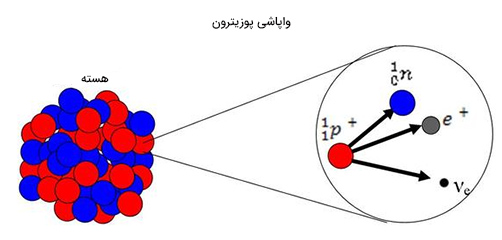
انتشار یا پوزیترون چیست ؟
انتشار پوزیترون هنگامی رخ میدهد که تعداد پروتونها زیادتر از حد معمول باشد. در این صورت، یک پروتون به یک نوترون، یک پوزیترون و یک نوترینو تبدیل میشود. پس از تولید این ذرات، نوترون در هسته باقی میماند، اما پوزیترون و نوترینو منتشر میشوند. در اینجا، به پوزیترون ذره بتا گفته میشود. واکنش این فرایند به صورت زیر نوشته خواهد شد:
در واکنش فوق، n برابر نوترینو، برابر پروتون، برابر پوزیترون و برابر نوترینو هستند.
مثال ذرات زیراتمی
تعداد پروتونها، الکترونها، نوترونها و پوزیترونها را در هر یک از موارد داده شده بهدست آورید:
پاسخ: تعداد ذرات زیراتمی هر یک از موارد فوق در ادامه آورده شده است:
-
- تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر ۶، ۸ و ۶ است.
-
- تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر ۲، ۲ و صفر است. ذره آلفا میتواند به صورت نوشته شود. تعداد پروتونها برابر ۲ است، زیرا عنصر موردنظر هلیوم است. همچنین، تعداد الکترونها برابر صفر است زیرا ۰=۲-۲. تعداد نوترونها نیز برابر ۲ است زیرا ۲=۲-۴.
-
- تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر ۱۷، ۱۸ و ۱۸ است. همان گونه که دیده میشود تعداد الکترونها و پروتونها با یکدیگر برابر نیستند، زیرا در اینجا یون کلر با بار -۱ داریم.
-
- در اینجا، تعداد پروتونها، نوترونها، الکترونها و پوزیترونها به ترتیب برابر صفر، صفر، صفر و یک هستند.
-
- تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر صفر، صفر و یک هستند.
-
- تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر ۱۲، ۱۲ و ۱۰ هستند. مورد داده شده یون منیزیوم با بار ۲+ است.
-
- تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر ۲۷، ۳۳ و ۲۷ هستند.
-
- تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر ۱، ۲ و ۱ هستند. عنصر مورد نظر هیدروژن است، بنابراین تعداد پروتونهای آن برابر ۱ است. همچنین، چون اتم از نظر الکتریکی خنثی است، تعداد الکترونها، مساوی تعداد پروتونها و برابر یک است. برای بهدست آوردن تعداد نوترونها، عدد اتمی را از عدد جرمی کم میکنیم.
-
- در اینجا، تعداد پروتونها، نوترونها و الکترونها به ترتیب برابر ۱۸، ۲۲ و ۱۸ هستند.
-
- مثال داده شده نوترون آزاد و دارای صفر پروتون، یک نوترون و صفر الکترون است.
تاکنون با مفاهیم اتم چیست و ذرات زیراتمی به زبان ساده آشنا شدیم. در ادامه، در مورد مدلهای اتمی مختلف صحبت خواهیم کرد.
مدل های اتمی
مدلهای مختلفی برای اتم و ساختار آن ارائه شده است که مهمترین آنها عبارت هستند از:
- مدل اتمی دالتون
- مدل اتمی کیک کشمشی
- مدل اتمی رادرفورد
- مدل اتمی بور
- مدل اتمی ابر الکترونی/مدل اتمی کوانتومی
قبل از آنکه با مدلهای اتمی فوق آشنا شوید، به جدولهای زیر دقت کنید. در این جدولها خلاصهای از دستاوردها و محدودیتهای این مدلها بیان شده است و به شما دید کلی در مورد مدلهای اتمی خواهد داد. در ادامه، در مورد هر یک از این مدلها توضیح داده میشود.
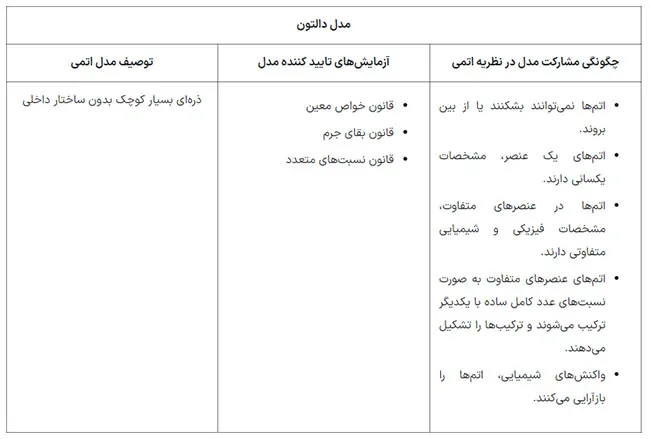
مدل تامسون در تصویر زیر به طور خلاصه توضیح داده شده است.
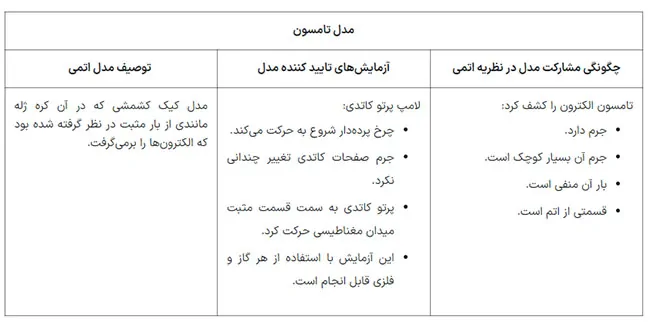
در تصویر زیر در مورد مدل اتمی رادرفورد به طور خلاصه توضیح داده شده است.
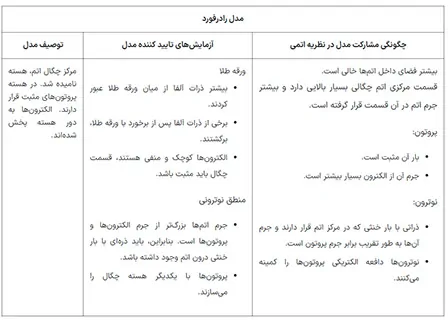
مدل اتمی بور و دستاورهای آن به طور خلاصه در تصویر زیر نشان داده شده است.

تصویر نشان داده شده در ادامه در مورد آخرین مدل اتمی، یعنی مدل اتمی شرودینگر، به اختصار توضیح داده است.

مدل اتمی دالتون
در حدود سال ۱۸۰۰ میلادی، شیمیدان و فیزیکدانی انگلیسی به نام «جان دالتون» (John Dalton) به نظریه قدیمی «دموکریت» (Democritus) در مورد اتم مراجعه کرد. دالتون در خانوادهای از طبقه کارگر به دنیا آمد و بزرگ شد. او از طریق تدریس به دانشآموزان، امرار معاش میکرد و در اوقات فراغت به پژوهش در زمینه موردعلاقه خود میپرداخت. پژوهشهای انجام شده توسط این شیمیدان به یکی از مهمترین نظریههای مطرح شده در علوم منتهی شد. بر طبق نتایج به دست آمده از این پژوهشها، وجود اتم به اثبات رسید.

بر طبق نظریه اتمی دالتون، تمام مواد از اتمها ساخته شدهاند. در حالیکه اندازه و جرم اتمهای عنصری مشخص یکسان هستند، عنصرهای متفاوت از اتمهایی با اندازهها و جرمهای مختلف تشکیل شدهاند.
قانون های بنیادی نظریه اتمی
قبل از آنکه در مورد مدل اتمی دالتون صحبت کنیم، ابتدا در مورد قانونهای نظریه اتمی صحبت خواهیم کرد.
قانون بقای جرم
بر طبق قانون بقای جرم، تغییر کلی جرم واکنشدهندهها و محصولات واکنش قبل و بعد از واکنش شیمیایی برابر صفر است. این جمله بدان معنا است که جرم نه به وجود میآید و نه از بین میرود. به بیان دیگر، جرم کل در واکنش شیمیایی ثابت باقی میماند. این قانون در سال ۱۷۸۹ میلادی توسط «آنتوان لاووازیه» (Antonie Lavoisier) به صورت فرمولبندی نوشته شد. بعدها مشخص شد که این قانون کمی نادرست است، زیرا در واکنشهای شیمیایی جرم میتواند به گرما و انرژی پیوندی تبدیل شود. گرچه، جرم از دست رفته بسیار کوچک خواهد بود و چندین مرتبه کوچکتر از جرم واکنشدهندهها است. بنابراین، این قانون با تقریب بسیار خوبی صحیح است.
قانون نسبتهای ثابت
بر طبق این قانون، هنگامی که پیوندی شکسته میشود، نسبت جرم عنصرهای تشکیلدهنده یکسان باقی خواهد ماند. به بیان دیگر، در یک ترکیب شیمیایی، عنصرها همواره به نسبت مشخصی بر حسب جرم وجود دارند. این قانون توسط «جوزف لوییس» (Joseph Louis) در سال ۱۷۹۹ میلادی اثبات شد.
قانون نسبتهای چندگانه
بر طبق این قانون، هنگامی که دو عنصر دو یا بیشتر از دو ترکیب را تشکیل میدهند، نسبت جرم عنصرهای سازنده در هر ترکیب میتواند به صورت عددهای کوچک و صحیح بیان شود. این قانون توسط دالتون مطرح شد.
فرضیههای نظریه اتمی دالتون عبارت هستند از:
- تمام مواد از ذرات کوچک و غیرقابل مشاهدهای به نام اتمها ساخته شدهاند.
- اندازه، جرم و دیگر مشخصات تمام اتمهای سازنده یک عنصر مشخص یکسان هستند. اما، اتمهای عنصرهای مختلف، اندازه، جرم و ویژگیهای متفاوتی دارند.
- اتمها نه به وجود میآیند و نه از بین میروند. به علاوه، اتمها نمیتوانند به ذرات کوچکتری تقسیم شوند.
- اتمهای عنصرهای متفاوت میتوانند با یکدیگر با نسبتهای ثابت و صحیح، ترکیب شوند.
- اتمها میتوانند در واکنشهای شیمیایی بازآرایی، ترکیب یا جدا شوند.
دالتون معتقد بود که نظریه اتمی میتواند به خوبی توضیح دهد که چرا آب گازهای متفاوت با نسبتهای مختلف را جذب میکند. به عنوان مثال، دالتون به این نکته پی برد که آب گاز دیاکسیدکربن را بسیار بهتر از گاز نیتروژن جذب میکند.
محدودیت های نظریه اتمی دالتون
نظریه دالتون با محدودیتهای مختلفی همراه بود.
- در این نظریه، ذرات زیراتمی مانند الکترون، پروتون و نوترون در نظر گرفته نشدند. دالتون بیان کرد که اتمها غیرقابل مشاهده هستند. اما، پس از کشف ذرات زیراتمی، این فرضیه زیر سوال رفت.
- در این نظریه، ایزوتوپها در نظر گرفته نشدند. بر طبق این نظریه، جرم و چگالی اتمها در عنصری مشخص یکسان هستند، اما ایزوتوپهای متفاوت عنصرها، جرمهای اتمی متفاوتی دارند (به عنوان مثال، هیدروژن، دوتریوم و تریتیوم).
- در این نظریه، ایزوبارها در نظر گرفته نشدهاند. بر طبق نظریه اتمی دالتون، جرمهای این ذرات در عنصرهای متفاوت باید با یکدیگر فرق داشته باشند. اما، گاهی ممکن است عدد جرمی دو عنصر مختلف، یکسان باشد. به این اتمها ایزوبار گفته میشود (به عنوان مثال، و ).
- برای تشکیل ترکیبهای مختلف، نیازی نیست که عنصرها با نسبتهای کوچک و صحیح با یکدیگر ترکیب شوند. در برخی از ترکیبهای آلی پیچیده نسبتهای ساده اتمهای تشکیل شونده رعایت نشده است (مانند شکر).
- در این نظریه آلوتروپها در نظر گرفته نشدهاند. به عنوان مثال، الماس و گرافیت تنها از اتمهای کربن ساخته شدهاند، اما مشخصات آنها با یکدیگر بسیار متفاوت هستند. نظریه اتمی دالتون قادر به توضیح این تفاوت نیست.
شکاف اصلی نظریه دالتون بعدها توسط آووگادرو تصحیح شد. بر طبق اصل آووگادرو، حجمهای مساوی از هر دو گاز دلخواهی، در دما و فشار یکسان، از تعداد مولکولهای یکسانی تشکیل شدهاند. به بیان دیگر، جرم ذرات گاز بر حجمی که گاز اشغال کرده است، تاثیر نمیگذارند. سالها بعد با انجام آزمایشهای مختلف توسط تامسون، رادرفورد و «نیلز بور» (Neils Bohr)، ساختار کاملتر این ذرات شناخته شد.
در مدلهای اتمی در مبحث اتم چیست با اولین مدل اتمی ارائه شده یعنی مدل اتمی دالتون و کاستیهای آن آشنا شدیم. در ادامه، در مورد مدل ارائه شده تامسون در سال ۱۹۰۴ صحبت میکنیم.

مدل اتمی کیک کشمشی
دموکریت هزاران سال قبل فرض کرد که ذرات بسیار کوچکی به نام اتم وجود دارند. پس از اعلام این فرضیه، مدلهای متفاوتی برای ساختار این ذرات پیشنهاد شد. بسیاری از این مدلها پس از گذشت مدت زمان مشخصی رد و مدلهای پذیرفته شده در طی سالها تکمیل شدند. تا سالها تصور میشد که اتمها از اجزای سازنده کوچکتری تشکیل نشدهاند، اما با پیشرفت علم و استفاده از تکنولوژیهای پیشرفتهتر مشخص شد که اتمها از ذرات کوچکتری ساخته شدهاند. این ذرات به صورت الکترومغناطیسی با یکدیگر برهمکنش میکنند.
تامسون با انجام آزمایشهای جدید در اواخر قرن نوزدهم و اوایل قرن بیستم میلادی نشان داد که این ذرات از ذرات کوچکتری به نام الکترون تشکیل شده است. وجود پروتونها نیز مورد پذیرش قرار گرفته بود، زیرا اتمها از نظر الکتریکی خنثی فرض میشدند. گام بعدی پس از کشف ذرات زیراتمی، یافتن چگونگی آرایش این ذرات داخل اتم بود. یافتن مدل مناسب به دلیل اندازه بسیار کوچک این ذرات، بسیار مشکل بود. بنابراین، دانشمندان مناسبترین مدلهایی را که در ذهن داشتند، پیشنهاد دادند. هدف از یافتن بهترین مدل اتمی، نمایش مشخصات اتم با سادهترین و گویاترین راه ممکن است.
با کشف الکترون، تحول نوینی در مدلهای ارائه شده برای اتم رخ داد. تامسون پس از کشف الکترون، مدل تازهای به نام «مدل کیک کشمشی» را برای این ذرات پیشنهاد داد. در این مدل فرض شده بود که اتم از بیش از یک واحد بنیادی تشکیل شده است. کیک کشمشی در تصویر زیر نشان داده شده است. این کیک مشابه دسری انگلیسی به نام پودینگ آلو تهیه میشود. همان گونه که در تصویر زیر دیده میشود، کشمشها به صورت پراکنده داخل کیک پخش شدهاند. در مدل ارائه شده توسط تامسون، الکترونها نقش کشمشها را بازی میکنند.

در این مدل، الکترونها در کره یکنواختی از بارهای مثبت قرار میگرفتند (مانند قرار گرفتن کشمشها داخل کیک). جنس کره مثبت مانند سوپ غلیظ، ژلهای در نظر گرفته شد. در توضیح این مدل الکترونها تا اندازهای متحرک فرض شده بودند. هنگامی که الکترونها به قسمت خارجی اتم نزدیک میشدند، بار مثبت داخل کره که از بارهای منفی همسایه بزرگتر بود، الکترون را به سمت داخل میکشید، و در نتیجه الکترون به قسمت مرکزی این ذرات برگردانده میشد.
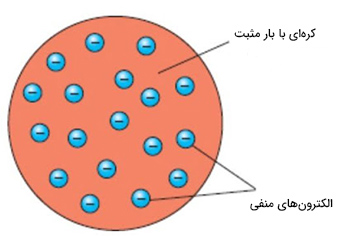
آزمایش تامسون و کشف الکترون
همان گونه که در مطالب فوق عنوان شد، تامسون در اواخر قرن نوزدهم میلادی آزمایشهایی را با استفاده از لامپ پرتو کاتدی انجام داد. لامپ پرتو کاتدی، لوله شیشهای مهروموم شدهای است که بیشتر هوای آن توسط پمپ خلا، تخلیه شده است. ولتاژ بسیار بالایی در دو انتهای لامپ اعمال میشود و پرتوی از ذرات از الکترود کاتدی (الکترود با بار منفی) به سمت الکترود آندی (الکترود با بار مثبت) حرکت خواهند کرد. به این لامپ، لامپ پرتو کاتدی گفته میشود، زیرا منشا پرتو کاتدی، الکترود کاتدی است.
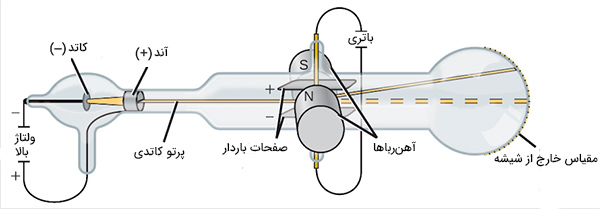
تامسون برای آزمایش مشخصات ذرات از دو صفحه الکتریکی با بارهای مخالف به دور پرتو کاتدی، استفاده کرد. پرتو کاتدی به هنگام عبور از میان این دو صفحه، از صفحه باردار منفی دور و به صفحه باردار مثبت نزدیک شد. این انحراف نشان داد که پرتو کاتدی از ذرات با بار منفی تشکیل شده بود.
همچنین، تامسون برای بهدست آوردن نتایج کاملتر، دو آهن ربا را در دو طرف لوله قرار داد. مشاهده شد که پرتو کاتدی به هنگام عبور از میان میدان مغناطیسی ایجاد شده توسط آهن ربا، منحرف شد. نتایج بهدست آمده از این آزمایش به تامسون در تعیین نسبت جرم به بار ذرات پرتو کاتدی کمک کرد.
نتیجه آزمایش بسیار قابل تامل بود، جرم محاسبه شده برای ذرات داخل پرتو کاتدی بسیار کوچکتر از جرم هر اتم شناخته شدهای بود. تامسون برای کسب اطمینان از نتیجه بهدست آمده، آزمایش را با فلزات مختلفی تکرار کرد. بر طبق یافتههای او، مشخصات پرتو کاتدی، بدون توجه به جنس کاتد مورداستفاده، بدون تغییر باقی ماند. تامسون پس از انجام این آزمایش و تکرار آن با کاتدهایی با جنسهای مختلف، به نتایج زیر دست یافت:
- پرتو کاتدی از ذراتی با بار منفی تشکیل شده است.
- ذرات تشکیلدهنده پرتو کاتدی به عنوان ذرات تشکیلدهنده اتم در نظر گرفته شدند، زیرا جرم هر یک از آنها در حدود جرم اتم هیدروژن است.
- این ذرات زیراتمی میتوانند داخل اتمهای تمام عناصر یافت شوند.
این نتایج در ابتدا بسیار چالشبرانگیز بودند، اما کمکم توسط دانشمندان دیگر پذیرفته شدند.
کاستی های مدل اتمی کیک کشمشی
همان گونه که در مورد مدل کیک کشمشی گفته شد، الکترونها داخل کرهای با بار مثبت پخش شدهاند و جهت نیروی کل وارد شده بر این الکترونها به سمت مرکز کره است. الکترونها با بار منفی یکدیگر را دفع میکنند و لایههایی را تشکیل میدهند. مدل ارائه شده توسط تامسون تا چند سال به عنوان مدل اتمی پذیرفته شد. در سال ۱۹۱۱ رادرفورد مدل جدیدی را برای اتم پیشنهاد داد.
مدل کیک کشمشی کاستیهای زیادی داشت. مهمترین آنها عبارت هستند از:
- پایداری اتم با استفاده از این مدل قابل توجیه نبود. همچنین، این مدل نتوانست در مورد اینکه بار مثبت چگونه الکترونهای با بار منفی را داخل اتم نگه میدارد، توضیح مناسبی ارائه دهد. بنابراین، این مدل در مورد مکان قرارگیری هسته در اتم توضیح قابل قبولی نداشت.
- مدل تامسون توضیحی در مورد پراکندگی ذرات آلفا توسط فویلهای فلزی نداد (آزمایش رادرفورد در سال ۱۹۱۱ میلادی).
- هیچ آزمایش تجربی در حمایت و توجیه این مدل انجام نشد.
گرچه مدل کیک کشمشی مدل دقیقی برای ساختار اتمی نبود، اما از آن به عنوان مدل پایه برای پیشرفت مدلهای اتمی دیگر استفاده شد.
تاکنون به پرسش اتم چیست به زبان ساده پاسخ دادیم و در مورد مدلهای اتمی دالتون و کیک کشمشی صحبت کردیم. مدل اتمی کشمشی توسط تامسون در اوایل قرن بیستم میلادی ارائه شد و با انجام آزمایشی توسط رادرفورد در سال ۱۹۱۱ میلادی، به چالش کشیده شد.
مدل اتمی رادرفورد
یکی دیگر از آزمایشهای مهم در مورد اتم، توسط فیزیکدانی نیوزلندی به نام ارنست رادرفورد انجام شد. رادرفورد بیشتر سالهای عمر خود را در کشورهای کانادا و انگلستان گذراند. او در آزمایش معروف خود از ورقه بسیار نازک طلا استفاده کرد، بنابراین این آزمایش به آزمایش ورقه طلا معروف شده است.
رادرفورد پرتویی از ذرات آلفا را به ورقه بسیار نازکی از طلای خالص تاباند. ذرات آلفا هستههای هلیوم () هستند که در فرایندهای مختلف واپاشی رادیواکتیو تولید میشوند. برای تولید این ذرات نیاز به عنصری رادیواکتیو بود. برای این کار، رادرفورد از فلز رادیوم استفاده کرد. او مقداری از این فلز را در جعبهای سربی با سوراخی بسیار کوچک در آن، قرار داد. بیشتر تشعشع توسط سرب جذب شد، اما پرتو نازکی از ذرات آلفا از حفره کوچک خارج و به ورقه طلا تابیده شدند. در این آزمایش آشکارسازهای مختلفی اطراف ورقه طلا قرار داده شدند.
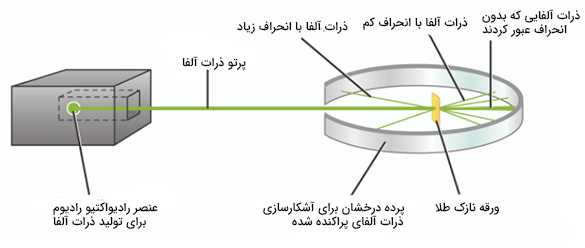
نخستین سوالی که ممکن است مطرح شود آن است که چرا رادرفورد از ورقه طلا استفاده کرد؟ آیا نمیتوانست به جای هزینه اضافی برای خرید طلا، از فلز نیکل استفاده کند؟ باور داشته باشید یا نه، استفاده از طلا به دلیل ذوق سرشار رادرفورد نبود. طلا فلزی به شدت چکشخوار است، بنابراین میتواند به شکل ورقههای بسیار نازک در بیاید. در حقیقت، نازکترین ورقههای طلا میتوانند ضخامتی به کوچکی ۰/۰۰۰۰۴ سانتیمتر داشته باشند. این ضخامت برابر چند صد اتم است. ورقهای به این نازکی لازمه انجام موفقیتآمیز آزمایش رادرفورد بود. اگر ضخامت ورقه طلا از این مقدار بیشتر میبود، ذرات آلفا داخل آن نفوذ نمیکردند.
مدل کیک کشمشی توسط تامسون چند سال قبل از آزمایش رادرفورد ارائه شد. رادرفورد با استفاده از این مدل پیشبینی کرد که بیشتر ذرات آلفای تابیده شده به ورقه طلا، بدون انحراف از مسیر خود از آن عبور میکنند. دلیل این پیشبینی آن بود که بر طبق مدل تامسون، بارهای مثبت در سراسر حجم اتم پخش شده بودند. بنابراین، اندازه و قدرت میدان الکتریکی حاصل از کره باردار مثبت آنقدر زیاد نیست که بر مسیر حرکت ذرات آلفا با جرم و سرعت زیاد، تاثیر بسزایی بگذارد.
نتایج بهدست آمده از این آزمایش قابلتوجه بودند. بر طبق این نتایج، ذرات آلفا پس از تابیده شدن به ورقه آلفا به سه دسته تقسیم شدند:
- بیشتر آنها بدون انحراف و به طور مستقیم از ورقه طلا عبور کردند.
- تعداد کمی از آنها (یک از ۲۰۰۰۰) با زاویهای بیشتر از ۹۰ درجه از مسیر اولیه، منحرف شدند.
- تعداد کمی نیز با زاویه بسیار کوچکی نسبت به مسیر اولیه، منحرف شدند.
رادرفورد در توصیف این نتیجه شگفتانگیز گفت:
این رخداد به همان اندازه باورنکردنی است که گلوله کوچکی را به سمت دستمال کاغذی شلیک کنی و گلوله پس از اصابت به دستمال برگردد و به تو برخورد کند، باورنکردنی است.
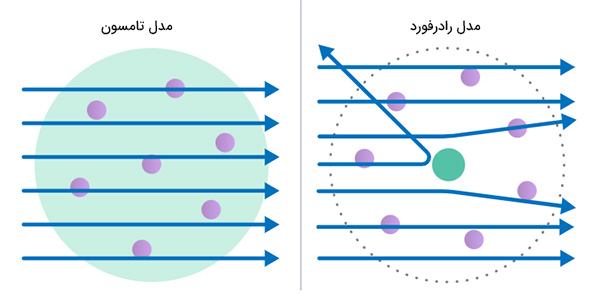
مشاهدات رادرفورد
رادرفورد از نتایج بهدست آماده از آزمایش بسیار شگفتزده شد. او مشاهدات خود را به صورت زیر بیان کرد:
- بخش عمدهای از ذرات آلفای تابیده شده به ورقه طلا بدون هیچ انحرافی از آن عبور کردند. از این مشاهده میتوان این گونه نتیجه گرفت که قسمت بیشتر فضای داخل اتم، خالی است.
- تعدادی از ذرات آلفا پس از عبور از ورقه نازک طلا، با زاویه بسیار کوچکی منحرف میشوند. بنابراین، بار مثبت داخل اتم به صورت یکنواخت پخش نشده و در حجم بسیار کوچکی متمرکز شده است.
- تعداد بسیار کمی از ذرات آلفا پس از برخورد با ورقه طلا، با زاویه ۱۸۰ درجه نسبت به مسیر اولیه بازگشتند. بنابراین، حجم اشغال شده توسط بارهای مثبت در مقایسه با حجم کلی اتم بسیار کوچک است.
بر طبق مشاهدات فوق و نتایج بهدست آمده، رادرفورد مدلی را برای اتم پیشنهاد داد:
- بار مثبت و بیشتر جرم اتم در حجم بسیار کوچکی متمرکز شده است. رادرفورد این ناحیه از اتم را هسته نامید.
- بر طبق مدل رادرفورد، الکترونها با بار منفی، به دور هسته با بار مثبت قرار گرفتهاند. همچنین، رادرفورد ادعا کرد که الکترونها در مسیرهای دایرهای و با سرعت بسیار بالایی به دور هسته میچرخند. او نام این مسیرهای دایرهای را مدار گذاشت.
- الکترونها با بار منفی و هسته با بار مثبت توسط نیروی جاذبه الکترواستاتیکی در کنار یکدیگر قرار گرفتهاند.
آیا مدل رادرفورد، مدل اتمی بدون نقصی بود؟ خیر، این مدل نیز همانند مدل تامسون با سوالاتی مواجه شد که قادر به پاسخ آنها نبود.
کاستی های مدل اتمی رادرفورد
گرچه مدل اتمی رادرفورد براساس نتایج آزمایشگاهی بود، اما این مدل در توضیح برخی مشاهدات ناکام ماند:
- براساس مدل رادرفورد، الکترونها در مسیرهای ثابتی به نام مدار به دور هسته میچرخند. ماکسول به این نتیجه رسیده بود که ذرات باردارِ دارای شتاب، تشعشع الکترومغناطیسی ساطع میکنند. بنابراین، الکترونی که به دور هسته میچرخد، تابش الکترومغناطیسی ساطع میکند. این تشعشع منجر به گرفتن انرژی از حرکت الکترون و در نتیجه کوچکتر شدن مدار حرکت میشود. فاصله حرکت الکترونها از هسته کمتر و کمتر میشود و در نهایت بر روی هسته اتم سقوط میکنند. بر طبق محاسبات انجام شده بر روی مدل رادرفورد، الکترون در مدت زمان کمتر از ثانیه بر روی هسته سقوط میکند. بنابراین، مدل اتمی رادرفورد مطابق با نظریه ماکسول و قادر به توضیح پایداری اتم نیست.
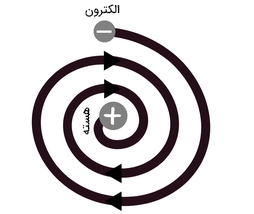
- یکی دیگر از کاستیهای مدل اتمی رادرفورد آن بود که در مورد آرایش الکترونها در اتم توضیحی نداد. بنابراین، این نظریه کامل نبود.
- گرچه مدلهای اتمی اولیه غیردقیق و قادر به توضیح نتایج بهدست آمده نبودند، اما این مدلها پایه و اساس پیشرفت برای مدلهای اتمی بعدی شدند.
گفتیم مدل رادرفورد قادر به توضیح پایداری اتم نیست و بر طبق این مدل، اتم در مدت زمان بسیار کوتاهی از بین خواهد رفت. نیروی کولنی که بین ذرات با بار مخالف بیانگر این موضوع است که هسته مثبت و الکترونهای منفی باید یکدیگر را جذب کنند، و در نتیجه اتم از بین خواهد رفت. به منظور جلوگیری از این فروپاشی، فرض شد که الکترون در مدارهایی به دور هسته میچرخد. از نیروی کولن برای تغییر جهت سرعت استفاده میشود.
تا اینجا میدانیم مدلهای مختلف اتم چیست و گفتیم رادرفورد در سال ۱۹۱۱ با تابش ذرات آلفا بر روی ورقه نازکی از طلا، مدل بسیار متفاوتتری از اتم را پیشنهاد کرد. اما این مدل با کاستیهایی همراه بود. ۴ سال بعد، در سال ۱۹۱۵ میلادی، نیلز بور مدل اتمی بور را پیشنهاد داد.
مدل اتمی بور
بور در راستای رفع نقصهای مدل رادرفورد، مدل جدیدی پیشنهاد داد. در مدل رادرفورد، هسته با بار مثبت در مرکز و الکترونها در مدارهایی به دور آن در چرخش هستند.
بور مدل اتمی رادرفورد را تکمیل و تصحیح کرد. او پیشنهاد داد که الکترونها در مدارهای ثابتی (لایهها) به دور هسته حرکت میکنند. بر طبق مدل ارائه شده توسط بور، الکترونها تنها در این لایهها و نه در فضای میان آنها قرار دارند. رادرفورد در مورد هسته اتم توضیح داد و بور مدل رادرفورد را بهبود بخشید.
بر طبق مدل پیشنهاد شده توسط بور، هسته با بار مثبت در مرکز اتم قرار گرفته است و الکترونها در لایههای ثابتی به دور آن در حرکت هستند. الکترونهایی که در مدارهای نزدیک به هسته قرار گرفتهاند انرژی کمتر و الکترونهایی که در مدارهای دورتر از هسته قرار دارند، انرژی بیشتری دارند.
در سال ۱۹۱۳ میلادی، بور تلاش کرد با نادیده گرفتن پیشبینی الکترومغناطیس کلاسیک، پارادوکس اتمی را حل کند. به جای آن، بور از ایدههای پلانک در مورد انرژی کوانتومی و یافتههای اینشتین در مورد آنکه نور از ذراتی به نام فوتون تشکیل شده است، برای پاسخ به پرسش اتم چیست و ارائه مدل کاملتری برای ساختار اتم استفاده کرد. او فرض کرد که الکترون به هنگام چرخش به دور هسته، هیچ تشعشعی ساطع نمیکند (فرضیه حالت مانا). اما الکترون اگر از مداری به مدار دیگر حرکت کند، فوتون را جذب یا ساطع میکند. مقدار انرژی جذب شده یا منتشر شده به صورت زیر بهدست میآید:
در این رابطه، h ثابت پلانک و و به ترتیب انرژیهای مداری اولیه و نهایی هستند. بوهر برای تکانه زاویهای، انرژی و شعاع مداری مقدارهای گسستهای را در نظر گرفت. بر طبق محاسبات بور، انرژی به صورت زیر نوشته میشود و دارای مقدارهای گسسته است:
در رابطه فوق n میتواند هر مقدار صحیح مثبتی را داشته باشد. همچنین، k ثابتی متشکل از ثابتهای بنیادی مانند جرم الکترون، بار آن و ثابت پلانک است. با ادغام دو رابطه فوق داریم:
کمترین سطوح انرژی در تصویر زیر نشان داده شدهاند. یکی از بنیادیترین قوانین فیزیک آن است که ماده در کمترین مقدار انرژی، در پایدارترین حالت ممکن خود قرار دارد. بنابراین، الکترون در اتم هیدروژن در مدار شماره ۱ (n=1) حرکت میکند، زیرا این مدار کمترین مقدار انرژی را دارد. حالت زمینه اتم هنگامی رخ میدهد که الکترون در مداری با کمترین انرژی قرار گرفته باشد. اگر اتم از منبعی خارجی انرژی دریافت کند، الکترون میتواند به مداری با n بزرگتر برود، در این حالت گفته میشود که اتم برانگیخته شده است.
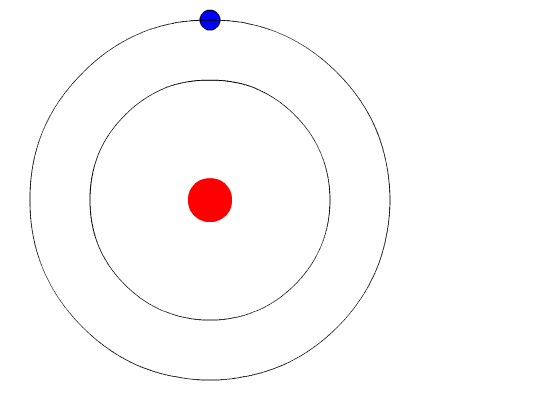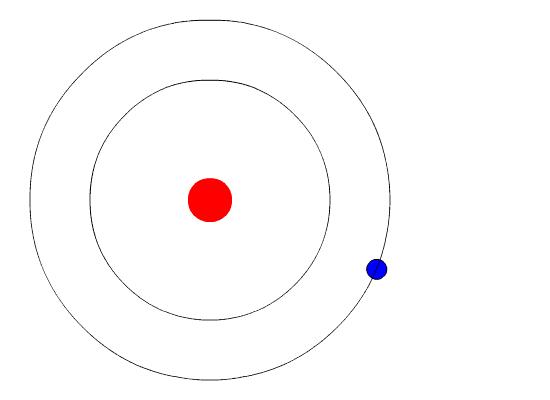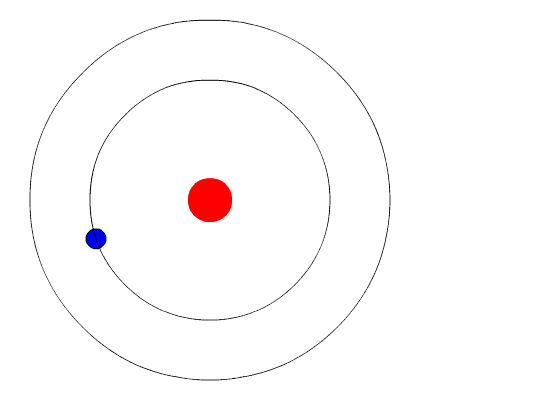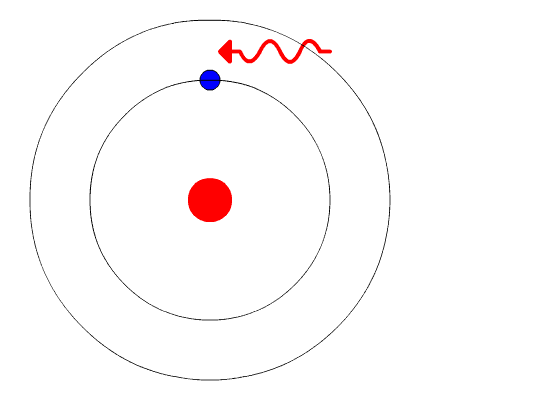
هنگامی که الکترون از حالت برانگیخته به حالت پایه (یا حالتی با برانگیختگی کمتر) منتقل شود، تفاوت انرژی به صورت فوتون منتشر خواهد شد. به طور مشابه، اگر فوتونی توسط اتمی جذب شود، انرژی فوتون جذب شده سبب حرکت الکترون از مداری با انرژی کمتر به مداری با انرژی بیشتر (حالت برانگیخته) میشود.
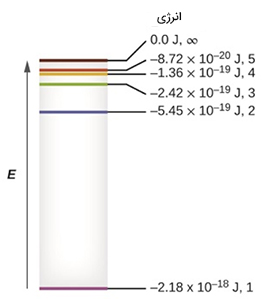
بر طبق قانون پایستگی انرژی، انرژی نه از بین میرود و نه به وجود میآید. بنابراین، اگر برای برانگیختگی الکترون از حالت انرژی ۱ به ۳ مقدار E انرژی لازم باشد، هنگامی که الکترون از حالت ۳ به حالت ۱ برمیگردد انرژی آزاد شده برابر E خواهد بود.
از آنجایی که مدل بور تنها شامل یک الکترون است، از آن میتوان برای توصیف یونهای تک الکترونی مانند و استفاده کرد. در اینجا به نکته مهمی در مورد مدل اتمی بور پی میبریم. در این مدل، از برهمکنش الکترونهای داخل اتم صرفنظر شده است، در نتیجه این مدل برای اتمهایی با بیش از یک الکترون مناسب نخواهد بود. در واقع، این مدل برای توصیف اتمهای هیدروژن مانند، مناسب هستند. انرژی بهدست آمده برای اتمهای هیدروژن مانند، تعمیم انرژی محاسبه شده برای اتم هیدروژن است، تنها تفاوت در آن است که عدد Z که برابر با بار مثبت هسته است به آن اضافه میشود. به عنوان مثال، مقدار Z برای هیدروژن برابر 1+ و برای هلیوم برابر 2+ است. همچنین، مقدار k برابر خواهد بود.
اندازههای مدارهای دایرهای در مدارهای هیدروژن مانند بر حسب شعاعهای آنها و به صورت زیر بیان میشود:
در رابطه فوق، ثابت شعاع بور و مقدار آن برابر متر است.
به رابطه فوق برای انرژی دقت کنید. در این رابطه، n بیانگر شماره لایههای الکترونی است. مقدار انرژی با منفی مجذور n رابطه عکس دارد، یعنی هر چه مقدار آن افزایش یابد، انرژی نیز افزایش خواهد یافت. در این حالت، الکترونها در فاصله دورتری از هسته یافت میشوند.
نیروی جاذبه الکترواستاتیک بین الکترون و هسته را به یاد بیاورید. نیرو با مجذور فاصله بین الکترون و هسته، رابطه معکوس دارد، یعنی هر چه این فاصله زیادتر شود، اندازه این نیرو کمتر خواهد شد. همچنین، هر چه مقدار n زیادتر شود، شعاع مدار دور هسته بزرگتر و مقدار انرژی کوچکتر میشود. اگر مقدار n و r به سمت بینهایت میل کنند، مقدار انرژی برابر صفر خواهد شد. در این حالت، اتم یونیزه شده و الکترون از دست داده است. مقدار انرژی لازم برای یونیزاسیون اتم هیدروژن برابر است با:
طیف اتمی چیست ؟
آیا تاکنون به لامپهای روشنایی دقت کردهاید؟ داخل این لامپها سیم بسیار نازکی قرار دارد که با افزایش دما، نور ساطع میکند. به این سیم، رشته گفته میشود. این سیم در بیشتر لامپها از جنس تنگستن است. چرا؟ زیرا نور تابیده شده از رشته تنگستن از تمام فرکانسها تشکیل شده است و به رنگ سفید دیده میشود. هر عنصری به هنگام گرم شدن یا عبور جریان الکتریکی از آن، نور تابش میکند.
هر عنصری طیف اتمی منحصربهفردی دارد.
فرکانسهای نور ساطع شده از اتمها در چشم با یکدیگر مخلوط میشوند، بنابراین ما رنگی مخلوط میبینیم. فیزیکدانهای زیادی مانند آنگستروم در سال ۱۸۶۸ میلادی و بالمر در سال ۱۸۷۵ میلادی، نور تابیده شده از اتمهای پرانرژی را از منشورهای شیشهای برای دیدن فرکانسهای تکی، عبور دادند. طیف تابشی یا طیف اتمی یک عنصر شیمیایی، الگوی منحصربهفردی از نور تابیده شده از آن عنصر به هنگام افزایش دما یا عبور جریان الکتریکی از آن است.
هنگامی که گاز هیدروژن داخل لولهای قرار داده میشود و جریان الکتریکی از آن میگذرد، رنگ نور تابیده شده برابر صورتی است. با جداسازی این رنگ میبینیم که طیف هیدروژن از چهار فرکانس تکی تشکیل شده است. نور صورتی داخل لوله به دلیل مخلوط شدن این چهار رنگ در چشم است.

مفروضات مدل اتمی بور
بور برای توصیف مدل اتمی پیشنهادی خود فرضیههای زیر را در نظر گرفت:
- در اتم، الکترونها با بار منفی به دور هسته (بار مثبت) در مسیرهای دایرهای مشخصی میچرخند. به این مسیرهای دایرهای مدار یا لایه گفته میشود.
- هر مدار یا لایه انرژی ثابتی دارد و به لایههای اوربیتالی معروف هستند.
- ترازهای انرژی با عدد صحیح و مثبت n (عدد کوانتومی) نشان داده میشوند. تراز n=1 کمترین مقدار انرژی و فاصله با هسته را دارد. هنگامی که الکترونی در لایه n=1 قرار دارد، به اصطلاح گفته میشود که در حالت زمینه قرار گرفته است.
- الکترونها در اتم با بهدست آوردن انرژی از تراز انرژی پایینتر به تراز انرژی بالاتر میروند. همچنین، الکترون با از دست دادن انرژی از تراز انرژی بالاتر به تراز انرژی پایینتر خواهد رفت.
- انرژی جذب شده یا تابیده شده برابر با تفاوت بین انرژیهای دو تراز انرژی است (، ). این تفاوت انرژی با استفاده از رابطه پلانک تعیین میشود.
- الکترون با قرار گرفتن و حرکت در تراز یا حالت انرژی مشخص، نه انرژی از دست میدهد و نه انرژی بهدست میآورد. انرژی الکترون در تراز انرژی مشخص همواره ثابت یا مانا باقی میماند.
آیا مدل اتمی بور کامل است؟ خیر. این مدل نیز مانند مدل ارائه شده توسط رادرفورد دارای محدودیتها و کاستیهایی بود.
کاستی های مدل اتمی بور
گرچه مدل اتمی بور در توضیح پایداری اتم و خطوط طیفی اتم هیدروژن به طور کامل موفق بود، اما محدودیتهای این مدل را نمیتوان نادیده گرفت:
- گفتیم مدل اتمی بور به خوبی طیف اتم هیدروژن را توضیح داد، اما این مدل در توضیح خطوط طیفی اتمهایی با بیش از یک الکترون (اتمهای چند الکترونی) ناموفق ماند.
- مدل بور در مورد اثر میدان مغناطیسی بر طیفهای اتمها یا یونها توضیح قابل قبولی ارائه نداد. هنگامی که اتم تابش کنندهای در میدان مغناطیسی بسیار قوی قرار بگیرد، هر خط طیفی به خطهای بیشتری تقسیم میشود. به این پدیده اثر زیمان گفته میشود. مدل اتمی بور در توضیح این اثر ناکام ماند.
- مدل بور نتوانست اثر میدان الکتریکی بر طیفهای اتمها (اثر اشتارک) را توضیح دهد. هنگامی که مادهای با طیف انتشار خطی در میدان الکتریکی خارجی قرار بگیرد، خطهای آن به خطهایی به فاصله فضایی نزدیک تقسیم میشوند. این نظریه نمیتواند در مورد شدتهای نسبی خطوط طیفی پیشگویی کند.
- نظریه اتمی بور در مورد شکل مولکولهای بهدست آمده از پیوند مستقیم بین اتمها، توضیحی نداده است.
- بر طبق مدل ارائه شده توسط بور، هنگامی که الکترون از یک تراز انرژی به تراز انرژی دیگر میرود، تشعشع رخ میدهد. اما بور در مورد چگونگی رخ دادن این تشعشع توضیحی نداده است.
- این مدل با اصل عدم قطعیت هایزنبرگ در تناقض است. در مدل اتمی بور اندازه شعاع و مدار الکترونها به طور همزمان مشخص است. بر طبق اصل عدم قطعیت، دانستن این دو مقدار به طور همزمان غیرممکن خواهد بود. بور فرض کرد که الکترون داخل اتم در فاصله مشخصی از هسته قرار گرفته است و با سرعت مشخصی به دور آن میچرخد. این فرضیه بر طبق اصل عدم قطعیت، صحیح نیست.
برخلاف محدودیتهای عنوان شده برای مدل اتمی بور، این مدل دستاوردهای بزرگی داشت که عبارت هستند از:
- این مدل پایداری اتم را توضیح میدهد.
- بر طبق نظریه بور، الکترون تا هنگامی که در مدار مشخصی به دور هسته میچرخد، انرژی از دست نمیدهد. همچنین، الکترون نمیتواند از اولین مدار به مدار پایینتر بپرد، زیرا مداری کوچکتر از یک وجود ندارد. بنابراین، این مدل محدودیت مدل اتمی رادرفورد را حذف کرد.
- مدل اتمی بور در محاسبه انرژی الکترونها در اتم هیدروژن و ترکیبات هیدروژن مانند، کمک شایانی کرد.
- بر طبق فرضیههای ارائه شده توسط بور، محاسبه انرژی الکترون در nامین مدار ترکیب هیدروژن مانند ممکن است.
- مدل اتمی بور طیفهای اتمی اتمهای هیدروژن را توضیح داد.
- بر طبق بور، الکترونها در اتم تنها انرژیهای مشخصی دارند. به حالتی که الکترونی در کمترین تراز انرژی ممکن قرار داشته باشد، حالت زمینه گفته میشود. هنگامی که الکترونی از منبعی خارجی انرژی دریافت کند، به تراز انرژی بالاتر میرود.
در گام نخست سعی کردیم به پرسش اتم چیست به زبان ساده پاسخ دهیم. در ادامه، در مورد ذرات تشکیلدهنده اتم مانند الکترونها، پروتونها و نوترونها و مدلهای اتمی تا مدل اتمی بور صحبت کردیم. فهمیدیم که مدل اتمی بور کاستیهای مربوط به مدل اتمی رادرفورد را برطرف کرد، اما برای محدودیتهای خود راه حلی نداشت. با ظهور فیزیک کوانتوم، تحول نوینی در فیزیک رخ داد. این شاخه از فیزیک توانست با ارائه مدل بسیار کاملتری موسوم به مدل کوانتومی، توضیح قابل قبولی برای ساختار اتم ارائه دهد.
مدل مکانیک کوانتومی اتم چیست ؟
یکی از مهمترین نتایج فیزیک کوانتوم، کشف دوگانگی موج - ذره و طول موج دوبروی بود. بدین ترتیب، مدل کوانتومی اتم مطرح شد. در ادامه مفهوم دوگانگی موج ذره را توضیح میدهیم.
دوگانگی موج - ذره و طول موج دوبروی
یکی از بزرگترین پیشرفتهای مکانیک کوانتوم توسط فیزیکدانی فرانسوی به نام «لوییس دوبروی» (Louis De Broglie) انجام شد. براساس کارهای انجام شده توسط پلانک و اینشتین که بیان کردند امواج نوری ویژگیهای ذره مانند میتوانند از خود نشان دهند، دوبروی فرض کرد ذرات میتوانند مشخصات موج مانند داشته باشند. این پدیده دوگانگی موج - ذره نام دارد.
دوبروی برای طول موج ذرهای به جرم m (کیلوگرم) که با سرعت متر بر ثانیه حرکت میکند، رابطه زیر را بهدست آورد:
در رابطه فوق طول موج دوبروی بر حسب متر و ثابت پلانک است.
به این نکته توجه داشته باشید که طول موج دوبروی و جرم ذره به صورت معکوس به یکدیگر مربوط میشوند. به همین دلیل متوجه رفتار موج مانند اجسام ماکروسکوپی اطراف خود نمیشویم. رفتار موجی ماده هنگامی قابلملاحظه است که موج با مانع یا شکافی با اندازه مشابه موج دوبروی روبرو شود. اما هنگامی که جرم ذرهای در حدود باشد، مانند الکترون، رفتار موجی بسیار آشکار میشود و پدیدههای بسیار جالبی به وجود میآیند.
مثال محاسبه موج دوبروی
سرعت حرکت الکترونی در انرژی حالت زمینه هیدروژن برابر متر بر ثانیه است. اگر جرم الکترون برابر کیلوگرم باشد، طول موج دوبروی الکترون را بهدست آورید.
پاسخ: با قرار دادن ثابت پلانک، سرعت و جرم الکترون در رابطه نوشته شده برای طول موج دوبروی داریم:
طول موج دوبروی برای الکترون برابر متر است. این مقدار از مرتبه بزرگی قطر اتم هیدروژن است.
امواج ایستاده
مشکل اصلی مدل اتمی بور آن بود که الکترونها به صورت ذراتی در مدارهای معین تعریف شده بودند. شرودینگر با استفاده از ایده دوبروی در مورد رفتار موج مانند ذرات، به این نتیجه رسید که رفتار الکترونها در اتم را میتوان با استفاده از امواج ماده به زبان ریاضی توضیح داد.
این حقیقت که الکترون در اتم تنها انرژیهای مجاز و معینی میتواند داشته باشد به موج ایستاده و ویژگیهای آن شباهت دارد. برای داشتن درک بهتری از رفتار موجی الکترون، در ادامه در مورد مهمترین ویژگیهای امواج ایستاده صحبت میکنیم.
به طور حتم با برخی آلات موسیقی مانند گیتار آشنا هستید. امواج ایستاده در گیتار نقش مهمی ایفا میکنند. به عنوان مثال، هنگامی که یکی از سیمهای گیتار کشیده میشود، به شکل امواج ایستاده (تصویر زیر) شروع به نوسان میکند.
به این نکته دقت کنید که برخی از نقطهها در امواج ایستاده جابجایی صفر دارند که به آنها گره میگوییم. این نقطهها به رنگ قرمز در تصویر فوق نشان داده شدهاند.
معادله شرودینگر
چگونه میتوانیم امواج ایستاده را به الکترونها مرتبط کنیم؟ الکترونها را به صورت امواج ایستاده با انرژیهای معینی در نظر میگیریم. شرودینگر، مدلی براساس رفتار موجی الکترونها برای اتم فرمولبندی کرد. شکل ساده رابطه شرودینگر به صورت زیر نوشته میشود:
در رابطه فوق، برابر تابع موج، H برابر عملگر هامیلتونی و E برابر انرژی پیوندی الکترون است. حل معادله شرودینگر، تعداد تابع موج است. هر تابع موج، مقدار انرژی مشخصی دارد. تفسیر دقیق تابع موج کار آسانی نیست. بر طبق اصل عدم قطعیت هایزنبرگ، تعیین همزمان موقعیت و انرژی الکترون غیرممکن است. از آنجایی که دانستن انرژی الکترون برای پیشبینی فعالیت شیمیایی اتم لازم است، شیمیدانها موقعیت مکانی الکترون را حدودی در نظر میگیرند. اما سوالی که ممکن است مطرح شود آن است که شیمیدانها چگونه مکان الکترون را به صورت تخمینی تعیین میکنند؟
به توابع موجی که از معادله شرودینگر برای اتمی خاصی بهدست میآیند، اوربیتالهای اتمی گفته میشود. به ناحیهای در اتم که الکترون بیش از ۹۰ درصد مواقع در آنجا قرار دارد، اوربیتال اتمی میگوییم.
اوربیتال ها و چگالی احتمال
اوربیتالها مکان احتمالی حضور الکترون در اطراف هسته اتم بر اساس معادله شرودینگر هستند. مقدار تابع موج در نقطهای در فضا متناسب با دامنه موج الکترونی در آن نقطه است. توجه به این نکته مهم است که بسیاری از تابعهای موج بهدست آمده، توابع مختلط هستند و دامنه آنها معنای فیزیکی ندارد.
مربع تابع موج بسیار مهم است. در واقع، مربع تابع موج متناسب با احتمال یافتن الکترون در حجم مشخصی داخل اتم است. به مربع تابع موج، یعنی ، چگالی احتمال گفته میشود.
چگالی احتمال الکترون میتواند با استفاده از راههای متفاوتی تجسم شود. به عنوان مثال، چگالی احتمال میتواند به صورت نموداری رنگی نشان داده شود. از شدت رنگها برای نشان دادن احتمال نسبی یافتن الکترون در ناحیه داده شده در فضا استفاده میشود. هرچه احتمال یافتن الکترون در حجم مشخصی داخل اتم بیشتر باشد، تراکم رنگ (شدت رنگ) در آن ناحیه بیشتر خواهد بود. تصویر زیر توزیع احتمال اوربیتالهای کروی 1s و 2s و 3s را نشان میدهد.
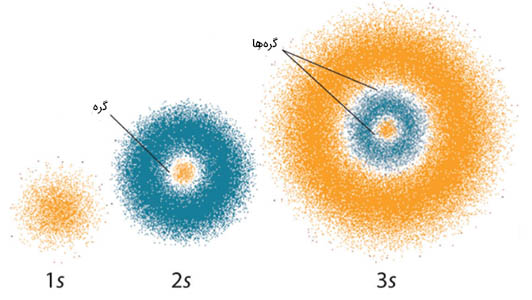
به این نکته توجه داشته باشید که اوربیتالها 2s و 3s گره دارند (گره در امواج ایستاده را به یاد آورید). وجود گره در این اوربیتالها بدان معنا است که احتمال یافتن الکترون در ناحیهای در فضا برابر صفر خواهد بود. راه دیگر برای به تصویر درآوردن احتمال یافتن الکترونها در اوربیتالها، رسم چگالی سطحی بر حسب فاصله از هسته اتم است.
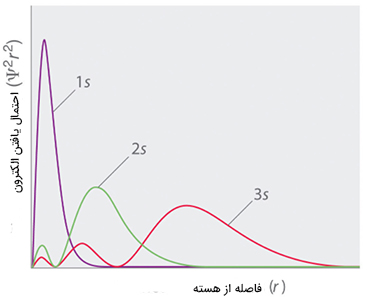
چگالی سطحی به صورت احتمال یافتن الکترون در لایه نازکی با شعاع r تعریف میشود. به نمودار فوق، نمودار احتمال شعاعی میگوییم.
شکل اوربیتال های اتم چیست ؟
تاکنون در مورد اوربیتالهای s صحبت کردیم. شکل این اوربیتالها کروی است. توجه به این نکته مهم است که فاصله از هسته، r، عامل اصلی تاثیرگذار بر توزیع احتمال الکترون است. در مورد اوربیتالهای دیگر چه میتوان گفت؟ در اوربیتالهای p و d و f، موقعیت زاویهای الکترون نسبت به هسته، عامل مهم دیگری در چگالی احتمال است. بنابراین، شکلهای اوربیتالی بیشتری مانند تصویر زیر، بهدست خواهند آمد.

اسپین الکترون | آزمایش اشترن گرلاخ
اسپین یکی از ویژگیهای ذرات بنیادی اتم است که با عنوان تکانه زاویه ذاتی شناخته میشود و میتواند ۲ مقدار مثبت و منفی نیم داشته باشد. در سال ۱۹۲۲ میلادی، دو فیزیکدان آلمانی به نامهای «اوتو اشترن« (Otto Stern) و «والتر گرلاخ» (Walther Gerlach) فرض کردند که الکترونها مانند آهن رباهای میلهای کوچکی رفتار میکنند. هر یک از این الکترونها دارای قطبهای منفی و مثبت هستند. برای آزمایش این نظریه، این دو فیزیکدان پرتویی از اتمهای نقره را به سمت فضای بین قطبهای آهن ربایی دائم فرستادند. در این آهن ربا، قطب شمال از قطب جنوب قویتر بود.
بر طبق فیزیک کلاسیک، جهت دوقطبی در میدان مغناطیسی خارجی، تعیینکننده جهت انحراف پرتو است. از آنجایی که آهن ربای میلهای میتواند گسترهای از جهتگیریهای مختلف را نسبت به میدان مغناطیسی خارجی داشته باشد، انتظار میرفت که اتمها با مقدارهای متفاوتی منحرف شوند. اما، اشترن و گرلاخ مشاهده کردند که این ذرات بین دو قطب شمال و جنوب تقسیم شدند.
نتایج آزمایشهای انجام شده نشان داد که برخلاف آهن رباهای میلهای معمولی، الکترونها میتوانند تنها دو جهتگیری ممکن را نشان دهند: در جهت میدان مغناطیسی یا در خلاف جهت آن. این حالت با استفاده از فیزیک کلاسیک قابل توجیه نبود. دانشمندان به این ویژگی الکترون، اسپین الکترون میگویند. هر الکترونی در جهان یا در حالت اسپین بالا یا اسپین پایین قرار دارد. گاهی الکترونها را به صورت پیکانهای عمودی به سمت بالا یا پایین نشان میدهیم.
ویژگیهای مدل مکانیک کوانتومی برای این ذرات، در ادامه خلاصه شدهاند:
- انرژی الکترون کوانتیزه است، یعنی الکترون تنها میتواند مقدارهای مشخصی برای انرژی داشته باشد.
- انرژی کوانتومی الکترون از حل معادله موج شرودینگر بهدست میآید و حاصل ویژگی موجی الکترون است.
- بر طبق اصل عدم قطعیت هایزنبرگ، مکان و تکانه دقیق الکترون نمیتوانند همزمان تعیین شوند.
- اوربیتال اتمی، تابع موج الکترون داخل اتم است. هر زمانی که الکترون با استفاده از تابع موج توصیف شود، اوربیتال اتمی را اشغال کرده است. الکترون میتواند تعداد زیادی تابع موج داشته باشد، بنابراین اوربیتالهای اتمی زیادی برای الکترون وجود دارند. هر تابع موج یا اوربیتال اتمی شکل و انرژی معینی دارد. تمام اطلاعات لازم در مورد الکترون در اتم، داخل تابع موج اوربیتالی ذخیره شده است.
- احتمال یافتن الکترون در نقطهای داخل اتم متناسب با مربع تابع موج اوربیتالی است.
پیوند اتم با اتم چیست ؟
اتمها برای پایداری بیشتر الکترونهای لایه ظرفیت، پیوند شیمیایی تشکیل میدهند. پیوند شیمیایی، پایداری اتمهایی که آن را تشکیل دادهاند به حداکثر میرساند. در پیوند یونی یک اتم، الکترونی را به اتم دیگر اهدا میکند. این پیوند هنگامی تشکیل میشود که یک اتم با از دست دادن الکترونهای لایه ظرفیت و اتم دیگر با پر کردن لایه ظرفیت (دریافت الکترون از اتم مقابل)، تکمیل شود. پیوند یونی به طور معمول بین فلز و نافلز تشکیل میشود.
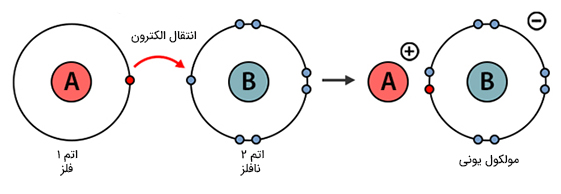
پیوندهای کووالانسی هنگامی تشکیل میشوند که اتمها برای پایداری بیشتر، الکترونهای خود را به اشتراک میگذارند.
پیوندها و الکترون های ظرفیت
در اولین لایه الکترونی تنها دو الکترون وجود دارند. اتم هیدروژن (با عدد اتمی یک) تنها یک پروتون در هسته و یک الکترون در تنها لایه خود دارد، بنابراین آن را با لایه بیرونی این ذرات دیگر به اشتراک میگذارند. اتم هلیوم (با عدد اتمی ۲) دو پروتون در هسته و دو الکترون در لایه ظرفیت دارد. در نتیجه، لایه ظرفیت هلیوم کامل و این اتم از نظر الکتریکی و شیمیایی خنثی است و تمایلی به تشکیل پیوند شیمیایی ندارد.
جدا از هلیوم و هیدروژن، با استفاده از قانون هشتتایی میتوان در مورد اینکه دو اتم با یکدیگر تشکیل پیوند خواهند داد یا خیر و همچنین تعداد پیوندهای بین آنها (در صورت تشکیل پیوند) تصمیم گرفت. بیشتر الکترونها برای کامل کردن لایه بیرونی خود به هشت الکترون نیاز دارند. بنابراین، اتمی که دو الکترون ظرفیت دارد با اتمی که به دو الکترون برای تکمیل لایه ظرفیت خود نیاز دارد، تشکیل پیوند خواهد داد.
به عنوان مثال، سدیم یک الکترونِ تنها در لایه بیرونی خود دارد. در مقابل، کلر تنها با گرفتن یک الکترون لایه ظرفیت خود را کامل میکند. در نتیجه، سدیم به راحتی الکترون لایه بیرونی را اهدا میکند و به یون سدیم تبدیل میشود، در حالیکه کلر یون اهدا شده از طرف سدیم را به راحتی میپذیرد و با کامل کردن لایه ظرفیت خود، به یون پایدار کلر تبدیل میشود. کلر و یون با یکدیگر تشکیل پیوند یونی میدهند و از پیوند آنها نمک طعام تشکیل میشود.
چرا اتم ها با یکدیگر پیوند تشکیل میدهند؟
با استفاده از جدول تناوبی میتوانید در مورد تشکیل پیوند اتمهای مختلف با یکدیگر و نوع پیوند، پیشبینیهای متعددی را انجام دهید. در دسته بندی عناصر در جدول تناوبی و سمت راست جدول تناوبی، گروهی از عنصرها به نام گازهای نجیب قرار گرفتهاند. لایه ظرفیت اتمهای این عنصرها (مانند هلیوم، کریپتون و نئون) کامل است. بنابراین، این ذرات پایدار هستند و با احتمال بسیار اندکی با اتمهای دیگر تشکیل پیوند خواهند داد.
یکی از بهترین راهها برای پیشبینی آنکه این ذرات با یکدیگر تشکیل پیوند خواهند داد یا خیر و تشخیص نوع پیوند، مقایسه الکترونگاتیوی آنها با یکدیگر است. به میزان تمایل این ذرات به جذب الکترونها در پیوند شیمیایی، الکترونگاتیوی گفته میشود. تفاوت زیاد بین الکترونگاتیوی دو اتم نشاندهنده آن است که یکی از اتمها تمایل به از دست دادن الکترونهای خود و ذرات دیگر تمایل به پذیرش آنها دارد. به طور معمول، این اتمها با یکدیگر تشکیل پیوند یونی میدهند. این نوع پیوند بین عنصر فلز و نافلز تشکیل میشود.
با دانستن مقدارهای الکترونگاتیوی عنصرهای متفاوت در جدول تناوبی و مقایسه آنها با یکدیگر، میتوان در مورد امکان تشکیل پیوند بین آنها صحبت کرد. الکترونگاتیوی روندی مشابه جدول تناوبی دارد، بنابراین بدون نگاه کردن به مقدار دقیق آن میتوانیم پیشبینیهای کلی انجام دهیم. با حرکت از سمت چپ جدول تناوبی به سمت راست، الکترونگاتیوی افزایش مییابد (گازهای نجیب استثنا هستند). با حرکت به سمت بالا به پایین در یک ستون یا گروه، الکترونگاتیوی کاهش خواهد یافت.
اتمهای سمت چپ جدول تناوبی با اتمهای سمت راست، تشکیل پیوند یونی میدهند. به عنوان مثال سدیم در سمت چپ جدول تناوبی و کلر در سمت راست آن قرار دارد، بنابراین این ذرات با یکدیگر تشکیل پیوند یونی خواهند داد. اتمهایی که در میانه جدول قرار دارند در بیشتر موارد با یکدیگر تشکیل پیوند فلزی یا کووالانسی میدهند.
اکنون میدانیم اتم چیست و دید واضحی در مورد ساختار اتم داریم. در ادامه، تاریخچه اتم را بررسی واهیم کرد.
تاریخچه اتم چیست ؟
در مطالب فوق به پرسش اتم چیست به زبان ساده پاسخ دادیم و در مورد ساختارهای مختلف اتم که در طی سالها پیشنهاد شده بود صحبت کردیم. در این بخش، در مورد تاریخچه اتم به اختصار توضیح خواهیم داد.
دموکریت اتم را معرفی کرد
تاریخچه اتم در حدود ۴۵۰ سال قبل از میلاد مسیح و با فیلسوفی یونانی به نام دموکریت آغاز شد. این سوال در ذهن دموکریت نقش بست که اگر مادهای به قطعههای کوچکتر بریده شود، چه اتفاقی میافتد؟ او فکر کرد ماده پس از تقسیم کردنهای متوالی، به نقطهای میرسد که نمیتواند به قطعههای کوچکتر تقسیم شود. او این قطعههای غیر قابلبرش را «اتوموس» (atomos) نامید. نام اتم از این نامگذاری گرفته شده است. ۱۰۰ سال بعد، ارسطو ایده دموکریت در مورد اتم را رد کرد. متاسفانه، ایدههای ارسطو بیش از دو هزار سال مورد پذیرش قرار گرفتند.

دالتون پرونده اتم را باز کرد
در حدود سال ۱۸۰۰ میلادی، دالتون ایدههای دموکریت در مورد اتم را احیا کرد.
تامسون الکترون ها را به ساختار اتم اضافه کرد
زمینه موردعلاقه تامسون الکتریسیته بود. او آزمایشهایی بر روی عبور جریان الکتریکی از لوله خلا انجام داد. این آزمایشها نشان داد که جریان الکتریکی از ذرات باردار منفی تشکیل شده است. اما چرا این کشف مهم بود؟ زیرا بیشتر دانشمندان معاصر با تامسون فکر میکردند که جریان الکتریکی از پرتوها (مانند پرتوهای نور) تشکیل شده است، و این پرتوها بار مثبت و نه منفی دارند. همچنین، آزمایشهای تامسون نشان داد که این ذرات باردار مشابه یکدیگر و کوچکتر از اتم هستند. در ادامه، همان گونه که مطرح شد، تامسون مدل کیک کشمشی برای ساختار اتم را ارائه داد.

رادرفورد هسته را کشف کرد
پس از تامسون، رادرفورد کشف مهم دیگری در مورد اتم انجام داد و به وجود هسته در آن پی برد. او با تاباندن ذرات آلفا بر روی ورقه بسیار نازکی از جنس طلا و مشاهده مسیر این ذرات پس از برخورد به ورقه، به وجود هسته پی برد. در ادامه، رادرفورد مدل اتمی کاملتر از مدل کیک کشمشی ارائه داد. مدل رادرفورد توانست کاستیهای مدل کیک کشمشی را برطرف کند، اما این مدل با کاستیهایی همراه بود.

نیلز بور و تکمیل مدل اتمی رادرفورد
در سال ۱۹۱۰ میلادی، نیلز بور با مدل اتمی سیارهای اتم موافقت کرد، اما میدانست که این مدل با کاستیهایی همراه است. او با استفاده از دانش خود در زمینه انرژی و فیزیک کوانتوم، مدل رادرفورد را تکمیل کرد. او توضیح داد که چرا الکترونها بر روی هسته فرود نمیآیند.

آخرین نظریه مدل اتمی تاکنون
در سال ۱۹۲۰ میلادی، اروین شرودینگر با استفاده از اصل عدم قطعیت هایزنبرگ، مدل اتمی جدیدی را ارائه کرد. این مدل در مقایسه با مدلهای قبلی بسیار کاملتر بود.
شکل اتم چیست ؟
بیشتر کتابهای شیمی تصویرهای مختلفی از اتمها ارائه میکنند. در بیشتر موارد، هسته به صورت کرهای کوچک در مرکز نشان داده شده است که توسط اوربیتالهای الکترونی احاطه میشود. اوربیتالها شکلهای مختلفی دارند، اما ذکر این نکته مهم است که اوربیتالها بیانگر احتمال یافتن الکترون در نقطه مشخصی در فضا هستند و چیزی در مورد شکل اتم نمیگویند. پژوهشگران مختلفی در سراسر جهان تلاش کردند تا نشان دهند اوربیتالهای الکترونی مشابه همان چیزی است که در کتابهای درسی نشان داده شدهاند.
«ایگور میکاییلوفسکی» (Igor Mikhailovkij) و همکارانش در موسسه فیزیک و تکنولوژی خارکوف با استفاده از بهبود تکنیک تصویربرداری قدیمی به نام میکروسکوپ گسیل میدانی، از شکلهای اوربیتالی در اتمهای کربن تصویربرداری کردند.
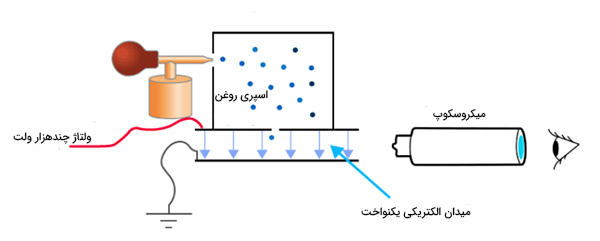
محققان زنجیرهای از اتمهای کربن ساختند و آن را از نوک گرافیت آویزان کردند. سپس این مجموعه را جلوی پرده آشکارسازی قرار دادند. میدان الکتریکی به بزرگی هزاران ولت بین گرافیت و پرده آشکارساز اعمال شد. پس از اعمال میدان، الکترونها یکییکی در صفحه گرافیت و سپس در امتداد زنجیره کربن، حرکت کردند تا جایی که میدان الکتریکی آنها را از آخرین اتم زنجیره بیرون کشید. با استفاده از مکانهای قرارگیری الکترونها بر روی پرده آشکارساز، ردپای الکترونهایی که اوربیتالها را در آخرین اتم ترک کردند با دقت دنبال شد. اطلاعات الکترونهای بسیاری جمعآوری و با یکدیگر ترکیب شدند.

پرسش های اتم چیست ؟
با توجه به اهمیت مفهوم اتم چیست و داشتن درک بهتری از مفهوم آن، به پرسشهای زیر پاسخ میدهیم.
پرسش ۱
کدامیک از ذرات زیراتمی، اوربیتالهای اطراف هسته را اشغال کردهاند؟
- پروتونها
- نوترونها
- پوزیترونها
- الکترونها
پاسخ: پاسخ صحیح الکترونها، یعنی گزینه ۴ است.
پرسش ۲
کدام سه ذره زیر، ذرات سازنده اتم هستند؟
- پروتونها، نوترونها و فوتونها
- پروتونها، نوترونها و الکترونها
- پوزیترونها، نوترونها و الکترونها
- پروتونها، الکترونها و پوزیترونها
پاسخ: پاسخ صحیح گزینه ۲ است.
پرسش ۳
کدامیک سازنده بنیادی تمام مواد در جهان است؟
- اتمها
- نوترونها
- هلیوم
- پروتئین
پاسخ: پاسخ صحیح گزینه یک، یعنی اتمها است.
جمعبندی
در این مطلب یاد گرفتیم که اتم چیست و به زبان سادهای تعریف آن را بیان کردیم. در ابتدا در مورد ذرات زیراتمی الکترون، پروتون و نوترون صحبت کردیم. فهمیدیم که بار الکتریکی الکترون منفی، بار الکتریکی پروتون مثبت و بار الکتریکی نوترون خنثی است. در حالت کلی در اتم، تعداد بارهای مثبت و منفی با یکدیگر برابر و اتمها از نظر الکتریکی خنثی هستند. هنگامی که اتمی الکترون از دست بدهد به یونی با بار مثبت و هنگامی که الکترونی به دست آورد به یونی با بار منفی تبدیل خواهد شد.
در ادامه، در مورد پنج مدل اتمی معروف صحبت کردیم:
- مدل دالتون
- مدل تامسون
- مدل رادرفورد
- مدل بور
- مدل مکانیک کوانتومی اتم
گفتیم در حدود ۲۵۰۰ سال قبل فیلسوفی یونانی به نام دموکریت ایده اتم را مطرح کرد. ایده او در حدود ۲۰۰۰ سال مسکوت ماند، تا آنکه دالتون در حدود سال ۱۸۰۰ میلادی، ایده دموکریت را مطرح و اولین مدل اتمی را پیشنهاد داد. او اتم را کوچکترین سازنده تمام مواد در جهان معرفی کرد.
سالها بعد با انجام آزمایشهای بیشتر مشخص شد که اتم از ذرات ریزی به نام الکترونها، پروتونها و نوترونها ساخته شده است. تامسون با انجام آزمایش لامپ پرتو کاتدی به وجود الکترون پی برد. رادرفورد با انجام آزمایش ورقه طلا، وجود پروتون را کشف کرد.
آزمون اتم چیست
۱. اتم از نگاه علم شیمی چگونه تعریف میشود و ذرات سازنده آن چه نقشی در خصوصیات اتم دارند؟
اتم کوچکترین واحد عنصر است که شامل سه ذره پروتون، نوترون و الکترون بوده، با تعداد پروتون هویت شیمیایی و با تعادل بار پروتون و الکترون، خنثی بودن خود را نشان میدهد.
اتم کوچکترین واحد تشکیل دهندهی ماده است که صرفا با پروتون مشخص و با عدد اتمی خود متمایز میشود.
اتم کوچکترین واحد عنصر است و از پروتون، نوترون و الکترون ساخته میشود که مجموع جرم در هسته است و بار مثبت اتم را تعیین میکند.
اتم کوچکترین بخش عنصری است که فقط از الکترون ساخته شده و رفتار واکنشی اتم وابسته به این ذره است.
تعریف شیمیایی اتم تاکید دارد که اتم کوچکترین واحد عنصر بوده و از سه ذره زیراتمی اصلی تشکیل شده است: پروتون، نوترون و الکترون. 'تعداد پروتون' مشخصکننده هویت شیمیایی هر عنصر است و بر اساس آن عناصر در جدول تناوبی مرتب میشوند. بار مثبت پروتون و بار منفی الکترون در حالت معمول به تعادل میرسد و باعث خنثی بودن اتم میشود. 'مجموع جرم' عمدتا در هسته (پروتون و نوترون) وجود دارد، اما بار کلی فقط با وجود برابری تعداد پروتون و الکترون خنثی است. پاسخهایی که تنها وجود پروتون یا فقط الکترون را منشا ویژگیهای اتم میدانند، ناقص هستند؛ هر سه ذره نقش اساسی دارند.
۲. تفاوت اصلی عدد اتمی (Z) و عدد جرمی (A) در چیست و هرکدام چه ویژگیای از اتم را بیان میکنند؟
عدد اتمی تعداد پروتونها و عدد جرمی مجموع پروتون و نوترون را نشان میدهد.
عدد اتمی تعداد الکترونها و عدد جرمی فقط جرم واقعی اتم را نشان میدهد.
عدد اتمی مجموع پروتون و الکترون و عدد جرمی تعداد نوترون را بیان میکند.
عدد اتمی تعداد نوترونها و عدد جرمی مجموع نوترون و الکترون را مشخص میکند.
گزینه «عدد اتمی تعداد پروتونها و عدد جرمی مجموع پروتون و نوترون را نشان میدهد» درست است چون عدد اتمی هر اتم فقط تعداد پروتونهای آن را مشخص میکند و این شاخص هویت عنصر و محل آن در جدول تناوبی است. عدد جرمی (A) مجموع تعداد پروتون و نوترون موجود در هسته را نشان میدهد و میتواند برای یک عنصر خاص متفاوت باشد (ایزوتوپها). گزینههای دیگر اطلاعاتی نادرست درباره محتوای عدد اتمی یا عدد جرمی میدهند و به نقش الکترون یا نوترون اشارههای اشتباه دارند.
۳. عنصری با عدد اتمی ۱۷ و عدد جرمی ۳۵ دارای چه تعداد پروتون، نوترون و الکترون است؟
۱۸ پروتون، ۱۷ نوترون، ۱۷ الکترون
۱۷ پروتون، ۱۷ نوترون، ۱۸ الکترون
۱۷ پروتون، ۱۸ نوترون، ۱۷ الکترون
۱۷ پروتون، ۱۸ نوترون، ۱۸ الکترون
در ساختار اتم، تعداد پروتون برابر با عدد اتمی (در اینجا ۱۷) است. تعداد نوترون از اختلاف عدد جرمی و عدد اتمی به دست میآید؛ یعنی ۳۵ منهای ۱۷ که نتیجه آن ۱۸ نوترون است. اتم خنثی، تعداد الکترون برابر با تعداد پروتون (۱۷) دارد. بنابراین ترکیب «۱۷ پروتون، ۱۸ نوترون، ۱۷ الکترون» صحیح است.
۴. در مدل کوانتومی اتم، نقش اوربیتال در تعیین محل احتمالی الکترونها چیست؟
اوربیتال مقدار بار الکتریکی هر الکترون را تعیین میکند.
اوربیتال محل چرخش دائمی و ثابت الکترون دور هسته را مشخص میکند.
اوربیتال اندازه هسته و تعداد پروتونهای اتم را تعیین میکند.
اوربیتال فضاهایی را نشان میدهد که احتمال حضور الکترونها بیشتر است.
در مدل کوانتومی، «اوربیتال فضاهایی را نشان میدهد که احتمال حضور الکترونها بیشتر است»، زیرا تابع موج الکترون در این مدل، چگالی احتمال حضور او را در پیرامون هسته نمایش میدهد. اوربیتالها مسیر یا حلقه ثابت برای حرکت الکترون نیستند، پس پاسخ درباره تعیین محل چرخش دائمی یا مقدار بار الکتریکی درست نیست؛ همچنین هیچ ارتباطی میان اوربیتال و تعیین اندازه هسته یا تعداد پروتونها وجود ندارد؛ این ویژگیها مستقل از اوربیتال هستند.
۵. ایزوتوپها چه تفاوتی با یکدیگر دارند و چگونه میتوان آنها را برای یک عنصر شناسایی کرد؟
ایزوتوپها عدد اتمی یکسان و عدد جرمی متفاوت دارند و با مقایسه این دو عدد شناسایی میشوند.
ایزوتوپها ساختار هستهای کاملا متفاوت دارند و با نماد عنصر قابل شناسایی نیستند.
ایزوتوپها همیشه تعداد الکترون متفاوت دارند و برای شناسایی باید رفتار شیمیایی بررسی شود.
ایزوتوپها فقط جرم متفاوت دارند و عدد اتمی و عدد جرمی ارتباطی به شناسایی آنها ندارد.
ایزوتوپهای یک عنصر همیشه عدد اتمی یا تعداد پروتون یکسان دارند اما تعداد نوترون و عدد جرمی آنها با یکدیگر متفاوت است. این اختلاف در عدد جرمی پایه شناسایی ایزوتوپهاست و با توجه به عدد اتمی و عدد جرمی، هویت هر ایزوتوپ به راحتی به دست میآید. «داشتن عدد اتمی یکسان و عدد جرمی متفاوت» تعریف اصلی ایزوتوپ است و مقایسه همین دو عدد راه تمایز آنها از یکدیگر است. در مقابل، تفاوت در تعداد الکترون یا رفتار شیمیایی فقط نشان دهنده یونها یا حالتهای مختلف اتم است، نه ایزوتوپ. ساختار هستهای هم کلیت مشترکی دارد و نماد عنصری همراه با عدد جرمی برای شناسایی استفاده میشود. جمله «فقط جرم متفاوت دارند و عدد اتمی و عدد جرمی ارتباطی به شناسایی آنها ندارد» نادرست است چون عددهای اتمی و جرمی معیار اصلی شناسایی ایزوتوپ هستند.
۶. اگر دو اتم عدد اتمی یکسان اما عدد جرمی متفاوت داشته باشند، این حالت مربوط به کدام مفهوم است؟
پیوند شیمیایی بین عناصر مختلف
تشکیل یون با بارهای متفاوت
تغییر مدل اتمی از دالتون به بور
وجود ایزوتوپهای یک عنصر
وقتی دو اتم عدد اتمی برابر دارند اما عدد جرمی آنان فرق میکند، این وضعیت به «وجود ایزوتوپهای یک عنصر» اشاره دارد. در این حالت، پروتونهای دو اتم برابرند اما تعداد نوترون متفاوت است و همین باعث اختلاف عدد جرمی میشود. «پیوند شیمیایی بین عناصر مختلف» به ترکیب اتمهای با عدد اتمی متفاوت میپردازد و رابطهای با این موضوع ندارد. «تشکیل یون با بارهای متفاوت» صرفا به تفاوت تعداد الکترونها اشاره دارد و عدد اتمی یا عدد جرمی را تغییر نمیدهد. همچنین «تغییر مدل اتمی از دالتون به بور» ربطی به تفاوت عدد جرمی بین اتمهای یک عنصر ندارد.
۷. مدل بور چه تفاوت اصلی با مدل رادرفورد داشت و محدودیت مهم آن چه بود؟
مدل بور، توضیح پایداری اتم و طیف هیدروژن را ارائه داد اما فقط برای هیدروژن مناسب بود.
مدل بور، وجود نوترون را افزود و جرم الکترونها را توضیح داد.
مدل بور، جای هسته را مشخص کرد اما رفتار موجی الکترون را نادیده گرفت.
مدل بور، ساختار کوانتومی کامل الکترون را پیشنهاد کرد و همه عناصر را پوشش داد.
مدل بور نسبت به مدل رادرفورد توانست پایداری اتم و چگونگی ایجاد طیف گسسته برای هیدروژن را توضیح دهد. مهمترین محدودیت این مدل آن بود که تنها برای اتمهای سادهای مانند هیدروژن پاسخگو بود و برای عناصر پیچیدهتر کارایی نداشت. در حالی که «توضیح طیف هیدروژن و پایداری» ویژگی کلیدی بور بود، بخشهایی مانند «تعیین جای هسته» یا «وجود نوترون» متعلق به مدلهای دیگر هستند. همچنین مدل کوانتومی بعد از بور، ساختار موجی و کاملتر را مطرح کرد. در نتیجه، عبارت «توضیح پایداری اتم و طیف هیدروژن اما محدود به هیدروژن» ویژگی و محدودیت مدل بور است.
۸. برای یون منفی کلرید با نماد ، برای به دست آوردن تعداد پروتون، نوترون و الکترون، چه مراحلی لازم است؟
تعداد پروتون یک بیشتر از عدد اتمی، نوترون از جمع عدد جرمی و عدد اتمی و الکترون یک کمتر از پروتون
تعداد پروتون برابر با عدد اتمی، تعداد نوترون از اختلاف عدد جرمی و عدد اتمی و تعداد الکترون یک بیشتر از پروتون
تعداد پروتون و الکترون هر دو برابر عدد جرمی و نوترون برابر عدد اتمی
تعداد پروتون از اختلاف عدد جرمی و عدد اتمی، نوترون برابر با عدد جرمی و الکترون برابر عدد اتمی
برای محاسبه ذرات زیراتمی یون ، باید عدد اتمی را برای پروتون، اختلاف عدد جرمی و عدد اتمی را برای نوترون، و تعداد الکترون را با افزودن یک به عدد اتمی (به دلیل بار منفی یون) محاسبه کرد. گزینه «تعداد پروتون برابر با عدد اتمی، تعداد نوترون از اختلاف عدد جرمی و عدد اتمی و تعداد الکترون یک بیشتر از پروتون» تنها روش درست را بیان میکند. سایر پاسخها تعریف یا رابطه درستی برای یکی از ذرات ارائه نمیدهند و مطابق توضیحات پست نیستند.
۹. در جدول تناوبی، چه ارتباطی بین محل عناصر و پیشبینی نوع پیوند شیمیایی آنها وجود دارد؟
عناصر نزدیک به هم معمولا پیوند کووالانسی ایجاد میکنند.
عناصر با فاصله زیاد در جدول میل بالاتر به پیوند یونی دارند.
فقط عناصر دوره آخر جدول وارد پیوند یونی میشوند.
پیوند شیمیایی به جایگاه عناصر در جدول بیارتباط است.
قاعده کلی این است که عناصر با فاصله زیاد در جدول تناوبی—مانند یک فلز قوی از گروه ۱ و یک نافلز از گروه ۱۷—تمایل به انجام پیوند یونی دارند، چون اختلاف الکترونگاتیوی آنها بالاست. عبارت «عناصر نزدیک به هم معمولا پیوند کووالانسی ایجاد میکنند» بخشی از قضیه را بیان میکند، اما نزدیکی صرف کافی نیست و ارتباط با نوع عنصر نیز مهم است. گفته اینکه «پیوند شیمیایی به جایگاه عناصر بیارتباط است» اشتباه بوده و جایگاه عناصر نقش کلیدی دارد. همچنین فقط عناصر دوره آخر وارد پیوند یونی نمیشوند، زیرا سایر عناصر نیز میتوانند چنین پیوندی برقرار کنند.
۱۰. در اتم، پروتون، نوترون و الکترون چه تفاوتهایی از نظر بار، جرم و محل قرارگیری دارند؟
پروتون و الکترون هر دو بار مثبت دارند؛ پروتون داخل هسته و الکترون خارج از هسته است و نوترون بیبار است.
پروتون بار مثبت دارد و در هسته است، الکترون بار منفی دارد و خارج هسته، نوترون بیبار است و در هسته قرار دارد.
الکترون و نوترون هر دو بار منفی دارند و خارج هستهاند، اما پروتون بار مثبت و در هسته است.
نوترون بار منفی دارد و خارج از هسته، پروتون و الکترون هر دو داخل هستهاند و بار مثبت دارند.
در ساختار اتم، پروتون بار مثبت دارد و همراه با نوترون که بیبار است، در مرکز اتم یا همان هسته جای میگیرند. الکترونها بار منفی داشته و فضای اطراف هسته را پر میکنند و جرم آنها نسبت به پروتون و نوترون بسیار کمتر است. متن بهوضوح اشاره میکند که پروتون و نوترون هسته را تشکیل میدهند، اما الکترون در بیرون هسته است و بارش با پروتون متفاوت است. اطلاعاتی مانند داشتن بار منفی برای نوترون یا قرارگیری پروتون و الکترون هر دو داخل هسته، یا بار منفی الکترون و نوترون صحیح نیستند و با توضیح موجود همخوانی ندارند.
۱۱. چه عاملی موجب تفاوت پایداری ایزوتوپها میشود؟
تعداد الکترون بیشتر
تعداد پروتون متفاوت
عدد اتمی متفاوت
تعداد نوترون متفاوت
پایداری یا ناپایداری ایزوتوپها به دلیل تفاوت در تعداد نوترونها در اتمهایی با عدد اتمی یکسان ایجاد میشود.
۱۲. برای نوشتن نماد یک اتم، چه پارامترهایی باید درج شود و این نمادگذاری چه هدفی دارد؟
در نمادگذاری اتم باید تعداد الکترونهای ظرفیت و دمای ذوب آنها نوشته شود تا واکنشپذیری خوانا باشد.
در نمادگذاری اتم فقط باید نام لاتین عنصر نوشته شود تا طبقهبندی عناصر ساده شود.
در نمادگذاری اتم باید نام عنصر و رنگ آن ذکر شود تا ویژگیهای فیزیکی مشخص گردد.
در نمادگذاری اتم باید عدد اتمی، عدد جرمی و نماد شیمیایی عنصر درج شود که تعیین ذرات زیراتمی را آسان میکند.
در روش صحیح نمادگذاری اتم، همیشه عدد اتمی (تعداد پروتون)، عدد جرمی (مجموع پروتون و نوترون) و نماد شیمیایی عنصر درج میشود تا بتوان تعداد ذرات زیراتمی را به آسانی محاسبه کرد. درج نام و رنگ عنصر، تعداد الکترونهای ظرفیت یا بر اساس دمای ذوب در نمادگذاری علمی موضوعیتی ندارد و برای کاربردهای شیمی و طبقهبندی عناصر معتبر نیست. تنها روش قراردادی صحیح همان درج نماد، عدد اتمی و عدد جرمی است که امکان محاسبه و مقایسه انواع اتم و ایزوتوپ را فراهم میکند.
۱۳. چه رابطهای میان موج-ذره بودن الکترون و تعریف اوربیتال در مدل کوانتومی اتم وجود دارد؟
موج-ذره بودن سبب شد الکترون در مدارهای ثابت طبق مدل بور باقی بماند.
این ویژگی فقط برای توضیح پیوند شیمیایی بین اتمها به کار رفت و ربطی به شکلگیری مدل اوربیتال نداشت.
موج-ذره بودن تنها به شناسایی بار الکترون کمک کرد و در تعریف اوربیتال کاربردی نداشت.
مدل موج-ذره بودن پیشبینی چگالی احتمال حضور الکترون را ممکن کرد و به تعریف اوربیتال انجامید.
مفهوم موج-ذره بودن الکترون باعث شد دانشمندان دریابند که الکترون رفتاری ترکیبی از موج و ذره دارد. این درک زمینهساز ارائه معادله شرودینگر شد که براساس آن، تابع موج الکترون تعریف شد. مربع این تابع موج، چگالی احتمال حضور الکترون را در فضا مشخص میکند و به این صورت، مفهوم اوربیتال یعنی نواحی بیشترین احتمال حضور الکترون شکل گرفت. برخلاف مدل بور که به مدارهای ثابت اشاره میکرد، مدل کوانتومی و دوگانگی موج-ذره، وجود اوربیتال را توضیح داد. ایدههایی مانند «شناسایی بار الکترون» یا «توضیح پیوند شیمیایی» با موج-ذره بودن در تعریف اوربیتال نقشی نداشتند و مدل بور با مدار ثابت نیز توصیف معاصر اوربیتال را ارائه نمیدهد.
۱۴. اگر در یک اتم، تعداد پروتونها و الکترونها برابر نباشد، چه اتفاقی میافتد؟
اتم خاصیت ایزوتوپ پیدا میکند.
جرم اتم تغییر میکند.
اتم به یون تبدیل میشود.
اتم به مولکول تبدیل میشود.
زمانی که تعداد پروتون و الکترون در یک اتم برابر نباشد، بار الکتریکی آن دیگر خنثی نیست و اتم به یون تبدیل میشود. یون به اتمی گفته میشود که تعداد بار مثبت (پروتون) و منفی (الکترون) متعادل نباشد. اگر تعداد پروتونها بیشتر از الکترونها شود، کاتیون و اگر کمتر شود، آنیون بهوجود میآید. «جرم اتم تغییر میکند» تنها به دلیل متفاوت بودن تعداد نوترونها رخ میدهد و ربطی به پروتون و الکترون ندارد. «اتم به مولکول تبدیل میشود» نتیجه ترکیب اتمها با پیوند شیمیایی است نه عدم توازن بار. «اتم خاصیت ایزوتوپ پیدا میکند» زمانی رخ میدهد که تعداد نوترون متفاوت باشد، نه الکترون.
۱۵. چه چیزی باعث شد دانشمندان مدلهای قدیمی اتم را به مدلهای جدیدتر تغییر دهند؟
کشف رفتارهای جدید و ناسازگار با مدلهای پیشین
گستردهتر شدن کاربرد اتمها در صنعت و پزشکی
پیشرفت ابزارهای تصویربرداری از ساختار اتم
نیاز به هماهنگی با نظریه نسبیت اینشتین
مهمترین عامل تغییر مدلهای اتمی، مشاهده رفتارهایی بود که مدلهای قبلی توانایی توضیح آنها را نداشتند. مثلا مدلهای ابتدایی قادر به تبیین طیف نشری هیدروژن یا پایداری اتم نبودند. با کشف این ناسازگاریها، مدلهایی مثل مدل بور و سپس مدل کوانتومی پیشنهاد شدند که توانستند شواهد جدید را توضیح دهند. «پیشرفت ابزارهای تصویربرداری» و «گسترش کاربرد اتمها» از دلایل توسعه علمی بودند اما انگیزه اصلی برای تغییر مدل، ناتوانی مدل قبلی در تبیین پدیدههای جدید بود. «هماهنگی با نظریه نسبیت» نیز ارتباط مستقیمی با جایگزینی مدلهای اتمی نداشت.
۱۶. طبق مدل کوانتومی اتم، چه عاملی باعث میشود مکان دقیق الکترون قابل تعیین نباشد و تنها بتوان درباره احتمال حضور آن صحبت کرد؟
اثر جرم بزرگ پروتون و نوترون نسبت به الکترون
سرعت بالای گردش الکترون دور هسته
وجود حالت موجی ذرهای برای الکترون
تعدد مدلهای کلاسیک اتم در گذشته
در مدل کوانتومی اتم، چون الکترون هم خصوصیت موجی و هم ذرهای دارد (wave-particle duality)، دقیقا تعیین مکان آن ممکن نیست و فقط میتوان درباره احتمال حضورش در ناحیهای صحبت کرد. عباراتی مانند «سرعت بالای گردش الکترون» یا «اثر جرم بزرگ پروتون و نوترون» به توضیح مدل کوانتومی و محدودیت تعیین مکان الکترون ربط ندارند. از سوی دیگر، «تعدد مدلهای کلاسیک» اساس علمی مدل کوانتومی را بیان نمیکند. تنها وجود حالت موجی ذرهای برای الکترون علت ناتوانی تعیین دقیق مکان آن است.
۱۷. کدام جمله نقش الکترونهای ظرفیت را در پیوند شیمیایی بهتر نشان میدهد؟
الکترونهای ظرفیت فقط عدد جرمی اتم را تعیین میکنند.
الکترونهای ظرفیت ارتباطی با جدول تناوبی ندارند.
الکترونهای ظرفیت در تشکیل پیوند شیمیایی شرکت میکنند.
الکترونهای ظرفیت فقط در گازهای نجیب هستند.
پاسخ «الکترونهای ظرفیت در تشکیل پیوند شیمیایی شرکت میکنند» صحیح است چون اتمها برای دستیابی به پایداری بیشتر و کامل شدن لایه ظرفیت خود تمایل به تشکیل پیوند دارند. الکترونهای ظرفیت نقش کلیدی در این فرایند دارند و تعیین میکنند که اتم قادر به ساخت پیوند یونی یا کووالانسی باشد. جمله «الکترونهای ظرفیت فقط عدد جرمی اتم را تعیین میکنند» اشتباه است چون عدد جرمی وابسته به مجموع پروتون و نوترون است، نه الکترونهای ظرفیت. عبارت «الکترونهای ظرفیت ارتباطی با جدول تناوبی ندارند» غلط است چون تعداد الکترونهای ظرفیت تعیینکننده خواص شیمیایی عنصر و جایگاه آن در جدول تناوبی است. گزینه «الکترونهای ظرفیت فقط در گازهای نجیب هستند» نادرست است زیرا همه عناصر، بهجز آنهایی که لایه ظرفیتشان کامل باشد، الکترونهای ظرفیت دارند.
۱۸. چرا شکل اتم که در کتابهای شیمی دیده میشود، تصویر واقعی اتم نیست و مفهوم اوربیتال به چه چیزی اشاره دارد؟
چون این شکلها تنها جرم دقیق هسته اتم را نمایش میدهند و اوربیتالها شکل هستهاند.
زیرا این تصاویر فقط مدلهای ساده هستند و اوربیتالها محل احتمالی حضور الکترون را نشان میدهند.
زیرا اوربیتالها همیشه دایرهای هستند، اما تصویر واقعی اتم بیضوی است.
چون تصاویر تنها عدد اتمی را بیان میکنند و ارتباطی با آرایش الکترون ندارند.
آنچه در کتابهای شیمی به عنوان شکل اتم نمایش داده میشود، در واقع مدلسازی از اوربیتالهای الکترونی است که احتمال حضور الکترون را پیرامون هسته با نواحی مختلف مشخص میکند، نه مسیر قطعی یا شکل واقعی اتم. برخلاف این تصویرسازیها، موقعیت دقیق الکترون نامعلوم است و ساختار اتم با مدل کوانتومی تنها به احتمال حضور در اوربیتالها توصیف میشود. گزینههایی مثل «نمایش جرم هسته» یا «دایرهای بودن اوربیتال» نادرست است، چرا که این تصاویر بیانگر آرایش احتمالی الکترونها هستند و نه مشخصات عددی یا هندسی هسته یا اتم.







در قسمت ساختار اتم جای نوترون و الکترون اشتباه نوشته شده. نوشته را تصحیح کنید.
با سلام؛
نکته اشاره شده در تصویر اصلاح و جایگزین شد.
با تشکر از همراهی شما با مجله فرادرس
خیر اتم ها ذرات بنیادی در جهان نیستند
شما اشتباه میکنید
کوارک ها و گلوئون ها و الکترون ها ذرات بنیادی در جهان هستند
اصلاح کنید
با سلام خدمت شما همراه گرامی؛
نکته بیان شده صحیح است و اصلاحات لازم در متن انجام شد.
از بازخورد و همراهی شما با مجله فرادرس سپاسگزاریم.
در قسمت مثال ذرات زیر اتمی قسمت 3درباره آنیون کار بحث میشود علامت اختصاری کربن Cنمایش داده شده است و اشتباه نوشته شده در واقع تعداد الکترون با پروتون برابر نیست ولی نوترون نوشته شده،چون تعداد الکترون با بار منفی یک واحد بیشتر از پروتون میباشد که اشتباه نوترون نوشته شده است
ممنون
با سلام خدمت شما؛
نکته بیان شده صحیح است و اصلاحات لازم در متن اعمال شد.
از همراهی شما با مجله فرادرس سپاسگزاریم.
سلام. سوالم اینه که گرانش اتم باعث میشه که الکترون به دور هسته بچرخد؟
اگر بله پس چرا با اینکه نیروی الکترومغناطیسی الکترون و پروتون از گرانش اتم بسیار بیشتر است این دوذره را به هم نمی چسباند؟
سلام و روز شما به خیر؛
مقدار نیروی گرانشی که به یک الکترون وارد میشود با توجه به جرم ذره بسیار ناچیز است و عموماً در محاسبات بررسی نمیشود. نیرویی که در این مقیاس بین ذرات برقرار است نیروی الکتریکی است که به مقدار بار ذرات بستگی دارد. ترکیب بین این دو ذره یعنی الکترون و پروتون نیز در طبیعت اتفاق میافتد که در نتیجه آن انرژی و هلیوم خواهیم داشت. ولی ارتباط بین الکترون و پروتون با انرژی گرانشی مشخص و واضح نبود.
از همراهی شما با فرادرس خرسندیم.
عالی
فوق العاده
مطالبتون عالیه،
سلام،ببخشید یه سوال دارم، برای بدست آوردن اتم هلیوم میتونیم دو عدد دوتریوم را با هم ترکیب هسته ای بدیم؟
بله میشه؛اصل تعداد پروتون هست و تفاوتدر نوترون فقط سبب تولید ایزوتوپی جدید یا متفاوت از هلیم می شود.