اکسیژن چیست؟ | خواص، واکنش ها، انواع و جرم اتمی
اکسیژن عنصری است که توسط عموم مردم بواسطه نقش حیاتی آن شناخته شده است. بدون این عنصر، انسان و دیگر موجودات زنده توانایی تنفس و زندگی کردن نخواهند داشت. اکسیژن نه تنها برای زنده ماندن مهم است، بلکه نقشی اساسی را در بسیاری از واکنشهای شیمیایی بازی میکند. در این مطلب از مجله فرادرس میآموزیم اکسیژن چیست، چه خواصی دارد و در چه واکنشهای شیمیایی شرکت میکند.
- میآموزید اکسیژن چیست و ویژگیهای شیمیایی آن کدام است.
- با منشاء و تاریخچه اتم اکسیژن و مولکول اکسیژن آشنا میشوید.
- میتوانید ویژگیها و خواص اکسیژن ۱۸ را درک کنید.
- با اکسیدهای حاصل از واکنش مواد با اکسیژن آشنا میشوید.
- واکنش اکسیژن با عناصر گروههای جدول تناوبی را به شکلی کامل یاد میگیرید.
- با خواص اکسیژن و روشهای تولید و نگه داری آن آشنا میشوید.


اکسیژن چیست؟
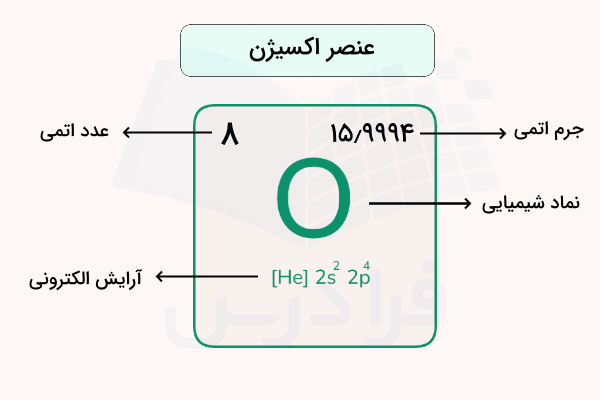
اکسیژن یکی از عناصر موجود در زمین است که عموما به شکل گازی و دواتمی وجود دارد. این عنصر عدد اتمی ۸ دارد و اولی عنصر از عناصر گروه ۱۶ جدول تناوبی است. عنصر غیرفلزی اکسیژن بسیار فعال و واکنشپذیر است و میتواند با بسیاری از عناصر فلزی و غیرفلزی وارد واکنش شود. اکسیژن معمولترین عنصر در پوسته زمین است و در حدود ۲۰ درصد هوای تنفسی ما را تشکیل میدهد.
منشاء و تاریخچه اکسیژن
اکسیژن با جرم اتمی ۱۵٫۹۹۹۴ در گروه ۱۶ از جدول تناوبی عناصر یافت میشود که به این گروه «کالکوژن» (Chalcogen) نیز میگویند. این عنصر در سالهای ۱۷۷۲ و ۱۷۷۴ به طور جداگانه توسط «شیل» (Scheele) و «پریستلی» (Priestly) کشف شد. نام اکسیژن را دانشمند فرانسوی آنتوان لاوازیه بر آن نهاد.
شیل، اکسیژن را از طریق یک آزمایش کشف کرد که در آن منگنز اکسید سوزانده میشد. او متوجه شد که منگنز اکسید داغ موجب تولید گازی میشود که او آن را «هوای آتشین» (Fire Air) نامید. شیل همچنین دریافت زمانی که این گاز با ذغالسنگ در تماس قرار میگیرد، جرقههای روشن و زیبایی را تولید میکند.
با وجود اینکه او این عنصر را کشف کرد اما یافتههای علمی خود را تا ۳ سال بعد از آن منتشر نکرد که مصادف بود با کشف این عنصر توسط پریستلی. پریستلی آزمایش شیل را با کمی تغییرات در دستگاههای آزمایشگاه دوباره تکرار کرد. او از یک عدسی استفاده کرد تا نور خورشید را مستقیم به مرکوریک اکسید بتاباند. در نتیجه، او هوایی را کشف کرد که به کمک آن عمر یک موش آزمایشگاهی را ۴ برابر بیشتر کرد و همچنین آزمایش سوختن را با شدت بیشتری انجام داد.
برخلاف تمام این یافتهها، این دو دانشمند متوجه نشدند که دقیقا چه عنصری را کشف کردهاند. در نهایت این آنتوان لاوازیه بود که در سال ۱۷۷۵ به ماهیت اکسیژن پی برد.
اکسیژن در جو زمین
جو زمین در حال حاضر شامل ۲۱ درصد از این گاز است. اکسیژن از راههای مختلفی به تولید میرسد. فرآیند «تجزیه فوتوشیمیایی» (Photochemical Dissociation) که در آن مولکولهای آب توسط اشعه ماورا بنفش شکسته میشوند در حدود ۱-۲ درصد از اکسیژن ما را تولید میکند. فرآیند دیگری که موجب تولید اکسیژن میشود، فوتوسنتز است که توسط گیاهان و باکتریهای فوتوسنتزی به تولید میرسد. واکنش کلی فوتوسنتز در زیر آورده شده است:
مواد آلی +
اکسیژن ۱۸ چیست؟
اکسیژن-۱۸، ایزوتوپ پایدار و طبیعی اکسیژن و یکی از «پریکرسرها» (Precursers) در تولید «فلودئوکسی گلوکز» (Fludeoxyglucose) یا همان FDG است و این ایزوتوپ پایدار در «توموگرافی با گسیل پوزیتورن» (Positron Emission Tomography) کاربرد دارد.

واکنشهای اکسیژن با گروههای اصلی در جدول تناوبی
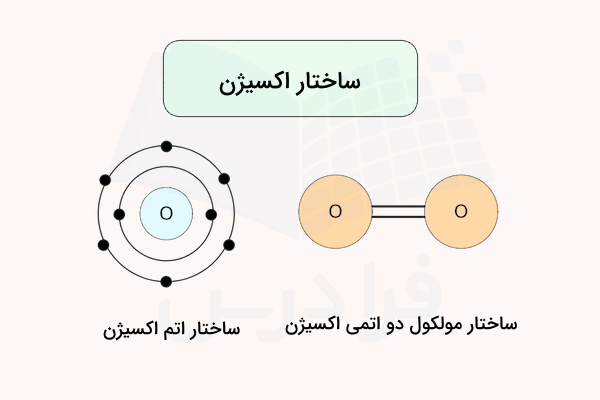
اکسیژن عنصری بسیار فعال و فراوان در زمین و بدن انسان است و در ترکیبات بسیاری یافت میشود. این ترکیباتِ شامل اکسیژن، از جمله مواد مورد علاقه شیمیدانها است. در حقیقت، به دلیل واکنشپذیری بالا، این عنصر، بیشتر به صورت ترکیبات مختلف قابل مشاهده است. دلیل واکنشپذیری آن را میتوان در آرایش الکترونی و داشتن دو جفت الکترون ناپیوندی جستجو کرد.
این عنصر دارای دو آلوتروپ با نامهای دیاکسیژن با فرمول و اوزون با فرمول است که هردو به عنوان اکسندههایی بسیار قوی به شمار میآیند. اکسیژن معمولا عدد اکسایش دارد که در شکل یافت میشود اما میتواند یونهای پراکسید و سوپراکسید را به ترتیب با فرمولهای شیمیایی و تشکیل دهد. با داشتن اعداد اکسایش مختلف، ترکیبات زیادی در واکنش با اکسیژن به تولید میرسند. در بسیاری از فرآیندهای بیولوژیکی شامل فوتوسنتز و تنفس، ردی از اکسیژن در واکنشهای شیمیایی آنها دیده میشود.
اکسیدها
اکسیدها ترکیبات شیمیایی هستند که در آنها حداقل یک اتم اکسیژن و یک اتم دیگر وجود داشته باشد. ۴ نوع عدد اکسایش برای اکسیژن در نظر میگیرند که به ترتیب برابر است با: ، ، و .
روندهای واکنش اکسیژن در جدول تناوبی
روندهایی کلی در خصوص واکنش این عنصر با گروههای اصلی در جدول تناوبی وجود دارد که در زیر آورده شدهاند:
- بیشتر نافلزات، اکسیدهایی را با بالاترین عدد اکسایش ممکن تشکیل میدهند. البته هالیدها از این قانون، جدا و بیشتر اکسیدهای فلزات هم شامل عدد اکسایش هستند.
- به عنوان یک قاعده کلی، اکسیدهای فلزی، بازی هستند و اکسیدهای نافلزی، خاصیت اسیدی دارند. خاصیت بازی یک اکسید با افزایش خاصیت یونی (فلزی) افزایش مییابد. اکسیدهای فلزی، پراکسیدها و سوپراکسیدها با حل شدن در آب، برای تولید یک محلول بازی با آن واکنش میدهند. علاوه بر این، اکسیژن با نافلزات، اکسیدهای کووالانسی تشکیل میدهد که در واکنش با آب، محلولهای اسیدی را تولید میکنند.
واکنش اکسیژن با هیدروژن
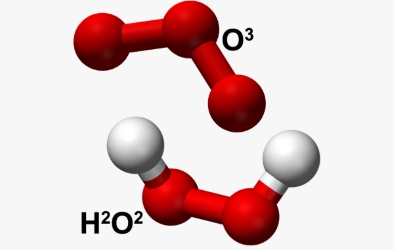
اکسیژن با هیدروژن واکنش میدهد تا دو ترکیب مختلف را تشکیل دهد: آب و «هیدروژن پراکسید» . آب ترکیبی است که در واکنشهای اکسید و احیا و واکنشهای تعادلی اسید و باز کاربرد فراوان دارد. آب میتواند به عنوان یک اسید، باز، اکسنده و کاهنده نیز عمل کند. این خاصیت چندگانه آب، آن را به مهمترین ترکیب در روی زمین تبدیل کرده است. واکنش اکسیژن با هیدروژن برای تولید آب را میتوانید در زیر مشاهده کنید:
قدرت اکسندگی هیدروژن پراکسید موجب استفاده از آن در صنعت شده که واکنش تولید آن در زیر آورده شده است:

واکنش اکسیژن با عناصر گروه 1 جدول تناوبی
این عنصر به سرعت با عناصر گروه ۱ جدول تناوبی واکنش میدهد. تمامی اکسیدهای فلزات قلیایی به هنگام حل شدن در آب، محلولهایی بازی تشکیل میدهند. محصولات حاصل از سوختن فلزات قلیایی، پایداری بالایی دارند. به طور مثال، اگر را نماد فلز قلیایی در نظر بگیریم، با کنترل دقیق اکسیژن میتوان اکسیدهایی به شکل تولید کرد اما زمانی که به آنها حرارت بدهیم، لیتیوم، سدیم، پتاسیم، روبیدیم و سزیم در واکنش با اکسیژن میسوزند و شعلهور میشوند.
واکنش اکسیژن با لیتیوم
لیتیوم، اولین فلز در گروه اول جدول تناوبی، با اکسیژن، برای تولید واکنش میدهد و به هنگام سوختن، شعلهای قرمز ایجاد میکند. اکسیژن موجود در این ترکیب به صورت اکسید وجود دارد که واکنش سوختن آن به صورت زیر است:
در صورتیکه اکسیژن اضافی در واکنش داشته باشیم، ممکن است مقادیری از ترکیب نیز تولید شود. در این ترکیب، از آنجایی که فلزات قلیایی همواره عدد اکسایشی برابر با دارند، اکسیژن نیز در ترکیب با آنها به صورت ظاهر میشود. واکنش تولید پراکسید در اثر اکسیژن اضافی را میتوانید در زیر مشاهده کنید:
واکنش اکسیژن با سدیم
رنگ شعله سدیم به هنگام سوختن به صورت نارنجی پررنگ است. استفاده از مقادیر زیاد سدیم یا سوزاندن آن با اکسیژن خالص، شعلهای قوی به رنگ نارنجی تولید میکند. بر اثر این اتقاق، جامد سفید رنگ مخلوطی از سدیم اکسید و سدیم پراکسید تشکیل خواهد شد. معادلههای واکنش تشکیل سدیم اکسید و سدیم پراکسید نیز مانند واکنشهای لیتیوم است:

واکنش اکسیژن با پتاسیم
اگر مقادیر کمی از پتاسیم را در مجاورت با هوا حرارت بدهیم، به سرعت ذوب میشود و بدون هیچ شعلهای، مخلوطی از پتاسیم پراکسید و پتاسیم سوپراکسید تشکیل میدهد:
واکنش اکسیژن با سایر فلزات قلیایی
سایر فلزات قلیایی ترکیباتی به شکل سوپراکسید تولید میکنند. در واکنش زیر، حرف نشاندهنده عناصر پتاسیم، روبیدیم، سزیم و فرانسیم است:
این ترکیبات، اکسندههایی قوی هستند چراکه تنها با گرفتن یک الکترون به آرایش الکترونی پایدار گاز نجیب میرسد. در نتیجه به سادگی کاهش مییابد و به عنوان یک اکسنده عمل میکند.
واکنش اکسیژن با عناصر گروه ۲ جدول تناوبی
عناصر گروه ۲ شامل برلیم، منیزیم، کلسیم، استرانسیم، باریم و رادیم است. فلزات قلیایی نیز با این عنصر وارد واکنش میشوند اما نه به سرعت فلزات قلیایی. علاوه بر این، انجام این واکنشها نیاز به دادن حرارت دارند.
اکسیدها و هیدروکسیدهای گروه ۲ حلالپذیری کمی در آب دارند و به هنگام انحلال، محلولهایی بازی تولید میکنند. واکنشهای سوختن و تشکیل ترکیباتی با یون را میتوان به صورت زیر نشان داد که در آن نشاندهنده فلزات قلیایی خاکی است:
تنها عناصر استرانسیم و باریم در گروه دوم میتوانند پراکسید تشکیل بدهند که واکنشهای آنها نیاز به اکسیژن اضافی و گرما دارند:
واکنش اکسیژن با برلیم
برلیم با آب و هوا وارد واکنش نمیشود. این رفتار شیمیایی برلیم را باید در اندازه کوچک و انرژی یونش بالای اتمهای آن جستجو کرد.

واکنش اکسیژن با سایر عناصر گروه ۲
به غیر از برلیم، سایر فلزات قلیایی خاکی، اکسیدهایی را در مجاورت هوا و دمای اتاق تشکیل میدهند:
همچنین به غیر برلیم، تمامی فلزات قلیایی خاکی در واکنش با اکسیژن تولید پراکسید میکنند:
اکسیدهای منیزیم، کلسیم، استرانسیم و باریم در واکنش با آب، هیدروکسیدها را تشکیل میدهند:
به غیر از برلیم، تمامی اکسیدها و هیدروکسیدهای حاصل از گروه ۲، خاصیت بازی دارند.

واکنش اکسیژن با عناصر گروه ۱۳ جدول تناوبی
گروه ۱۳ شامل عناصر بور، آلومینیوم، گالیم، ایندیم و تالیم است. بور تنها عنصری در این گروه است که هیچ خاصیت فلزی ندارد. عناصر این گروه، واکنشهای متفاوتی با اکسیژن دارند. به یاد دارید که اکسیدهای فلزات، بازی و اکسیدهای نافلزات اسیدی هستند. این مورد برای عناصر گروه ۱۳ نیز صدق میکند؛ البته آلومینیوم و گالیم از این قانون تبعیت نمیکنند. بقیه عناصر این گروه، ترکیباتی با فرمول شیمیایی تشکیل میدهند و رفتار اسیدی-بازی مطابق با قونین اکسیدهای فلزی و نافلزی دارند. در زیر، واکنش اکسیژن با عناصر گروه ۱۳ آورده شده است:
در دماهای بالا، تالیم در واکنش با اکسیژن، تولید میکند:
واکنش اکسیژن با بور
با حرارت دادن بوریک اسید، پایدارترین شکل اکسید بور، یعنی بور تریاکسید تشکیل خواهد شد:
واکنش اکسیژن با آلومینیوم
عدد اکسایش آلومینیوم در ترکیب با اکسیژن، به صورت +۳ است. این عنصر در واکنش با اکسیژن هوا، به سرعت لایهای نامحلول از را تشکیل میدهد. این لایه تشکیل شده مانع از خوردگی بیشتر فلز خواهد بود که واکنش آن به صورت زیر است:
«آلومینیوم تریاکسید» ، یک آمفوتر است یعنی هم خاصیتی بازی و هم اسیدی دارد که واکنشهای آن را در زیر مشاهده میکنید:
برخلاف تالیم که در آن، عدد اکسایش +۱ پایدارتر از +۳ است، آلومینیوم، گالیم و ایندیم تمایل به داشتن عدد اکسایش +۳ دارند. واکنش تمامی عناصر گروه ۱۳ موجب تشکیل اکسیدهای سه ظرفیتی میشود:
در این میان، تالیم تنها عنصری در گروه ۱۳ است که تمایل به تشکیل اکسید به جای تریاکسید دارد:
واکنش اکسیژن با عناصر گروه ۱۴ جدول تناوبی
گروه ۱۴ از فلزات، شبهفلزات و نافلزات تشکیل شده است. اکسیدهای بالای گروه ۱۴ تقریبا اسیدی هستند. اگر از بالای گروه به پایین حرکت کنیم، این خاصیت اسیدی کاهش پیدا میکند.
- کربن در گروه ۱۴، به هنگام سوختن، دیاکسید و مونو اکسید کربن تولید میکند که هردو تحت شرایط مختلف، خاصیتی اسیدی دارند. مونو اکسید کربن حلالیت کمی در آب دارد و با آن واکنش نمیدهد.
- شبه فلز سیلیکون در واکنش با اکسیژن، تنها یک ترکیب پایدار با فرمول تولید میکند که انحلالپذیری کم در آب و خاصیت اسیدی ضعیفی دارد.
- فلزات این گروه، اکسیدهای مختلفی را تشکیل میدهند که همگی آمفوتر هستند. این اکسیدها عبارتند از:
- ژرمانیوم: و
- قلع: و
- سرب: ، و
واکنش اکسیژن با عناصر گروه ۱۵ جدول تناوبی
گروه نیتروژن، با روشهای مختلفی با این اتم واکنش میدهد. نیتروژن و فسفر نافلز، آرسنیک و آنتیموان شبهفلز و بیسموت فلز هستند.
واکنش اکسیژن با نیتروژن
نیتروژن در واکنش با اکسیژن، اکسیدهای مختلفی با اعداد اکسایش از +۱ تا +۵ تشکیل میدهد. تمامی این اکسیدها در دمای اتاق به صورت گاز وجود دارند به جز که جامد است. فرمول شیمیایی اکسیدهای نیتروژن را در زیر ملاحظه میکنید:
، ، ، ،
تمامی این واکنشها گرماگیر هستند به این معنی که اکسیژن برای واکنش با به انرژی نیاز دارد. اکسیدهای نیتروژن خاصیت اسیدی دارند. و در واکنش با آب «اکسی اسیدها» (Oxoacid) را تشکیل میدهند. واکنشهای مربوط به نیتروژن در زیر آورده شده است:
نیتروس اسید:
نیتریک اسید:
واکنش اکسیژن با فسفر
فسفر دو آلوتروپ مهم دارد: فسفر سفید و فسفر قرمز. واکنشپذیری فسفر قرمز از سفید کمتر است. بسته به مقدار اکسیژن موجود در واکنش، دو نوع اکسید فسفر خواهیم داشت: زمانی که اکسیژن کمی داریم و ، زمانی که مقدار اکسیژن زیاد است. در موارد معدودی، اکسیدهایی با فرمول ، و تولید میشوند. همچنین، و برای تولید اکسیاسیدها با آب واکنش میدهند که این واکنشها در زیر آورده شدهاند:
فسفروس اسید:
فسفریک اسید:
واکنش اکسیژن با سایر عناصر گروه 15
آرسنیک، آنتیموان و بیسموت در زمان انجام فرآیند سوختن، با اکسیژن واکنش میدهند. اعداد اکسایش معمول در این سه عنصر، +۳ و +۵ است. برای هر عنصر، دو نوع مختلف از اکسید وجود دارد که در زیر آورده شده است:
- آرسنیک: و
- آنتیموان: و
- بیسموت: و
واکنش اکسیژن با عناصر گروه ۱۶ جدول تناوبی
عناصر گروه ۱۶ شامل اکسیژن، گوگرد، سلنیم، تلوریم و پولونیوم است. اکسیژن با عناصر گروه خود واکنش و تشکیل اکسیدهای مختلفی به شکل و میدهد.
اکسیژن
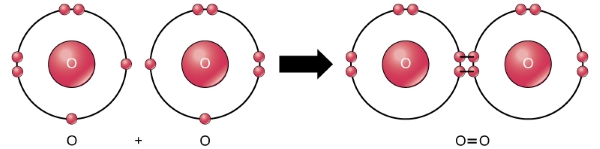
اکسیژن الکترونگاتیوی بالایی دارد که سبب میشود به سادگی الکترون جذب کند و پیوندهای هیدروژنی تشکیل دهد. از آنجایی که اکسیژن، کوچکترین عنصر در گروه خود است، میتواند پیوندهایی دوگانه تشکیل دهد و آرایش الکترونی آن فاقد اوربیتال است. این عنصر آلوتروپهایی به نام «اوزون» و «دی اکسیژن» را از طریق واکنش با خود تولید میکند.
واکنش اکسیژن با گوگرد
تنها اکسیدهای گوگرد شامل «دیاکسید گوگرد» و «تریاکسید گوگرد» میشوند. واکنش گوگرد با اکسیژن سبب تولید اکسیدها و اکسیاسیدها خواهد بود. این مواد همگی اکسندههای بسیار قوی هستند. از بیشتر در تولید بهره میگیرند که این ماده در واکنش با آب، سولفوریک اسید تولید میکند. واکنشهای گوگرد، دیاکسید گوگرد و تریاکسید گوگرد در زیر آمده است:
واکنش تولید دیاکسید گوگرد:
واکنشهای تولید تریاکسید گوگرد و سولفوریک اسید:
واکنش اکسیژن با سلنیوم و تلوریم
سلنیوم و تلوریم ترکیبهایی را به شکل ، و تشکیل میدهند.
واکنش اکسیژن با عناصر گروه 17 جدول تناوبی
عناصر گروه ۱۷ شامل فلوئور، کلر، برم و ید است که به طور کلی به آنها هالوژن میگویند. هالوژنها با اکسیژن واکنش میدهند اما بسیاری از ترکیبات حاصل از این واکنشها پایدار نیستند و تنها برای لحظاتی وجود دارند. ترکیباتی که از این واکنشهای بدست میآیند دارای ساختاری به شکل تا هستند.
واکنش اکسيژن با فلوئور
الکترونگاتیوترین عنصر است که عدد اکسایشی برابر با -۱ دارد. فلوئور و اکسیژن در ترکیب با یکدیگر، اکسیژن فلوراید را با فرمول تولید میکند.
سایر هالوژنها به جای اکسیدها، اکسیاسیدها را تولید میکنند که در جدول زیر آورده شدهاند:
| کلر | برم | ید | عدد اکسایش |
| و | |||
| و |
واکنش اکسیژن با عناصر گروه ۱۸ جدول تناوبی
گروه ۱۸ موسوم به گازهای نجیب شامل هلیوم، نئون، آرگون، کریپتون، زنون و رادون است. گازهای نجیب، به طور شیمیایی بیاثر هستند و با اکسیژن واکنش نمیدهند به جز زنون که در دمای پایین و فشار بالا ترکیباتی به صورت و تشکیل میدهد. انرژی یونش زنون به اندازه کافی پایین هست تا اتم الکترونگاتیو اکسیژن، الکترونهای آن را جذب کند.
اکسیژن چگونه تولید میشود؟
سالانه در حدود ۱۰۰ میلیون تن توسط فرآیندهای صنعتی از هوا استخراج میشود. معروفترین روش تولید این گاز از طریق تقطیر جزء به جزء است که در آن، گاز نیتروژن، بخار و گاز اکسیژن به صورت مایع از آن جدا میشود. یک روش دیگر در تولید اکسیژن، عبور جریان هوای خشک از یک جفت الک (غربال) مولکولی زئولیتی است که نیتروژن را جذب میکند و جریان هوایی با خلوص ۹۰ تا ۹۳ درصد از اکسیژن را بوجود میآورد.
علاوه بر این، اکسیژن را میتوان از طریق الکترولیز (برقکافت) آب نیز تولید کرد که موجب تولید هیدروژن و اکسیژن میشود. در الکترولیز آب باید از جریان مستقیم استفاده کرد. در صورت استفاده از جریان متناوب، در هر ستون، هیدروژن و اکسیژن با نسبت انفجاری 2 به ۱ حضور خواهند داشت.
صنایع تولید فولاد از بزرگترین مصرفکنندههای اکسیژن خالص به شمار میآیند. در حقیقت، استفاده از اکسیژن به جای هوا در فرآیند تولید موجب افزایش سرعت تولید و کنترل ناخالصیها میشود. همچنین استفاده از اکسیژن تجاری یا هوای غنی از اکسیژن در فرآیندهای تولید صنعتی مواد شیمیایی همچون اتیلن و متانول کاربرد دارد.
سمی بودن اکسیژن
این گاز در صورت افزایش فشار جزئی آن میتواند سمی باشد و سبب تشنج و دیگر مشکلات شود. سمی شدن اکسیژن معمولا در فشارهای جزئی بالاتر از ۵۰ کیلوپاسکال اتفاق میافتد. شایان ذکر است که فشار جزئی اکسیژن در سطح دریان حدود ۲۱ کیلوپاسکال ذکر میشود. در گذشته، نوزادان زودرس را داخل محفظههایی غنی از اکسیژن نگهداری میکردند اما این روش بعدها منسوخ شد چراکه به علت محتوای بالای اکسیژن، در مواردی نوزادان دچار نابینایی میشدند. همچنین، در غواصیهای زیر آب، تنفس اکسیژن میتواند موجب آسیب به سیستم عصبی مرکزی شود.
احتراق و دیگر خطرات اکسیژن
منابع غلیظ از اکسیژن، افزایش سرعت احتراق را به همراه خواهند داشت. زمانی که مواد قابل اشتعال همچون سوختها و اکسندهها در مجاورت یکدیگر قرار بگیرند تنها یک جرقه یا حرارت کافی است تا موجب انفجار شود.
عاملی که سبب انتقال سریع آتش انفجار آپولو ۱ به خدمه آن شد به این خاطر بود که کپسولهای اکسیژن خالص در آن، فشاری بالاتر از فشار اتمسفر داشتند که معمولا این مقدار فشار به هنگام ماموریت فضایی، در حدود یکسوم فشارِ معمول است. علاوه بر این اگر قطرات اکسیژن مایع روی مواد آلی همچون چوب، آسفالت و مواد پتروشیمی غوطهور شوند، سبب انفجار پیشبینی نشده آنها خواهند بود.

نگهداری اکسیژن و کاربرد اکسیژن مایع
به دلیل مسائل اقتصادی، این گاز را به حالت مایع و در تانکرهای عایق حمل و نقل میکنند چراکه یک لیتر اکسیژن مایع برابر با ۵۴۰ لیتر گاز اکسیژن در دمای ۲۰ درجه و فشار اتمسفری است. از این تانکرها برای پرکردن مخازن اکسیژن مایع در بیمارستانها و سایر مراکز صنعتی استفاده میشود. اکسیژن را همچنین در سیلندرهای کوچکتر نیز حمل میکنند که در پزشکی و برشکاری کاربرد دارند.
اگر این مطلب برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای نرمافزارهای مهندسی شیمی
- آموزش آشنایی با تصفیه آب به روش اسمز معکوس (RO) با نرم افزار ROSA
- قانون هس — به زبان ساده
- آلیاژ چیست؟ — به زبان ساده
^^












