عنصر آلومینیوم و فرآیند هال – از صفر تا صد
آلومینیوم فلزی است که بیشترین استفاده را بعد از آهن در صنعت دارد. چکشخواری و سادگی خمش و برش در این فلز از مزایای آن به شمار میآید. هادی خوب الکتریسیته و گرما و همچنین در برابر خوردگی مقاوم است. برای بهبود خواص آن میتوان به کمک ترکیب کردن آلومینیوم با عناصر دیگر، آلیاژهای متفاوتی تولید کرد. تمامی این ویژگیها در فراگیر شدن استفاده از آلومینیوم نقش اساسی داشتهاند. تولید آلومینیوم عموما از طریق «فرآیند هال» (Hall Process) صورت میگیرد. لازم به ذکر است که مصرف برق در فرآیند هال بسیار بالا است و واحدهای تولید آلومینیوم باید به منابع عظیم برق دسترسی داشته باشند.


کاربردهای آلومینیوم
آلومینیوم خالص به طور عمده در صنایع الکترونیک و در خازنها، هارد دیسکها و پردازندههای سیلیکونی استفاده میشود. ترکیب کردن آن با فلزاتی همچون مس، روی، منیزیم، و سیلیکون، آلیاژهایی سخت از آن بدست میدهد که در مواردی حتی سختتر از فولاد (استیل) میشود. به طور مثال «دورآلومین» (Duralumin) آلیاژی از آلومینیوم، منیزیم، مس و منگنز است.
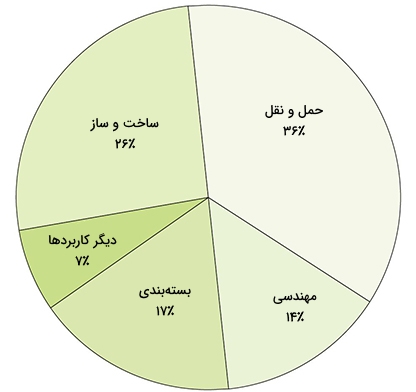
آلومینیوم و آلیاژهای آن بیشتر در صنایع حمل و نقل مورد استفاده قرار میگیرند چراکه چگالی پایین آن سبب کاهش مصرف سوخت در حمل و نقل میشود. همچنین، تولید دوچرخهها با آلومینیوم موجب کاهش وزن در محصول نهایی خواهد بود.
کاربرد دیگر آلومینیوم در بستهبندی غذاها مخصوصا بطریهای نوشیدنیها دیده میشود. ساخت لوازم خانگی، پخت و پز و اسکلتهای فلزی، از کاربردهای دیگر این فلز به شمار میآیند.
تولید سالانه
جدول زیر، «تولید اولیه» (Primaty Production) از سنگ معدن بوکسیت را نشان میدهد و شامل تولید ثانویه آن به کمک بازیافت مواد نیست:
| کل دنیا | ۵۸/3 میلیون تن |
| چین | 32 میلیون تن |
| روسیه | 3/5 میلیون تن |
| کانادا | 2/9 میلیون تن |
| هند | 2/4 میلیون تن |
| امارات | 2/3 میلیون تن |
تولید آلومینیوم با فرآیند هال
تولید اولیه آلومینیوم با فرآیند هال شامل چهار مرحله است:
- جداسازی سنگ معدن بوکسیت
- خالصسازی بوکسیت به آلومینیوم اکسید خالص (آلومینا)
- سنتز «کریولیت» و آلومینیوم فلوراید، به منظور استفاده از فرآیند کاهش الکترولیتی
- «کاهش الکترولیتی» (Electrolytic Reduction) آلومینیوم اکسید به آلومینیوم
آلومینیوم فلزی سبک، مقاوم و قابل بازیافت است که در صنایع مختلف کاربرد دارد. انواع آن شامل آلومینیوم خالص، آلیاژها و فویلها هستند. از خودرو و ساختمان تا بستهبندی و هوافضا استفاده میشود. اگر میخواهید کاربردهای عملی و انواع آلومینیوم را بهتر ببینید، فیلم آموزش رایگان زیر را مشاهده کنید.
جداسازی سنگ معدن بوکسیت
بوکسیت یکی از فراوانترین سنگمعدنها در جهان است و با مقادیر زیاد در جاماییکا، برزیل، گینه، چین و هند به صورت و یافت میشوند.

خالصسازی بوکسیت به آلومینیوم اکسید
ناخالصیهای اصلی در بوکسیت شامل آهن (III) اکسید، «سیلیکیا» ، و تیتانیوم دیاکسید هستند. پودر بوکسیت به همراه محلول 10 درصد سدیم هیدروکسید مخلوط میشود و تحت فشار ۴ اتمسفر و دمای 147 درجه سانتیگراد حرارت میبیند. در این شرایط، «آلومینیوم هیدروکسید» ، در سدیم هیدروکسید حل و به «سدیم آلومینات» تبدیل میشود، اما اکسیدهای آهن و تیتانیوم نامحلول باقی میمانند. تحت این شرایط ممکن است مقادیری از سیلیکیا نیز حل شود و بهتر است تا انحلال آن به حداقل ممکن برسد. این فرآیند بین یک تا دو ساعت زمان میبرد:
به رسوبات باقیمانده که به علت رنگ اکسید آهن به گِل قرمز موسوماند، زمان میدهند تا تهنشین شوند و بعد از شستشو، سدیم هیدروکسید از این رسوبات بازیافت میشود.
محلول سدیم آلومینات به تانکرهای «تهنشین کننده» (Precipitator) با مقیاس بزرگ پمپ میشود. این تانکرها ارتفاعی در حدود 24 متر و حجمی بیش از 1000 متر مکعب دارند. محلول حاصل را خنک و با بلورهای سدیم هیدروکسید مخلوط میکنند تا به پودر تبدیل شوند. این کار در حدود ۳ روز به طول میانجامد تا عمل تبلور به صورت کنترل شده روی دهد. در این شرایط، «توزیع اندازه ذرات» (Particle Size Distribution) برای ادامه فرآیند به طور بهینه خواهد بود. واکنش زیر موجب تولید آلومینیوم هیدروکسید خالص میشود:
به کمک فیلتراسیون، آلومینیوم هیدروکسید خالص از سدیم هیدروکسید جدا میشود. بخشی از آلومینیوم هیدروکسید برای مخلوط کردن به صورت پودر جدا میشود و باقیمانده آن در کورههای دوار تا دمای 1000 درجه سانتیگراد حرارت میبیند. نتیجه این کار، تولید آلومینیوم اکسید (آلومینا) است:

سنتز کریولیت و آلومینیوم فلوراید
علت اصلی کاهش الکترولیتی آلومینیوم، استفاده از کریولیت است تا آلومینا را در خود حل و برای الکترولیز (برقکافت) آماده کند. کریولیت با روشهای متقاوتی سنتز میشود. یکی از این روشها، آماده سازی محلول «سدیم آلومینات» از آلومینا است:
به محلول سدیم آلومینات، هیدروژن فلوراید و «سدیم کربنات» اضافه میشود. با انجام واکنش در دمای 57 درجه سانتیگراد، رسوب سدیم آلومینیوم فلوراید (کریولیت) به تولید میرسد:
همچنین آلومینیوم فلوراید نیز به محلول اضافه میشود تا ترکیبات الکترولیت و مقدار فلوراید را در طول الکترولیز تنظیم کند. برای تولید آلومینیوم فلوراید، از واکنش آلومینیوم هیدروکسید با «هگزا فلوروسیلیسیک اسید» (Hexafluorosilicic Acid) استفاده میکنند:
از فرآوردههای این واکنش، سیلیکا به کمک فیلتراسیون جدا میشود و به کمک شستشو با هیدروفلوریک اسید، هگزا فلولوروسیلیسیک اسید بازیافت میشود.
کاهش الکترولیتی آلومینیوم اکسید به آلومینیوم
عملیات تبدیل آلومینا به آلومینیوم یک فرآیند الکترولیتی است که جداگانه اما به طور همزمان در سال 1886 توسط دو دانشمند به نامهای «پائول هرولت» (Paul Heroult) در فرانسه و «چارلز هال» (Charles Hall) در آمریکا ابداع شد. این روش که به «فرآیند هال-هرولت» (Hall–Héroult Process) نیز معروف است، به مقادیر زیادی از الکتریسیته نیاز دارد به طوری که برای تولید هر کیلوگرم آلومینیوم، 10-13 کیلواتساعت برق نیاز است. بنابراین واحدهای تولید آلومینیوم باید به منابعی ارزان قیمت از برق دسترسی داشته باشند.
فرآیند هال به کمک یک سلول احیائی (Reduction Cell) از جنس استیل به ابعاد 8 در 4 متر و به عمق 1 متر اجرا میشود. در کف و دیوارههای این سلول، یک آستر از جنس گرافیت (کربن) وجود دارد که به عنوان کاتد بکار میرود. در طول واکنش، سلول از کریولیت مذاب و مقادیر کم (در حدود ۲-۵ درصد) از آلومینا پر میشود. طراحی این سلول به گونهای است که کریولیت به صورت لایهای جامد در سطح الکترولیت تشکیل شود. همچنین بلوکهایی غوطهور در الکترولیت که از جنس گرافیت (کُک مذاب) هستند، آند را تشکیل میدهند.

یک کارخانه به طور معمول ۴۰۰ عدد از این سلولها را به منظور تولید سالانه 300000 تن بکار میگیرد. علاوه بر این، به کارخانهای نیاز است تا سالانه 100000 تن آند تولید کند. همچنین کارخانهای نیز برای استفاده از این مواد در تولید آلیاژهای فلزی باید پیشبینی شود. طبیعت دقیق الکترولیت در این سلول، شناختهشده نیست اما واکنش کلی آن در الکترودها را میتوان به صورت زیر نشان داد:
کاتد:
آند:
واکنش به طور کلی:
در واقع، گاز دیاکسید کربن بیشتری در مقایسه با گاز مونو اکسید کربن در آند تشکیل میشود:
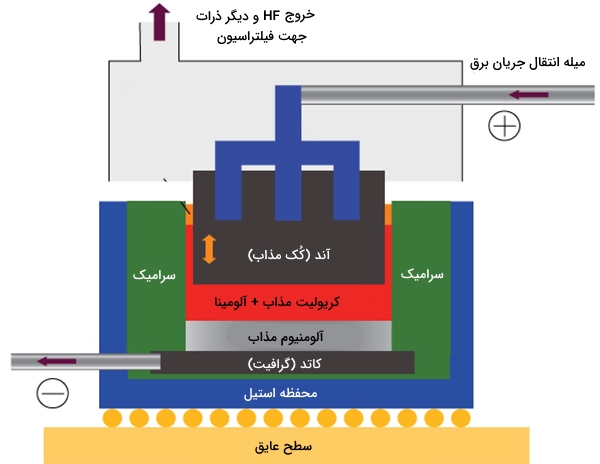
آلومینیوم مذاب از کریولیت چگالتر است و در پایین سلول جمع و به حوضچه آلومینیوم تبدیل میشود. به طور معمول این حوضچه عمقی برابر با ۱۰ سانتیمتر دارد که عمق آن را با تخلیه روزانه آلومینیوم، ثابت نگه میدارند. این فلز به صورت شمشهایی با خلوص ۹۹ درصد تولید میشود که مقادیر کمی از آهن و سیلیکون را تحت عنوان ناخالصی در خود دارند. علاوه بر این، با تصفیه آلومینیوم میتوان به خلوصی تا 99/999 درصد رسید.
در روش دیگر، آلومینیوم را به صورت مذاب در کوره نگهداری میکنند و قبل از سرد کردن، عناصر دیگری را برای تولید آلیاژهای مختلف به آن اضافه میکنند.
این فرآیند با اضافه کردن مداوم آلومینا ادامه پیدا میکند. غلظت آلومینا در الکترولیت را به صورت 2-5 درصد وزنی ثابت نگه میدارند. همچنین همانطور که گفته شد، در طول فرآیند، آلومینیوم فلوراید نیز به سلول اضافه میشود. علاوه بر این، اضافه کردن آلومینیوم فلوراید، کاهش نقطه ذوب مخلوط آلومینا-کریولیت را به همراه دارد که همین امر موجب کاهش مصرف انرژی خواهد شد. بخشی از فلوراید در طول مدت الکترولیز از بین میرود که علت آن هیدرولیز بوسیله رطوبت هوا است که محصول این واکنش، هیدروژن فلوراید است:
کربن نیز در آند با استفاده از گاز اکسیژن آزاد شده، مصرف میشود:
بنابراین، بلوکهای آند به طور مداوم باید جایگزین شوند. هر سلول معمولا در حدود ۲۰ بلوک آندی دارد که هر روز یکی از آنها جایگزین میشود تا در یک دوره بیست روزه، کل بلوکها تعویض شوند. درواقع این بلوکها طوری طراحی شدهاند که هر کدام ۲۰ الی ۲۱ روز دوام داشته باشند. سلولهای جدید با جریان 150-350 هزار آمپر و ولتاژ 4-4/5 ولت کار و روزانه ۱-۲ تن آلومینیوم تولید میکنند.
مصرف کربن در آند، موجب تولید مقادیر زیادی از گاز دیاکسید کربن میشود. راه ایدهآل این است که از آندهایی خنثی استفاده کنیم تا در طول فرآیند مصرف نشوند. برخی از تحقیقات، استفاده از مواد سرامیکی بر پایه اکسیدهای قلع، آنتیموان و مس را توصیه کردهاند. با بهرهگیری از این مواد که هادی الکتریسته و مقاوم در برابر گرما هستند، تولید گاز دیاکسید کربن به طور قابل ملاحظهای کاهش مییابد.

تولید ثانویه
بیش از ۵۰ درصد آلومینیومی که در ساخت محصولات بکار میرود، از مواد بازیافتی ساخته شده است. آلومینیوم به سادگی و با صرف هزینه بسیار کم بازیافت میشود. این هزینه در حدود ۵ درصد هزینه تولید اولیه است. تخمین زده شده است که در حدود دو سوم کل آلومینیوم تولیدی از سال 1886 تا به امروز، همچنان در حال استفاده است.
ضایعات آلومینیوم در کورههای نفتی یا گازی که داخل آنها با بلوکهای آلومینا پوشیده شده است، حرارت میبینند. در نهایت آلومینیوم مذاب از آن خارج و به شمش تبدیل میشود. این فلز را میتوان به طور مداوم ذوب کرد و مورد استفاده قرار داد. هر کیلوگرم آلومینیوم بازیافتی، موجب صرفه جویی در مصرف 8 کیلوگرم بوکسیت و ۴ کیلوگرم مواد معدنی دیگر است.
ضایعات کهنه، شامل آلیاژهایی با ترکیبات مختلف هستند بنابراین بهتر است که از این مواد برای تولید دوباره همان محصول استفاده شود. به طور مثال، بازیافت قوطیهای نوشابه برای تولید دوباره همان قوطیها بکار میرود. به همین منظور، محصولات مختلف در یک محل جمع و ذوب میشوند. همچنین به منظور ارتقا بهرهوری بازیافت این محصولات میتوان از گازی که به هنگام سوزاندن روکش این بطریها تولید میشود، در ذوب کردن آنها استفاده کرد.

اگر این مطلب برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای مهندسی شیمی
- آموزش هایسیس HYSYS برای شبیه سازی فرایندهای شیمیایی
- آمونیاک و فرآیند هابر — از صفر تا صد
- استخراج طلا با سیانوراسیون — از صفر تا صد
^^













اجزای تشکیل دهنده سلول احیا را جز به جز بگویید
با سلام؛
اجزای سلول احیا برای عنصر آلومینیوم در فرایند هال عبارتند از: الکترود کاتد (آند منفی در ظرف کربنی)، الکترود آند (میلههای کربنی مثبت)، یونهای Al3+ در مذاب، الکترولیت (کریولیت مذاب Na3AlF6 بههمراه Al2O3)، الکترونها، منبع جریان الکتریکی مستقیم (DC)
با تشکر از همراهی شما با مجله فرادرس
چرا عدد اکسایش اکسیژن ثابت باقی مونده مگه الکترون از دست نداد
با سلام؛
برای آشنایی با موضوعات عدد اکسایش و واکنش اکسایش کاهش، مطالعه مطالب زیر پیشنهاد میشود.
عدد اکسایش و تعیین آن — به زبان ساده (+ دانلود فیلم آموزش گام به گام)
واکنش اکسایش کاهش (ردوکس) — به زبان ساده
با تشکر از همراهی شما با مجله فرادرس