هیدروکربن چیست؟ – به زبان ساده + فرمول و انواع
هیدروکربنها مولکولهایی آلی هستند که تنها از اتم دو عنصر کربن و هیدروژن به وجود آمدهاند. این ترکیبها بهصورت گازی بیرنگ و فاقد بو حضور دارند. در این مطلب میخواهیم بدانیم هیدروکربن چیست و چه انواعی دارد. همچنین در مورد نامگذاری این دسته از ترکیبات و واکنشهای شیمیایی آنها صحبت خواهیم کرد.
- میآموزید که هیدروکربن چیست و چگونه طبقهبندی میشود.
- میتوانید ساختار، فرمول و روش نامگذاری هر خانواده هیدروکربنی را تحلیل کنید.
- خواهید دانست اصول نامگذاری IUPAC و قواعد شاخهای را چگونه بهکار بگیرید.
- میآموزید کاربردهای صنعتی و زیستمحیطی هیدروکربنها را ارزیابی کنید.
- قدرت حل تمرین، تشخیص نوع و نامگذاری عملی ساختارها را کسب میکنید.
- یاد میگیرید درجه غیراشباعی را محاسبه و اهمیت آن را تحلیل کنید.
هیدروکربن چیست ؟
ابتدا باید بدانیم هیدروکربن چیست و به چه اشکالی وجود دارد. هیدروکربنها سادهترین مولکولهای آلی هستند که تنها از اتمهای دو عنصر کربن و هیدروژن تشکیل شدهاند. در یک دستهبندی کلی میتوان هیدروکربنها را به چهار خانواده زیر تقسیمبندی کرد.
- «آلکان» (Alkane)
- «آلکن» (Alkene)
- «آلکین» (Alkyne)
- «هیدروکربن آروماتیک» (Aromatic Hydrocarbon)
در ادامه به بررسی چیستی هر یک از هیدروکربنهای ذکر شده در بالا میپردازیم. مطالعه هیدروکربنها از این جهت اهمیت دارد که پیشنیازی برای درک و مطالعه گروههای عاملی موجود روی هیدروکربنهای پیچیدهتر است.
انواع هیدروکربن
برای اینکه بدانیم هیدروکربن چیست نیاز داریم با انواع آن آشنا شویم. هیدروکربنها را با توجه به ساختارشان به دستههای مختلفی تقسیمبندی میکنند. در اینجا یکی ار مهمترین این دستهبندیها را میآوریم.
- «هیدروکربن آروماتیک» (Aromatic Hydrocarbon): ساختار این نوع هیدروکربنها حاوی حلقه ۶ عضوی به نام «بنزن» (Benzene) است.
- «هیدروکربن آلیفاتیک» (Aliphatic Hydrocarbon): این نوع از هیدروکربنها دارای ساختاری زنجیرهای هستند.
هیدروکربن آلیفاتیک چیست ؟
در این بخش میخواهیم بدانیم معنای آلفیاتیک در هیدروکربن چیست . این نوع هیدروکربن از زنجیرههایی متوالی از عنصر کربن ساخته شده است و خود دارای سه زیرشاخه است.
- «آلکان» (Alkane): آلکانها زنجیرههای هیدروکربنی هستند که تنها دارای پیوند یگانه کربن-کربن هستند.
- «آلکن» (Alkene): در این نوع هیدروکربن حداقل یک پیوند کربن-کربن دوگانه در زنجیره وجود دارد.
- «آلکین» (Alkyne): آلکینها دارای زنجیره هیدروکربنی هستند که حداقل یک پیوند کربن-کربن سهگانه در آن دیده میشود.
علاوه بر این هیدروکربنهای آلیفاتیکی وجود دارند که دارای حلقه هستند و به آن ها «آلکان حلقوی» (Cycloalkane)، «آلکن حلقوی» (Cycloalkene) و «آلکین حلقوی» (Cycloalkyne) میگویند. در ادامه میخواهیم بدانیم هر یک از انواع خانوادههای این هیدروکربن چیست و چطور قابل تشخیص است.
آلکان چیست ؟
در ابتدا نیاز داریم بدانیم خانواده آلکان در هیدوکربن چیست . در ترکیبهایی که به خانواده آلکانها تعلق دارند، تنها پیوند یگانه بین کربن-کربن وجود دارد و پیوند دوگانه یا پیوند سهگانه مشاهده نمیشود. سادهترین آلکانها بهصورت خطی و بدون شاخه وجود دارند و به آنها «آلکان نرمال» (Normal Alkane) گفته میشود.
این مولکولها با توجه به تعداد کربنهای موجود در زنجیره خود نامگذاری میشوند. فرمول آلکانها بهصورت است. با در دست داشتن فرمول هیدروکربن میتوان به تعداد اتمهای موجودر در آن پی برد.
| نام آلکان | فرمول شیمیایی | تعداد اتمهای کربن |
| متان | ۱ | |
| اتان | ۲ | |
| پروپان | ۳ | |
| بوتان | ۴ | |
| پنتان | ۵ | |
| هگزان | ۶ | |
| هپتان | ۷ | |
| اکتان | ۸ | |
| نونان | ۹ | |
| دکان | ۱۰ |
متان
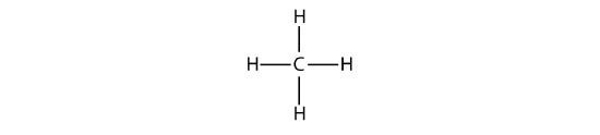
سادهترین مولکول آلکان «متان» (Methane) نامیده میشود. ساختار این مولکول را در زیر مشاهده میکنید.
اتان
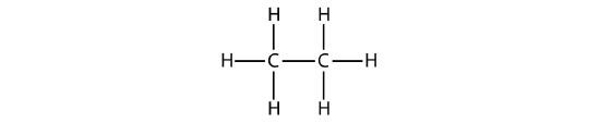
دومین آلکان ساده، «اتان» (Ethane) نامیده میشود و از ۲ اتم کربن ساخته شده است. این دو اتم کربن بهصورت کووالانسی کنار یکدیگر قرار گرفتهاند. توجه داشته باشید که هر اتم کربن به ۳ اتم هیدروژن متصل است تا ۴ ظرفیت خود را پر کند. فرمول مولکولی اتان است و میتوانید ساختار آن را در تصویر زیر مشاهده کنید.
پروپان
«پروپان» (Propane) دارای ۳ اتم کربن است که بهصورت زنجیرهای بدون شاخه به یکدیگر متصل شدهاند. فرمول مولکولی این ساختار بهصورت است. مولکول اتان را در تصویر زیر مشاهده میکنید.
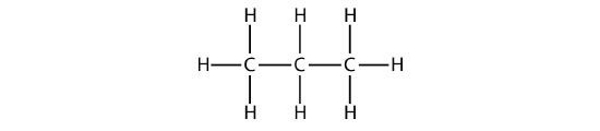
به نحوه نمایش مولکولها در تصاویر بالا «فرمول ساختاری» (Structral Formula) گفته میشود و تعداد اتمهای هر عنصر و نحوه اتصال آنها را به سادهترین و بهترین شکل ممکن نشان میدهد. هرچه مولکول بزرگتر باشد، این ساختار نیز پیچیدهتر میشود. روش دیگری نیز برای نشان دادن هیدروکربنها وجود دارد که «فرمول ساختاری فشرده» (Condensed Structural Formula) نامیده میشود. این ساختار نیز گویا و مختصر است. در زیر، لیست تعدادی از آلکانها به همراه فرمول ساختاری فشرده آنها را مشاهده میکنید.
- متان:
- اتان:
- پروپان:
- بوتان:
- پنتان:
- هگزان:
- هپتان:
- اکتان:
- نونان:
- دکان:
انواع آلکان
گفتیم که آلکانها هیدروکربنهایی شامل پیوندهای یگانه کربن-کربن هستند و به همین دلیل آنها را هیدروکربن اشباع نیز مینامیم. آلکانها را میتوان با توجه به ساختارشان به سه دسته زیر طبقهبندی کرد.
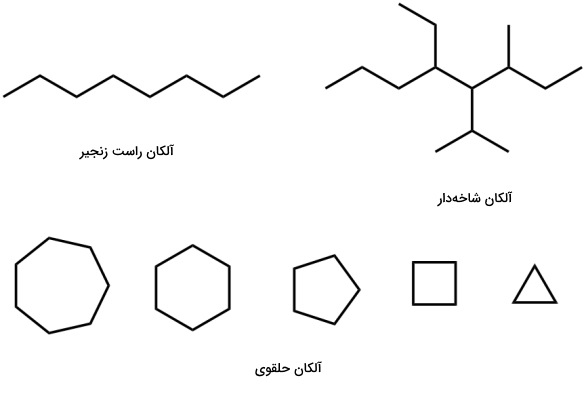
- «آلکان راستزنجیر» (Linear Straight-chain Alkane)
- «آلکان شاخهدار» (Branched Alkane)
- «آلکان حلقوی» (Cycloalkane): در بخش هیدروکربنهای حلقوی در این مورد به تفضیل صحبت میکنیم.
آلکن چیست ؟
برای تسلط کامل نیاز داریم بدانیم خانواده آلکن در هیدوکربن چیست . آلکنها ترکیبهایی هستند که دارای یک پیوند کربن-کربن دوگانه باشند و از آنجا که تمام ظرفیت اتم کربن آنها با پیوند کووالانسی پر نشده است، هیدروکربن غیراشباع نیز نامیده میشوند. فرمول شیمیایی کلی آلکنها را میتوان بهصورت نشان داد.
در جدول زیر ۹ آلکن ابتدایی را مشاهده میکنید. توجه داشته باشید از آنجا که ترکیب آلکن حداقل یک پیوند دوگانه بین کربن-کربن دارد، امکان حضور آلکن با ۱ اتم کربن وجود ندارد.
| نام آلکن | فرمول شیمیایی | تعداد اتم کربن |
| اتن | ۲ | |
| پروپن | ۳ | |
| بوتن | ۴ | |
| پنتن | ۵ | |
| هگزن | ۶ | |
| هپتن | ۷ | |
| اکتن | ۸ | |
| نونن | ۹ | |
| دکن | ۱۰ |
توجه داشته باشید که نامگذاری آلکنها درست مانند آلکانها است با این تفاوت که به جای «ان» (ane) در انتهای تعداد اتمهای کربن از «ن» (ene) استفاده میشود.
اتن
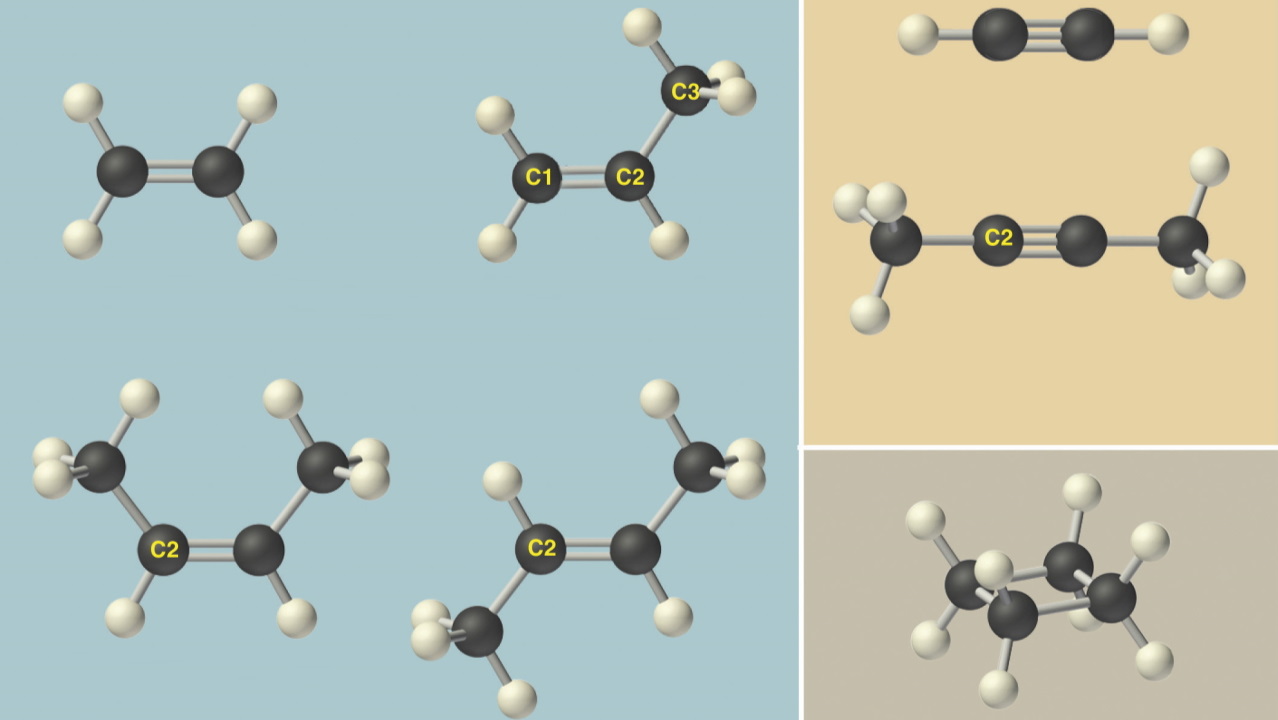
«اتن» (Ethene) که «اتیلن» (Ethylene) نیز نامیده میشود، سادهترین آلکن با دو اتم کربن و ۱ پیوند دوگانه کربن-کربن است. ساختار این مولکول را میتوان بهصورت زیر نمایش داد.
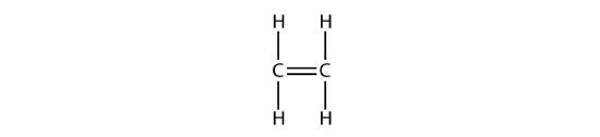
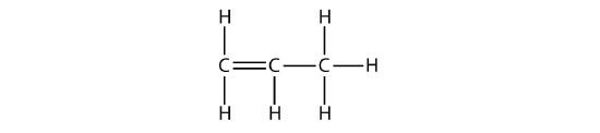
پروپن
دومین عضو خانواده آلکنها «پروپن» (Propene) نامیده میشود که از ۳ اتم کربن و یک پیوند دوگانه تشکیل شده است. به این مولکول «پروپیلن» (Propylene) نیز گفته میشود.
بوتن
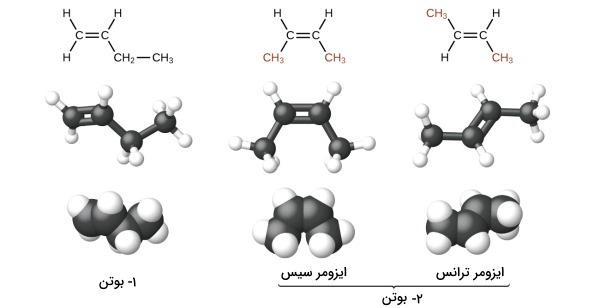
سومین عضو این خانواده «بوتن» (Buthene) نامیده میشود و دارای ۴ اتم کربن و یک پیوند دوگانه است. با بزرگتر شدن مولکول، مسئله موقعیت پیوند دوگانه مطرح میشود. همانطور که در تصویر زیر مشاهده میکنید، دو بوتن متفاوت امکان حضور دارند، بهصورتی که این پیوند دوگانه میتواند هم بین اتم کربن ۱ و اتم کربن ۲ قرار بگیرد (تصویر سمت چپ)، هم بین اتم کربن ۲ و اتم کربن ۳. (در تصویر سمت راست نشان داده شده است.)
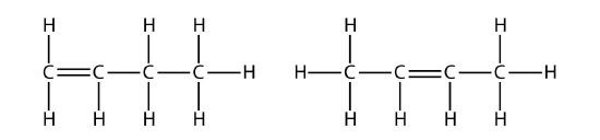
نحوه نامگذاری آلکن
همانطور که مشاهده کردید، آلکنها با توجه به موقعیت پیوند دوگانه میتوانند دارای ایزومر باشند. در نامگذاری آلکنها نیاز است که موقعیت این پیوندها مشخص باشد. برای مثال در تصویر بالا مولکول سمت چپ ۱-بوتن و مولکول سمت راست ۲-بوتن نامیده میشود. این اعداد کربنی را مشخص میکنند که پیوند دوگانه از آنجا شروع شده است. برای نامگذاری آلکنها از سمتی شروع میکنیم که به کربن دارای پیوند دوگانه کمترین عدد تعلق بگیرد. به مثال زیر توجه کنید.
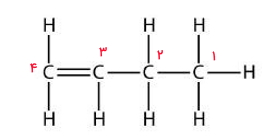
نحوه نامگذاری در تصویر بالا اشتباه است زیرا از سمتی است که به اولین کربن دارای پیوند دوگانه عدد بزرگی نسبت داده میشود.
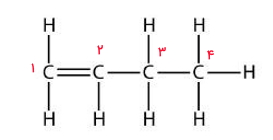
نحوه صحیح نامگذاری این مولکول را در تصویر بالا مشاهده میکنید. به اولین اتم کربن دارای پیوند دوگانه عدد ۱ تعلق گرفته است و آن را بهصورت ۱-بوتن مینامیم. همین قاعده برای مولکولهای طولانیتر با تعداد کربنهای بیشتر نیز صدق میکند. به دلیل این نوع نامگذاری در نام ترکیبهای آلی، اعداد بهوفور به چشم میآیند.
توجه داشته باشید که این دو ایزمر با وجود داشتن فرمول مولکولی یکسان، دارای ویژگیهای شیمیایی و فیزیکی متفاوتی هستند و در شیمی آلی حضور پررنگی دارند.
ایزومر سیس و ترانس
اگر استخلافهای روی پیوند دوگانه هر دو در یک جهت باشند، آلکن را سیس مینامیم و اگر در دو جهت باشند، به آن آلکن ترانس میگوییم. این را میتوانید بهخوبی در تصویر زیر مشاهده کنید. این دو ساختار ایزومر فضایی یکدیگر هستند.

آلکین چیست ؟
در نهایت میخواهیم بدانیم معنای آلکین در هیدوکربن چیست . فرمول شیمیایی کلی ترکیبهای مربوط به خانواده آلکینها را میتوان بهصورت نمایش داد. در جدول زیر ۹ آلکین ابتدایی را مشاهده میکنید. توجه داشته باشید از آنجا که ترکیب آلکن حداقل یک پیوند سهگانه بین کربن-کربن دارد، امکان حضور آلکین با ۱ اتم کربن وجود ندارد.
| نام آلکین | فرمول شیمیایی | تعداد اتم کربن |
| اتین | ۲ | |
| پروپین | ۳ | |
| بوتین | ۴ | |
| پنتین | ۵ | |
| هگزین | ۶ | |
| هپتین | ۷ | |
| اکتین | ۸ | |
| نونین | ۹ | |
| دکین | ۱۰ |
مانند آلکنها، آلکینها نیز به روش یکسانی نامگذاری میشوند، با این تفاوت که به جای «ان» در آلکان و «ن» در آلکن، از «ین» (yne) استفاده میشود.
اتین
سادهترین آلکین، «اتین» (Ethyne) نامیده میشود. این مولکول دارای ۲ اتم کربن و یک پیوند سهگانه است. به این مولکول، «استیلن» (Acetylene) نیز گفته میشود.
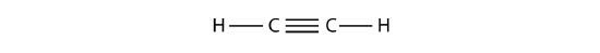
پروپین
دومین عضو خانواده آلکینها با نام «پروپین» (Propyne) نامیده میشود. برای نامگذاری این مولکول عددگذاری کربنها را از سمت چپ شروع میکنیم تا به اولین اتم کربن درگیر در پیوند سهگانه عدد کوچکتری تعلق بگیرد. بنابراین نام صحیح این مولکول ۱-پروپین است و نباید از نام ۲-پروپین استفاده کرد.
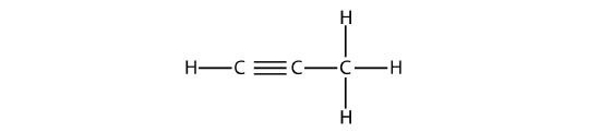
بوتین
این عضو خانواده آلکینها دارای دو ایزومر است که تصویر آنها را در زیر مشاهده میکنید. توجه داشته باشید که مانند موارد پیشین باید به اتم درگیر در پیوند سهگانه کمترین عدد ممکن نسبت داده شود.
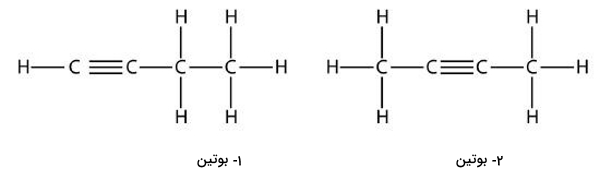
در دو ساختار بالا، ایزومر ۱-بوتین دارای پیوند سهگانه بین کربن شماره ۱ و کربن شماره ۲ است، درحالی که پیوند سهگانه در ایزومر ۲-بوتین بین کربن شماره ۲ و کربن شماره ۳ برقرار شده است.
آلکن و آلکین انتهایی چیست ؟
آیا میدانید معنای آلکن و آلکین در هیدروکربن چیست ؟ آلکنهایی با تعداد کربن ۴ و بیشتر، میتوانند به دو فرم وجود داشته باشند.
- «آلکن ترمینال/ انتهایی» (Terminal Alkene): به آلکن خطی که پیوند دوگانه آن در انتهای زنجیره هیدروکربنی باشد، آلکن ترمینال گفته میشود.
- آلکن داخلی» (Internal Alkene): آلکنی که پیوند دوگانه در هر جایی غیر از دو سر زنجیره هیدروکربن آن باشد، داخلی گفته میشود.
در تصویر زیر بوتن ترمینال را مشاهده میکنید. به پیوند دوگانه که در سر زنجیره قرار دارد، توجه کنید.
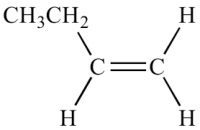
تصویر زیر مربوط به بوتن داخلی است زیرا زنجیره هیدروکربنی در دو طرف پیوند دوگانه امتداد دارد.
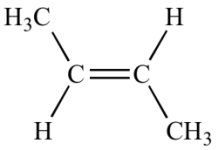
آلکینها نیز مانند آلکنها دارای دو نوع ترمینال و داخلی هستند. این دو نوع آلکن در برخی ویژگیها مانند واکنشپذیری از خود رفتارهای متفاوتی نشان میدهند.
هیدروکربن آروماتیک چیست ؟
در این بخش میخواهیم بدانیم معنای آروماتیک در هیدروکربن چیست . همانطور که پیشتر گفتیم هیدروکربنهای آروماتیک دارای حلقه ۶ عضوی به نام بنزن هستند. الکترونهای حلقه بنزنی دارای ویژگیهایی در انرژی خود هستند که به آن ویژگیهای شیمیایی و فیزیکی خاصی میدهد که باعث تفاوت آنها از آلکانها میشود. در ابتدا از کلمه آروماتیک برای این ترکیبها استفاده میشد زیرا ترکیبهای این خانواده از خود عطر خوشایندی ساطع میکردند. با این حال در شیمی آلی جدید واژه آروماتیک فارغ از ویژگی معطر بودن به این ترکیبها داده میشود.
بنزن حلقهای ۶ عضوی و پیوندهای آن یک در میان دوگانه است. فرمول مولکولی بنزن بهصورت است. ساختار آن را میتوانید در تصویر زیر مشاهده کنید.
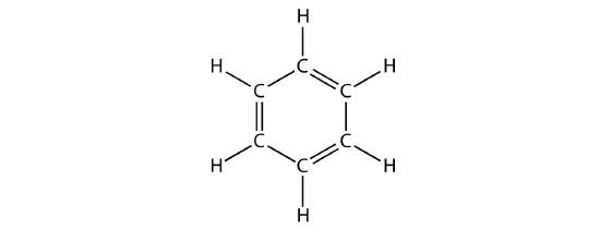
این مولکول ساختاری ۶ ضلعی دارد و به هر کربن آن یک هیدروژن متصل است تا هر ۴ ظرفیت کووالانسی اتم کربن پر شود. همانطور که مشاهده میکنید هر کربن دارای یک پیوند دوگانه با کربنی دیگر، یک پیوند یگانه با کربنی دیگر و یک پیوند یگانه با هیدروژن است.
ویژگی خاص بنزن به همین پیوند یک در میان دوگانه ربط دارد. بنزن بسیار پایدار است و مانند آلکنها وارد واکنش نمیشود. هیدروکربنهای آروماتیک پیچیدهتری نیز وجود دارند که به جای هیدروژن، استخلافهای بزرگتری داشته باشند. نمونهای از آن را میتوانید در ساختار تصویر زیر مشاهده کنید.
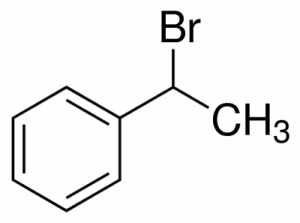
در مولکول بالا جایگزین یک اتم هیدروژن شده است.
برخی از هیدروکربنهای آروماتیک در نفت خام وجود دارند و بسیار معروف و پرتکرار هستند. تعدادی از آنها را میتوانید در تصویر زیر مشاهده کنید.
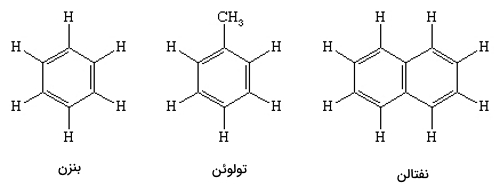
هیدروکربن راست زنجیر چیست ؟
در این بخش میخواهیم بدانیم معنای راستزنجیر در هیدروکربن چیست . هیدروکربنهای راست زنجیر بهصورت خطی هستند و دارای شاخه (استخلاف) یا حلقه نیستند. این نوع از هیدروکربنها سادهترین نوع هستند و میتوانند دارای پیوند دوگانه و سهگانه نیز باشند. برای نامگذاری این هیدروکربنها تنها کافی است پیشوند مناسب برای تعداد اتمهای کربن را همراه با «ان» برای آلکان، «ن» برای آلکن و «ین» برای آلکین بیاوریم. توجه داشته باشید که برای آلکن و آلکین آوردن موقعیت پیوند دوگانه و سهگانه مورد نیاز است. در تصویر زیر نمونهای از هیدروکربن راست زنجیر را در مقایسه با هیدروکربن شاخهدار مشاهده میکنید.
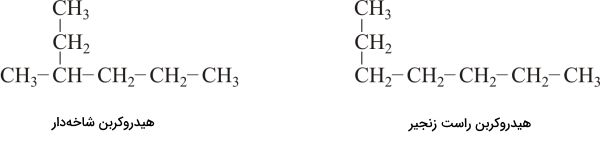
هیدروکربن شاخه دار چیست ؟
در این بخش میخواهیم بدانیم حضور شاخه در ساختار هیدروکربن چیست . تمامی هیدروکربنها آنقدر ساده نیستند که بهصورت راست زنجیر وجود داشته باشند. برخی از آنها دارای شاخههایی متشکل از اتمهای کربن هستند. این هیدروکربنها درواقع ایزومر هیدروکربنهای راست زنجیر با تعداد کربن یکسان اما دارای ویژگیهای شیمیایی و فیزیکی متفاوتی هستند و باید به شکلی نامگذاری شوند که از هیدروکربنهای راست زنجیر قابل تشخیص باشند. در این نامگذاری باید به نکات زیر توجه کرد.
- همیشه زنجیرهای اصلی است که دارای بیشترین تعداد اتم کربن باشد. همچنین در مورد هیدروکربنهای غیراشباع این زنجیره باید پیوند دوگانه و سهگانه را در بر بگیرد.
- تلاش بر این است که به استخلافها کمترین عدد ممکن داده شود.
- نام استخلافها به همراه موقعیت آنها پیش از نام اسکلت هیدروکربنی آورده میشود.
مثال هیدروکربن آروماتیک و آلیفاتیک
به مولکولهای زیر دقت کنید و بگویید آلفاتیک هستند یا آروماتیک؟ در صورت آلیفاتیک بودن، نوع آن را نیز مشخص کنید. (آلکان، آلکن، آلکین)
مولکول ۱
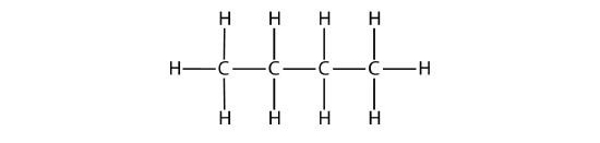
پاسخ: این مولکول فاقد حلقه بنزنی و در نتیجه هیدروکربنی آلفاتیک است. به دلیل عدم وجود پیوند دوگانه و سهگانه به خانواده آلکانها تعلق دارد و نام آن بوتان است.
مولکول ۲
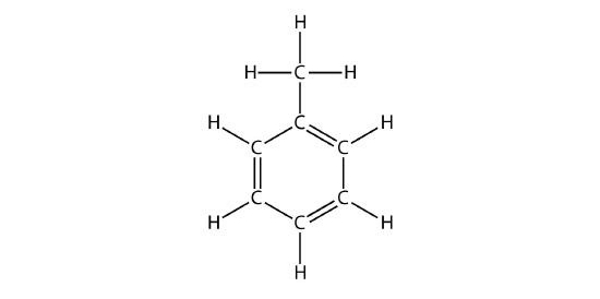
پاسخ: به دلیل وجود حلقه ۶ کربنی بنزنی، این هیدروکربن آروماتیک است.
مولکول ۳
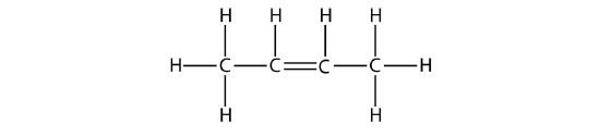
پاسخ: مولکول بالا فاقد حلقه بنزنی است، بنابراین به خانواده هیدروکربنهای آلیفاتیک تعلق دارد. از آنجا که در ساختار آن یک پیوند دوگانه وجود دارد، آلکن است و ۲-بوتن نامیده میشود. در این مثال زنجیره هیدروکربنی را از هر سمتی نامگذاری کنیم، نتیجه یکسان خواهد بود.
مولکول ۴
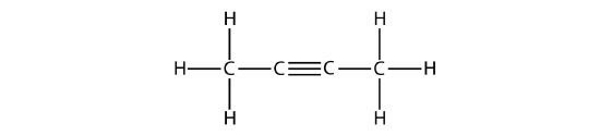
پاسخ: مانند مورد قبل در این مولکول نیز حلقه بنزنی مشاهده نمیشود، بنابراین هیدروکربن آروماتیک نیست. وجود پیوند سهگانه در زنجیره یعنی به خانواده آلکینها تعلق دارد و نام آن ۲-بوتین است. در این مورد چه مولکول از سمت راست عددگذاری شود، چه از سمت چپ، تفاوتی ایجاد نمیشود.
مولکول ۵
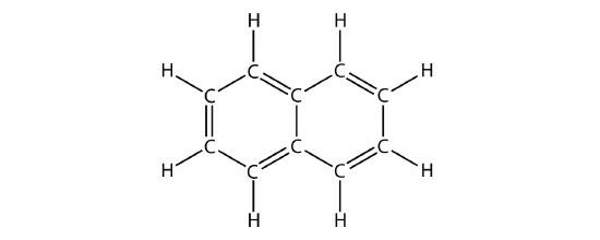
پاسخ: در این مثال وجود حلقه بنزنی در هیدروکربن یعنی آروماتیک است.
مولکول ۶
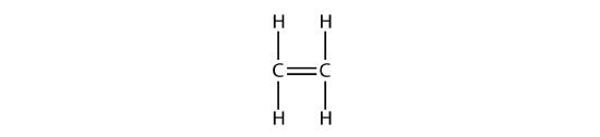
پاسخ: همانطور که مشاهده میکنید در این ساختار حلقه بنزنی وجود ندارد، بنابراین هیدروکربن آلیفاتیک است. حضور پیوند دوگانه یعنی آلکن است و اتن نامیده میشود. این مولکول سادهترین آلکن است.
مولکول ۷
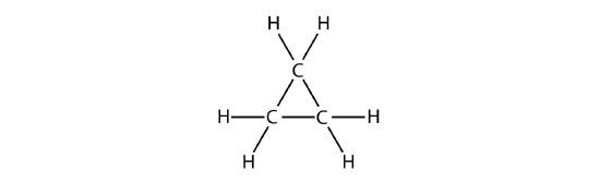
پاسخ: این ساختار حلقه بنزنی ندارد بنابراین آروماتیک نیست. همچنین به دلیل عدم وجود پیوند دوگانه و سهگانه، آلکان است و پروپان حلقوی (سیکلوپروپان) نامیده میشود.
مولکول ۸
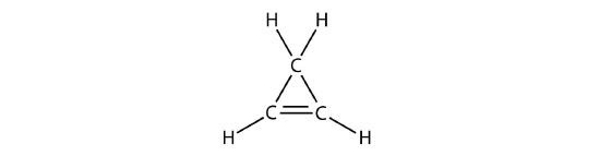
پاسخ: مولکول بالا فاقد حلقه بنزنی است و به هیدروکربنهای آلیفاتیک تعلق دارد. در ساختار آن یک پیوند دوگانه وجود دارد، بنابراین آلکن است. نام این ساختار پروپن حلقوی (سیکلوپروپن) است.
مولکول ۹
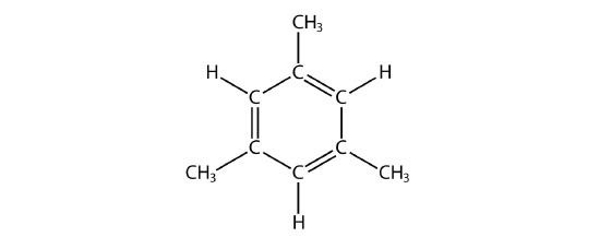
پاسخ: در این ساختار یک حلقه بنزنی وجود دارد و آروماتیک است.
مولکول ۱۰
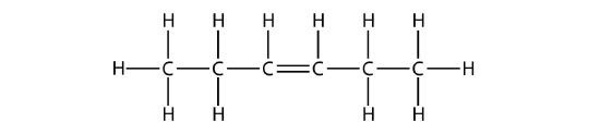
پاسخ: این مولکول فاقد حلقه ۶ عضوی بنزن و هیدروکربنی آلفاتیک است. با توجه به وجود پیوند دوگانه آلکن نامیده میشود. نام این زنجیره هیدروکربنی ۳-هگزن است. توجه داشته باشید که مولکول از هر جهتی عددگذاری شود، همین نام را خواهد داشت.
مولکول ۱۱
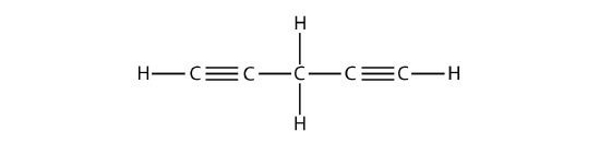
پاسخ: این مولکول نیز فاقد حلقه بنزنی و آلیفاتیک است. به دلیل وجود پیوند سهگانه به خانواده آلکینها تعلق دارد و ۱و۵-پنتین نامیده میشود.
هیدروکربن حلقوی چیست ؟
در این بخش میخواهیم بدانیم حضور حلقه در هیدروکربن چیست . هیدروکربن حلقوی، هیدروکربنی است که در آن زنجیره کربنی با حذف هیدروژن به خودش متصل شده باشد. این دسته از هیدروکربنها را میتوان بهصورت زیر طبقهبندی کرد.
- «آلکان حلقوی» (Cycloalkane)
- «آلکن حلقوی» (Cycloalkene)
- «آلکین حلقوی» (Cycloalkyne)
در بخشهای پیش رو میخواهیم بدانیم هر یک از این هیدروکربن ها چیست.
آلکان حلقوی
به همین صورت به هیدروکربنهای حلقوی که تنها دارای پیوند یگانه باشند، آلکان حلقوی میگوییم. آلکانهای حلقوی مانند خود آلکانها، ترکیبهایی اشباع هستند. فرمول کلی این ترکیبها را میتوان بهصورت نمایش داد. در تصویر زیر سادهترین آلکان حلقوی را میبینید که پروپان حلقوی نامیده میشود.
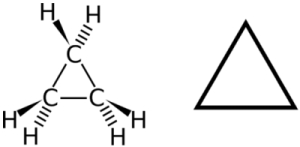
در تصویر سمت چپ هیدروژنهای هر اتم کربن نشان داده شده است و در تصویر سمت راست برای سهولت کار آن را به شکل سادهتری با حذف نماد عنصرها، نشان دادهایم. توجه داشته باشید که هر راس مثلث یک اتم کربن است. اتمهای کربن در آلکانهای حلقوی مانند آلکانها دارای هیبریداسیون و زاویه پیوندی برابر با ۱۰۹٫۵ درجه هستند.
مطالعه پروپان حلقوی نشان داده است که زاویه پیوندی در آن به ۶۰ درجه میرسد. این انحراف از مقدار اصلی در پروپان حلقوی را به مفهومی به نام «فشار حلقه» (Ring Strain) نسبت میدهند که باعث ناپایداری این مولکول و واکنشپذیری بالای آن میشود. با بالا رفتن تعداد اتمهای حلقه از ۳ به ۴ از این فشار کاسته میشود، بهصورتی که زاویه پیوند در بوتان حلقوی برابر با ۹۰ درجه است. این مقدار همچنان غیرقابل اغماض است و باعث ناپایداری مولکول میشود. در جدول زیر روند تغییر زاویه پیوندی را با افزایش تعداد اتمهای کربن هر ساختار مشاهده میکنید.
| نام ساختار | تعداد اتم کربن | فشار زاویهای |
| پروپان حلقوی | ۳ | ۶۰ |
| بوتان حلقوی | ۴ | ۹۰ |
| پنتان حلقوی | ۵ | ۱۰۸ |
| هگزان حلقوی | ۶ | ۱۰۹٫۵ |
همانطور که مشاهده میکنید زاویه پیوندی برای پنتان حلقوی با ۵ اتم کربن به ۱۰۸ درجه میرسد و همین باعث پایداری این مولکول میشود. در تصویر زیر ساختار بوتان و پنتان حلقوی را آوردهایم.
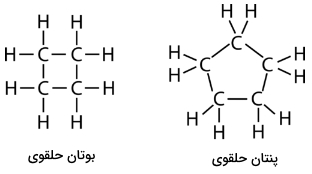
ساختار هگزان حلقوی با ۶ اتم کربن را در زیر مشاهده میکنید. توجه داشته باشید که با اینکه این رسم شکل غلط نیست اما در مورد این مولکول گمراهکننده است زیرا آن را بهصورت تخت نشان میدهد. درواقع هگزان حلقوی برای کاهش فشار زاویهای کمی خم میشود.
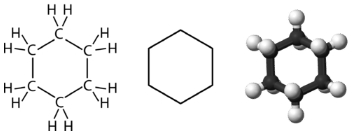
این خمشدگی بهصورتی است که اتمهای کربن به شکل یک در میان در پایین و بالای صفحه قرار میگیرند. در تصویر زیر دو «صورتبندی» (Conformation) مهم این مولکول را مشاهده میکنید. به شکل سمت راست «صورتبندی صندلی» (Chair Conformation) و به شکل سمت چپ «صورتبندی قایق» (Boat Conformation) گفته میشود.
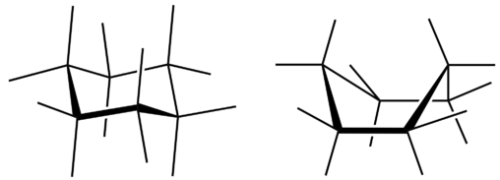
هر دوی این صورتبندیها باعث کاهش فشار زاویهای میشوند اما فرم صندلی ارجحیت دارد. به این دلیل که برهمکنش از نوع دافعه بین هیدروژنهای موجود روی کربنها در فرم صندلی کمتر است. با این حال باید به این نکته توجه داشته باشیم که این دو صورتبندی به آسانی به یکدیگر تبدیل میشوند. آلکانهای حلقوی با تعداد اتم کربن بیشتر نیز امکان حضور دارند اما رواج کمتری دارند.
ایزومری در آلکان حلقوی
در این بخش میخواهیم بدانیم معنای ایزومری در هیدروکربن چیست .آلکانهای حلقوی میتوانند دارای «ایزومرهای فضایی» (Stereoisomers) باشند. ایزومرهای فضایی دارای فرمول مولکولی و نحوه اتصال یکسان هستند اما در جهتگیری فضایی با یکدیگر متفاوت هستند.
آلکانهای حلقوی شباهت بسیاری به آلکانهای خطی دارند. هر دو گروه ناقطبی و با واکنشپذیری پایینی هستند اما آلکانهای حلقوی آزادی حرکت بسیار کمتری دارند. میدانیم که آلکانهای خطی توانایی چرخش حول پیوند یگانه سیگمای خود را دارند. این توانایی در آلکانهای حلقوی وجود ندارد و باعث صلبیت آنها میشود.
آلکانهای حلقوی دارای دو استخلاف از جمله مولکولهایی هستند که میتوانند ایزومر فضایی داشته باشند. این مسئله را با بررسی مثالی، روشن خواهیم کرد.
آلکان حلقوی ۱و۲-دی برمو سیکلوپنتان میتواند دو ایزومر داشته باشد.
- سیس-۱و۲-دیبرمو سیکلوپنتان
- ترانس-۱و۲-دیبرمو سیکلو پنتان
این دو مولکول در تصویر زیر آورده شده است. توجه کنید که هر دو دارای فرمول مولکولی و نحوه اتصال مشابه هستند. تفاوت آنها تنها در جهتگیری استخلافهای برم روی حلقه است.
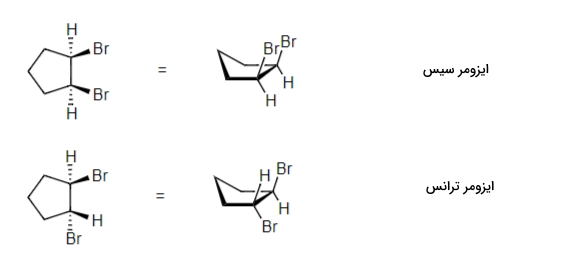
با توجه به تصویر بالا متوجه میشویم که در ایزومری که بهصورت سیس است، هر دو استخلاف برم در یک سمت قرار دارند اما در مورد ایزومر ترانس این صدق نمیکند.
شیمیدانها برای نمایش این اختلاف از گوه (مثلث مشکی) برای نمایش استخلافهایی استفاده میکنند که بیرون از صفحه و به سمت بیننده قرار دارد. خطچین نیز برای نمایش استخلافهایی بهکار گرفته میشود که درون صفحه و دور از بیننده قرار دارند.
مثال ایزومر در هیدروکربن
ایزومرهای ممکن مولکول پنتن را رسم کنید و آنها را نام گذاری کنید.
پاسخ: این ساختار دارای دو ایزومر بهصورت زیر است.
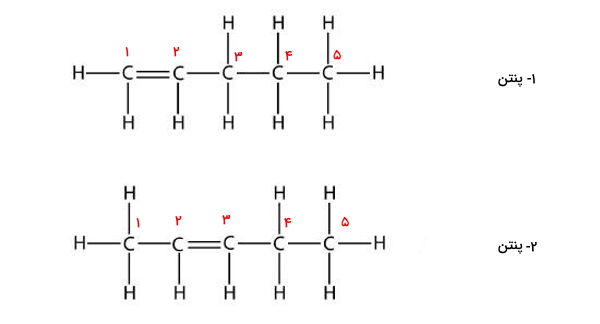
اعداد منتسب به کربنها باید بهصورتی باشد که کوچکترین عدد ممکن به کربن درگیر در پیوند دوگانه تعلق بگیرد. به همین دلیل ایزومری به نام ۳-پنتن وجود ندارد.
هیدروکربن حلقوی غیراشباع
هیدروکربنهای حلقوی فقط بهصورت آلکان حلقوی حضور ندارند. آلکن حلقوی، هیدروکربنی حلقوی است به شکلی که حداقل دارای یک پیوند دوگانه باشد. به همین ترتیب به هیدروکربنهای حلقوی که دارای پیوند سهگانه باشند، آلکین حلقوی گفته میشود. در تصویر زیر نمونهای از این ترکیبها را مشاهده میکنید.
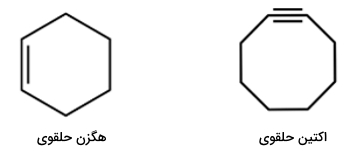
مثال هیدروکربن حلقوی
در این بخش به نام گذاری تعدادی هیدروکربن حلقوی میپردازیم.
مثال اول
نام هیدروکربنهای حلقوی زیر را بر اساس قوانین آیوپاک مشخص کنید.
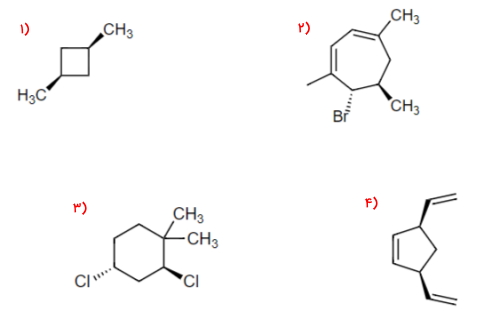
مولکول ۱
در هیدروکربنهای حلقوی نیز نیاز داریم که اتمهای کربن را پیش از هر کاری عددگذاری میکنیم و این اعداد باید بهصورتی باشد که پیوند دوگانه و سهگانه و استخلافهای کمترین اعداد ممکن را داشته باشند. برای این مولکول عددگذاری صحیح به شکل زیر انجام میشود تا به دو استخلاف متیل اعداد ۱ و ۳ تعلق بگیرد.
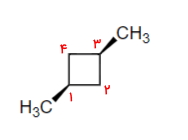
نیاز است که پیش از نام حلقه که سیکلوبوتان است، استخلافهای را همراه با موقعیت آنها بیاوریم. از طرفی باید به جهتگیری فضایی این استخلافها نیز توجه کنیم. مشاهده میکنید که دو استخلاف متیل هر دو در جهت بیرون صفحه قرار دارند و مولکول سیس است. بنابراین نام این آلکان حلقوی «سیس-۱و۳-دیمتیل سیکلوبوتان» است.
مولکول ۲
در این هیدروکربن حلقوی دو پیوند دوگانه، ۳ استخلاف متیل و ۱ استخلاف برم وجود دارد. برای این مولکول عددگذاری صحیح به شکل زیر انجام میشود تا به سه استخلاف متیل اعداد ۱ و ۴ و ۶ تعلق بگیرد. توجه داشته باشید که اولویت عددگذاری با این است که پیوندهای دوگانه کمترین اعداد را داشته باشند.
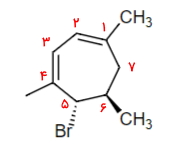
نیاز است که پیش از نام حلقه استخلافهای را همراه با موقعیت و جهتگیری فضایی آنها بیاوریم. همانطور که مشاهده میکنید دو استخلاف برم و متیل که روی کربنهای مجاور هم هستند، دارای جهتگیری متفاوتی هستند و این یعنی استخلاف دیگر این کربنها که هیدروژن است، نیز دارای جهتگیری مخالف هستند و باید از واژه ترانس پیش از نام این هیدروکربن حلقوی استفاده کنیم. بنابراین نام صحیح این آلکن حلقوی «ترانس-۵-برمو ۱و۴و۶-تریمتیل ۱و۳-سیکلوهپتادین» است.
مولکول ۳
در این هیدروکربن حلقوی پیوند دوگانه و سهگانه نداریم بنابراین برای عددگذاری باید تنها به استخلافهای آن توجه کنیم. برای این مولکول عددگذاری صحیح به شکل زیر انجام میشود تا به دو استخلاف متیل اعداد ۱ و ۳ و به دو استخلاف کلر اعداد ۲ و ۴ تعلق بگیرد.
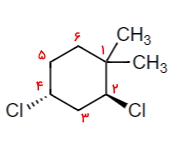
نیاز است که پیش از نام حلقه که سیکلوبوتان است، استخلافها را همراه با موقعیت و جهتگیری آنها بیاوریم. همانطور که مشاهده میکنید دو استخلاف کلر یکی روی صفحه و دیگری پشت آن است و بهصورت ترانس نسبت به یکدیگر قرار دارند و این را حتما در نام مولکول باید ذکر کنیم. از طرفی بین استخلاف کلر و متیل، کلر به دلیل جلوتر بودن در حروف الفبای انگلیسی ارجح است. بنابراین نام این آلکان حلقوی «ترانس ۲و۴-دیکلرو ۱و۲-دیمتیل سیکلوهگزان» است.
مولکول ۴
این مثال با مثالهای پیش اندکی متفاوت است. برای این مولکول عددگذاری صحیح به شکل زیر انجام میشود تا پیوند دوگانه موجود در حلقه عدد ۱ را داشته باشد. در این حالت به دو استخلاف وینیلی عدد ۳ و ۵ تعلق میگیرد
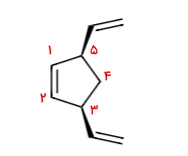
نیاز است که پیش از نام حلقه که سیکلوپنتن است، استخلافهای را همراه با موقعیت آنها بیاوریم. از طرفی دو استخلاف وینیلی با یکدیگر در حالت سیس هستند، زیرا هر دو با گوه نشان دادهشدهاند و به جهت روی صفحه قرار دارند. بنابراین نام این آلکن حلقوی «سیس-۳و۵-دیوینیل سیکلوپنتن» است.
مثال دوم
نام این هیدروکربنهای زیر چیست ؟
مولکول ۱
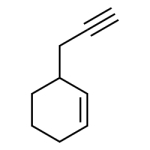
پاسخ: در این مثال استخلاف روی هیدروکربن حلقوی دارای پیوند سهگانه و از خانواده آلکینیلها است. ابتدا نیاز است که اتمهای کربن داخل حلقه را نامگذاری کنیم. این کار را به شکلی انجام میدهیم که به پیوند دوگانه داخل حلقه عدد ۱ تعلق بگیرد. همچنین با عددگذاری بهصورت پادساعتگرد به استخلاف، عدد ۳ نسبت داده میشود. اگر جهت عددگذاری را ساعتگرد در نظر میگرفتیم این استخلاف دارای عدد ۶ و نادرست بود.
توجه داشته باشید که برای عددگذاری استخلاف آلکینیل خارج از حلقه باید این کار را از نزدیکترین اتم کربن نسبت به حلقه انجام دهیم، هرچند که این کار باعث میشود به پیوند سهگانه عدد بزرگتری تعلق بگیرد.
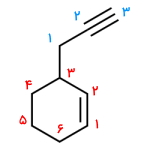
نام اسکلت حلقوی این هیدروکربن هگزن است و نیاز است که نام استخلاف را نیز پیش از آن ذکر کنیم. بنابراین نام این آلکن حلقوی «۳-(۲-پروپینیل) سیکلوهگزن» است.
مولکول ۲
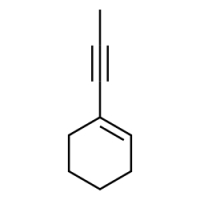
پاسخ: در این مثال استخلاف روی هیدروکربن حلقوی دارای پیوند سهگانه و از خانواده آلکینیلها است. ابتدا نیاز است که اتمهای کربن داخل حلقه را نامگذاری کنیم. این کار را به شکلی انجام میدهیم که به پیوند دوگانه داخل حلقه عدد ۱ تعلق بگیرد. همچنین با عددگذاری بهصورت ساعتگرد به استخلاف پروپینیل نیز عدد ۱ نسبت داده میشود.
توجه داشته باشید که برای عددگذاری استخلاف آلکینیل خارج از حلقه باید این کار را از نزدیکترین اتم کربن نسبت به حلقه انجام دهیم، و به این روش پیوند سهگانه نیز دارای عدد ۱ خواهد بود.
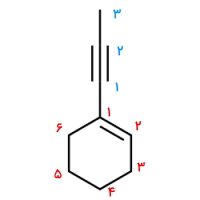
نام اسکلت حلقوی این هیدروکربن سیکلوهگزن است و نیاز است که نام استخلاف را نیز پیش از آن ذکر کنیم. بنابراین نام این آلکن حلقوی «۱-(۱-پروپینیل) سیکلوهگزن» است.
مولکول ۳
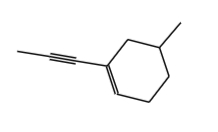
پاسخ: این مثال نیز دارای استخلاف با پیوند سهگانه و از خانواده آلکینیلها است. ابتدا اتمهای کربن داخل حلقه را نامگذاری میکنیم. این کار را به شکلی انجام میدهیم که به پیوند دوگانه داخل حلقه عدد ۱ تعلق بگیرد. همچنین با عددگذاری بهصورت پادساعتگرد به استخلاف پروپینیل نیز عدد ۱ نسبت داده میشود. در این هیدروکربن استخلاف متیلی نیز وجود دارد که به اتم کربن آن عدد ۵ تعلق میگیرد.
همانطور که پیش از این گفتیم برای عددگذاری استخلاف آلکینیل خارج از حلقه باید این کار را از نزدیکترین اتم کربن نسبت به حلقه انجام دهیم، و به این روش پیوند سهگانه نیز دارای عدد ۱ خواهد بود.
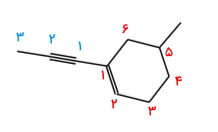
نام اسکلت حلقوی این هیدروکربن سیکلوهگزن است و نیاز است که نام استخلافها را نیز پیش از آن ذکر کنیم. از طرفی آوردن نام استخلاف متیل به پروپینیل ارجح است. بنابراین نام این آلکن حلقوی «۵-متیل ۱-(۱-پروپینیل) سیکلوهگزن» است.
مولکول ۴
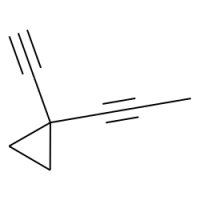
پاسخ: این مثال دارای دو استخلاف با پیوند سهگانه و از خانواده آلکینیلها است. ابتدا اتمهای کربن داخل حلقه را نامگذاری میکنیم. این کار را به شکلی انجام میدهیم که به دو استخلاف عدد ۱ تعلق بگیرد. توجه داشته باشید که در این مورد جهت اعداد بعدی اهمیتی ندارد.
همانطور که پیش از این گفتیم برای عددگذاری استخلاف آلکینیل خارج از حلقه باید این کار را از نزدیکترین اتم کربن نسبت به حلقه انجام دهیم، و به این روش هر دو پیوند سهگانه دارای عدد ۱ خواهد بود.
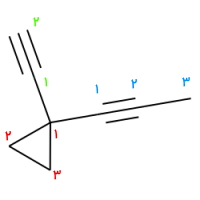
نام اسکلت حلقوی این هیدروکربن سیکلوپروپان است و نیاز است که نام استخلافها را نیز پیش از آن ذکر کنیم. از طرفی آوردن نام استخلاف اتینیل به پروپینیل ارجح است. بنابراین نام این آلکن حلقوی «۱-اتینیل ۱-(۱-پروپینیل) سیکلوپروپان» است.
مولکول ۵
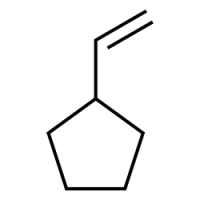
پاسخ: این مثال دارای استخلافی با پیوند دوگانه و از خانواده آلکنیلها است. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به استخلاف عدد ۱ تعلق بگیرد. توجه داشته باشید که در این مورد جهت اعداد بعدی اهمیتی ندارد.
در این مورد از آنجا که استخلاف بهصورت وینیل و دارای ۲ اتم کربن است، نیازی به تخصیص عدد ندارد.
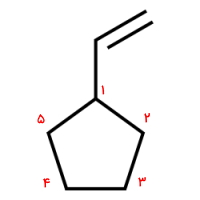
از آنجا که وینیل در جایگاه ۱ قرار دارد، لزومی بر آوردن ۱ پیش از نام آن نیست و نام این آلکان حلقوی «وینیل سیکلوپنتان» است.
مولکول ۶
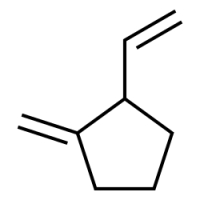
پاسخ: این مثال دارای دو استخلاف با پیوندهای دوگانه و از خانواده آلکنیلها است. ابتدا اتمهای کربن داخل حلقه را نامگذاری میکنیم. این کار را به شکلی انجام میدهیم که به استخلافها عدد کمتری تعلق بگیرد. توجه داشته باشید که به دلیل اولویت استخلاف متیلن به وینیل عددگذاری را از آن شروع میکنیم.
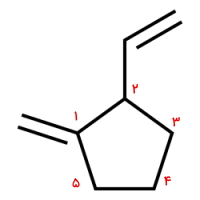
بنابراین به وینیل عدد ۲ و به متیلن عدد ۱ تعلق گرفت. نام این آلکان حلقوی «۱-متیلن ۲-وینیل سیکلوپنتان» است.
مولکول ۷
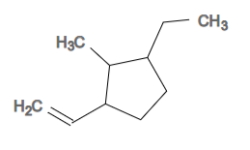
پاسخ: این مثال دارای دو استخلاف آلکانی و یک استخلاف از خانواده آلکنیلها است. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به استخلافها عدد کمتری تعلق بگیرد. توجه داشته باشید که به دلیل اولویت استخلاف اتنیل به اتیل و متیل، عددگذاری را از آن شروع میکنیم و بهصورت ساعتگرد ادامه میدهیم.
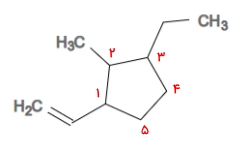
بنابراین به استخلاف اتنیل عدد ۱، به استخلاف اتیل عدد ۳ و به استخلاف متیل عدد ۲ نسبت داده میشود. نام این آلکان حلقوی «۱-اتنیل ۳-اتیل ۲-متیل سیکلوپنتان» است.
مولکول ۸
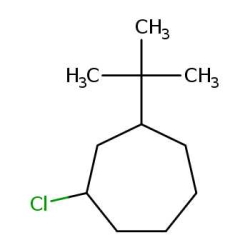
پاسخ: این مثال دارای دو استخلاف ترشیو بوتیل و کلر است. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به استخلافها عدد کمتری تعلق بگیرد. توجه داشته باشید که اولویت با بوتیل است و نباید به دلیل حضور پیشوند «ترشیو» آن را در اولویت دوم نسبت به کلر قرار دهیم.
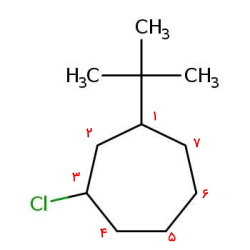
بنابراین به استخلاف ترشیوبوتیل عدد ۱ و به استخلاف کلر عدد ۳ نسبت داده میشود. نام این آلکان حلقوی «۱-ترشیوبوتیل ۳-کلرو سیکلوهپتان» است.
مولکول ۹
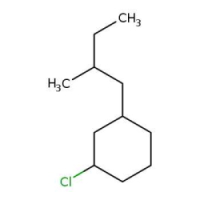
پاسخ: این مثال دارای استخلافی آلکانی است که روی خود استخلافی متیلی دارد. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به استخلافها عدد کمتری تعلق بگیرد. توجه داشته باشید که در اینجا اولویت با کلر است. همچنین نیاز است که استخلاف بوتیل را نیز عددگذاری کنیم. (با رنگ آبی نشان داده شده است) این نامگذاری از کربن نزدیک به حلقه انجام میشود و به متیل عدد ۲ تعلق میگیرد.
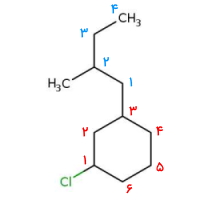
نام این آلکان حلقوی «۱-کلرو ۳-(۲-متیل بوتیل) سیکلوهگزان» است.
مولکول ۱۰
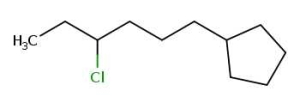
پاسخ: این مثال دارای استخلافی آلکانی است که روی خود استخلافی کلری دارد. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به تنها استخلاف آن عدد ۱ برسد. جهت عددگذاری حلقه چه ساعتگرد باشد چه پادساعتگرد تفاوتی ایجاد نمیشود. همچنین نیاز است که استخلاف هگزیل را نیز عددگذاری کنیم. (با رنگ آبی نشان داده شده است) این نامگذاری از کربن نزدیک به حلقه انجام میشود و به کلر عدد ۴ تعلق میگیرد.
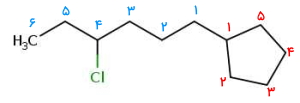
نام این آلکان حلقوی «۱-(۴-کلرو هگزیل) سیکلوهپتان» است.
مولکول ۱۱
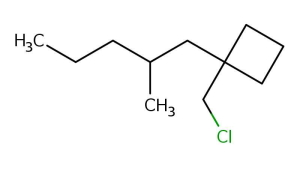
پاسخ: این حلقه دارای استخلافی آلکانی است که روی خود استخلافی متیلی دارد. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به دو استخلاف آن عدد ۱ برسد. جهت عددگذاری حلقه چه ساعتگرد باشد چه پادساعتگرد تفاوتی ایجاد نمیشود. همچنین نیاز است که استخلاف پنتیل را نیز عددگذاری کنیم. (با رنگ آبی نشان داده شده است) این نامگذاری از کربن نزدیک به حلقه انجام میشود و به متیل عدد ۲ تعلق میگیرد.
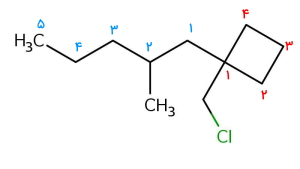
توجه داشته باشید که در آوردن نام استخلافها اولویت با کلرومتیل خواهد بود. نام این آلکان حلقوی «۱-(کلرومتیل) ۱-(۲-متیل پنتیل) سیکلوبوتان» است.
هیدروکربن اشباع و هیدروکربن غیر اشباع
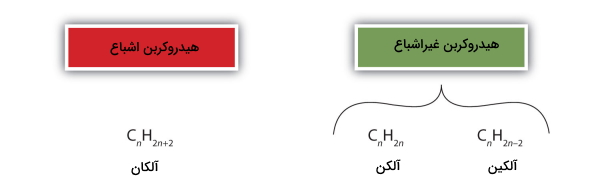
برای شناخت کامل باید بدانیم مفهوم اشباعی و غیراشباعی در هیدروکربن چیست . هیدروکربنها را میتوان به دو دسته اشباع و غیراشباع طبقهبندی کرد. در این بخش به بررسی هر کدام خواهیم پرداخت.
- به آلکانها «هیدروکربن اشباع» (Saturated Hydrocarbon) نیز گفته میشود زیرا تمام ظرفیتهای کووالانسی آن اشغال شده است. در هیدروکربنهای اشباع اتمهای کربن و هیدروژن توسط پیوندهای یگانه به یکدیگر متصل میشوند و سادهترین هیدروکربنهای ممکن را به وجود میآورند. هیدروکربنهای اشباع فاقد پیوند دوگانه و سهگانه کربن-کربن هستند.
- به آلکنها و آلکینها که دارای پیوند دوگانه و سهگانه هستند به دلیل خالی بودن ظرفیت کووالانسی آنها، «هیدروکربن غیراشباع» (Unsaturated Hydrocarbon) میگویند.
ویژگی هیدروکربن
در این بخش میخواهیم بدانیم مهمترین ویژگی هیدروکربن چیست . هیدروکربنها مولکولهایی هستند که بهوفور در صنایع و حوزههای مختلف و در زندگی انسان حضور دارند. در این بخش میخواهیم به تعدادی از ویژگیهای این گروه از ترکیبها اشاره کنیم.
- فرمول کلی هیدروکربنها را میتوان بهصورت نمایش داد.
- هیدروکربنهای میتوانند زنجیرهای بسیار طولانی از اتمهای کربن داشته باشند. به توانایی اتم کربن در اتصال به خود و تشکیل مولکولهای حجیم، «کاتناسیون» (Catenation) گفته میشود. به این ترتیب است که مولکولهایی مانند هگزان حلقوی و بنزن وجود دارند.
- بیشتر هیدروکربنها «غیرقطبی» (Nonpolar) هستند زیرا الکترونگاتیوی کربن و هیدروژن به یکدیگر نزدیک است. به همین دلیل نیز به مقدار بسیار کمی در آب و دیگر حلالهای قطبی حل میشود.
- هیدروکربنهای کوچک مانند متان و اتان در دمای اتاق بهصورت گاز حضور دارند اما هیدروکربنهای بزرگتر مانند هگزان و اکتان در همین شرایط مایع هستند. هیدروکربنهای بزرگتر از اینها در دمای اتاق جامد هستند و حالتی شبیه به موم دارند.
- مشتقهای هیدروکربنی در گیاهان و درختها وجود دارند. برای مثال کاروتن رنگدانهای آلی است که در برگهای سبز و هویج وجود دارد.
- هیدروکربنهای بزرگ طی فرایندی به نام «شکست هیدروکربن» (Cracking Of Hydrocarbon) شکافته میشوند و هیدروکربنهای کوچکتری برجا میگذارند. این واکنش در حضور فشار و دمای کافی صورت میگیرد. در برخی موارد نیز از کاتالیزور برای افزایش سرعت آن استفاده میشود. این واکنش در تولید سوخت گازوئیل و بنزین نقش بهسزایی دارد.
- آلکانها به دلیل ضعیف بودن نیروی واندروالسی بینمولکولی، نقطه ذوب و نقطه جوش پایینی دارند.
نقطه جوش هیدروکربن
نقطه جوش هیدروکربنها در حالت کلی به دو عامل زیر بستگی دارد.
- جرم مولکولی
- شاخه هیدروکربن
هر چه جرم مولکولی هیدروکربنی بیشتر باشد، نقطه جوش آن نیز افزایش پیدا میکند. برای مثال نقطه جوش اتان با دو اتم کربن از متان با ۱ اتم کربن بیشتر است.
در حالتی که دو آلکان جرم مولکولی برابری داشته باشد، اما در نوع و تعداد شاخههای خود با یکدیگر متفاوت باشند، آلکانی که شاخه کمتری دارد، نقطه جوش بالاتری خواهد داشت. این اختلاف به دلیل بیشتر بودن نیروی بینمولکولی واندروالس در آلکانهای غیرشاخهای است. در زیر مثالی از این مورد را بررسی خواهیم کرد.
سه مولکول زیر دارای تعداد اتم کربن برابر با یکدیگر، ۶ عدد، هستند. همانطور که پیشتر گفتیم، نقطه جوش با افزایش شاخههای آلکان کاهش مییابد.
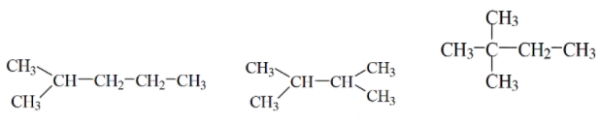
در تصویر بالا، بیشترین نقطه جوش مربوط به ساختار سمت چپ با ۶۰ درجه سانتیگراد و کمترین نقطه جوش مربوط به ساختار سمت راست با ۵۰ درجه سانتیگراد است. مولکول میانی نیز نقطه جوشی برابر با ۵۸ درجه سانتیگراد دارد.
ترتیب نقطه جوش در هیدروکربن
در این بخش میخواهیم بدانیم ترتیب افزایش نقطه جوش هیدروکربن چیست . در حالت کلی میتوان روند تغییر نقطه جوش در هیدروکربنها را بهصورت زیر نشان داد.
آلکین > آلکن > آلکان راستزنجیر > آلکان شاخهدار > آلکان حلقوی
ترتیب نقطه ذوب در هیدروکربنها
در این بخش میخواهیم بدانیم ترتیب افزایش نقطه ذوب در هیدروکربن چیست . روند تغییر نقطه ذوب در انواع هیدروکربنها را میتوان بهصورت زیر نمایش داد.
آلکین > آلکن ترانس > آلکن سیس > آلکان حلقوی > آلکان شاخهدار > آلکان راستزنجیر
در جدول زیر میتوانید خلاصهای از آنچه در بالا آورده شده است را برای آلکانها میبینید.
| نام | نقطه ذوب (درجه سانتیگراد) | نقطه جوش (درجه سانتیگراد) |
| متان | ۱۸۲٫۵- | ۱۶۴- |
| اتان | ۱۸۳٫۳- | ۸۸٫۶- |
| پروپان | ۱۸۹٫۷- | ۴۲٫۱- |
| بوتان | ۱۳۸٫۴- | ۰٫۵- |
| پنتان | ۱۲۹٫۷- | ۳۶٫۱ |
| هگزان | ۹۵- | ۶۸٫۹ |
| هپتان | ۹۰٫۶- | ۹۸٫۴ |
| اکتان | ۵۶٫۸- | ۱۲۵٫۷ |
| نونان | ۵۱- | ۱۵۰٫۸ |
| دکان | ۲۹٫۷- | ۱۷۴٫۱ |
هیبریداسیون هیدروکربن
در ابن بخش میخواهیم بدانیم انواع هیبریداسیون در هیدروکربن چیست . آلکانها دارای پیوند یگانه با هیبریداسیون ، آلکنها دارای پیوند دوگانه با هیبریداسیون و آلکینها دارای پیوند سهگانه با هیبریداسیون هستند.
کاربرد هیدروکربن
در این بخش میخواهیم به این سوال پاسخ دهیم که کاربرد هیدروکربن چیست . هیدروکربنها ترکیباتی هستند که در زندگی روزمره انسان و در صنایع بهوفور مورد استفاده قرار میگیرند و نقشی اساسی دارند. در این بخش به برخی از مهمترین کاربردهای این خانواده مهم آلی میپردازیم.
- هیدروکربنها در تولید پلیمرهایی مانند «پلیاتیلن» (Polyethene) و «پلیاستایرن» (Polystyrene) کاربرد دارند.
- این مواد به عنوان روانکننده در روغنها اضافه میشود.
- هیدروکربنهایی مانند پروپان و بوتان به فرم گاز مایع (LPG) کاربرد صنعتی دارند.
- بنزن که یکی از سادهترین هیدروکربنهای آروماتیک است، ماده خام در سنتز بسیاری از ترکیبهای دارویی به شمار میآید.

واکنش های هیدروکربن ها
در این بخش میخواهیم بدانیم انواع واکنش در هیدروکربن چیست . هیدروکربنها ترکیبهای واکنشپذیری نیستند با این حال در چند واکنش شیمیایی شرکت میکنند. در این بخش میخواهیم به برخی از مهمترین واکنشهایی که هیدروکربنها را به خود مشغول میکنند، بپردازیم.
واکنش جانشینی با هالوژن
در این «واکنش جانشینی» (Substitution Reaction) مولکول هالوژن مانند با هیدروکربن وارد واکنش میشود و یک اتم هالوژن جایگزین یک اتم هیدروژن میشود. در کنار محصول این واکنش یک هیدروژن هالید نیز باقی خواهد ماند. نمونهای از این نوع واکنش را در زیر مشاهده میکنید. در برخی موارد حضور نور به پیشبرد این واکنش کمک میکند.
واکنش افزایشی
واکنش بالا در صورتی که با حضور آلکن و آلکین انجام شود، «واکنش افزایشی» (Addition Reaction) نامیده میشود. در این حالت هالوژن با پیوند دوگانه و سهگانه کربن-کربن وارد واکنش میشود و در این پیوندها جا میگیرد. نمونهای از این واکنش را در زیر آوردهایم. محصول واکنش زیر اتیلن دیکلرید نامیده میشود.
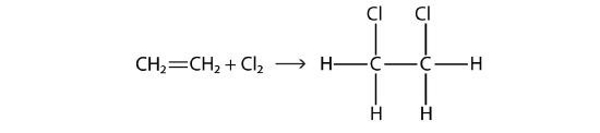
این واکنش در شرایط ملایم صورت میگیرد و در بسیاری موارد بلافاصله بعد از قرارگیری کنار هم رخ میدهد.
واکنش هیدروژناسیون
هیدروژن نیز مانند هالوژن این توانایی را دارد که به پیوندهای چندگانه افزوده شود و «واکنش هیدروژناسیون» (Hydrogenation Reaction) را به وجود بیاورد. هرچند در این واکنش شرایط مانند واکنش افزایشی ملایم نیست و ممکن است به گاز هیدروژن فشار بالا نیاز باشد. همچنین در این واکنش از پلاتین یا پالادیوم به عنوان کاتالیزور استفاده میشود تا به افزایش سرعت واکنش کمک کنند. نمونهای از این واکنش در زیر نشان داده شده است.
این واکنش یکی از مسیرهایی است که میتوان توسط آن آلکانها را از آلکن و آلکین سنتز کرد. همچنین میتوان از ، «کاتالیزور آدام» (Adams Catalyst) با فرمول و «کاتالیزور ویلکینسون» (Wilkinson Catalyst) با فرمول نیز بهره برد.
واکنش سوختن
رایجترین واکنشی که هیدروکربنها انجام میدهند «واکنش سوختن» (Combustion Reaction) است. در این واکنش یک هیدروکربن با وارد واکنش میشود و دو محصول آب و کربن دیاکسید را تولید میکند. این واکنش انرژی بسیار زیادی آزاد میکند و منبع اولیه تامین انرژی در زندگی بشر است. در زیر نمونهای از این واکنش که هیدروکربن آن بنزین با فرمول شیمیایی است را مشاهده میکنید.
مثال واکنش هیدروکربن
تا اینجا واکنشهای هیدروکربنها را مورد بررسی قرار دادیم و میخواهیم تعدادی مثال در این رابطه بیاوریم.
مثال اول
با توجه به اطلاعات داده شده در بخش بالا، واکنشهای زیر را بنویسید.
واکنش افزایشی بین اتن و کلر
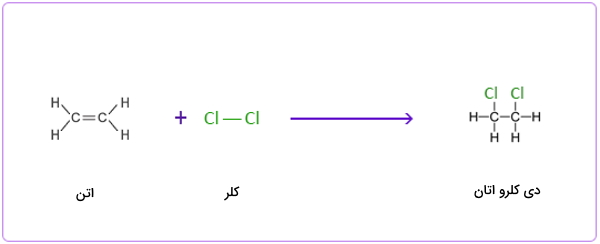
واکنش افزایشی بین اتن و برم
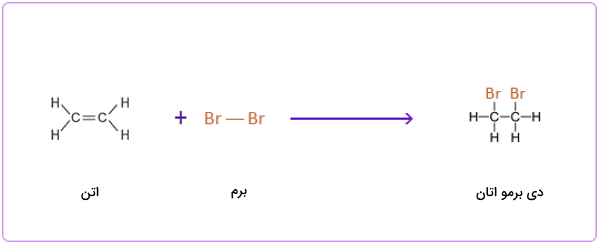
واکنش افزایشی بین اتن و ید
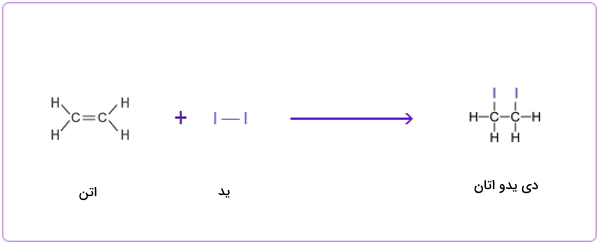
واکنش افزایشی بین پروپن و کلر
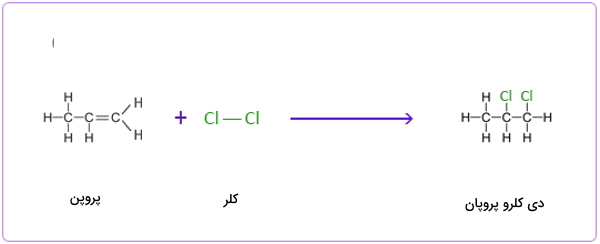
واکنش افزایشی بین پروپن و برم
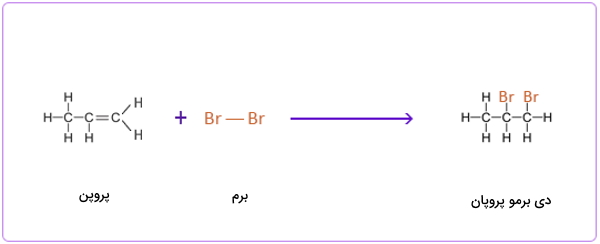
واکنش افزایشی بین پروپن و ید
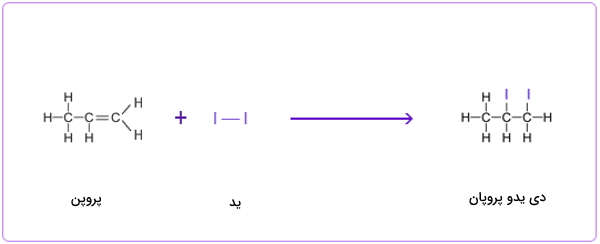
واکنش افزایشی بین بوتن و کلر
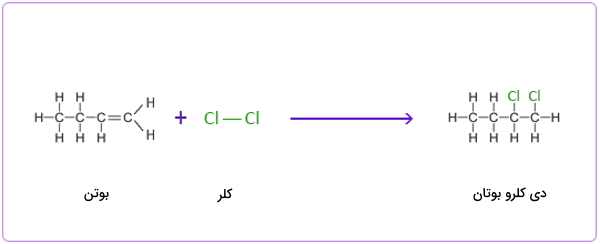
واکنش افزایشی بین بوتن و برم
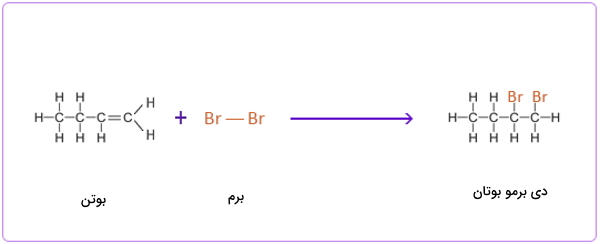
واکنش افزایشی بین بوتن و ید
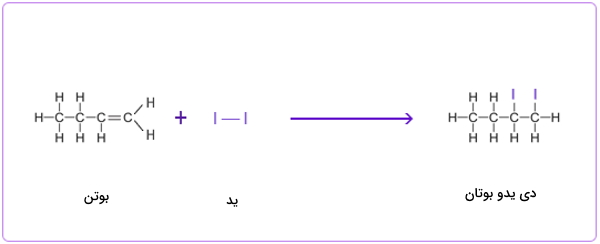
واکنش افزایشی بین پنتن و کلر
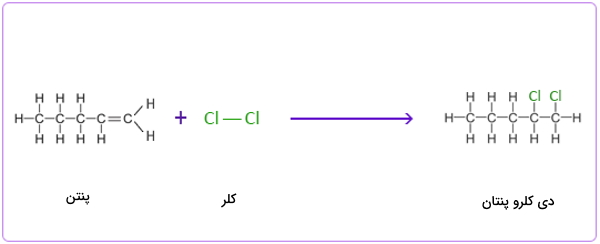
واکنش افزایشی بین پنتن و برم
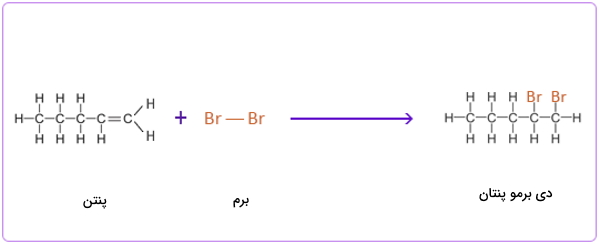
واکنش افزایشی بین پنتن و ید
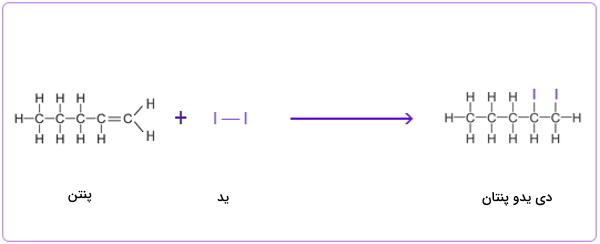
مثال دوم
واکنشی بنویسید که دو واکنشدهنده آن برم و متان باشد.
پاسخ: این واکنش نمونهای از واکنش جانشینی هالوژن بین یک آلکان و هالوژن است و میتوان آن را بهصورت زیر نمایش داد.
مثال سوم
واکنش زیر را که بین هیدروکربن اتان و کلر صورت میگیرد، کامل کنید.
پاسخ: واکنش بالا از نوع جانشینی است و میتوان آن را بهصورت زیر تکمیل کرد.
مثال چهارم
واکنش سوختن هپتان را بنویسید و آن را موازنه کنید.
پاسخ: واکنش سوختن آلکانها با اکسیژن، دیاکسید کربن و آب تولید میکند بنابراین میتوان آن را بهصورت زیر نشان داد.
برای موازنه باید تعداد اتمهای موجود از هر عنصر در دو طرف معادله با یکدیگر برابر باشد. نتیجه بهصورت زیر خواهد بود.
مثال پنجم
محصولی که از واکنش بین برم و پروپن به دست میآید را رسم کنید.
پاسخ: محصول این واکنش بهصورت زیر خواهد بود.
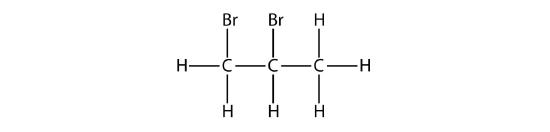
مثال ششم
واکنش بین برم و هیدروکربن متان را بنویسید.
پاسخ: این واکنش را میتوان بهصورت زیر نمایش داد.
واکنش تولید هیدروکربن
در اینجا میخواهیم سراغ این سوال برویم که روشهای تولید هیدروکربن چیست . برای تولید و سنتز هیدروکربنهای میتوان از واکنشهای متعددی استفاده کرد. در این بخش میخواهیم به برخی از مهمترین و کاربردیترین این واکنشها بپردازیم.
واکنش تولید آلکان
آلکانها که هیدروکربنهایی اشباع هستند را میتوان از واکنشهای زیر به دست آورد.
- هیدروژناسیون آلکن و آلکین: در این واکنش هیدروژن به پیوندهای دوگانه و سهگانه افزوده میشود و از این طریق آلکن و آلکین را به آلکان تبدیل میکند. این واکنش در حضور کاتالیزور پیش میرود.
- از آلکیل هالید: آلکیل هالیدها را میتوان در محیطی با حلال پروتیک و استفاده از روی به آلکان تبدیل کرد. در این واکنش تنها آلکانهایی با تعداد اتم کربن فرد به دست میآیند. همچنین استفاده از عوامل کاهنده روی آلکیل هالیدها نیز منجر به تولید آلکان میشود. در این واکنش کاهشی میتوان از «لیتیم آلومینیوم هیدرید» ، «سدیم بوروهیدرید» و «سدیم آمید» استفاده کرد. لیتیم آلومینیوم هیدرید توانایی کاهش هالید نوع ۳ و سدیم بورهیدرید توانایی کاهش هالید نوع ۱ را ندارد.
همچنین میتوان با واکنشهایی از کتون و آلدهید با کمک «واکنش کاهش کلمنسن» (Clemmensen's Reduction) و «واکنش کاهش ولف-کیشنر) (Wolf-Kishner Reduction) و از دکربوکسیلاسون کربوکسیلیک اسید به کمک «الکترولیز کلبه» (Kolbe's Electrolysis) نیز آلکانها را تولید کرد.
قوانین نام گذاری هیدروکربن
در این بخش میخواهیم بدانیم قوانین آیوپاک برای نامگذاری هیدروکربن چیست . گستردگی ترکیبهای هیدروکربنی در دنیای شیمی لزوم یادگیری صحیح روش نامگذاری آنها را مشخص میکند. برای اینکه بتوانیم از این ترکیبات استفاده کنیم، ابتدا باید توانایی تمایز بین آنها را داشته باشیم. قوانین حاکم بر نامگذاری خانوادههای هیدروکربنی تا حدی با یکدیگر شباهت دارند. در این بخش میخواهیم روش نامگذاری خانوادههای مهم هیدروکربنی را با بررسی مثالهایی مورد مطالعه قرار دهیم.
قوانینی که در اینجا برام نامگذاری به کار میبریم، قوانین «آیوپاک» (International Union Of Pure And Applied Chemistry) هستند. در گذشته این ترکیبها با روشهای متفاوتی نامگذاری میشدند اما امروزه روشی که برای تمامی جوامع علمی قابل قبول است، همین روش است. پیش از بررسی این قوانین نیاز است که تعریفی از گروههای آلکیلی، آلکنیلی و آلکینیلی داشته باشیم.
گروه آلکیلی چیست ؟
معنای گروه آلکیل در هیدروکربن چیست ؟ به استخلافی که از آلکان همتای خود یک هیدروژن کمتر داشته باشد، «آلکیل» (Alkyl) میگویند. برای نامگذاری ترکیبهای آلکیلی به جای «ان» در اسم آلکان، «ایل» آورده میشود. به دو آلکان اولیه و همتای آلکیلی آنها در شکل زیر توجه کنید.
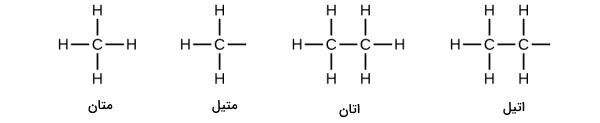
همانطور که در ساختارهای بالا میبینید، آلکیلها از آلکان همتای خود یک هیدروژن کمتر دارند و توانایی این را پیدا میکنند تا بهصورت استخلاف روی یکی از اتمهای کربن زنجیرههای هیدروکربنی به جای هیدروژن قرار بگیرند. پیوندی که در تصاویر بالا خالی گذاشته شده است، محل اتصال این گروه به کربن است. در زیر برخی از مهمترین و پرتکرارترین گروههای آلکیلی که در زنجیرههای هیدروکربنی مشاهده میشوند را آوردهایم. برای نامگذاری هیدروکربنها دانستن نام این استخلافها ضروری است.
| نام آلکنیل | فرمول شیمیایی آلکنیل |
| متیل | |
| اتیل | |
| پروپیل | |
| بوتیل | |
| پنتیل | |
| هگزیل | |
| هپتیل | |
| اکتیل | |
| نونیل |
توجه داشته باشید که آلکیلهایی با تعداد اتم کربن برابر با توجه به محل اتصالشان به زنجیره هیدروکربنی نامگذاری میشوند. گروههای آلکیلی ترکیبهای پایداری نیستند که بهصورت جداگانه وجود داشته باشند و همیشه به مولکول دیگری متصل خواهند بود.
گروه آلکنیل چیست ؟
مفهوم گروه آلکنیل در هیدروکربن چیست ؟ به استخلافی که از آلکن همتای خود یک هیدروژن کمتر داشته باشد، «آلکنیل» (Alkenyl) میگویند. برای نامگذاری ترکیبهای آلکنیلی به جای «ن» در اسم آلکن، «ایل» آورده میشود. به دو گروه آلکنیل کوچک در شکل زیر توجه کنید.
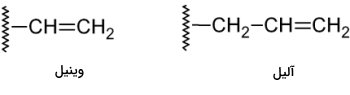
در این تصویر دو عضو کوچک خانواده آلکنیلها را مشاهده میکنید. «وینیل» (Vinyl) نام رایج اتنیل و «آلیل» (Allyl) نام رایج ۲-پروپنیل است. برای اعضای بزرگتر خانواده آلکنیلها از همان روش سیستماتیک نامگذاری که در بالا ذکر کردیم، استفاده میشود. توجه داشته باشید که باقی قواعد در این نامگذاری مانند قوانین حاکم بر نامگذاری آلکنها است.
گروه آلکینیل چیست ؟
منظور از گروه آلکینیل در هیدروکربن چیست ؟ به استخلافی که از آلکین همتای خود یک هیدروژن کمتر داشته باشد، «آلکینیل» (Alkynyl) میگویند. برای نامگذاری ترکیبهای آلکبنیلی به جای «ین» در اسم آلکین، «ایل» آورده میشود. در زیر ساختار عضوی از این خانواده را مشاهده میکنید. این استخلاف ۱-پروپینیل نامیده میشود.
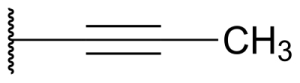
برای نامگذاری دیگر اعضای این خانواده از قواعد حاکم بر نامگذاری آلکینها پیروی میکنیم.
نکته دیگری که در نامگذاری هیدروکربنها باید در نظر داشته باشیم این است که در صورت داشتن استخلافهای مشابه، از تکرار نام آنها پرهیز میکنیم. در این موارد تنها موقعیت آنها را به همراه نامشان و پیشوند نشاندهنده تعداد، میآوریم. این پیشوندهای بهکار رفته برای تعداد را در جدول زیر مشاهده میکنید.
| تعداد استخلاف مشابه | پیشوند |
| ۲ | دی |
| ۳ | تری |
| ۴ | تترا |
| ۵ | پنتا |
| ۶ | هگزا |
| ۷ | هپتا |
| ۸ | اکتا |
| ۹ | نونا |
در این مورد به مثال زیر توجه کنید.
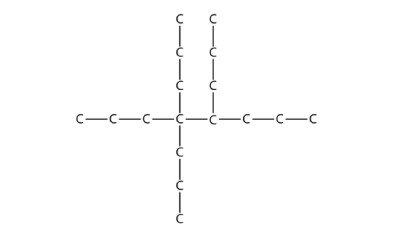
این مولکول دارای سه شاخه آلکیلی هست که همگی یکسان و پروپیلی هستند. برای نامگذاری، مولکول را از سمت چپ عددگذاری میکنیم تا به دو استخلاف آن عدد ۴ نسبت داده شود. زنجیره اصلی دارای ۸ اتم کربن است و میتوان مولکول را بهصورت «۴و۴و۵-تریپروپیل اکتان» نامگذاری کرد. همانطور که مشاهده میکنید نام پروپیل سه بار تکرار نشده است و از تریپروپیل استفاده کردهایم.
نام گذاری آلکان
برای نامگذاری ترکیبهای آلکانی میتوانیم از مجموعه قوانین زیر استفاده کنیم.
- ابتدا طولانیترین زنجیره هیدروکربنی موجود در مولکول را پیدا کنید. سپس نیاز است که به پیشوند نشاندهنده تعداد این کربنها، عبارت «ان» (Ane) را اضافه کنید. در جدول زیر نامی که نشاندهنده تعداد اتمهای کربن از ۱ تا ۲۰ است را مشاهده میکنید. برای سهولت در نامگذاری باید این نامها را به خاطر بسپارید.
| تعداد اتم کربن بلندترین زنجیره | پیشوند |
| ۱ | مت |
| ۲ | ات |
| ۳ | پروپ |
| ۴ | بوت |
| ۵ | پنت |
| ۶ | هگز |
| ۷ | هپت |
| ۸ | اکت |
| ۹ | نون |
| ۱۰ | دک |
| ۱۱ | اندک |
| ۱۲ | دودک |
| ۱۳ | تریدک |
| ۱۴ | تترادک |
| ۱۵ | پنتادک |
| ۱۶ | هگزادک |
| ۱۷ | هپتادک |
| ۱۸ | اکتادک |
| ۱۹ | نونادک |
| ۲۰ | ایکوز |
- گروههایی که بهصورت استخلاف روی زنجیره اصلی وجود دارند را شناسایی کنید. گروه استخلافی به گروه یا اتمی گفته میشود که جایگزین هیدروژن متصل به کربن بلندترین زنجیره شده باشد.
- بعد از شناسایی گروههای استخلافی باید بلندترین زنجیره هیدروکربنی را بهطریقی عددگذاری کنید که به استخلافها کمترین عددهای ممکن تعلق بگیرد.
- در نامگذاری بخش اسکلت هیدروکربن که تعداد اتمهای کربن را نشان میدهد، در انتها آورده میشود. در ابتدا باید نام گروههای استخلافی را به همراه موقعیتی که در زنجیره هیدروکربنی دارند، بیاوریم. برای جدا کردن نام استخلاف از موقعیت آن از خط افقی استفاده میکنیم. اگر روی یک کربن دو استخلاف متفاوت وجود داشته باشد، باید پیش از نام هر دو استخلاف موقعیت آنها را ذکر کنیم. اگر یک استخلاف مشخص روی یک کربن یکسان یا دو کربن متفاوت وجود داشته باشد، ابتدا موقعیتهای آنها و سپس نام استخلاف را به همراه تعداد آن میآوریم. توجه داشته باشید که اولویت آوردن استخلافها بهصورتی است که ترتیب حروف الفبای انگلیسی رعایت شود.
مثال نام گذاری آلکان
در این بخش با استفاده از قوانین ذکر شده در بالا، تعدادی هیدروکربن آلکانی را نامگذاری میکنیم.
مثال اول
میخواهیم برای مولکول زیر با توجه به قوانین گفته شده، نامی بنویسیم.
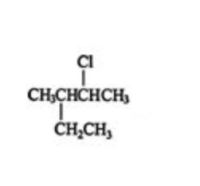
- ابتدا طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص میکنیم. این زنجیره دارای ۵ اتم کربن است. بنابراین نام اسکلت این آلکان پنتان است.
- روی این زنجیره ۵ کربنی، یک اتم کلر و یک گروه متیل وجود دارد و عددگذاری بلندترین زنجیره باید بهصورتی باشد که به این دو استخلاف کوچکترین اعداد ممکن نسبت داده شود. این کار را به شکل زیر انجام میدهیم.
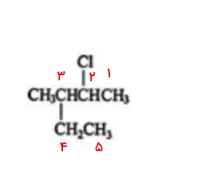
- به این طریق به استخلاف کلر عدد ۲ و به استخلاف متیل عدد ۳ نسبت داده میشود.
- نام استخلافها و موقعیت آنها را با توجه به اولویت آنها در حروف الفبای انگلیسی پیش از نام اسکلت ساختار هیدروکربنی میآوریم. نام این مولکول «۲-کلرو ۳-متیل پنتان» است.
مثال دوم
نام مولکول زیر را با توجه به قوانین آیوپاک مینویسیم.
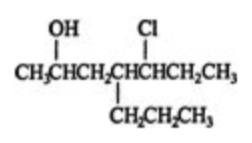
- ابتدا طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص میکنیم. این زنجیره دارای ۷ اتم کربن است و در امتداد خط افقی ادامه دارد. بنابراین نام اسکلت این آلکان هپتان است.
- روی این زنجیره ۷ کربنی، یک اتم کلر، یک گروه پروپیل و یک هیدروکسی وجود دارد و عددگذاری بلندترین زنجیره باید بهصورتی باشد که به این سه استخلاف کوچکترین اعداد ممکن نسبت داده شود. این کار را به شکل زیر انجام میدهیم.
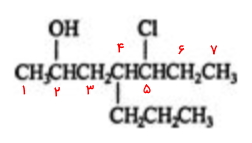
- به این طریق به استخلاف کلر عدد ۵، به هیدروکسی عدد ۲ و به استخلاف پروپیل عدد ۴ نسبت داده میشود.
- نام استخلافها و موقعیت آنها را با توجه به اولویت آنها در حروف الفبای انگلیسی پیش از نام اسکلت ساختار هیدروکربنی میآوریم. اولویت اول مربوط به کلر، اولویت دوم مربوط به هیدروکسی و اولویت آخر برای پروپیل است. بنابراین نام این مولکول «۵-کلرو ۲-هیدروکسی ۴-پروپیل هپتان» است.
مثال سوم
میخواهیم با توجه به قوانین آیوپاک نام آلکان زیر با دو استخلاف مشابه را بنویسیم.
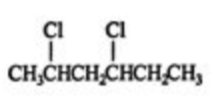
- ابتدا باید طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص کنیم. این زنجیره دارای ۶ اتم کربن است و در امتداد خط افقی ادامه دارد. بنابراین نام اسکلت این آلکان هگزان است که از افزودن «هگز» به پسوند آلکانها، «ان» به وجود میآید.
- روی این زنجیره ۶ کربنی، دو استخلاف کلر وجود دارد و عددگذاری بلندترین زنجیره باید بهصورتی باشد که به این دو استخلاف کوچکترین اعداد ممکن نسبت داده شود. این کار را به شکل زیر انجام میدهیم.
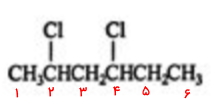
- به این طریق به استخلافهای کلر عدد ۲ و ۴ نسبت داده میشود.
- از آنجا که اولویت دو استخلاف کلر یکسان است، تنها نیاز داریم که موقعیت آنها را پیش از نام اسکلت هیدروکربنی با دیکلرو ذکر کنیم. بنابراین نام این مولکول «۲و۴-دیکلرو هگزان» است.
نام گذاری آلکن
در این بخش میخواهیم بدانیم قوانین حاکم بر نامگذاری آلکن در هیدروکربن چیست . برای نامگذاری آلکنها نیز باید از قوانین آیوپاک استفاده کنیم. اساس این قوانین مانند آلکانها است. در این بخش خلاصهای از مراحل صحیح نامگذاری آلکنها را میآوریم.
- ابتدا بلندترین زنجیره هیدروکربنی را بهصورتی مشخص میکنیم که پیوند دوگانه کربن-کربن را در بر بگیرد. برای نامگذاری این زنجیره از پیشوندی که تعداد آن را نشان میدهد به علاوه «ن» استفاده میکنیم. مثلا برای آلکنی با زنجیره ۴ کربنی، نام بوتن را میآوریم.
- در مرحله بعد زنجیره را به شکلی عددگذاری میکنیم که به اولین کربن درگیر در پیوند دوگانه عدد کوچکتری تعلق بگیرد. توجه داشته باشید که ممکن است در آلکنها بیش از یک پیوند دوگانه وجود داشته باشد.
- موقعیت پیوند دوگانه را با گذاشتن عدد کربن درگیر در پیوند مشخص میکنیم.
- در این مرحله نیاز است که استخلافهای موجود روی کربنهای دیگر را شناسایی کنیم. برای نامگذاری این استخلافها، نام آنها را همراه با موقعیت مشخصشده از قبل، می آوریم.
- آلکنها با توجه به موقعیت قرارگیری استخلافهای خود میتوانند دارای دو ایزومر سیس و ترانس باشند. همانطور که میدانید اتمهای کربن درگیر در پیوند یگانه میتوانند بچرخند اما زمانی که درگیر پیوند دوگانه و سهگانه میشوند، این توانایی خود را از دست میدهند. این پیوندهای صلب امکان وجود ایزومرهای سیس و ترانس را فراهم میکنند. به آلکنهای زیر دقت کنید.
- آلکن ۱-بوتن فاقد ایزومر فضایی است، اما ۲-بوتن میتواند به دو صورت متفاوت وجود داشته باشد. در حالتی که دو متیل متصل به کربنهای درگیر در پیوند دوگانه در یک طرف باشند، ایزومر سیس-۲-بوتن و در حالتی که این دو گروه در دو سمت متفاوت پیوند دوگانه باشند، ایزومر را ترانس-۲-بوتن مینامیم. این دو ایزومر در ویژگیهای فیزیکی مانند نقطه جوش با یکدیگر تفاوت دارند.
- در انتها نام هر استخلاف و موقعیت آن را پیش از نام اسکلت هیدروکربنی و موقعیت پیوند دوگانه میآوریم.
مثال نام گذاری آلکن
در این بخش با استفاده از قوانین ذکر شده در بالا، تعدادی هیدروکربن آلکنی را نامگذاری میکنیم.
مثال اول
در مثال اول سراغ آلکنی ساده با یک پیوند دوگانه و تنها یک استخلاف میرویم.
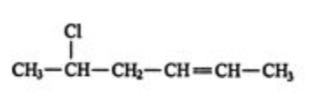
- ابتدا باید طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص کنیم. این زنجیره دارای ۶ اتم کربن است و در امتداد خط افقی ادامه دارد. انتخاب طولانیترین زنجیره در آلکنها باید به شکلی باشد که پیوند دوگانه را در بر بگیرد. بنابراین نام اسکلت این آلکن هگزن است که از افزودن «هگز» به پسوند آلکنها، «ن» به وجود میآید.
- روی این زنجیره ۶ کربنی، یک استخلاف کلر وجود دارد و عددگذاری بلندترین زنجیره باید بهصورتی باشد که به اولین کربن درگیر در پیوند دوگانه کمترین عدد نسبت داده شود، بنابراین عددگذاری این مولکول از راست به چپ انجام میشود.
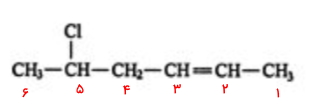
- به این طریق به پیوند دوگانه عدد ۲ و به استخلاف کلر عدد ۵ نسبت داده میشود.
- در پایان، نام استخلاف و موقعیت آن را پیش از نام آلکن با ذکر موقعیت پیوند دوگانه میآوریم. بنابراین نام این مولکول «۵-کلرو ۲-هگزن» است.
مثال دوم
در مثال اول سراغ آلکنی میرویم که میتوان تفاوت ایزومر سیس و ترانس را در آن مشخص کرد.
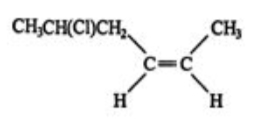
- ابتدا باید طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص کنیم. این زنجیره نیز مانند مثال قبل، دارای ۶ اتم کربن است. انتخاب طولانیترین زنجیره در آلکنها باید به شکلی باشد که پیوند دوگانه را در بر بگیرد. بنابراین نام اسکلت این آلکن هگزن است.
- روی این زنجیره ۶ کربنی، یک استخلاف کلر وجود دارد و عددگذاری بلندترین زنجیره باید بهصورتی باشد که به اولین کربن درگیر در پیوند دوگانه کمترین عدد نسبت داده شود، بنابراین عددگذاری این مولکول از راست به چپ انجام میشود.
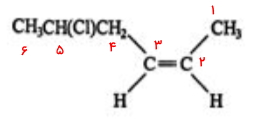
- به این طریق به پیوند دوگانه عدد ۲ و به استخلاف کلر عدد ۵ نسبت داده میشود. توجه داشته باشید که این ایزومر به فرم سیس وجود دارد زیرا دو استخلاف یکسان هیدروژن روی پیوند دوگانه در یک جهت قرار دارند و نیاز است که این در نام آلکن آورده شود.
- در پایان نام استخلاف و موقعیت آن را پیش از نام آلکن با ذکر موقعیت پیوند دوگانه میآوریم. بنابراین نام این مولکول «سیس-۵-کلرو ۲-هگزن» است.
مثال سوم
در این مثال سراغ آلکنی میرویم که دارای دو پیوند دوگانه است. قوانین کلی نامگذاری مانند موراد قبلی خواهد بود.
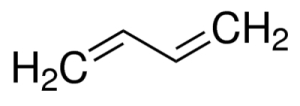
- ابتدا باید طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص کنیم. این زنجیره دارای ۴ اتم کربن است.
- روی این زنجیره ۴ کربنی، استخلافی وجود ندارد و بلندترین زنجیره باید بهصورتی باشد که به اولین کربن درگیر در پیوند دوگانه کمترین عدد نسبت داده شود. با توجه به تصویر زیر چه این عددگذاری از راست به چپ باشد (اعداد قرمز)، چه از چپ به راست (اعداد آبی)، نتیجه یکسان خواهد بود.
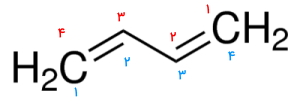
- به این طریق به پیوندهای دوگانه عدد ۱ و ۳ نسبت داده میشود.
- در پایان موقعیت هر پیوند دوگانه را پیش از نام آلکن میآوریم. استفاده از «دی» نشاندهنده این است که در ساختار دو پیوند دوگانه وجود دارد. نام صحیح این هیدروکربن «۱و۳-بتادین» است.
نام گذاری آلکین
در این بخش میخواهیم بدانیم قوانین حاکم بر نامگذاری آلکین در هیدروکربن چیست . نامگذاری آلکینها شباهت زیادی به آلکنها دارد.
- ابتدا بلندترین زنجیره هیدروکربنی را بهصورتی مشخص میکنیم که پیوند سهگانه کربن-کربن را در بر بگیرد. برای نامگذاری این زنجیره از پیشوندی که تعداد آن را نشان میدهد به علاوه «ین» استفاده میکنیم. مثلا برای آلکینی با زنجیره ۴ کربنی، نام بوتین را میآوریم.
- در مرحله بعد زنجیره را به شکلی عددگذاری میکنیم که به اولین کربن درگیر در پیوند سهگانه عدد کوچکتری تعلق بگیرد. توجه داشته باشید که ممکن است در آلکینها بیش از یک پیوند سهگانه وجود داشته باشد.
- موقعیت هر پیوند سهگانه را با گذاشتن عدد کربن درگیر در پیوند مشخص میکنیم.
- در مرحله بعد نیاز است که استخلافهای موجود روی کربنهای دیگر را شناسایی کنیم. برای نامگذاری این استخلافها، نام آنها را همراه با موقعیت مشخصشده از قبل، می آوریم.
مثال نام گذاری آلکین
در این بخش بعد از اینکه دانستیم روشهای نامگذاری آلکین در هیدروکربن چیست ، برای درک بهتر قوانین نامگذاری، تعدادی مثال متنوع را مورد بررسی قرار میدهیم.
مثال اول
در اولین مثال سراغ مولکول ساده زیر با تنها یک پیوند سهگانه میرویم.
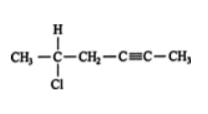
- در ابتدا طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص میکنیم. این زنجیره خطی افقی و دارای ۶ اتم کربن است.
- روی این زنجیره ۶ کربنی، یک استخلاف کلر وجود دارد و بلندترین زنجیره باید بهصورتی باشد که به اولین کربن درگیر در پیوند سهگانه کمترین عدد نسبت داده شود. با توجه به تصویر زیر این عددگذاری از سمت راست به چپ انجام میشود.
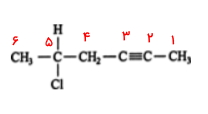
- استخلاف کلر در موقعیت ۵ و پیوند سهگانه در موقعیت ۲ قرار دارد.
- در پایان موقعیت استخلاف و پیوند سهگانه را همراه با نام آنها میآوریم. این مولکول «۵-کلرو ۲-هگزین» نامیده میشود.
مثال دوم
نام مولکول زیر را بر اساس قوانین آیوپاک مینویسیم.
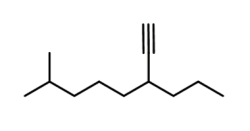
- در ابتدا طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص میکنیم. این زنجیره دارای ۸ اتم کربن است و باید پیوند سهگانه کربن-کربن را در بر بگیرد.
- روی این زنجیره ۸ کربنی، یک استخلاف متیل و یک استخلاف پروپیل وجود دارد. با توجه به تصویر زیر این عددگذاری به شکل زیر خواهد بود.
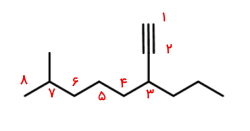
- در این حالت به پیوند سهگانه کربن-کربن موقعیت کمترین عدد، یعنی ۱ تعلق میگیرد. استخلاف پروپیل در موقعیت ۳ و استخلاف متیل در موقعیت ۷ است.
- برای نامگذاری هر استخلاف را همراه با موقعیتش میآوریم. اولویت متیل از پروپیل بیشتر است، بنابراین نام این ساختار «۳-پروپیل ۷-متیل ۱-اکتین» است.
مثال سوم
در مثال پایانی سراغ مولکولی میرویم که کمی پیچیده است.
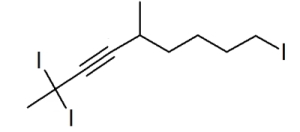
- در ابتدا طولانیترین زنجیره هیدروکربنی موجود در ساختار را مشخص میکنیم. این زنجیره دارای ۹ اتم کربن است که پیوند سهگانه کربن-کربن را در بر میگیرد.
- روی این زنجیره ۹ کربنی، سه استخلاف ید و یک استخلاف متیل وجود دارد. با توجه به تصویر زیر این عدد گذاری از سمت چپ به راست انجام میشود.
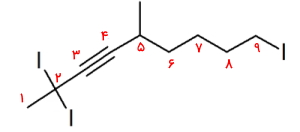
- در این حالت به پیوند سهگانه کربن-کربن موقعیت ۳ تعلق میگیرد. همچنین سه استخلاف ید روی کربنهای شماره ۱ و ۹ قرار دارند.
- برای نامگذاری، هر استخلاف را همراه با موقعیتش میآوریم. اولویت ید بیشتر از متیل است و نام آن بهصورت «۲و۲و۹-ترییدو ۵-متیل ۳-نونین» خواهد بود.
مثال نام گذاری هیدروکربن
مثال اول: هیدروکربنهای زیر را نامگذاری کنید.
مولکول ۱
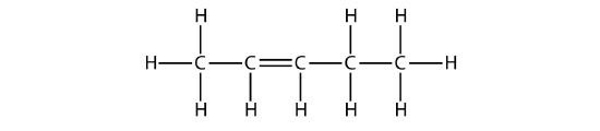
پاسخ: این ساختار مربوط به مولکول پنتن است و باید برای نامگذاری آن، ابتدا مولکول را از جهت درست عددگذاری کنیم. توجه داشته باشید که جهت اعداد نسبت داده شده به هر اتم کربن باید بهصورتی باشد که به اولین کربن دارای پیوند دوگانه، کمترین عدد نسبت داده شود. این را میتوانید در تصویر زیر مشاهده کنید.
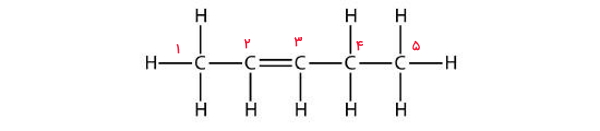
بنابراین نام صحیح این مولکول ۲-پنتن است.
مولکول ۲
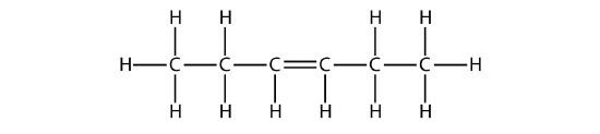
پاسخ: این ساختار مربوط به پنجمین عضو خانواده آلکنها، هگزن است. میدانیم که در آلکنها نیاز به عددگذاری اتمهای کربن است. این عددگذاری باید بهصورتی باشد که اولین اتم کربن درگیر در پیوند دوگانه کمترین عدد را داشته باشد اما در این مورد چه عددگذاری از سمت راست باشد (با رنگ آبی)، چه از سمت چپ (با رنگ قرمز)، پاسخ صحیح و یکسان خواهد بود.
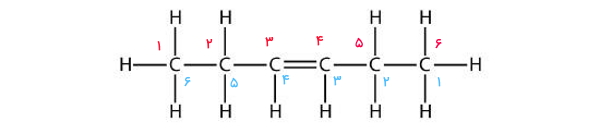
نام این مولکول ۳-هگزن است.
درجه غیر اشباعی چیست ؟
در این بخش میخواهیم بدانیم معنای درجه اشباعی در هیدروکربن چیست . پیشتر در مورد هیدروکربنهای غیراشباع گفتیم. این هیدروکربنها دارای پیوند دوگانه و سهگانه هستند، به گونهای که یک یا دو ظرفیت کووالانسی آنها اشغال نشده است. در این بخش میخواهیم نحوه محاسبه «درجه غیراشباعی» (Degree Of Unsaturation)، که به اختصار با DU نمایش داده میشود را برای این نوع مولکولها بیاموزیم. ابتدا به لیست زیر توجه کنید.
- : تعداد اتمهای کربن
- : تعداد اتمهای نیتروژن
- : تعداد اتمهای هالوژن (فلوئور، کلر، برم و ید)
- : تعداد اتمهای هیدروژن
آلکانها ساختارهایی هستند که حداکثر هیدروژن را دارند. در این ترکیبها تعداد هیدروژنها از رابطه به دست می آید. مثلا برای مولکولی با فرمول شیمیایی تعداد هیدروژنهایی که میتواند وجود داشته باشند برابر با ۸ است.
بنابراین این مولکول با ۴ اتم هیدروژن، برای اشباع شدن نیاز به ۴ اتم هیدروژن دیگر نیز دارد. همانطور که در رابطه بالا دیدیم، تعداد هیدروژنهای مورد نیاز برای اشباع شدن را میتوان بر عدد ۲ تقسیم کرد و درجه اشباعی را به دست آورد. درجه اشباعی برای مولکولی با ۳ اتم کربن و ۴ اتم هیدروژن برابر با ۲ است. از آنجا که هیدروکربنها میتوانند دارای استخلافهای هالوژنی باشند که یک ظرفیت را اشغال میکند، در صورت حضور، باید در نظر گرفته شوند. مثلا مولکول کلرواتان با فرمول شیمیایی ، از مولکول اتان با فرمول شیمیایی یک هیدروژن کمتر دارد.
اگر در مولکولی اتم عنصر نیتروژن وجود داشته باشد، برای اشباع بودن به ۱ عدد اتم هیدروژن بیشتر نیاز است و به همین دلیل در صورت حضور نیتروژن باید آن را به فرمول اضافه کنیم. این گفته را میتوان در مولکول در مقایسه با مولکول مشاهده کرد. حضور اکسیژن تاثیری روی تعداد هیدروژنها ندارد. از این مورد دو مولکول و را با یکدیگر مقایسه کنید.
از این فرمول میتوان برای پیبردن به ساختار صحیح هیدروکربنها با داشتن فرمول مولکولی آنها استفاده کرد. در جدول زیر برخی از حالتهای ممکن برای درجه اشباعیهای متفاوت را مشاهده میکنید.
| درجه اشباعی | تعداد حلقه | تعداد پیوند دوگانه | تعداد پیوند سهگانه |
| ۱ | ۱ | ۰ | ۰ |
| ۱ | ۰ | ۱ | ۰ |
| ۲ | ۲ | ۰ | ۰ |
| ۲ | ۰ | ۲ | ۰ |
| ۲ | ۰ | ۰ | ۱ |
| ۲ | ۱ | ۱ | ۰ |
| ۳ | ۳ | ۰ | ۰ |
| ۳ | ۲ | ۱ | ۰ |
| ۳ | ۱ | ۲ | ۰ |
| ۳ | ۰ | ۱ | ۱ |
| ۳ | ۰ | ۳ | ۰ |
| ۳ | ۱ | ۰ | ۱ |
این نکته را به یاد داشته باشید که درجه اشباعی عددی است که جمع پیوند دوگانه و حلقه یا پیوند سهگانه و حلقه را نشان میدهد. برای مثال اگر مولکولی دارای درجه عدم اشباعی برابر با ۳ باشد، طبق جدول بالا میتواند به سه فرم زیر وجود داشته باشد.
- دارای ۳ حلقه
- دارای ۲ حلقه و ۱ پیوند دوگانه
- دارای ۱ حلقه و ۲ پیوند دوگانه
- دارای ۱ حلقه و ۱ پیوند سهگانه
- دارای ۱ پیوند دوگانه و ۱ پیوند سهگانه
- دارای ۳ پیوند دوگانه
حال که دانستیم معنای درجه اشباعی در هیدروکربن چیست ، میخواهیم تعدادی مثال را مورد بررسی قرار دهیم.
مثال درجه اشباعی
مثال اول
درجه اشباعی بنزن را پیدا کنید.
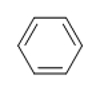
پاسخ: فرمول مولکولی بنزن بهصورت و فاقد نیتروژن یا هالوژن است، بنابراین میتوان اینطور نوشت.
درجه اشباعی بنزن برابر با ۴ است و این در ساختار مولکول نیز قابل مشاهده است. ۱ درجه اشباعی مربوط به حلقه و ۳ تای دیگر هرکدام دلالت بر وجود یک پیوند دوگانه دارند.
توجه داشته باشید که با این فرمول مولکولی و درجه اشباعی میتوان سه ساختار دیگر بهصورت زیر نیز داشت. بنزن پایداری نامعمولی دارد و در دنیای شیمی آلی بهوفور به چشم میآید.
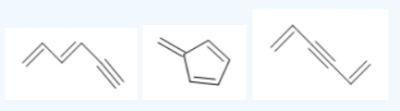
مثال دوم
با توجه به رابطه درجه اشباعی، در مورد اشباع بودن یا نبودن هر یک از مولکولهای زیر اظهار نظر کنید.
مولکول ۱)
در جدول مربوط به اشباعی، برای هر حلقه ۱ درجه اشباعی در نظر گرفتیم. بنابراین این ساختار از آنجا که بهصورت حلقوی حضور دارد، غیراشباع است.
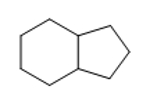
همچنین میتوان از رابطه درجه اشباعی برای اثبات و تایید این پاسخ استفاده کرد. این رابطه بهصورت زیر است.
در این مثال:
- تعداد اتمهای کربن= ۹
- تعداد اتمهای هیدروژن=۱۶
این مولکول دارای دو درجه غیراشباعی است که هر کدام به یکی از حلقههای آن نسبت داده میشود.
مولکول ۲)
این ساختار به دلیل داشتن پیوند دوگانه اشباع نیست، زیرا اتمهای کربن آن، حداکثر ظرفیت خود را با پیوندهای کووالانسی پر نکردهاند.
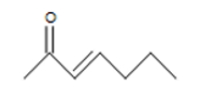
برای به کار بردن رابطه درجه غیراشباعی در این مثال:
- تعداد اتمهای کربن= ۷
- تعداد اتمهای هیدروژن=۱۲
توجه داشته باشید که حضور اتم عنصر اکسیژن تفاوتی در مقادیر موجود در رابطه ایجاد نمیکند. این مولکول دارای دو درجه غیراشباعی است که هر کدام به یکی پیوندهای دوگانه نسبت داده میشود.
مولکول ۳)
این ساختار فاقد حلقه، پیوند دوگانه و سهگانه است. بنابراین میتوان گفت که هیدروکربنی اشباع است.
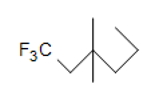
برای اثبات گفته خود مقادیر آن را در رابطه درجه غیراشباعی قرار میدهیم. توجه داشته باشید که باید مقادیر اتمهای هالوژن موجود در ساختار را نیز مدنظر داشته باشیم.
- تعداد اتمهای کربن= ۸
- تعداد اتمهای هیدروژن=۱۵
- تعداد اتمهای فلوئور=۳
همانطور که حدس زده بودیم، درجه غیراشباعی این ساختار ۰ است.
مولکول ۴)
در این مثال میخواهیم با داشتن فرمول شیمیایی یک مولکول در مورد اشباع و غیراشباع بودن آن اظهار نظر کنیم. فرمول شیمیایی این ماده بهصورت است.
- تعداد اتمهای کربن= ۱۰
- تعداد اتمهای هیدروژن= ۶
- تعداد اتمهای نیتروژن= ۴
این مولکول غیراشباع و دارای درجه غیراشباعی برابر با ۱۰ است.
مولکول ۵)
در این مثال سراغ مولکولی با فرمول شیمیایی میرویم. برای پیبردن به اشباع بودن یا نبودن، در حالتی که ساختار در دست نیست، حتما باید از رابطه درجه غیراشباعی کمک بگیریم. در این مثال:
- تعداد اتمهای کربن= ۹
- تعداد اتمهای هیدروژن= ۲۰
با جایگذاری این اعداد در رابطه داریم:
این مولکول اشباع است، زیرا درجه غیراشباعی برای آن برابر با ۰ به دست آمد.
مولکول ۶)
در این مثال سراغ مولکولی با فرمول شیمیایی میرویم. ابتدا تعداد اتمهای موجود از عنصرهایی که در رابطه غیراشباعی نقش دارند را مییابیم.
- تعداد اتمهای کربن= ۷
- تعداد اتمهای هیدروژن= ۸
با جایگذاری این اعداد در رابطه داریم:
درجه غیراشباعی این مولکول غیر صفر و برابر با ۴ است. این ۴ درجه میتواند بهشکل حلقه، پیوند دوگانه یا پیوند سهگانه حضور داشته باشد.
مولکول ۷)
در این مثال سراغ مولکولی با فرمول شیمیایی میرویم. از آنجا که در رابطه درجه غیراشباعی باید هالوژنها را لحاظ کرد، به تعداد اتمهای کلر نیز نیاز داریم.
- تعداد اتمهای کربن= ۵
- تعداد اتمهای هیدروژن= ۷
- تعداد اتمهای کلر= ۱
با جایگذاری این اعداد در رابطه داریم:
این مولکول غیراشباع و دارای درجه غیراشباعی برابر با ۲ است.
مولکول ۸)
در این مثال سراغ مولکولی با فرمول شیمیایی میرویم. تعداد اتمهای اکسیژن تاثیری روی درجه غیراشباعی ندارند و داخل رابطه لحاظ نمیشوند اما نیاز است که تعداد اتمها نیتروژن را در نظر داشته باشیم.
- تعداد اتمهای کربن= ۹
- تعداد اتمهای هیدروژن= ۹
- تعداد اتمهای نیتروژن= ۱
با جایگذاری این اعداد در رابطه داریم:
این مولکول نیز دارای درجه غیراشباعی برابر با ۶ است.
مثال سوم
در مثال بالا، با توجه به درجه غیراشباعی بگویید برای مولکول ۶، ۷ و ۸ چه حالتهایی از غیر اشباعی ممکن است وجود داشته باشد.
پاسخ: همانطور که میدانید، از رابطه درجه غیراشباعی تنها میتوان به جمع تعداد حلقه، پیوند دوگانه و پیوند سهگانه پیبرد و حضور یا عدم حضور یکی با قطعیت بیان نمیشود. به همین دلیل برای هر درجه غیراشباعی حالتهای متفاوتی از ترکیب این سه میتواند وجود داشته باشد.
مولکول ۱)
درجه غیراشباعی این مولکول برابر با ۴ بود، بنابراین میتوان حالتهای زیر را برای آن متصور شد.
- ۴ عدد حلقه
- ۲ عدد پیوند دوگانه + دو عدد حلقه
- ۱ عدد پیوند دوگانه + ۳ عدد حلقه
- ۳ عدد پیوند دوگانه + ۱ عدد حلقه
- ۱ عدد پیوند سهگانه + ۲ عدد حلقه
- ۲ عدد پیوند سهگانه
- ۱ عدد پیوند سهگانه + ۱ عدد پیوند دوگانه + ۱ عدد حلقه
- ۱ عدد پیوند سهگانه + ۲ عدد پیوند دوگانه
مولکول ۲)
درجه غیراشباعی این مولکول برابر با ۲ بود، بنابراین میتوان حالتهای زیر را برای آن متصور شد.
- ۱ عدد پیوند سهگانه
- ۱ عدد حلقه + ۱ عدد پیوند دوگانه
- ۱ عدد حلقه
- ۲ عدد پیوند دوگانه
مولکول ۳)
درجه غیراشباعی این مولکول برابر با ۶ بود، حالتهای ممکن برای این درجه از غیراشباعی بسیار متنوع و زیاد است، در اینجا تنها برخی از آنها را به عنوان نمونه میآوریم.
- ۳ عدد پیوند سهگانه
- ۲ عدد پیوند سهگانه + ۲ عدد پیوند دوگانه
- ۲ عدد پیوند سهگانه + ۱ عدد پیوند دوگانه + ۱ عدد حلقه
- ...
تاثیر هیدروکربنها
از آنجا که این ترکیبها استفاده گستردهای دارند، نیاز است که تاثیرات آنها را مورد بررسی قرار دهیم.
تاثیر محیطزیستی هیدروکربن
آیا میدانید تاثیر محیطزیستی هیدروکربن چیست . استفاده از هیدروکربنها به عنوان منبع اولیه سوخت زندگی انسانها، هزینه سنگینی برای کره زمین دارد. سوختهای فسیلی مانند نفت و گاز طبیعی حاوی کربن و هیدروژن هستند و با سوختن گازهای گلخانهای که عمدتا شامل کربن دیاکسید است، تولید میکنند. آزاد شدن این گاز و وارد شدن آن به هوا باعث ایجاد آلودگی و تغییر الگوی آب و هوایی شوند.
با این حال این تنها آسیب هیدروکربن نیست. فرایند استخراج نفت و گاز نیز به سطح کره زمین و آبهای اطراف از طریق نفود آلاینده، آسیب وارد میکند.
جایگزین هیدروکربن
در مورد تاثیر مخرب هیدروکربن بر محیط زیست گفتیم و میخواهیم بدانیم جایگزین هیدروکربن چیست .افراد فعال در محیط زیست بر لزوم استفاده از منابعی به جای هیدروکربن با آسیب کمتر تاکید میکنند. این منابع تجدیدپذیر شامل باد و آب میشود. آنها بر این باورند که با جایگزینی این منابع نو با هیدروکربن میتوان به حفظ کره زمین کمک بهسزایی کرد.

مثال و حل تمرین
حال که دانستیم هیدروکربن چیست ، میخواهیم برای درک بهتر به بررسی تعدادی مثال و تمرین بپردازیم و درک متن را عمیقتر کنیم.
مثال آشنایی با هیدروکربن
حال که میدانیم هیدروکربن چیست و چگونه نامگذاری میشود، مثالهایی را در همین راستا بررسی خواهیم کرد.
مثال اول
چرا استفاده از نام ۳-بوتن برای ساختار زیر غلط است؟
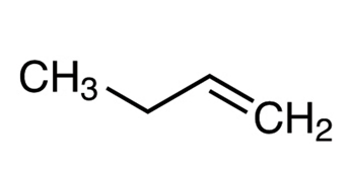
پاسخ: عددگذاری کربنهای آلکن باید بهصورتی باشد که کوچکترین عدد به کربن درگیر در پیوند دوگانه تعلق بگیرد. این را در تصویر زیر مشاهده میکنید.
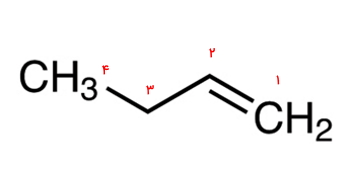
بنابراین نام صحیح این ساختار ۱-بوتن است. اگر آن را ۳-بوتن بنامیم، یعنی عددگذاری بهصورت زیر انجام شده که غلط است.
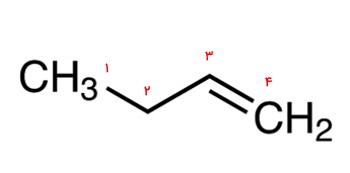
مثال دوم
نام این هیدروکربن چیست ؟
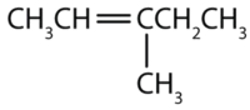
پاسخ: ابتدا باید طولانیترین زنجیره هیدروکربنی موجود در ساختار را پیدا کنیم. در این مورد طولانیترین زنجیره شامل ۵ کربن است و پیوند دوگانه را در بر میگیرد. بنابراین این مولکول یک پنتن است.
در مرحله بعد باید زنجیره را بهطریقی عددگذاری کنیم که به اولین کربن درگیر در پیوند دوگانه کوچکترین عدد ممکن نسبت داده شود. این کار را از چپ به راست انجام میدهیم و به اولین کربن پیوند دوگانه شماره ۲ تعلق میگیرد. بنابراین این مولکول یک ۲-پنتن است. عددگذاری را میتوان بهصورت زیر انجام داد.
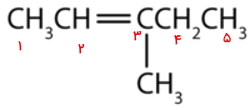
در پایان نیاز است نام استخلافهای روی هر کربن را نیز بیاوریم. روی کربن شماره ۳ یک گروه متیل وجود دارد، بنابراین نام کامل این آلکن ۳-متیل ۲-پنتن است.
مثال سوم
نام این هیدروکربن چیست ؟
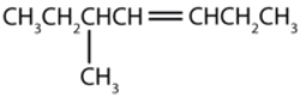
پاسخ: ابتدا باید طولانیترین زنجیره هیدروکربنی موجود در ساختار را پیدا کنیم. در این مورد طولانیترین زنجیره شامل ۷ اتم کربن است و پیوند دوگانه را در بر میگیرد. بنابراین این مولکول یک هپتن است.
در مرحله بعد باید زنجیره را بهطریقی عددگذاری کنیم که به اولین کربن درگیر در پیوند دوگانه کوچکترین عدد ممکن نسبت داده شود. این کار را از راست به چپ انجام میدهیم و به اولین کربن پیوند دوگانه شماره ۳ تعلق میگیرد. بنابراین این مولکول یک ۳-هپتن است. عددگذاری را میتوان بهصورت زیر انجام داد.
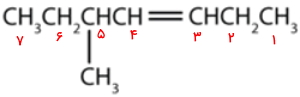
در این مرحله نیاز است تا تمام استخلافهای موجود را پیش از اسم هیدروکربن بیاوریم همانطور که مشاهده میکنید روی کربن شماره ۵ یک متیل وجود دارد، بنابراین نام کامل این هیدروکربن ۵-متیل ۳-هپتن است.
مثال چهارم
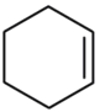
ساختار هیدروکربن هگزن حلقوی را رسم کنید.
پاسخ: پیشوند هگز به معنای ۶ عدد اتم کربن است، بنابراین متوجه میشویم که این مولکول یک حلقه ۶ عضوی است و از آنجا که هگزن یک آلکن است، دارای یک پیوند دوگانه خواهد بود. این ساختار را میتوان بهصورت زیر نمایش داد.
مثال پنجم
نام این هیدروکربن چیست ؟
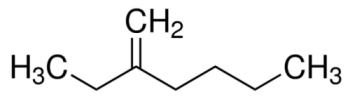
پاسخ: در ابتدا باید بلندترین زنجیره هیدروکربنی این ساختار را پیدا کنیم. بلندترین زنجیرهای که شامل پیوند دوگانه شود، شامل ۶ عدد اتم کربن است. عددگذاری این زنجیره باید بهصورتی باشد که اولین کربن درگیر در پیوند دوگانه کوچکترین عدد ممکن را داشته باشد. این کار را به شکل زیر انجام میدهیم.
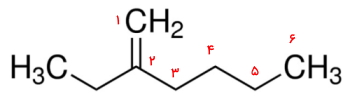
بنابراین این هیدروکربن یک ۱-هگزن است. در این مرحله باید استخلافهای آن را نیز بهصورت پیشوند وارد نام کنیم. همانطور که مشاهده میکنید روی کربن شماره ۲ یک گروه اتیل وجود دارد. نام کامل این ترکیب ۲-اتیل ۱-هگزن است.
مثال ششم
به هیدروکربن زیر توجه کنید و مراحل نامگذاری آن را توضیح دهید.
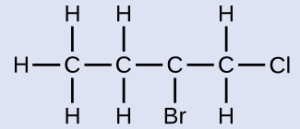
پاسخ: در ابتدا نیاز است که زنجیره را عددگذاری کنیم. این زنجیره هیدروکربنی از ۴ اتم کربن تشکیل شده است و باید از راست به چپ عددگذاری شود تا به استخلافهای آن کوچکترین اعداد ممکن تعلق بگیرد. بنابراین بهصورت زیر میتوان نوشت. توجه داشته باشید که در این حالت به استخلاف کلر و برم بهترتیب عدد ۱ و ۲ تعلق میگیرد اما در صورتی که عددگذاری از سمت دیگر انجام میشود، این اعداد به ۳ و ۴ تغییر پیدا میکرد.
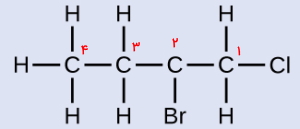
بنابراین دو استخلاف ۱-کلرو و ۲-برمو باید پیش از نام اسکت ساختار، بوتان آورده شوند. اولویت با استخلافی است که در زبان انگلیسی، حرف شروع آن مقدم باشد. بنابراین استخلاف ۲-برمو به ۱-کلرو ارجحیت دارد. نام کامل این مولکول را میتوان بهصورت ۲-برمو ۱-کلرو بوتان نوشت.
مثال هفتم
با توجه به مولکول زیر که متعلق به خانواده آلکانها است، آن را نامگذاری کنید.
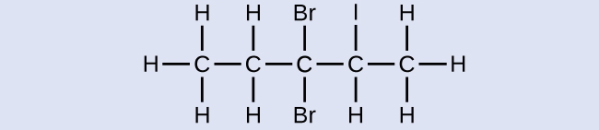
پاسخ: در ابتدا نیاز است که کربنهای آلکان را عددگذاری کنیم. این زنجیره هیدروکربنی از ۵ اتم کربن تشکیل شده است و باید از راست به چپ عددگذاری شود تا به استخلافهای ید و برم آن کوچکترین اعداد ممکن تعلق بگیرد. بنابراین بهصورت زیر میتوان نوشت.
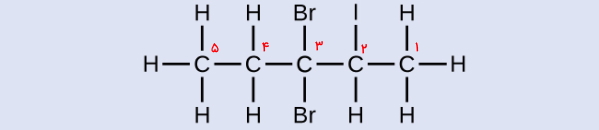
همانطور که مشاهده میکنید روی کربن ۲ یک استخلاف ید و روی اتم کربن شماره ۳ دو استخلاف برم وجود دارد و از آنجا که در حروف الفبای انگلیسی برم قبل از ید قرار دارد، باید آن دو را با رعایت اولویت پیش لز نام اسکلت آلکانی بیاوریم. در نهایت نام مولکول بهصورت ۳و۳-دیبرمو ۱-یدو پنتان خواهد شد.
مثال هشتم
نام ترکیب زیر را طبق قوانین نامگذاری آیوپاک بنویسید.
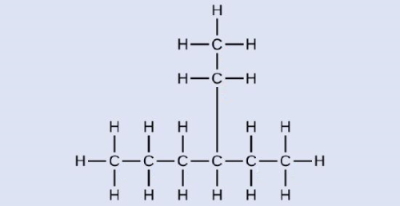
پاسخ: بلندترین زنجیره هیدروکربنی این ساختار شامل ۶ اتم کربن و بهصورت خطی افقی است، بنابراین نام اسکلت این ساختار از آنجا که یک آلکان است، هگزان خواهد بود. برای اینکه تنها استخلاف این هیدروکربن که اتیل است دارای کمترین عدد ممکن باشد، عددگذاری اتمهای کربن را مانند تصویر زیر از سمت راست به چپ مولکول انجام میدهیم. اگر این عددگذاری در جهت برعکس یعنی چپ به راست بود، عدد کربنی که اتیل روی آن قرار دارد، ۴ میشد.
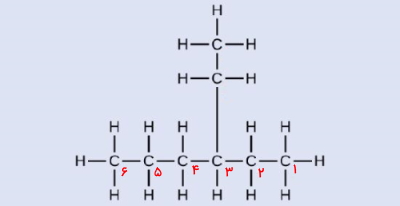
نام کامل این مولکول بهصورت ۳-اتیل هگزان خواهد بود.
مثال نهم
نام ترکیب زیر را طبق قوانین نامگذاری آیوپاک بنویسید.
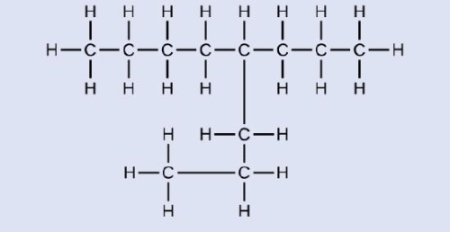
پاسخ: بلندتربن زنجیره هیدروکربنی این مولکول شامل ۸ اتم کربن و بهصورت خطی افقی است، بنابراین نام اسکلت این ساختار از آنجا که یک آلکان است، اکتان خواهد بود.برای اینکه تنها استخلاف این هیدروکربن که گروه پروپیل است دارای کمترین عدد ممکن باشد، عددگذاری اتمهای کربن را مانند تصویر زیر از سمت راست به چپ مولکول انجام میدهیم تا استخلاف روی کربن شماره ۴ قرار بگیرد.
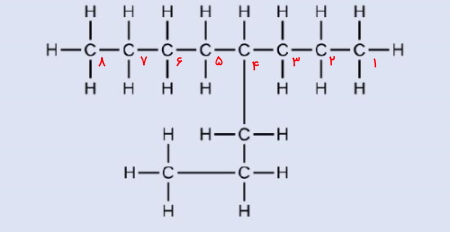
نام کامل این مولکول ۴-پروپیل اکتان است.
مثال دهم
نام ۴ آلکن موجود در تصویر زیر را با توجه به قوانین آیوپاک بنویسید.
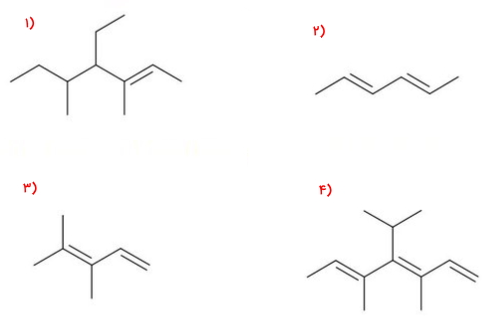
مولکول ۱
بلندترین زنجیره هیدروکربنی در این مولکول شامل ۷ اتم کربن است. عددگذاری زنجیره آلکنها باید بهصورتی باشد که پیوند دوگانه را در بر بگیرد و به آن کمترین عدد ممکن را نسبت دهد. این عددگذاری را به شکل زیر از سمت راست به چپ انجام میدهیم.
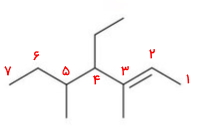
همانطور که مشاهده میکنید کربن درگیر در پیوند دوگانه در موقعیت ۲ قرار دارد. همچنین این آلکن دارای سه استخلاف است. استخلاف اول اتیلی است که روی کربن شماره ۴ قرار دارد. استخلاف دوم و سوم متیلی هستند که یکی روی کربن شماره ۵ و دیگری روی کربن شماره ۳ است. توجه داشته باشید که اولویت با استخلافی است که حرف اول آن در حروف الفبا جلوتر باشد.
باید نام هر استخلاف و موقعیت آن را به نام اسکلت این آلکن اضافه کنیم. نام مولکول «۴-اتیل ۳و۵-دیمتیل ۲-هپتن» است.
مولکول ۲
بلندترین زنجیره هیدروکربنی در این مولکول شامل ۶ اتم کربن است. عددگذاری زنجیره آلکنها باید بهصورتی باشد که پیوند دوگانه را در بر بگیرد و به آن کمترین عدد ممکن را نسبت دهد. این عددگذاری را در مورد مولکول زیر از هر طرفی که انجام دهیم، نتیجه یکسان خواهد بود.
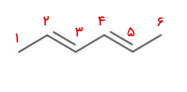
همانطور که مشاهده میکنید کربنهای درگیر در پیوند دوگانه در موقعیت ۲ و ۴ قرار دارند. استخلاف دیگری در این ساختار وجود ندارد. بنابراین میتوان نام آن را بهصورت «۲و۴-هگزادین» نوشت.
مولکول ۳
بلندترین زنجیره هیدروکربنی در این مولکول شامل ۵ اتم کربن است. عددگذاری زنجیره آلکنها باید بهصورتی باشد که پیوند دوگانه را در بر بگیرد و به آن کمترین عدد ممکن را نسبت دهد. این عددگذاری اگر از راست به چپ باشد، موقعیت ۱ و ۳ و اگر از سمت چپ به راست باشد موقعیت ۲ و ۴ به پیوند دوگانه تعلق میگیرد بنابراین بهصورت زیر عمل میکنیم.
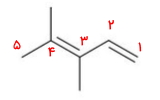
این آلکن دارای دو استخلاف متیلی در موقعیت ۳ و ۴ است. بنابراین نام آن بهصورت «۳و۴-دیمتیل ۱و۳-پنتادین» است.
مولکول ۴
بلندترین زنجیره هیدروکربنی در این مولکول شامل ۷ اتم کربن است. عددگذاری زنجیره آلکنها باید بهصورتی باشد که پیوند دوگانه را در بر بگیرد و به آن کمترین عدد ممکن را نسبت دهد. این عددگذاری در مورد مولکول زیر از راست به چپ خواهد بود. در این حالت پیوندهای دوگانه در موقعیت ۱ و ۳ و ۵ قرار میگیرند. اگر عددگذاری در خلاف این جهت انجام دهیم این موقعیتها دارای اعداد بالاتری هستند و غلط است.
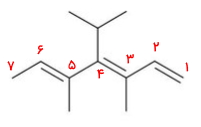
استخلافهای این مولکول دو عدد متیل در موقعیت ۳ و ۵ و یک ایزوپروپیل در موقعیت ۴ هستند که باید در ابتدای نام آلکن آورده شوند. همچنین استخلاف ایزوپروپیل اولویت بیشتری نسبت به متیل دارد. بنابراین نام این مولکول «۴-ایزوپروپیل ۳و۵-دیمتیل ۱و۳و۵-هپتاترین» است.
مثال یازدهم
به ۴ مولکول زیر دقت کنید و نام آنها را با توجه قوانین آیوپاک برای نامگذاری آلکینها بنویسید.
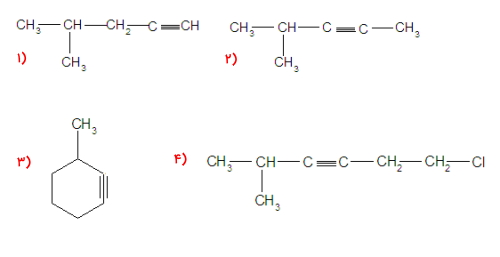
مولکول ۱
بلندترین زنجیره هیدروکربنی در این مولکول شامل ۵ اتم کربن است. عددگذاری زنجیره آلکینها باید بهصورتی باشد که حتما پیوند سهگانه را در بر بگیرد و به آن کمترین عدد ممکن را نسبت دهد. این عددگذاری در مورد مولکول زیر از راست به چپ خواهد بود. در این حالت پیوند سهگانه در موقعیت ۱ قرار میگیرد.
این مولکول دارای یک عدد استخلاف متیل در موقعیت ۴ است که باید در ابتدای نام آلکین آورده شود. بنابراین نام این مولکول «۴-متیل ۱-پنتین» است.
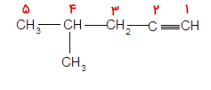
مولکول ۲
این مولکول دقیقا مانند مثال قبل است، با این تفاوت که موقعیت پیوند سهگانه در آن تغییر کرده است. عددگذاری آن نیز مانند مثال اول است.
بنابراین نام این مولکول «۴-متیل ۲-پنتین» است.
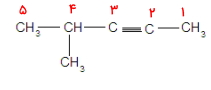
مولکول ۳
این مثال کمی متفاوت است. در این مثال یک آلکین حلقوی وجود دارد. برای نامگذاری آن مانند مثالهای قبلی، بلندترین زنجیره را انتخاب میکنیم و کوچکترین عدد را به پیوند سهگانه نسبت میدهیم. این گفته را میتوانید در تصویر زیر مشاهده کنید.
این مولکول حلقوی دارای یک عدد استخلاف متیل در موقعیت ۳ است که باید در ابتدای نام آلکین آورده شود. بنابراین نام این مولکول «۳-متیل ۱-سیکلوهگزین» است.
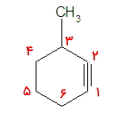
مولکول ۴
بلندترین زنجیره هیدروکربنی در این مولکول شامل ۶ اتم کربن است. عددگذاری زنجیره آلکینها باید بهصورتی باشد که حتما پیوند سهگانه را در بر بگیرد و به آن کمترین عدد ممکن را نسبت دهد. این عددگذاری را در مورد مولکول زیر از راست به چپ خواهد بود. در این حالت پیوند سهگانه در موقعیت ۳ قرار میگیرد.
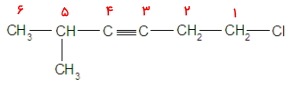
این مولکول دارای یک عدد استخلاف متیل در موقعیت ۵ و یک استخلاف کلر در موقعیت ۱ است که باید در ابتدای نام آلکین آورده شوند. توجه داشته باشید که اولویت استخلاف کلر بالاتر از استخلاف متیل است. بنابراین نام این مولکول «۱-کلرو ۵-متیل ۳-هگزین» است.
مثال دوازدهم
آلکنهای حلقوی زیر را با توجه به قوانین آیوپاک نامگذاری کنید.
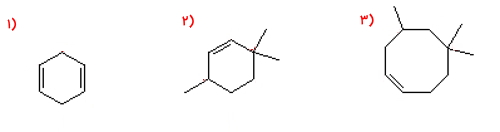
مولکول ۱
عددگذاری حلقه آلکنها باید بهصورتی باشد که به پیوند دوگانه کمترین عدد ممکن را نسبت دهد. این عددگذاری را به شکل زیر از سمت راست به چپ انجام میدهیم. از آنجا که پیوندهای دوگانه موجود در این حلقه متقارن هستند، اگر نامگذاری از سمت دیگر نیز انجام میشد، نتیجه یکسان بود.
همانطور که مشاهده میکنید کربنهای درگیر در پیوند دوگانه در موقعیت ۱ و ۴ قرار دارند و این حلقه فاقد استخلاف است، بنابراین میتوانیم نام آن را بهصورت «۱و۴-سیکلوهگزدین» بنویسیم.
مولکول ۲
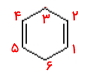
عددگذاری آلکنهای حلقوی باید بهصورتی باشد که به پیوند دوگانه کمترین عدد ممکن را نسبت دهد. این عددگذاری را در مورد مولکول زیر از پیوند دوگانه شروع میکنیم و ساعتگرد ادامه میدهیم. در این حالت پیوند دوگانه در موقعیت ۱ قرار میگیرد..
استخلافهای این مولکول ۳ عدد متیل است که در موقعیت ۳ و ۵ هستند که باید در ابتدای نام آلکن همراه با موقعیت خود آورده شوند. بنابراین نام این مولکول «۳و۳و۶-تریمتیل سیکلوهگزن» است. اگر پیوند دوگانه ۱ عدد باشد و به آن عدد ۱ نسبت داده شود، میتوان در نام مولکول از آن صرف نظر کرد.
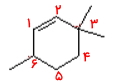
مولکول ۳
عددگذاری آلکنهای حلقوی باید بهصورتی باشد که به پیوند دوگانه کمترین عدد ممکن نسبت داده شود، همچنین ترجیح با این است که مجموع استخلافها نیز روی کربنهایی با شمارههای پایینتر قرار داشته باشند. این عددگذاری را در مورد مولکول زیر از پیوند دوگانه شروع میکنیم و ساعتگرد ادامه میدهیم. در این حالت پیوند دوگانه در موقعیت ۱ قرار میگیرد.
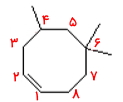
استخلافهای این مولکول ۳ عدد متیل است که در موقعیت ۴ و ۶ هستند و باید در ابتدای نام آلکن همراه با موقعیت خود آورده شوند. بنابراین نام این مولکول «۴و۶و۶-تریمتیل سیکلواکتن» است. در این نمونه نیز مانند بالا، از آوردن موقعیت ۱ پیش از سیکلواکتن خودداری کردیم.
مثال سیزدهم
در این مثال سعی داریم با در دست داشتن نام یک مولکول ساختار آن را رسم کنیم.
مولکول ۱
ساختار هیدروکربنی با نام «۲و۳و۴-تریمتیل پنتان» را رسم کنید.
پاسخ: در مرحله اول بهتر است برای راحتی کار اسکلت اصلی هیدروکربن را رسم کنیم. از آنجا که در انتهای نام این هیدروکربن پنتان داریم، باید زنجیرهای حاوی ۵ اتم کربن رسم کنیم.
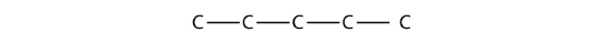
سپس باید استخلافها را روی اسکلت اصلی وارد کنیم. با توجه به نام مولکول، روی کربن دوم، سوم و چهارم گروههای متیلی حضور دارند. با قرار دادن این سه متیل روی ساختار، کار تمام میشود.
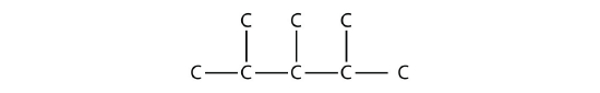
توجه داشته باشید که وقتی هیدروکربنی را به این شکل نشان میدهیم یعنی تمام ظرفیتهای خالی اتمهای کربن توسط هیدروژن اشغال شده است و ما برای سهولت کار و جلوگیری از ایجاد تراکم، آنها را رسم نمیکنیم.
مولکول ۲
ساختار هیدروکربنی با نام «۳-اتیل ۶و۷-دیمتیل اکتن» را رسم کنید.
پاسخ: این ساختار یک آلکن است. در مرحله اول بهتر است برای راحتی کار اسکلت اصلی هیدروکربن را رسم کنیم. از آنجا که در انتهای نام این هیدروکربن ۲-اکتن داریم، باید زنجیره حاوی ۸ اتم کربن باشد و بین کربن دوم و سوم یک پیوند دوگانه قرار میدهیم.
سپس باید استخلافها را روی اسکلت اصلی وارد کنیم. با توجه به نام مولکول، روی کربن سوم یک استخلاف متیل و روی کربن ششم و هفتم گروههای متیلی حضور دارند. با قرار دادن این سه استخلاف روی ساختار، کار تمام میشود.
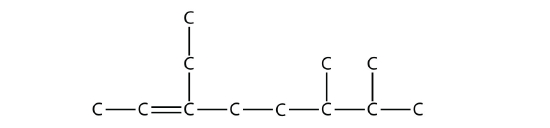
اگر این زنجیره را از چپ به راست عددگذاری کنیم، متوجه میشویم که پیوند دوگانه و استخلافها در موقعیت خواستهشده هستند و رسم شکل صحیح انجام گرفته است.
مولکول ۳
ساختار هیدروکربنی با نام «۱و۱و۲و۲-تتراکلرو اتیلن» را رسم کنید.
پاسخ: این ساختار یک آلکن است. در مرحله اول بهتر است برای راحتی کار اسکلت اصلی هیدروکربن را رسم کنیم که تنها حاوی ۲ اتم کربن است که توسط پیوندی دوگانه به هم متصل هستند.
سپس باید استخلافها را روی اسکلت اصلی وارد کنیم. با توجه به نام مولکول، روی هر اتم کربن ۲ عدد اتم کلر حضور دارد. با قرار دادن این چهار استخلاف روی ساختار، کار تمام میشود.
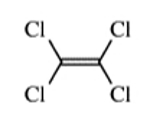
توجه داشته باشید که اگر نوع این استخلافها متفاوت بود، ساختار میتوانست به دو نوع سیس و ترانس وجود داشته باشد. اما در اینجا به دلیل یکسان بودن ۴ استخلاف چنین چیزی مطرح نیست. در مثال بعد نمونهای از آلکنهای سیس و ترانس را میتوانید مشاهده کنید.
مولکول ۴
ساختار دو هیدروکربن با نامهای «سیس-۱و۲-دیکلرو اتن» و «ترانس-۱و۲-دیکلرو اتن» را رسم کنید.
پاسخ: در این مثال میخواهیم ساختار یک آلکن را هم بهصورت سیس هم ترانس رسم کنیم. در مرحله اول بهتر است برای راحتی کار اسکلت اصلی هیدروکربن را رسم کنیم که تنها حاوی ۲ اتم کربن است که توسط پیوندی دوگانه به هم متصل هستند.
سپس باید استخلافها را روی اسکلت اصلی وارد کنیم. با توجه به نام مولکول، روی هر اتم کربن ۱ عدد اتم کلر و ۱ عدد اتم هیدروژن حضور دارد. با قرار دادن این چهار استخلاف روی ساختار، کار تمام میشود.

این استخلافها اگر هر دو در یک طرف پیوند دوگانه باشند، ساختار سیس است (مانند تصویر سمت چپ) و اگر دو استخلاف کلر در دو طرف پیوند دوگانه قرار داشته باشند، آلکن از نوع ترانس است. (مانند تصویر سمت راست)
مولکول ۵
ساختار دو هیدروکربن حلقوی با نامهای «سیس-۱و۲-دیکلرو سیکلوهگزان» و «ترانس-۱و۲-دیکلرو سیکلوهگزان» را رسم کنید.
پاسخ: این دو نام مربوط به آلکانهای حلقوی هستند. در مرحله اول حلقهای متشکل از ۶ اتم کربن را رسم میکنیم. از آنجا که ساختار مربوط آلکان است، فاقد پیوند دوگانه و سهگانه خواهد بود.
سپس باید استخلافها را روی اسکلت اصلی وارد کنیم. با توجه به نام مولکول، روی دو اتم کربن مجاور هم، دو استخلاف کلر وجود دارد.

این دو استخلاف اگر در دو سمت متفاوت حضور داشته باشند، ترانس و اگر در یک سمت قرار داشته باشند، سیس نامیده میشوند. در دو ساختار بالا گوه نشاندهنده استخلاف بیرون از صفحه و نزدیک به بیننده و خطچین نشاندهنده استخلاف پشت صفحه و دور از بیننده است. بنابراین شکل سمت راست مربوط به «ترانس-۱و۲-دیکلرو سیکلوهگزان» و شکل سمت چپ مربوط به «سیس-۱و۲-دیکلرو سیکلوهگزان» است.
مثال چهاردهم
در تصویر زیر ۵ ایزومر ساختاری هگزان را مشاهده میکنید. با توجه به قوانین آیوپاک برای هر کدام نامی بنویسید.
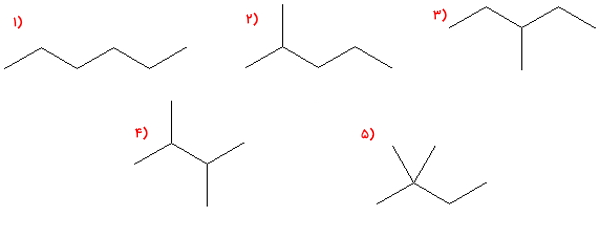
مولکول ۱
بلندترین زنجیره هیدروکربنی در این آلکان شامل ۶ اتم کربن است. عددگذاری را در مورد مولکول زیر از هر طرفی که انجام بدهیم تفاوتی ایجاد نمیشود زیرا هیچ استخلافی رو اتمهای کربن آن وجود ندارد.
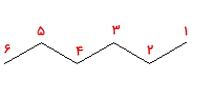
بنابراین نام این مولکول «هگزان» است.
مولکول ۲
بلندترین زنجیره هیدروکربنی در این آلکان شامل ۵ اتم کربن است. برای عددگذاری اتمهای کربن آن از سمت چپ شروع میکنیم تا به تنها استخلاف آن عدد ۲ تعلق بگیرد. اگر عددگذاری را از سمت دیگر شروع میکردیم به استخلاف متیل عدد ۴ نسبت داده میشد و صحیح نبود. این را در تصویر زیر میتوانید مشاهده کنید.
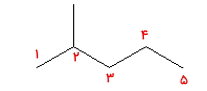
همانطور که گفتیم این مولکول دارای یک عدد استخلاف متیل در موقعیت ۲ است که باید نام آن را همراه با موقعیت قبل از نام زنجیره اصلی بیاوریم. بنابراین نام این مولکول «۲-متیل پنتان» است.
مولکول ۳
بلندترین زنجیره هیدروکربنی در این آلکان نیز شامل ۵ اتم کربن است. عددگذاری اتمهای کربن آن از هر طرفی که انجام بشود تفاوتی ایجاد نمیشود و به تنها استخلاف آن عدد ۳ تعلق میگیرد. این را در تصویر زیر میتوانید مشاهده کنید.
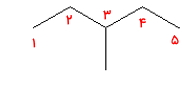
این مولکول دارای یک عدد استخلاف متیل در موقعیت ۳ است که باید نام آن را همراه با موقعیت قبل از نام زنجیره اصلی بیاوریم. بنابراین نام این مولکول «۳-متیل پنتان» است.
مولکول ۴
بلندترین زنجیره هیدروکربنی در این آلکان شامل ۴ اتم کربن است. برای عددگذاری اتمهای کربن از سمت چپ شروع کردهایم، اما توجه داشته باشید که اگر از سمت راست انجام شود نیز صحیح است زیرا در هر دو حالت به دو استخلاف متیل اعداد ۲ و ۳ تعلق میگیرد. این را در تصویر زیر میتوانید مشاهده کنید.
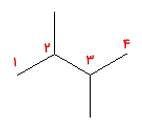
همانطور که میدانید نیازی به تکرار استخلافهای مشابه در نامگذاری نیست. تنها نیاز است موقعیت آنها و تعداد را بیاوریم. بنابراین نام این مولکول «۲و۳-دیمتیل بوتان» است.
مولکول ۵
بلندترین زنجیره هیدروکربنی در این آلکان نیز شامل ۴ اتم کربن است. برای عددگذاری اتمهای کربن آن از سمت چپ شروع میکنیم تا به دو استخلاف آن عدد ۲ تعلق بگیرد. اگر عددگذاری را از سمت دیگر شروع میکردیم به استخلافهای متیل عدد ۳ نسبت داده میشد و صحیح نبود. این را در تصویر زیر میتوانید مشاهده کنید.
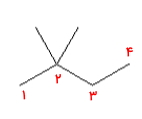
بنابراین نام این مولکول «۲و۲-دیمتیل بوتان» است.
مثال پانزدهم
نحوه نامگذاری هیدروکربن حلقوی زیر را با توجه به قوانین آیوپاک توضیح دهید.
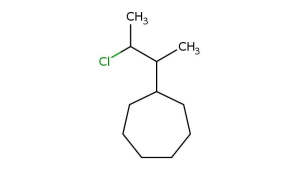
پاسخ: این حلقه دارای استخلافی آلکانی است که روی خود استخلافی کلری دارد. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به استخلاف آن عدد ۱ برسد. جهت عددگذاری حلقه چه ساعتگرد باشد چه پادساعتگرد تفاوتی ایجاد نمیشود. همچنین نیاز است که استخلاف بوتیل را نیز عددگذاری کنیم. (با رنگ آبی نشان داده شده است) این نامگذاری از کربنی شروع میشود که طولانیترین زنجیره را در بر بگیرد. در این حالت به کلر عدد ۳ تعلق میگیرد.
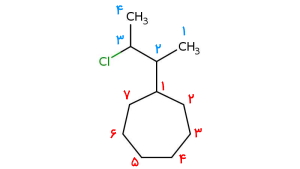
وقتی از ۱-(۳-کلرو۲-بوتیل) استفاده میکنیم یعنی روی کربن شماره ۱ استخلافی بوتیلی داریم که از کربن شماره ۲ خود به حلقه وصل است و روی کربن شماره ۳ خود یک استخلاف کلر دارد. نام این آلکان حلقوی «۱-(۳-کلرو۲-بوتیل) سیکلوهپتان» است.
مثال شانزدهم
نحوه نامگذاری هیدروکربنی که دارای هر دو پیوند دوگانه و سهگانه است را توضیح دهید.
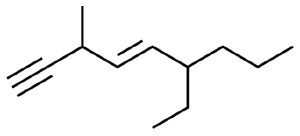
پاسخ: این زنجیره همزمان هم پیوند دوگانه هم پیوند سهگانه دارد. برای نامگذاری آن ابتدا باید بلندترین زنجیره هیدروکربنی را عددگذاری کنیم. این کار را از سمتی انجام میدهیم که به این پیوندها نزدیکتر باشد. همانطور که مشاهده میکنید در تصویر زیر عددگذاری از چپ به راست انجام شده است و به پیوند دوگانه عدد ۴ و پیوند سهگانه عدد ۱ رسیده است.
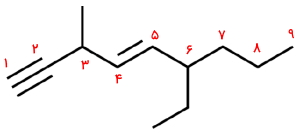
همچنین دو استخلاف این زنجیره ۹ اتمی، یک متیل روی کربن شماره ۳ و یکی اتیل روی کربن شماره ۶ است. هر دو آنها را باید همراه با موقعیتشان پیش از اسم زنجیره و با رعایت اولویت اتیل بر متیل بیاوریم. بنابراین نام این هیدروکربن خطی «۶-اتیل ۳-متیل نون-۴-ن-۱-این» است.
مثال هفدهم
نحوه نامگذاری هیدروکربن زیر را توضیح دهید.
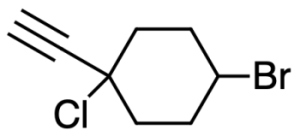
پاسخ: این حلقه دارای یک استخلاف آلکینی، یک استخلاف برمی و یک استخلاف کلری است. ابتدا اتمهای کربن داخل حلقه را عددگذاری میکنیم. این کار را به شکلی انجام میدهیم که به استخلافها کوچکترین عدد ممکن برسد. جهت عددگذاری حلقه چه ساعتگرد باشد چه پادساعتگرد تفاوتی ایجاد نمیشود.
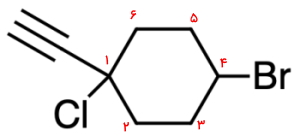
نام این آلکان حلقوی «۴-برمو ۱-کلرو ۱-اتینیل سیکلوهگزان» است.
مثال هجدهم
در تصویر زیر ۴ هیدروکربن آروماتیک را مشاهده میکنید. با توجه به قوانین آیوپاک، نحوه نامگذاری آنها را توضیح دهید.
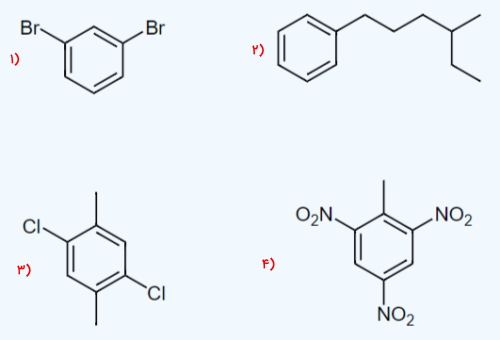
مولکول ۱
در این مثال میخواهیم با نحوه نامگذاری هیدروکربنهای آروماتیک آشنا شویم که شباهت بسیار زیادی به مثالهایی به تا اینجا بررسی شده، دارد.
همانطور که میدانید عددگذاری را بهصورت انجام میدهیم که به استخلافها عددهای کوچکتری تعلق بگیرد. این کار را به شکل زیر انجام میدهیم.
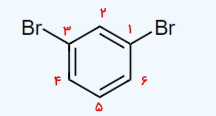
به دو استخلاف برم روی بنزن اعداد ۱ و ۳ نسبت داده شده است، بنابراین نام این مولکول «۱و۳-دیبرمو بنزن» است.
مولکول ۲
در حالتی که حلقه بنزن، خود بهصورت استخلاف روی زنجیره هیدروکربنی دیگری باشد، آن را فنیل مینامیم. بلندترین زنجیره هیدروکربنی در این مثال شامل ۶ اتم کربن است. اولویت با استخلاف فنیل است و نباید ابتدا متیل را بیاوریم. هر استخلاف را همراه با موقعیت پیش از اسم اسکلت اصلی هیدروکربنی میآوریم.
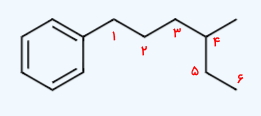
نام این مولکول «۱-فنیل ۴-متیل هگزان» است.
مولکول ۳
این مولکول دارای ۲ استخلاف کلر و ۲ استخلاف متیل است. اگر عددگذاری آن را بهصورت زیر انجام دهیم به کلرها عدد ۱ و ۴ و به متیلها اعداد ۲ و ۵ تعلق میگیرد. از آنجا که اولویت با کلر است، عددگذاری را از یکی از آنها شروع میکنیم و ساعتگرد ادامه میدهیم.
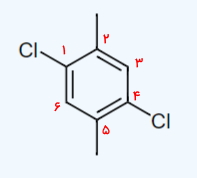
نام این مولکول «۱و۴-دیکلرو ۲و۵-دیمتیل بنزن» است.
مولکول ۴
این مولکول دارای ۳ استخلاف نیترو و ۱ استخلاف متیل است. اگر عددگذاری آن را بهصورت زیر انجام دهیم به نیتروها عدد ۱، ۳ و ۵ و به متیل عدد ۲ تعلق میگیرد..
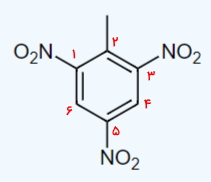
نام این مولکول «۲-متیل ۱و۳و۵ترینیترو بنزن» است.
تمرین آشنایی با هیدروکربن
در بخش قبلی بعد از اینکه دانستیم هیدروکربن چیست به بررسی مثالهای متعددی پرداختیم. در این بخش میخواهیم با تمرینهایی چندگزینهای درک مفهوم این مطلب را بالا ببریم.
تمرین یکم
تمرین و آزمون
تمرین دوم
تمرین و آزمون
تمرین سوم
تمرین و آزمون
تمرین چهارم
تمرین و آزمون
تمرین پنجم
تمرین و آزمون
تمرین ششم
تمرین و آزمون
تمرین هفتم
تمرین و آزمون
تمرین هشتم
تمرین و آزمون
تمرین نهم
تمرین و آزمون
تمرین دهم
تمرین و آزمون
تمرین یازدهم
تمرین و آزمون
تمرین دوازدهم
تمرین و آزمون
تمرین سیزدهم
تمرین و آزمون
تمرین چهاردهم
تمرین و آزمون
تمرین پانزدهم
تمرین و آزمون
تمرین شانزدهم
تمرین و آزمون
تمرین هفدهم
تمرین و آزمون
تمرین هجدهم
تمرین و آزمون
تمرین نوزدهم
تمرین و آزمون
تمرین بیستم
تمرین و آزمون
تمرین بیست و یکم
تمرین و آزمون
تمرین بیست و دوم
تمرین و آزمون
تمرین بیست و سوم
تمرین و آزمون
تمرین بیست و چهارم
تمرین و آزمون
تمرین بیست و پنجم
تمرین و آزمون
تمرین بیست و ششم
تمرین و آزمون
تمرین بیست و هفتم
تمرین و آزمون
تمرین بیست و هشتم
تمرین و آزمون
تمرین بیست و نهم
تمرین و آزمون
تمرین سیام
تمرین و آزمون
تمرین سی و یکم
تمرین و آزمون
تمرین سی و دوم
تمرین و آزمون
تمرین سی و سوم
تمرین و آزمون
تمرین سی و چهارم
تمرین و آزمون
تمرین سی و پنجم
تمرین و آزمون
تمرین سی و ششم
تمرین و آزمون
تمرین سی و هفتم
تمرین و آزمون
تمرین سی و هشتم
تمرین و آزمون
تمرین سی و نهم
تمرین و آزمون
تمرین چهلم
تمرین و آزمون
تمرین چهل و یکم
تمرین و آزمون
تمرین چهل و دوم
تمرین و آزمون
تمرین چهل و سوم
تمرین و آزمون
تمرین چهل و چهارم
تمرین و آزمون
تمرین چهل و ششم
تمرین و آزمون
تمرین چهل و هفتم
تمرین و آزمون
تمرین چهل و هشتم
تمرین و آزمون
تمرین چهل و نهم
تمرین و آزمون
تمرین پنجاهم
تمرین و آزمون
تمرین پنجاه و یکم
تمرین و آزمون
تمرین پنجاه و دوم
تمرین و آزمون
تمرین پنجاه و سوم
تمرین و آزمون
تمرین پنجاه و چهارم
تمرین و آزمون
تمرین پنجاه و پنجم
تمرین و آزمون
تمرین پنجاه و ششم
تمرین و آزمون
سوالات متداول
تا اینجا دانستیم که هیدروکربن چیست و در این بخش میخواهیم به برخی از مهمترین سوالهای پیرامون این موضوع بپردازیم.
انواع هیدروکربن چیست ؟
هیدروکربنها را میتوان با توجه به ساختار و ویژگیهایی که دارند به گروههای متنوعی دستهبندی کرد. یکی دستهبندی کلی تقسیم هیدروکربنها به آروماتیک و آلیفاتیک است.
سه خانواده اصلی هیدروکربن چیست ؟
هیدروکربنهای آلیفاتیک به سه دسته کلی آلکان، آلکن و آلکین تقسیمبندی میشوند.
معنای آروماتیسیته در هیدروکربن چیست ؟
به هیدروکربنی که دارای حلقه ۶ عضوی بنزن باشد، آروماتیک گفته میشود.
آلکان نرمال در هیدروکربن چیست ؟
به آلکانهایی که بهصورت خطی و فاقد شاخه باشند، آلکان نرمال گفته میشود.
عناصر تشکیل دهنده هیدروکربن چیست ؟
هیدروکربنها از دو عنصر هیدروژن و کربن ساخته میشوند و بهوفور در نفت خام حضور دارند.
مهم ترین ویژگی های فیزیکی هیدروکربن چیست ؟
هیدروکربنهای ترکیبهایی بیرنگ و فاقد بو هستند.
مهم ترین واکنشی انجام شده توسط هیدروکربن چیست ؟
واکنش سوختن متدوالترین واکنشی است که هیدروکربنها انجام میدهند. در این واکنش هیدروکربن و اکسیژن وارد واکنش میشوند و از خود آب و کربن دیاکسید به جا میگذارند.
کدام هیدروکربن کمترین واکنش پذیری را دارد ؟
هیدروکربنهای متعلق به خانواده آلکانها بهدلیل پایداری بالا، واکنشپذیری بسیار کمی دارند. آلکانها تنها دارای پیوند یگانه سیگما هستند که برای شکستن آن به انرژی بالایی نیاز است.
آیا هیدروکربن سمی است ؟
بهطور کلی هیدروکربنها سمیت کمی دارند و همین باعث استفاده گسترده از آنها به عنوان سوخت شده است. با این حال هیدروکربنی مانند بنزن به شدت سمی است و میتواند باعث بهوجود آمدن سرطان شود. اشتعالپذیری هیدروکربنهای نیز مشکلزا است.
تاثیر محیط زیستی هیدروکربن چیست ؟
هیدروکربنها بهعنوان سوخت مورد استفاده قرار میگیرند و از خود کربن دیاکسید و آب برجا میگذارند که باعث گرمایش کره زمین میشود.
هیدروکربن راست زنجیر چیست ؟
هیدروکربن راست زنجیر مولکولی بدون شاخه است که از زنجیرهای متشکل از اتمهای کربن تشکیل شده است.
تفاوت آلکن ترمینال و آلکن داخلی در هیدروکربن چیست ؟
در آلکن ترمینال، پیوند دوگانه در یکی از دو سر زنجیره هیدروکربنی وجود دارد، اما در آلکن داخلی در دو سمت پیوند دوگانه زنجیره هیدروکربنی ادامه دارد.
فرمول شیمیایی آلکن در هیدروکربن چیست ؟
فرمول شیمیایی این هیدروکربنهای غیراشباع را میتوام بهصورت نشان داد.
معنای غیراشباعی در هیدروکربن چیست ؟
هیدروکربنی که دارای حلقه، پیوند دوگانه و پیوند سهگانه باشد، غیراشباع است. درواقع زمانی که تمام ظرفیتهای کووالانسی اتمهای کربن یک هیدروکربن اشغال نشده باشد، غیراشباع نامیده میشود.
جمع بندی
هدف از این مطلب این بود که بدانیم هیدروکربن چیست و چه انواعی دارد. همچنین در مورد روشهایی که برای نامگذاری و ایجاد تمایز بین هیدروکربنها وجود دارد صحبت کردیم. در ادامه با بررسی تعدادی مثال و تمرین متنوع درک عمق بخشیدیم.
آزمون هیدروکربن ها
۱. هیدروکربن به چه ترکیبی در شیمی گفته میشود و ساختار آن شامل کدام دو عنصر است؟
ترکیبی شامل فسفر و هیدروژن
ترکیبی شامل کربن و نیتروژن
ترکیبی شامل کربن و هیدروژن
ترکیبی شامل اکسیژن و هیدروژن
هیدروکربن تنها به ترکیباتی اطلاق میشود که مولکول آنها فقط از دو عنصر کربن و هیدروژن ساخته شده است. مطابق تعریف ارائه شده، وجود هر عنصر دیگر مثل نیتروژن، اکسیژن یا فسفر باعث میشود این ترکیب هیدروکربن نباشد.
۲. کدام چهار گروه اصلی بهعنوان خانوادههای هیدروکربن در شیمی آلی شناخته میشوند؟
آلکن، کتون، آمید و اسید
آلکان، الکل، آمین و فنول
آلکین، آلدهید، اسید و اتر
آلکان، آلکن، آلکین و آروماتیک
چهار خانواده مهم هیدروکربنها عبارتند از «آلکان»ها، «آلکن»ها، «آلکین»ها و «آروماتیک»ها که تنها از اتمهای کربن و هیدروژن تشکیل شدهاند. گزینههایی همچون «الکل»، «آمین»، «کتون»، «آمید»، «اسید» و «اتر» گروههای عاملی یا دستههایی از ترکیبات آلی دیگر هستند که اجزایی غیر از کربن و هیدروژن در ساختارشان دارند و جزء خانوادههای اصلی هیدروکربن محسوب نمیشوند.
۳. فرمول عمومی آلکانها چیست و چه ویژگی ساختاری مهمی آنها را از دیگر گروههای هیدروکربن متمایز میسازد؟
فرمول آلکانها است و دارای پیوند دوگانه هستند.
فرمول آلکانها است و حلقه بنزنی تشکیل میدهند.
فرمول آلکانها است و معمولا پیوند سهگانه دارند.
فرمول آلکانها است و فقط پیوند یگانه کربن-کربن دارند.
آلکانها با فرمول شناخته میشوند و فقط دارای پیوندهای یگانه بین اتمهای کربن هستند. این موضوع آنها را از آلکنها که پیوند دوگانه و فرمول دارند، و از آلکینها که پیوند سهگانه و فرمول دارند متمایز میکند. ساختار حلقه بنزنی با فرمول مربوط به هیدروکربنهای آروماتیک است و ارتباطی با آلکانها ندارد.
۴. چه تفاوت کلیدی میان ساختار هیدروکربنهای آروماتیک و آلیفاتیک وجود دارد؟
هیدروکربنهای آروماتیک دارای حلقه بنزنی هستند، هیدروکربنهای آلیفاتیک از زنجیره کربنی تشکیل شدهاند.
هیدروکربنهای آروماتیک و هیدروکربنهای آلیفاتیک همگی ساختار مشابه دارند.
هر دو نوع فقط پیوند سهگانه دارند.
هیدروکربنهای آروماتیک فقط اتم اکسیژن و هیدروکربنهای آلیفاتیک فقط اتم نیتروژن دارند.
در ساختار هیدروکربنهای آروماتیک، وجود حلقه بنزنی ویژگی اصلی است که پایداری بالایی به این ترکیبات میبخشد. در مقابل، هیدروکربنهای آلیفاتیک فاقد حلقه بنزنی بوده و ساختارشان مبتنی بر زنجیرههای کربنی است که میتواند خطی، شاخهای یا حلقوی بدون آروماتیسیته باشد.
۵. کدام نوع پیوند کربن-کربن در ساختار آلکنها وجود دارد و این ویژگی چگونه در نامگذاری آنها موثر است؟
آلکنها فقط پیوند سهگانه دارند و نامگذاری بر اساس تعداد کربن صورت میگیرد.
آلکنها دارای حلقه بنزنی بوده و نامگذاری آنها مستقل از محل پیوند است.
آلکنها دارای یک پیوند دوگانه هستند و موقعیت این پیوند در نامگذاری مشخص میشود.
آلکنها فقط پیوند یگانه دارند و محل آن در نامگذاری اهمیت ندارد.
در ساختار آلکنها یک پیوند دوگانه کربن-کربن قرار دارد که آنها را از سایر هیدروکربنها متمایز میکند. اهمیت اصلی این پیوند در نامگذاری به این دلیل است که موقعیت پیوند دوگانه باید به وضوح در اسم مولکول ذکر شود تا ترکیبات مختلف با ساختارهای متفاوت به طور دقیق متمایز گردند.
۶. اشباع و غیراشباع بودن هیدروکربنها چه تاثیری بر ویژگیهای فیزیکی آنها دارد؟
وجود پیوند چندگانه در غیراشباعها باعث کاتناسیون کمتر میگردد.
هیدروکربنهای اشباع معمولا نقطه ذوب و جوش پایینتری نسبت به غیراشباعها دارند.
غیراشباع بودن باعث افزایش قطبیت مولکولها و حل شدن آنها در آب میشود.
اشباع بودن ساختار، باعث رنگی شدن ترکیبات میشود.
هیدروکربنهای اشباع مانند آلکانها به دلیل داشتن فقط پیوند یگانه بین اتمهای کربن، معمولا نقطه ذوب و جوش پایینتری نسبت به غیراشباعها دارند. غیراشباع بودن ساختار معمولا تاثیر زیادی روی قطبیت یا رنگیبودن ترکیب ندارد و ارتباطی هم با قابلیت ایجاد زنجیره (کاتناسیون) ندارد. بنابراین تفاوت اصلی در ویژگیهای فیزیکی، پایینتر بودن نقطه ذوب و جوش هیدروکربنهای اشباع است.
۷. تفاوت کلیدی ساختار هیدروکربنهای راستزنجیر و شاخهدار چیست و این تفاوت چه اثری در روش نامگذاری آنها دارد؟
در راستزنجیرها، همیشه حلقه بنزنی وجود دارد و نامگذاری سادهتر است، اما شاخهدارها بدون حلقهاند و نامگذاری پیچیده ندارند.
در هیدروکربنهای راستزنجیر، زنجیره کربن پیوسته و بدون استخلاف است و شاخهدارها دارای گروه جانبی هستند که باعث اختصاص عدد به استخلافها در نامگذاری میشود.
در شاخهدارها، زنجیره کربن کوتاهتر از راستزنجیر است و اثر قابل توجهی در قواعد نامگذاری وجود ندارد.
شاخهدارها فقط در هیدروکربنهای آروماتیک دیده میشود و راستزنجیرها همواره ساختار آلیفاتیک دارند.
در ساختار هیدروکربنهای راستزنجیر، اتمهای کربن به صورت پیوسته و بدون حضور گروه جانبی به یکدیگر متصل هستند، بنابراین نامگذاری آنها ساده است و تنها طول زنجیره مدنظر قرار میگیرد. اما در هیدروکربنهای شاخهدار، وجود استخلاف یا شاخه جانبی باعث میشود که در فرآیند نامگذاری، باید مکان و نوع این شاخهها نیز مشخص و با عددگذاری دقیق ذکر شود. بنابراین، تفاوت ساختار در «پیوستگی یا حضور شاخه» مستقیما باعث تفاوت در روش نامگذاری، بهویژه اختصاص عدد و ذکر نام استخلاف، میشود.
۸. فرآیند شکست چه نقشی در صنایع نفت ایفا میکند؟
باعث تجزیه هیدروکربنهای سنگین به سبک میشود.
تبدیل مستقیم آب به سوخت را ممکن میکند.
واکنش استخلافی بین آلکانها و هالوژنها است.
موجب افزایش غلظت بنزن در محصولات میگردد.
فرآیند شکست به تقسیم یا تجزیه هیدروکربنهای سنگین به مولکولهای کوچکتر و سبکتر اشاره دارد که اهمیت زیادی برای صنایع نفت دارد، زیرا سبب تولید سوختها و مواد با ارزشتر میشود.
۹. برای یک هیدروکربن دارای یک حلقه و دو پیوند دوگانه، روش صحیح محاسبه درجه غیراشباعی چیست؟
تعداد اتمهای کربن منهای تعداد اتمهای هیدروژن تقسیم بر دو
مجموع تعداد پیوند دوگانه ضربدر دو بعلاوه تعداد حلقه
جمع تعداد حلقه و همه پیوندهای چندگانه بهصورت جداگانه
جمع تعداد حلقه و تعداد پیوندهای دوگانه با هم
در روش استاندارد محاسبه درجه غیراشباعی، هر حلقه یا هر پیوند دوگانه، یک درجه غیراشباعی به ساختار میافزاید. بنابراین کافی است تعداد حلقه و تعداد پیوندهای دوگانه را با هم جمع کنید.
۱۰. کدام ویژگی ساختاری به درستی برای تشخیص یک هیدروکربن آروماتیک نسبت به سایر انواع ذکر شده کاربرد دارد؟
داشتن فقط پیوند یگانه کربن-کربن در ساختار
حضور دستکم یک پیوند دوگانه در زنجیره کربنی
وجود فقط پیوند سهگانه بین دو اتم کربن
دارا بودن حلقه بنزنی با پیوندهای دوگانه یکی در میان
«دارا بودن حلقه بنزنی با پیوندهای دوگانه یکی در میان» ویژگی متمایز هیدروکربن آروماتیک است؛ آلکانها فقط پیوند یگانه کربن-کربن دارند، آلکنها دستکم یک پیوند دوگانه دارند و آلکینها دارای پیوند سهگانه هستند. فقط هیدروکربنهای آروماتیک حلقه بنزنی با پیوندهای خاص دارند و ساختارشان با دیگر انواع فرق دارد.
۱۱. برای نامگذاری صحیح یک آلکین بر اساس قواعد IUPAC، کدام اصل باید برای انتخاب عددگذاری زنجیره اصلی رعایت شود؟
زنجیره اصلی همیشه باید مستقیم و بدون شاخه باشد.
زنجیره باید طوری عددگذاری شود که بیشترین تعداد کربنها در آن قرار گیرد.
نام زنجیره بر اساس محل پیوند دوگانه انتخاب شود.
کمترین عدد ممکن به اولین کربن پیوند سهگانه اختصاص داده شود.
در قواعد IUPAC، برای نامگذاری آلکین باید زنجیره اصلی را طوری عددگذاری کرد که کمترین عدد به اولین کربن دارای پیوند سهگانه داده شود. این اصل باعث تعیین صحیح محل پیوند سهگانه در نام ترکیب میشود.
۱۲. در مقایسه ایزومرهای فضایی سیس و ترانس یک آلکن، کدام ویژگی فیزیکی میتواند بین این دو بیشتر تفاوت ایجاد کند؟
فرمول شیمیایی آنها در ساختار سیس پیچیدهتر از ترانس است.
نقطه جوش آنها بسته به آرایش میتواند تفاوت قابل توجهی داشته باشد.
جرم مولکولی آنها در هر دو آرایش متفاوت است.
هر دو نوع چگالی برابری دارند و تفاوتی در رفتار فیزیکی نیست.
تفاوت در نقطه جوش ایزومرهای سیس و ترانس به آرایش فضایی پیوند دوگانه در آلکنها باز میگردد. در حالت سیس، به دلیل نزدیکی گروهها، نیروهای بین مولکولی شدیدتر و نقطه جوش بالاتر است؛ اما در حالت ترانس فاصله بیشتر گروهها و تقارن موجب کاهش این نیروها و در نتیجه پایینتر بودن نقطه جوش میشود.
۱۳. افزایش جرم مولکولی و تعداد شاخههای ساختاری چه اثری بر نقطه جوش هیدروکربن دارد؟
افزایش جرم و شاخه هر دو باعث کاهش نقطه جوش میشوند.
افزایش جرم و شاخه هر دو نقطه جوش را بالا میبرند.
افزایش جرم نقطه جوش را کاهش داده و شاخهدار بودن آن را افزایش میدهد.
افزایش جرم نقطه جوش را بالا میبرد اما شاخهدار بودن آن را کاهش میدهد.
بر طبق مطالب بیان شده، «افزایش جرم مولکولی» منجر به افزایش نقطه جوش هیدروکربن میشود، زیرا قدرت نیروهای بینمولکولی بیشتر میگردد. در مقابل، «شاخهدار بودن» باعث کاهش نقطه جوش است؛ وجود شاخه ساختار را فشرده کرده و سطح تماس بین مولکولی را کاهش میدهد.
۱۴. در هیدروکربنها، کدام عامل ساختاری مستقیما نوع هیبریداسیون اتم کربن را تعیین میکند و این هیبریداسیون چه اثری بر زاویه پیوندهای مولکول دارد؟
طول زنجیره کربنی و آرایش شاخهها
تعداد پیوندهای کووالانسی کربن با هیدروژن
حضور یا عدم حضور حلقه بنزنی در ساختار
نوع و تعداد پیوندهای یگانه، دوگانه یا سهگانه بین اتمهای کربن
عامل تعیین کننده نوع هیبریداسیون اتم کربن در هیدروکربنها، وجود پیوند یگانه، دوگانه یا سهگانه بین اتمهای کربن است؛ به طوری که آلکانها با پیوند یگانه دارای هیبریداسیون sp3 (زاویه تقریبی ۱۰۹.۵ درجه)، آلکنها با پیوند دوگانه دارای sp2 (زاویه حدود ۱۲۰ درجه) و آلکینها با پیوند سهگانه دارای sp (زاویه نزدیک ۱۸۰ درجه) هستند. بنابراین تفاوت نوع پیوند مستقیما روی زاویه پیوندها و شکل فضایی مولکول تاثیر میگذارد.
۱۵. برای نامگذاری آلکانها طبق سیستم IUPAC، کدام ترتیب مراحل اصلی صحیح است؟
عددگذاری زنجیره کربنی، انتخاب شاخه اصلی، تعیین نوع پیوند، ذکر محل استخلاف
بررسی نوع پیوند اول، انتخاب گروههای استخلافی، سپس عددگذاری و تعیین طول زنجیره
یافتن بلندترین زنجیره کربنی، عددگذاری، شناسایی شاخهها، نوشتن نام طبق ترتیب الفبا
انتخاب زنجیره شاخهدار، یافتن شاخه اصلی، عددگذاری، نوشتن پیشوندها
در فرایند نامگذاری آلکانها طبق سیستم IUPAC، ابتدا باید بلندترین زنجیره کربنی را شناسایی کرد تا اسکلت اصلی ترکیب تعیین شود، سپس عددگذاری از سمتی که به شاخههای جانبی (استخلافها) عدد کمتری میدهد صورت میگیرد. بعد از آن شاخههای جانبی را شناسایی میکنیم و در پایان نام شاخهها را به ترتیب حروف الفبا و با ذکر محل آنها قبل از نام زنجیره اصلی مینویسیم.
۱۶. اصلیترین تفاوت واکنش جانشینی و واکنش افزایشی در هیدروکربنها چیست؟
در جانشینی اتمهای یک گروه با هالوژن عوض میشود، اما در افزایشی پیوند چندگانه شکسته و اتمهای جدید اضافه میشوند.
واکنش افزایشی به تولید آب منجر میشود ولی جانشینی گاز تولید میکند.
جانشینی خاص آلکینهاست و افزایشی فقط در هیدروکربنهای آروماتیک رخ میدهد.
در هر دو نوع واکنش، فقط آلکانها شرکت میکنند.
در واکنش جانشینی یک اتم هیدروژن هیدروکربن (معمولا در آلکان) با اتم هالوژن جایگزین میشود، اما در واکنش افزایشی، هیدروکربن غیراشباع (مانند آلکن یا آلکین) با شکستن پیوند دوگانه یا سهگانه، اتمهای جدید مثل هالوژن یا هیدروژن را جذب میکند.
۱۷. کدام مورد نشاندهنده یکی از مزیتهای اصلی انرژیهای تجدیدپذیر نسبت به هیدروکربنها برای محیطزیست است؟
حفظ پایداری ترکیبات هیدروکربنی
افزایش مصرف آب در صنایع انرژی
کاهش انتشار و کاهش گرمایش زمین
بالا بردن استخراج منابع نفتی
استفاده از انرژیهای تجدیدپذیر مانند باد و آب به دلیل عدم تولید و گازهای گلخانهای سبب کاهش گرمایش زمین و آسیب کمتر به اکوسیستمها میشود. در مقابل، هیدروکربنها عامل اصلی تولید این گازها و آلودگی محیطزیست هستند. بنابراین 'کاهش انتشار و کاهش گرمایش زمین' مزیت اصلی انرژیهای تجدیدپذیر است
۱۸. در شرایط آزمایشگاهی چگونه میتوان آلکان را از آلکیل هالید بهدست آورد؟
انجام احتراق با اکسیژن
انجام کاهش با معرفهای کاهنده مانند
استفاده از واکنش هیدروژناسیون با کاتالیزور
افزودن هیدروژن هالید به آلکیل هالید
کاهش آلکیل هالید با معرفهایی مانند یا باعث حذف گروه هالوژن و جایگزینی آن با هیدروژن میشود و در نتیجه آلکان به دست میآید. «کاهش با معرفهای کاهنده مانند » روشی متداول برای تولید آلکان از آلکیل هالید است.












سلام وقت بخیر ممنون بابت مطالب. در اولین خط توضیحان به اشتباه به جای هیدروژن نوشتید اکسیژن “هیدروکربنها مولکولهایی آلی هستند که تنها از اتم دو عنصر کربن و اکسیژن به وجود آمدهاند.”
با سلام . این کامل ترین مطلب از هیدرو کربن ها بود که تا به حال دیده بودم. ممنون از شما
سلام و روز شما بهخیر؛
ممنونیم از دقت شما دوست عزیز. متن تصحیح شد.
خوشحالیم که با مجله فرادرس همراه هستید.
سلام روز بخیر
امکانش هست نحوه استخراج و تولید گاز اتان از نفت رو هم توضیح بفرمایید ؟
با سلام؛
پیشنهاد میکنم مطلب «جداسازی اجزای تشکیل دهنده نفت خام | به زبان ساده» را مطالعه کنید.
با تشکر از همراهی شما با مجله فرادرس
سلام . آیا درنفت خام در یک برش نفتی اتم هایی که نقطه جوش نزدیکی دارند تعداد کربن ها برابر است؟
با سلام؛
یک برش نفتی، مخلوطی از هیدروکربنها است که مولکولهای آن شامل تعداد اتم کربن برابر باشند. این موضوع به طور کامل در مطلب «جداسازی اجزای تشکیل دهنده نفت خام | به زبان ساده» توضیح داده شده است.
با تشکر از همراهی شما با مجله فرادرس
سلام اصلاحات هیدرو کربن چیه؟
سلام ببخشید یه سوال داشتم هیدروکربن هایی که تعدادکربنشون کمتر از 5 قطبی حساب میشن؟
با تشکر از مجله فرادرس یه سوال داشتم
چجوری میشه همهی ساختار های یک هیدروکربن رو رسم کرد ؟
سلام و روز شما بهخیر؛
برای یافتن تعداد ایزومرهای یک هیدروکربن با تعداد اتم کربن مشخص ، هیچ روش ساده و فرمول ثابتی وجود ندارد. برای مثال برای هیدروکربنهایی که دارای مرکز کایرال هستند، میتوان از فرمول 2n استفاده کرد که در آن n تعداد مراکز کایرال موجود در ساختار است. با این حال در همین مورد نیز وجود ایزومرهای مزو، تعداد کل ایزومرها را کاهش میدهد. بهترین راه برای یافتن تعداد ایزومرها، رسم آنهاست. در این روش باید تمام حالتهای مختلف اتصال اتمها را در نظر گرفت و رسم کرد.
با تشکر از همراهی شما دوست عزیز با مجله فرادرس.
اگر ۱هیدروژن داشته باشند،تا ۵تا کربن ظرفیت دارن تا قطبیت خودشونو حفظ کنند اما اگر به ازای ۱هیدروژن بیشتر از ۵کربن وجود داشته باشه بخش ناقطبی بر قطبی غالب خواهد بود پ اصطلاحا مولکول را ناقطبی و در اب نامحلول است.
امیدوارم مفید باشه براتون
سلام خسته نباشید میتونم بپرسم تفاوت و شباهت سوختن هیدروکربن ها چیه و مفید و خطرناک ترینشون چی هست
سلام
چطور میتوانیم نقطه جوش متیل سیکلو بوتان و سیکلو بوتان رو مقایسه کنیم فقط تعداد کربن مهمه؟
با سلام؛
همانطور که در داخل متن نیز به آن اشاره شده است، نقطه جوش هیدروکربنها به عوامل مختلفی وابسته است. همچنین برای مطالعه بیشتر میتوانید مطلب «نقطه جوش — از صفر تا صد» را مطالعه کنید.
با تشکر
با سلام؛
شباهت هیدروکربنها را میتوان در نام آنها یعنی ترکیباتی متشکل از هیدروژن و کربن مشاهده کرد. تمامی هیدروکربنها اشتعالپذیر و از اینرو خطرناک هستند اما آنچه که میتوان به عنوان تفاوت در این خصوص مشاهده کرد، تفاوت در «نقطه سوختن» (Flash Point) است که برای هیدروکربنی مانند بنزین، این نقطه (دما) برابر با منفی ۴۰- درجه سانتیگراد است یعنی در این دمای منفی، بنزین با آزاد کردن بخار و ترکیب با اکسیژن هوا میتواند مشتعل شود اما ترکیبی مانند فنول، در دمای ۷۹ درجه سانتیگراد مشتعل میشود.
با تشکر از همراهی شما با مجله فرادرس
سلام
از بین اینا الان پایداریشون به چه شکله کدوم پایدارتره ؟
سلام آقای کاظمی خیلی ممنون از مقاله خوبتون فقط میخوساتم بدونم ترتیب واکنش پذیری هیدروکربن ها چجوریه؟؟
سلام .یه سوال داشتم در مورد الکل ها چرا میل به واکنش tersiyer الکل ها نسبت به sekonder alkoller بیشتره ؟مربوط میشه به تعداد شاخه های فرعی؟
با سلام؛
الکلهای نوع دوم و سوم با اسیدها قوی قوی HX از طریق مکانیسم واکنش SN1 واکنش میدهند. در این نوع واکنشها، مرحله تعیین کننده سرعت، تشکیل کربوکاتیون و وابسته به حمله کلریدهای نوکلئوفیل است. اثر القایی گروه R از الکلها، کربوکاتیونها را پایدار میکند و دلیل واکنشپذیری را باید در این اثر القایی جستجو کرد. برای اطلاعات بیشتر پیشنهاد میکنیم مطالب زیر را مطالعه کنید:
کربوکاتیون چیست؟ — به زبان ساده
واکنش جانشینی — به زبان ساده
با تشکر از همراهی شما با مجله فرادرس
با سلام؛
از شما بابت مطالعه این مطلب سپاسگزاریم. به طور کلی ترتیب واکنشپذیری هیدروکربنها از آلکان تا آلکین افزایش مییابد. همچنین پیشنهاد میکنیم برای بررسی هیدروکربنهای آروماتیک و آشنایی با اوربیتال مولکولی، مطالب زیر را مطالعه کنید:
«هیدروکربن های آروماتیک | به زبان ساده»
«اوربیتال مولکولی — به زبان ساده»
با تشکر