آلدهیدها – به زبان ساده
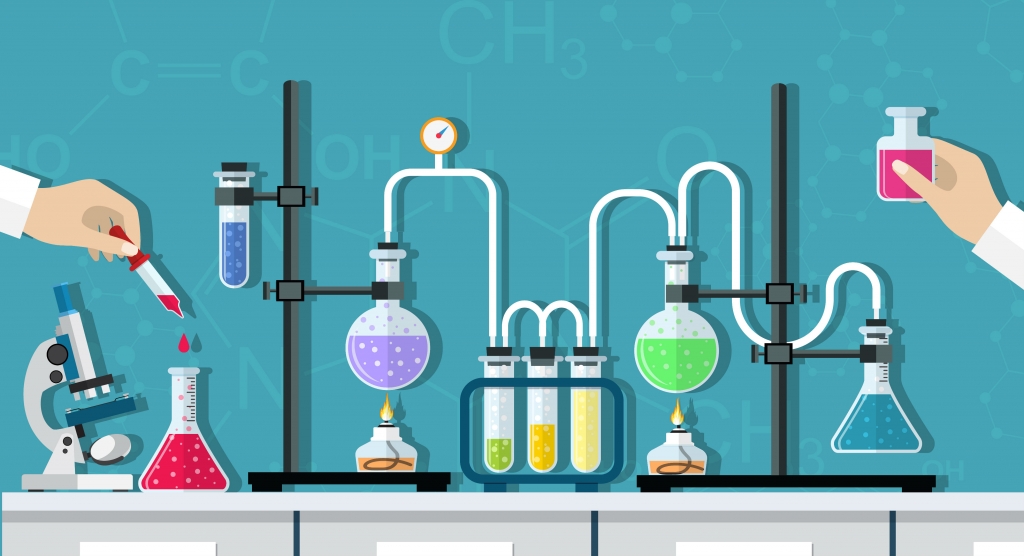
یک آلدهید ترکیبی با گروه عاملی و شامل گروه عاملی کربونیل (پیوند دوگانه کربن با اکسیژن) است. این کربن از دو طرف نیز به زنجیر آلکیل و هیدروژن متصل است. آلدهیدها در شیمی آلی بسیار مورد بررسی قرار میگیرند و بیشتر عطرها در حقیقت آلدهید هستند.

خواص فیزیکی
آلدهیدها خواص متنوعی دارند و این خواص به نوع مولکول آنها وابسته است. آلدهیدهای کوچکتر همچون فرمالدهید و استالدهید، حلالپذیری بیشتری در آب دارند. همچنین آلدهیدهای فرار، با بویی تند شناخته میشوند. آلدهیدها و خصوصا آریل آلدهیدها در واکنشهای اکسیداسیون خود به خودی شرکت میکنند. فرمالدهید و استالدهید، دو نوع از مهمترین آلدهیدها در صنعت هستند که رفتار پیچیدهای از خود نشان میدهند.
علت این امر «اولیگومر شدن» (Oligomerize) یا «پلیمر شدن» (Polymerize) است. فرمالدهید عموما به صورت پلیمر پارافرمالدهید با فرمول به فروش میرسد. عدد در این پلیمر معمولا بین ۵۰ تا ۱۰۰ است. علاوه بر این، آلدهیدها به خوبی با روشهای اسپکتروسکوپی شناسایی میشوند.
کاربردها
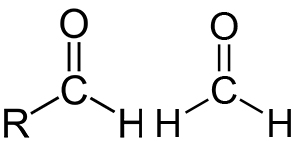
بسیاری از آلدهیدها در روغنهای گیاهی یافت میشوند. این ترکیبات بواسطه بویی که دارند از بقیه متمایز هستند. از نمونههای آنها میتوان به گشنیز و وانیلین اشاره کرد که شامل آلدهیدها هستند. آلدهیدها به دلیل فعالیت بالایی که دارند در آمینو اسیدها، نوکلئیک اسیدها و لیپیدها دیده نمیشوند. البته بسیاری از قندها، مشتقاتی از آلدهیدها هستند.
سنتز آلدهید
روشهای مختلفی برای آمادهسازی و سنتز آلدهیدها وجود دارد که اصلیترین آن شامل هیدروفرمیلاسیون (Hydroformylation) است. در این روش، بوتانال (بوتیر آلدهید) با استفاده از هیدروفرمیلاسیون پروپن بوجود میآید.
سنتز با اکسیداسیون الکلها
آلدهیدها معولا از طریق اکسیداسیون الکلها به تولید میرسند. در صنعت، فرمالدهید از طریق اکسیداسیون متانول بدست میآید. در واکنشهای اکسیداسیون صنعتی از اکسیژن به دلیل سازگاری با محیط زیست و در دسترس بودن، به عنوان اکسنده استفاده میشود؛ اما در آزمایشگاه، از اکسندههای بهتری کمک میگیرند. در این میان، واکنشگر کروم (VI) محبوبیت بیشتری دارد.
به کمک گرم کردن الکلها در محیط اسیدی پتاسیم دیکرومات، میتوان آلدهیدها را سنتز کرد. در این شرایط، دیکرومات اضافه، آلدهید را اکسید و آن را به کربوکسیلیک اسید تبدیل میکند. در این حالت، آلدهید را در صورت فرار بودن میتوان تقطیر کرد یا اینکه از واکنشگرهایی مانند «پیریدیوم کلروکرومات» (PCC) استفاده کرد که در زیر با نشان داده شده است:
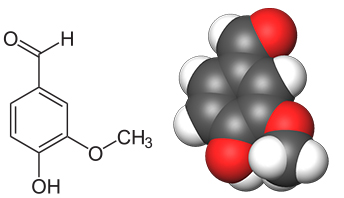
روش دیگر تولید آلدهیدها در صنعت استفاده از «فرآیند واکر» (Wacker Process) است. در این فرآیند، اتیلن در حضور کاتالیزورهای مس و پالادیوم، اکسید و به استالدهید تبدیل میشود. البته استالدهید از طریق هیدراسیون استیلن نیز به تولید میرسد.
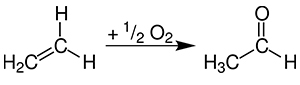
واکنشهای معمول در آلدهید
آلدهیدها ترکیباتی بسیار فعال هستند و در واکنشهای زیادی شرکت میکنند. واکنشهای مهم شامل تراکم و کاهش است. از واکنشهای تراکمی (میعانی) برای آمادهسازی «پلاستی سایزرها» (Plasticizers) و «پلی اولها» (Polyols) استفاده میشود. واکنشهای کاهشی نیز در تولید الکلها کاربرد دارند. عموما گروه فرمیل به سادگی به الکل نوع اول کاهش پیدا میکند. البته این امر به کمک هیدروژناسیون مستقیم یا انتقالی قابل انجام است.
اکسیداسیون
گروه فرمیل به سادگی به گروه کربوکسیل متناظر با خود اکسید میشود. اکسیژن از معروفترین اکسندهها در صنعت است اما در آزمایشگاه، اکسندههای دیگری همچون پتاسیم پرمنگنات، نیتریک اسید، کروم (VI) اکسید و «کرمیک اسید» (Chromic Acid) مورد استفاده قرار میگیرند. ترکیب «منگنز دی اکسید» ، سیانید، استیک اسید و متانول موجب تبدیل آلدهید به متیل استر میشود.
واکنش دیگر اکسیداسیون، بر پایه «آزمایش آینه نقرهای» (Silver-Mirror) بنا شده است. در این واکنش، یک آلدهید با «واکنشگر تولنس» (Tollens) وارد واکنش میشود. این واکنشگر، آلدهید را بدون دخالت در پیوند کربن-کربن به کربوکسیلیک اسید تبدیل میکند. به دلیل اینکه در این فرآیند، رسوب نقره تشکیل میشود که در حضور آن میتوان به وجود آلدهید پی برد، این آزمایش به آینه نقرهای موسوم است. علاوه بر این، با استفاده از واکنشگر فهلینگ، کمپلکس یون به رسوب تبدیل میشود. این رسوب به رنگ قرمز آجری است.
در صورتی که آلدهید یک انولات تشکیل ندهد، اضافه کردن یک باز قوی موجب القای شرایط واکنش کانیزارو میشود. این واکنش به کمک «تسهیم نامتناسب» (Disprpportionation)، مخلوطی از الکل و کربوکسیلیک اسید تولید میکند که در تصویر زیر نشان داده شده است:
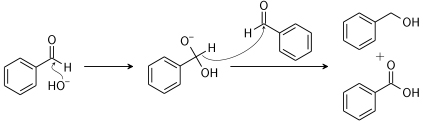
واکنشهای افزایشی هسته دوست
هستهدوستها به سادگی به گروههای کربونیل اضافه میشوند. در محصول نهایی، کربن متصل به گروه کربونیل به صورت «هیبرید شده» (Hybridized) و متصل به یک هسته دوست خواهد بود.
در مقابل، اکسیژن نیز پروتوناسیون (پروتون دهی) میشود. در رابطه زیر، نماد نشادندهنده یک هستهدوست (نوکلئوفیل) است:
دی آلدهیدها
دیآلدهیدها ترکیبات آلی شامل دو گروه آلدهید هستند. در نامگذاری آنها از عبارات «دیال» یا «دی آلدهید» استفاده میکنیم. آلدهیدهای آلیفاتیکی با زنجیر کوتاه کربنی معمولا بعد از دی اسیدهای خود نامگذاری میشوند. به طور مثال، «بوتان دیال» (Butanedial) را «سوکسین آلدهید» مینامند چراکه از «سوکسینیک اسید» (Succininc Acid) با فرمول مشتق میشود.

اگر این مطلب برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای نرمافزارهای مهندسی شیمی
- آموزش شیمی آلی ۱
- هیدروکربن ها — به زبان ساده
- کتون ها — به زبان ساده
^^













سلام وقت بخیر میشه لطفاً مکانیسم تبدیل الکلهای نوع اول به آلدهید در حضور pcc رو محبت بفرمایید؟
با سلام؛
در اولین مرحله از مکانیسم تبدیل الکلهای نوع اول به آلدهید توسط پیریدینیوم کلروکرومات، اکسیژن الکل به اتم کروم حمله کرده و پیوند کروم – اکسیژن تولید میکند. سپس یک یون هیدروژن که به اکسیژن الکل متصل است، به یکی از اکسیژنهای کروم متصل میشود. این کار به واسطه نمک پیریدینیوم انجام میشود. پس از آن یک یون کلرید در واکنشی شبیه به واکنش حذفی ۱ و ۲، توسط یک هیدروژن جابهجا شده و به اتم کروم متصل میشود. ماده تولید شده در این مرحله یک استر کرومات خواهد بود.
پیوند دوگانه کربن – اکسیژن، با جدا شدن یکی از هیدروژنهای کربن توسط یک باز یا پیریدین تشکیل میشود. در واکنش E2 الکترونهای پیوند کربن – هیدروژن، پیوند دوگانه کربن – اکسیژن را تشکیل میدهند. در این فرآیند، پیوند اکسیژن – کروم شکسته میشود. در این فرآیند، کروم (VI) دو الکترون دریافت کرده و به کروم (IV) تبدیل میشود.
پیشنهاد میکنیم بری درک بهتر مکانیسم این فرآیند، مطلب «واکنش حذفی» مجله فرادرس را مطالعه کنید.
با تشکر از همراهی شما با مجله فرادرس
با سلام
آلدهیدهای اروماتیک در چه حلالهای به خوبی حل می شوند؟
آسیل کلرید یا کلرید اسید در حضور کاتالیزوری مانند باریم سولفات (BaSO4) یا پالادیم (Pd) برای تهیه آلدهیدها استفاده میشود. تشکیل آلدهید با افزودن ترکیباتی مانند گوگرد یا کینولون امکانپذیر است. برای آشنایی بیشتر «واکنش روزنموند» (Rosenmund Reaction) مطالعه شود.