ایزومر فضایی چیست؟ – به زبان ساده
ایزومر فضایی به ایزومرهایی میگویند که در آرایش فضایی اتمهای خود با یکدیگر اختلاف دارند. یکی از مهمتین ایزومرها، ایزومرهایی هستند که تصویر آینهای آنها بر یکدیگر منطبق نیستند. این نوع از مولکولها نیز با مفهوم کایرالیته توضیح داده میشوند. در مطالب پیشین «مجله فرادرس» با مباحثی همچون ایزومرها و انواع آنها و همچنین شیمی فضایی آشنا شدیم. در این آموزش قصد داریم ایزومر فضایی را مورد بررسی قرار دهیم.

مقدمه
ترکیبات آلی به مولکولهایی میگویند که از زنجیرههای اتمهای کربن تشکیل شدهاند و نقش مهمی را در شیمی ایفا میکنند. این مولکولها اهمیت خود را به دلیل انرژی موجود در خود کسب کردهاند و این انرژی به صورت انرژی پتانسیل اتم مولکولهای این ترکیبات، ذخیره شده است. از آنجایی که این انرژیها میتوانند متاثر از تغییرات در نحوه قرارگیری اتمها باشند، اهمیت درک مفهوم ایزومرها نیز بیشتر میشود. اهمیت ایزومر فضایی و کایرالیته در شیمی آلی جدید بسیار زیاد است چراکه این مفاهیم به ما در درک علتهای نظری و فیزیکی تشکیل مولکولهای آلی و ساختار آنها کمک میکنند. برخلاف مفهوم شناخته شده ایزمور ساختاری، ایزومر فضایی پیوندهای برابر را شامل میشود و همچنین، در ایزومر فضایی تعداد اتمها و نوع پیوندها نیز یکسان است.
اما برای درک بهتر ایزومرهای فضایی باید بتوان تصوری سهبعدی از مولکولها داشت چراکه ایزومرهای فضایی ایزومرهایی هستند که اتمهای آنها آرایش فضایی متفاوتی نسبت به یکدیگر دارند. در صورتیکه با مباحث مربوط به شیمی فضایی آشنایی ندارید پیشنهاد میکنیم مطلب «شیمی فضایی — به زبان ساده» را مطالعه کنید تا با مباحثی همچون کنفیگراسیون، صورتبندیها (کانفورماسیون) و مباحثی از این دست، آشنایی بیشتری داشته باشید.
آرایش فضایی
اولین موضوعی که باید برای درک ایزومر فضایی و کایرالیته مطرح کرد، آرایش فضایی است. آرایش فضایی به نحوه قرارگیری ذرات اتمی و مولکولها در فضای اطراف ترکیب آلی یا همان زنجیر کربنی میگویند. به این ترتیب، آرایش فضایی یک مولکول آلی با جابجایی یک اتم آن در یکی از محورهای سهبعدی، مولکولهای مختلفی را بوجود خواهد آورد.
ایزومر فضایی و ساختاری
همانطور که میدانید، ایزومرها ترکیبات متفاوتی هستند که فرمول مولکولی یکسانی دارند. هنگامی که گروهی از اتمهای تشکیل دهنده مولکولهایی از ایزومرهای مختلف به شکلهای مختلفی با یکدیگر پیوند برقرار کنند، این ترکیبات را با نام «ایزومر ساختاری» (Constitutional Isomers) میشناسیم.
به طور مثال، هیدروکربنهایی با فرمول شامل ایزومرهایی به طور معمول از نوع ایزومر ساختاری هستند. در تصویر زیر، این ایزومرها را مشاهده میکنید.

توجه داشته باشید که ۱۲ اتم تشکیل دهنده ترکیبات بالا، به شکلهای مختلفی با یکدیگر پیوند دارند. این ایزومرهای ساختاری هرکدام نام آیوپاک متفاوتی خواهند داشت. از آنجایی که تعداد دو اتم هیدروژن کمتر از آلکان چهار کربنه یعنی بوتان با فرمول است، در نتیجه تمامی ایزومرها باید دارای یک حلقه یا پیوندی دوگانه باشند. ایزومر محتمل پنجم با فرمول ، ترکیبی با فرمول خواهد بود. بر اساس نامگذاری آیوپاک، این ترکیب را باید ۲-بوتن نامگذاری کرد. با این وجود، اگر با دقت بیشتری به این مولکول نگاه کنیم، خواهیم دید که دو ساختار محتمل برای آن وجود خواهد داشت. این دو ایزومر مختلف، ترکیباتی کاملا مجزا با خواصی متفاوت هستند که در تصویر زیر، با پیشوندهای «سیس» (cis) و «ترانس» (trans) نمایش داده شدهاند.
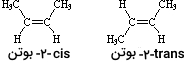
الگوهای پیوندی در این دو ایزومر با یکدیگر برابر هستند با این تفاوت که چرخش نسبی یا به عبارتی آرایش دو گروه متیل در دو مولکول با یکدیگر تفاوت دارند. در ایزومر سیس، گروههای متیل در یک طرف قرار دارند درحالیکه این گروهها در ایزومر ترانس، در دو طرف مولکول دیده میشوند. به ایزومرهایی که تنها در چرخش فضایی اتمها - یا گروههای اتمی - با یکدیگر تفاوت دارند ایزومرهای فضایی میگویند. به طور معمول برای مشخص کردن چرخش فضایی از پیشوندهایی استفاده میشود.
انانتیومرها
انانتیومرها که آنها را با نام ایزومر نوری نیز میشناسند، به دو ایزومر فضایی میگویند که تصویر آینهای یکدیگر باشند و بر روی یکدیگر انطباق نداشته باشند. انانتیومرها را میتوان با دستهای انسان مقایسه کرد چراکه این دستها تصویر آینهای یکدیگر هستند اما بر روی یکدیگر انطباق ندارند. دو ترکیبی که انانتیومر یکدیگر باشند، خواص فیزیکی یکسانی به جز در یک مورد دارند و آن، چرخاندن نور پلاریزه است. در نتیجه، انانتیومرهای مختلف یک ترکیب میتوانند اثرات بیولوژیکی مختلفی داشته باشند.
انانتیومرهای خالص، پدیدهای موسوم به «فعالیت نوری» (Optical Activity) از خود نشان میدهند و آنها را تنها به کمک یک عامل کایرال میتوان از یکدیگر جداسازی کرد. در تصویر زیر میتوانید نمونهای از انانتیومرها را مشاهده کنید.
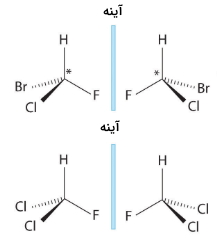
توجه داشته باشید که در تصاویر بالا حتی اگر یک مولکول را مقابل یک مولکول دیگر قرار دهیم، بازهم چرخش فضایی آنها یکسان نخواهد بود. در اینجا مفهوم کایرالیته ظاهر میشود که بخش مهمی از مفهوم ایزومر فضایی را تشکیل میدهد.
کایرالیته
کایرالیته به طور کلی با مفهوم تصویر آینهای و مولکولهای غیرمنطبق بر هم تعریف میشود. اگر بگوییم یک مولکول کایرال است به این معناست که این مولکول بر تصویر آینهای آن منطبق نمیشود. اینکه یک مولکول کایرال یا «اکایرال» (Achiral) باشد به شرایط مختلفی وابسته است.
دیاسترومرها
دیاسترومرها ایزومرهای فضایی هستند که تصویر آینهای یکدیگر نیستند و همچنین بر یکدیگر انطباق ندارند. ایزومرهای فضایی که یک یا چند مرکز فضایی داشته باشند را میتوان به عنوان دیاسترومر در نظر گرفت. در برخی موارد، دشوار است که بگوییم دو مولکول دیاسترومر یکدیگر هستند. دو مولکول زیر را در نظر بگیرید.
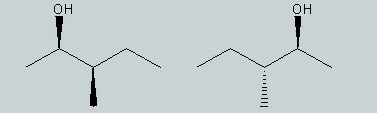
این مولکولها تصویر آینهای یکدیگر نیستند. علاوه بر این، بر یکدیگر نیز انطباق ندارند در نتیجه، این مولکولها دیاسترومر هستند.
ترکیباتی با چندین مرکز کایرال
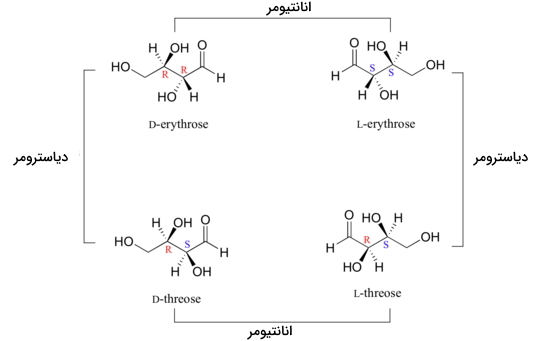
در ادامه، مولکولهایی را بررسی میکنیم که بیش از یک مرکز فضایی داشته باشد. کار خود را با یک قند چهارکربنه به نام «D-erythrose» آغاز میکنیم.
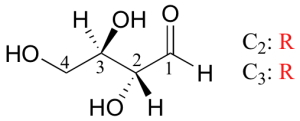
همانطور که مشاهده میکنید، این مولکول، کایرال است و کربن ۲ و ۳ مراکز فضایی آن هستند که هردو کنفیگراسیون R دارند. علاوه بر این، فارغ از کانفورماسیون (صورتبندی) مولکول، میتوان صفحهای متقارن را در مولکول مشاهده کرد. با توجه به اینکه مولکولی کایرال داریم، یک انانتیومر نیز به نام «L-ertyhrose» نیز برای آن وجود خواهد داشت که در تصویر زیر مشاهده میکنید. توجه داشته باشید که در این مولکول، کنفیگراسیون S خواهیم داشت.
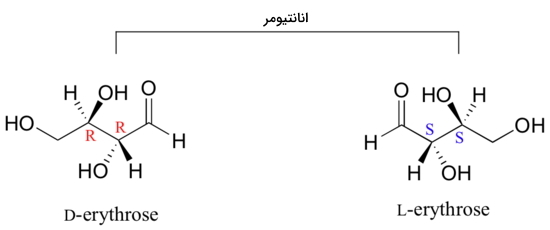
اگر ایزومر فضایی از این مولکول رسم کنیم که کنفیگراسیون S در کربن ۲ و R در کربن ۳ داشته باشد به مولکولی با نام «D_threose» میرسیم که تصویر آینهای Erythrose نیست و همانطور که در بالا مشاهده کردیم، به آن دیاسترومر میگویند.
ایزومرهای cis-trans و E_Z
از آنجایی که چرخش حول پیوند دوگانه محدود است و سبب میشود گروههای استخلافی نسبت به یکدیگر ثابت باشند باید نسبت به بررسی ایزومر فضایی حول پیوند دوگانه نیز اقدام کرد. اگر دو استخلاف (گروه جانشین) بر روی حداقل یک سر پیوند دوگانه، یکسان باشند، هیچ ایزومر فضایی نخواهیم داشت و پیوند دوگانه نیز یک مرکز فضایی نیست که از نمونههای آن میتوان به پروپن با فرمول اشاره کرد. در این مولکول، هر دو استخلاف در یک طرف مولکول، اتمهای هیدروژن هستند.
از گذشته پیوندهای دوگانه را در شیمی فضایی به صورت cis یا trans توصیف میکردند. از نمونههای ایزمرهای سیس-ترانس میتوان به ترکیبات دو استخلافی اتن مثل دیکلرو اتن اشاره کرد که ایزومرهای آن در زیر آورده شدهاند.

مولکول سمت چپ، سیس-۱و۲ دیکلرواتن و مولکول سمت راست، ترانس-۱و۲ دیکلرواتن است. به دلیل دشواری نامگذاری، آیوپاک سیستمی را بر اساس عدد اتمی ارائه داد. اگر استخلافها با اولویت بالاتر، در یک طرف پیوند قرار داشته باشند، به آن حرف «Z» و اگر در طرف مقابل یکدیگر باشند به آن حرف «E» اختصاص پیدا میکند.
با توجه به اینکه کلر، عدد اتمی بزرگتری نسبت به هیدروژن دارد، گروهی با اولویت بالا به شمار میآید. با استفاده از این روش نامگذاری، نام مولکول سمت چپ (Z)-۱و۲ دیکلرواتن و نام مولکول سمت راست (E)-۱و۲ دیکلرواتن است. البته این بدان معنی نیست که میتوان ایزومر فضایی سیس یا ترانس را با E و Z معادلسازی کرد. مولکول زیر با نام فلوئورمتیل پنتن را در نظر بگیرید.
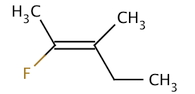
نام مناسب این ترکیب را میتوان ترانس-۲-فلوئورو-۳-متیل پنت-۲-ان یا (Z)--۲-فلوئورو-۳-متیل پنت-۲-ان ذکر کرد. فلوئور، گروهی با بیشترین اولویت در سمت چپ پیوند دوگانه است و اتیل در سمت راست نیز بیشترین اولویت را در سمت راست دارد.
کانفورمرها
ایزومرهای کانفورماسیونی نوعی از ایزومرها هستند که فرمول ساختاری یکسان اما به دلیل چرخش یک یا دو پیوند، شکل متفاوتی دارند. کانفورماسیونهای مختلف، انرژیهای متفاوتی دارند که قابل تبدیل به یکدیگر هستند. به طور مثال، سیکلوهگزان در کانفورماسیونهای مختلفی وجود دارد اما این کانفورماسیونها را نمیتوان جداسازی کرد.
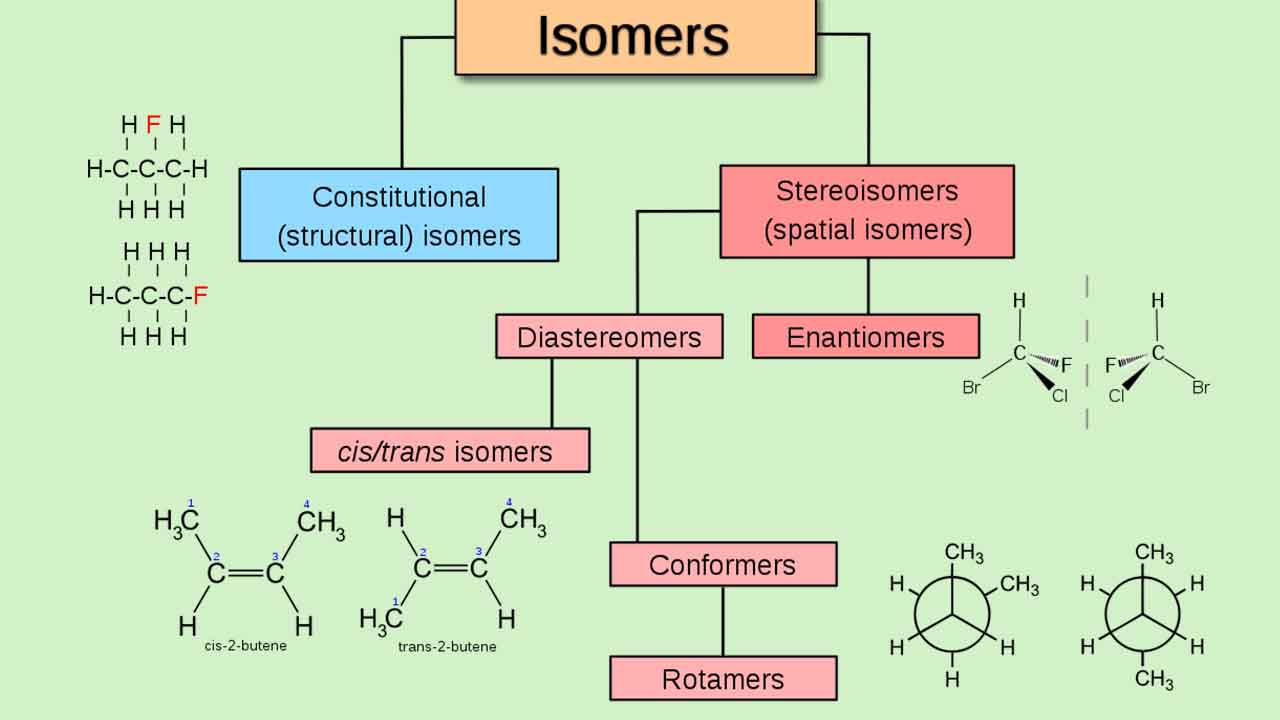
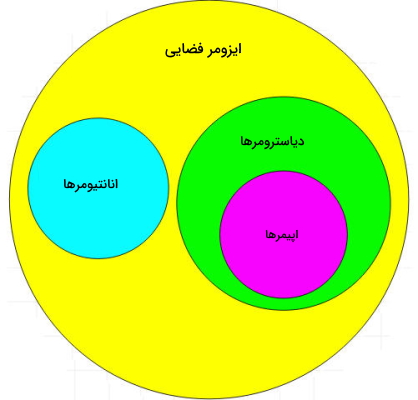
در تصویر زیر، انواع ایزومرهای فضایی نشان داده شدهاند.
معرفی فیلم آموزش شیمی آلی ۱
تا اینجا سعی شد به شکلی ساده به ایزومر فضایی پرداخته شود اما ایزومرهای فضایی بخش اصلی شیمی آلی را در دروس دانشگاه تشکیل میدهند. به همین دلیل، «فرادرس» دورهای ۶ ساعت و ۴۰ دقیقهای را در قالب ۹ درس تدوین کرده است که به توضیح دروس آن خواهیم پرداخت.
در درس یکم، آلکانها آموزش داده میشوند که از مباحث مهم این درس میتوان به دیاگرام انرژی آلکانها و نامگذاری آلکانها اشاره کرد. درس دوم به شیمی فضایی یا استریوشیمی اختصاص دارد. مباحث مهمی همچون فعالیت نوری و تعیین مراکز فضایی در این درس بررسی میشود. آلکیل هالیدها در درس سوم مورد بررسی قرار میگیرند و درس چهارم، الکلها و اترها بررسی میشوند. در درس پنجم انوع حلالهای قطبی و ناقطبی مرور خواهند شد و درس ششم نیز به نحوه تهیه آلکنها اختصاص دارد.
درس ششم و هفتم، ساختار و واکنشهای آلکنها مورد بررسی قرار میگیرد که از جمله مباحث مهم آن باید به واکنشهای حذفی و قانون مارکونیکوف اشاره کرد. در درس هشتم، فضاگزینی و فضاویژگی آموزش داده خواهد شد و در نهایت در درس نهم، آلکینها بویژه از نظر ساختار و ویژگی مورد بررسی قرار میگیرند.
ایزومر فضایی در آلکن ها
پیوند دوگانه کربن-کربن در آلکنها بین دو کربن هیبرید شده بوجود میآید و شامل دو اوربیتال مولکولی سیگما و پای است. چرخش گروههای انتهایی پیوند دوگانه نسبت به یکدیگر سبب تخریب همپوشانی اوربیتال p خواهد شد. از آنجایی که پیوند پای، انرژی پیوندی برابر با 60 کیلوکالری بر مول دارد، این مقاومت در بر چرخش سبب پایداری کنفیگراسیون سطحی این گروه عاملی خواهد شد. در نتیجه، برخی از آلکنهای دو استخلافی به صورت جفتهایی از ایزومرهای فضایی کنفیگراسیونی وجود خواهند داشت که به طور معمول به صورت سیس و ترانس خواهند بود.
برای اینکه این نوع از ایزومر فضایی را داشته باشیم باید هر کربن پیوند دو گانه، دو گروه استخلافی متفاوت داشته باشد. این مورد را در مثالهای زیر مشاهده میکنید. در مثال اول (سمت چپ)، پیوند دوگانه کربن در طرف چپ دارای دو استخلاف یکسان (A) است و در نتیجه، ایزومرهای فضایی مرتبط با پیوند دوگانه نخواهیم داشت. در دو مثال بعد، هر پیوند دوگانه در اتم کربن شامل دو گروه استخلافی متفاوت است و ایزومر فضایی خواهیم داشت.
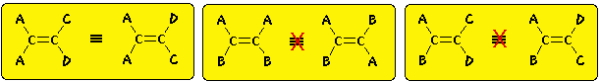
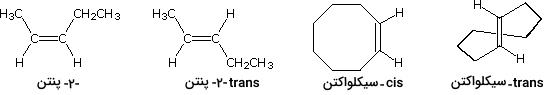
از نمونههای این ایزومرها میتوان به مثالهای زیر اشاره کرد. توجه داشته باشید که سیکلوآلکانهایی با کمتر از هشت اتم کربن به دلیل «کرنش» (Strain) در حلقه نمیتوانند به صورت ایزومرهای پایدار ترانس وجود داشته باشند. با توجه به اینکه آلکینها، مولکولهایی خطی هستند، ایزومر فضایی برای پیوند سهگانه کربن-کربن نمیتوان در نظر گرفت.