آب در شیمی | ساختار، خواص و واکنشها | به زبان ساده
مادهای که تنها از دو عنصر شیمیایی هیدروژن و اکسیژن تشکیل شده است و در حالتهای گاز، مایع و جامد آنرا دیدهایم یکی از فراوانترین ترکیبها بر روی زمین به شمار میآید. مادهای بیرنگ، بیطعم و بیبو که از ضروریترین مواد مورد نیاز ما است. در دمای اتاق به حالت مایع قرار دارد و توانایی مهم آن حل کردن بسیاری از مواد در خود است. در واقع همهکاره بودن آب به عنوان یک حلال (حل کننده) آن را برای جانداران ضروری ساخته است.


تصور بر این است که حیات نخستین در محلولهای آبی و درون اقیانوسها شکل گرفته و زنده ماندن جانداران وابسته به محلولهای آبی است که مانند خون و شیرههای گوارشی، در فرایندهای زیستی بدن جانداران نقش دارند. اکنون میخواهیم نگاهی به شیمی، فیزیک و نقشها و ویژگیهای منحصر به فرد این ماده حیاتی داشته باشیم.

هرچند مولکولهای آب، ساختار سادهای دارند، اما خاصیتهای فیزیکی و شیمیایی این ترکیب بسیار پیچیده و در کمتر ترکیبی بر روی زمین مشاهده شده است. برای نمونه، اگر چه مشاهده قالبهای مکعبی یخ که در لیوان بر روی آب یخ شناور هستند امری عادی به نظر میآید، این رفتار در میان دیگر ترکیبهای شیمیایی نامعمول است.
برای سایر ترکیبها، حالت جامد چگالتر از حالت مایع است. پس جامد آنها در مایع فرو میرود. این واقعیت که یخ بر روی آب شناور میشود برای طبیعت جهان بسیار مهم و اساسی است، زیرا یخی که بر روی دریاچهها و تالابها در منطقههای سردسیر به وجود میآید همانند یک سد نارسانا، از حیات زیر آن آبها محافظت میکند. اگر یخ چگالتر از آب مایع بود، یخ تشکیل شده بر روی تالاب در آن فرو میرفت، در نتیجه آب بیشتری در معرض هوای سرد قرار میگرفت که به دنبال آن، همه تالاب دچار یخزدگی میشد و حیات موجودات حاضر در تالاب از بین میرفت.
بر روی سطح زمین و تحت شرایط عادی، آبها به حالت مایع یافت میشوند که انتقال آن را به زیستگاه بسیاری از گیاهان و جانوران امکانپذیر میکند. ساگی تبدیل این ماده به بخار، اجازه میدهد انتقال آن از مسیر اتمسفر بین اقیانوسها و منطقههای خشک انجام شود و با میعان آن به شکل باران، بسیاری از گیاهان و حیات وحش را سیراب کند. به انتقال آبها در طبیعت، «چرخه آب» (Water Cycle) گفته میشود زیرا در این چرخه، آبها از بین نمیروند و با تغییر در حالت فیزیکی، گردش و انتقال آن بر روی زمین اتفاق میافتد.
به سبب اهمیت آب، در تاریخ بشر، این ماده نقشی مهمی در دین و فلسفه بازی کرده است. در قرن ششم قبل از میلاد، تالس که با عنوان بنیانگذار فلسفه یونانی از او یاد میشود، این ماده را تنها بلوک بنیادی ساختار ماده میدانست:
آن آب است که حالتهای گوناگونی به خود میگیرد، زمین، جو، آسمان، کوهها، خدایان و انسانها، جانوران و پرندگان، علف و درختان و جاندارانی به کوچکی کرمها، مگسها و مورچهها را تشکیل میدهد. همه اینها حالتهایی از آب هستند. پس بر روی آب تمرکز کنید!
پس از دو قرن، ارسطو این ماده را به عنوان یکی از چهار عنصر اساسی ماده همراه با خاک، هوا و آتش در نظر گرفت. این عقیده که آب، عنصری اساسی است بیش از 2000 سال دوام داشت تا اینکه آزمایشها در نیمه دوم قرن هجدهم نشان داد که آب یک ترکیب است و از عنصرهای هیدروژن و اکسیژن ساخته شده است.
این ماده بر روی سطح زمین، بیشتر در اقیانوسها به میزان ۹۷/۲۵ درصد و کلاهکهای یخی قطبی و یخچالها در حدود ۲/۰۵ درصد یافت میشود و بقیه در دریاچههای آب شیرین، رودخانهها و آبهای زیر زمینی وجود دارد. از آنجایی که جمعیت بر روی زمین رشد میکند و تقاضا برای این مایع در حال فزونی است، تصفیه و بازیابی آن بسیار مهم شده است.
جالب است بدانید خلوص آب مورد نیاز برای استفاده صنعتی اغلب بیشتر از خلوص مورد نیاز برای مصرف روزانه انسانها است. برای نمونه، آب استفاده شده در دیگهای پرفشار میبایست خلوص کمتر از ۹۹/۹۹۹۹۹۸ درصد نداشته باشد. چون آب دریا دارای مقدار زیادی نمک حل شده است، برای استفادههای بیشتر میبایست نمکزدایی شود.
ساختار آب
در ادامه، ساختار این ماده را مورد بررسی قرار میدهیم. پیشنهاد میکنیم برای بررسی بیشتر خواص فیزیکی و شیمیایی آب و بررسی نحوه اندازهگیری کیفیت و آلایندههای آن، فیلم آموزش فرادرس که در ادامه آورده شده است را مشاهده کنید.
آب مایع
مولکول این مایع از دو اتم هیدروژن ساخته شده است که هر دو با یک پیوند شیمیایی به یک اتم اکسیژن متصل هستند. بیشتر اتمهای هیدروژن دارای هستهای با یک پروتون هستند. دو ایزوتوپ دیگر آن یعنی دوتریم و ترتیُم، هستههایی دارند که علاوه بر پروتون، به ترتیب دارای یک و دو نوترون هستند و به مقدار بسیار بسیار کم در آب یافت میشوند. دوتریم اکسید که آب سنگین نامیده میشود، در تحقیقات شیمیایی اهمیت دارد و به عنوان تعدیل کننده نوترون در راکتور (واکنشگاه) هستهای به کار میرود.
هر چند فرمول شیمیایی این مایع، ساده به نظر میرسد، اما خواص فیزیکی و شیمیایی پیچیدهای از خود نشان میدهد. برای نمونه، نقطه ذوب آن، صفر درجه سانتیگراد و نقطه جوش آن، ۱۰۰ درجه سانتیگراد، بسیار بالاتر از میزان انتظار در مقایسه با ترکیبهای مشابه، مانند هیدروژن سولفید و آمونیاک است. شکل جامد آن، یخ، چگالی کمتری از حالت مایع دارد که خاصیت غیرمنتظره دیگری به شمار میآید. ریشه این خاصیت را باید در ساختار الکترونی مولکول این ماده جستجو کرد.
مولکول این مایع به صورت خطی نیست اما خمیدگی آن هم ویژه است. دواتم هیدروژن بهاتم اکسیژن با زاویهای برابر ۱۰۴/۵ درجه، متصل هستند.
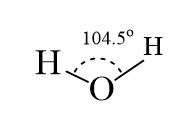
فاصله O-H (طول پیوند) برابر ۹۵/۷ پیکومتر، است. چون اتم اکسیژن الکترونگاتیوتر از اتم هیدروژن است، پیوندهای O-H در مولکول آب، قطبی هستند، چنانکه اتم اکسیژن مقداری بار جزئی منفی (δ-) و اتمهای هیدروژن مقداری بار جزئی مثبت (δ+) دارند.
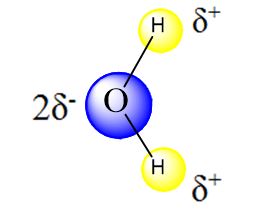
اتمهای هیدروژن در مولکولهای آب، با نواحی دارای چگالی الکترونی زیاد، برهمکنش میکنند و میتوانند اتصالهای ضعیفی موسوم به پیوندهای هیدروژنی را با آن نواحی برقرار کنند. این بدان معنی است که اتمهای هیدروژن در یک مولکول آب، با جفتالکترونهای ناپیوندی بر روی اتم اکسیژنِ مولکول دیگر، برهمکنش دارند. به نظر میرسد که ساختار آب مایع از گرد هم آمدن مولکولهای آن و تشکیل و گسست مداوم این برهمکنشها به وجود میآید. همچنین این پدیده سبب خاصیتهای غیرمنتظره دیگر این ماده مانند گرانروی (ویسکوزیته) و کشش سطحی زیاد آب میشود. ساختار لوویس آب را میتوان به شکل زیر نشان داد.
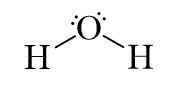
هر جفت نقطه نشاندهنده جفت الکترونهای ناپیوندی است که تنها بر روی اتم اکسیژن حضور دارند. همچنین این وضعیت را میتوان با قرار دادن مولکول آب، درون یک مکعب نشان داد.
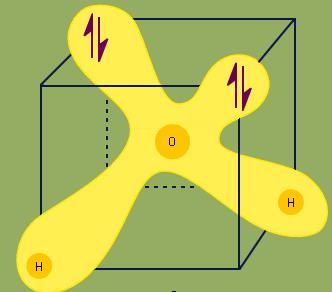
هر کدام از نشانهای ↑↓ مربوط به یک جفتالکترون ناپیوندی است. این ساختار الکترونی منجر به تشکیل پیوندهای هیدروژنی بین مولکولهای این ماده میشود.

ساختارهای یخ
در حالت جامد (یخ)، برهمکنشهای بین مولکولی منجر به ساختاری بسیار منظم اما سست میشود که در آن هر اتم اکسیژن با چهار اتم هیدروژن احاطه شده است. دو اتم هیدروژن هیدروژن با پیوندهای کووالانسی به اتم اکسیژن متصل و دو اتم دیگر (با فاصله بیشتر)، هیدروژنهایی هستند که به جفتالکترونهای ناپیوندی اکسیژن نزدیک هستند.
این ساختار باز سبب میشود چگالی جامد، کمتر از حالت مایع شود، اگر ساختار منظم آن به گونه جزئی بشکند، مولکولهای این ماده میتوانند به طور متوسط به هم نزدیکتر شوند. وقتی این مایع، منجمد میشود، ساختارهای گوناگونی بسته به شرایط بوجود میآیند. نُه حالت مختلف یخ شناخته شدهاند که میتوانند بسته به تغییر در شرایط دما و فشار خارجی به یکدیگر تبدیل شوند.
اهمیت ساختار آب مایع
حالت مایع آب، ساختار بسیار پیچیدهای دارد که بدون شک ارتباط قابل توجهی با مولکولهای آن دارد. پیوند هیدروژنی گسترده بین مولکولها در مایع سبب بالا رفتن مقدار خاصیتهایی مانند گرانروی (ویسکوزیته)، کشش سطحی و نقطه جوش میشود که از مقدار مورد انتظار برای مولکولی به این کوچکی بیشتر است.
برای نمونه، بر اساس اندازه مولکولهای آن، از این ماده انتظار میرود نقطه جوشی پایین و نزدیک به ۲۰۰ درجه سانتیگراد زیر نقطه جوش مشاهده شده را داشته باشد. بر خلاف حالتهای چگالتر ماده (جامد و مایع) که وابستگی زیادی بین مولکولهای آن مشاهده میشود، فاز گازی (بخار) وابستگی به نسبت کمتری بین مولکولهای آب دارد و فاصله مولکولها از هم بیشتر است.
قطبی بودن مولکول آب، نقش بزرگی در امکان حل شدن ترکیبهای یونی در آن و تشکیل محلولهای آبی بازی میکند. اقیانوسهای روی زمین دارای مقدار زیادی از نمکهای حل شده هستند که منبع طبیعی بزرگی برای آنها است. افزون بر این، صدها واکنش شیمیایی که در هر لحظه در بدن جانداران برای زنده نگه داشتن آنها اتفاق میافتد، همگی در محلولهای آبی انجام میشوند. همچنین، توانایی طعم دادن به غذاهایی که میپزیم با حل شدن موادی مانند شکر و نمک در این ماده امکان پذیر است.
اگر چه حل شدن مواد در آب، فرایندی بسیار پیچیده است، برهمکنش بین مولکولهای قطبی این حلال و ماده حلشونده در آن نقش بزرگی بازی میکنند. وقتی یک جامد یونی در آب حل میشود، انتهای مثبت مولکولهای آب به سمت آنیونها (یونهای منفی) قرار میگیرند، در حالی که انتهای منفی مولکولها به سمت کاتیونها (یونهای مثبت) قرار میگیرند. این فرایند آبپوشی نامیده میشود. آبپوشی یونها در آب سبب تفکیک و حل شدن آنها میشود. در فرایند انحلال، نیروهای جاذبه قوی بین یونهای مثبت و منفی در جامد با برهمکنشهای قوی بین یون- آب، جایگزین میشوند.
وقتی مواد یونی در این ماده حل شوند، به اجزای خود که کاتیونها و آنیونهای مجزا هستند، تفکیک خواهند شد. برای نمونه، وقتی سدیم کلرید (NaCl) در آب حل میشود، محلول حاصل دارای یونهای مجزای و است.
در این معادله، (s) نشاندهنده حالت جامد و (aq) مخففی برای «Aqueous» است که نشان میدهد یونها آبپوشی شدهاند، به این معنی که تعدادی از مولکولهای آب به آنها چسبیدهاند. همچنان که سدیم کلرید حل میشود، چهار مولکول آب، یون سدیم را میپوشانند (عدد آبپوشی چهار است). درست در بیرون این کره داخلی آبپوشی، منطقهای هست که مولکولهای آب، به گونهای جزئی با حضور یون آبپوشیده مرتب شدهاند. این ناحیه به گونه جزئی منظم، با ناحیه توده آب مایع مخلوط است.
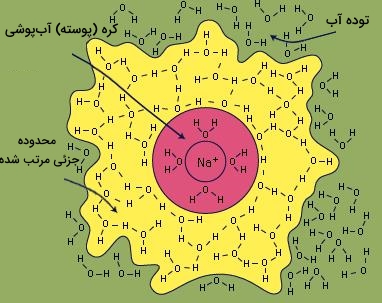
به طور کلی، با چگالی بار بزرگتر (نسبت بار به سطح) یک یون، عدد آبپوشی آن بزرگتر خواهد شد. به عنوان یک قاعده، یونهای منفی، اعداد آبپوشی کمتری نسبت به یونهای مثبت دارند زیرا تراکم بیشتر زمانی اتفاق میافتد که اتمهای هیدروژن مولکولهای آب، به سمت آنیونها جهتگیری میکنند.
بسیاری از ترکیبهای غیریونی نیز در آب حل میشوند. برای نمونه، اتانول ، الکل حاصل از تخمیر قندها، بسیار در آب، محلول است و درصد قابل توجهی از آن را همراه با ترکیبهای دیگر تشکیل میدهد. اتانول به دلیل ساختارش در این حلال، حل میشود. مولکول، مشابه با آب، دارای یک پیوند قطبی است و اجازه برهمکنش مؤثر با حلال را میدهد.
ترکیبهای فراوانی وجود دارند که به هیچ وجه در این مایع حیات حل نمیشوند. چربی حیوانی برای نمونه، در آب خالص نامحلول است زیرا طبیعت غیر قطبی مولکولهای چربی، آن را با مولکولهای قطبی آب، ناسازگار میکند. به طور کلی، ترکیبهای قطبی و یونی در آب حل میشوند. یک راه مهم برای تشخیص اینکه دو ترکیب قابل حل در یکدیگر هستند (تشکیل محلول میدهند)، این قاعده است که هر ترکیبی شبیه خود را حل میکند. این بدان معنی است که دو ماده قطبی به احتمال زیاد تشکیل محلول میدهند و همچنین دو ماده غیر قطبی نیز ممکن است در یکدیگر حل شوند.
رفتار و خواص
در ادامه متن، رفتار و خواص این ماده شگفتانگیز را بررسی میکنیم.
آب در دماها و فشارهای بالا
ماهیت توانایی این ماده برای رفتار به عنوان یک حلال قطبی (ماده حلکننده)، در دما و فشار بالا، دچار تغییر میشود. هرقدر آب، گرمتر میشود، به نظر میرسد مولکولهای آن بیشتر با مولکولهای ناقطبی برهمکنش میکنند. برای نمونه، در دمای ۳۰۰ درجه سانتیگراد و فشار بالا، خاصیت حلکنندگی آب بسیار شبیه به استون میشود که یک حلال آلی رایج است.
آب در ورای دما و فشار بحرانیاش (374 درجه سانتیگراد و ۲۱۸ اتمسفر) رفتار نامعمول و ویژهای از خود نشان میدهد. بالاتر از دمای بحرانی، تفاوت بین حالتهای مایع و گازی آب از بین میرود و تبدیل به یک «سیال فوق بحرانی» (Supercritical Fluid) میشود که چگالی آن میتواند از حالت شبیه به مایع تا حالت شبیه به گاز بر اساس تغییر دما و فشار آن تغییر کند.
اگر چگالی آب فوق بحرانی به اندازه کافی بالا باشد، ترکیبهای یونی را به آسانی حل میکند که برای آب معمولی هم به همین صورت است، اما به گونهای تعجب آور، این سیال فوق بحرانی همچنین میتواند به آسانی مواد غیرقطبی را در خود حل کند که آب معمولی توانایی انجام آن را ندارد. به دلیل توانایی آن در حل کردن مواد غیرقطبی، از این سیال به عنوان محیط احتراق برای از بین بردن پسابهای سمی بهره میگیرند.
برای نمونه، پسابهای آلی میتوانند با اکسیژن در آب فوق بحرانی با چگالی مناسب مخلوط و در سیال سوزانده شود. شعله در واقع «داخل آب» (Underwater) میسوزد. اکسایش در این سیال فوق بحرانی میتواند برای از بین بردن ترکیبهای آلی خطرناک و گونهگون مورد بهرهگیری قرار گیرد، چرا که واکنشگاه آب فوق بحرانی، سربسته است و بنابراین هیچ آلایندهای از آن وارد جو نمیشود.
خواص فیزیکی
آب، چندین ویژگی مهم فیزیکی دارد. این ویژگیها آشنا هستند چرا که آب را به گونه گسترده دیدهایم، اما بیشتر خاصیتهای فیزیکی آب بیقاعده هستند. با توجه به جرم مولی کم مولکولهای سازنده آن، آب مقدارهای نامعمول و زیادی برای گرانروی، کشش سطحی، گرمای تبخیر و آنتروپی تبخیر دارد که همه آنها را میتوان به برهمکنشهای گسترده از گونه پیوندهای هیدروژنی در آب مایع دانست. ساختار باز یخ که اجازه برقراری پیوند هیدروژنی را به شکلی متفاوت میدهد، توصیف کننده این نکته است که چرا آب جامد چگالی کمتری از آب مایع دارد که خاصیتی نامعمول در میان مواد رایج است.
خواص شیمیایی
در ادامه متن، خواص شیمیایی این ماده و واکنشهای مختلف در آن، بررسی میشوند.
واکنشهای اسید و باز
آب در واکنشهای شیمیایی گونهگونی شرکت میکند. یکی از مهمترین ویژگیهای شیمیایی آب، توانایی رفتار آن چه در نقش یک اسید (یک پروتون دهنده) و چه در نقش یک باز (یک پذیرنده پروتون) است که به آن ماهیتی همانند ترکیبهای آمفوتر (با تمایل ترکیب با اسید و باز) میدهد. این رفتار را به گونهای بسیار واضح و روشن در «خود یونش» (Autoionization) آب میتوان مشاهده کرد:
\begin{equation}\mathrm{H}_{2} \mathrm{O}(\mathrm{l})+\mathrm{H}_{2} \mathrm{O}(\mathrm{l}) \rightleftarrows \mathrm{H}_{3} \mathrm{O}^{+}(\mathrm{aq})+\mathrm{OH}^{-}(\mathrm{aq})\end{equation}
که (l) نشان دهنده حالت مایع، (aq) نشان دهنده گونههای حل شده در آب و پیکان دوطرفه نشان دهنده واکنش است که میتواند در هر دو جهت رفت و برگشت انجام گیرد تا شرایط تعادل ایجاد شود. در دمای ۲۵ درجه سانتیگراد، غلظت پروتون هیدراته (یون که به آن یون هیدرونیوم هم گفته میشود) در آب است که M نشان دهنده غلظت برحسب مول بر لیتر است. از آنجایی که یک یون در برابر هر یون تولید میشود، غلظت نیز در 25 درجه سانتیگراد برابر است. در آب و دمای 25 درجه سانتیگراد، حاصلضرب غلظت یونهای و همیشه میبایست برابر با باشد:
که نشان دهنده غلظت پروتون هیدراته است که پیشتر به آن با نام یون هیدرونیوم اشاره شد و نیز غلظت یون هیدروکسید است که بر حسب مول بر لیتر بیان میشوند.
وقتی یک اسید - ترکیبی که میتواند یونهای تولید کند - در آب حل میشود، هر دو اسید و آب ایجاد کننده یونهای ، محلول هستند. این منجر به شرایطی میشود که غلظت بیش از است. از آنجایی که باید همیشه رابطه بالا در دمای ۲۵ درجه سانتیگراد برقرار باشد، غلظت کمتر از میزان تعادلی ذکر شده در بالا میشود.
یکی از مهمترین روشهای مشخص کردن خصلت اسیدی یک محلول، استفاده از pH است که با رابطه زیر غلظت یون هیدروژن تعیین میشود:
که نماد «» نشان دهنده لگاریتم بر پایه 10 است. در آب خالص که است، pH برابر 7/0 میشود. وقتی یک باز - ماده پذیرنده یون پروتون - در آب حل میشود، غلظت کاهش مییابد و کمتر از یون میشود. با توجه به این نکته، یک محلول زمانی بازی است که pH آن، بزرگتر از ۷ باشد.

واکنشهای اکسایش-کاهش
هنگامی که یک فلز فعال مانند سدیم در تماس با آب مایع قرار میگیرد، یک واکنش به شدت گرماده رخ میدهد که همراه با شعله سوختن گاز هیدروژنِ به وجود آمده از واکنش است.
این نمونهای از یک واکنش اکسایش- کاهش است، واکنشی که در آن الکترونها از یک اتم به دیگری انتقال مییابند. در این حالت، الکترونها بین اتمهای سدیم - که تشکیل یون میدهد - و مولکولهای آب جابجا میشوند که سبب تولید گونههای هیدروژن گازی و یونهای میشود. دیگر فلزهای قلیایی نیز واکنشهای مشابهی با آب میدهند. فلزهای کمتر فعال به آهستگی با آب واکنش میدهند. برای نمونه، آهن با سرعت کم با آب واکنش میدهد اما با سرعت بسیار بیشتری با بخار بسیار داغ وارد واکنش میشود که سبب تولید اکسید آهن و گاز هیدروژن میشود.
\begin{equation}3 \mathrm{Fe}(\mathrm{s})+4 \mathrm{H}_{2} \mathrm{O}(\mathrm{g}) \stackrel{\mathrm{H}_{2} \mathrm{O}}\rightarrow \mathrm{Fe}_{3} \mathrm{O}_{4}(\mathrm{s})+4 \mathrm{H}_{2} \mathrm{O}(\mathrm{g})\end{equation}
فلزهای نجیبتر مانند طلا و نقره به گونه کلی با آب هیچ واکنشی نشان نمیدهند.
این مطلب توسط نویسنده مهمان، «وحید نوروزی چرندابی»، نوشته شده است.












سلام مطالب عنوان شده بسیار جالب و شگفت انگیز بود. سوالی همیشه برای من وجود داشته این هست که ایا ترکیب اتم ها بطور مثال اکسیژن و هیدروژن و بوجود آمدن یک مولکول اب توسط انسان امکان پذیر است؟ و ایا میتوان گفت حداقل مقداری از آبی که روی زمین وجود دارد از ترکیب این دو اتم پر روی همین سیاره بوجود آمده؟
باتشکر
ببخشید اگه طلا و نقره را در سیال فوق بحرانی بگذاریم اتفاقی میافتد یا چون غیر قطبی و قطبی را حل میکند در درون خودش
با سلام
چگالش واژه ای فارسی و مترادف condensation است و در متن نخست به درستی استفاده شده است. تبدیل بخار آب موجود در جو به باران همراه با چگال تر شدن آن است و از نظر واژه شناسی بهره گیری از آن صحیح است.
عالی بود
خیلی کامل و جامع بود
دستت شما درد نکنه
سلام ممنون از مطلب مفیدتون
در این خط:
انتقال آن از مسیر اتمسفر بین اقیانوسها و منطقههای خشک انجام شود و با چگالش آن به شکل باران، بسیاری از گیاهان و حیات وحش را سیراب کند.
به جای میعان نوشتید چگالش که درست نیست
با سلام؛
از توجه شما سپاسگزاریم. متن اصلاح شد.
با تشکر