کربوکاتیون چیست؟ – به زبان ساده
یک کربوکاتیون به یونی میگویند که در آن، اتم کربن دارای بار مثبت و ۳ پیوند باشد. در حقیقت، نام کربوکاتیون را میتوان به صورت کاتیون کربن نیز بیان کرد. در گذشته، به جای نام کربوکاتیون از نام «یون کربونیوم» (Carbonium Ion) استفاده میکردند. از سادهترین نمونههای کربوکاتیون میتوان به متنیوم ، متانیوم و اتانیوم () اشاره کرد. برخی از کربوکاتیونها ممکن است بیش از دو بارِ مثبت داشته باشند که نمونهای از این کربوکاتیونها، اتیلن دیکاتیون با فرمول است.
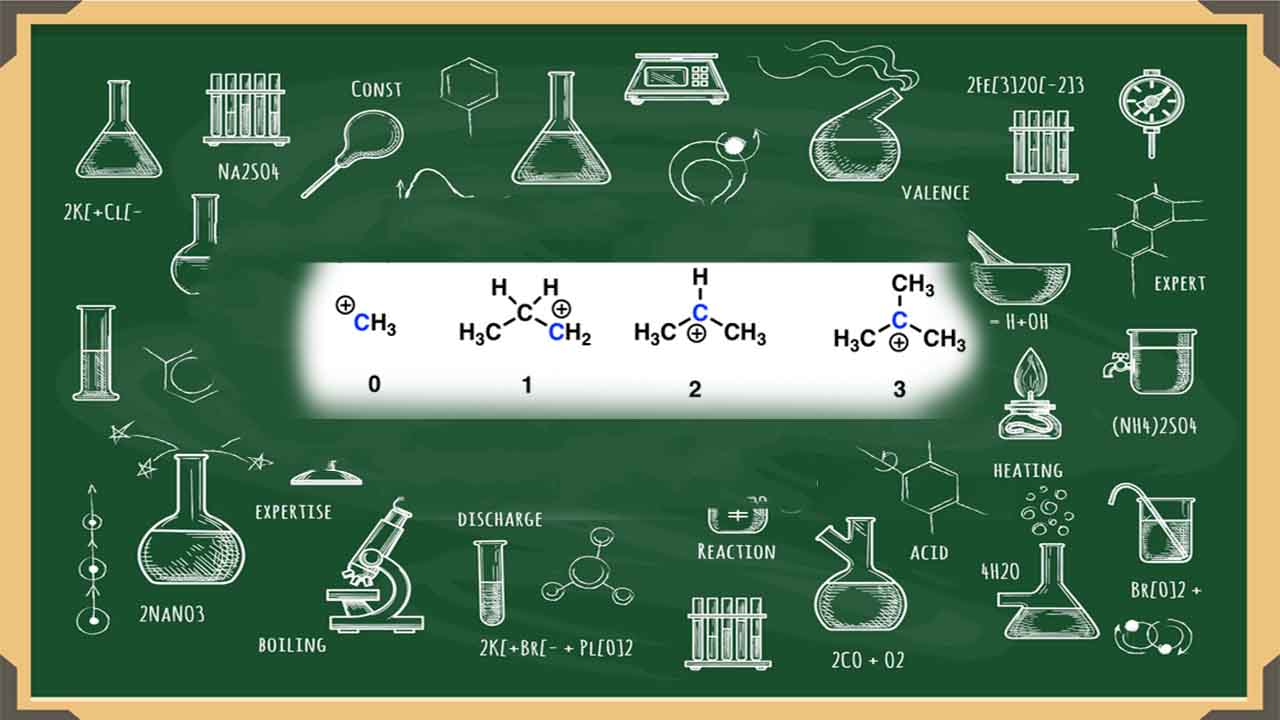

تعریف کربوکاتیون
تا اوایل دهه ۱۹۷۰، به تمامی کربوکاتیونها نام یون کربونیوم اطلاق میشد اما امروزه، یک کربوکاتیون به اتم کربنی میگویند که بار مثبت داشته باشد و بسته به ظرفیت اتم باردار، در دو دسته اصلی طبقهبندی میشود:
- در یون کربِنیوم
- یا در یون کربانیوم
مشخصههای کلی یک کربوکاتیون
مشخصههای مختلفی را میتوان در خصوص کربوکاتیونها بیان کرد. به طور کلی، کربوکاتیونها به دلیل کامل نبودن تعداد الکترون لایه ظرفیت، بسیار واکنشپذیر و ناپایدار هستند. به بیان سادهتر، کربوکاتیونها در لایه آخر خود هشت الکترون ندارند و بنابراین، قاعده اوکتت را تکمیل نمیکنند.
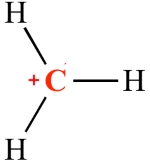
هیبریداسیون کربوکاتیون
در یک کربوکاتیون، هیبریداسیون کربن به صورت و شکل آن سهضلعی مسطح است. همچنین، در این ساختار یک اوربیتال p خالی وجود دارد که بیانگر طبیعت کربوکاتیونها یعنی الکترون کمتر است. به عبارت دیگر، اتم کربن در کربوکاتیونها دارای ۶ الکترون در لایه ظرفیت خود و فقیر از الکترون هستند و میتوان نام الکتروفیل (الکتروندوست) را به آنها اختصاص داد. کربوکاتیون در واکنشهای حذفی و واکنشهایی با مکانیسم شرکت میکند.
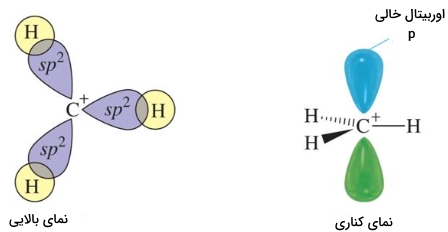
دسته بندی کربوکاتیونها
کربوکاتیونهای مختلف بر اساس تعداد گروههای کربنی متصل به اتم کربن، طبقهبندی میشوند. بسته به تعداد اتمها (گروههای کربنی) متصل به اتم کربن، کربوکاتیونها را به دستههای متیل، کربوکاتیون نوع اول، دوم و سوم تقسیمبندی میکنند.
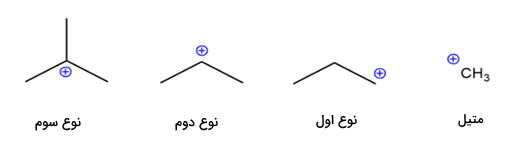
- اگر یک پیوند دوگانه کربن-کربن در کنار اتم کربن با بار مثبت داشته باشیم،به آنها کربوکاتیونهای «آلیلی» (Allylic) میگویند.
- به طور مشابه، اگر کربن با بار مثبت، به یک پیوند دوگانه متصل شده باشد، این نوع از کربوکاتیونها را با نام کربوکاتیونهای وینیلی میشناسند. تحت این شرایط، هیبریداسیون کربن مثبت به صورت sp و شکل آن خطی خواهد بود.
- هرگاه کربن مثبت، بخشی از یک حلقه بنزنی باشد، به کربوکاتیونهای حاصل، کربوکاتیونهای آریل میگویند.
- اگر کربن مثبت، دقیقا بعد از یک حلقه بنزنی قرار بگیرد، نام کربوکاتیون بنزیلی به آن اطلاق میشود.
علاوه بر انواع ذکر شده در بالا، انواع دیگری از کربوکاتیونها موسوم به کربوکاتیونهای هرمی وجود دارند. در این نوع از کربوکاتیونها، یونها شامل یک اتم کربن هستند که به طور معمول تمایل دارند در راس یک هرم چهار یا پنجوجهی قرار بگیرند. یون هرمی چهاروجهی شامل بار و یون هرمی پنجوجهی شامل بار خواهد بود.
نحوه تشکیل کربوکاتیونها
کربوکاتیونها به کمک یکی از دو روش اصلی زیر تشکیل میشوند.
- گسست پیوند کربن
- واکنش افزایشی الکتروندوست
گسست پیوند کربن
هرگاه بین کربن و اتمهای متصل به آن، گسستی رخ بدهد، «گروه ترککننده» (Leaving Group)، الکترونهای اشتراکی را از آن خود میکند و اتم کربنی فقیر از الکترون به جای میگذارد. در نتیجه، بار مثبتی به همراه تشکیل کربوکاتیون ایجاد میشود. هرقدر تمایل گسست پیوند یا تشکیل کربوکاتیون پایدارتر، بیشتر باشد، انرژی اکتیواسیون کمتری خواهیم داشت. در بسیاری از واکنشهای شیمی همچون مکانیسمهای و ، کربوکاتیون به صورت فرآورده فرعی واکنش، به تولید میرسد.
واکنش افزایشی الکترون دوست
در یک واکنش افزایشی الکتروندوست، یک الکتروفیل به نقطهای غیراشباع (پیوند دوگانه یا سهگانه) حمله میکند. در نتیجه این اتفاق، پیوند پای، شکسته و یک کربوکاتیون تشکیل میشود. در تصویر زیر، واکنش افزایشی الکتروندوست، به کمک واکنش (یک الکتروندوست) با پروپن، آورده شده است:
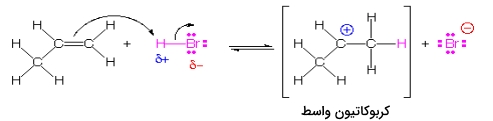
توجه داشته باشید که تشکیل کربوکاتیون نوع دوم بر تشکیل کربوکاتیون نوع اول، برتری دارد چراکه کربوکاتیون نوع دوم، به دلیل وجود رزونانس، پایدارتر خواهده بود. این امر همچنین از قانون «مارکونیکوف» (Markonikov) پیروی میکند. چنین واکنشهای افزایشی الکتروندوستی را میتوان در آلکنها، آلکینها و حلقههای بنزنی مشاهده کرد.
پایداری کربوکاتیونها
همانطور که میدانیم، کربوکاتیونها به علت کمبود الکترون و دارا بودن اوربیتال خالی، بسیار واکنشپذیر هستند. بنابراین، پایداری آنها به تکمیل قاعده اوکتت و دریافت الکترونها بستگی دارد. بر اساس سه فرآیندزیر، میتوان به بررسی پایداری کربوکاتیونها پرداخت:
اضافه شدن هسته دوست
همانطور که گفته شد، کربوکاتیونها برای تکمیل قاعده اوکتت به الکترون نیاز دارند. بار مثبت روی کربوکاتیونها از طریق اضافه شدن یک هستهدوست، پایدار میشود و بنابراین، در اثر این اتفاق، پیوند کووالانسی تشکیل و موجب پایداری کربوکاتیونها خواهد شد. به هنگام بررسی پایداری کربوکاتیونها، این روش به عنوان معمولترین روش به شمار میآید چراکه کربوکاتیونها بسیار واکنشپذیر هستند و در نتیجه، حتی یک هستهدوست ضعیف نیز امکان اتصال به کربوکاتیون را دارد.
تشکیل پیوند پای
کربوکاتیونها برای تکمیل قاعده اوکتت و حذف بار مثبت خود میتوانند از هیدروژن نزدیک به خود، الکترون جذب کنند که در اثر این اتفاق، یک پیوند پای جدید تشکیل خواهد شد. به طور کلی، اتم هیدروژن باید به کمک یک باز حذف شود. به دلیل واکنشپذیری بالای کربوکاتیونها، وجود یک باز ضعیف همچون آب یا یون ید نیز میتواند فرآیند «دپروتوناسیون» (Deprotonation) یا پروتونزدایی را انجام دهند. زمانیکه چنین فرآیندی انجام شود، دو نوع فرآورده تولید میشوند که فرآورده بیشتر، پایدارتر خواهد بود.
بازآرایی
با جابجایی الکترون پیوندی کربوکاتیونها در بین اتمهای مجاور، کربوکاتیون پایدارتری تشکیل خواهد شد. به طور مثال، اگر یک کربوکاتیون نوع اول، به کربوکاتیون نوع دوم تبدیل شود، برای پایداری کربوکاتیون، بازآرایی، اولویت خواهد داشت. دلیل این امر نیز بسیار ساده است زیرا کربوکاتیونهای نوع دوم، پایداری بیشتری نسبت به کربوکاتیونهای نوع اول دارند. در ادامه قصد داریم تا به بررسی انواع مختلف بازآرایی کربوکاتیونها بپردازیم.
جابجایی هیدرید
در این بازآرایی، هیدروژن از کربن اول به کربن دوم جابجا میشود. در نتیجه، کربوکاتیون از نوع اول به نوع دوم تبدیل خواهد شد و ساختار پایدارتری خواهیم داشت.
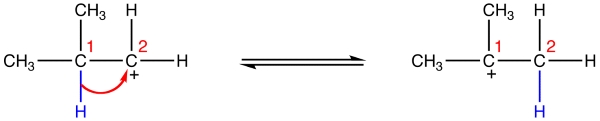
جابجایی متیل
در این حالت، گروه متیل، با جابجایی به طرف کربن، سبب تشکیل کربوکاتیون پایدارتر نوع دوم میشود.
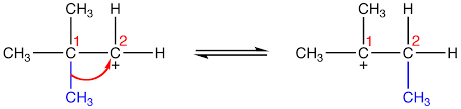
جابجایی فنیل
گروه فنیل میتواند در اثر جابجایی، کربوکاتیون پایدارتر نوع دوم یا سوم را ایجاد کند. خوب است بدانید که جابجایی فنیل، نسبت به جابجایی متیل، اولویت بیشتری دارد.

عوامل موثر بر پایداری کربوکاتیون
عوامل موثر بر پایداری کربوکاتیونها را در ادامه بررسی خواهیم کرد.
رزونانس
با افزایش رزونانس، پایداری کربوکاتیونها نیز افزایش پیدا میکند. هرقدر تعداد ساختارهای رزونانس بیشتر باشند، پایداری کربوکاتیونها نیز بیشتر خواهد بود. دلیل این امر را باید در متمرکز نبودن بار مثبت ذکر کرد.در اثر این اتفاق، کمبود الکترون (فقر الکترونی) افزایش پیدا خواهد کرد و سبب افزایش پایداری کربوکاتیون خواهد بود.
زمانی که این اثر را با واکنش جانشینی مقایسه کنیم، تاثیر رزونانس، عامل مهمتری در پایداری کربوکاتیونها به شمار میآید. در نتیجه، ساختارهای شامل رزونانس، نسبت به سایر ساختارها، پایداری بیشتری دارند. کربوکاتیون سیکلوپروپان، به دلیل وجود رزونانس، پایداری بسیاری بالایی دارد و به همین دلیل، کربوکاتیون تریسیکلو پروپان، پایدارترین نوع از کربوکاتیونها به شمار میآید.
اثر القایی و فوق مزدوج شدن
افزایش جانشینی موجب افزایش «فوق مزدوج شدن» (Hyperconjucation) و به دنبال آن افزایش پایداری خواهد شد. هرقدر میزان فوق مزدوج شدن بیشتر باشد، پایداری نیز بیشتر خواهد بود. پایداری کربوکاتیونها به تعداد گروههای کربنی متصل به کربن مثبت وابسته است.
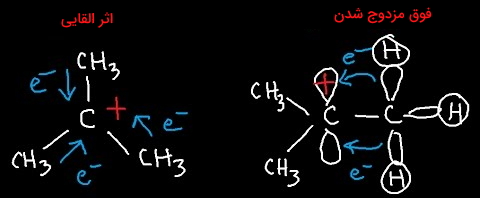
الکترونگاتیوی
الکترونگاتیوی نشاندهنده ظرفیت یک اتم برای جذب الکترون است. هرقدر الکترونگاتیوی بیشتری در یک اتم داشته باشیم، به همان میزان نیز جاذبه الکترونها به طرف آن اتم بیشتر خواهد بود. بنابراین، الکترونگاتیوی کربن با بار مثبت، به طور مستقیم بر پایداری کربوکاتیونها تاثیر دارد.
با مقایسه الکترونگاتیوی مشاهده میکنیم هرقدر الکترونگاتیوی اتم کربن افزایش پیدا می کند، پایداری کربوکاتیونها کاهش پیدا میکند.
هیبریداسیون اتم کربن با بار مثبت در کربوکاتیونهای وینیلی به صورت است و الکترونگاتیوی آن بیشتر از هیبریداسیون کربن در کربوکاتیون آلکیل ذکر میشود. به همین دلیل، پایداری کربوکاتیونهای وینیلی نوع اول، کمتر از پایدار کربوکاتیونهای آلکیل نوع اول ذکر میشود. به همین شکل میتوان پایداری کمتر کربوکاتیونهای آریل را در مقایسه با پایداری کربوکاتیونهای آلکیل نوع دوم توضیح داد. به دلیل پایداری کم کربوکاتیونهای وینیل و آریل، این نوع از کربوکاتیونها را کمتر میتوان یافت کرد.
مثالهایی برای بررسی پایداری کربوکاتیونها
در ادامه، برای درک بهتر پایداری کربوکاتیون، چندین مثال ارائه میکنیم.
مثال ۱
کدامیک از ساختارهای زیر، کربوکاتیون پایدار به شمار میآیند؟
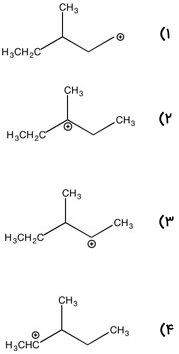
تصویر ۲ با توجه به اینکه کربوکاتیون نوع سوم است، پایداری بیشتری دارد.
مثال ۲
دو اتم کربن را در ترکیبات زیر در نظر بگیرید:

در کدامیک از حالتها، به ترکیب، هیدروژن اضافه خواهد شد؟
در حالت کربن نوع اول، امکان اضافه شدن هیدروژن وجود دارد چراکه در اثر این اتفاق، کربوکاتیون پایدارتر نوع دوم خواهیم داشت.
مثال ۳
کربوکاتیونهای زیر را بر طبق کاهش پایداری، مرتب کنید.
$$I. {C H } _ {3} - {C } ^ {+} {H } - {C H } _ {3} II. {CH } _ { 3}- {C } ^ {+} {H } - {O C H }_{3 III. {C H }_ {3} - { C } ^ {+} { H }- { C H } _ {2} - {O C H } _{3}$$
پاسخ به صورت زیر خواهد بود:
در ترکیب (II)، جفتالکترونهای ناپیوندی اکسیژن به پایداری کربوکاتیون کمک میکنند. ترکیب I، خاصیت فوق مزدوج شدگی بیشتری نسبت به ترکیب III دارد.
مثال ۴
کدامیک از کربوکاتیونهای زیر، بیشترین پایداری دارند:
ترکیب (I) دارای بیشترین پایداری است زیرا رزونانس بیشتری دارد. به عبارت دیگر، بار روی کربوکاتیون با وجود دو گروه فنیل، رزونانس و پایداری بیشتری خواهد داشت.













درود . در پرسش ۳ ، صورت سوال مشخص نیس .
با سلام؛
مورد ذکر شده در متن اصلاح شد.
با تشکر از همراهی شما با مجله فرادرس
سایتتون عااالیههه…واقعا دستتون درد نکنه…تمام چیزهایی که برام سواله به بهترین شکل توضیح میدید
سلام.پایدارترین کربوکاتیون برای خرید توی بازار چیه؟