آموزش فیزیولوژی عصب عضله – به زبان ساده + اتصال و انتقال پیام
فیزیولوژی بخشی از زیستشناسی است که فعالیت اندامها مختلف بدن و ارتباط ساختارهای آن را بررسی میکند. عصب مجموعهای از نورونها است که با انتقال پیام عصبی فعالیتهای بدن را کنترل میکند. عضلات سلولهای تحریکپذیر تمایزیافتهای هستند که در قلب به پمپ خون، در لوله گوارش به گوارش غذا و در اندامهای تحتانی به حرکت کمک میکنند. در این مطلب از مجله فرادرس فیزیولوژی عصب عضله را به همراه ارتباط این دو سیستم بدن و ساختارهای عملکردی آن توضیح میدهیم.
- نحوه انتقال پیام عصبی از طریق نورون تا عضله را خواهید آموخت.
- سازوکار انقباض عضلات اسکلتی و نقش پروتئینهای اکتین و میوزین را یاد میگیرید.
- عملکرد پمپها و کانالهای یونی در تولید و انتقال پیام عصبی را میآموزید.
- تفاوتهای ساختاری و عملکردی بین عضلات اسکلتی و صاف را خواهید شناخت.
- نقش کلسیم، کلمودولین و سیگنالینگ سلولی در انقباض عضله صاف را خواهید آموخت.
- کاربرد الکترومیوگرام در بررسی عملکرد عصب-عضله را خواهید شناخت.

فیزیولوژی عصب عضله چیست ؟
فیزیولوژی عصب عضله ارتباط بین فعالیتهای اعصاب و عضلات بدن را بررسی میکند. ساختار غشایی اعصاب، تشکیل پیام عصبی، انتقال پیام عصبی در اعصاب، انتقال پیام عصبی از اعصاب به ماهیچهها، ویژگیهای ساختاری و مولکولی فیبر ماهیچهای، تغییرات سلول ماهیچهای و مکانیسمهای انقباض ماهیچه فرایندهایی است که در فیزیولوژی عصب عضله توضیح داده میشود.
غشای عصب چیست ؟
نورونها سلولهای اصلی سیستم عصبی مرکزی و محیطی هستند. شکل این سلولها با سلولهای دیگر بدن تفاوت زیادی داشته و مکانیسمهای تقسیم میتوز در آنها غیرفعال شده است. اما ساختار غشایی آنها شبیه تمام سلولهای بدن در دو لایه فسفولیپید تشکیل شده است که برای تبادل مواد با محیط اطراف به پروتئینهای غشایی نیاز دارد. کانالهای ولتاژی (سدیم، پتاسیم و کلسیم)، کانالهای همیشهباز (سدیم و پتاسیم) و پمپ سدیم-پتاسیم سه ساختار غشایی نورون هستند که در فیزیولوژی عصب عضله نقش بسیار مهمی دارند.
کانال های ولتاژی عصب
کانالهای ولتاژی پروتئینهای عرض غشایی هستند و از یک دریچه فعالکننده و یک دریچه مسدودکننده تشکیل شدهاند. کنفورماسیون هر یک از این دریچهها با پتانسیل الکتریکی متفاوتی تغییر میکند. به همین دلیل کانالهای حساس به ولتاژ (پتانسیل الکتریکی) نام گذاری میشوند.
دریچه فعالکننده این کانالها در سطح خارجی غشای سلولی قرار دارد و کنفورماسیون بخشی از زنجیره پلیپپتیدی (توالی آمینواسیدهای مثبت آرژنین) آن در پاسخ به تغییرات پتانسیل الکتریکی غشا تغییر کرده و مسیری برای ورود یونها به سیتوپلاسم سلول باز میکند. دریچه مسدودکننده این کانالها در انتهای سیتوزولی کانال قرار دارد و تغییر کنفورماسیون آن مسیر ورود یونها را مسدود میکند.
تعداد زیادی کانال ولتاژی سدیم و پتاسیم در غشای نورون از دندریتها تا پایانه آکسون وجود دارد که در مراحل مختلف انتقال جریان الکتریکی نورون فعال میشوند. در نورونهای میلیندار این کانالها فقط در گرههای رانویه قرار دارند. اما تعداد کانالهای ولتاژی کلسیم در غشای پایانه آکسون از بخشهای دیگر بیشتر است و در اگزوسیتوز انتقالدهنده عصبی نقش دارد.
کانال های همیشهباز عصب
این کانالهای پروتئینهای عرض غشایی هستند که مسیری برای عبور مولکولهای آب، قطبی و یونها از غشای هیدروفوب و منفی ایجاد میکنند. بار الکتریکی و قطر بخش داخلی این کانال به یک یون مشخص اجازه عبور میدهد. کانالهای همیشهباز سدیم و پتاسیم در بخشهای مختلف غشای نورون قرار دارند و در پتانسیل استراحت غشا را تثبیت میکنند.
پمپ سدیم پتاسیم عصب
پمپ سدیم-پتاسیم ساختار پروتئینی چند زیرواحدی غشای نورونها است که از انرژی شیمیایی موجود در پیوند فسفات مولکول ATP برای تغییر کنفورماسیون و انتقال یونها خلاف جهت شیب غلظت استفاده میکند. جایگاه اتصال یونها و فعالیت آنزیمی در زیر دو زیرواحد آلفای این پمپ قرار دارد. دو زیرواحد بتا پروتئینهای عرض غشایی هستند که به حفظ ساختار پمپ در غشا کمک میکنند.
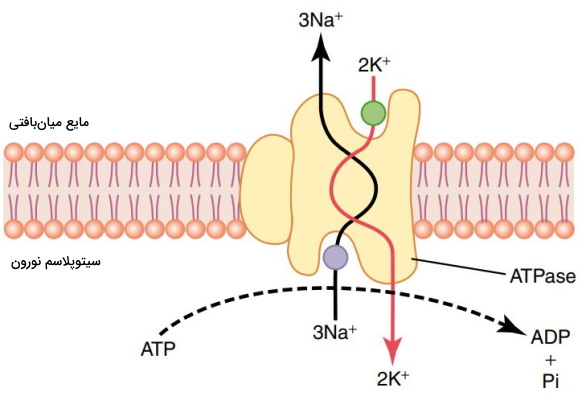
این پمپ با مصرف هر مولکول ATP دو یون سدیم را وارد سیتوپلاسم و سه یون سدیم را از سیتوپلاسم خارج میکند. این پمپ غلظت یونهای سدیم و پتاسیم و پتانسیل استراحت غشای نورون را تثبیت میکند. به همین دلیل در حالت استراحت پتانسیل الکتریکی درون سلول همیشه مثبتتر از مایع میانبافتی است.
پتانسیل الکتریکی غشای عصب
انتقال پیام عصبی و تمام وقایعی که در فیزیولوژی عصب عضله اتفاق میافتد به پتانسیل الکتریکی غشای عصب بستگی دارد. این پتانسیل الکتریکی به دلیل اختلاف غلظت شیمیایی (تعداد یون) یا الکتریکی یونها (بار الکتریکی مثبت یا منفی) در دو طرف غشا (سیتوپلاسم و مایع میانبافتی) ایجاد میشود. یون پتاسیم و سدیم دو ترکیب اصلی در ایجاد اختلاف غلظت الکتروشیمیایی غشای عصب هستند. غلظت یون سدیم در مایع میانبافتی عصب و غلظت یون پتاسیم در سیتوپلاسم این سلولها بیشتر است. در نتیجه هر یک از این یونها تمایل دارد بر اساس شیب غلظت (از غلظت بیشتر به کمتر) حرکت کند.
در شرایط طبیعی و حالت استراحت فیبر عصبی اختلاف پتانسیل الکتروشیمیایی بین سیتوپلاسم و مایع میانبافتی ۹۰- mV است. این اختلاف پتانسیل بهوسیله عوامل تغییردهنده نفوذپذیری غشای سلولی به کاتیونها و آنیونها تغییر میکند. افزایش کاتیونها و بار مثبت سیتوپلاسم منجر به تحریک سلول عصبی میشود. اما افزایش بار الکتریکی سیتوپلاسم به دلیل خروج کاتیونها یا ورود آنیونها منجر به مهار سلول عصبی میشود. در نتیجه غلظت یونها عامل کنترلی فیزیولوژی عصب عضله است.
آناتومی عضله اسکلتی
بافت عضله اسکلتی از کنار هم قرار گرفتن تعداد زیادی فیبرهای عضلانی ۱۰ تا ۸۰ میلیمتری تشکیل شده است. این فیبرهای بهوسیله چند لایه بافت پیوندی کنار هم قرار گرفته و بافت عضله اسکلتی را میسازند. اطراف هر فیبر عضله اسکلتی غشای پلاسمایی و لایهای از بافت پیوندی رشتهای به نام سارکولما وجود دارد.
این بافت پیوندی در دو طرف عضله با تاندونها یکی شده و عضله را به استخوان متصل میکند. هر فیبر ماهیچهای از تعداد زیادی میوفیبریل تشکیل شده که واحدهای عملکردی عضله را تشکیل میدهند و نقش مهمی در انقباض ماهیچه و فیزیولوژی عصب عضله دارند. آرایش پروتئینهای انقباضی در میوفیبریل سبب میشود این عضله زیر میکروسکوپ مخطط دیده شود. قبل از این در مطلب «ماهیچه اسکلتی چیست» از مجله فرادرس آناتومی و انواع حرکت عضله اسکلتی را توضیح دادهایم.
پروتئین های انقباضی عضله
میکروفیلامنتهای اکتین، مولکولهای میوزین، پروتئینهای صفحه Z، تیتین و تروپونین اسکلت پروتئینی میوفیبریلهای عضله را تشکیل میدهند. پروتئینهای Z صفحه طولی در سیتوپلاسم میوفیبریل تشکیل میدهد و غشای دو طرف میوفیبریلها متصل میشود. فاصله هر دو خط Z در عضله سارکومر نام دارد.
میکروفیلامنتهای اکتین از کنار هم قرار گرفتن مولکولهای G اکتین تشکیل میشود و جفت شدن آن با مولکولهای میوزین یکی از مراحل انقباض عضله است. در هر مولکول G اکتین یک جایگاه اتصال به سر میوزین و یک جایگاه اتصال به پروتئین ترومونین وجود دارد. تروپونین پروتئینی کروی با با سه زیرواحد C، I و T و مولکول تنظیمی فیزیولوژی عصب عضله است. اتصال کلسیم به زیرواحد C کنفورماسیون مولکول را تغییر میدهد. تروپومیوزین گروه دیگر مولکولهای تنظیمی اتصال اکتین و میوزین هستند که دور رشتههای اکتین میپیچند. نبولینهای رشتههای پروتئینی دیگری هستند که در اطراف رشتههای اکتین قرار دارند.
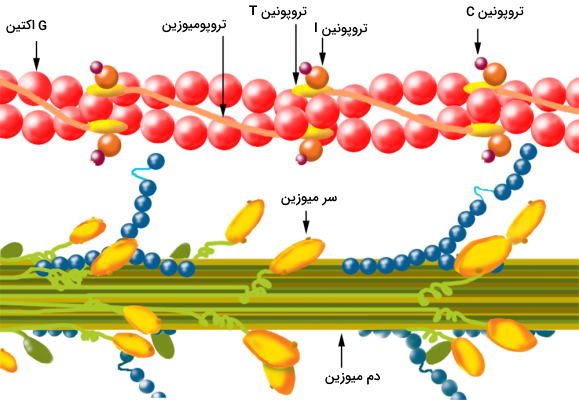
میوزینها مولکولهای پروتئینی در سلولهای مختلف هستند که در حرکات مولکولی سلول نقش دارند و به انها موتورپروتئین گفته میشود. میوزین II موتورپروتئینی است که در فیزیولوژی عصب عضله شرکت میکند. این مولکول از سه دومین سر، گردن و دم تشکیل شده است.
- دومین سر: جایگاه اتصال به مولکولهای اکتین و آنزیم ATPase در این بخش از مولکول قرار دارد و با هیدرولیز مولکولهای ATP از انتهای مثبت اکتین به انتهای منفی این فیلامنت حرکت میکند.
- دومین گردن: این بخش از میوزین سر را به دم متصل میکند و اهرمی برای انتقال نیروی ایجاد شده در سر به دم است. زنجیره سبک میوزین در این بخش قرار دارد و جایگاه تنظیمی مولکول است.
- دومین دم: این جایگاه بهوسیله پروتئینهای تیتین صفحه Z متصل شده و مثل فنری نیروی انقباضی را به این پروتئینها منتقل میکند.
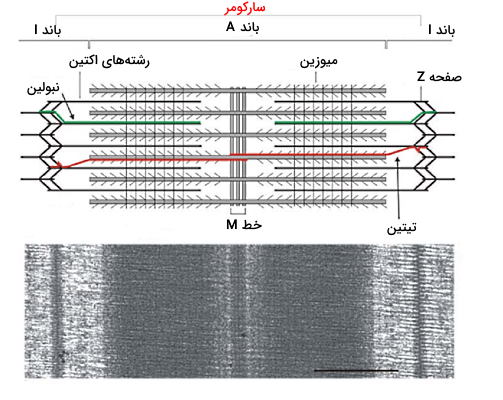
آرایش و تراکم متفاوت این پروتئینها در سارکومر سبب ایجاد باندهای تیره و روشن باند I، باند A، خط M و ناحیه H در بافت عضله اسکلتی میشود که اندازه آنها در حالت استراحت و انقباض عضله متفاوت است.
- باند A: باند A ناحیه تیره سارکومر و محل تجمع میکروفیلامنتها و مولکولهای میوزین است.
- باند I: باند I ناحیه روشن نزدیک دو خط Z انتهای سارکومر و محل تجمع میکروفیلامنتهای اکتین است.
- ناحیه H: بخش روشنی وسط باند A است که دوم مولکولهای میوزین در آن قرار دارند.
- خط M: خط M خطی تیره وسط ناحیه H است. این خط از رشتههای پروتئینی میومیوزین تشکیل شده که میوزین را به تیتین متصل میکند.
اندامک های عضله
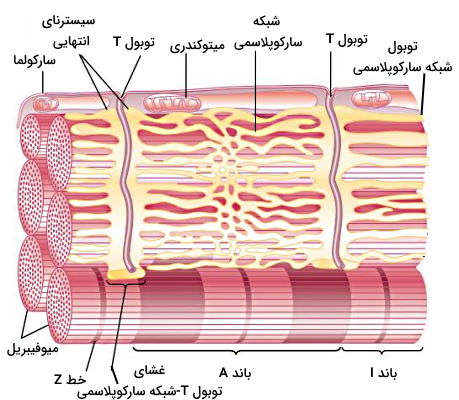
سارکوپلاسم مایعی با یونهای منیزیوم، فسفات و پتاسیم فراوان است که بین میوفیبریلهای فیبر ماهیچهای را پر میکند. تعداد زیادی میتوکندری در این مایع و نزدیک غشای هر میوفیبریل قرار دارد که ATP لازم برای انقباض ماهیچه را فراهم میکند.
شبکه اندوپلاسمی صاف گسترده یکی دیگر از اندامکهای سارکوپلاسم است که به نام شبکه سارکوپلاسمی گفته میشود. این اندامک از کیسهها (سیسترنای انتهایی) و لولههایی (توبولهای طولی) تشکیل شده است که کلسیم لازم برای انجام مکانیسم انقباض در فیزیولوژی عصب عضله را تامین میکند. تعداد کانالهای انتقال کلسیم به سیتوپلاسم در غشای سیسترنای انتهایی و تعداد کانالهای بازجذب کلسیم از سیتوپلاسم در غشای توبولهای طولی بیشتر است.
غشای سلول ماهیچهای چینخوردگیهایی دارد که لومن آن از مایع میانبافتی پر شده است و توبول T یا «توبول عرضی» (Transverse Tubules) نام دارد. این توبولها وارد میوفیبریل شده و دو طرف فیبر ماهیچهای را به هم متصل میکند. وظیفه توبولهای T انتقال پتانسیل ایجاد شده در غشای ماهیچه اسکلتی به بخشهای عمقی سلول است. سیسترنای انتهایی دو طرف توبول T قرار دارد.
پتانسیل عمل عصب
پیام عصبی تغییرات ناگهانی پتانسیل الکتریکی غشا است که از دندریتها تا پایانه آکسون ادامه پیدا میکند. به این تغییرات ناگهانی پتانسیل عمل گفته میشود. برای ایجاد پتانسیل عمل پتانسیل غشای نورون به سرعت از حالت منفی به مثبت و از مثبت به منفی تغییر میکند. این تغییرات از از سه مرحله اصلی استراحت، دپلاریزه شدن غشا و ریپلاریزه شدن غشا تشکیل شده است. کانالهای ولتاژی نقش اصلی در ایجاد پتانسیل عمل دارند و اختلال در ساختار و عملکرد آنها فیزیولوژی عصب عضله را تغییر میدهد.
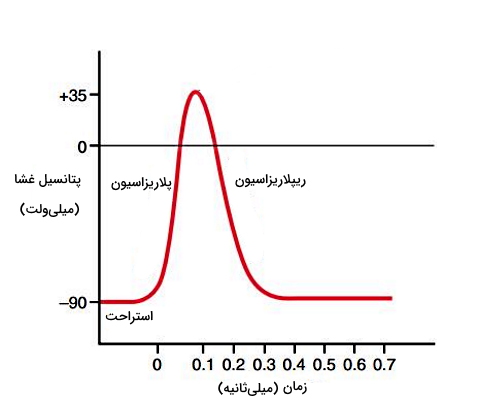
استراحت غشای عصب
پتانسیل الکتریکی غشای عصب در حالت استراحت ۹۰ mV منفیتر از مایع خارج سلولی است و غشا دو قطبی یا پلاریزه است. در این حالت فعالیت پمپ سدیم-پتاسیم فعال است. به علاوه این دو یون در جهت شیب غلظت از کانالهای همیشهباز غشا عبور میکنند. در این حالت کانالهای ولتاژی سدیم و پتاسیم بسته هستند. در شرایط طبیعی بدن تا زمانی که هیچ تحریک خارجی وجود نداشته باشد، پتانسیل غشای نورون در حالت استراحت باقی میماند.
دپلاریزاسیون غشای عصب
اتصال انتقالدهنده عصبی به گیرندههای نورون پسسیناپسی ورود یونها به سیتوپلاسم و پتانسیل الکتریکی غشا را تغییر میدهد. اگر تغییر پتانسیل الکتریکی ایجاد شده به آستانه تحریک (۶۵- mV) کانالهای کانالهای ولتاژی سدیم برسد، پتانسیل عمل دپلاریزاسیون و پتانسیل عمل ایجاد میشود.
در این مرحله کانالهای ولتاژی سدیم باز شده و نفوذپذیری غشا به یون سدیم افزایش مییابد. در نتیجه جریانی از کاتیونهای سدیم در کسری از ثانیه وارد سیتوپلاسم میشود. در دپلاریزاسیون اختلاف پتانسیل الکتریکی غشا و مایع میانبافتی به حدود ۳۵+ mV افزایش مییابد. در این حالت غشا از حالت دپلاریزه خارج شده است. در این ولتاژ کنفورماسیون دریچه مسدودکننده تغییر کرده و ورود کاتیونهای سدیم به سیتوپلاسم متوقف میشود. سرعت تغییر کنفورماسیون دریچه مسدودکننده این کانالها کمتر از سرعت تغییر کنفورماسیون دریچه فعالکننده آنها است و تا زمانی که پتانسیل غشا به حالت استراحت برنگردد، کانال غیرفعال میماند. به همین دلیل با افزایش دفعات یا شدت تحریک، پتانسیل عمل جدید در غشا ایجاد نشده و غشا در دوره تحریکناپذیری کامل است.
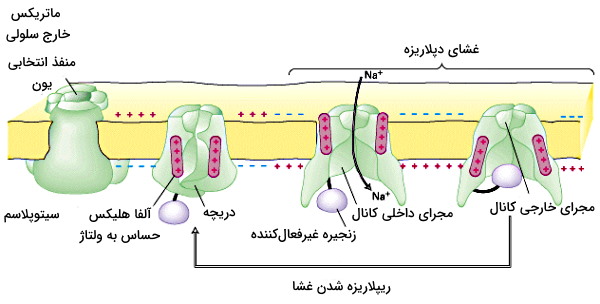
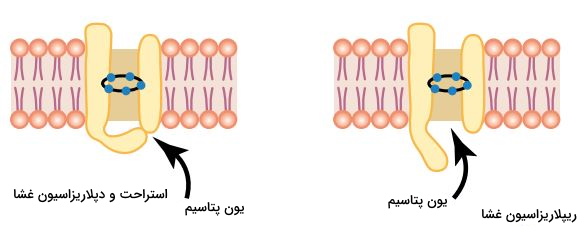
ریپلاریزاسیون غشای عصب
در این وضعیت مثبت شدن پتانسیل الکتریکی سلول سبب تغییر کنفورماسیون دریچه مسدودکننده کانالهای پتاسیمی و خروج پتاسیم از سیتوپلاسم میشود. همزمان دریچه مهاری مسیر حرکت یونهای سدیم از مایع خارج سلولی به سیتوپلاسم را مسدود میکند. در نتیجه پتانسیل الکتریکی سیتوپلاسم نسبت به مایع خارج سلولی منفیتر شده و غشا دوباره پلاریزه میشود. در یکسوم پایانی این مرحله اگر شدت تحریک بسیار زیاد باشد، پتانسیل عمل جدید ایجاد میشود. به این دوره تحریکناپذیری نسبی غشای عصبی میگویند.
انتقال پتانسیل الکتریکی در عصب
پتانسیل عمل ایجاد شده در یک نقطه از غشای نورون و ورود یونهای سدیم، پتانسیل غشا در نقاط اطراف را تغییر میدهد. در نتیجه پتانسیل عمل در طول آکسون حرکت کرده و به پایانه آکسون انتقال مییابد. به دلیل بازه تحریکناپذیری غشای نورون، حرکت پتانسیل عمل و جریان الکتریکی در عصب یکطرفه است و در یک بازه زمانی مشخص بخشی از غشای آکسون در حالت استراحت، بخشی در حالت استراحت، بخشی در حالت ریپلاریزه و بخش دیگر دپلاریزه است. در شرایط طبیعی بدن پتانسیل الکتریکی در تمام غشای آکسونی منتقل میشود یا اصلا منتقل نمیشود.
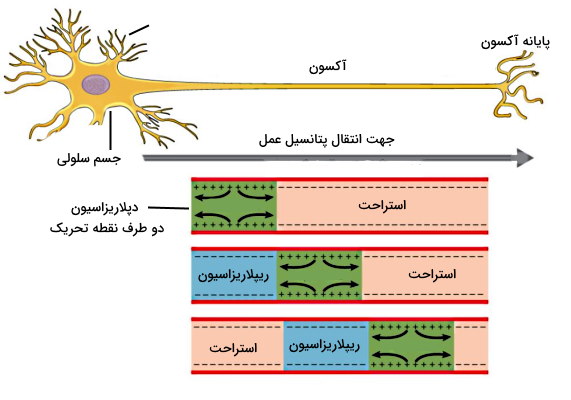
سرعت انتقال پتانسیل عمل به قطر عصب و غلاف میلین اطراف آن بستگی دارد. در نورونهای میلیندار سدیم فقط از کانالهای ولتاژی گرههای رانویه وارد سیتوپلاسم میشود و جهش پتانسیل سرعت انتقال پیام را افزایش میدهد. در بخشهای میلیندار پتانسیل عمل ایجاد نمیشود.
سیناپس عصب عضله
سیناپس عصب عضله یا صفحه حرکتی انتهایی از غشای فیبرهای ماهیچهای، غشای تعداد زیادی پایانه آکسونی و فضای بسیار کوچک (۲۰ تا ۳۰ نانومتر) بین این دو غشا تشکیل شده است. یک یا دو سلول پشتیبان شوآن اطراف سیناپس عصب عضله این ساختار از بافتهای اطراف جدا میکند. در نتیجه پتانسیل عمل از هر عصب به یک فیبر ماهیچهای منتقل میشود. چینخوردگیهای غشای عضله در این سیناپس گیرندههای در دسترس انتقالدهنده عصبی را افزایش میدهد.
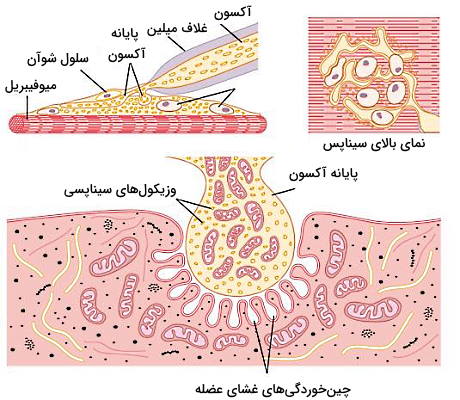
در بخش قبلی این مطلب از مجله فرادرس توضیح دادیم که در غشای پایانه آکسون تعداد زیادی کانال حساس به ولتاژ کلسیم وجود دارد. تغییر کنفورماسیون دریچه این کانالها به دلیل پتانسیل عمل پایانه آکسونی با ورود جریان یون کلسیم به سیتوپلاسم همراه است. افزایش غلظت یون کلسیم تجمع و اتصال پروتئینهای اگزوسیتوزی (SNAREs) به وزیکولهای سیناپسی و غشای پایانه آکسون را تحریک میکند. در نتیجه غشای وزیکول با پایانه آکسون ادغام شده، استیل کولین وارد شکاف سیناپسی شده و وزیکول سیناپسی به سیتوپلاسم برمیگردد.
استیل کولین آزاد شده از پایانه آکسون نورون حرکتی وارد فضای سیناپسی شده و به گیرندههای غشای سلولهای ماهیچه اسکلتی متصل میشود. این گیرندهها کانالهای دریچهدار لیگاندی هستند که پنج زیرواحد پروتئینی آلفا (۲)، بتا (۱)، دلتا (۱) و گاما در ساختار آنها وجود دارد. اتصال دو مولکول استیل کولین به زیرواحد آلفای این کانالها با تغییر کنفورماسیون دریچه و باز شدن کانال همراه است. این کانال کاتیونی غیراختصاصی و کاتیونهای سدیم، پتاسیم و کلسیم از آن عبور میکنند. اما غلظت یون سدیم مایع میانبافتی و پتاسیم سیتوپلاسم از کلسیم بیشتر و پتانسیل الکتریکی سلول ماهیچهای ۸۰- تا ۹۰- mV است. در نتیجه یونهای سدیم بیشتر از دو یون دیگر وارد سارکوپلاسم میشود.
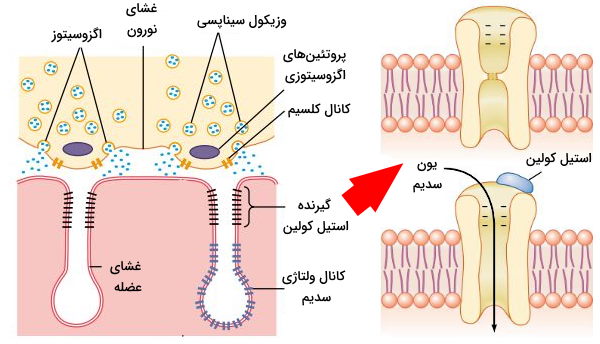
سنتز و تجزیه استیل کولین
استیل کولین انتقالدهده عصبی مهم در فیزیولوژی عصب عضله اسکلتی است. وزیکولهای سیناپسی از دستگاه گلژی در جسم سلولی نورونهای حرکتی جدا و بهوسیله سیستم توبولی انتقال آکسون به پایانه منتقل میشود. این وزیکولها محل ذخیره استیل کولین سنتز شده در سیتوپلاسم پایانه آکسونی است.
استیل کولین در واکنشی یکمرحلهای از استیل کوآ و کولین بهوسیله آنزیم استیل کولین ترانسفراز سنتز میشود. استیل کوآ از محصولات گلیکولیز در میتوکندری است و کولین با عبور از سیپورتر کولین-سدیم وارد سیتوپلاسم پایانه آکسون میشود. در غشای وزیکولهای سیناپسی استیل کولین تعداد زیادی پمپ پروتون وجود دارد که با مصرف ATP پروتونهای سیتوپلاسم را به وزیکول منتقل کرده و pH وزیکول را کاهش میدهد. سپس آنتیپورتر استیل کولین (VAChT) با انتقال هر پروتون به سیتوپلاسم پایانه، یک مولکول استیل کولین را از غشای وزیکول منتقل میکند.
استیل کولین مدت کوتاهی به گیرندههای سلول ماهیچه اسکلتی متصل شده و پس از باز شدن دریچه از این پروتئین جدا میشود. آنزیم استیل کولین استراز به سرعت استیل کولین آزاد در شکاف سیناپسی را به کولین و استات هیدرولیز میکند. در نتیجه سلول برای انقباض بعضی آماده میشود.
فیزیولوژی انقباض عضله
در بخش اول این مطلب از مجله فرادرس توضیح دادیم که هر فیبر ماهیچه اسکلتی از تعداد زیادی میوفیبریل تشکیل میشود کهبهوسیله سارکولما احاطه شده است. گیرندههای استیل کولین در غشای سارکولما و پروتئینهای انقباضی در میوفیبریلها هستند. برای انقباض همزمان و یکنواخت ماهیچه اسکلتی پتانسیل عمل باید از غشا به میوفیبریلها انتقال یابد. اما فاصله میوفیبریلهای مرکزی با غشا زیاد است. بنابراین پتانسیل عمل بهوسیله توبولهای T به این میوفیبریلها منتقل میشود.
ورود یون سدیم از کانالهای لیگاندی (گیرنده استیل کولین) سارکولما به سارکوپلاسم پتانسیل الکتریکی سلول ماهیچهای را تغییر میدهد. اگر تغییر پتانسیل الکتریکی به آئتانه تغییر کنفورماسیون دریچه کانالای ولتاژی برسد این کانالها باز، جریان سدیم وارد سارکوپلاسم و پتانسیل عمل ایجاد میشود. پتانسیل عمل ایجاد شده در دپلاریزاسیون، کنفورماسیون گیرندههای حساس به ولتاژ دیهیدروپریدین (DHP) در غشای توبولهای T را تغییر میدهد. این گیرندهها با کانالهای کلسیم در غشای سیسترنای انتهایی در ارتباط هستند. در نتیجه یون کلسیم وارد سارکوپلاسم میشود.
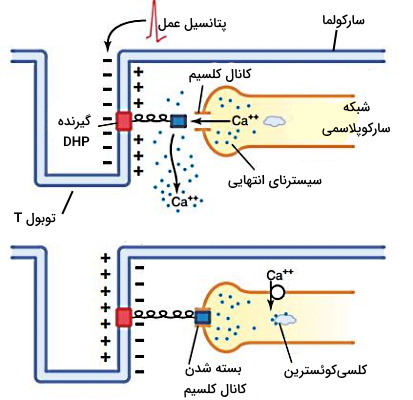
مکانیسم مولکولی انقباض عضله
اتصال چهار یون کلسیم به زیرواحد C تروپونین منجر به تغییر کنفورماسیون این مولکول میشود. تغییر کنفورماسیون تروپونین، کنفورماسیون تروپومیوزین را تغییر میدهد و دو مولکول از میکروفیلامنتهای اکتین جدا خواهند شد. در نتیجه جایگاه اتصال اکتین به میوزین آزاد و آماده اتصال است. این آنزیم ATP را به ADP و Pi هیدرولیز میکند. اما این دو مولکول به سر میوزین متصل میمانند. تغییر کنفورماسیون سر میوزین را سمت فیلامنتهای اکتین کشیده و دو مولکول به هم متصل میشوند.
اتصال اکتین میوزین سبب تغییر یک تغییر کنفورماسیون دیگر در سر میوزین میشود. این تغییر سر میوزین را به سمت دم مولکول خمکرده و نیروی لازم برای کشیده شدن فیلامنتهای اکتین سمت خط Z را فراهم میکند. در نتیجه این تغییر کنفورماسیون ADP یون فسفات از سر میوزین و سر میوزین از اکتین جدا میشود. سپس یک مولکول ATP دیگر به سر میوزین متصل شده و چرخه انقباض تا زمانی که فیلامنتهای اکتین خط Z را به انتهای میوزین نزدیک کند یا زمانی که کشش ایجاد شده بیش از تحمل ساختار عضله باشد، ادامه پیدا میکند.
ریپلاریزه شدن با پایان انقباض و بازگشت یون کلسیم به شبکه سارکوپلاسمی همراه است. پمپ کلسیک غشای این اندامک با مصرف ATP کلسیم را از سیتوپلاسم به شبکه سارکوپلاسمی منتقل میکند. این یون در سارکوپلاسم به پروتئین کلسیکوئستین متصل میشود.
فیزیولوژی نیروی انقباضی عضله
نیروی کششی ایجاد شده در انقباض عضله به تعداد پروتئینهای انقباضی و طول ماهیچه بستگی دارد. هر چه همپوشانی رشتههای اکتین و مولکولهای میوزین در انقباض افزایش یابد، کشش بیشتر در ماهیچه ایجاد میشود. در نتیجه طول ماهیچه کاهش یافته و قطر بخش مرکزی آن بیشتر میشود.
اگر نیروی خارجی وجود نداشته باشد، ماهیچه سریع منقبض میشود. اما وجود نیروی خارجی سرعت انقباض ماهیچه را کاهش میدهد. در این حالت نیرو کششی ایجاد شده در ماهیچه، نیروی خارجی را خنثی میکند. در نتیجه نیرویی برای کاهش طول سارکومر وجود ندارد. در این حالت پروتئینهای انقباضی فعال هستند اما طول سارکومر تغییر نمیکند. به این انقباض ایزومتریک گفته میشود. اگر مقدار نیروی خارجی ثابت باشد، طول سارکومر در انقباض کاهش مییابد اما نیروی کششی ایجاد شده در ماهیچه ثابت است. به این انقباض ایزوتونیک گفته میشود.
فیزیولوژی عضله صاف
ساختار، عملکرد و مکانیسم شروع انقباض در عضلات اسکلتی و صاف متفاوت است. اما پروتئینهای انقباضی در هر دو اکتین و میوزین هستند که در عضله صاف آرایش متفاوتی دارند. به علاوه نورونهای حرکتی در ایجاد پتانسیل عمل لازم برای انقباض این ماهیچهها نقشی ندارند. سیناپس عصب عضله در ماهیچههای صاف بین غشای این سلولها با نورونهای سیستم عصبی سمپاتیک و پاراسمپاتیک ایجاد میشود. انتقالدهنده عصبی این نورونها پس از انتشار به گیرندههای غشایی متصل شده و با تغییر پتانسیل الکتریکی انقباض ماهیچهها را مهار یا تحریک میکند.
آناتومی عضله صاف
فیبرهای ماهیچه صاف با دو آرایش چندواحدی و تکواحدی کنار هم قرار میگیرند. در آرایش چندواحدی فیبرهای ماهیچهای از هم جدا هستند و بین آنها لایهای از بافت پیوندی با رشتههای کلاژنی فراوان وجود دارد. در نتیجه جریان الکتریکی از یک فیبر به فیبر دیگر منتقل نمیشود. هر فیبر ماهیچه صاف چندواحدی مثل ماهیچه اسکلتی، با یک پایانه عصبی سیناپس دارند. انقباض این ماهیچهها بهوسیله سیستم عصبی کنترل میشود. ماهیچههای مژگانی چشم، ماهیچههای عنبیه و ماهیچههای ریشه مو از انواع چندواحدی هستند.
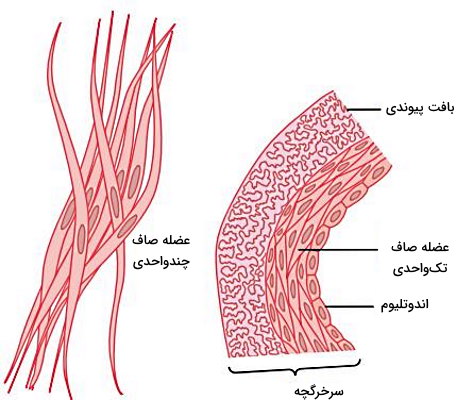
ماهیچههای صاف تکواحدی یا احشایی از کنار هم قرار گرفتن صفحهای یا دستهای تعداد زیادی فیبر ماهیچهای تشکیل میشوند که همزمان منقبض میشوند. غشای پلاسمایی این ماهیچه در چند نقطه به هم متصل است تا نیروی انقباضی را بین فیبرها منتقل کند. اتصالات شکافدار بین دو غشا محل عبور یون و جریان الکتریکی از سیتوپلاسم یک فیبر ماهیچهای به فیبر دیگر است. عضله صاف دیواره تمام مجراهای بدن (رگها، مسیرهای تنفسی، مجاری ادراری، مجاری تولید مثلی، لوله گوارش، مجرای صفرا، رحم و مثانه) از نوع تکواحدی است.
سیناپس عصب عضله صاف
سیناپس اعصاب سمپاتیک و پاراسمپاتیک با عضله صاف از غشای فیبرهای ماهیچهای، فاصله بین دو غشا و گرههای عصب تشکیل شده است. گرههای عصب محل تجمع انتقالدهندههای عصبی اپینفرین و استیل کولین است که پس از انتشار در شکاف سیناپسی به گیرندههای موسکارینی (M3 و M2)، آلفا ( و ) و بتا () در غشای سلول ماهیچهای متصل میشوند.
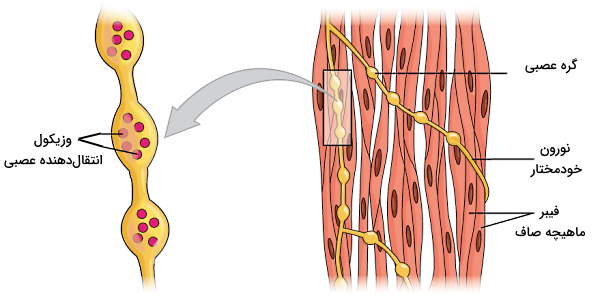
گیرندههای آلفا و بتا پروتئینهای عرض غشایی همراه با پروتئین G هستند. پروتئین G همراه گیرنده آلفا ۱ از نوع Gq است که غلظت یون کلسیم در سلول ماهیچه صاف را افزایش داده و انقباض را تحریک میکند. پروتئین G همراه گیرنده آلفا ۲ از نوع Gi است که با کاهش cAMP انقباض ماهیچه صاف را تحریک میکند و پروتئین G همراه گیرنده آلفا از نوع Gs است که با افزایش cAMP استراحت ماهیچه صاف را تحریک میکند. گیرنده استیل کولین در این سلولها از انواع موسکارینی و از انواع پروتئینهای عرض غشایی همراه پروتئین G هستند. پروتئین G همراه گیرندههای M2 از نوع Gi و M3 از نوع Gq است. پروتئینهای G از سه مسیر متفاوت فیزیولوژی عصب عضله صاف را تغییر میدهد.
- Gs: اتصال انتقالدهنده عصبی به گیرنده سبب فعال شدن پروتئینهای G تحریکی (Stimulatory Protein) و تبادل GDP با GTP میشود. Gs فعال آنزیم آدنیلاز سیکلاز غشایی را فعال کرده و این آنزیم ATP را به cAMP تبدیل میکند. cAMP پیامرسان ثانویه سلول است که با فعال کردن پروتئین کیناز A آبشاری از فسفوریلاسیونهای غشایی را فعال میکند.
- Gq: اتصال انتقالدهده عصبی به گیرنده سبب فعال شدن Gq و و تبادل GDP با GTP میشود. Gq فعال آنزیم فسفولیپاز c در غشا را فعال و این آنزیم فسفاتیدیل بیس فسفات غشا را به دیآسیل گلیسرول (DAG) و اینوزیتول تری فسفات (IP3) تجزیه میکند. DAG با فعال کردن پروتئین کیناز C و واکنشهای آبشاری فسفوریلاسیون فعالیت سلول را تغییر میدهد و IP3 خروج کلسیم از شبکه سارکوپللاسمی را تحریک میکند.
- Gi: اتصال انتقالدهنده عصبی به گیرنده با سبب فعال شدن پروتئینهای G مهاری (Inhibitory G Protein) و تبادل GDP با GTP میشود. Gi فعال آنزیم آدنیلات سیکلاز را مهار و خروج پتاسیم از سلول را تحریک میکند.
نوراپینفرین مدت کوتاهی پس از ایجاد تغییر در ماهیچه صاف از گیرنده جدا شده و بهوسیله ناقل غشایی به سیتوپلاسم نورون خودمختار انتقال داده میشود. در سیتوپلاسم آنزیمهای مونوآمین یا کتکول-اُ-متیل ترانسفراز تجزیه شده یا در وزیکولهای سیناپسی ذخیره میشود. استیل کولین در سیناپس ماهیچههای صاف مثل سیناپس ماهیچههای اسکلتی و با فعالیت آنزیم استیلکولین استراز حذف میشود.
فیزیولوژی پتانسیل عمل عضله صاف
پتانسیل غشای ماهیچه صاف در حالت استراحت بین ۵۰- تا ۶۰- mV و بیشتر از پتانسیل غشای عضله اسکلتی است. تعداد کانالهای ولتاژی کلسیم در غشای سلولهای ماهیچه صاف بسیار بیشتر از کانالهای ولتاژی سدیم است و یون کلسیم در ایجاد پتانسیل عمل این سلولها نقش بیشتری دارد. ورود یون کلسیم به سیتوپلاسم ماهیچه صاف با ایجاد تغییرات پتانسیل الکتریکی غشا همراه است و اگر این تغییرات پتانسیل لازم برای تغییر کنفورماسیون دریچه کانالهای ولتاژی کلسیم را ایجاد کند، کانالها باز شده و جریان نوع کلسیم پتانسیل عمل ایجاد میکند.
نمودار پتانسیل عمل در بسیاری از ماهیچههای صاف تکواحدی شبیه پتانسیل عمل ماهیچههای اسکلتی و «نیزهای» (Spike) است. در این نوع پتانسیل عمل، پتانسیل الکتریکی غشا در کسری از ثانیه (۱۰ تا ۵۰ میلیثانیه) تغییر میکند. اما در بعضی از ماهیچههای صاف تکواحدی ازجمله رحم و میزنای ریپلاریزاسیون مثل ماهیچههای قلبی آهسته (۱۰۰ میلیثانیه تا ۱ ثانیه) و نمودار پتانسیل عمل کفهای است.
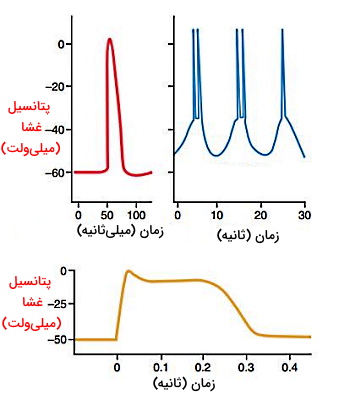
تغییر خودبهخودی پتانسیل الکتریکی و موج آهسته در ماهیچههای صاف دیواره لوله گوارش ایجاد شده و به حرکت غذا در این دستگاه کمک میکند. «سلولهای کجال» (Cajal Cells) مثل گره سینوسی در قلب، سلولهای جریانساز این بافت ماهیچهای است. تغییر غلظت یون کلسیم در سلولهای کجال بهوسیله اتصالات شکافدار به سلولهای ماهیچه صاف منتقل میشود و موج آهسته را ایجاد میکند.
پتانسیل عمل ماهیچه چندزیرواحدی
سلولهای ماهیچه صاف چندزیرواحدی در پاسخ به تحریک عصبی سمپاتیک یا پاراسمپاتیک منقبض میشوند. اتصال انتقالدهنده عصبی به گیرنده این سلول با دپلاریزه شدن غشا و انقباض ماهیچه همراه است. اما از آنجا که فیبر ماهیچهای این سلولها بسیار کوچک اس ، پتانسیل عمل ایجاد نمیشود.
فیزیولوژی انقباض عضله صاف
انقباض ماهیچه صاف مثل ماهیچه اسکلتی به افزایش غلظت یون کلسیم در سیتوپلاسم نیاز دارد. این تغییر ممکن است به دلیل تحریک اعصاب خودمختار (عضله تکواحدی و چندواحدی)، کشش فیبرهای ماهیچهای (عضله تکواحدی)، اتصال هورمون به گیرنده غشایی (عضله تکواحدی و چندواحدی) یا تغییر ترکیب شیمیایی مایع میانبافتی (عضله تکواحدی) ایجاد شود. در این ماهیچهها تروپونین وجود ندارد و کلمودولین برهمکنش میکروفیلامنتهای اکتین و میوزین را تنظیم میکند. یک سر میکروفیلامنتهای اکتین بهوسیله پروتئینهای اینتگرین به غشای پلاسمایی متصل و اجسام متراکم سر دیگر این رشتهها را به هم متصل میکند. در این ماهیچهها خط Z وجود ندارد.
کمپلکس کلمودولین-کلسیم، کیناز زنجیره سبک میوزین را فعال میکند. این آنزیم با اضافه کردن گروه فسفات به زنجیره سبک سر میوزین و القای تغییر کنفورماسیون، اتصال اکتین به میوزین را تحریک میکند. نیروی ایجاد شده از اتصال و جدا شدن پروتئینهای اکتین و میوزین بهوسیله اینتگرین به غشا منتقل و سلول منقبض میشود. کاهش یون کلسیم در سیتوپلاسم، آنزیم دیگری به نام میوزین فسفاتاز را فعال میکند. این آنزیم گروه فسفات زنجیره سبک میوزین را هیدرولیز کرده و انقباض پایان مییابد.
اثر هورمون بر انقباض عضله صاف
هورمونها و ترکیبات شیمیایی مایع میانبافتی ماهیچههای صاف یکی دیگر از عواملی هستند که انقباض این ماهیچه را بدون ایجاد پتانسیل عمل تحریک میکنند. برای مثال در بافت مکاهیچه صاف سرخرگچهها و اسفنکترهای مویرگی عصبی وجود ندارد و تغییر ترکیبات مایع میانبافتی انقباض ماهیچه را تحریک میکند.
در شرایط طبیعی بدن این ماهیچهها منقبض هستند. اما اگر جریان خون مورد نیاز بافت افزایش یابد، ماهیچه دیواره از انقباض خارج شده و حجم خون افزایش مییابد. کاهش اکسيژن بافت، افزایش دیاکسید کربن و کاهش pH مایع میانبافتی فاکتورهای اصلی است که انقباض این عضله را کنترل میکند. آدنوزین، لاکتیکاسید، افزایش غلظت پتاسیم مایع میانبافتی، کاهش غلظت کلسیم و افزایش دمای بدن با کاهش انقباض ماهیچههای صاف و افزایش قطر ماهیچه همراه است.
اتصال هورمونهای اپینفرین، نوراپینفرین، اندوتلین، وازو پرسین، آنژیوتانسین، هیستامین، سروتونین و اوسیتوسین به گیرنده غشای ماهیچه صاف، انقباض این ماهیچه را تحریک را مهار میکند. اگر گیرنده این هورمونها ورود یونهای سدیم یا کلسیم به سیتوپلاسم را افزایش دهند، انقباض ماهیچه تحریک میشود. اما اگر کانالهای سدیمی و کلسیمی مهار یا کانالهای پتاسیمی باز شوند، غشا هایپرپلاریزه شده و انقباض ماهیچه مهار میشود.
سوالات متداول
در این بخش از مطلب مجله فرادرس سوالات متداول پیرامون فیزیولوژی عصب عضله را پاسخ میدهیم.
کزازی شدن عضله چیست؟
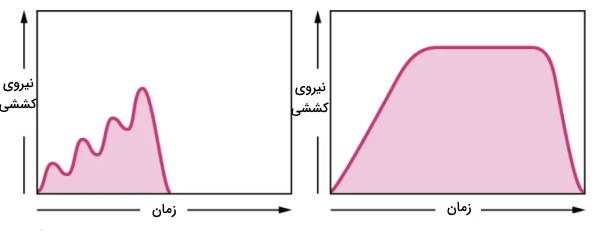
«کزازی شدن عضله اسکلتی» (Tetanic Contraction) در شرایطی ایجاد میشود که سرعت تحریک غشای عضله بهوسیله نورون حرکتی بسیار زیاد است و سلول فرصت کافی برای استراحت قبلا از شروع انقباض بعدی ندارد (کزازی شدن نسبی) یا بدون استراحت از یک دوره انقباضی وارد دوره انقباضی بعدی میشود (کزازی شدن کامل). در کزازی شدن کامل نیروی کششی ماهیچه تغییری نمیکند، اما طول آن بر اساس نوع ماهیچهای ممکن است ثابت باشد یا تغییر کند.
نوار عصب عضله چیست؟
نوار عصب عضله یا الکترومیوگرام منحنی است که ارتباط جریان الکتریکی عصب و انقباض عضله اسکلتی را نشان میدهد. به کمک این روش میتوان اختلالهای فیزیولوژی عصب عضله اسکلتی را بررسی کرد. الکترودهای سوزنی این دستگاه در ماهیچه قرار میگیرد و جریان الکتریکی ایجاد شده از انقباض ارادی را به دستگاه منتقل میکند.