هورمون چیست؟ – به زبان ساده
به پیامرسانهای شیمیایی بدن که توسط غدد درونریز تولید و ترشح میشود، سپس با استفاده از جریان خون به اندام یا بافت هدف خود میرسند تا روی آن اثری به جا بگذارند، «هورمون» میگویند. هورمونها مختص به جانوران نیستند و گیاهان نیز هورمونهای خود را دارند که به آنها «فیتوهورمون» (Phytohormone) میگوییم. هورمونهای گیاهی به موادی گفته میشوند که برای رشد و تمایز بافتهای گیاهان ضروری هستند. در این مطلب از مجله فرادرس یاد میگیریم که هورمون چیست و آنها را چطور دستهبندی میکنند. ویژگیهای هورمونها و نحوه انتقال پیام توسط آنها را میشناسیم و پس از آشنایی با الگوهای ترشحی هورمونها، یاد میگیریم که روش کنترل ترشح هورمون چیست.
- یاد میگیرید ساختار شیمیایی و انواع اصلی هورمونها را تمایز دهید.
- خواهید آموخت عملکرد هورمونها چگونه فرآیندهای حیاتی بدن را تنظیم میکند.
- میآموزید چه تفاوتهایی بین هورمونهای جانوری و گیاهی وجود دارد.
- خواهید توانست مسیر تولید، انتقال و اثر هورمون در بدن را شرح دهید.
- با الگوهای ترشح، کنترل و بازخوردهای هورمونی تخصصیتر آشنا میشوید.
- یاد میگیرید چگونه اختلال در تعادل هورمونها سلامتی را تهدید میکند.
هورمون چیست؟
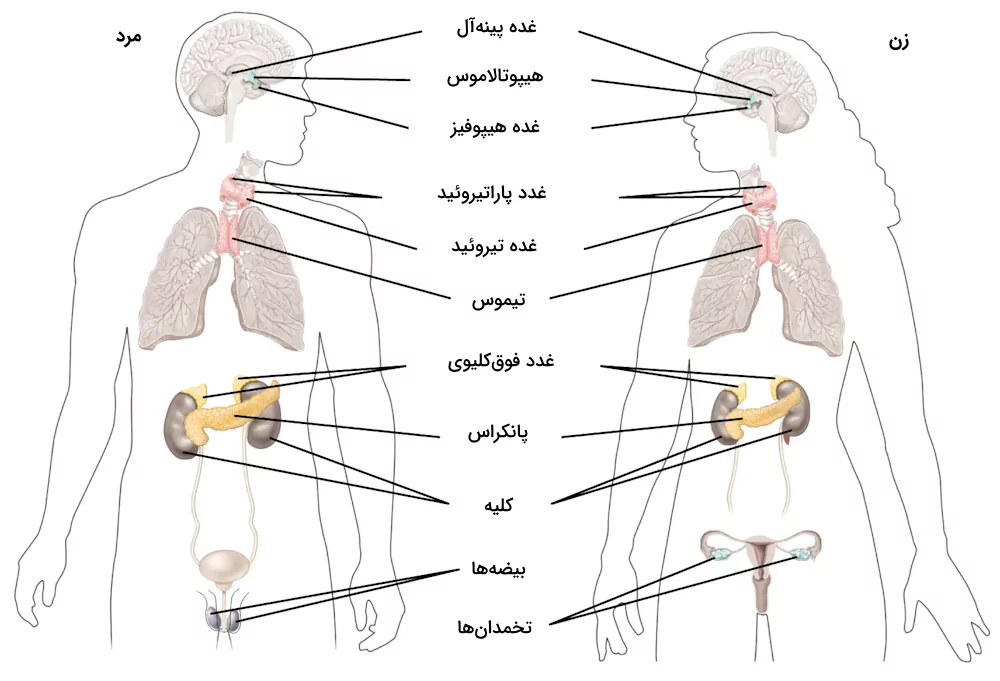
در فیزیولوژی به مادهای که توسط غدد درونریز تولید و ترشح میشود، «هورمون» (Hormone) میگویند. غده درونریز، غدهای بدون مجرا است که جزو «دستگاه درونریز» یا همان «دستگاه اندوکرین» (Endocrine System) بدن است. در جدول زیر غدههای موجود در دستگاه اندوکرین را معرفی میکنیم.
| جدول غدههای موجود در دستگاه اندوکرین بدن | |
| «غده پینهآل» (Pineal Gland) | «غدد فوق کلیوی» (Adrenal Gland) |
| «هیپوتالاموس» (Hypothalamus) | «غده تیروئید» (Thyroid Gland) |
| «غده هیپوفیز» (Pituitary Gland) | «پانکراس» (Pancreas) |
| «تخمدان» (Ovaries) | «بیضهها» (Testes) |
| «غده پاراتیروئید» (Parathyroid Gland) | «تیموس» (Thymus) |
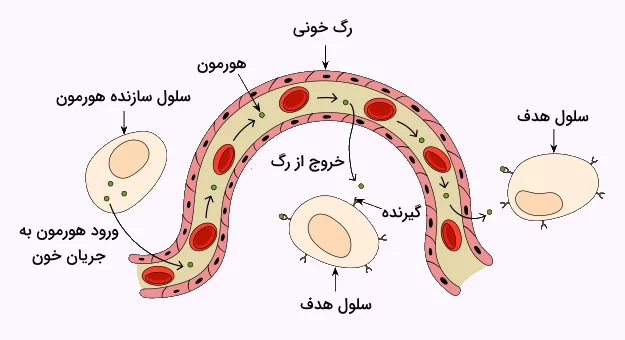
پیامرسانی در دستگاه اندوکرین به این صورت است که سلول سازنده هورمون را سنتز و با استفاده از فرآیند اگزوسیتوز به جریان خون ترشح میکند.
برای آشنایی با هورمون و یادگیری نکات آن پیشنهاد میکنیم فیلم آموزش رایگان هورمون همراه با ویژگیها و تفاوت آن با آنزیم در فرادرس را تماشا کنید که آن را در بخش زیر آوردهایم.
هورمونها به کمک گردش خون در بدن به سلولهای هدف خود میرسند و این سلولها را از طریق پروتئینهایی که روی غشا آنها قرار دارند یا گیرندههای خارج سلولی، شناسایی میکنند.
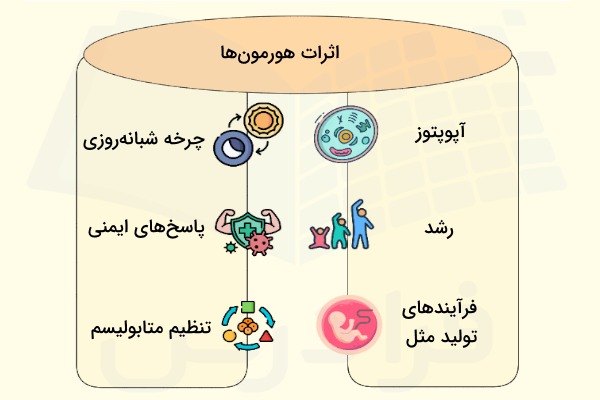
اثر هورمونها بر سلولهای بدن
تاثیراتی که هورمونهای مختلف روی سلولها دارند، متفاوت است و میتوانند باعث فعالسازی یا مهار یک فرآیند در سلول هدف بشوند. اتفاقات زیادی در بدن تحت کنترل هورمونها است که در ادامه از آنها نام میبریم.
- رشد
- «چرخه شبانهروزی» (Circadian Rhythm)
- مرگ برنامه ریزی شده سلول یا «آپوپتوز» (Apoptosis)
- پاسخهای ایمنی
- تنظیم متابولیسم
- فرآیندهای تولیدمثل
- هومئوستازی
بعضی هورمونها، مانند انسولین ساختاری آبدوست دارند و به همین دلیل گیرندههای آنها روی غشای سلولی قرار دارد. ساختار بعضی دیگر از انواع هورمونها لیپیددوست است و گیرندههای داخل سلولی دارند، ازجمله این هورمونها میتوان استروئیدها را مثال زد.
هورمونها را میتوان به صورت مصنوعی نیز ساخت و به عنوان دارو برای رفع و درمان کمبودهایی که در بدن بعضی بیماران وجود دارد، مصرف کرد. این هورمونهای سنتز شده هم به صورت داروی خوراکی و هم به صورت داروی تزریقی تولید میشوند.
ویژگیهای هورمون چیست؟
هورمونها ویژگیهای منحصر به فردی دارند که در فعالیت آنها نقش دارند. حالا که یاد گرفتیم هورمون چیست در این بخش با تعدادی از ویژگیهای هورمونها آشنا میشویم. در صورتی که تمایل دارید با ساختار ماکرومولکولهای زیستی آشنایی کاملتری داشته باشید، فیلم آموزش رایگان ساختار ماکرومولکول های زیستی را به شما پیشنهاد میدهیم.
- سنتر و ترشح: هورمونها توسط بافتها یا غدههای درونریز خاصی ساخته میشوند و سپس با ترشح به جریان خون و جابهجایی به کمک گردش خون خود را به بافتها و اندامهای هدف میرسانند.
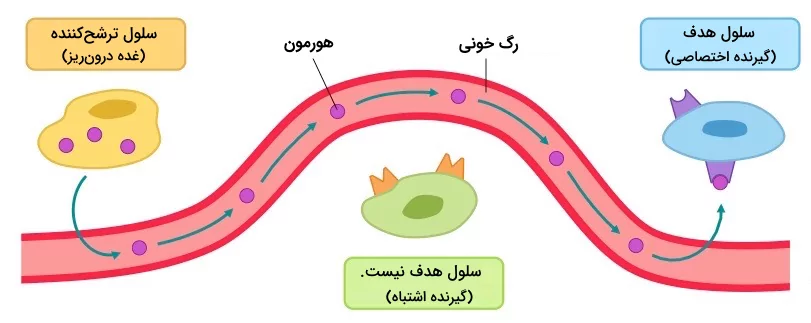
- داشتن اهداف مشخص: هورمونها اندامها یا سلولهای هدف به خصوصی دارند که تحت تاثیر ترشح هورمونها قرار میگیرند، زیرا روی سطح غشا یا درون سیتوپلاسم این سلولها گیرندههای هورمونی قرار دارند.
- بروز علائم برای کمبود یا عدم حضور هورمون: در صورتی که غده سازنده یک هورمون آسیب ببیند یا از بدن به وسیله روشهایی مثل جراحی، حذف شود؛ موجود زنده علائمی را نشان میدهد که با کمبود هورمون مرتبط هستند. این موضوع نشاندهنده اهمیت بالای نقش هورمونها در فعالیتهای طبیعی بدن است.
- درمانهای جایگزین: برای رفع کمبود بدن ممکن است بافت ترشحکننده هورمون را به بدن پیوند بزنند یا خود هورمون را به صورت داروهای تزریقی در اختیار بدن قرار بدهند.
- وزن مولکولی پایین: به طور معمول هورمونها مولکولهایی کوچک هستند که به خاطر وزن مولکولی پایینی که دارند، میتوانند به راحتی به کمک جریان خون در بدن منتقل شوند.
- انحلالپذیری و ضریب انتشار بالا: هورمونها مولکولهایی کوچک و انحلالپذیر هستند که ضریب انتشار بالایی دارند. این خاصیتها به آنها این امکان را میدهد که در خون به سرعت حرکت کنند و به سلولهای هدف برسند. با این وجود اثرات هورمونها پایدار نیست و با توجه به شرایط محیطی و فیزیولوژیکی دچار تغییر میشوند.
- کارآمد در غلظتهای کم: هورمونها مولکولهایی با پتانسیل اثرگذاری بسیار بالا هستند، به طوری که در غلظتهای کم نیز میتوانند اثرات گستردهای در بافتها و سلولهای هدف خود ایجاد کنند.
- انتقال از طریق خون: هورمونها به وسیله گردش خون در بدن جابهجا میشوند و همین کمک گرفتن از سیستم گردش خون به هورمونها این قابلیت را داده است که بتوانند به اهدافی که در فاصله بسیار دوری از بافت ترشحکننده آنها قرار دارد، رسیده و روی آنها اثر بگذارند.
- فعالیت در بافتهای دور: به طور معمول محل ساخت هورمون با محل فعالیت آن متفاوت است، بنابراین هورمونها باید در بدن جاندار جابهجا شده و خود را به بافت یا اندام هدف خود برسانند تا بتوانند اثراتی که از آنها انتظار میرود را ایجاد کنند.
- عدم اختصاصیت برای یک موجود زنده: هورمونها اختصاصیت بسیار زیادی در فعالیتهای خود دارند ولی میتوانند یک اثر به خصوص را در جانداران متفاوتی که شرایط یکسانی دارند، ایجاد کنند.
پیامرسانی به وسیله هورمون چیست؟
تا اینجای این مطلب از مجله فرادرس یادگرفتیم هورمون چیست، در تعریف این مولکولهای زیستی گفتیم که وظیفه آنها انتقال پیام است. در این بخش قصد داریم به همین فعالیتها بپردازیم و تشریح کنیم که منظور از پیامرسانی توسط هورمون چیست.
پیامرسانی هورمونی یک فرآیند پایهای است که در طی آن هورمونها از غدد درونریز مستقیم به فضای خارج سلولی ترشح میشوند، سپس با ورود به مویرگها به جریان خون میپیوندند و به سمت سلول هدف خود حرکت میکنند. این سیستم به هورمونها این امکان را میدهد که بتوانند روی اندامها و بافتهایی اثر خود را اعمال کنند که فاصله زیادی با بافت ترشحکننده هورمون دارند.
برای مثال سلولهای «تیروسیت» (Thyrocyte) در غده تیروئید را در نظر بگیرید که هورمون های تیروئیدی را سنتز میکنند و این هورمونها با ورود به جریان خون خود را به بافتهای مختلف میرسانند تا متابولیسم سلولها را تنظیم کنند. بافتهای مختلف به پیامهای رسیده توسط این هورمون به یک شکل پاسخ نمیدهند. در حقیقت بافتهای مختلف پاسخهای متفاوتی به یک هورمون میدهند.
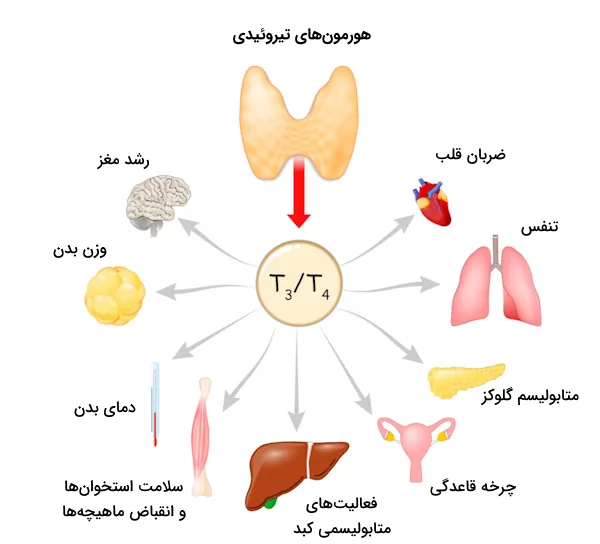
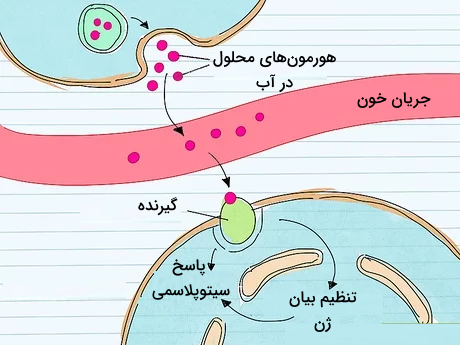
پیچیدگی پیامرسانی هورمونی در نحوه ارتباط هورمونها با سلولهای هدف خود نهفته است. گیرنده بعضی هورمونها روی سطح سلول قرار دارد، بنابراین هورمون نیاز به ورود به سلول ندارد و با وصل شدن به گیرنده خود روی غشا سلولی اثر خود را اعمال میکند اما گیرنده بعضی از هورمونها درون سیتوپلاسم یا حتی درون هسته سلول قرار دارد و هورمون باید برای رسیدن به گیرنده خود از غشا سلول عبور کند.
اتصال هورمونها به گیرندههای خود باعث به راه افتادن آبشارهای پیامرسانی در سلول میشود که در نهایت بیان بعضی ژنها را تحت تاثیر قرار میدهد. تنظیم فعالیت هورمونها نیز وابسته به مکانیسمهای پاسخ است که تولید هورمونها را تنظیم میکند تا هومئوستازی بدن به خطر نیفتد.
هورمونهای محلول در چربی، مانند هورمونهای استروئیدی، همان دسته از هورمونهایی هستند که گیرندههایی درون هسته سلول دارند و علاوه بر عبور از غشا سلولی باید از غشا هسته نیز بگذرند. حضور گیرندههای این هورمونها درون هسته سلول و در مجاورت ماده ژنتیکی سلولها باعث میشود که این هورمونها نقش بسیار پررنگی در کنترل بعضی فعالیتهای سلولی و فرآیندهای زیستی داشته باشند.
مسیر انتقال پیام توسط هورمونها
برای بررسی مسیر انتقال پیامهای هورمونی باید از سنتز هورمونها شروع کنیم و گام به گام پیش برویم تا یاد بگیریم که مکانیسم انتقال پیام توسط یک هورمون چیست. در ادامه مراحل مختلف این مسیر را توضیح میدهیم.
- سنتز هورمون: هورمونها توسط سلولهایی تخصصیافته در غدد یا بافتهای درونریز سنتز میشوند. هر هورمونی برای پاسخ دادن به یکی از نیازهای فیزیولوژیک بدن مانند استرس، رشد یا تغییر سطح متابولیسم بدن ساخته و ترشح میشود.
- ذخیره و ترشح هورمون: پس از سنتز هورمون، امکان دارد که این مولکولها در وزیکولهای ترشحی ذخیره شوند یا به محض سنتز به گردش خون ترشح شوند. آزادسازی هورمونها به سیگنالهای تحریک ترشح مانند تغییر ترکیبات خون یا تحریک عصبی، بستگی دارد. ذخیرهسازی هورمونهای پپتیدی مانند انسولین درون وزیکولهای ترشحی رایج است، زیرا این موضوع به بدن این امکان را میدهد که به محض افزایش گلوکز خون، انسولین را آزاد کند و برای سنتز هورمون وقت صرف نکند.
- انتقال به محل سلول هدف: هنگامی که هورمون ترشح شد، باید به کمک گردش خون خود را به سلولها، بافتها و اندامهای هدف برساند. هورمونها میتوانند به صورت آزاد یا متصل شده به پروتئینهای حامل در جریان خون وجود داشته باشند، روش انتقال آنها به وسیله آبدوست بودن یا آبگریز بودن ساختار مولکولی هورمون تعیین میشود.
- شناسایی توسط گیرنده: هورمونها اثرات خود را به وسیله اتصال به گیرندههایی خاص اعمال میکنند که ممکن است روی سطح یا درون سلول وجود داشته باشند. هورمونهایی با ساختار آبگریز مانند هورمونهای استروئیدی وارد سلول میشوند و به گیرندههای درونسلولی متصل میشوند، در حالی که هورمونهایی با ساختار آبدوست مانند هورمونهای پپتیدی به گیرندههای مستقر روی سطح سلول متصل میشوند. اتصال هورمون به گیرنده باعث تغییرات کنفورماسیونی میشود که میتواند مسیرهای پیامرسانی پاییندست را در سلول هدف به راه بیاندازد.
- انتقال و تشدید سیگنال: پس از اتصال هورمون به گیرنده خود، آبشاری از پیامرسانیهای مختلف در سلول هدف به راه میافتد که باعث میشود یک پیام به مجموعهای از پیامها تبدیل شود، بنابراین این فرآیند را با عنوان «تشدید سیگنال» (Amplification) میشناسیم. به وجود آمدن این آبشار پیامها درون سلول، باعث بروز پاسخهای زیستی قابل مشاهده میشود.
- پاسخ سلولی: به محض تشدید پیام، سلول شروع به پاسخ دادن به هورمون میکند. این پاسخ زیستی میتواند تغییر میزان بیان یک ژن، تغییر فعالیت آنزیمی یا به وجود آوردن تغییراتی در فعالیت سلول باشد.
- مکانیسمهای بازخورد: برای حفظ تعادل فعالیت هورمونی و پیشگیری از ترشح بیش از حد هورمونها، مکانیسمهای پاسخ به راه میافتند که باعث تنظیم سطح هورمونها میشوند. بازخوردهای منفی از رایجترین انواع پاسخها هستند که باعث میشوند از ترشح بیشتر هورمون جلوگیری شود.
روش سنتز هورمون چیست؟
سنتز هورمونها فرآیندی پیچیده است که مراحل تنظیمی ژنتیکی آن را کنترل میکنند. بسته به نوع هورمون که میتواند پپتیدی، آمینی یا استروئیدی باشد، مسیرهای سنتز متفاوتی برای مطالعه و بررسی وجود دارند. هورمونهای پپتیدی طی مسیرهای بیان ژنتیکی خاصی تولید میشوند، اما هورمونهای غیرپپتیدی مثل هورمونهای تیروئیدی یا هورمونهای استروئیدی بااستفاده از مسیرهای بیوشیمیایی متفاوت و منحصر به فرد خود تولید میشوند. در ادامه با هر کدام از این مسیرها بیشتر آشنا میشویم تا به طور کامل یاد بگیریم که روش سنتز هورمون چیست.
مسیر سنتز هورمونهای پپتیدی
هورمونهای پپتیدی در شبکه آندوپلاسمی زبر ساخته میشوند، زیرا محل ترجمه mRNA کدکننده آنها و شکل گیری ساختار سه بعدی این هورمونها این اندامک سلولی است. مولکول mRNA حاصل رونویسی از ژنهای خاصی است که هورمون را کد کردهاند و با ترجمه آن، «پیشهورمون» (Prohormone) ساخته میشود.
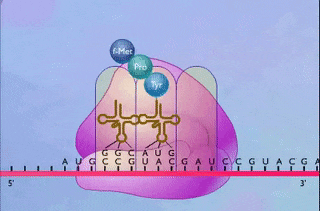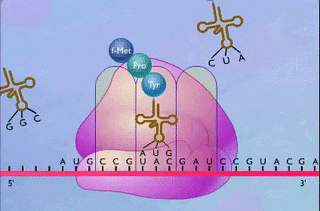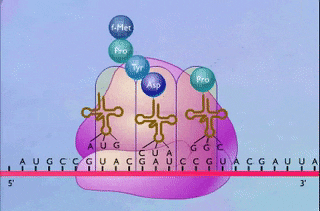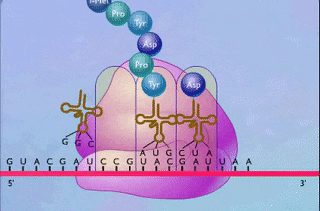
پیشهورمون در قسمت پایانه آمینی خود دارای توالی است که «پپتید پیشرو» یا «سیگنال پپتید» (Signal Peptide) نام دارد. سیگنال پپتید به پیشهورمون برای عبور از غشا شبکه آندوپلاسمی کمک میکند، اما در این اندامک سلولی از توالی پپتیدی جدا میشود تا پیشهورمون بتواند ساختار دوم خود را به درستی شکل دهد و به جسم گلژی فرستاده شود.
ممکن است پیشهورمون توسط آنزیمهای موجود در جسم گلژی دچار تغییر شده و تبدیل به هورمون بالغ شود. ازجمله این تغییرات میتوان به اضافه شدن کربوهیدرات به هورمونهای گلیکوپروتئینی مانند FSH و LH اشاره کرد. پس از طی کردن این مراحل، هورمونها در وزیکولهای خاصی ذخیره میشوند تا در زمان مناسب ترشح شوند.
مسیر سنتز هورمونهای غیرپپتیدی
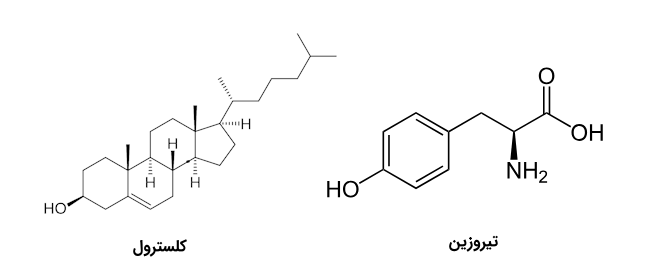
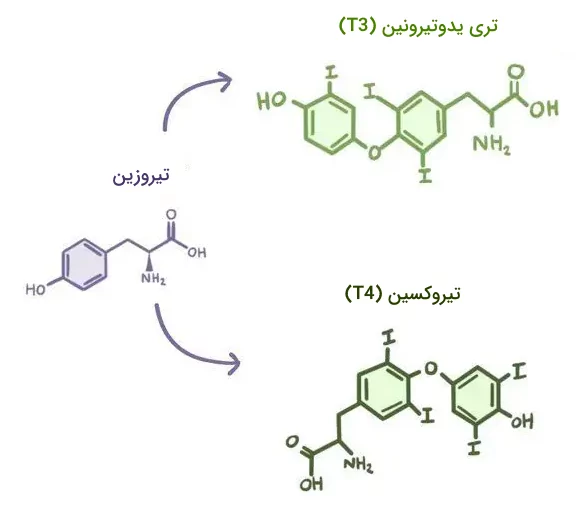
هورمونهای آمینی و استروئیدی با هورمونهای پپتیدی متفاوت هستند، زیرا این دسته از هورمونها از مولکولهای پیشساز ساخته میشوند. مولکول پیشساز هورمونهای آمینی، تیروزین و پیشساز هورمونهای استروئیدی، کلسترول است. در تصویر زیر میتوانید ساختار مولکولی این دو ماده پیشساز را ببینید.
این مولکولهای پیشساز در سلولها به وسیله واکنشهای آنزیمی متفاوتی دچار تغییر شده و محصولات نهایی را شکل میدهند که هورمونها نیز ازجمله این محصولات هستند. هورمونهای آمینی و استروئیدی برخلاف هورمونهای پپتیدی درون وزیکولهای خاصی ذخیره نمیشوند و چون خاصیت انحلالپذیری در چربیها را دارند به سادگی از غشای پلاسمایی سلول عبور میکنند.
تغییرات پس از سنتز هورمونها
بعضی از هورمونها ممکن است پس از ترک محل سنتز خود فعال شوند. برای مثال هورمونی که کاملا فعال نشده است ممکن است در جریان خون یا در بافت هدف به وسیله آنزیمهای موجود در آن بافت فعال شود. این روند فعالسازی باعث کنترل بیشتر بدن بر فعالیت هورمونها میشود. در حقیقت سیستم اندوکرین بدن به وسیله این روش کنترلی مطمئن میشود که هورمونها در زمان و مکانی فعال شوند که به حضور و فعالیت آنها نیاز است.
جدول غدد درون ریز و هورمونهای اصلی هر غده
غدد درونریز بدن انسان مسئول ساخت هورمونهای مختلف هستند. با توجه به اینکه تا اینجای این مطلب فرادرس یاد گرفتیم که هورمون چیست، در این بخش قصد داریم به کمک یک جدول با غدد درونریز دستگاه اندوکرین آشنا شویم و هورمونهای اصلی هر غده را به همراه فعالیت آنها معرفی کنیم.
در صورتی که علاقه به کسب اطلاعات بهتر و کاملتر راجع به سیستم غدد بدن دارید، مطالعه مطلب «سیستم غدد بدن — به زبان ساده» از مجله فرادرس را به شما توصیه میکنیم.
| غده درونریز | هورمون - ساختار شیمیایی | اثر |
| هیپوفیز | هورمون رشد (GH) - پپتید | تحریک رشد بافتهای بدن |
| پرولاکتین (PRL) - پپتید | تحریک تولید شیر | |
| هورمون محرک تیروئید (TSH) - پپتید | تحریک آزادسازی هورمونهای تیروئيدی | |
| هورمون آدرنوکورتیکوتروپین (ACTH) - پپتید | تحریک آزادسازی هورمونهای قشر فوقکلیه | |
| هورمون محرکه فولیکولی (FSH) - پپتید | تحریک تولید گامت | |
| هورمون لوتئینهکننده (LH) - پپتید | تحریک تولید آندروژن از غدههای جنسی | |
| هورمون آنتی دیورتیک (ADH) - پپتید | تحریک بازجذب آب توسط کلیهها | |
| اکسیتوسین -پپتید | تحریک انقباضات رحم در حین زایمان | |
| تیروئید | تیروکسین (T4) - آمین | تحریک نرخ متابولیسم پایه بدن |
| ترییدوتیرونین (T3) - آمین | ||
| کلسیتونین - پپتید | کاهش سطح یون کلسیم خون | |
| پاراتیروئید | هورمون پاراتیروئید (PTH) - پپتید | افزایش سطح یون کلسیم خون |
| فوقکلیه (قشر) | آلدسترون - استروئید | افزایش سطح یون سدیم خون |
| کورتیزول، کورتیکوسترون، کورتیزون - استروئید | افزایش سطح گلوکز خون (قند خون) | |
| فوقکلیه (بخش میانی) | اپینفرین، نوراپینفرین - آمین | تحریک پاسخ جنگ و گریز |
| پینهآل | ملاتونین - آمین | تنظیم چرخه خواب |
| پانکراس (لوزالمعده) | انسولین - پپتید | کاهش میزان گلوکز خون |
| گلوکاگون - پپتید | افزایش سطح گلوکز خون | |
| بیضه | تستسترون - استروئيد | تحریک شکلگیری صفات ثانویه جنسی مردانه و تولید اسپرم |
| تخمدان | استروژن و پروژسترون - استروئید | تحریک شکلگیری صفات ثانویه جنسی زنانه و آمادهسازی بدن برای باروری و زایمان |
انواع هورمونها
هورمونها پیامرسانهای شیمیایی بدن هستند که در فعالیتهای مختلف نقشهایی حیاتی دارند. به روشهای مختلف میتوان این مولکولهای زیستی را دستهبندی کرد تا درک بهتری نسبت به نحوه کار، جابهجایی و خصوصیات ساختاری و مولکولی آنها به دست آورد. تا اینجای این مطلب از مجله فرادرس یاد گرفتیم که هورمون چیست، بنابراین در این بخش قصد داریم به سراغ روشهای دستهبندی هورمونها برویم تا اطلاعات مربوط به هورمونها را به روش موثری طبقهبندی کنیم.
بررسی بیوشیمی هورمونها در درک بهتر فعالیتهای این پیامرسانهای شیمیایی کمک شایان توجهی میکند، برای یادگیری کامل و بهتر این مبحث فیلم آموزش جامع و به زبان ساده بیوشیمی عمومی را توصیه میکنیم. لینک این فیلم آموزشی در کادر زیر در دسترس شما است.
انواع هورمونها بر اساس ساختار شیمیایی
تقسیمبندی هورمونها بر اساس ساختار شیمیایی آنها باعث میشود که درک بهتری از فعالیتهای تنظیمی هر نوع از آنها در بدن داشته باشیم. دستهبندی هورمونها بر این اساس، از این جهت اهمیت دارد که ساختار شیمیایی یک هورمون تعیینکننده موارد زیر است.
- انحلالپذیری
- ساختار مولکولی
- روش انتقال
- نحوه برقراری ارتباط هورمون با سلول هدف

هورمونهای بدن انسان از لحاظ ساختار شیمیایی به ۵ دسته اصلی تقسیم میشوند.
- هورمون های استروئيدی
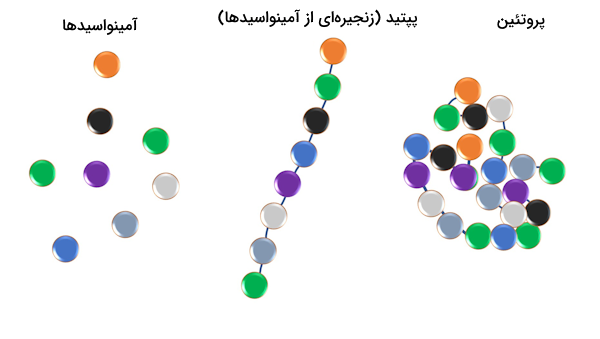
- هورمونهای پروتئینی یا پپتیدی
- هورمونهای مشتق شده از آمینواسیدها
- هورمونهای گلیکوپروتئینی
- هورمونهای ایکوزانوئیدی
در جدول زیر ضمن معرفی دستههای مختلف هورمونی، مشخص کردهایم که ماده سازنده هر هورمون چیست.
| دسته هورمونی | اجزا | مثال |
| هورمونهای آمینی | آمینواسیدهایی با گروههای جانبی تغییرکرده | نوراپینفرین |
| هورمونهای پپتیدی | زنجیرههای آمینواسیدی کوتاه | اکسیتوسین |
| هورمونهای پروتئینی | رشتههای پلیپپتیدی ساخته شده از آمینواسید | هورمون رشد انسانی |
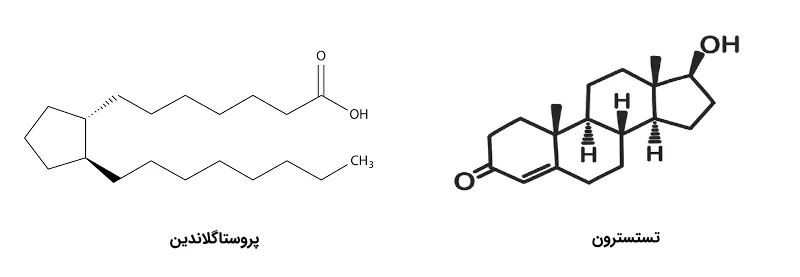
| هورمونهای استروئیدی | مشتق شده از کلسترول | تستسترون و پروژسترون |
| هورمونهای گلیکوپروتئینی | پروتئین و گروه کربوهیدرات | TSH و LH |
| هورمونهای ایکوزانوئیدی | مشتق شده از اسیدهای چرب | پروستاگلاندینها |
هورمونهای استروئیدی
هورمونهای استروئیدی از کلسترول ساخته میشوند و محلول در چربی هستند. به دلیل طبیعت آبگریز این هورمونها، جابهجایی آنها در خون به کمک حاملهای پروتئینی اتفاق میافتد.

محل گیرندههای هورمونهای استروئیدی درون سلول است، زیرا قادر به عبور از دو لایه فسفولیپیدی غشا سلولی هستند و به این ترتیب پاسخهای سلولی بلندمدتی را به راه میاندازند. در جدول زیر تعدادی از هورمونهای استروئیدی را معرفی کردهایم.
| هورمونهای استروئیدی و اثرات آنها | |
| تستسترون و دیهیدروتستسترون (آندروژنها) | تنظیم ویژگیهای مردانه و فعالیتهای تولیدمثلی |
| استرادیول، استرون، استریول (استروژنها) | اثرگذار در فعالیتهای تولیدمثلی زنان و توسعه صفات جنسی ثانویه |
| پروژسترون | تاثیر در حفظ بارداری |
| کورتیزول و کورتیزون | نقش کلیدی در متابولیسم گلوکز و پاسخهای ضدالتهابی |
| آلدوسترون | حفظ تعادل آب و الکترولیتهای بدن |
هورمونهای پروتئینی یا پپتیدی
هورمونهای پپتیدی زنجیرههای آمینواسیدی هستند که گستره وسیعی از پپتیدهای کوچک تا هورمونهای بزرگ را در برمیگیرند. این هورمونها آبدوست و محلول در آب هستند، بنابراین به سادگی در جریان خون جابهجا میشوند. با توجه به عدم توانایی هورمونهای پپتیدی برای عبور از غشا سلولی، گیرندههای آنها روی سطح سلولهای هدف قرار دارند.
نیمهعمر هورمونهایی با ساختار پپتیدی به طور معمول کوتاه است و پاسخهایی کوتاهمدت ایجاد میکنند. در ادامه تعدادی از مهمترین هورمونهای این دسته را معرفی میکنیم.
| هورمونهای پپتیدی و اثرات آنها | |
| انسولین | تنظیم قند خون |
| هورمون رشد | تحریک رشد و تقسیم سلولی |
| اکسیتوسین | موثر در زایمان و شیردهی |
| هورمون محرکه فولیکولی (FSH) | تنظیم فرآیندهای تولیدمثلی |
هورمونهای مشتق شده از آمینواسیدها
آمینواسیدهای «تیروزین» و «تریپتوفان» پیشساز این دسته از هورمونها هستند. بر اساس ساختار نهایی، امکان دارد هورمون آبدوست یا آبگریز باشد و همین موضوع محل جایگیری گیرنده هورمون را تعیین میکند. برای مثال گیرنده هورمونهای آبدوستی مانند کاتکولآمینها سطح سلول است؛ در حالی که هورمونهای تیروئیدی به گیرندههای درون سلولی متصل میشوند، زیرا ساختاری آبگریز دارند.
| هورمونهای مشتق شده از آمینواسیدها و اثرات آنها | |
| اپینفرین و نوراپینفرین (کاتکولآمینها) | موثر در پاسخ جنگ و گریز |
| دوپامین | اثرگذار روی خلق و خو و حرکات بدن |
| هورمونهای تیروئیدی (T3 و T4) | تنظیم متابولیسم و رشد |
هورمونهای گلیکوپروتئینی
هورمونهای گلیکوپروتئینی حاصل اتصال پروتئینها به گروههای کربوهیدرات مانند مانوز یا فوکوز هستند. این هورمونها ساختارهایی پیچیده و نقشهای تنظیمی منحصر به فردی دارند. در جدول زیر با تعدادی از شناختهشدهترین هورمونهای این دسته آشنا میشویم.
| هورمونهای گلیکوپروتئینی و اثرات آنها | |
| هورمون محرک تیروئید (TSH) | تحریک غده تیروئید |
| هورمون لوتئینهکننده (LH) | تنظیم فعالیتهای تولیدمثلی |
| FSH | فرآیندهای تولیدمثلی |
هورمونهای ایکوزانوئیدی
ایکوزانوئیدها از اسیدهای چرب، به خصوص آراشیدونیک اسید مشتق میشوند. به طور معمول این هورمونها عمر کوتاهی دارند و به صورت محلی یعنی پاراکرین یا اتوکرین فعالیت میکنند. ایکوزانوئیدها در پاسخهای التهابی، انقباضات ماهیچهای و عملکرد عروق نقش دارند.
| هورمونهای ایکوزانوئیدی و اثرات آنها | |
| پروستاگلاندینها | تنظیم التهاب، انقباضات ماهیچهها و رشد سلولی |
| ترومبوکسان و پروستاسیکلین | نقش در انعقاد خون و عملکرد عروق |
| لکوترین | میانجیگر در پاسخهای ایمنی و واکنشهای آلرژیک |
انواع هورمونها بر اساس فاصله بین محل سنتز و سلول هدف
هورمونها را میتوان بر اساس فاصلهای که بین غده سازنده آنها با محل اثر هورمون دارند، به سه دستهای تقسیم کرد که در ادامه نام میبریم.
- «هورمونهای اندوکرین» (Endocrine Hormones)
- «هورمونهای پاراکرین» (Paracrine Hormones)
- «هورمونهای اتوکرین» (Autocrine Hormones)
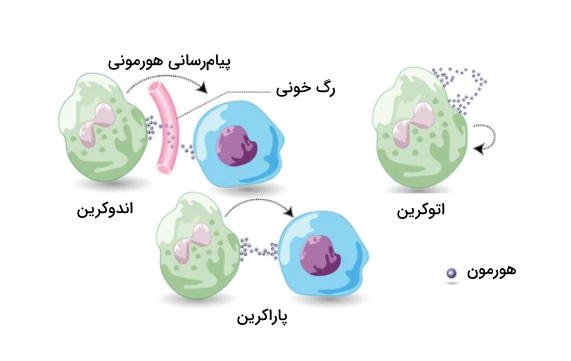
هورمونهای اندوکرین
سلولهای هدف هورمونهای اندوکرین با محل تولید این هورمونها فاصله زیادی دارد. این هورمونها پس از سنتز در سلولهای اندوکرین (سلولهای درونریز) به جریان خون ترشح میشوند تا به کمک آن در بدن جابهجا شوند و به بافت یا اندام هدف خود برسند.
به طور معمول هورمونهای اندوکرین پاسخهای آهستهتری را در بدن ایجاد میکنند، اما اثرات آنها بلندمدت است. برای مثال هورمون FSH و LH توسط «غده هیپوفیز قدامی» (Anterior Pituitary Gland) تولید میشوند، سپس به کمک گردش خون خود را به اندامهای تولیدمثلی یعنی تخمدانها و بیضهها میرسانند.
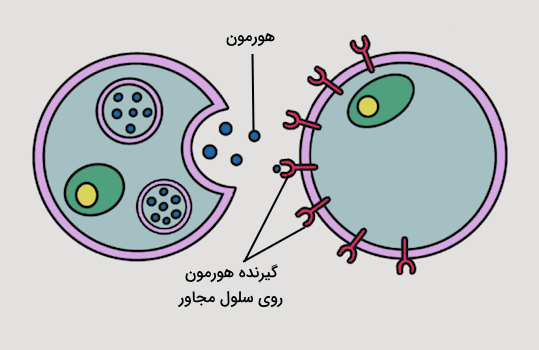
هورمونهای پاراکرین
هورمونهای پاراکرین روی سلولهای نزدیکی اثر میگذارند که همسایه سلولهای تولیدکننده هورمون هستند. این هورمونها به مایع خارج سلولی ترشح میشوند و وارد جریان خون نمیشوند. اثر هورمونهای پاراکرین کوتاهمدت است، اما میتوانند به سرعت پاسخهای مدنظر خود را ایجاد کنند.
«سوماتواستاتین» (Somatostatin) نمونهای از هورمونهای پاراکرین است که توسط سلولهای دلتای پانکراس ترشح میشود. این هورمون از ترشح انسولین از سلولهای بتا و گلوکاگون از سلولهای آلفای پانکراس جلوگیری میکند. محل قرارگیری هر دو این سلولها نزدیک به سلولهای دلتا است و به همین دلیل سوماتواستاتین با آزاد شدن در مایع خارج سلولی میتواند اثرات خود را اعمال کند.
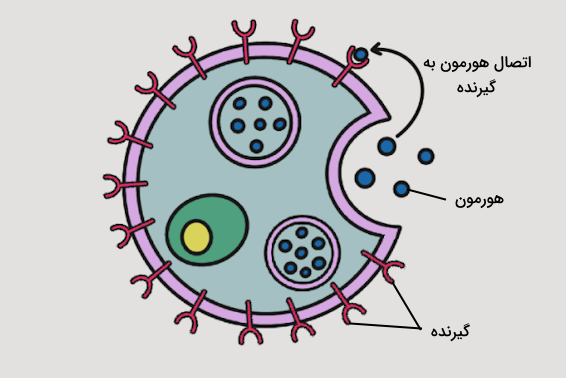
هورمونهای اتوکرین
هورمونهای اتوکرین روی سلولهای سازنده خود یا سلولهایی مشابه با آنها اثرگذار هستند و فرآیندهای درون این سلولها را تحت تاثیر قرار میدهند. برای مثال «فاکتور رشد شبه انسولین ۱» (IGF1) از سلولهایی مانند فیبروبلاستها و استئوبلاستها ترشح میشود، سپس به گیرندههای خود روی سلولها مشابه متصل شده و گسترش و رشد سلول را تحریک میکند.
انواع هورمونها بر اساس مکانیسم فعالیت
هورمونها را میتوان بر اساس مکانیسم فعالیت آنها نیز دستهبندی کرد. مکانیسم فعالیت به نحوه ارتباط گیرنده با هورمون و اثرگذاری روی سلول هدف اشاره دارد. با معیار قرار دادن مکانیسم فعالیت، هورمونها را به دو دسته تقسیم میکنند که در ادامه با آنها آشنا میشویم.
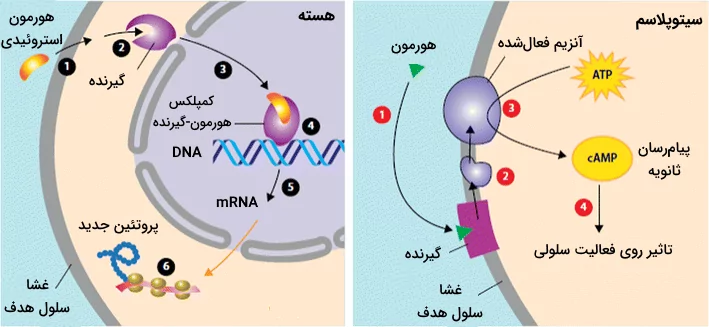
- هورمونهای گروه ۱: این هورمونها لیپیددوست هستند و به سادگی از غشای سلولی عبور میکنند و به گیرندههای درونسلولی متصل میشوند تا «کمپلکس هورمون-گیرنده» (HRC) تشکیل شود. این کمپلکس وارد هسته سلول شده و با DNA برای تنظیم بیان ژن ارتباط برقرار میکند. این هورمونها به کمک پروتئینهای حامل در خون حرکت میکنند به همین دلیل نیمهعمر آنها افزایش یافته و ساعتها یا حتی روزها در خون حضور دارند. تستسترون، پروژسترون و هورمونهای تیروئیدی ازجمله این هورمونها هستند.
- هورمونهای گروه ۲: هورمونهای این گروه توانایی عبور از غشا را ندارند، بنابراین به گیرندههایی که روی سطح سلول هستند، متصل میشوند. این اتصال، پیامرسانهای ثانویه را درون سلول فعال میکند تا آنها پیام هورمون را در سلول پیادهسازی کنند. این هورمونها اغلب نیمهعمر کوتاهی در حد چند دقیقه دارند. زیرگروههای این هورمونها بر اساس نوع پیامرسان ثانویه شکل گرفتهاند.
- هورمونهایی که از cAMP استفاده میکنند.
- هورمونهایی که از فسفولیپید، اینوزیتول یا استفاده میکنند.
- هورمونهایی که پیامرسانهای ثانویه ناشناخته دارند.
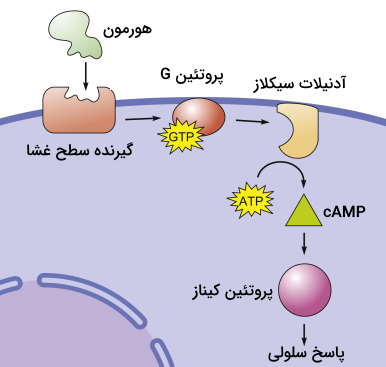
انواع هورمونها بر اساس تحریککنندگی غدد درونریز
اگر بخواهیم هورمونها را بر اساس فعالیتهای خاص و محلهای اثرگذاری که در بدن دارند، تقسیم کنیم؛ به این ۳ دسته میرسیم.
- «هورمونهای تروفیک» (Trophic Hormones): هورمونهای تروفیک محرک رشد و گسترش بافتها و اندامها هستند، آنها تکثیر و افزایش اندازه سلولها در بافتهای هدف را تحریک میکنند. برای مثال «TSH» هورمونی محرک برای غده تیروئید است و باعث رشد و فعالیت این غده میشود. «ACTH» نیز اندازه و فعالیت سلولها را در غده فوقکلیه افزایش میدهد. ترشح بیش از حد این دسته از هورمونها میتواند باعث رشد غیرطبیعی بافت هدف شده و منجر به بروز بیماری شود.
- «هورمونهای گرایشی» (Tropic Hormones): هورمونهای گرایشی غدد را برای ترشح هورمونها تحریک میکنند و تاثیری روی بافت غدد نمیگذارند. این هورمونها به عنوان حدواسطهایی در مسیرهای هورمونی عمل میکنند. برای مثال «GnRH» توسط هیپوتالاموس برای تحریک هیپوفیز قدامی به منظور تحریک ترشح FSH و LH آزاد میشود. سپس این هورمونها روی عملکرد بیضه یا تخمدان اثر میگذارند. هورمونهای گرایشی برای حفظ ارتباطات بین غدد درونریز بدن و هماهنگی فرآیندهای پیچیده بدن حیاتی هستند.
- «هورمونهای بدون گرایش» (Non-Tropic Hormones): هورمونهای بدون گرایش به طور مستقیم سلولهای متعلق به بافت و اندامهای غیردرونریز را هدف قرار میدهند و اثری روی غدد درونریز ندارند. هورمون آنتیدیورتیک یا ضدادرار از مثالهای این دسته است که از هیپوفیز خلفی ترشح شده و روی کلیهها اثر میگذارد.
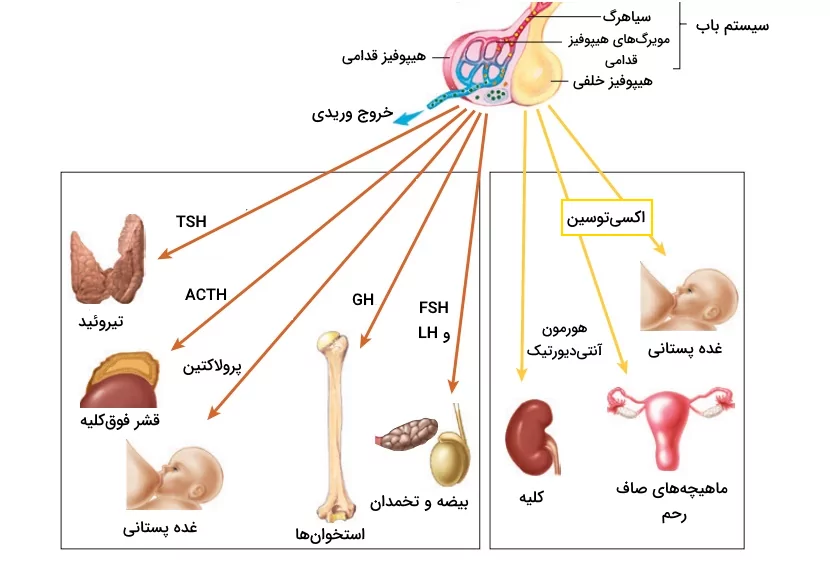
انواع هورمونها بر اساس ماهیت فعالیت
هورمونها را میتوان با توجه به ماهیت فعالیت آنها، به خصوص نحوهای که اثر خود را بر بدن اعمال میکنند، دستهبندی کرد. این کار به تشریح وظایف خاص و مکانیسم عمل آنها کمک میکند. بر همین مبنا، هورمونها به دو دسته اصلی و تعدادی زیر گروه تقسیم میشوند.
- هورمونهای موضعی
- هورمونهای عمومی
در ادامه با این دو نوع و زیرگروهای آنها بیشتر آشنا میشویم تا دید واضحتری از این موضوع به دست آوریم که هورمون چیست.
هورمونهای موضعی
این هورمونها در وهله اول روی سلولهای اطراف سلول ترشحکننده خود اثر میگذارند، سپس از طریق جریان خون به بخشهای مختلف بدن میروند. فعالیت این هورمونها را در اغلب مواقع به صورت پاراکرین میدانیم که نشاندهنده این است که این هورمونها روی سلولهای همسایه در همان بافتی که از آن ترشح شدهاند، اثر میگذارند.
خصوصیات هورمونهای موضعی
به طور کلی این هورمونها اثرگذاری سریعی دارند و مدت زمان زیادی برای اعمال اثر خود نیاز ندارند، به همین دلیل برای پاسخهای فیزیولوژیک بدن گزینههایی مناسب هستند. این هورمونها در بافتهای خاصی تولید و آزاد میشوند و بدون استفاده از گردش خون وظایف خود را انجام میدهند. ازجمله هورمونهای موضعی میتوان به این دو مورد اشاره کرد.
- تستسترون: با وجود اینکه این هورمون اثرات عمومی نیز بر بدن دارد، میتواند روی سلولهای همسایه در بیضهها برای کمک به اسپرماتوژنسیس و دیگر فعالیتهای بیضهها اثر بگذارد.
- پروستاگلاندینها: این ترکیبات محلول از اسیدهای چرب ساخته میشوند و التهاب، پیام درد و دیگر پاسخهای موضعی نقش دارند.
هورمونهای عمومی
برخلاف هورمونهای موضعی، هورمونهای عمومی از طریق سیستم گردش خون به نقاط دیگر بدن میروند تا بافتها یا اندامهایی غیر از اندام ترشحکننده خود را تحت تاثیر قرار بدهند. تاثیرات این هورمونها فراگیر است و فرآیندهای فیزیولوژیکی متعددی را در دستگاههای مختلف بدن هدف میگیرند.
خصوصیات هورمونهای عمومی
به طور معمول هورمونهای عمومی نیمهعمرهای طولانی دارند و میتوانند اثر خود را در طی یک بازه زمانی بلندمدت روی بدن اعمال کنند؛ به همین دلیل این هورمونها برای تنظیم فعالیتهای فیزیولوژیکی بلندمدت بسیار ضروری هستند. این هورمونها میتوانند اثرات گستردهای داشته باشند و اغلب در حفظ هومئوستازی یا شروع پاسخهای پیچیده در بدن نقش دارند. دو هورمونی که در ادامه نام میبریم از مثالهای هورمونهای عمومی هستند.
- هورمونهای تیروئیدی (T۳ و T۴): این هورمونها متابولیسم و تولید انرژی در بدن را تنظیم میکنند و اندامهای گوناگونی مانند قلب، کبد و ماهیچهها را تحت تاثیر قرار میدهند.
- انسولین: این هورمون توسط پانکراس ترشح میشود و در تنظیم سطح قند خون نقشی کلیدی دارد. نحوه عمل انسولین به این صورت است که دریافت گلوکز را در بافتهای مختلف بدن آسان میکند و به این ترتیب تعادل انرژی در بدن را حفظ میکند.
انواع هورمونها بر اساس اثرات آنها
هورمونها را میتوانیم بر اساس اثرات آنها روی فرآیندهای فیزیولوژیکی بدن نیز دسته بندی کنیم. این دستهبندی اثرات گوناگون هورمونها در تنظیم فعالیتهای زیستی مختلف را مشخص میکند و شامل این سه گروه اصلی است.
- «هورمونهای سینتیکی» (Kinetic Hormones)
- «هورمونهای متابولیسمی» (Metabolic Hormones)
- «هورمونهای ریختزایی» (Morphogenetic Hormones)
در ادامه با این هورمونها و خصوصیات مربوط به آنها بیشتر آشنا میشویم.

هورمونهای سینتیکی
این هورمونها مسئول تسهیل حرکت و تغییرات فیزیولوژیکی در بدن هستند. آنها فعالیتهای مختلفی را به راه میاندازند که مثالهای زیر ازجمله این فعالیتها هستند.
- انقباض عضلات
- ترشحات غدد مختلف
ازجمله خصوصیات این هورمونها میتوان به اثرات سریع آنها اشاره کرد که باعث ایجاد پاسخهای فیزیولوژیکی آنی میشود. هورمونهای سینتیکی میتوانند گستره وسیعی از فعالیتهای مختلف، مانند اعمال بافتهای ماهیچهای، پوششی و اندوکرین را تحت تاثیر قرار بدهند. در ادامه سه مورد از هورمونهای سینتیکی را معرفی میکنیم.
- «هورمون محرک ملانوسیت» (Melanocyte-Stimulating Hormone | MSH): در تنظیم رنگدانههای پوست به وسیله تحریک ملانوسیتها برای تولید رنگدانه، نقش دارند.
- «اپینفرین» (Epinephrine): اپینفرین یا آدرنالین یکی از هورمونهای کلیدی در پاسخ جنگ و گریز است. این هورمون انقباض ماهیچهها را تقویت میکند و همچنین ضربان قلب و فشار خون به سمت ماهیچهها را افزایش میدهد.
- هورمونهای پینهآل: این هورمونها و به طور خاص «ملاتونین»، روی چرخه شبانهروزی بدن و الگوی خواب تاثیر میگذارند و به این ترتیب روی فرآیندهای فیزیولوژیکی گوناگونی اثرگذار هستند.
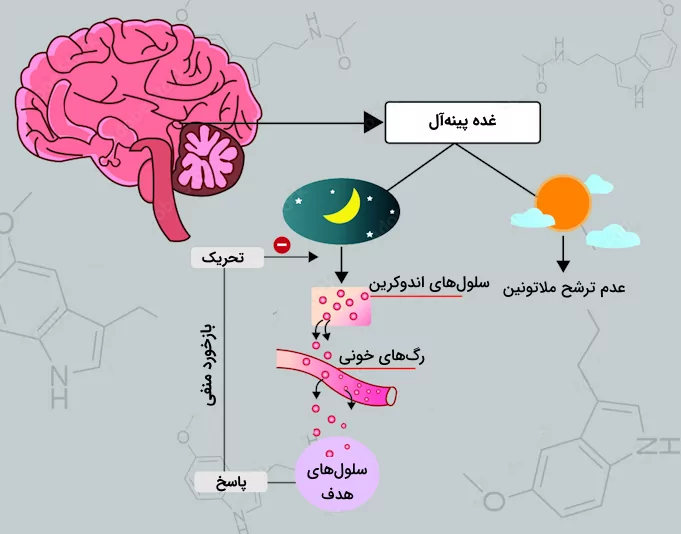
هورمونهای متابولیسمی
هورمونهای متابولیسمی اثرات بسیار مهمی روی متابولیسم بدن و حفظ تعادل انرژی بدن دارند. این دسته از هورمونها روی نحوه استفاده بدن از مواد مغذی اثر گذاشته و ذخایر انرژی بدن را مدیریت میکنند. هورمونهای متابولیسمی هم میتوانند میزان متابولیسم را افزایش دهند و هم میتوانند آن را کاهش دهند، آنها این اثرات متفاوت را بر اساس نیاز بدن اعمال میکنند. این هورمونها در فرآیندهایی مانند تنظیم سطح گلوکز، متابولیسم چربی و هومئوستازی کلی بدن فعال هستند. در ادامه با تعدادی از آنها آشنا میشویم.
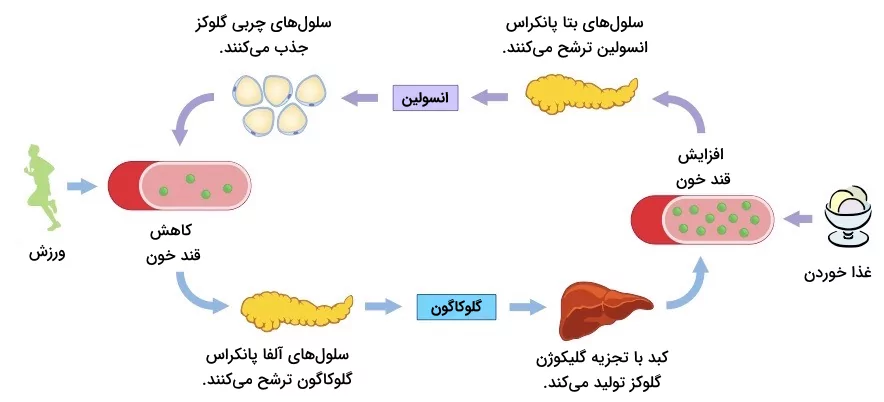
- «گلوکاگون» (Glucagon): گلوکاگون توسط پانکراس برای افزایش سطح گلوکز خون ترشح میشود. این هورمون با تحریک کبد برای «گلیکوژنولیز» و «گلوکونئوژنز» نقش خود را ایفا میکند.
- «انسولین» (Insulin): انسولین نیز توسط پانکراس تولید میشود اما هدف آن افزایش جذب گلوکز توسط سلولهای بدن و کاهش میزان قند خون است. انسولین در تنفس سلولی نیز همکاری میکند.
- «هورمون پاراتیروئید» (Parathyroid Hormone | PTH): این هورمون متابولیسم کلسیم و فسفات را تنظیم میکند و به این ترتیب سلامت استخوان و متابولیسم مواد معدنی را تحت تاثیر قرار میدهد.
هورمونهای ریختزایی
این هورمونها برای رشد، تمایز و نمو در بدن ضروری هستند و فرآیندهایی را به راه میاندازند که به تغییرات ساختاری و بلوغ در بسیاری از بافتها منتهی میشوند. هورمونهای ریختزایی یا «هورمونهای مورفوژنتیکی» برای مراحل تمایز و تعمیر و بازسازی بافت اهمیت زیادی دارند. آنها به طور معمول رشد اندامها و دستگاههای بدن را تحت تاثیر قرار میدهند و باعث ایجاد فعالیت سلولی مناسب میشوند. در ادامه سه مثال از این هورمونها آوردهایم.
- «هورمون محرک فولیکولی» (Follicle-Stimulating Hormone | FSH): رشد و بلوغ فولیکولهای تخمدان را در زنان افزایش میدهد و در مردان باعث تحریک اسپرماتوژنوسیس میشود.
- «هورمون رشد» (Growth Hormone | GH): باعث رشد، تقسیم سلولی و بازسازی در بدن انسان و حیوانات میشود.
- «هورمونهای تیروئیدی» (Thyroid Hormones): هورمونهای تیروئیدی یعنی T۳ و T۴ فرآیندهای متابولیسمی زیادی را تنظیم میکنند، علاوه بر این برای رشد و نمو عادی بدن، به خصوص دستگاه عصبی، ضروری هستند.
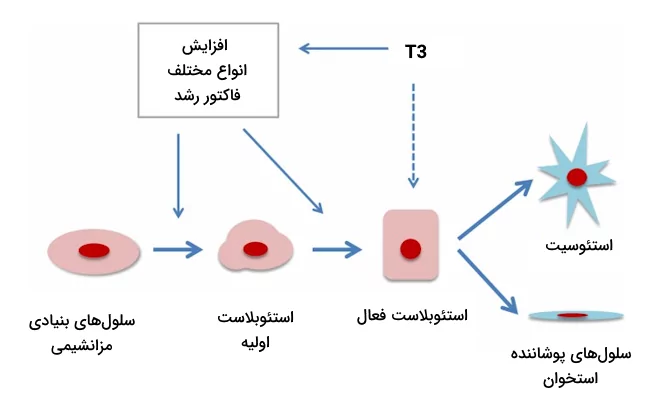
کار هورمون چیست؟
با یاد گرفتن این که هورمون چیست، تا حدی راجع به فعالیتهای هورمون نیز آموختیم، اما به طور ساده میتوان هورمونها را مسئول برقراری ارتباط بین اندامهای مختلف بدن دانست. به همین دلیل این مولکولهای شیمیایی در بدن کاربردهای بسیاری دارند و بر سلامت جاندار زنده اثرگذار هستند. هورمونها میتوانند پیامهای بسیار متنوعی را به سلولها برسانند و فعالیتهای سلولی را تغییر بدهند.
در این بخش قصد داریم راجع به مهمترین فعالیتهایی که در بدن به حضور هورمونها وابسته هستند، صحبت کنیم. این فعالیتهای هورمونی در بدن انسان شامل مواردی است که در ادامه نام میبریم.
- فعالیتهای تنظیمی و هومئوستازی
- رشد و نمو
- تحریک فعالیت هورمونهای دیگر
- تولیدمثل
- تنظیم تعادل انرژی در بدن
- کنترل مرگ برنامهریزی شده سلول
- فعالسازی یا مهار فعالیت سیستم ایمنی
در ادامه با جزئیات مربوط به هر یک از این موارد آشنا میشویم تا درک کاملتری نسبت این که فعالیت هورمون چیست، به دست بیاوریم.
فعالیتهای تنظیمی و هومئوستازی
هورمونها یک محیط داخلی باثبات را به کمک تنظیم مواردی مثل فشار خون، تعادل مایعات و ترکیب الکترولیتها در بدن میسازند. «وازوپرسین» و «آلدسترون» هورمونهای اصلی در هومئوستازی هستند. این دو هورمون تعادل الکترولیتها و آب بدن را تحت کنترل دارند و به همین دلیل روی فشار خون و حجم مایع خارج سلولی اثرگذار هستند.
مدیریتی که هورمونها روی بافتهای دیگر دارند فقط به تنظیم فشار خون محدود نمیشود. تنظیم فعالیت و اطمینان از سلامتی استخوانها، ماهیچهها و ذخایر چربی توسط همکاری بین هورمونهای PTH، استروژنها، آندروژنها، هورمون رشد، انسولین، گلوکاگون و کاتکولآمین صورت میگیرد. هورمون پاراتیروئید، کلسیتونین و ۱ و ۲۵-دیهیدروکسی-ویتامین D۳ نیز سطح کلسیم و فسفات پلاسما را تنظیم میکنند تا استخوانهای بدن سالم باشند و ماهیچهها بتوانند فعالیت خود را به درستی انجام دهند.

رشد و نمو
هورمونهایی مانند هورمون رشد، هورمونهای تیروئیدی و «فاکتورهای رشد شبهانسولینی» (IGFs) جزو محورهای اصلی کنترل رشد بدن و گسترش بافتها هستند. هورمون رشد با استفاده از فاکتور رشد شبهانسولینی، رشد بدن را تحریک میکند اما از طرفی IGFs نیز برای به حداکثر رساندن فعالیت خود به تیروکسین نیاز دارد. در حقیقت هورمون رشد بدون تیروکسین نمیتواند باعث رشد بهینه اسکلت بدن شود.
این هورمونها مراحل اولیه تقسیم و تمایز سلولی را نیز تنظیم میکنند، بنابراین میتوان گفت که برای رشد و نمو جنین حیاتی هستند. اما فعالیت این هورمونها فقط تحریک رشد نیست و میتوانند دستور مهار رشد را نیز بدهند. برای مثال سوماتواستاتین از تولید و ترشح بسیاری از هورمونهای سیستم درونریز بدن جلوگیری میکند که هورمون رشد، هورمون محرک غده تیروئید و پرولاکتین ازجمله مثالهای هورمونهای هدف قرار گرفته توسط سوماتواستاتین هستند.

تحریک فعالیت هورمونهای دیگر
هورمونها قادر به افزایش فعالیت مواد یا هورمونهای دیگر هستند و به این ترتیب از فعالیت درست و بهینه سلولها و حرکت مواد به درون یا بیرون از بدن اطمینان مییابند. برای مثال تیروکسین باعث میشود که هورمون رشد حداکثر اثر خود را روی رشد اسکلت بدن بگذارد و به این ترتیب فعالیتهای مشترکی که دارند به درستی پیش میرود.
تولیدمثل
فعالیت هورمونها در مرکز فرآیندهای تولیدمثلی بدن قرار دارد. ازجمله این فعالیتها میتوان به رشد و فعالیت اندامهای تولیدمثلی، گامتزایی و رفتارهای جنسی اشاره کرد. استروژنها و تستسترون گسترش صفات اولیه و ثانویه جنسی را تحت تاثیر قرار میدهند. گنادوتروپینهایی مانند LH و FSH، تخمکگذاری در زنان و اسپرماتوژنوسیس در مردان را تنظیم میکنند تا باروری و سلامت تولیدمثلی فرد تضمین شود.
تنظیم تعادل انرژی در بدن
هورمونها نقشی اساسی در حفظ هومئوستازی انرژی بازی میکنند و تاثیر خود را از طریق ایجاد تعادل بین میزان دریافت انرژی بدن و هزینه این انرژی برای فعالیتهای مختلف پیادهسازی میکنند. هیپوتالاموس پیامهای گرسنگی و نرخ متابولیسمی بدن را زیر نظر داشته و آنها را هماهنگ میکند. هورمونهایی مانند انسولین، گلوکاگون و هورمونهای تیروئیدی روش ذخیره و مصرف انرژی در بدن را تحت تاثیر قرار میدهند.
کنترل مرگ برنامهریزیشده سلول
مرگ برنامهریزی شده سلول که به آن «آپوپتوز» میگوییم، تحت تاثیر فعالیت هورمونهای گوناگونی مانند سایتوکاینها و فاکتورهای رشد قرار دارد. این هورمونها میتوانند آپوپتوز را مهار کنند اما هورمونهای دیگر نیز قادر به القای دستور آپوپتوز به سلولها هستند. به عنوان مثال هورمونهای استروئیدی تنظیمکنندههای بالقوه آپوپتوز در سلولهای وابسته به استروئیدها و بافتهایی مثل بافت غده پستان، پروستات، تخمدانها و بیضهها هستند.

فعالسازی یا مهار فعالیت سیستم ایمنی
در سطح سلولهای سیستم ایمنی گیرندههای به خصوصی وجود دارد که هورمونهای استروئيدی به آنها متصل میشوند و باعث سازگاری فعالیتهای مختص به همان نوع سلول میشوند. خودتنظیمی منفی باعث مهار پیامهای هورمونی بالادست میشود، حتی خود سلولهای ایمنی قادر به کنترل ترشح هورمونهای بالادست به وسیله ترشح سایتوکاینها در نواحی خاصی از مغز هستند.
انتقال و متابولیسم هورمونها
تا اینجا متوجه شدیم که هورمون چیست، در این بخش قصد داریم به روشهای انتقال و متابولیسم هورمونها بپردازیم؛ زیرا این موارد در تعیین کارآیی و مدت زمان فعالیت هورمون در بدن اثرگذار هستند. پس از سنتر و ترشح هورمونها، این مولکولهای زیستی باید همراه با گردش خون خود را به سلولهای هدف برسانند و اثرات فیزیولوژیک ایجاد کنند، بنابراین در ابتدا به این مسئله میپردازیم که روش انتقال هورمون چیست.
یادگیری پایهای متابولیسم به درک بهتر بسیاری از واکنشهای زیستی کمک میکند، برای آشنایی با بیوانرژتیک و متابولیسم مشاهده فیلم آموزش رایگان بیوانرژتیک و متابولیسم را توصیه میکنیم و برای دسترسی راحتتر لینک آن را در کادر زیر درج کردهایم.
روشهای انتقال هورمون چیست؟
هورمونها در جریان خون میتوانند به دو صورت آزاد و متصل به پروتئینهای حامل حرکت کنند.
- آمینها، پپتیدها و هورمونهای پروتئینی: این دسته از هورمونها به طور معمول به صورت آزاد در خون حرکت میکنند، همین موضوع باعث میشود که سرعت حرکت بالایی داشته باشند و سریع به بافت هدف خود برسند.
- استروئیدها و هورمونهای تیروئیدی: این هورمونها با اتصال به پروتئینهای حامل در جریان خون حرکت میکنند. این اتصال به تثبیت غلظت پلاسمایی آنها کمک میکند که باعث طولانیتر شدن نیمهعمر این هورمونها میشود. برای آشنایی با پروتئینهای حامل، در ادامه تعدادی از رایجترین انواع این پروتئینها را مثال میزنیم.
- «گلوبولین متصلشونده به هورمون تیروئیدی» (TBG): حامل هورمونهای تیروئید
- «گلوبولین متصلشونده به تستسترون» (TeBG): حامل تستسترون
- «گلوبولین متصلشونده به کورتیزول» (CBG): حامل کورتیزول
یکی از استثناهایی که در این دستهبندی وجود دارد مربوط به «فاکتور رشد شبهانسولین» است که هورمونی پلیپپتیدی است اما با اتصال به پروتئینهای خاصی در خون جریان دارد.
مکانیسم فعالیت هورمون چیست؟
هورمونها با رسیدن به بافت هدف میتوانند باعث پاسخهای فیزیولوژیک آنی شوند یا آغازگر تغییراتی بلندمدت باشند. همین نوع تاثیر هورمونها است که ضرورت غیرفعالسازی هورمونها پس از ایجاد تاثیر دلخواه را تعیین میکند، زیرا تحریک هورمونی به صورت مداوم میتواند باعث بروز بیماریهای متعدد شود.
سرعت پاکسازی هورمون چیست؟
«سرعت پاکسازی هورمون» (Metabolic Clearance Rate | MCR) سرعت حذف هورمون از پلاسما را تعیین میکند و نمایشدهنده اثرگذاری و مدت زمان فعالیت هورمون است. در شرایط ثابت و پایدار، MCR به صورت میزان پلاسمای پاکسازی شده در هر واحد زمان تعریف میشود. این واحد اندازهگیری روشی مناسب برای درک تحرک و پویایی هورمونها است.
نیمهعمر یک هورمون در پلاسما بسیار به MCR آن هورمون ربط دارد. مقدار بالای MCR به معنای نیمهعمر پایین است که این گزاره به ما توضیح میدهد که هورمون به سرعت از گردش خون حذف میشود.
جایگاه پاکسازی هورمون چیست؟
کبد و کلیه اندامهای اصلی مسئول در پاکسازی هورمونها هستند. این اندامها از آنزیمهای گوناگونی برای تجزیه بهینه هورمونها استفاده میکنند. فرآیند تجزیه هورمونها شامل موارد زیر است.
- «هیدرولیز» (Hydrolysis): تجزیه ترکیبات مختلف به دلیل واکنش با آب
- «اکسیداسیون» (Oxidation): اضافه کردن اکسیژن یا حذف هیدروژن از ترکیب هدف
- «هیدروکسیلدار کردن» (Hydroxylation): اضافه کردن گروه هیدروکسیل به ساختار مولکول
- «متیلاسیون» (Methylation): اضافه کردن گروه متیل
- «کربوکسیلزدایی» (Decarboxylation):حذف گروه کربوکسیل از ساختار مولکول
- «سولفاته کردن» (Sulfation): اضافه کردن گروه سولفات
- «گلوکورونیداسیون» (Glucuronidation): اتصال اسید گلوکورونیک به ساختار مولکول برای تسهیل دفع به وسیله ادرار

الگوی ترشح هورمون چیست؟
ترشح هورمون فرآیندی پیوسته و مداوم نیست و بین بازههای ترشحی هورمونهای مختلف الگوهای خاصی وجود دارند. کسب اطلاعات راجع به این الگوها باعث میشود که درک بهتری نسبت به نحوه تنظیم فعالیتهای فیزیولوژیکی متفاوت توسط هورمونها به دست بیاوریم. مواردی که در ادامه نام بردیم ازجمله این الگوهای ترشح هستند.
- «ترشح ضربانی» (Pulsatile Secretion)
- «الگوهای دارای ریتم» (Rhythmic Patterns)
- «اثر مکانیسمهای پاسخ» (Influence of Feedback Mechanisms)
در ادامه این الگوها را بیشتر توضیح میدهیم و از تصاویر مختلف برای درک بهتر مفاهیم مربوطه کمک میگیریم تا به طور کامل یاد بگیریم که الگوی ترشح یک هورمون چیست.
ترشح ضربانی هورمون چیست؟
بیشتر هورمونها طبق این الگو ترشح میشوند. بر طبق الگوی ترشح ضربانی هر ۵ الی ۱۰ دقیقه یکبار هورمون ترشح میشود. پس از هر بار ترشح، غلظت پلاسمایی هورمون در بازه زمانی که ترشح هورمون متوقف شده است، کاهش مییابد و به سطح پایه میرسد، بنابراین نیاز است که دوباره هورمون ترشح شود. این چرخه ترشح باعث تنظیم سطح هورمون میشود و نیاز بدن به تدریج و بدون افزایش یکباره میزان هورمون تامین میشود.
الگوهای دارای ریتم ترشح هورمون چیست؟
فراوانی و میزان ترشح هورمونها با توجه به نیازهای فیزیولوژیک و مکانیسمهای تنظیمی میتواند الگوهای متنوعی داشته باشد. در ادامه با این الگوهای دارای ریتم بیشتر آشنا میشویم.
- «ریتم شبانهروزی» (Circadian Rhythm):هورمونهایی که به طور حدودی هر ۲۴ ساعت ترشح میشوند از الگوی شبانهروزی پیروی میکنند. ACTH مثالی از این نوع هورمونها است که صبحها اوج ترشح آن را داریم و در طول روز ترشح این هورمون کاهش مییابد.
- «چرخه تندآهنگ» (Ultradian Rhythm): بازههای زمانی ترشح بعضی از هورمونها کوتاهتر از ۲۴ ساعت است و هر چند ساعت یکبار شاهد ترشح آنها به خون هستیم. هورمونهایی که برای رفع نیازهای متابولیسمی بدن و واکنش به شرایط محیطی ساخته میشوند، ازجمله هورمونهایی با این الگوی ترشحی هستند.
- «چرخه دایرهای» (Circhoral Rhythm): این الگو نوعی خاص از چرخه تندآهنگ است و به هورمونهایی اشاره دارد که به طور تقریبی هر یک ساعت ترشح میشوند. این نوع تنظیم ترشح هورمون به حفظ فعالیتهای فیزیولوژیکی مداوم در بدن کمک میکند.
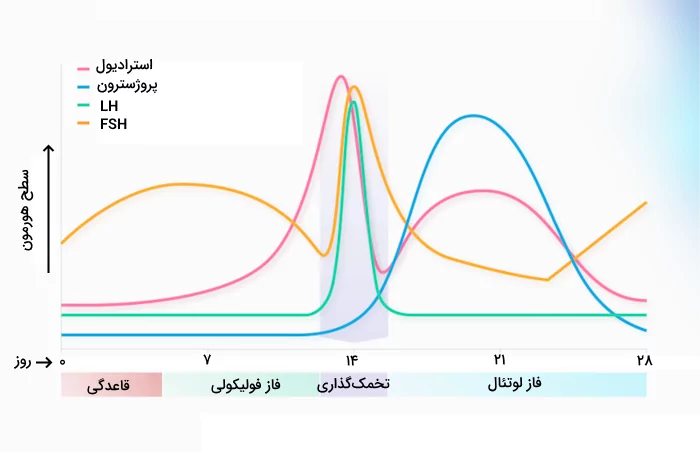
- «چرخه سی روزه» (Circatrigintan Rhythm): بعضی هورمونها مانند گنادوتروپینها، الگوهای ترشحی ماهانه دارند که یعنی به طور حدودی هر سی روز ترشح میشوند. این الگو را به طور خاص در فیزیولوژی تولیدمثلی زنان میبینیم و مثال واضح آن چرخه قاعدگی است.
- «چرخه سالانه» (Circannual Rhythm): هورمونهایی که دورههای سالانه دارند، در طی چند ماه یا چند فصل دچار تغییر میشوند. این الگو به طور معمول به چرخههای تولیدمثلی، تنظیمات متابولیسمی و عادت به تغییراتی محیطی در فصلهای مختلف مربوط است.
- «تغییرات طولانیمدت» (Long-Term Variations): میزان حضور بعضی از هورمونها، مانند تیروکسین، در طول یک بازه زمانی طولانی دچار تغییراتی میشود که نشاندهنده نیاز بدن به تنظیم سطح هورمون در طولانیمدت است. بنابراین این دسته از هورمونها نیازی به بازخوردهای کوتاهمدت ندارند.
اثر مکانیسمهای بازخورد
الگوی ترشح هورمونها تحت تاثیر مکانیسمهای بازخورد، به خصوص خودتنظیمی منفی قرار دارد. حذف یک پیام مهاری میتواند باعث افزایش تشدید پیام و ترشح هورمون شود. این پاسخها برای بهینهسازی سطح پایهای هورمونهای بدن با توجه به شرایط فیزیولوژیک موجود و تحریکات خارجی، ضروری هستند.
کنترل ترشح هورمونها
تنظیم ترشح هورمونها فرآیندی پیچیده و کنترلشده است که برای حفظ هومئوستازی و هماهنگی فعالیتهای بدن ضروری است. سطح هورمونها تحت تاثیر فاکتورهای متعددی مانند پیامهای عصبی، هورمونهای دیگر و بازخوردهای هورمونی، قرار میگیرد. در این بخش قصد داریم به این موضوع بپردازیم که روش کنترل ترشح هورمون چیست و با ذکر مثال هر کدام از روشهای کنترلی را بشناسیم.
کنترل عصبی
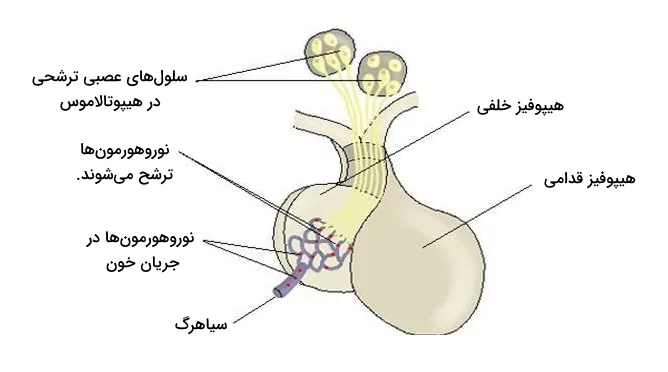
پاسخهای عصبی به صورت مستقیم بعضی از ترشحات دستگاه اندوکرین را کنترل میکنند، به عنوان مثال در شرایط استرسزا یا پاسخهای احساسی، عصبهای اسپلانکیک (Splanchnic Nerve) غدد فوقکلیوی را برای سنتز و ترشح کاتکولآمینهایی مثل اپینفرین و نوراپینفرین تحریک میکنند. همچنین انواعی از گیرندهها به نام «اسمورسپتور» (Osmoreceptor) که در هیپوتالاموس قرار دارند، با تشخیص تغییراتی در فشار اسمزی میتوانند ترشح وازوپرسین از نوروهیپوفیز را تحریک کنند.
محرکهای عصبی که از بخشهای مختلف مغز سرچشمه میگیرند میتوانند باعث آزادسازی انتقالدهندههای عصبی مانند استیلکولین شوند. این ناقلهای عصبی قادر به تنظیم ترشح هورمونهای هیپوتالاموس هستند که در ادامه تعدادی از آنها را نام میبریم.
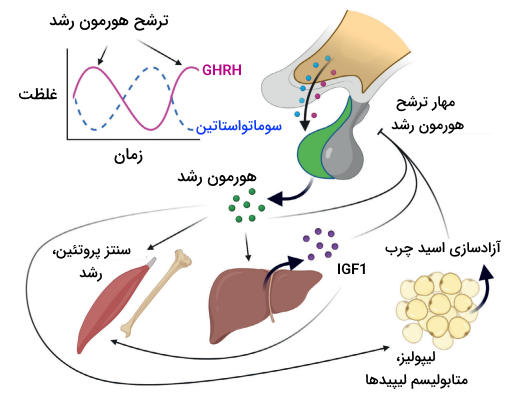
- «هورمون آزادکننده هورمون رشد» (Growth Hormone-Releasing Hormone | GHRH)
- «هورمون آزادکننده کورتیکوتروپین» (Corticotropin-Releasing Hormone | CRH)
- «هورمون آزادکننده تیروتروپین» (Thyrotropin-Releasing Hormone | TRH)
کنترل درونریز
هورمونها به طور معمول ترشح هورمونهای دیگر را تنظیم میکنند و یک سیستم طبقهبندی شده بین غدد مختلف دستگاه درونریز بدن میسازند. برای مثال ACTH از هیپوفیز قدامی ترشح میشود تا ترشح هورمونهای قشر فوقکلیه را تحریک کند. TSH نیز باعث ترشح هورمونهای تیروئيدی میشود.
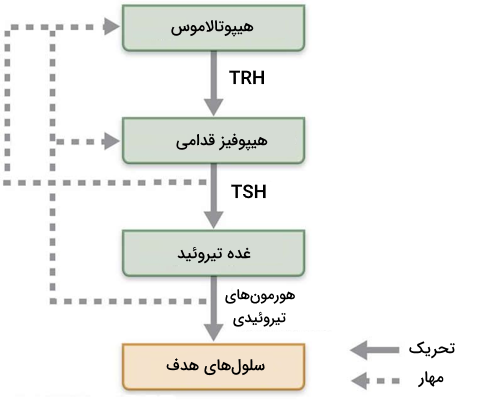
هورمونهای گرایشی ترشح شده از هیپوفیز توسط هورمونهای هیپوتالاموس (CRH و TRH برای دو مثال فوق) تنظیم میشوند و به این ترتیب یک چرخه بازخورد ساخته میشود که از تعادل هورمونی و نیاز بدن به پاسخ فیزیولوژیک اطمینان پیدا میکند.
تنظیم بازخوردی
مکانیسم بازخورد، سیستم تنظیم فیزیولوژی بدن جانداران است که باعث میشود بدن پس از تغییرات گوناگون به شرایط عادی و دلخواه بازگردد، به این فرآیند «هومئوستازی» میگویند. بنابراین مکانیسمهای بازخورد باعث حفظ هومئوستازی بدن میشوند.
بازخوردهای هورمونی نقشی کلیدی در تعدیل ترشح هورمونها دارند. دو نوع بازخورد منفی و مثبت در سیستمهای هورمونی وجود دارد که اهمیت بازخورد یا خودتنظیمی منفی بیشتر از دیگری است و سطح هورمونهای زیادی با استفاده از این مکانیسم تنظیم میشود. در ادامه با هر کدام از این بازخوردها بیشتر آشنا میشویم.
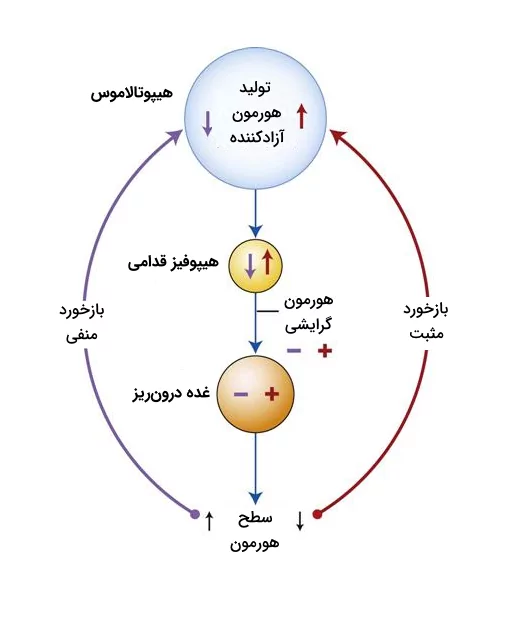
خودتنظیمی یا بازخورد منفی
در خودتنظیمی منفی افزایش غلظت هورمون میتواند به عنوان مانعی برای ترشح همان هورمون عمل کند. این روش کنترلی به منظور حفظ هومئوستازی رایج است. برای مثال افزایش سطح کورتیزول ترشحشده از قشر فوقکلیه باعث آزادسازی ACTH از هیپوفیز و CRH از هیپوتالاموس میشود که فعالیت این دو منجر به کاهش ترشح کورتیزول میشود. البته سطح بالای هورمونهای گرایشی نیز میتواند مانع ترشح فاکتورهای تحریککننده ترشح آنها از هیپوتالاموس شود.
بعضی از متابولیتها و یونها نیز میتوانند روی ترشح هورمونها از طریق همین مکانیسمهای بازخورد اثر بگذارند. به عنوان مثال افزایش میزان کلسیم سرم، باعث کاهش ترشح هورمون پاراتیروئید میشود. میزان بالای گلوکز خون نیز میتواند ترشح گلوکاگون را کاهش بدهد.
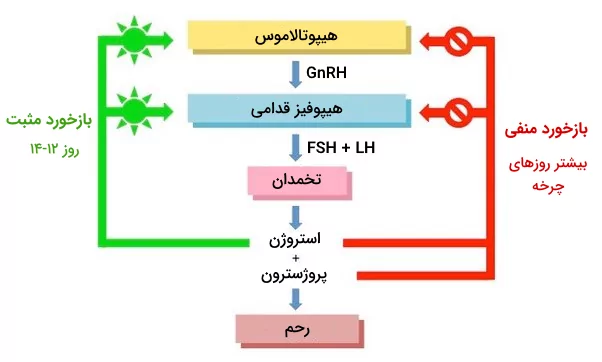
خودتنظیمی یا بازخورد مثبت
در خودتنظیمی مثبت، افزایش سطح هورمون باعث ترشح هر چه بیشتر همان هورمون میشود. افزایش هورمون LH در طول چرخه قاعدگی خانومها ازجمله مثالهای این نوع خودتنظیمی است. افزایش سطح کلسیم سرم نیز باعث تحریک ترشح کلسیتونین از غده تیروئید میشود.
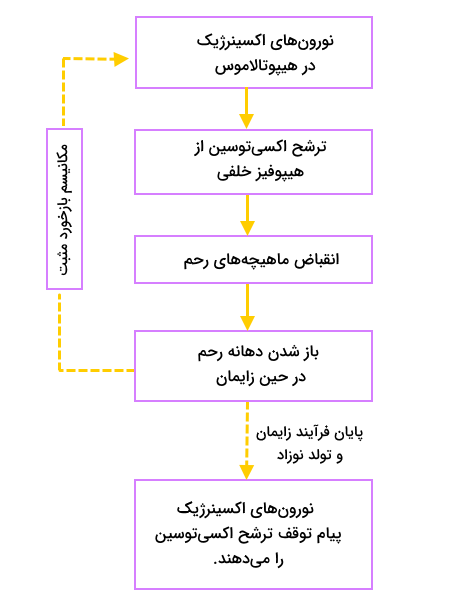
اکسیتوسین نیز یکی دیگر از هورمونهایی است که از فرآیند خودتنظیمی مثبت برای کمک به روند زایمان استفاده میکند. این هورمون برای انقباضات رحم و باز شدن دهانه رحم ضروری است، ترشح بیشتر اکسیتوسین باعث افزایش تحریک هیپوتالاموس و دستور ترشح به میزان بیشتر میشود. بدن این روند ترشحی را تا زمان خاتمه زایمان و به دنیا آمدن نوزاد ادامه میدهد. در تصویر زیر میتوانید جزئیات سلسله مراتب ترشح و فعالیت اکسیتوسین را ببینید.
شناخت هورمونها و انتقالدهندههای عصبی با فرادرس
در جانداران پرسلولی ارتباط بین دستگاهها، اندامها و سلولهای مختلف بدن اهمیت بالایی دارد زیرا تمام این سلولهای مختلف که برای انجام کارهای مختلف تمایز یافتهاند برای بقا به یکدیگر نیاز دارند. انتقالدهندههای عصبی و هورمونها جزو مهمترین مولکولهایی هستند که روی سلولهای مختلف تاثیر میگذارند و فعالیتهای آنها را به شکل دلخواه خود تغییر میدهند. عدم تعادل یا حضور این مولکولهای زیستی متفاوت میتواند منجر به بیماریهای گوناگونی بشود که گاهی مهلک و کشنده هستند.
- فیلم آموزش بیوشیمی ویتامینها و هورمونها فرادرس
- فیلم آموزش بیوشیمی عمومی بخش پروتئین ها و آمینواسیدها فرادرس
- فیلم آموزش بیوشیمی پزشکی ۱ به همراه مفاهیم کلیدی فرادرس
- فیلم آموزش تیروئیدولوژی به همراه آناتومی، علائم و درمان بیماری های غده تیروئید فرادرس
- فیلم آموزش رایگان تفسیر برگه آزمایش هورمونی فرادرس
مکانیسمهای فعالیت هورمونها
فعالیت هورمونها در بدن به مکانیسمهایی تکیه کرده است که به هورمونها اجازه ارتباط بهینه با سلولهای هدف را میدهند. هورمونهای مختلف که توسط غدد مختلف بدن تولید میشوند باید به گیرندههای به خصوصی در سلولهای هدف متصل شوند تا بتوانند اثرات خود را اعمال کنند. مطالعه این مکانیسمها برای درک نحوه تنظیم فعالیتهای زیستی به وسیله هورمونها، ضروری است. در ادامه این بخش به طور خلاصه با این موضوع آشنا میشویم که مکانیسمهای عمومی فعالیت هر هورمون چیست.
ارتباطات هورمون و گیرنده
هورمونها اثرات خود روی سلولهای هدف را با اتصال به گیرندهها اعمال میکنند. این گیرندهها پروتئینهای تخصص یافتهای هستند که در بخشهای مختلفی ازجمله غشای سلول، سیتوزول و هسته، مستقر شدهاند. هر گیرنده در ساختار خود یک جایگاه اختصاصی برای اتصال به هورمون دارد. این جایگاه، هورمون مناسب خود را تشخیص میدهد و با اتصال به آن زنجیرهای از اتفاقات درون سلولی را آغاز میکند.
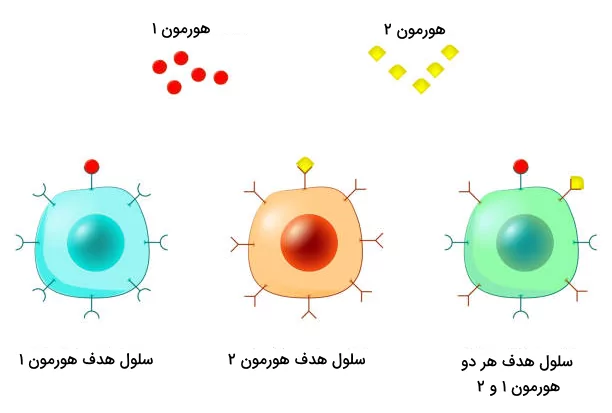
انواع گیرندهها
گیرندههای هورمونها را میتوان به دو دسته اصلی تقسیم کرد که به شرح زیر هستند.
- گیرندههای متصل به غشا: این گیرندهها روی سطح سلول واقع شدهاند و به هورمونهای آبدوست که محلول در آب هستند، مانند هورمونهای پپتیدی و کاتکولآمینها متصل میشوند.
- گیرندههای درونسلولی: این دسته از گیرندهها درون سیتوپلاسم یا هسته سلول جایگیری کردهاند و به طور معمول به هورمونهای لیپیددوست که محلول در چربی هستند متصل میشوند. هورمونهای استروئیدی و هورمونهای تیروئیدی ازجمله هورمونهایی هستند که گیرندههایی درون سلولی دارند.
شناسایی و اختصاصیت
فعالیت اصلی گیرندههای هورمونها شناسایی هورمونهایی است که برای اتصال به آنها اختصاصی شدهاند. برای مثال گیرندههای انسولین با وجود حضور هورمونهای دیگر در جریان خون یا مایع خارج سلولی میتوانند این هورمون را شناسایی کنند و با اتصال به انسولین برداشت گلوکز را توسط سلولهای هدف تسهیل کنند.
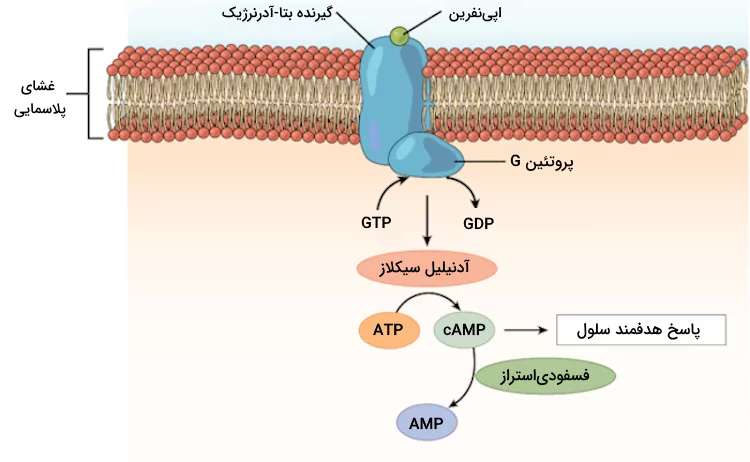
انتقال پیام
به محض اتصال هورمون و گیرنده، گیرنده دچار تغییرات کنفورماسیونی میشود که مسیرهای پیامرسانی درون سلولی را به راه میاندازد. این مسیرهای پیامرسانی باعث ایجاد پاسخهای سلولی گوناگونی میشوند. در این مرحله ممکن است پیامرسانهای ثانویه، مانند «آدنوزین مونوفسفات حلقوی» (Cyclic AMP) یا یون کلسیم ایفای نقش بکنند. پیامرسانهای ثانویه قادر به تشدید اثر پیام و ایجاد پاسخ سلولی هستند.
پاسخ بافت
همه سلولها یک گیرنده یکسان را نمیسازند و از آن استفاده نمیکنند، در حقیقت فعالیت هورمونها برای بافتها اختصاصی شده است. این بیان انتخابی گیرندهها در سلولهای مختلف باعث میشود که پاسخهای سلولی متنوعی به وسیله یک هورمون ایجاد شود.
مکمل فیزیولوژیکی
هنگامی که یک هورمون همزمان بافتهای متعددی را تحت تاثیر خود قرار میدهد، پاسخهای گوناگونی که ایجاد میشوند با یکدیگر هماهنگ میشوند تا به اثر فیزیولوژیکی خاصی دست یابند. برای مثال فعالیت هورمون استرادیول را در نظر بگیرید. اتصال این هورمون به گیرنده اختصاصی استروژن در بافتهای مختلف پاسخهای متفاوتی از قبیل افزایش تخمکگذاری در تخمدانها و اثر روی تراکم استخوان را ایجاد میکند.
تنظیم بر اساس بازخورد
پیامرسانی هورمونی در اغلب مواقع به وسیله مکانیسمهای بازخورد تنظیم میشود. چرخههای خودتنظیمی منفی از رایجترین انواع این پاسخها هستند که در طی آن محصول نهایی حاصل از فعالیت هورمون روی میزان ترشح هورمون اثر میگذارد. این مکانیسمهای تنظیمی به جهت اطمینان از حفظ شرایط پایدار فیزیولوژیکی شکل گرفتهاند تا مسیرهای هورمون بیش از حد یا کمتر از میزان مورد نیاز فعال نشوند.
تنوع اثرات هورمونی
هر هورمون میتواند اثرات متفاوتی را در بافتهای مختلف ایجاد کند. به عنوان مثال فعالیت اصلی گلوکاگون افزایش سطح گلوکز خون است اما میتواند روی متابولیسم چربی در بافتهای چربی نیز اثر بگذارد. همچنین ارتباط بین هورمونها و گیرندهها میتواند به پاسخهای فیزیولوژیک پیچیده و منظمی منتهی بشود.

نتایج زیستی
نتیجه نهایی اتصالات هورمونها و گیرندهها شامل تغییر متابولیسم، رشد و فعالیت سلول است. این اتفاقات ممکن است به روشهای مختلفی از قبیل تنظیم بیان ژن، تغییر فعالیت آنزیمها و تقسیم سلولی رخ بدهند.
هورمونهای زنانه و هورمونهای مردانه
تعدادی از هورمونها هستند که در بدن زنها یا مردها فعالیت بیشتری دارند یا حتی فقط در یک جنس تولید و ترشح میشوند. حالا که به طور کامل یاد گرفتهایم هورمون چیست، قصد داریم این هورمونهای اختصاصیافته به هر جنس را معرفی کنیم. در جدول زیر این هورمونها را نام بردهایم.
| هورمونهای زنانه | هورمونهای مردانه |
| استروژنها | تستسترون |
| پروژسترون | دیهیدروتستسترون |
| FSH | پرولاکتین |
| LH | FSH |
| پرولاکتین | LH |
| اکسیتوسین | دیهیدرواپیآندروسترون |
| تستسترون | هورمون رشد |
هورمونهای زنانه
همانطور که در جدول قابل مشاهده است هورمونهای زنانه هفت مورد هستند که در ادامه با آنها بیشتر آشنا میشویم تا یاد بگیریم که اهمیت حضور هر هورمون چیست.
- «استروژنها» (Estrogens): این دسته از هورمونها شامل ۳ نوع هورمون مختلف هستند.
- «استرادیول» (Estradiol): استرادیول نوع اصلی استروژن است که چرخه قاعدگی را تنظیم میکند و صفات ثانویه جنسی را تحت تاثیر قرار میدهد.
- «استرون» (Estrone): نوع ضعیفتر استروژن است که در فعالیتهای تولیدمثلی نقش دارد.
- «استریول» (Estriol): در حین بارداری تولید میشود و به آمادگی بدن برای زایمان کمک میکند.
- «پروژسترون» (Progesterone): رحم را برای لانهگزینی تخمک بارور شده آماده میکند و موجب حفظ بارداری میشود.
- «هورمون محرکه فولیکولی» (Follicle-Stimulating Hormone | FSH): رشد فولیکول تخمدانها و تولید استروژن را تحریک میکند.
- «هورمون لوتئینهکننده» (Luteinizing Hormone | LH): تخمکگذاری را به راه میاندازد و تولید پروژسترون را تحریک میکند.
- «پرولاکتین» (Prolactin): تولید شیر را برای شیردهی به فرزند افزایش میدهد.
- «اکسیتوسین» (Oxytocin): محرک انقباضات رحمی در حین زایمان و خروج شیر از سینه به هنگام شیردهی است.
- «تستسترون» (Testosterone): این هورمون به مقدار زیادی در بدن زنان تولید نمیشود ولی همین مقدار تولید شده در تحریک جنسی و تراکم استخوانها نقش دارد.

هورمونهای مردانه
در جدول با اسامی هورمونهای مردانه آشنا شدیم و دیدیم که بعضی هورمونها در زنان هم وجود دارند، اما این هورمونها در هر جنس فعالیتهای متفاوتی دارند. در ادامه خواهیم گفت که در مردان فعالیت مختص به هر هورمون چیست.
- تستسترون: اصلیترین هورمون مردان، تستسترون است که مسئول رشد و گسترش بافتهای تولیدمثلی و صفات ثانویه مردانه است.
- «دیهیدروتستسترون» (Dihydrotestosterone | DHT): یکی از مشتقات تستسترون است که در ایجاد صفات مردانه و سلامت پروستات نقش دارد.
- LH: محرک تولید تستسترون توسط «سلولهای لایدیگ» (Leydig Cells) است که در بیضه قرار دارند.
- FSH: تولید اسپرم در بیضهها را تحریک میکند.
- پرولاکتین: با وجود آن که نقش این هورمون در زنان بیشتر است اما در مردان نیز تولیدمثل و فعالیت سیستم ایمنی را تحت تاثیر قرار میدهد.
- «دیهیدرواپیآندروسترون» (Dehydroepiandrosterone| DHEA): یک هورمون پیشساز است که میتواند به تستسترون و استروژنها تبدیل شود.
- هورمون رشد: رشد، متابولیسم و توده ماهیچهای را تحت تاثیر قرار میدهد.

هورمونهای گیاهی
تا این بخش از این مطلب در جواب سوال هورمون چیست، تنها از هورمونهای جانوری صحبت کردیم در حالی که گیاهان نیز هورمونهای مخصوص به خود را دارند. «هورمونهای گیاهی» (Phytohormone) مولکولهای پیامرسانی هستند که توسط گیاهان در غلظتهای بسیار کم ساخته میشوند.
هورمونهای گیاهان تمام مواردی را که در ادامه نام میبریم، کنترل میکنند.
- مربوط به رشد و نمو گیاهان
- تنظیم اندازه بخشهای مختلف گیاه
- دفاع از گیاه در برابر عوامل بیماریزا
- تحمل استرس
- تولیدمثل
در صورتی که تمایل به آشنایی بیشتر با هورمونهای گیاهی و کسب اطلاعات کاملتر راجع به فعالکنندگان و مهارکنندگان رشد گیاهان دارید، مطالعه مطلب «هورمون های گیاهی — به زبان ساده» از مجله فرادرس را به شما توصیه میکنیم.

برخلاف حیوانات که تولید هورمون فقط توسط غدههای خاصی در بدن انجام میشود، تمام سلولهای گیاهی میتوانند به سنتز هورمونها بپردازند. این هورمونها بیان ژن و مراحل ترجمه، تقسیم سلولی و رشد را تحت تاثیر قرار می دهند. در جدول زیر اصلیترین انواع فیتوهورمونها را به همراه فعالیت کلیدی آنها معرفی کردهایم.
| هورمون | فعالیت اصلی |
| «آبسیزیک اسید» (Absicisic Acid) | مهارکننده رشد گیاه، غیرفعال شدن جوانهها، سازگاری در شرایط استرسزا و بستن روزنهها در هنگام کمآبی |
| «اکسین» (Auxin) | رشد و نمو، چیرگی رأسی، رشد گلها و میوهها، جلوگیری از ریزش برگها |
| «سیتوکینین» (Cytokinin) | تحریک تقسیم سلولی در حین جوانهزنی، تعدیل اثرات اکسین و حمایت از تشکیل برگهای جدید |
| «اتیلن» (Ethylene) | رسیدن میوه، پژمرده شدن گلها، ریزش برگها و افتادن میوهها |
| «جیبرلین» (Gibberellins) | افزایش طول ساقه، جوانهزنی بذر گیاه و بلوغ میوه و گلها |
جمعبندی
در این مطلب از مجله فرادرس یاد گرفتیم که هورمون چیست و دلیل اهمیت آنها در فعالیتهای مختلف بدن چیست. هورمونها پیامرسانهای شیمیایی بدن هستند که توسط اندامهای خاصی به نام «غدد درونریز» ساخته و ترشح میشوند. هورمونها با استفاده از جریان خون در بدن جابهجا میشوند و خود را به سلولهای هدف میرسانند.
از لحاظ ساختاری میتوان هورمونها را به سه دسته هورمونهای استروئیدی، هورمونهای پروتئینی و پپتیدی و هورمونهای مشتق شده از آمینواسیدها تقسیم کرد. در این مطلب انواع دستهبندی هورمونها را معرفی کردیم و با خصوصیات هر دستهبندی و مثالهای مرتبط با آن نیز آشنا شدیم.
در گام بعدی به سراغ روشهای سنتز هورمونها رفتیم و یاد گرفتیم که هورمونهای پروتئینی توسط ژنها کد میشوند و با دنبال کردن مراحل رونویسی و ترجمه ساخته میشوند اما هورمونهای استروئیدی و آمینی از پیشسازهایی مانند کلسترول و تیروزین ساخته میشوند. ماهیت متفاوت هورمونها باعث میشود که مکانیسمهای متفاوتی برای جابهجایی در خون داشته باشند؛ به طوری که هورمونهای پروتئینی و پپتیدی که آبدوست هستند به صورت آزاد در خون حرکت میکنند اما هورمونهای آبگریز مانند هورمونهای استروئیدی نیاز به حضور پروتئینهای حامل دارند.
یکی دیگر از سوالهای مهمی که در این مطلب از مجله فرادرس به آن جواب دادیم این بود که کار هورمون چیست؟ هورمونها اعمال متفاوتی را در بدن به پیش میبرند، در ادامه تعدادی از آنها را نام میبریم.
- تنظیم متابولیسم بدن
- تولیدمثل
- رشد و نمو
- حفظ هومئوستازی بدن
- کنترل آپوپتوز
در بخش پایانی نیز با هورمونهای گیاهی آشنا شدیم که توسط همه انواع سلولهای گیاهی ساخته میشوند و در فعالیتهایی مثل تحمل استرس، رشد و نمو و تولیدمثل نقش دارند.