بافت خون چیست؟ – به زبان ساده
خون تنها بافت مایع بدن و یکی از انواع بافت پیوندی است. وظیفه این بافت انتقال پروتئینها، مولکولهای چربی، گازهای تنفسی، پروتئینهای تنظیمی، مواد زائد از اندامها به قلب و کلیه است. یونهای معدنی محلول در پلاسمای خون فشار اسمزی بافتهای مختلف را تنظیم میکنند و گلبولهای سفید این بافت نقش اصلی در ایجاد پاسخ ایمنی ذاتی بدن دارند. در این مطلب انواع سلولهای بافت خون را به همراه ترکیب ماتریکس خارج سلولی آن (پلاسما)، وظیفه و بیماریهای این بافت را توضیح میدهیم.
- ساختار سلولی و ترکیبات اصلی بافت خون را شرح خواهید داد.
- تفاوت گلبولهای قرمز، سفید و پلاکت را تحلیل میکنید.
- روند تولید سلولهای خونی از سلول بنیادی را میآموزید.
- فرآیند انعقاد خون و مراحل آن را یاد میگیرید.
- نقش پلاسما و پروتئینهای آن را خواهید آموخت.
- با اختلالات رایج خونی و عوامل مؤثر بر آنها آشنا میشوید.
بافت خون چیست ؟
خون یکی از بافتهای پیوندی بدن است که سلولهای آن در ماتریکس مایع حرکت میکنند. بافت خون یک بزرگسال سالم حدود ۵ لیتر است و ۸٪ وزن فرد را به خود اختصاص میدهد. وظیفه اصلی این بافت پیوندی انتقال مواد غذایی (گلوکز، اکسیژن و دیاکسید کربن)، مولکولهای پیامرسان (هورمونها، سایتوکاینها و فاکتورهای رشد) و سلولها (گلبولهای سفید، گلبولهای قرمز و پلاکتها) از یک اندام به اندام دیگر است. ماتریکس مایع این بافت پلاسما نام دارد که از ترکیب آب، مواد آلی و معدنی بدن تشکیل میشود.
سلول های بافت خون
گلبولهای قرمز (RBC)، گویچههای قرمز یا «اریتروسیتها» (Erythrocytes)، پلاکتها، «ترومبوسیت» (Thrombocyte) یا گِردهها، گلبولهای سفید سلولهای بافت خون را تشکیل میدهند که ساختار و وظیفه متفاوتی دارند. اما همگی از سلولهای اجدادی مشترک (سلولهای خونساز | Hematopoietic) در مغز قرمز استخوان به وجود میآیند.
گلبول قرمز
اریتروسیتها سلولهای بدون هستهای با قطری بین ۷ تا ۸ میکرومتر هستند که غشای آنها در دو طرف مقعر (فرورفته) شبیه یک دونات توپر است. در نتیجه بخش محیطی قطر بیشتری از بخش مرکزی دارد. طی بلوغ سلول، سیتوپلاسم تمام اندامکها خود را از دست میدهد و با متالوپروتئین هموگلوبین پر میشود. هموگلوبین از چهار زنجیره پلیپپتیدی (آلفا ، بتا ، گاما و دلتا ) تشکیل شده است که هر کدام یک گروه عملکردی هِم (پروتئین اتصالی به اتم آهن) دارند. در نتیجه هر هموگلوبین همزمان به چهار اتم اکسیژن یا دیاکسید کربن متصل میشود.
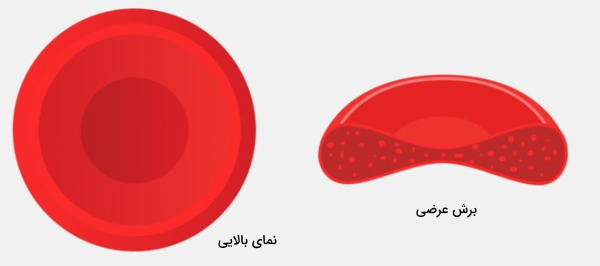
غشای پلاسمایی این سلولهای خونی مثل سایر سلولهای بدن از دو لایه فسفولیپید و پروتئین تشکیل شده است. پروتئینهای اینتگرال یا غرض غشایی که بخش اصلی پروتئینهای غشا را به خود اختصاص میدهند، در بخش سیتوپلاسمی به پروتئینهای اسکلت سلولی و هموگلوبین متصل میشوند. زنجیره کربوهیدرات خارجسلولی آنها آنتیژنهای خونی (ABO) را تشکیل میدهند. اما پروتئینهای سطحی به لیپیدهای نیمه داخلی غشای اریتروسیت متصل میشوندو برهمکنش این پروتئینها با اجزای اسکلت سلولی با افزایش استحکام و انعطافپذیری گلبول قرمز از شکستن غشا در مویرگها باریک بدن جلوگیری میکند.
گلبولهای قرمز از تمایز سلولهای خونساز مغز استخوان به سلولهای اریتروئیدی و سپس اریتروسیت تولید و وارد جریان خون میشوند. ارتروپویتین یکی از هورمونهایی است که تشکیل این سلولهای خونی در مغز استخوان را تحریک میکند. عمر این سلولهای خونی بین ۱۰۰ تا ۱۲۰ روز است و پس از آن بهوسیله ماکروفاژهای کبد، طحال، مغز استخوان یا غدد لنفاوی (سیستم رتیکواندوتلیال) بازیافت میشوند. زنجیره پلیپپتیدی هموگلوبین در فاگولیزوزوم ماکروفاژها به زیرواحدهای آمینواسیدی تجزیه شده و برای سنتز پروتئینهای جدید به جریان خون برمیگردد. به علاوه اتم آهن جداشده از هم برای شرکت در تشکیل اریتروسیتهای جدید به مغز استخوان انتقال مییابد و پروتئین هم پس از چند واکنشهای آنزیمی به بیلیروبین (رنگدانه زرد صفرا) تبدیل میشود. بیلیروبین پس از تغییر در کبد و رودهها بهوسیله ادرار و مدفوع دفع میشود.
پلاکت
پلاکتها یکی دیگر از سلولهای بدون هسته خون با قطری بین ۱ تا ۳ میکرومتر هستند که از مگاکاریوسیتهای مغز استخوان و با تحریک هورمون ترومبوپویتین تشکیل میشوند. ددر این فرایند مگاکاریوسیت پس از چند میتوز بدون سیتوکینز به سلولی چندهستهای تقسیم میشود و پلاکتها از شکستن این سلول ایجاد میشوند. سیتوپلاسم ترومبوسیتها از مولکول RNA، ریبوزومها، میتوکندری، لیزوزوم و وزیکولهای ذخیرهای پر شده است و غشای پلاسمایی آنها مثل سایر سلولهای بدن دولایه فسفولیپیدی است. سیتوپلاسم این سلولها را میتوان به سه ناحیه محیطی، اندامکی و غشایی تقسیم کرد.
- ناحیه محیطی: گلیکوپروتئینهای لازم برای اتصال پلاکت به سلولهای دیگر، فعال شدن و بههمچسبیدگی پلاکتها در این بخش قرار دارند.
- ناحیه اندامکی: گرانولهای آلفا و متراکم پلاکت در این ناحیه قرار دارند. تعداد و اندازه گرانولهای آلفا از گرانولهای متراکم بیشتر است و فاکتورهای انعقادی را ذخیره میکنند. گرانولهای دلتا یا متراکم کوچکتر هشتند و ADP، سروتونین و کلسیم ذخیره میکنند.
- ناحیه غشایی: این ناحیه باقیمانده شبکه اندوپلاسمی دانهدار مگاکاریوسیتها است که وظیفه سنتز ترومبوکسان A2 را بر عهده دارد. این ناحیه برای ترشح ترومبوکسیان A2 به بخش سیتوزولی غشای پلاسمایی پلاکت متصل میشود.
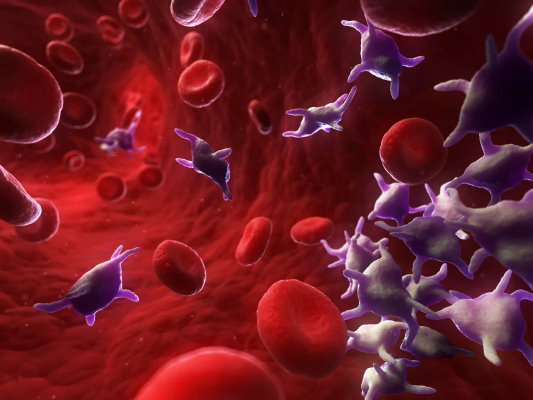
شکل پلاکتها قبل و بعد از فعال شدن متفاوت است. غشای پلاسمایی پلاکتهای غیرفعال جریان خون برخلاف گلبولهای قرمز از دو طرف محدب (برآمده) است. فعال شدن این پروتئین پس از آسیب بافت اندوتلیال با تشکیل زوائد سیتوپلاسمی همراه است.
پلاکت غیر فعال
نقش اصلی پلاکتها کمک به انعقاد خون و حفظ مایعات بدن است. به همین دلیل در شرایط معمول نیتریک اکسید (NO)، ADPase و پروستوگلاندین ۲ (PGl2) از سلولهای اندوتلیال رگ منجر به غیرفعال شدن پلاکت و مهار انعقاد میشود. فعال شدن پلاکت به تغییر جریان کلسیم سیتوپلاسمی و تغییر کنفورماسیون وابسته به پیامبر ثانویه cAMP بستگی دارد. مولکولهای آزاد شده از اندوتلیال با اتصال به گیرندههای سیتوپلاسمی پلاکت سنتز cAMP را از مسیرهای مختلف را افزایش میدهد.
- ADPase: مولکول ADP یکی از سیگنالهایی است که با اتصال به گیرندههای پروژنیک غشای پلاکت خروج کلسیم از سیتوپلاسم را مهار میکند. آنزیم ADPase با هیدرولیز ADP و مهار مسیرهای مولکولی، پلاکت را مهار میکند.
- پروستوگلاندین: این مولکولهای لیپیدی به گیرنده پروستانوئید غشای پلاکت متصل میشوند و پروتئین G این گیرنده را فعال میکنند. پروتئین G با افزایش فعالیت آنزیم آدنیلات سیکلاز غشای تبدیل ATP به cAMP را افزایش میدهد. این مولکول با اتصال به کانالهای لیگاندی کلسیم با افزایش خروج این یون از سیتوپلاسم پلاکت را غیرفعال میکند.
گلبول های سفید
گلبولهای سفید (WBC) یا لوکوسیتها سلولهای ایمنی خون هستند که از دو رده سلولی مختلف (میلوئید و لنفوئید) در مغز استخوان تشکیل میشوند و همه آنها مجموعهای از غشای دولایه لیپیدی و سیتوپلاسم و اندامکها (هسته، میتوکندری، دستگاه گلژی، سانتریول، شبکه اندوپلاسمی صاف و زبر، ریبوزوم، لیزوزوم و پراکسیزوم) هستند. اما شکل، اندازه، وظیفه و مسیر پیامرسانی آنها با هم متفاوت است.
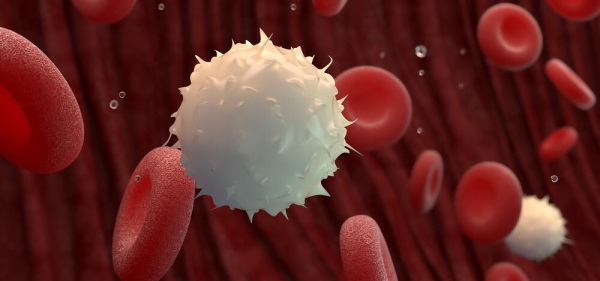
این سلولهای خون از بدن در برابر آنتیژنهای باکتریایی، قارچی، انگلی و ویروسی، آلرژنها، افرایش سلولهای توموری و سلولهای مرده محافظت میکنند. این سلولها را بر اساس رنگآمیزی سلولی سیتوپلاسم به دو گروه گرانولوسیت و آگرانولوسیت تقسیم میکنیم.
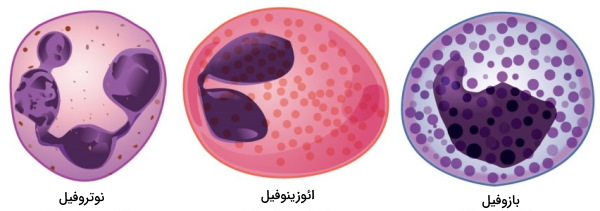
- گرانولوسیتها: سلولهایی هستند که از تمایز سلولهای میلوئیدی مغز استخوان تشکیل میشوند و سیتوپلاسم آنها پس از رنگآمیزی سلولی زیر میکروسکوپ دانهدار دیده میشود. بازوفیل، نوتروفیل، ائوزینوفیل و ماستسلهای نابالغ گرانولوسیتهای خون را تشکیل میدهند.
- نوتروفیل: قطر این سلولها بین ۱۲ تا ۱۵ میکرومتر است و هشته چند قسمتی دارند. این سلولها در پاسخ به سایتوکاینها فعال شده و با خروج از رگ به بافت عفونی منتقل میشوند. طول عمر این سلولهای خون چند روز است.
- ائوزینوفیل: قطر این سلولها حدود ۱۵ میکرومتر است و هسته دوقسمتی دارند. این گرانولوسیتها با رهایش گرانولهای سیتوپلاسمی در از بردن پاتوژنهای انگلی نقش دارند.
- بازوفیل: این سلولها هماندازه نوتروفیلها هستند و هسته دوقسمتی یا S شکل دارند. گرانولهای حاوی هیستامین این لوکوسیتها در پاسخ یه آلرژنها آزاد میشوند.
- ماستسل: این گرانولوسیتها سلولهای مستقر در بافت هستند و تنها شکل نابالغ آنها در خون وجود دارد. این لوکوسیتهای بیضی یا کروی در خون فعالیتی ندارند. اما در بافت شروعکننده پاسخ التهابی ایمنی ذاتی بدن هستند.
- آگرونولوسیتها: سلولهایی هستند که سیتوپلاسم آنها فاقد گرانول یا دانه است. لنفوسیتها و مونوسیتها در این گروه قرار میگیرند. مونوسیتها سلولهای کروی با هسته بزرگی هستند که پس از عبور از مویرگ به ماکروفاژ و سلولهای دندریتی سیستم ایمنی تمایز مییابند. این سلولها در خون فعالیتی ندارند. لنفوسیتها B و T گروه دیگر آگرانولوسیتها را تشکیل میدهند که در جریان لنف پاتوژنها، سلولهای آلوده به پاتوژن و سلولهای توموری را از بین میبرند.
ماتریکس خارج سلولی بافت خون
پلاسما ماتریکس خارج سلولی بافت پیوندی خون را تشکیل میدهد. در یک بزرگسال بالغ و سالم حدود ۹۰٪ این ماتریکس از آب و ۱۰٪ آن از دو نوع ترکیب جامد با pH ۷٫۳-۷٫۴ تشکیل شده است.

پروتئین پلاسما
این ترکیبات حدود ۷٪ ترکیب کلی پلاسما را به خود اختصاص میدهند که بخش کمی از آن هورمون و آنزیم هستند. آلبومین، گلوبینها و فیبرینوژن سه پروتئین اختصاصی پلاسما را تشکیل میدهند.
- آلبومین: آلبومین فراوانترین پروتئین پلاسما است که در کبد سنتز میشود. این پروتئین اسیدهای چرب هیدروفوب و هورمونهای استروئیدی را در خون حمل میکند. غلظت بالای این پروتئین در پلاسما منجر به ورود آب از مایع میانبافتی به خون و تنظیم فشار اسمزی خون میشود. تنظیم فشار اسمزی، به تنظیم فشار و حجم خون کمک میکند. آلبومین معمولا ۵۴٪ از کل حجم کلی پروتئینهای پلاسما (۳٫۵-۵ گرم بر دسیلیتر خون) را تشکیل میدهد.
- گلوبینها: گلوبینها دومین پروتئینهای فراوان خون هستند که ۳۸٪ حجم کل پروتئینهای پلاسما (۱-۱٫۵ گرم در دسیلیتر خون) را به خود اختصاص میدهند و در سه گروه آلفا، بتا و گاما تقسیمبندی میشوند. گلوبینهای آلفا و بتا حامل آهن، لیپیدها و ویتامینهای محلول در چربی به سلولهای مختلف هستند. این گلوبینها که در کبد ساخته میشوند، مثل آلبومین در تنظیم فشار اسمزی، حجم و فشار خون نقش دارند. اما گلوبینهای گاما که همان ایمونوگلوبولینها یا آنتیبادیهای سیستم ایمنی بدن هستند، پس از سنتز از پلاسموسیتها (لنفوسیتهای B فعال) به خون ترشح میشوند.
- فیبرینوژن: فیبرونوژین پروتئنی ضروری پلاسما برای انعقاد خون است که تنها ۷٪ حجم کل پروتئینهای این ماتریکس (۰٫۲-۰٫۴۵ گرم بر دسیلیتر) را به خود اختصاص میدهد.
ترکیبات محلول پلاسما
علاوه بر آب و پروتئین انواع الکترولیتها ازجمله یونهای پتاسیم، کلر، کلسیم و سدیم، گازهای خون (اکسیژن و دیاکسید کربن)، ویتامینهای محلول در آب، گلوکز، آمینواسیدها، لیپیدهای کوچک و مواد زائد در این بخش از بافت خون حل میشوند. تمام این ترکیبات تنها ۱٪ کل حجم پلاسما را به خود اختصاص میدهند.
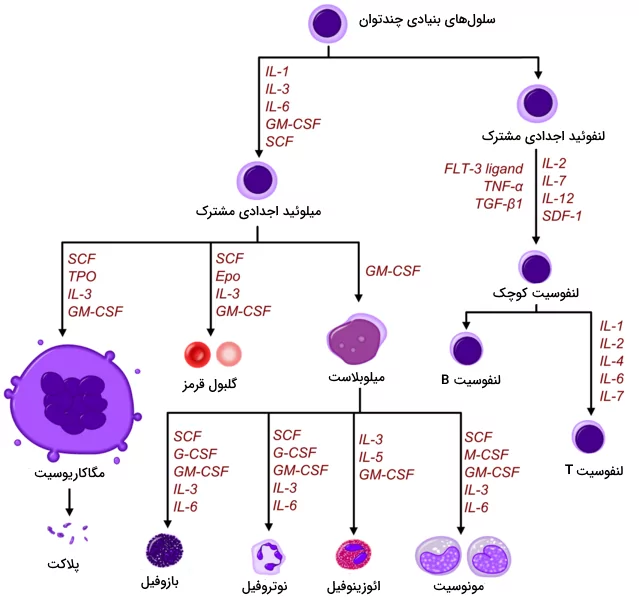
بافت خونساز
خونسازی یا «هماتوپویسیس» (Hematopoiesis) فرایند تولید تمام سلولهای خونی از سلولهای بنیادی خونساز یا هموسیتوبلاستها است. در ابتدای دوره جنینی این سلولهای بنیادی در کیسه زرده قرار دارند. با پیشرفت مراحل تکامل جنین و پس از تشکیل اندامها سلولهای خونی بهوسیله بافت خونساز طحال، کبد و در نهایت مغز قرمز استخوانها تولید میشود.
پس از تولد و قبل از بلوغ تشکیل سلولهای خونی فقط در مغز قرمز استخوانهای بلند ازجمله فمور و درشتنی تشکیل میشود. اما تکامل لنفوسیتهای سیستم ایمنی در طحال، تیموس و گرههای لنفاوی تکمیل میشود. پس از بلوغ مغز استخوان لگن، جمجمه، مهرهها و جناغ وظیفه تولید سلولهای خونی را بر عهده دارد.
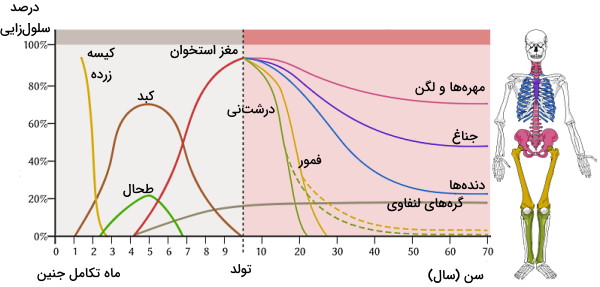
تمایز سلولهای خونساز به سلولهای بافت خون در چندین مرحله و با کمک تحریک فاکتورهای رشد (ازجمله فاکتور سلولهای بنیادی، اینترلوکینها و فاکتور تحریک کلونی)، هورمون اریتروپویتین و ترومبوپوئتین دارد. سلول خونساز اولیه در پاسخ به فاکتورهای رشد و اینترلوکینها به سلولهای میلوئیدی و لنفوئیدی اجدادی تمایز مییابد. تمام لنفوسیتهای سیستم ایمنی از تمایز لنفوئیدهای اجدادی و گلبولهای قرمز (در پاسخ به ارتروپویتین)، میلوبلاست و مگاکاریوسیتها (در پاسخ به ترومبوپویتین) از تمایز سلولهای میلوئیدی تشکیل میشوند. لوکوسیتهای بافت خون از تمایز میوبلاستها و پلاکت از تمایز مگاکاریوسیت تولید میشود.
وظیفه بافت خون چیست ؟
انتقال مواد، تنظیم هوموستازی و محافظت از بدن سه وظیفه اصلی بافت خون است.
- انتقال مواد: انتقال اکسيژن و مواد غذایی از لوله گوارش، ریه و اندامها ذخیرهکننده گلوکز (کبد و ماهیچه) به سلولها، انتقال دیاکسید کربن و ترکیبات نیتروژنی از سلولها به ریه و سیستم دفع مواد و انتقال هورمونها از غدد اندوکرین به بافتهای هدف، فعالیتهای خون برای انتقال مواد هستند.
- تنظیم هوموستازی: انتقال گرما از اندامهای فعال (برای مثال ماهیچه اسکلتی) به بافتعهای دیگر یا پوست، تنظیم فشار اسمزی بهوسیله الکترولیت و پروتئینهای پلاسما و تنظیم pH بهوسیله بافرهای پلاسما، فعالیتهای خون برای تنظیم هوموستازی بدن است.
- محافظت از بدن: مهار از دست دادن مایعات پس از آسیب رگ بهوسیله مکانیسم انعقاد، حفاظت از بدن در برابر پاتوژنها بهوسیله گلبولهای سفید، پروتئینهای مکمل و آنتیبادیهای لنفوسیت B، فعالیتهای بافت خون برای محافظت از بدن است.
انعقاد خون
انعقاد خون یا هموستازی مجموعهای از واکنشهای متوالی است که هر مرحله آن، مرحله بعدی را فعال میکند و در نهایت با تشکیل لخته خونی به پایان میرسد. انعقاد خون در سه مرحله انقباض رگ، «تشکیل لخته پلاکتی» (Formation of the Platelet Plug) و «تشکیل لخته خونی» (Coagulation) انجام میشود.
- انقباض رگ: آسیب دیواره رگها با آزاد شدن مولکولهای شیمیایی اندوتلین از سلولهای اندوتلیال همراه است. اتصال این مولکولها به گیرندههای صاف لایه زیری با تحریک انقباض این ماهیچهها، قطر رگ و جریان خون محل زخم را کاهش میدهد.
- تشکیل لخته پلاکتی: پس از آسیب دیواره رگ، بافت پیوندی لایه زیری و رشتههای کلاژن آن در تماس با خون قرار میگیرد. اندوتلینهای ترشح شده از سلولهای رگ با اتصال به گیرندههای پلاکت این سلول بافت خون را فعال میکند. رشتههای کلاژنی به کمک «فاکتور وون وینبرند» (von Willebrand Factor) که پروتئین محل در پلاسما است، مانند توری پلاکتها را به دام میاندازد. پلاکتها همزمان با تشکیل لخته مولکولهایی ترشح میکنند که مراحل بعدی انعقاد را فعال میکنند.
- آدنوزین دیفسفات (ADP) با فراخوانی پلاکتهای بیشتر به محل زخم، اندازه لخته پلاکتی را افزایش میدهد.
- سروتونین با اتصال اتصال به گیرندههای غشای اندوتلیال و کاهش قطر رگ، جریان خون به محل زخم را کاهش میدهد.
- پروستوگلاندینها و فسفولیپید علاوه بر کاهش قطر رگ و جریان خون محل زخم، سایر مولکولهای واکنش انعقاد را فعال میکنند.
- تشکیل لخته خونی: برای تشکیل لخته خون فعال شدن فاکتورهای انعقادی، تشکیل شبکهای از پروتئینهای رشتهای و به دام افتادن گلبولهای قرمز ضروری است. فاکتورهای انعقادی این مرحله بر اساس نوع آسیب از مسیر داخلی یا خارجی فعال و با مسیر مشترک منجر به تشکیل لخته میشوند.
- مسیر داخلی: مسیر داخلی سریعترین (در چند ثانیه) مسیر فعال شدن فاکتورهای انعقادی است و بر اثر تروما فعال میشود. در این مسیر سلولهای آسیبدیده بافت اطراف رگ در اثر تماس با پلاسمای خون ترومبوپلاستین یا فاکتور III انعقادی ترشح میکند. در مرحله بعد ترومبوپلاستین، فاکتور انعقادی VII یا پروکانورتین را فعال میکند و این دو فاکتور همراه یون کلسیم، یک کمپلکس آنزیمی تشکیل میدهند. این آنزیم با فعال کردن فاکتور X (فاکتور استورات پراور | Stuart–Prower factor) مرحله بعدی (مسیر مشترک) انعقاد را فعال میکند.
- مسیر خارجی: این روش از مسیر خارجی طولانیتر است وفاکتورهای انعقادی آن بهوسیله بافت رگ ترشح میشود. این مسیر با فعال شدن فاکتور انعقادی XII (فاکتور هاگمن | Hageman factor) بر اثر برخورد با آنیونها ازجمله پلیمرهای غیرآلی و مولکولهای فسفاتدار تشکیل شده در مسیر داخلی شروع میشود. این فاکتور واکنشهای فعالکننده فاکتور XI (فاکتور ضدخونریزی C) و فاکتور IX (فاکتور ضدخونریزی B) را تحریک میکند. همزمان مولکولهای شیمیایی آزاد شده از پلاکت سرعت این واکنشها را افزایش میدهد. در مرحله آخر فاکتور VIII (فاکتور ضدخونریزی A) آزاد شده از پلاکت و سلولهای اندوتلیال با فاکتور IX کمپلس آنزیمی تشکیل میدهند که فاکتور X را فعال میکند. فاکتور X (تروموبوکیناز)، مولکولهای مورد نساز برای شروع مرحله بعد (مسیر مشترک) را فعال میکند.
- مسیر مشترک: مسیر مشترک مرحله بعدی هر دو مسیر داخلی و خارجی است. در این مسیر فاکتور X فاکتور II (پروتروموبین غیرفعال) را به آنزیم فعال تروموبین تبدیل میکند. این آنزیم فاکتور I (فیبرینوژن نامحلول پلاسما) را به رشتههای فیبرین محلول تبدیل میکند. این رشتهها بهوسیله فاکتور XIII به لخته فیبرینی تبدیل میشوند که گلبولهای قرمز را به دام میاندازد.
بافر های خون
فعالیت بیولوژیک بدن به تنظیم دقیق تعادل اسید و باز در خون بستگی دارد. بافر سیستمی شیمیایی است که از تغییر شدید pH یک محلول در اثر اضافه شدن اسید یا باز جلوگیری میکند. پروتئينهای پلاسما، فسفات و بیکربنات سه سیستم بافری پلاسما هستند که با کمک کلیهها و دستگاه تنفس pH مایعات بدن را تنظیم میکنند.
- بافر پروتئینی پلاسما و سلولها: پروتئینها پلیمرهایی از زیرواحدهای آمینواسید با گروههای کربوکسیل (منفی)، آمین (مثبت) یا زنجیره جانبی باردار هستند. در نتیجه این پلیمرها میتواند با جذب پروتون و هیدروکسید از اسید و باز اضافه مثل بافری pH خون را تنظیم کند. دو-سوم قدرت بافری خون به دلیل وجود پروتئینهای آن است.
- بافر هموگلوبین: هموگلوبین بافر گلبول قرمز است. این پروتئین در بافتهای مرکزی بدن، پروتون آزاد شده از واکنش گاز دیاکسید کربن با آب را جذب و از تغییر pH سلول جلوگیری میکند.
- بافر فسفات: سدیم هیدروژن فسفات ( ) اسید ضعیف و سدیم مونوهیدروژن فسفات () باز ضعیفی است که بافر فسفات خون را میسازد. اجزای این بافر با دریافت هیدروکسید و پروتون، و تشکیل نمک از تغییر pH خون جلوگیری میکنند.
- بافر بیکربنات-اسید کربنیک: سدیم بیکربنات () باز ضعیف و کربونیک اسید () اسید ضعیف این سیستم بافری خون است. در pH فیزیولوژیک خون (۷٫۴) غلظت بیکربنات در خون ۲۰ برابر غلظت اسید کربونیک است. به همین دلیل این سیستم بیشتر ترکیبات اسیدی (متابولیتهای کتونی و اسیدلاکتیک) را خنثی میکند. غلظت بیکربنات خون بهوسیله فشار و آنزیم کربونیکانیدراز گلبول قرمز تنظیم میشود. انحلالپذیری دیاکسیدکربن در خون بسیار کمتر از اکسيژن و در واکنش آنزیمی با آب (در گلبول قرمز بافتها) به کربونیکاسید و سپس بیکربنات شکشته خواهد شد. بافر بیکربنات-کربونیکاسید با واکنش زیر و تشکیل نمک سدیم کلرید، از تغییر pH خون بر آزاد شدن پروتون اسید قوی مثل HCl جلوگیری میکند.
گروه خونی
گروههای خونی بهوسیله مولکولهای غشای گلبولهای قرمز تعیین میشوند. این مولکولها گلیکوپروتئین یا گلیوکولیپیدهای غشای پلاسمایی هستند که زنجیره کربوهیدراتی آنها نوع آنتیژنهای خونی یا گروههای خونی را تعیین میکنند. این گروهها در فرایندهای انتقال خون و پیوند عضو اهمیت زیادی دارند. اگر آنتیژن خون اهداکننده و دریافتکننده یکی نباشد، آنتیبادی موجود در خون فرد دریافتکننده به آنتیژنهای سطحی گلبول قرمز اهداکننده متصل شده و منجر به تشکیل لخته میشوند که ممکن است با مرگ فرد دریافتکننده همراه باشد.
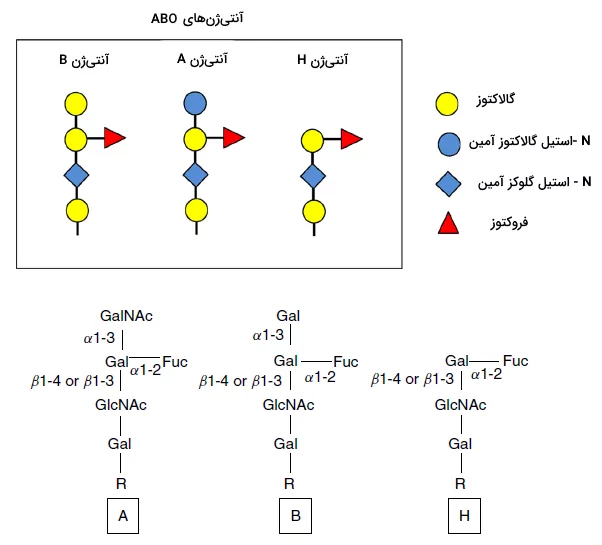
گروه خونی ABO
برخلاف اسم سهگانه گروه خونی ABO، این سیستم بر اساس وجود یا عدم وجود دو نوع آنتیژن در غشای پلاسمایی اریتروسیتها تعیین میشود. آنتیژن A و B دو گلیکوپروتئین غشایی هستند که توالی کربوهیدرات آنها در یک زیرواحد متفاوت است. زنجیره کربوهیدراتی آنتیژن A از گالاکتوز، N-استیل گلوکز آمین، گلاکتوز، زنجیره جانبی فروکتوز و گالاکتوز انتهایی (متصل به گالاکتوز قبلی) تشکیل میشود. اما در زنجیره کربوهیدراتی آنتیژن B گالاکتوز انتهای زنجیره جانبی با یک زیرواحد N-استیل گالاکتوز آمین جایگزین شده است.
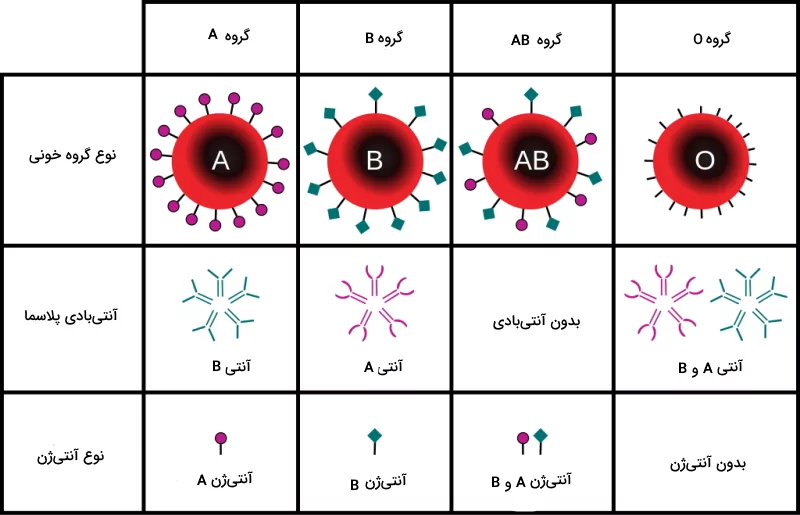
اگر این دو آنتیژن در غشای گلبول قرمز وجود داشته باشد، گروه خونی فرد AB و اگر ژن هیچ کدام در ژنوم وجود نداشته باشد، گروه خونی فرد O خواهد بود. آنتیبادی موجود در خون افراد A به آنتیژن B و آنتیبادی موجود در خون افراد B به آنتیژن A متصل میشود. به همین دلیل فردی با گروه خونی A نمیتواند به فردی با گروه خونی B، خون اهدا کند و انتقال خون به افرادی با گروه خونی O تنها از افراد همگروه (گروه خونی O) ممکن است. اما امکان انتقال خون از افراد با گروه خونی O به همه افراد (A، B و AB) وجود دارد. جدول زیر نوع گروههای خونی و آنتیژنهای آن را نشان میدهد.
گروه خونی Rh
Rh خون بر اساس وجود یا عدم وجود دسته دوم گروههای آنتیژنی در غشای گلبولهای قرمز تعیین میشود. این آنتیژن اولین بار در اریتروسیتهای «میمون رزوس» (Rhesus macaque) که بافت خون آن شباهت زیادی به انسان دارد، کشف شد. به همین دلیل نام آن آنتیژن Rh است. آنتیژن D مهمترین عضو گروه Rh است که در تعیین گروه خونی نقش دارد. اگر ژن این آنتیژن در فردی بیان شود، گروه خونی او مثبت (+) و اگر در فردی بیان نشود، گروه خونی او منفی (-) شناخته میشود. در نتیجه غشای پلاسمایی گلبول قرمز در فردی با گروه خونی ، هر سه آنتیژنهای A، B و Rh را دارد.
برخلاف آنتیبادی گروههای خونی ABO، آنتیبادی Rh پس از ورود آنتیژن به بدن ترشح میشود. در این فرایند که به آن حساسسازی گفته میشود، بر اثر انتقال خون در فرد یا در بارداری مادری با و نوزاد ایجاد خواهد شد. از آنجا که آنتیبادی در خون مادر وجود ندارد، حساسسازی در بارداری اول مشکلی ایجاد نخواهد کرد. اما اگر در زمان تولد بخشی از گلبولهای قرمز جنین () به مادر منتقل شود، آنتیبادی ترشح شده به خون مادر در بارداری دوم از راه جفت به جنین منتقل شده و در موارد خفیف منجر به آنمی نوزاد و در موارد حاد به تشکیل لخته، لیز شدن گلبولهای قرمز جنین و مرگ منجر میشود. آمپول روگام (ایمونوگلوبولین Rh | RhoGAM) دارویی است که در هفته ۶۶ تا ۲۸ بارداری و ۷۲ ساعت پس از تولد نوزاد به مادر با جنین تزریق میشود. این آنتیبادی گلبولهای قرمز (مثبت) که از راه جفت به مادر منتقل میشود را از بین برده و خطر مرگ جنین را کاهش میدهد.
تعیین گروه خونی
آزمایش «کراس مچ» (Cross Matching Blood Types) روش سادهای است که از آن برای تعیین گروه خونی استفاده میشود. این آزمایش به وسیله سه قطره خون و سرمهای تجاری آنتی A، B و Rh انجام میشود. اگر خون با اضافه کردن آنتی A لخته شود اما با اضافه کردن آنتی B تغییری در آن ایجاد نشود، گروه خونی فرد A تعیین میشود. شکل زیر انواع واکنشهای آنتیژن-آنتیبادی در تعیین گروههای خونی را نشان میدهد.
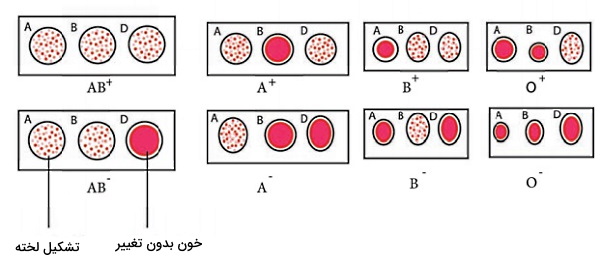
آزمایش بافت خون چیست ؟
آزمایش خون مجموعهای از آزمایشهای بیوشیمیایی است که به کمک آن میتوان وضعیت سلامت عمومی بدن را تعیین کرد. این آزمایش برای بررسی غلظت قند خون، تعداد سلولهای خونی، مواد معدنی ضروری (پتاسیم، کلسیم و آهن)، چربیها، ویتامینها، هورمونها (استروژن و هورمونهای تیروئیدی)، فاکتورهای التهابی، سطح اکسيژن و دیاکسیدکربن، مارکرهای توموری و سموم (سرب) به کار گرفته میشود. بر این اساس میتوان آزمایش خون را به دستههای زیر تقسیم کرد.
- شمارش کامل سلولهای خونی (CBC): شمارش کامل سلولهای خونی یکی از متداولترین آزمایشهای خون است که تعداد سلولهای خونی و درصد هر کدام از کل را مشخص میکند. در این آزمایش تعداد گلبولهای قرمز، گلبو.لهای سفید و پلاکتها تعیین میشود.
- گلبولهای قرمز: در این آزمایش تعداد گلبولهای قرمز، اندازه آنها، میزان هموگلوبین و هماتوکریت خون (درصد گلبولهای قرمز به کل خون) گزارش میشود. به کمک این فاکتور میتوان بیماریهای مختلف ازجمله کمخونی را بررسی کرد.
- پلاکتها: شمارش این سلولها به بررسی مشکلات انعقادی خون کمک میکند.
- گلبولهای سفید: شمارش لوکوسیتهای خون به تشخیص انواع عفونتها و تومورهای احتمالی کمک میکند.
- پنل متابولیتهای پایه (BMP): در این آزمایش غلظت گلوکز، کلسیم، سدیم، پتاسیم، کلر، کراتین، اوره خون (BUN) و بیکربنات اندازهگیری میشود که عدم تعادل هر کدام یکی از اختلالهای خون یا وابسته به خون را نشان میدهد.
- غلظت اوره و بیکربنات خون وضعیت سلامت کلیه را مشخص میکند.
- الکترولیتها وضعیت تعادل اسمزی خون را نشان میدهند.
- غلظت بیکربنات شاندهنده تعادل اسید و باز (وضعیت بافری) خون است.
- پنل متالبولیتهای جامع (CMP): در این تست علاوه بر متابولیتهای پایه غلظت پروتئین آلبومین و فاکتورهای سلاکمت کلیهها بررسی میشود.
- لیپیدها: در این آزمایش غظت تریگلیسیرید، لیپوپروتئین کمچگال (LDL)، لیپوپروتئین چگالی بالا (HDL) و کل کلسترول خون اندازهگیری میشود. این فاکتورها بیماریهای قلب-عروقی و خطر ایجاد سکته (به دلیل انسداد رگ یا خونریزی) را بررسی میکنند. غلظت بالای تمام لیپیدها احتمال ابتلا را افزایش میدهد. اما کاهش HDL (کلسترول خوب) احتمال ابتلا به بیماریای قلبی را افزایش میدهد.
- سایر تستها: در این آزمایشها فاکتورهای ویژه وابسته به اختلال یا سلامت بدن ازجمله آنزیمها و هورمونها را اندازهگیری میشود. به کمک این تستها میتوان اثر یک روند درمانی را بررسی کرد.
بافت خون زیر میکروسکوپ
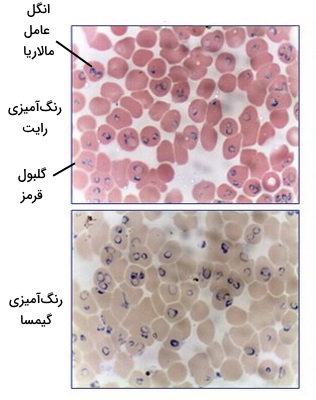
مشاهده بافت خون زیر میکروسکوپ یکی از روشهای شمارش سلولهای خونی، بررسی تغییر شکل آنها و بررسی انگلهای مختلف ازجمله مالاریا و فیلاریاز است. برای مشاهده خون زیر میکروسکوپ ابتدا قطرهای از این بافت روی لام شیشه پخش و در فضای آزمایشگاه خشک میشود. در مرحله بعد نیاز به تثبیت و رنگآمیزی بافت برای تشخیص راحت سلولها وجود دارد. برای رنگآمیزی بافت خون میتوان از روشهای «رنگآمیزی رایت» (Wright's stain) یا «گیمسا» (Giemsa stain) استفاده کرد. سپس میتوان بافت خون را زیر میکروسکوپ نوری مشاهده کرد.
فشار خون
خون بافتی مایع است که در شبکه لولهای رگها جریان دارد. ترکیب این مایع (ذرات کلوئیدی) و ساختار انتقالی آن دو فشار اسمزی و هیدروستاتیک در این بافت ایجاد میکند. تغییر هر یک از این فشارها با اختلال در عملکرد خون و اندامهای مربوط به آن همراه است.
فشار اسمزی بافت خون
فشار اسمزی یا فشار اونکوتیک، فشاری است که به دلیل وجود ذرات کلوئیدی به خصوص پروتئین آلبومین در خون ایجاد میشود. آلبومین پروتئین بزرگی است که از منافذ مویرگی خارج نمیشود. به همین دلیل افزایش یا کاهش آن در خون فشار اسمزی این مایع را تغییر میدهد. غلظت آب خون در ابتدای شبکه مویرگی بافتها بیشتر از مایع میانبافتی است. در نتیجه مواد غذایی و آب به مایع میان بافتی منتقل میشوند. اما در انتهای شبکه مویرگی که غلظت آب در خون کم و غلظت آلبومین زیاد است، اختلاف فشار اسمزی منجر به ورود آب از مایع میانبافتی به خون میشود. دو فرایند جذب و بازجذب (الکترولیتها و آب) در گلومرولهای کلیه به تنظیم این فشار کمک میکند.
فشار هیدروستاتیک خون
فشار هیدروستاتیک خون حاصل نیرویی است که مایع خون به دیوارههای رگ وارد میکند. بخش اصلی این فشار به دلیل نیروی انقباضی قلب ایجاد میشود و در ادامه مسیر دیواره انعطافپذیر رگها به تغییر آن کمک میکند. این فشار معمولا بر اساس فشار سیستول (حداکثر فشار در هر ضربان یا انقباض) به دیاستول (حداقل فشار در هر ضربان یا انقباض) قلب و بر حسب میلیمتر جیوه بیان میشود. خروجی قلب، مقاومت رگها، حجم خون، وضعیت احساسی فرد و گیرندههای فشاری سیستم عصبی، عوامل فیزیولوژیکی هستند که تنظیم این فشار نقش دارند.
بیماری های بافت خون
عوامل مختلف ژنتیکی و محیطی (داروها و کمبود فاکتورهای ضروری در رژیم غذایی) با تغییر نسبت سلولها به پلاسما، عملکرد یا مورفولوژی سلولهای خونی بیماریهای بافت خون را ایجاد میکنند. انواع کمخونی، سرطانها و اختلالهای انعقادی مهمترین بیماریهای بافت خون هستند.
- کمخونی: کمخونی یکی از اختلالهای متداول بافت خون است که به دلایل ژنتیکی یا مشکلات تغذیهای ایجاد میشود. تمام این اختلالها به دلیل تغییر در تعداد، مورفولوژی یا غلظت هموگلوبین گلبولهای قرمز ایجاد میشوند.
- کمخونی تغذیهای: این کمخونیها با کاهش تولید هموگلوبین، انتقال اکسیژن در خون را مشکل میکنند. کمخونی کشنده، فقر آهن و مگابلاستیک انواعی از بیماری هستند که به دلیل کمبود فولات، ویتامین B12 و B9 ایجاد میشوند.
- کمخونی وابسته به مغز استخوان: در این بیماریهای غیرسرطانی تمایز سلولهای بنیادی مغز استخوان به گلبولهای قرمز کاهش مییابد. کمخونی آپلازی یکی از این بیماریها است.
- کمخونی ارثی: تالاسمی و کمخونی داسیشکل دو بیماری وراثتی مهم بافت خون هستند. جهش ژنهای هموگلوبین در بیماری تالاسمی منجر به کاهش سنتز و در بیماری داسیشکل منجر به تغییر شکل این پروتئین میشود.
- کمخونی خودایمنی: در این بیماریهای خودایمنی بدن علیه گلبولهای قرمز آنتیبادی ترشح میکند. در نتیجه تعداد گلبولهای قرمز به دلیل لیز شدن کاهش مییابد.
- سرطان: «لوکمیا» (Leukemia)، «لنفوم» (Lymphoma) و «میلوم» (Myeloma) سه نوع سرطان بافت خونی هستند. در این بیماریها تغییر در تنظیم چرخه سلولهای بنیادی مغز قرمز استخوان با افزایش سرعت تقسیم آنها و افزایش سلولهای خونی به ویژه لنفوسیتها همراه است.
- اختلالهای انعقادی: این اختلالها پلاکتها یا فاکتورهای انعقادی خون را تغییر میدهند. در نتیجه انعقاد غیرطبیعی خون با ایجاد لخته مسیر رگها را مسدود میکند یا لخته نشدن خون در مواقع مورد نیاز، با خونریزی زیاد جان فرد را به خظر میاندازد. جهش در زن هورمون پروتروموبین، سندروم ضد فسفولیپید (بیماری خودایمنی)، کمبود پروتئین S، کمبود پروتئین C ازجمله اختلالهایی هستند که منجر به لخته شدن خون میشوند. بیماری ون ویلبرند (بیماری ژنتیکی غالب که به دلیل کاهش بیان فاکتور ون ویلبرند ایجاد میشود )، هموفیلی (بیماری ژنتیکی که با بیان پایین فاکتور VIII و IX انعقادی همراه است)، کمبود فیبرینوژن و ترومبوسیتوپنی (کاهش تعداد پلاکتهای خون) ازجمله بیماریهای عدم انعقاد خون هستند.
سوالات متداول
در این بخش به تعدادی از سوالات متداول پیرامون بافت خون پاسخ میدهیم.
یک واحد خون چند سی سی است ؟
یک واحد خون حدود ۵۲۵ سیسی یا میلیلیتر است که پس از خونریزیهای شدید به بیمار تزریق میشود.
بدن انسان چند لیتر خون دارد ؟
در بدن هر فرد سالم و بالغ حدود ۵ لیتر خون وجود دارد.
پلاسما خون چیست ؟
پلاسما ماتریکس خارج سلولی بافت خون است که از ترکیب آب، یونهای محلول و پروتئینهای انعقادی تشکیل میشود.
جمع بندی
در این مطلب توضیح دادیم که بافت خون یکی از انواع بافت پیوندی است که از گلبولهای قرمز، گلبولهای سفید، پلاکت و پلاسما تشکیل شده است. این بافت نقش مهمی در برقراری ارتباط بین دورترین سلولهای بدن دارد. به همین دلیل اولین تغییرات متابولیتها بر اثر بیماری را میتوان با بررسی درصد سلولها و ترکیب پلاسمای این بافت تشخیص داد.