هموگلوبین چیست؟ – به زبان ساده
هموگلوبین (Hemoglobin) (که به اختصار Hb نامیده میشود) یک متالوپروتئین یا پروتئین فلزی، حاوی اکسیژن در سلولهای قرمز خون است که در پستانداران و تقریباً سایر مهرهداران یافت میشود. برخی بیمهرگان نیز در حمل و نقل اکسیژن از هموگلوبین استفاده میکنند، مانند کرمهای آنلیدی که هموگلوبین را در خون خود حل می کنند. علاوه بر این، Hb به عنوان حامل برای انتقال اکسیژن در مراحل آبی زندگی لاروی برخی حشرات نیز مشاهده شده است. تنها تعداد معدودی از مهرهداران، مانند لارو مارماهی و برخی از گونههای یخ ماهیان قطب جنوب، فاقد هموگلوبین هستند. هموگلوبین کارآمدترین حامل اکسیژن به شمار میآید که تاکنون شناخته شده است.
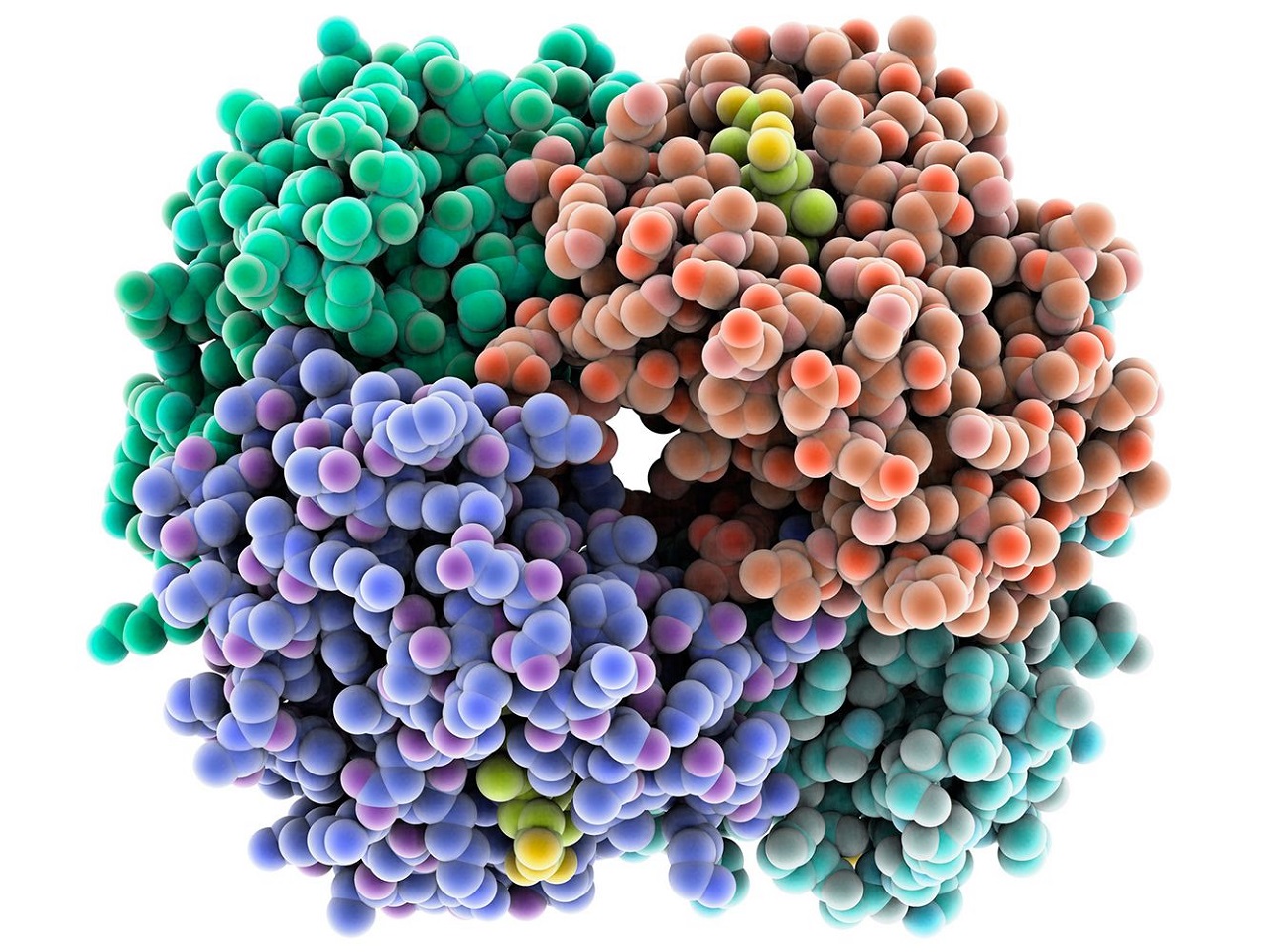


پروتئین هموگلوبین
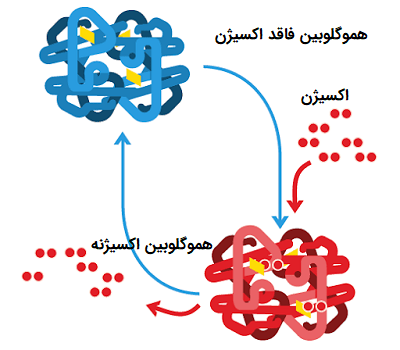
هموگلوبین به عنوان یک کمپلکس پروتئین - فلز، در شرایط مناسب با اتصالی سست و برگشت پذیر به اکسیژن متصل میشود و سپس گاز اکسیژن را تحت شرایط متفاوتی آزاد میکند. در مهرهداران، Hb اکسیژن را از ریهها یا آبششها به سایر بخشهای بدن مانند عضلات منتقل میکند، در واقع عضلات از مکانهایی هستند که هموگلوبین، اکسیژن را در آنها آزاد می کند. از نظر ساختاری، هموگلوبین یک پروتئین کروی است که در آن یک گروه آهن یا هِم (Heme) تعبیه شده است. هر گروه هِم دارای یک اتم آهن است و این گروه مسئول اتصال اکسیژن به هموگلوبین به شمار میآید. متداولترین انواع هموگلوبین شامل چهار زیر واحد است.
جهش در ژن پروتئین هموگلوبین منجر به گروهی از بیماریهای ارثی به نام «هموگلوبینوپاتی» (Hemoglobinopathies) میشود که رایجترین گونههای این گروه از اختلالات، بیماری کم خونی «سلول داسی شکل» (Sickle-Cell Disease) و «تالاسمی» (Thalassaemia) به شمار میآیند.
از آنجا که مونوکسید کربن نسبت به اکسیژن میل ترکیبی بیشتری به Hb دارد، استعمال دخانیات که موجب تولید مونو اکسید کربن در ریهها میشود، میتواند تأثیر زیادی بر حمل و نقل اکسیژن در خون داشته باشد و تا 20٪ از جایگاهای فعال اکسیژن روی هموگلوبین را مسدود میکند. این تنها یکی از تعداد بیشماری اثرات جدی و خطرناک مصرف دخانیات برای سلامتی محسوب میشود و نشانگر این است که مصرف این ترکیبات به تدریج سلولهای بدن را مسموم کرده و از بین میبرد.
هموگلوبین عاملی است که رنگ قرمز را در خون ایجاد میکند، در هنگامی Hb با اتصال به اکسیژن، مورد اکسیداسیون قرار میگیرد، رنگ قرمز روشن به خود میگیرد و زمانی که هموگلوبین اکسیژن خود را در کنار سلولهای بدن آزاد میکند به رنگ قرمز تیره در میآید. رنگ قرمز هموگلوبین به دلیل وجود اتمهای آهن در ساختار آن است.
از Hb برای تعیین روابط تکاملی در بین موجودات زنده استفاده شده است. زنجیرههای آلفا هموگلوبین انسان و شامپانزهها توالی یکسانی از اسیدهای آمینه را دارند، در حالی که انسان در یک اسید آمینه (از 141 اسید آمینه) با گوریل و در 25 اسید آمینه با خرگوش و 71 اسید آمینه با ماهی کپور متفاوت است.
ساختار هموگلوبین
مولکول هموگلوبین از چهار زیر واحد پروتئینی کروی تشکیل شده است. هر زیر واحد از یک زنجیره پروتئین محکم با یک گروه هِم غیرپروتئینی تشکیل شده است.
هر زنجیره پروتئینی جداگانه، مجموعهای از بخشهای ساختاری مارپیچ آلفا است که به هم وصل شدهاند و یک مارپیچ میوگلوبین را ایجاد کردهاند، این ساختارها، میوگلوبین نامیده میشود زیرا ترتیب قرارگیری این پروتئینها مشابه موتیفهایی است که در پروتئینهای میوگلوبین مورد استفاده قرار می گیرد. این الگوی فولدینگ یا تاخوردگی حاوی یک پاکت است که محلی مناسب برای اتصال با گروه هِم به شمار میآید.
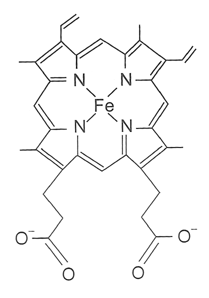
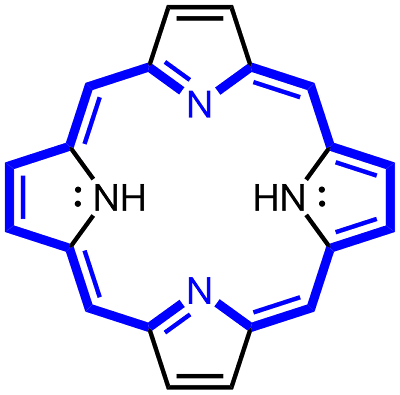
یک گروه هِم شامل یک اتم آهن است که در یک حلقه هتروسیکلیک نگهداری میشود، این حلقههای آلی هتروسیلیک «پورفیرین» (Porphyrin) نامیده میشود. اتم آهن محل اتصال اکسیژن در هموگلوبین محسوب میشود. اتم آهن به طور مساوی با هر چهار نیتروژن در مرکز حلقه پیوند خورده است که در یک صفحه قرار دارند. برای ایجاد موقعیتهای پنجم و ششم، دو پیوند اضافی عمود بر صفحه از هر طرف با آهن ایجاد میشود، یکی برای اتصال به پروتئین و دیگری برای اتصال اکسیژن مورد استفاده قرار میگیرد. اتم آهن میتواند به صورت یونهای Fe+2 یا Fe+3 باشد. شکلی از Hb که در آن یون Fe+3 وجود دارد، قادر به اتصال با اکسیژن نیست، به این شکل از Hb، «فری هموگلوبین» یا «متاموگلوبین» (Methaemoglobin) میگویند.
مولکول Hb انواع مختلفی دارد که ممکن است در شرایط گوناگون، هر یک از انواع آن موثر باشد. به عنوان مثال، یک نوع هموگلوبین وجود دارد که ممکن است در ارتفاعات زیاد کارایی بالاتری داشته باشد، این نوع هموگلوبین در حیواناتی مانند لاما دیده میشود. علاوه بر این برخی از انواع هموگلوبینها هم وجود دارند که در ارتفاعات پایین موثرتر عمل میکنند، از جمله این هموگلوبینها را میتوان در گردش خون گوزن دم سفید مشاهده کرد. هموگلوبین جنینی با هموگلوبین مادر نیز متفاوت است.
در انسان بالغ، متداولترین نوع Hb یک ساختار تترامر است (که شامل 4 زیر واحد پروتئینی) که به نام هموگلوبین A شناخته میشود. این نوع هموگلوبین از دو زیر واحد α و دو زیر واحد β به صورت غیر کووالانسی ساخته شده است. این ساختار تحت عنوان α2β2 شناخته میشود. زیر واحدها از نظر ساختاری مشابه و تقریباً در یک اندازه هستند. هر زیر واحد دارای وزن مولکولی حدود 16٫000 دالتون است، به این ترتیب در کل وزن مولکولی تترامر در حدود 64000 دالتون محاسبه میشود. در بین هموگلوبینها، هموگلوبین A بیشتر مورد مطالعه قرار گرفته و اطلاعات بیشتری از آن در دسترس است.
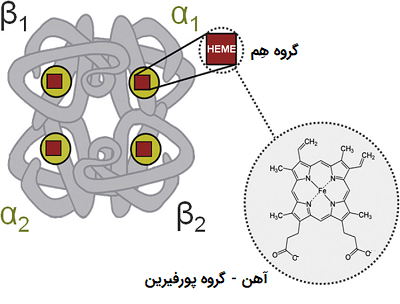
چهار زنجیره پلی پپتیدی توسط پلهای نمکی، پیوندهای هیدروژنی و تعامل آبگریز به یکدیگر متصل میشوند. بین زنجیرههای α و β دو نوع تماس وجود دارد: α1β1 و α1β2.
انواع هموگلوبین ها در انسان
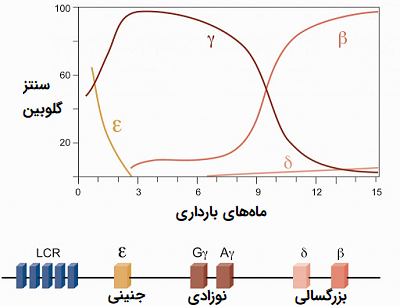
در ۱۲ هفته اول بعد از بارداری هموگلوبینهای زیر در جنین وجود دارند:
- در دو ماه بعد از لقاح و تشکیل جنین یک نوع هموگلوبین به نام هموگلوبین (Portland) با ساختار δ2γ2 وجود دارد.
- در هفته دهم تا دوازدهم جنینی دو نوع Hb با ترکیب ساختارهای ξ2ε2 و α2ε2 به ترتیب Grower1 و Grower2 نامیده میشود.
- در جنین بعد از ۱۲ هفتگی هموگلوبین دیگری به نام هموگلوبین F با ترکیب ساختاری α2γ2 تشکیل میشود.
- پس از این مرحله از هفته هجدهم بارداری تا هفته بیست و چهارم هموگلوبین A1 تشکیل میشود اما میزان هموگلوبین F در این دوران نسبت به هموگلوبین A بیشتر است.
بدن انسان در دوران بزرگسالی میتواند هموگلوبینهای زیر را داشته باشد:
- هموگلوبین A با ترکیب ساختاری α2β2 متداولترین نوع هموگلوبین در بدن است.
- هموگلوبین A2 با تترامر α2δ2 در بزرگسالان در حدود ۲٫۵ درصد از هموگلوبینهای خون را به خود اختصاص داده است.
- هموگلوبین F دارای ترکیب ساختاری α2γ2 است که در بزرگسالان در جمعیتهای محدود از گلبولهای قرمز که سلولهای F نامیده میشوند، وجود دارد.
نحوه اتصال هموگلوبین با مولکولهای مختلف
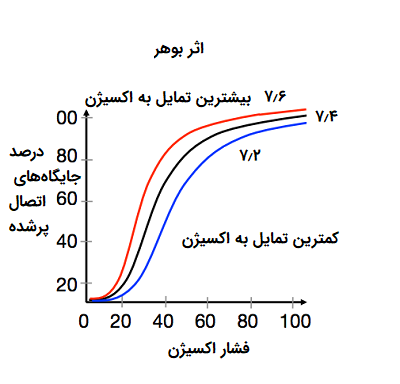
در فرم تترامری هموگلوبین طبیعی در بزرگسالان، اتصال اکسیژن یک «فرآیند تعاونی» (Cooperative Process) به شمار میآید. میل اتصال هموگلوبین به اکسیژن با اشباع این مولکول با اکسیژن افزایش مییابد. به همین دلیل، منحنی اتصال اکسیژن به هموگلوبین سیگموئیدی یا S شکل است، در حالی که منحنی برای اتصالات غیر تعاونی (Noncooperative) به شکل هایپربولیک طبیعی یا زنگولهای است.
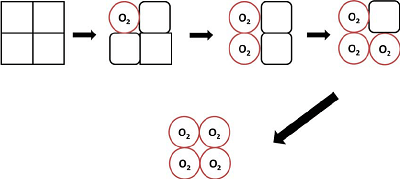
این اتصالات تعاونی مثبت از طریق تغییرات اثرات فضایی کمپلکس پروتئین هموگلوبین حاصل میشود: هنگامی که یک زیر واحد پروتئینی در هموگلوبین اکسیژن میگیرد، یک کانفورمیشن یا تغییر آرایش ساختاری را در کل مجموعه ایجاد میکند و باعث میشود که میل ترکیبی 3 زیر واحد دیگر پروتئینی به اکسیژن افزایش یابد.
یک مولکول هموگلوبین تنها میتواند چهار مولکول اکسیژن را منتقل کند. در مهرهداران، هموگلوبینها در گلبولهای قرمز یا اریتروسیتها یافت میشوند که هر یک از آنها حاوی حدود 300 میلیون مولکول هموگلوبین هستند. هموگلوبینهای موجود در گلبولهای قرمز حدود 98٪ از اکسیژن موجود در خون انسان را منتقل میکنند.
اتصال اکسیژن به هموگلوبین تحت تأثیر حضور مولکولهایی مانند مونوکسید کربن (CO) قرار میگیرد. مونو اکسید کربن در دود حاصل از مصرف دخانیات و آلودگیهای هوا ناشی از دود خودروها و کارخانهها وارد جریان خون میشود. میل ترکیبی هموگلوبین به اکسیژن در حضور مونوکسید کربن کاهش مییابد زیرا هر دو گاز برای جایگاههای یکسان اتصال در هموگلوبین با یکدیگر رقابت میکنند، این در حالی است که میل ترکیبی هموگلوبین به مونو اکسید کربن نسبت به اکسیژن بیشتر است.
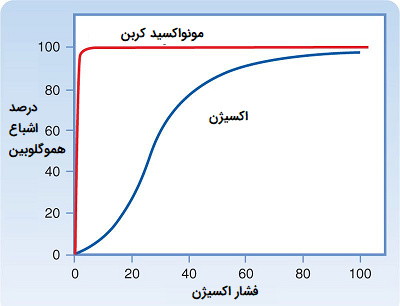
میل اتصال هموگلوبین به مونوکسید کربن 300 برابر بیشتر از میل اتصال آن به اکسیژن است، این امر به این معنی است که مقادیر اندک از مونواکسید کربن به طور چشمگیری توانایی هموگلوبین در انتقال اکسیژن را کاهش میدهد. هنگامی که هموگلوبین با مونوکسید کربن ترکیب شود، یک ترکیب قرمز بسیار روشن به نام کربوکسی هموگلوبین تشکیل میدهد. هنگامی که هوای استنشاقی حاوی میزان مونواکسید کربن به میزان کمی در حدود 0٫02٪ باشد، سردرد و حالت تهوع در فرد ایجاد میشود. اگر غلظت آن به 0٫1٪ افزایش یابد، ممکن است که فرد بیهوش شود. در افراد سیگاری با مصرف بالا، تا 20٪ از مکانهای فعال اکسیژن توسط مونواکسید کربن قابل انسداد هستند.
دی اکسید کربن (CO2) یک محل اتصال متفاوت در هموگلوبین را اشغال میکند. دی اکسید کربن با آب واکنش میدهد تا پروتونهای آزاد شده را به بیکربنات و اسید کربنیک (+H) انتقال دهد، این واکنش از طریق «آنهیدراز کربن» (Carbonic Anhydrase) کاتالیز میشود:
بنابراین، خون با میزان زیاد دی اکسید کربن دارای pH (اسیدیتر) پایینی است. هموگلوبین میتواند پروتونها و دی اکسید کربن را به هم متصل کند که به این ترتیب تغییر شکل در این پروتئین به وجود میآید و همین امر منجر به آزاد شدن اکسیژن از هموگلوبین میشود. پروتونها در نقاط مختلف در امتداد پروتئین به آن متصل میشوند و دی اکسید کربن از جایگاه گروه آلفا - آمینو به هموگلوبین اتصال مییابد و «کاربامات» (Carbamate) که از مشتقات اسید کاربامیک است را تشکیل میدهد. از سویی دیگر، هنگامی که سطح دی اکسید کربن در خون کاهش مییابد (به عنوان مثال، در اطراف ریهها)، دی اکسید کربن آزاد میشود و همین امر میل ترکیبی هموگلوبین به اکسیژن را افزایش میدهد. این کنترل میل ترکیبی هموگلوبین به اکسیژن با اتصال و آزاد کردن دی اکسید کربن به آن، تحت عنوان «اثر بوهر» (Bohr Effect) شناخته میشود.
هموگلوبین همچنین دارای میل ترکیبی رقابتی برای مونوکسید گوگرد (SO)، دی اکسید نیتروژن (NO2) و سولفید هیدروژن (H2S) است. اتم آهن در گروه هِم برای پشتیبانی از حمل و نقل اکسیژن باید در حالت اکسیداسیون Fe+2 باشد.
اکسیداسیون به حالت Fe+3 هموگلوبین را به همیگلوبین یا «مت هموگلوبین» (Methemoglobin) تبدیل میکند که نمیتواند اکسیژن را به هِم متصل کند. دی اکسید نیتروژن و اکسید نیتروژن قادر به تبدیل هموگلوبین به مت هموگلوبین هستند.

در خون افرادی که در ارتفاعات زیاد سکونت دارند یا کوهنوردان، غلظت 2،3-دیفسفوگلیسیرات (2،3-DPG) افزایش یافته است، این امر به این افراد امکان میدهد در شرایط کمبود فشار اکسیژن مقدار بیشتری از اکسیژن را به بافتها تحویل دهند. این پدیده که در آن مولکول Y با اتصال مولکول X بر یک مولکول انتقال دهنده Z تأثیر میگذارد، یک «اثر آلوستریک هتروتروپی» (Heterotropic Allosteric Effect) نامیده میشود.
یک گونه از هموگلوبین، به نام هموگلوبین جنین (Hb F ،α2γ2) که در جنین در حال رشد یافت میشود و به اکسیژن با میل بیشتری نسبت به هموگلوبین بالغ متصل میشود. این بدان معناست که درصد بالاتری از این نوع هموگلوبین در مقایسه با هموگلوبین بالغ، به اکسیژن در غلظتهای پایین متصل میشود. به همین دلیل است که خون جنین در جفت قادر به گرفتن اکسیژن از خون مادر است.
ساخت و تجزیه هموگلوبین
گلبولهای قرمز یا اریتروسیتها متداولترین سلولها در خون به شمار میآيند، به طوری که ۵ میلیون از گلبولهای قرمز در هر میلی لیتر خون وجود دارند. میانگین طول عمر هر گلبول قرمز در حدود ۱۲۰ روز است. در بزرگسالان، گلبولهای قرمز در مغز استخوان قرمز تولید میشوند، اما در جنین و نوزادان این سلولها در کیسه زرد، کبد و طحال ساخته میشوند.
در طول بلوغ گلبولهای قرمز، آنها هسته و میتوکندری خود را از دست میدهند و این سلولها تمام فعالیتهای خود را بر انتقال اکسیژن و دی اکسید کربن قرار میدهند. در حالت کلی، سلولهای قرمز خون به صورت میانگین دارای ۳۰۰ میلیون مولکول هموگلوبین هستند.
سنتز هموگلوبین با تولید هِم به صورت هماهنگ انجام میشود. هِم مسئول اتصال برگشت پذیر اکسیژن است، گلوبین پروتئینی است که هِم را در ساختار خود جای داده و از آن محافظت میکند. هِم در میتوکندری و سیتوزول گلبولهای قرمز خون ساخته میشود، این اتفاق زمانی رخ میدهد که سلولهای قرمز هنوز هسته خود را از دست ندادهاند.
نقص و کمبود در میزان آهن موجب کاهش سنتز هِم میشود و در نهایت کم خونی در فرد ایجاد میکند. کمبود آهن یکی از دلایل رایج کم خونی در افراد مختلف است. مهار سنتز هِم نیز کم خونی ایجاد میکند که بر اثر مصرف برخی از داروها و تاثیر سموم مختلف به وجود آید.
زمانی که عمر سلولهای قرمز خون به پایان میرسد یا این سلولها به دلایلی میمیرند، آنها شکسته شده و هموگلوبین از این گلبولها جدا میشود و آهن موجود در آن مورد بازیافت قرار میگیرد.
هنگامی که حلقه پورفیرین تخریب میشود، قطعات به طور معمول توسط کبد جمعآوری شده و به صفرا ترشح میشوند. محصول نهایی و اصلی تخریب هِم، «بیلی روبین» (Bilirubin) است که به عنوان یک ماده دفعی زرد رنگ شناخته میشود.
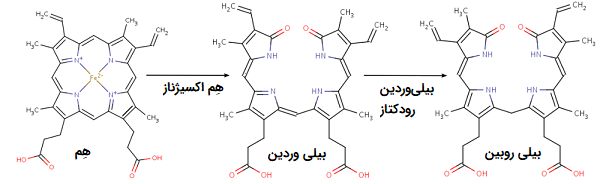
اگر سلولهای قرمز خون با سرعت بیشتری نسبت به حد معمول از بین بروند، افزایش سطح ماده شیمیایی بیلی روبین در خون قابل مشاهده میشود. پروتئین هموگلوبینی که به درستی تخریب نشده یا هموگلوبینی که به اشتباه از سلولهای خونی رها شده است، میتواند رگهای خونی کوچک، به خصوص عروق ظریف تصفیه خون کلیهها را مسدود کند و باعث آسیب به کلیه شود. آهن موجود در Hb در کبد ذخیره یا به صورت هموگلوبین جدید بازیافت میشود.
هموگلوبین در گیاهان تثبیت کننده نیتروژن
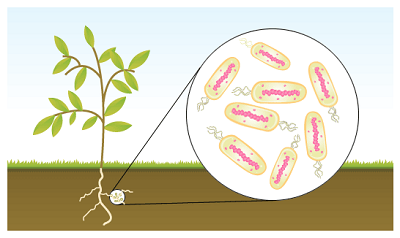
بسیاری از گونههای گیاهان مانند حبوبات و برخی دیگر از گیاهان قادر به دریافت نیتروژن جوی از هوا و تبدیل آن به نیترات برای تهیه مواد غذایی مورد نیاز گیاه هستند. این فرایند که تثبیت نیتروژن نامیده میشود، در شرایطی اتفاق میافتد که انواع خاص باکتریها، از جمله گونههای جنس «ریزوبیوم» (Rhizobium)، ریشههای گیاه را آلوده کرده و گرههایی را در آنجا تولید میکنند. نکته قابل توجه این است که این گرههای نیتروژن حاوی مقادیری Hb هستند. به جز این مورد، هموگلوبین در سلسله گیاهان دیده نشده است. به نظر میرسد که هموگلوبین با کنترل فشار جزئی اکسیژن در گرهها، تثبیت نیتروژن را به صورت غیرمستقیم تقویت میکند.
نقش هموگلوبین در بیماریها و تشخیص
کاهش سطح هموگلوبین در صورت کاهش میزان گلبولهای قرمز خون یا بدون کاهش آنها، منجر به بروز علائم کم خونی در فرد میشود. کم خونی میتواند دلایل مختلفی داشته باشد، اما مهمترین علت آن کمبود آهن به شمار میآید.
با کمبود آهن سنتز هِم کاهش مییابد و گلبولهای قرمز در آنمی یا کم خونی فقر آهن به دو شکل، هیپوکروم (فاقد رنگدانه قرمز هموگلوبین) و میکروسیتیک (کوچکتر از حد طبیعی) دیده میشوند. انواع دیگر کم خونیها وجود دارند که کمتر اتفاق میافتند. در «همولازیز» (Hemolysis) (تسریع در تجزیه گلبولهای قرمز)، زردی یا یرقان همراه با متابولیت هموگلوبین یعنی بیلی روبین، ایجاد میشود و هموگلوبین موجود در گردش خون نارسایی کلیوی به وجود میآورد. جهش در زنجیره گلوبین با «هموگلوبینوپاتی» (Haemoglobinopathies) یا اختلالات مربوط به ساختمان هموگلوبین، مانند کم خونی داسی شکل و تالاسمی در ارتباط است.
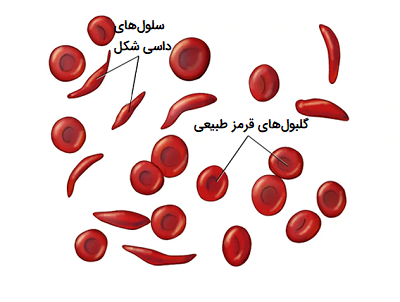
کم خونی داسی شکل یک بیماری مغلوب ژنتیکی است که باعث نقص در یک اسید آمینه در یکی از زنجیرههای پروتئینی هموگلوبین میشود، به طوری که در این جهش یک اسید آمینه والین جایگزین یک اسید امینه گلوتامیک اسید میشود. وجود این جهش در هموگلوبین باعث میشود در زمان کمبود اکسیژن (زمانی که فرد ورزش سنگین انجام میدهد)، شکل گلبولهای قرمز تغییر کند و آنها با یکدیگر ترکیب شوند. در افرادی با این جهش ژنتیکی، انسداد رگهای خونی اغلب زمانی که بدن به اکسیژن زیادی نیز دارد، اتفاق میافتد. در نتیجه افراد مبتلا به کم خونی داسی شکل، در دورههای مختلف و در شرایط مختلف دچار مشکلات حاد میشوند و عمر این افراد اغلب از حالت طبیعی کمتر است.
گروهی از اختلالات ژنتیکی وجود دارند که به عنوان «پورفیریا» (Porphyrias) شناخته میشوند. این اختلالات با خطاهایی در مسیرهای متابولیکی سنتز هِم مشخص میشوند. جورج سوم پادشاه انگستان، مشهورترین فرد مبتلا به پورفیری محسوب میشود. از دلایل این بیماری تولید و دفع بیش از حد پورفیرین است.
در برخی مواقع، هموگلوبین A به آهستگی با گلوکز در یک مکان مشخص درون مولکول ترکیب میشود. با افزایش غلظت گلوکز در خون Hb گلیکوزیله شده به نام HbA1c تشکیل میشود. همان طور که میزان گلوکز در خون افزایش مییابد، درصد Hb A که به HbA1c تبدیل میشود نیز افزایش پیدا میکند.
در افراد مبتلا به دیابت که گلوکز خون آنها معمولا بالا است، درصد HbA1c نیز افزایش مییابد. به دلیل فرایند آهسته ترکیب گلوکز با Hb، درصد HbA1c نشان دهنده میزان متوسط گلوکز خون در طول یک دوره تقریبا ۳ ماهه است.
تعیین میزان Hb یکی از بخشهای آزمایشهای خون روتین است و به عنوان قسمتی از یک آزمایش CBC یا شمارش کامل سلولهای خونی مورد بررسی قرار میگیرد. نتایج این آزمایشها به صورت گرم بر لیتر، گرم بر دسی لیتر یا میلیمول بر لیتر گزارش میشود (۱ گرم بر دسی لیتر برابر با ۰٫۶۲ میلیمول در لیتر است). از تعیین میزان هموگلوبین خون در آزمایش بررسی گلوکز خون استفاده میشود.
سطح گلوکز خون در هر ساعت میتواند بسیار متغیر باشد، بنابراین ممکن است یک یا تنها چند نمونه از بیمار برای بررسی میزان گلوکز خون در طولانی مدت بیانگر میزان واقعی گلوکز خون بیمار نباشد. به همین دلیل استفاده از HbA1c برای بررسی طولانی مدت گلوکز خون گزینه مناسبتری است زیرا میزان متوسط گلوکز خون را در طول یک دوره نشان میدهد.
اگر میزان HbA1c شش درصد یا کمتر را نشان دهد به معنی این است که گلوکز خون فرد به مدت طولانی تحت کنترل قرار گرفته است، اما زمانی که این میزان از ۷ بالاتر باشد، بیانگر دیابت کنترل نشده است. به همین دلیل بررسی و اندازهگیری میزان Hb گلیکوزیله شده A1C برای ارزیابی وضعیت بیماری افراد مبتلا به دیابت از اهمیت ویژهای برخورد است.
پروتئینهای دیگر متصل شونده به اکسیژن
هموگلوبین تنها پروتئین متصل شونده به اکسیژن در جانداران زنده نیست، بلکه گروههایی از انتقال دهندهها و پروتئینهای متصل شونده به اکسیژن در سلسله جانوران و گیاهان وجود دارد. ارگانیسمهای دیگر مانند باکتریها، آغازیان و قارچها دارای پروتئینهای مشابه Hb هستند که نقشهای شناخته شده و پیش بینی شده آنها شامل اتصال برگشت پذیر به لیگاندهای گازی است.
میوگلوبین (Myoglobin)
میوگلوبین در بافت ماهیچهای بسیاری از مهرهداران از جمله انسان یافت میشود و به ویژه در پستانداران دریایی مانند والها و فوکها (به بافت عضلانی رنگ قرمز یا خاکستری تیره میدهد)، وجود دارد. میوگلوبین از نظر ساختاری و توالی بسیار شبیه به هموگلوبین است، اما در این پروتئین چیدمان تترامری که در هموگلوبین مشاهده میشود، وجود ندارد و ساختار کلی آن از یک مونر ساخته شده است که به شکل تعاونی به اکسیژن متصل نمیشود و بیشتر برای ذخیره اکسیژن به جای انتقال آن استفاده میشود.
هموسیانین (Hemocyanin)
هموسیانین دومین پروتئین متداول برای انتقال اکسیژن به شمار میآید که در طبیعت یافت میشود. هموسیانین در خون بسیاری از گونههای بندپایان و صدفها وجود دارد. این پروتئین از گروههای پروستتیک مس به جای گروههای آهن هِم استفاده میکند و به این دلیل است که زمانی که هموسیانینها اکسیژن میگیرند، به رنگ آبی در میآیند.
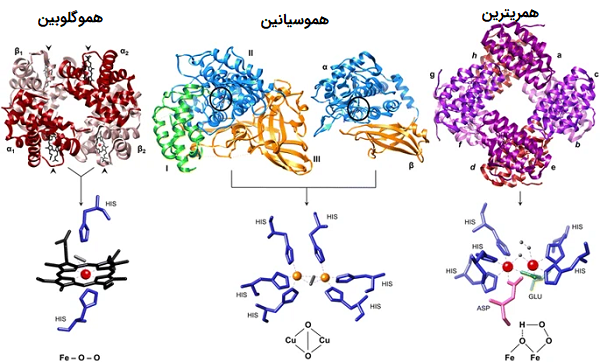
همریترین (Hemerythrin)
برخی از بیمهرگان دریایی و تعداد کمی از گونههای کرم آنلید از این پروتئین غیر هِم و دارای آهن برای انتقال اکسیژن در خون خود استفاده میکنند. این پروتئین زمانی که اکسیژن دریافت میکند، به رنگ صورتی یا بنفش در میآید و در حالت بدون اکسیژن فاقد رنگ است.
وانابینز (Vanabins)
این پروتئین به عنوان «وانادیوم کروماگن» (Vanadium Chromagen) نیز شناخته میشود، وانابینز در خون ماهیان دریایی وجود دارد و درون این پروتئینها از فلز نادر وانادیوم به عنوان گروه پروستتیک استفاده میشود، در واقع وانادیوم بخشی از وانابینز است که به اکسیژن متصل میشود.
اریتروکریون (Erythrocruorin)
این پروتئین در بسیاری از آنلیدها از جمله کرمهای خاکی یافت میشود. اریتروکرین یک پروتئین غول پیکر آزاد و شناور در خون است. این انتقال دهنده اکسیژن حاوی تعداد بسیار زیادی آهن هِم است که در زیر واحدهای متصل به هم این کمپلکس قرار میگیرند. از این رو، جرم مولکولی اریتروکریون بیش از ۳٫۵ میلیون دالتون محاسبه میشود.
پیناگلوبین (Pinnaglobin)
این پروتئین انتقال دهنده اکسیژن تنها در گونهای از نرمتنان به نام «پینا اسکواموسا» (Pinna Squamosa) دیده میشود. پیناگلوبین یک پروتئین پورفیرین بر پایه منگنز است که به رنگ قهوهای وجود دارد.
لگ هموگلوبین (Leghemoglobin)
این نوع از هموگلوبین در انواع گیاهان وابسته به خانواده حبوبات مانند یونجه و سویا یافت میشود. باکتریهایی که برای تثبیت نیتروژن در ریشه این گیاهان زندگی میکنند با آهن هِم (پروتئین متصل شونده به اکسیژن) در برابر اکسیژن محافظت میشوند.
اندازهگیری هموگلوبین
همان طور که در بالا اشاره شد، هموگلوبین معمولا به عنوان بخشی از آزمایش شمارش کامل سلولهای خونی در آزمایشهای خون روتین مورد بررسی قرار میگیرد. روشهای متعددی برای اندازهگیری هموگلوبین وجود دارد. اغلب این روشها در حال حاضر با دستگاههای اتوماتیک در تستهای خونی مورد استفاده قرار میگیرد.
درون این دستگاه گلبولهای قرمز خون شکسته میشوند تا هموگلوبین از آنها خارج شود و در محلول قرار بگیرد. هموگلوبینهای آزاد در معرض یک محلول شیمیایی قرار میگیرند که دارای سیانید است و با اتصالات محکمی به مولکولهای هموگلوبین متصل میشود تا سیانو متهموگلوبین ساخته شود. با تابش نور به این محلول و اندازهگیری میزان نور جذب شده (به خصوص در طول موج ۵۴۰ نانومتر) میزان هموگلوبین تعیین میشود.
چرا هموگلوبین خون باید اندازهگیری شود؟
Hb به عنوان یکی از فاکتورهای مهم خونی در اکثر آزمایشها مورد بررسی قرار میگیرد. از جمله شرایطی که نیاز به شمارش این پروتئین در خون دارند، شما موارد زیر هستند:
- بررسی سابقه خانوادگی مشکلات خونی مانند بیماری کم خونی داسی شکل
- وجود عفونت در بدن
- کمبود آهن در رژیم غذایی
- از دست دادن خون در حین عمل جراحی یا بر اثر جراحت شدید
- در زمان بارداری
- وجود بیماری در فرد که بر هموگلوبین تاثیر میگذارد.
برای انجام این آزمایش نیاز به شرایط ناشتایی نیست.
میزان هموگلوبین در خون
سن و جنسیت هر دو در تعیین بازه طبیعی تعداد این پروتئین در خون موثر هستند. در جدول زیر مقادیر نرمال Hb در خون آورده شده است.
| طبقهبندی | میزان Hb در واحد گرم بر دسی لیتر |
| نوزدان | ۱۸ - ۱۱ |
| کودکان | ۱۶٫۵ -۱۱٫۵ |
| مردان بزرگسال | ۱۶٫۵ -۱۳٫۵ |
| زنان بزرگسال | ۱۶ - ۱۲ |
| زنان باردار | ۱۶ - ۱۱ |
میزان Hb کمتر از ۱۳ گرم بر دسی لیتر در مردان به عنوان هموگلوبین کم در نظر گرفته میشود و در زنان این مقدار کمتر از ۱۲ گرم بر دسی لیتر است.
این مقادیر با توجه به روش اندازهگیری و آزمایشگاه ممکن است کمی متفاوت باشد، بنابراین میزان Hb تعیین شده را باید با توجه به بازه رفرنس هر آزمایشگاه مورد بررسی قرار داد.
میزان هموگلوبین بالا
میزان بالای Hb نشان دهنده برخی از بیماریهای نادر مانند «پلی سیتمی» (Polycythemia) است. در این بیماری بدن گلبولهای قرمز را بیش از حد طبیعی تولید میکند که باعث میشود غلظت خون افزایش یابد. غلظت خون موجب ایجاد رسوب و انسداد عروق، سکته و حملات قلبی میشود. این بیماری ممکن است در مواردی موجب مرگ بیمار شود.
میزان هموگلوبین میتواند دلایل دیگری از قبیل کمبود آب، بیماریهای مزمن قلبی یا ریوی، مصرف بیرویه اریتروپویتین، سیگار کشیدن یا زندگی در مناطقی با ارتفاع بالا داشته باشد.
از جمله علائم وجود میزان بالایی از این پروتئین در خون میتوان به موارد زیر اشاره کرد:
- خارش پوستی
- سردرد
- سرگیجه
- خونریزی مکرر
- تعریق بیش از حد معمول
- مفاصل دردناک
- کاهش وزن غیرطبیعی
- وجود لکههای زرد در چشم و پوست (زردی)
- احساس خستگی مفرط
- راشهای قرمز و کبود پوستی
میزان هموگلوبین پایین
میزان پایین Hb نشان دهنده کم خونی در فرد است. انواع متفاوتی از کم خونی وجود دارد که شامل موارد زیر هستند:
- کم خونی فقر آهن از متداولترین انواع کم خونی به شمار میآید. این آنمی زمانی که فرد به میزان کافی آهن در بدن خود برای تولید Hb ندارد، اتفاق میافتد. این نوع آنمی معمولا با کاهش میزان خون به وجود میآيد، اما گاهی این بیماری به دلیل جذب کم آهن رخ میدهد.
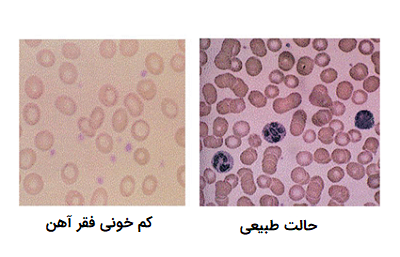
- کم خونی بارداری نوعی کم خونی فقر آهن است که به دلیل بارداری و زایمان که در این حالت بدن به مقادیر بالای آهن احتیاج دارد، اتفاق میافتد.
- کم خونی فقر ویتامین زمانی ایجاد میشود که در رژیم غذایی مواد مغذی مانند ویتامین B12 یا فولیک اسید بسیار کم باشد. این بیماری موجب تغییر در شکل و کارایی گلبولهای قرمز میشود.
- آنمی آپلاستیک نوعی اختلال است که در سلولهای بنیادی سازنده خون در مغز استخوان ایجاد میشود، زمانی که این سلولها توسط سیستم ایمنی بدن مورد حمله قرار میگیرند، گلبولهای قرمز کاهش پیدا میکنند.
- آنمی همولیتیک نوعی کم خونی است که در شرایط خاص و یا به صورت ارثی در فرد بروز مییابد. این بیماری زمانی رخ میدهد که گلبولهای قرمز خون در جریان خون یا در طحال شکسته شوند.
- کم خونی داسی شکل یک بیماری ژنتیکی است که در آن پروتئین هموگلوبین ساختار غیرطبیعی دارد. در این بیماری گلبولهای قرمز شکلی شبیه داس و ساختمان شکننده دارند، به همین دلیل در عبور از رگهای خونی باریک، اغلب این گلبولهای قرمز غیرطبیعی دچار مشکل میشوند و در این رگها انسداد ایجاد میکنند.
کم خونی گاهی در شرایطی دیگر نیز به وجود میآید، به عنوان مثال، در بیماریهای کلیوی و در طول دوره شیمی درمانی برای درمان سرطان ممکن است توانایی گلبولهای قرمز تحت تاثیر قرار گرفته و تغییر کند. از جمله علائم انواع کمی خونی و کمبود Hb میتوان به موارد زیر اشاره کرد:
- ضعف
- تنگی نفس
- سرگیجه
- ضربان نامظم قلب
- سردرد
- دستها و پاهای سرد
- رنگ پریدگی
- درد سینه













بسیار عالی ، کامل و روان بود ؛ سپاس
besiar awli va mofid bod kheili mamnonm
بسیار خوب ومفید بود فقط همه جا گفتیم میل ترکیبی اکسیژن با خون بالاست وبا مونکسید بیشتر از اینها.
این اعداد کدامند؟ یعنی بصورت عددی میل ترکیبی ها چیستند؟؟
خیلی جامع و کامل بود . ممنونم
عالی بود عالی
عالی بود ممنون
خیلی بهتر از کلاس های درس دانشگاهی توضیح دادید-باتشکر
خیلی مهم بود، واقعا من استفادە ازش کردم..
عالی بود??