زنجیره انتقال الکترون چیست؟ | زبان ساده
زنجیره انتقال الکترون (Electron Transport Chain) مجموعهای از پروتئينها است که الکترونها را در طول غشای میتوکندری مطابق با شیب پروتون برای تولید ATP منتقل میکنند. ATP به عنوان واحدهای انرژی برای فرایندهای متابولیکی سلولها مورد استفاده قرار میگیرد.
زنجیره انتقال الکترون کجا انجام میشود؟
در طی زنجیره انتقال الکترون، یک گرادیان پروتون ایجاد میشود تا پروتونها از ماتریکس میتوکندری به فضای بین غشایی سلول پمپ شوند که این امر به تسهیل تولید ATP نیز کمک میکند. غالباً، استفاده از گرادیان پروتون به عنوان مکانیسم «کمو اسموتیک» (Chemiosmotic) كه سنتز ATP را هدایت میكند، شناخته میشود. مکانیسم کمو اسموتیک به تولید غلظت بالاتری از پروتونها برای تولید نیروی محرکه پروتون متکی است. مقدار ATP ایجاد شده به طور مستقیم با تعداد پروتونهایی که در غشای داخلی میتوکندری پمپ میشوند، متناسب است.
زنجیره حمل و نقل الکترونی شامل یک سری واکنشهای اکسیداسیون و احیا است که برای انتقال الکترونها از یک مولکول دهنده به یک مولکول پذیرنده، متکی به کمپلکسهای پروتئینی است. در نتیجه این واکنشها، گرادیان پروتون تولید میشود و این امکان را فراهم میآورند تا کار مکانیکی به انرژی شیمیایی تبدیل شود و سنتز ATP صورت گیرد.
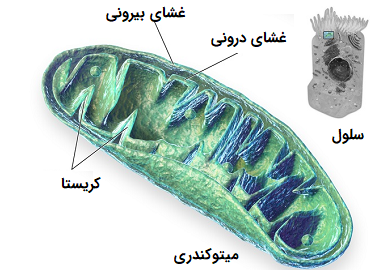
این کمپلکسها در غشای میتوکندری داخلی در بخشهایی به نام «کریستا» (Cristae) در یوکاریوتها تعبیه شدهاند. ماتریکس توسط غشای داخلی میتوکندری محصور شده است و درون آن، آنزیمهای لازم مانند «پیروات دهیدروژناز» (Pyruvate Dehydrogenase) و «پیروات کربوکسیلاز» (Pyruvate Carboxylase) قرار دارند. این فرآیند همچنین در یوکاریوتهای فتوسنتز کننده در غشای تیلاکوئید کلروپلاستها و پروکاریوتها مشاهده میشود.
فرآوردههای جانبی از چرخهها و فرآیندهای دیگر مانند چرخه اسید سیتریک یا کربس، اکسیداسیون اسید آمینه و اکسیداسیون اسید چرب در زنجیره انتقال الکترونی مورد استفاده قرار میگیرند. همان طور که در واکنش کلی اکسیداسیون و احیا مشاهده میشود:
در یک واکنش گرمازا زمانی که الکترونها از کمپلکسهای پروتئینی عبور میکنند، انرژی آزاد میشود. این انرژی در قالب سه مولکول ATP ایجاد میشود. فسفات موجود در ماتریکس میتوکندری از طریق گرادیان پروتون وارد شده و برای تولید ATP بیشتر مورد استفاده قرار میگیرد. فرایند تولید بیشتر ATP از طریق فسفوریلاسیون ADP را «فسفوریلاسیون اکسیداتیو» (Oxidative Phosphorylation) میگویند.
نحوه انجام فرایند زنجیره انتقال الکترون
زنجیره انتقال الکترون آخرین مرحله از تنفس هوازی و تنها بخشی از متابولیسم گلوکز است که از اکسیژن اتمسفر استفاده میکند. اکسیژن به طور مداوم در گیاهان پخش میشود و در حیوانات از طریق دستگاه تنفسی وارد بدن میشود. حمل و نقل الکترون مجموعهای از واکنشهای اکسیداسیون و احیا را در بر میگیرد که در آنها الکترونها به سرعت از یک جز به قسمت دیگر منتقل میشوند تا در انتهای زنجیره الکترونها به اکسیژن مولکولی رسیده و آن را احیا کنند و مولکولهای آب تولید شوند.
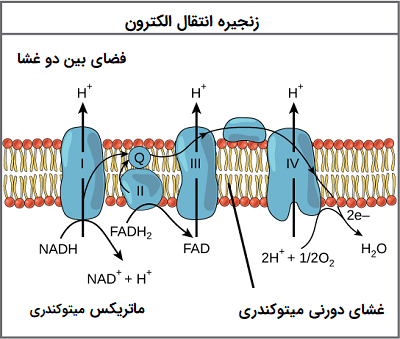
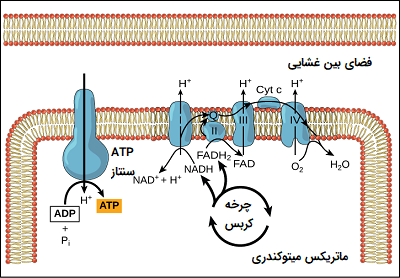
چهار کمپلکس از پروتئینها وجود دارند که در تصویر 1 آنها با برچسب I تا IV نشان داده شدهاند و جمع شدن این چهار کمپلکس به همراه حاملهای الکترونی و ترکیبات دیگر، زنجیره انتقال الکترون نامیده میشوند. این زنجیره در چندین نسخه در غشای داخلی میتوکندری یوکاریوتها و غشای پلاسمایی پروکاریوتها وجود دارد. البته توجه داشته باشید که زنجیره انتقال الکترونی پروکاریوتها ممکن است به اکسیژن احتیاج نداشته باشد زیرا برخی از پروکاریوتها در شرایط بی هوازی زندگی میکنند. ویژگی مشترک همه زنجیرههای انتقال الکترون وجود پمپ پروتون برای ایجاد شیب پروتون در سراسر یک غشا است.
کمپلکس یک
برای شروع، دو الکترون به اولین کمپلکس NADH منتقل میشوند. این مجموعه، با عنوان کمپلکس I، از فلاوین مونونوکلئوتید (FMN) و پروتئین حاوی آهن - گوگرد (Fe-S) تشکیل شده است. FMN از ویتامین B2 مشتق شده است و به آن «ریبوفلاوین» (Riboflavin) نیز گفته میشود. ریبوفلاوین یکی از چندین گروه پروستتیک یا فاکتورهای مشترک در زنجیره انتقال الکترون است. یک گروه پروستتیک یک مولکول غیرپروتئینی است که وجود آن برای فعالیت یک پروتئین ضروری محسوب میشود.
گروههای پروستتیک مولکولهای غیرپپتیدی آلی یا معدنی هستند که به پروتئین متصل شده و عملکرد آن را تسهیل میکنند. به عنوان مثال، گروههای پروستتیک میتوانند شامل کوآنزیمها باشند که به عنوان گروههای پروستتیک آنزیمها به شمار میآیند. آنزیم موجود در کمپلکس یک، «NADH دهیدروژناز» (NADH dehydrogenase) نام دارد، این آنزیم، پروتئین بسیار بزرگی است و 45 زنجیره اسید آمینه دارد. کمپلکس I میتواند چهار یون هیدروژن را از طریق ماتریکس به درون فضای بین غشایی پمپ کند و از این طریق است که شیب یون هیدروژن بین دو محفظه جدا شده توسط غشای داخلی میتوکندری ایجاد میشود.
کمپلکس دو و یوبی کینون
کمپلکس II مستقیماً FADH2 را دریافت میکند، این حامل الکترونی نمیتواند از کمپلکس I عبور کند. ترکیبی که کمپلکسهای اول و دوم را به کمپلکس سوم متصل میکند، یوبی کینون (Ubiquinone Q) نام دارد. این مولکول که به کوآنزیم کیو (ْQ) نیز معروف است، محلول در چربی بوده و آزادانه از طریق هسته آبگریز غشا حرکت میکند. پس از احیا این مولکول (QH2)، یوبی کینون الکترونهای خود را در زنجیره انتقال الکترون به کمپلکس بعدی منتقل میکند. یوبی کینون الکترونهای حاصل از NADH از کمپلکس I و الکترونهای مشتق شده از FADH2 از کمپلکس II را از طریق آنزیم «سوکسینات دهیدروژناز» (Succinate Dehydrogenase) دریافت میکند. این آنزیم و FADH2 یک کمپلکس کوچک را تشکیل میدهند که الکترونها را به طور مستقیم به زنجیره انتقال الکترون منتقل میکند، از آنجایی که این الکترونها انرژی لازم برای پمپ پروتون را در اولین کمپلکس انرژی تامین نمیکنند، بنابراین مولکولهای ATP کمتری از الکترونهای FADH2 ساخته میشوند. تعداد مولکولهای ATP به دست آمده مستقیماً با تعداد پروتونهای پمپ شده در غشای داخلی میتوکندری متناسب است.
کمپلکس سوم
کمپلکس سوم متشکل از سیتوکروم b، پروتئین حاوی آهن - گوگرد (Fe-S) به نام مرکز Rieske (بخشی از سیتوکروم bc1) و پروتئین سیتوکروم c است. به کمپلکس سوم «سیتوکروم اکسیدوردوکتاز» (cytochrome oxidoreductase) نیز گفته میشود. پروتئینهای سیتوکروم دارای گروه پروستتیک متشکل از «هِم» (Heme) هستند. این مولکول هِم شبیه به هِم موجود در هموگلوبین است، اما در اینجا برخلاف هموگلوبین که اکسیژن را در رگهای خونی انتقال میدهد، الکترون را حمل میکند. در نتیجه، با عبور الکترونها، یون آهن در هسته خود کاهش یافته و اکسیده میشود و در بین حالتهای مختلف اکسیداسیون نوسان میکند: ++Fe (کاهش یافته) و +++Fe (اکسید شده).
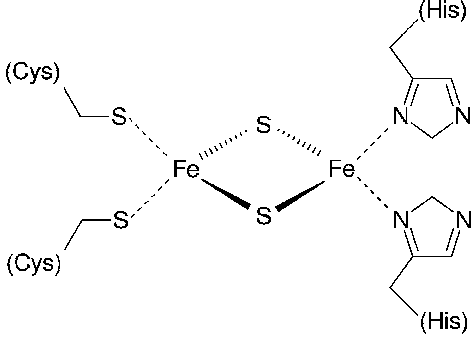
مولکولهای هِم موجود در سیتوکرومها به دلیل تأثیر پروتئینهای مختلف که آنها را به هم متصل میکنند، دارای ویژگیهای کمی متفاوت هستند و به هر یک از مجموعهها ویژگیهای کمی متفاوت میدهند. کمپلکس III پروتونها را از طریق غشا پمپ میکند و الکترونهای خود را به سیتوکروم c منتقل میکند تا به پروتئینها و آنزیمهای کمپلکس چهارم منتقل شوند (سیتوکروم c پذیرنده الکترونها از یوبی کینون است، با این حال، یوبی کینون معمولا یک جفت الکترون با خود حمل میکند، اما سیتوکروم c در یک زمان تنها میتواند یک الکترون را دریافت کند).
کمپلکس چهارم
کمپلکس چهارم از پروتئینهای سیتوکروم c ،a و a3 تشکیل شده است. این مجموعه شامل دو گروه هِم (در هر یک از دو سیتوکروم a و a3 یک گروه هِم وجود دارد) و سه یون مس (یک جفت CuA و یک CuB در سیتوکروم a3) است. سیتوکرومها یک مولکول اکسیژن را به صورت کاملا پایدار بین یونهای آهن و مس نگه میدارند تا اینکه اکسیژن کاملاً احیا شود. پس از کاهش اکسیژن، دو یون هیدروژن از محیط اطراف در کنار آن قرار میگیرند تا یک مولکول آب (H2O) ایجاد شود. حذف یونهای هیدروژن از سیستم به شیب یون مورد استفاده در فرایند اسمز شیمیایی منجر میشود.
اسمز شیمیایی
در اسمز شیمیایی یا کمو اسمز (Chemiosmosis)، انرژی آزاد شده حاصل از سری واكنشهای اکسیداسیون و احیا که در بالا توضیح داده شدند، برای پمپ یونهای هیدروژن (پروتونها) از طول غشا استفاده میشود. توزیع نامساوی یونهای هیدروژن در سراسر غشا، غلظت و شیبهای الکتریکی را ایجاد میکند (بنابراین یک گرادیان الکتروشیمیایی به وجود میآید)، این گرادیان به دلیل بار مثبت یونهای هیدروژن و تجمع آنها در یک طرف غشا ایجاد میشود.
اگر غشا برای انتشار یونهای هیدروژن باز باشد، یونها تمایل دارند که به داخل ماتریکس پخش شوند زیرا شیب الکتروشیمیایی آنها را این گونه هدایت میکند. باید این نکته را مد نظر قرار داد که بسیاری از یونها بدون کمک کانالهای یونی نمیتوانند در مناطق غیرقطبی غشاهای فسفولیپیدی پخش شوند. به همین ترتیب، یونهای هیدروژن موجود در فضای ماتریکس فقط میتوانند از طریق غشای میتوکندری داخلی و به وسیله یک پروتئین غشایی انتگرال به نام «ATP سنتاز» (ATP Synthase) عبور کنند. این پروتئین پیچیده به عنوان یک ژنراتور کوچک عمل میکند و با نیروی یونهای هیدروژن که از طریق آن انتشار مییابند، فعال شده و گرادیان الکتروشیمیایی آنها را کاهش میدهد. چرخش قسمتهایی از این دستگاه مولکولی اضافه کردن یک فسفات به ADP را برای ایجاد ATP تسهیل میکند، ATP سنتاز این کار را با استفاده از انرژی بالقوه شیب یون هیدروژن انجام میدهد.
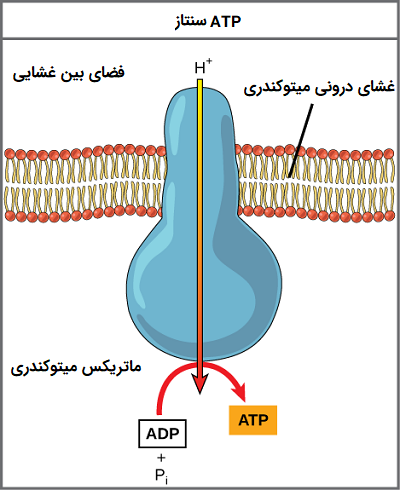
اسمز شیمیایی برای تولید 90 درصد ATP ساخته شده در هنگام کاتابولیسم گلوکز هوازی استفاده میشود. این فرایند همچنین روشی است که در واکنشهای نوری فتوسنتز به کار میرود تا انرژی نور خورشید را در فرآیند فتوفسفریلاسیون به دست آورد. باید به این نکته توجه کرد که تولید ATP با استفاده از فرایند اسمز شیمیایی در میتوکندری، فسفوریلاسیون اکسیداتیو نامیده میشود.
نتیجه کلی این واکنشها تولید ATP از انرژی الکترونهای برداشته شده از اتمهای هیدروژن است. این اتمها در اصل بخشی از یک مولکول گلوکز بودند. در انتهای مسیر از الکترونها برای احیای یک مولکول اکسیژن به یونهای اکسیژن استفاده میشود. الکترونهای اضافی موجود در اکسیژن، یونهای هیدروژن (پروتونها) را از محیط اطراف جذب میکنند و در نهایت آب تشکیل میشود.
بازده ATP
تعداد مولکولهای ATP حاصل از کاتابولیسم گلوکز میتواند متفاوت باشد. به عنوان مثال، تعداد یونهای هیدروژنی که کمپلکسهای پروتئینی زنجیره انتقال الکترون میتوانند از طریق غشا پمپ کنند، بین گونههای مختلف متفاوت است. منبع دیگر این تفاوتها از حاملهای الکترونی در غشاهای میتوکندری ناشی میشود. NADH حاصل از گلیکولیز به راحتی وارد میتوکندری نمیشود.
بنابراین، الکترونها توسط +NAD یا +FAD در داخل میتوکندری جمع میشوند. همان طور که قبلاً نیز اشاره شد، مولکولهای +FAD میتوانند یونهای کمتری را حمل کنند. در نتیجه، هنگامی که +FAD به عنوان حامل عمل کند، کمتر مولکول ATP تولید میشود. +NAD به عنوان انتقال دهنده الکترون در کبد مورد استفاده قرار میگیرد و +FAD در سلولهای مغز این کار را انجام میدهد.
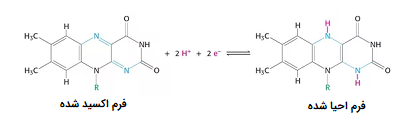
یکی دیگر از عواملی که بر عملکرد مولکولهای ATP ایجاد شده از گلوکز تأثیر میگذارد، این واقعیت است که ترکیبات واسطه در این مسیرها برای مقاصد دیگر استفاده میشوند. کاتابولیسم گلوکز با مسیرهایی که سایر ترکیبات بیوشیمیایی موجود در سلولها را می سازند یا تجزیه میکنند در ارتباط است. به عنوان مثال، قندهایی غیر از گلوکز برای استخراج انرژی در مسیر گلیکولیتیک تغذیه میشوند. علاوه بر این، قندهای پنج کربنی که اسیدهای نوکلئیک را تشکیل میدهند از ترکیبات واسطه موجود در گلیکولیز ساخته میشوند. برخی اسیدهای آمینه غیرضروری نیز میتوانند از ترکیبات واسطه فرایند گلیکولیز و چرخه اسید سیتریک تشکیل شوند. لیپیدها مانند کلسترول و تری گلیسیرید نیز از ترکیبات واسطه این مسیرها ساخته شده و هر دو اسید آمینه و تری گلیسیرید برای انرژی از طریق این مسیرها تجزیه میشوند. به طور کلی، در سیستمهای زنده، این مسیرهای کاتابولیسم گلوکز حدود 34 درصد از انرژی موجود در گلوکز را استخراج میکند.
خلاصه مطلب
زنجیره انتقال الکترون بخشی از تنفس هوازی است که از اکسیژن آزاد به عنوان پذیرنده نهایی الکترونهای برداشته شده از ترکیبات میانی در کاتابولیسم گلوکز استفاده میکند. زنجیره انتقال الکترون از چهار کمپلکس پروتئینی بزرگ تشکیل شده که در غشای میتوکندری داخلی قرار دارند و دو حامل الکترونی کوچک و قابل انتشار میتوانند الکترونها را بین این کمپلکسهای پروتئینی منتقل کنند. الکترونها از طریق مجموعه واکنشهای اکسیداسیون و احیا عبور میکنند که در این حین، مقدار کمی انرژی آزاد در سه نقطه برای انتقال یونهای هیدروژن در طول غشا استفاده میشود.
این فرآیند به شیب استفاده شده در اسمز شیمیایی کمک میکند. الکترونهایی که از طریق زنجیره انتقال الکترون عبور میکنند به تدریج انرژی خود را از دست میدهند، الکترونهای پرانرژی که توسط NADH یا FADH2 به زنجیره منتقل میشوند، زنجیره را کامل میکنند، زیرا الکترونهای کم انرژی، مولکولهای اکسیژن را احیا کرده و مولکولهای آب را تشکیل میدهند. سطح انرژی آزاد الکترونها از حدود 60 کیلو کالری در مول در NADH یا 45 کیلو کالری در مول در FADH2 به حدود صفر کیلو کالری در مول در آب میرسد.
محصولات نهایی زنجیره انتقال الکترونی آب و ATP هستند. تعدادی از ترکیبات میانی چرخه اسید سیتریک را میتوان به مسیرهای آنابولیسم یا سنتز سایر مولکولهای بیوشیمیایی مانند اسیدهای آمینه غیرضروری، قندها و لیپیدها منتقل کرد. همین مولکولها میتوانند به عنوان منبع انرژی برای مسیرهای گلوکز استفاده شوند.













نسبت فسفریلاسیون به اکسیداسیون (P/O) برای NADH ، ده چهارم (۱۰/۴) است. یعنی نسبت تعداد ATP تولید شده به ازای مصرف هر مولکول اکسیژن ۲.۵ است.
و برای FADH2 این نسبت برابر ۱.۵ است.
این اعداد از کجا می آیند؟؟ اگر ممکنه جواب بدید.
هر 4 پروتون که از داخل کانال یونی ATPسنتتاز عبور کنند یه دونه ATP تولید میشه، و از طرفی به ازای اکسایش هر مولکول NADH تعداد 10 تا H وارد فضای بین دو غشا میشه، از تقسیم 10 بر 4 میشه 2/5 ، به ازای هر مولکول FADH2 هم 6 تا پروتون H وارد فضای بین دو غشا میشه که با این تفاسیر 1/5 مولکول ATP تولید میشود