گاز نجیب – به زبان ساده
آیا تا به حال به چگونگی عملکرد لامپ نئون چراغ خودرو خود یا فلش زنون دوربین عکاسی دقت کردهاید؟ به بادکنکهای پر شده از گاز هلیوم چطور؟ احتمالاً عنوان گاز نجیب به گوشتان آشنا باشد، اگر علاقهمند هستید تا بیشتر با انواع این گازها و خصوصیاتشان آشنا شوید، با ما در ادامه این مقاله همراه باشید تا به زبانی ساده به معرفی آنها بپردازیم.
- با اتمهای گاز نجیب و نام آنها آشنا میشوید.
- ویژگی اتمهای آخرین گروه جدول تناوبی را میشناسید.
- میآموزید دلیل نامگذاری گازهای نجیب و بیاثر بودن آنها چیست.
- میتوانید آرایش الکترونی گازهای نجیب را بنویسید.
- با روشهای تولید گازهای نجیب و فراوانی آنها آشنا میشوید.
- یاد میگیرید کاربرد گازهای نجیب در پزشکی و سایر صنایع چیست.


گاز نجیب چیست؟
گازها نجیب به گازهای گروه آخر جدول تناوبی گفته میشود. این گروه شامل گازهای هلیوم، نئون، آرگون، کریپتون، زنون و رادون است. آخرین لایه الکترونی تمامی این گازها شامل اوربیتالها و زیرلایههایی کاملا پر است. به همین علت این گازها تمایلی به تشکیل یون، تشکیل پیوند و شرکت در واکنش شیمیایی ندارد. به همین علت به این گازها کاز نجیب یا گاز بیاثر گفته میشود.
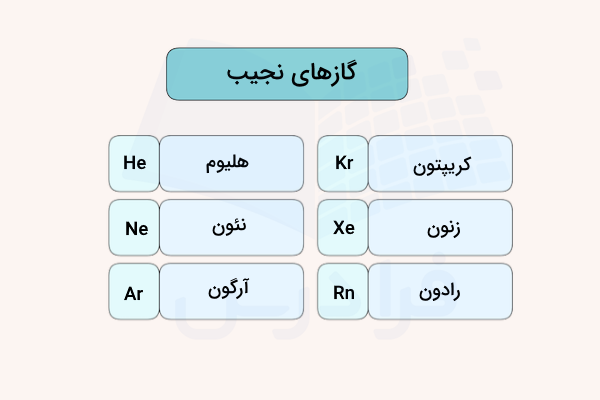
آخرین گروه جدول تناوبی
اگر نگاهی به جدول تناوبی عناصر انداخته باشید، ۷ عنصر را در آخرین گروه (از سمت چپ، گروه ۱۸ - VIIIa) میبینید. این ۷ گاز (البته گازی شکل در دمای اتاق) به ترتیب از بالا به پایین بر اساس افزایش عدد اتمی عبارتاند از:
- هلیوم (Helium) با نماد He با عدد اتمی ۲
- نئون (Neon) با نماد Ne با عدد اتمی ۱۰
- آرگون (Argon) با نماد Ar با عدد اتمی ۱۸
- کریپتون (Krypton) با نماد Kr با عدد اتمی ۳۶
- زنون (Xenon) با نماد Xe با عدد اتمی ۵۴
- رادئون (Radon) با نماد Rd با عدد اتمی ۸۶
- اگانسون (Oganesson) با نماد Og با عدد اتمی ۱۱۸ (سنگینترین عنصر جدول تناوبی)
اخیرا در سال 2017 عنصر اگانسون (Og) با عدد اتمی ۱۱۸ به این گروه اضافه شده است.
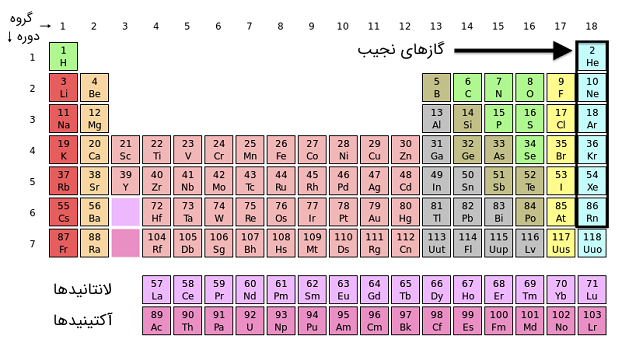
گاز نجیب (Noble Gas) بیرنگ، بیبو، بدون مزه و غیر قابل اشتعال است. تا چندین دهه پس از کشف این عناصر، به طور سنتی به آنها عناصر گروه صفر جدول تناوبی میگفتند. چرا که معتقد بودند این گازها نمیتوانند با دیگر اتمها پیوندی برقرار کنند و یا با دیگر ساختارهای شیمیایی واکنش داده و ترکیب شوند.
در ویدیوی کوتاه زیر میتوانید ببینید که گاز نجیب چیست و انواع آن کدام است.
از آنجا که عناصر این گروه به سختی با دیگر عناصر تشکیل پیوند میدهند، نام گازهای نجیب برای آنان نیز انتخاب شد. با پیشرفت علم و کامل شدن مدلهای اتمی، ساختار الکترونی و همچنین ظهور برخی کاربردها، واژه مناسبتر گروه ۱۸ به آنها اطلاق شد.

نام گروه گازهای نجیب
احتمالا عنوان گازهای نادر را نیز شنیدهاید. در آن زمان به نظر کاشفان، این گازها در جهان بسیار نادر و همچنین از لحاظ شیمیایی خنثی بودند (ترکیب نمیشدند). به همین دلیل این عناصر را گازهای نادر (Rare Gases) یا گازهای راکد (Inert Gases) نامگذاری کردند. امروزه میدانیم که این عناصر در جهان هستی فراوان هستند، از این حیث کلمه نادر میتواند گمراه کننده باشد. همچنین کلمه Inert این مفهوم را میرساند که عناصر این گروه نمیتوانند ترکیبات شیمیایی را ایجاد کنند، پس بهتر است که از این کلمه نیز استفاده نکنیم.
در علم شیمی، برای فلزاتی نظیر طلا و پلاتین که تمایلی به واکنش شیمیایی ندارند، کلمه نجیب استفاده میشود. پس بهتر است که برای این عناصر گازی شکل که تمایلی به ترکیب و یا واکنش شیمیایی ندارند، نیز کلمه نجیب را به کار بریم. دلیل این عدم تمایل به ایجاد پیوند را میتوان در آرایش الکترونی این عناصر که در شکل زیر آمده است، جستوجو کرد. همانطور که مشخص است اوربیتالهای لایه آخر (ظرفیت) این عناصر از الکترون پر بوده و از این حیث پایدارند.

فراوانی گازهای نجیب
فراوانی گازهای نجیب با افزایش عدد اتمی آنها کاهش پیدا میکند. هلیوم نیز همانند هیدروژن یکی از فراوانترین عناصر جهان هستی است. دیگر عناصر گروه ۱۸ جدول تناوبی جز رادئون (Rn)، در هوایی که تنفس میکنیم، یافت میشوند. با سرد کردن هوا تا نقطه انجماد این گازها، تقطیر و جداسازی، میتوان به آنها دست پیدا کرد. البته دستیابی به هلیوم (He) به دلیل سبکی و رفتن به سمت لایههای بالایی جو دشوار است. اکثراً هلیوم را به طور تجاری از چاه و منابع گاز طبیعی به دست میآورند.
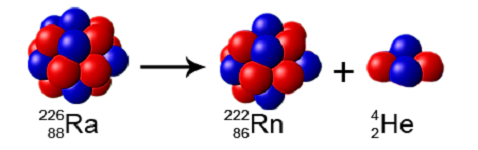
رادئون (Rn) نیز معمولا حاصل تجزیه رادیواکتیو عنصر رادیوم (Radium) با عدد اتمی ۸۸ است. هسته اتم پرتوزا رادیوم (Ra) به صورت خودبهخودی با تابش ذره و انرژی فرو میریزد. ذره تابش شده هستههای هلیوم () بوده که به ذره آلفا نیز معروف است. با تابش ذره آلفا، در واقع هسته هلیوم با عدد اتمی ۲، از تعداد پروتون و نوترونهای رادیوم (Ra) کم شده و در نتیجه تبدیل به اتم رادئون (Rn) میشود.
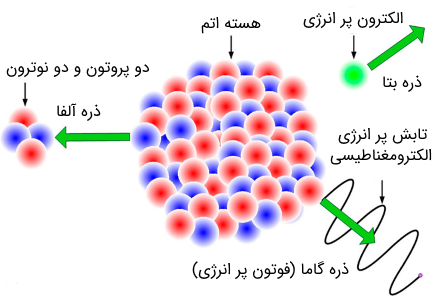
هسته اتمهای سنگین و رادیواکتیو پس از تجزیه و فروپاشی ۳ نوع تابش از خود بر جای میگذارند. این ۳ نوع تابش در شکل زیر نشان داده شده است.
ویژگیهای گاز نجیب
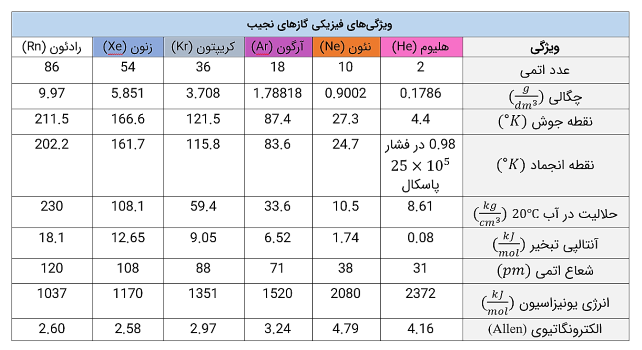
ویژگیهای فیزیکی گاز نجیب نظیر چگالی، الکترونگاتیوی، آنتالپی تبخیر و ... در جدول زیر خلاصه شدهاند:
کاربرد گاز نجیب
مطابق با جدول تناوبی عناصر، هر عنصر گاز نجیب بین گروه ۱۷ (هالوژنها) و گروه ۱ (فلزهای قلیایی) قرار گرفته است. در واقع عناصر گازی شکل گروه ۱۸، بین الکترونگاتیوترین (Electronegative) عناصر (گروه ۱۷ - هالوژنها) و الکتروپوزیتیوترین (Electropositive) عناصر (گروه ۱ - فلزات قلیایی) جای گرفتهاند. لازم به ذکر است که الکترونگاتیوی یک اتم به معنی تمایل نسبی آن برای جذب الکترون به سمت هسته خود است. پس هر چه تمایل یک عنصر به گرفتن الکترون بیشتر باشد، الکترونگاتیوتر است. الکتروپوزیتیوی نیز مفهومی عکس دارد. پس بیدلیل نیست که عناصر گروه ۱۸ تمایلی به اشتراک گذاشتن الکترونهای خود و ایجاد پیوند ندارند.
از آنجا که گازهای نجیب تمایلی به ایجاد پیوند ندارند، نسبت به اکسیژن بیتفاوت بوده و لذا اشتعالپذیر نیستند. این خاصیت به نوبه خود میتواند دارای کاربردهای فراوانی باشد. گازهای نجیب، به دلیل عدم واکنش در بسیاری از فرآیندها نظیر جوشکاری، برش و لایهنشانی در صنعت و کاربردهایی پزشکی نظیر ضد عفونی کردن زخم، اغلب در مهندسی پلاسما به کار میروند.
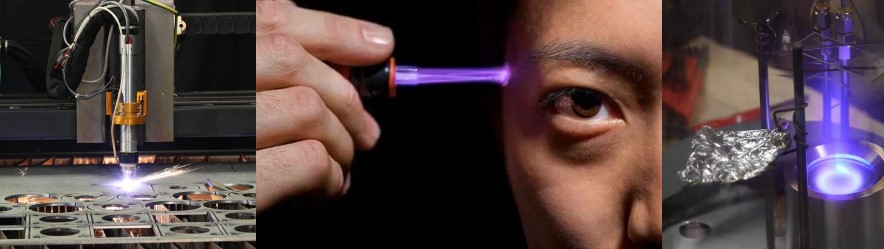
در این تصاویر از گاز آرگون (Ar) برای تشکیل پلاسما استفاده شده است. سمت چپ یک برش دهنده پلاسما، تصویر وسط یک پلاسما جت جهت کاربردهای پزشکی و تصویر سمت چپ فرآیند لایهنشانی به کمک پلاسما را نشان میدهد. در فرآیندهای صنعتی که به وسیله پلاسما (گاز یونیزه شده) انجام میشوند، از گازهای نجیب نظیر آرگون (به دلیل قیمت کمتر) برای تولید پلاسما استفاده میشود. همانطور که در تصاویر مشخص است، پلاسمای آرگون طیفی بنفش دارد. در واقع با اعمال اختلاف پتانسیل و تبدیل شدن گاز آرگون به پلاسما، اتمهای برانگیخته آرگون فوتونی در فرکانس (رنگ) بنفش تابش میکنند.

از دیگر کاربردهای گاز های نجیب میتوان به جذب و انتشار تابش الکترومغناطیسی اشاره کرد. از این خاصیت در لامپهای تخلیه الکتریکی و دستگاههای روشنایی نظیر لامپهای پرنور فلورسنت (Fluorescent)، چراغ خودروها، تابلوهای تبلیغاتی و ... استفاده میکنند. اگر یک گاز نجیب در فشار کم در یک محفظه شیشهای محدود شود، با اعمال ولتاژی متناسب با فشار گاز درون محفظه، الکترونهای اتمهای گاز برانگیخته شده (تشکیل پلاسما) و با تابش فوتونی در فرکانس (رنگ) خاص به حالت پایه بر میگردند. با اعمال پیوسته ولتاژ میتوانیم نور پیوستهای نظیر آنچه در تابلوهای تبلیغاتی مشاهده میکنید، داشته باشیم.
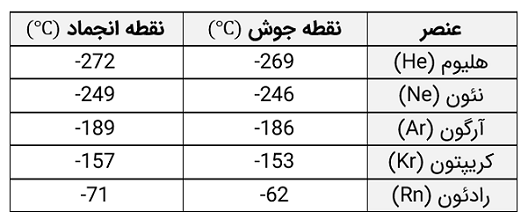
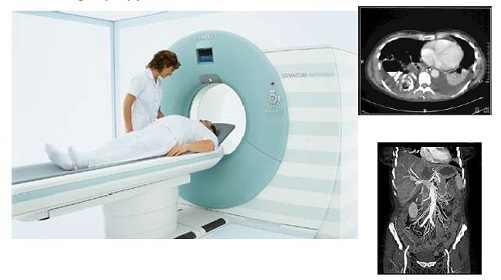
از نقطه جوش بسیار کم و نقطه ذوب پایین این عناصر، میتوان در مطالعه ماده در دماهای پایین بهره جست. یکی از کاربردهای قابل توجه از هلیوم مایع، خنکسازی قطعات ابررسانا در دستگاههای MRI پیشرفته است.

مخلوط کردن هلیوم در کپسولهای اکسیژن برای تنفس بهتر غواصان نیز میتواند مفید باشد. چرا که هلیوم با خون واکنشی نداشته، تشکیل حباب نمیدهد و به راحتی از بدن دفع میشود. همچنین از زنون نیز علیرغم قیمت بالای آن، به عنوان یک گاز بیهوشی استفاده میکنند. چرا که غیر قابل اشتعال بوده، واکنشی با خون ندارد و به راحتی از بدن دفع میشود. رادئون نیز عنصری سنگینن و رادیواکتیویته است و کاربردهای محدودی در پرتو پزشکی و درمان سرطان دارد.
اگانسون (Og) که سنگینترین عنصر جدول تناوبی است، در آزمایشگاه به طور محدودی مشاهده شده و طول عمر بسیار کوتاهی دارد. در نتیجه خواص فیزیکی و شیمیایی آن به طور دقیق مشخص و مستند نیست. به دلیل بالابودن عدد اتمی که به منزله زیاد بودن تعداد پروتونها است، نیروی دافعه بین بارهای مثبت بر نیرو هستهای قوی قلبه کرده و هسته عنصر اگانسون شکلی شبیه به حباب دارد. این عنصر به افتخار کاشف آن «یوری اگانسون» (Yuri Oganessian) به همین نام در جدول تناوبی عناصر در سال ۲۰۱۷ قرار گرفت.

در صورتی که مطلب بالا برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای مهندسی شیمی
- آموزش شیمی عمومی
- مجموعه آموزشهای فیزیک
- آموزش مقدمه ای بر مهندسی شیمی
- عدد اتمی، عدد جرمی و ایزوتوپ — به زبان ساده
- طیف اتمی — از صفر تا صد
^^













باسلام فیلمی که قرار دادین متاسفانه نه پخش میشه و نه دانلود میشه لطفا اصلاح کنید ممنونم
با سلام؛
از بازخورد شما سپاسگزاریم. فیلم اصلاح شد.
با تشکر از همراهی شما با مجله فرادرس