نوترکیبی چیست؟ – تعریف، انواع و کاربردها – به زبان ساده
نوترکیبی DNA چگونه کار میکند؟ این اتفاق به طور مکرر در انواع مختلف سلول رخ میدهد و پیامدهای مهمی در یکپارچگی ژنومی، تکامل و بیماریهای انسانی دارد. نوترکیبی در ژنتیک، مکانیزم اولیهای است که از طریق آن تنوع به جمعیتها وارد میشود. توالی DNA یک کروموزوم میتواند در بخشهای بزرگ نیز با فرایندهای نوترکیبی و جابجایی تغییر کند. نوترکیبی تولید مولکولهای DNA جدید از دو مولکول DNA والدین یا بخشهای مختلف مولکول DNA یکسان است. این موضوعات در این مقاله بررسی خواهد شد.
نوترکیبی چیست؟
نوترکیبی فرآیند شکسته شدن و ترمیم رشتههای DNA، تولید ترکیبات جدید آللها (حالات مختلف ژنی) بوده که تقریباً در همه ارگانیسمهای چند سلولی و برخی از تک سلولیها رخ میدهد و پیامدهای مهمی برای بسیاری از فرایندهای تکاملی دارد. اثرات نوترکیبی میتوانند خوب باشند زیرا ممکن است سازگاری موجود را تسهیل کنند، اما هنگامی که ترکیبی از قرارگیری مفید آللها را برهم زند مضر است، نوترکیبی بین آرایهها (Taxa)، گونهها، افراد یک گونه و در سراسر ژنوم بسیار متغیر است. نوترکیبی زمانی اتفاق میافتد که دو مولکول DNA تکههایی از مواد ژنتیکی خود را با یکدیگر مبادله کنند.
نوترکیبی DNA چیست؟
مولکولهای DNA از دو گونه مختلف که در ارگانیسم میزبان قرار میگیرند و ترکیبات ژنتیکی جدیدی تولید میکنند برای علم پزشکی، کشاورزی و صنعت دارای ارزش هستند. نوترکیبی DNA فرآیندی است که در آن پروتئینهای تخصصی با DNA ارتباط برقرار میکنند و مولکولهایی با محتوای توالی نوکلئوتیدی تغییر یافته ایجاد میکنند.
بسته به جزئیات واکنش، نتایج نوترکیبی حذف، کپی یا یک ترتیب جدید از تغییرات آللی است. همچنین نوترکیبی DNA یکی از ابزارهای اساسی است که در مهندسی ژنتیک استفاده میشود. نوترکیبی را میتوان به عناوین سایت خاص یا همولوگ طبقه بندی کرد. نوترکیبهای اختصاصی سایت، توالیهای سیگنال خاصی را در مولکولهای DNA هدف تشخیص میدهند. در مقابل، برای شروع واکنش نوترکیبی همولوگ، نیاز به همسانی توالی بین یا درون مولکولی دارد. DNA نوتركيب برای تغيير شكل ژنوم در تمام شكلهای زندگی بكار میرود.
در حالی که نوترکیبی جایگاه اختصاصی در درجه اول توسط ویروسها و ترانسپوزونها برای ورود و خروج به ژنوم میزبان خود استفاده میشود، نوترکیبی همولوگ تبادلات میوز بین کروموزومها و تفکیک جهشهای مفید و مضر را امکان پذیر میکند. تنوع ژنتیکی در جاهایی که برخی از خصوصیات فیزیکی مانند رنگ چشم انسان متغیر است رخ میدهد. این تنوع نتیجه توالیهای DNA متناوب است که همان ویژگی فیزیکی را کد میکنند. این توالیها معمولاً آلل نامیده میشوند. آللهای مختلف مرتبط با یک ویژگی خاص فقط کمی با یکدیگر متفاوت هستند و آنها همیشه در همان مکان (یا منبع) درون DNA ارگانیسم یافت میشوند. به عنوان مثال، فارغ از اینکه شخصی چشم آبی، قهوهای یا چشم سبز داشته باشد، آللهای رنگ چشم در همان ناحیه از همان کروموزوم در همه انسانها یافت میشوند. ترکیب منحصر به فرد آللها که همه ارگانیسمهای دارای تولید مثل جنسی از والدین خود دریافت میکنند، نتیجه مستقیم نوترکیبی کروموزومها در هنگام تقسیم میوز است.
در نوترکیبی چه اتفاقی می افتد؟
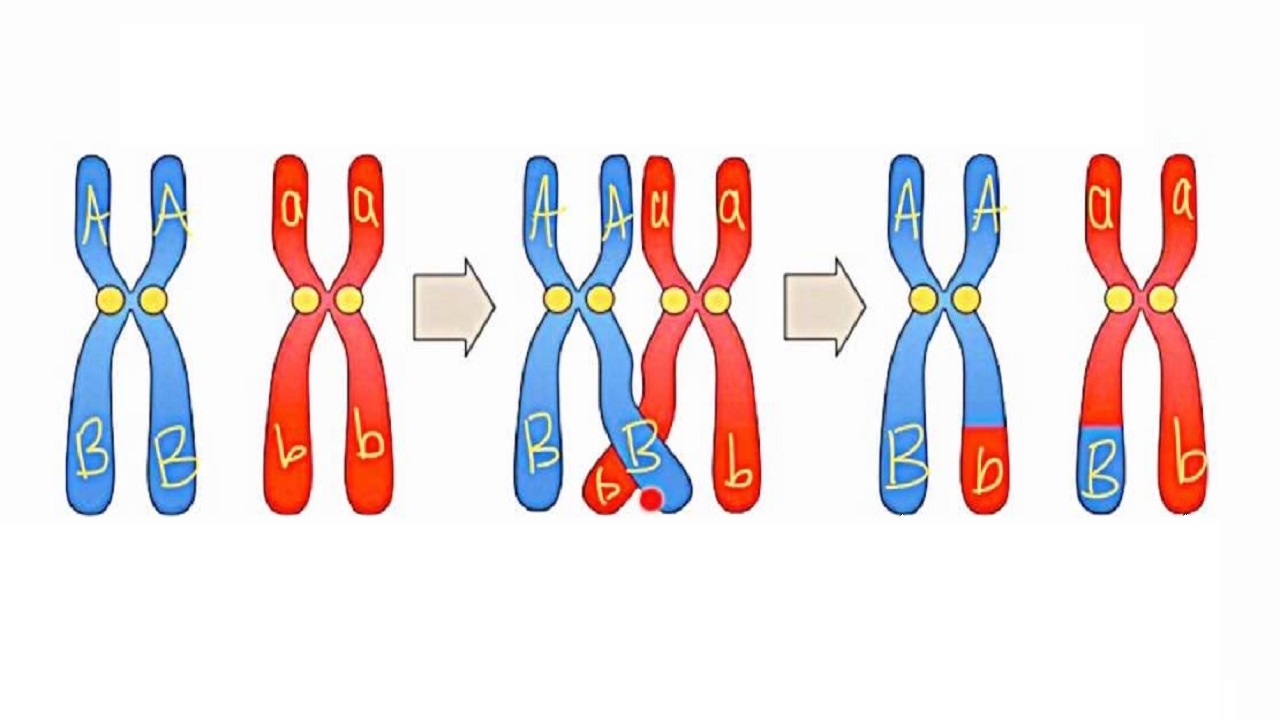
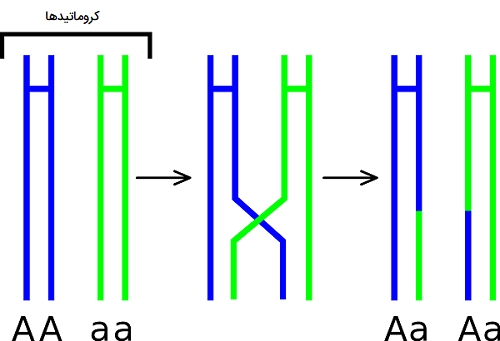
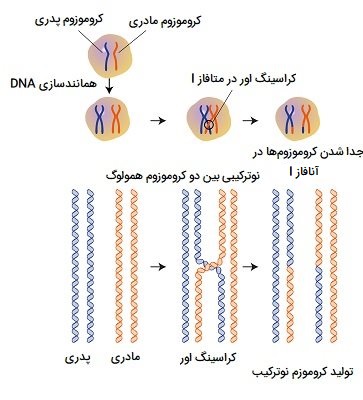
نوترکیبی ژنتیکی یک فرآیند پیچیده است که شامل تراز شدن دو رشته DNA همولوگ، شکستگی دقیق هر رشته، تبادل مساوی بخشهای DNA بین دو رشته و قرارگیری مولکولهای DNA نوترکیب حاصل از طریق عملکرد آنزیمهایی به نام لیگازها است. علی رغم پیچیدگی این فرآیند، در اکثر موارد، وقایع نوترکیبی با دقت و صحت قابل توجهی رخ میدهد. وقتی نوترکیبی در حین تقسیم میوز رخ میدهد، کروموزومهای همولوگ سلول بسیار نزدیک به هم قرار میگیرند. سپس، رشته DNA درون هر کروموزوم دقیقاً در همان مکان میشکند و دو انتهای آزاد بر جای میگذارد.
سپس هر انتهای آن به داخل کروموزوم دیگر عبور کرده و پیوندی به نام کیاسما ایجاد میکند. در طی این فرایند، عبور مقاطع زیادی از DNA که حاوی ژنهای مختلفی هستند از یک کروموزوم به کروموزوم دیگر معمول است. سرانجام، با نزدیک شدن پروفاز به متافاز و شروع آن، فرآیند عبور از هم به پایان میرسد و کروموزومهای همولوگ آماده جدایی میشوند. وقتی بعداً در طی آنافاز I کروموزومهای همولوگ از هم جدا شوند، هر کروموزوم دارای ترکیبات آللی جدید و منحصر به فردی است که نتیجه مستقیم فرایند نوترکیبی است.
نوترکیبی در چه سلول هایی رخ میدهد؟
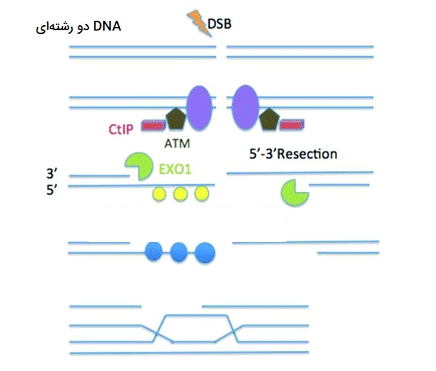
فراتر از نقش آن در میوز، نوترکیبی برای سلولهای سوماتیک در یوکاریوتها مهم است زیرا میتوان از آن برای کمک به ترمیم DNA شکسته استفاده کرد، حتی اگر شکسته شدن، هر دو رشته مارپیچ دوگانه را درگیر کند. این شکستها به عنوان شکستهای دو رشتهای یا DSB شناخته میشوند. هنگامی که DSB ها اتفاق میافتند، یک کروموزوم همولوگ میتواند به عنوان الگویی برای سنتز هر بخشی از ماده ژنتیکی که در نتیجه شکستن از بین رفته است، استفاده شود. پس از سنتز، این DNA جدید میتواند در رشته DNA شکسته قرار گیرد و در نتیجه آن را ترمیم کند. در واقع، این نوعی نوترکیبی است، زیرا ناحیه شکسته شده با مواد جدید از یک کروموزوم همولوگ جایگزین میشود. از نوترکیبی میتوان به روشی مشابه برای ترمیم شکستهای كوچکتر وتک رشتهای استفاده كرد.
به طور کلی، هر زمان که کروموزومهای همولوگ جفت شوند، نوترکیبی ممکن است اتفاق بیفتد، چه در طول میوز به راحتی پشت سر هم شناور باشند و چه در صفحه متافاز صف کشیده شوند. با این حال، نوترکیبی فقط به یوکاریوتها محدود نمیشود. نوع خاصی از نوترکیبی به نام هم یوغی یا ترانسداکسیون در بسیاری از پروکاریوتها وجود دارد و به ویژه در باکتری E. coli به خوبی مورد مطالعه و توصیف قرار گرفته است. در طی هم یوغی، مواد ژنتیکی حاصل از یک باکتری به باکتری دیگر منتقل میشوند و سپس در سلول گیرنده ترکیب میشوند. نوترکیبی همچنین در ترمیم DNA در ارگانیسمهای پروکاریوتی نقش مهمی دارد، همانطور که در موجودات یوکاریوتی انجام میشود.
نوترکیبی در طبیعت
مهمترین ویژگی موجودات زنده سازگاری در محیط و حفظ توالی DNA آنها در سلولها به نسلهای بعدی همراه با تغییرات بسیار اندک است. در طولانی مدت زنده ماندن موجودات به تغییرات ژنتیکی بستگی دارد، یک ویژگی اصلی نوترکیبی این است که از طریق آن ارگانیسم میتواند با محیطی سازگار شود و با گذشت زمان تغییر کند. این تنوع در بین ارگانیسمها از طریق توانایی DNA برای انجام بازآرایی ژنتیکی و در نتیجه تغییر کمی در ترکیب ژن رخ میدهد. تنظیم مجدد DNA از طریق نوترکیبی ژنتیکی اتفاق میافتد. موجودات جدید علاوه بر ساختار ژنتیکی، تغییر در فنوتیپ (بروز ظاهری) را نیز نشان میدهند. بیشتر یوکاریوتها یک چرخه کامل زندگی جنسی از جمله میوز را نشان میدهند، رویداد مهمی که با نوترکیبی، ترکیبات آللی جدید ایجاد میکند. در ادامه به انواع حالات نوترکیبی در طبیعت خواهیم پرداخت.
مدل هالیدی برای نوترکیبی عمومی
نوترکیبی عمومی فقط بین رشتههای مکمل دو مولکول DNA همولوگ اتفاق میافتد. اسمیت در 1989، نوترکیبی همولوگ را در پروکاریوتها بررسی کرد. نوترکیبی عمومی در E. coli توسط فعل و انفعالات جفت سازی بازها بین رشتههای مکمل دو مولکول DNA همولوگ هدایت میشود. مارپیچ دوتایی دو مولکول DNA میشکند و دو انتهای شکسته شده به رشتههای مخالف خود میپیوندند تا دوباره به هم پیوسته و مارپیچ دوتایی جدیدی ایجاد کنند. سایت تبادل میتواند در هر مکانی از توالی نوکلئوتیدهای همولوگ رخ دهد که در آن یک رشته از یک مولکول DNA با رشته دوم جفت شود و هترو دابلکس درست بین دو مارپیچ دوتایی تولید میکند. در هترودابلکس هیچ توالی نوکلئوتیدی در محل تبادل به دلیل شکستن و پیوستن تغییر نمیکند.
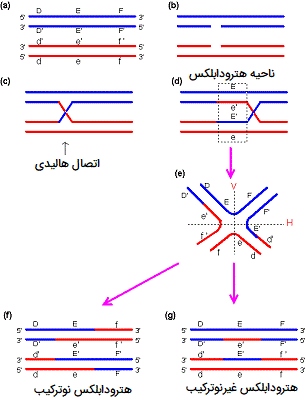
نوترکیبی عمومی به عنوان نوترکیبی همولوگ نیز شناخته میشود زیرا به کروموزومهای همولوگ نیاز دارد. در باکتریها و ویروسها نوترکیبی عمومی توسط محصولات ژنهای rec مانند پروتئین RecA انجام میشود. هالیدی در 1974 مدلی را برای نشان دادن ترکیب عمومی ارائه داد. طبق این مدل، نوترکیبی در پنج مرحله مانند شکستگی رشته، جفت شدن رشته، هجوم و جذب رشته، تشکیل کیاسما (کراسینگ اور)، شکستگی و پیوند مجدد و «ترمیم عدم تطابق» (Mismatch Repair) رخ میدهد. مراحل نوترکیبی عمومی را در ادامه توضیح داده ایم.
مرحله اول شکستگی رشته
نوترکیبی عمومی از طریق کراسینگ اور در جفت شدن بین تک رشتههای مکمل دابلکس DNA اتفاق میافتد. دو منطقه همولوگ مارپیچ دوتایی DNA تحت یک واکنش تبادل قرار میگیرند. منطقه همولوگ شامل یک توالی طولانی از جفت شدن بازهای مکمل بین یک رشته از یک یا دو مارپیچ دوتایی اصلی و یک رشته مکمل از دیگری است. با این حال، مشخص نیست که چگونه نواحی همولوگ DNA یکدیگر را تشخیص میدهد. ژنها و پروتئینهای مختلف بسیاری مانند پروتئینهای RecBCD و ژنهای recBCD یا recJ در در نوترکیبی اِکلای نقش دارند.
این پروتئین از یک انتهای مارپیچ دوتایی وارد DNA میشود و در امتداد DNA با مارپیچ دوتایی حرکت میکند و سرعت آن حدود 300 نوکلئوتید در ثانیه است. این یک حلقه از DNA دورشتهای (ssDNA) در طول DNA در حال حرکت ایجاد کرده و از انرژی حاصل از هیدرولیز مولکولهای ATP استفاده میکند. یک سایت شناسایی خاص توالی هشت نوکلئوتید پراکنده در سراسر کروموزوم E. coli در حلقه در حال حرکت DNA تشکیل شده توسط پروتئین RecBCD دیده میشود.
مرحله دوم جفت شدن بازها
پروتئینهای RecBCD به عنوان DNA هلیکاز عمل میکنند زیرا این آنزیمها هیدرولیزکنندههای ATP هستند و در امتداد مارپیچ DNA حرکت میکنند. بنابراین، پروتئینهای RecBCD منجر به تشکیل گودی تک رشتهای در محل شناسایی میشوند که از مارپیچ جدا و جابجا شده است. این تعامل، جفت سازی بازها بین دو توالی مکمل مارپیچ دوگانه DNA را آغاز میکند.
مرحله سوم هجوم و جذب رشته
گودی تک رشتهای تولید شده از یک مارپیچ دوتایی DNA به مارپیچ دوتایی دیگر حمله میکند. در E. coli ژن recA پروتئین RecA تولید میکند که برای نوترکیبی بین کروموزومها مانند پروتئینهای اتصالی تک رشته (SSB) مهم است. پروتئین RecA محکم به DNA تک رشته متصل میشود و یک رشته نوکلئو پروتئین ایجاد میکند. پروتئین RecA باعث تجدید رشد سریع دی ان ای دو رشتهای ssDNA مکمل از طریق فرآیند هیدرولیز ATP میشود. پروتئین RecA دارای چندین محل اتصال است بنابراین، میتواند یک ssDNA و متعاقباً یک dsDNA را متصل کند. پروتئین RecA ابتدا به ssDNA متصل میشود، سپس به دنبال همسانی بین رشته دهنده و مولکول گیرنده میگردد.
به دلیل وجود این سایتها، پروتئین RecA یک واکنش چند مرحلهای (که سیناپسیس نامیده میشود) بین ناحیه همولوگ ssDNA و مارپیچ مضاعف DNA را کاتالیز میکند. پروتئین SSB باکتری E. coli، به پروتئین Rec کمک میکند تا این واکنشها را انجام دهد. هنگامی که یک منطقه از همسانی توسط جفت شدن بازهای اولیه بین توالیهای مکمل شناسایی میشود، مرحله مهم در سیناپسیس اتفاق میافتد. آزمایشات In Vivo نشان داده است که چندین نوع کمپلکس بین یک ssDNA پوشیده شده با پروتئین RecA و یک مارپیچ dsDNA ایجاد میشود. این مجموعه ناپایدار است و یک هترودابلکس DNA به همراه یک ssDNA جابجا شده را از مارپیچ اصلی بیرون میزند.
مرحله چهارم مهاجرت شاخه
مرحله بعدی همانند ادغام رشتهها و بستن شکافها است. رشته دهنده به تدریج رشته گیرنده را جابجا میکند که این فرایند مهاجرت شاخه نامیده میشود. پس از تشکیل سیناپسیس، منطقه هترودابلکس (از طریق مهاجرت شاخههای هدایت پروتئین که توسط پروتئین RecA کاتالیز میشود) بزرگ میشود. مهاجرت شاخهای هدایت شده توسط پروتئین RecA به دلیل افزودن پروتئین RecA بیشتر به یک انتهای پروتئین RecA روی DNA دو رشتهای ssDNA و با سرعت یکنواختی در یک جهت پیش میرود. مهاجرت شاخهها میتواند در هر نقطهای که دو رشته منفرد با توالی سعی در جفت شدن با همان رشته مکمل داشته باشند، انجام شود.
یک منطقه جفت نشده از تک رشته دیگر به حرکت شاخه بدون تغییر تعداد کل جفت بازهای DNA منجر میشود. هلیکازهای DNA ویژه که مهاجرت شاخهای هدایت شده توسط پروتئین را کاتالیز میکنند، در نوترکیبی نقش دارند. در مقابل، مهاجرت خود به خود شاخه تقریباً با همان سرعت در هر دو جهت پیش میرود، بنابراین، در مسافت طولانی کمی پیشرفت میکند.
مرحله پنجم تشکیل کراسینگ اور و کیاسما
تبادل یک رشته واحد بین دو مارپیچ دوتایی گام متفاوتی در یک نوترکیبی عمومی است. تصور میشود که پس از مبادله رشتهای متقابل اولیه، مبادلات رشتهای بیشتر بین دو مارپیچ کاملاً مخالف با سرعت بیشتری پیش رود. یک نوکلئاز DNA را قطع میکند و در بعضی نقاط حلقه D را تخریب میکند. در این مرحله موجودات مختلف احتمالاً مسیرهای مختلفی را دنبال میکنند. با این حال، در بیشتر موارد یک ساختار مهم به نام تبادل متقاطع (که تقاطع هالیدی یا ساختار chi یا کیاسما نامیده میشود) توسط دو مارپیچ DNA شرکت کننده تشکیل میشود.
شکل chi دو مارپیچ همولوگ که در ابتدا با مبادله متقابل دو تا از چهار رشته که یک رشته از هر یک از مارپیچها منشا میگیرد، جفت شده و با هم نگه داشته میشوند. فرم چی دارای دو ویژگی مهم است، اولی این است که محل مبادله میتواند به سرعت و در امتداد مارپیچها با مهاجرت دو شاخه مهاجرت کند و دوم اینکه شامل دو جفت رشته، یک جفت رشته عبورکننده و یک جفت رشته غیر عبورکننده است.
مرحله ششم شکستن و باز پیوست
ساختار chi میتواند چندین چرخش را ایزومریزه کند. این منجر به تغییر دو رشته اصلی غیر عبورکننده به داخل رشتههای عبورکننده و رشتههای عبورکننده به رشتههای غیر عبورکننده میشود. به منظور بازسازی دو مارپیچ DNA جداگانه، شکستن و پیوند مجدد در دو رشته عبورکننده لازم است. اگر شکستن و پیوستن مجدد قبل از ایزومریزاسیون رخ دهد، دو رشته عبور نمیکنند. بنابراین، ایزومریزاسیون برای شکستن و پیوستن دو مارپیچ دوتایی همولوگ حاصل از نوترکیبیِ ژنتیکی عمومی، لازم است. شکست و بازپیوست در سطح عمودی یا افقی رخ میدهد. اگر شکستگی به صورت افقی رخ دهد، ترکیبات حاوی ژنوتیپ جفت همولوگ (ABlab) با کمی تغییر در توالی اصلی در منطقه داخلی همراه است. اما، اگر شکستگی به صورت عمودی رخ دهد، ترکیبات ناشی از نوترکیبی حاوی Ab / aB هستند. پروتئینهای RurC و RecG به ترتیب بیان شده از ژنهای ruvC و recG اندونوکلئازهای جایگزین خاص برای ساختار هالیدی هستند.
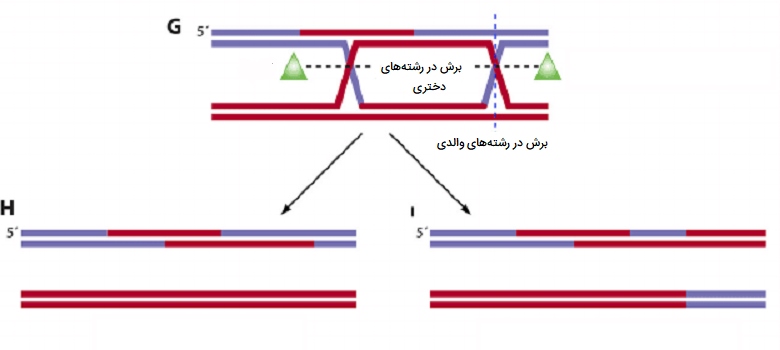
مرحله هفتم ترمیم نواحی عدم تطابق
این یک سیستم تعمیر است که جفت بازهای ناسازگار مناطق جفت نشده را پس از نوترکیبی اصلاح میکند. این سیستم عملکرد ناسازگار DNA پلیمراز را تشخیص میدهد. این مکانیزم شامل برداشتن یکی دیگر از بازهای ناسازگار همراه با حدود 3000 نوکلئوتید است. این RecFJO در ترمیم عدم تطابق کوتاه یا در مرحله اولیه یا در پایان نوترکیبی نقش دارد. دو پروتئین MutS و MutL در باکتریها و یوکاریوتها وجود دارند. پروتئین MutS به جفت باز ناسازگار متصل میشود، در حالی که MutL DNA را برای یافتن شکافها اسکن میکند. هنگامی که یک شکاف تشکیل میشود، MutL تخریب رشته شکافدار را از طریق عدم تطابق آغاز میکند، از آنجا که شکافها تا حد زیادی محدود به رشتههای تازه تکرار شده در یوکاریوتها هستند، خطاهای همانندسازی به طور انتخابی حذف میشوند. در باکتریها این مکانیسم یکسان است با این تفاوت که پروتئین اضافی MutH توالیهای غیرمتیله GATC را میشکند و فرایند را آغاز میکند.
در مخمرها و باکتریها ثابت شده است که همان سیستم ترمیم عدم تطابق که خطاهای تکثیر را حذف میکند، همچنین وقایع نوترکیبی ژنتیکی بین توالیهای DNA کاملاً منطبق را قطع میکند. بررسی شده است که ژنهای همولوگ در دو باکتری نزدیک به هم مانند E. coli و S.typhimurium حتی پس از داشتن 80 درصد توالی نوکلئوتیدی یکسان به طور کلی ترکیب نخواهند شد. با این حال، هنگامی که سیستم تعمیر عدم تطابق با جهش غیرفعال میشود، فرکانس چنین نوترکیبی بین گونهها 100 برابر افزایش مییابد. این مکانیسم ژنوم باکتری را از تغییرات توالی که میتواند در اثر نوترکیبی با مولکولهای DNA خارجی وارد سلول شود، محافظت میکند.
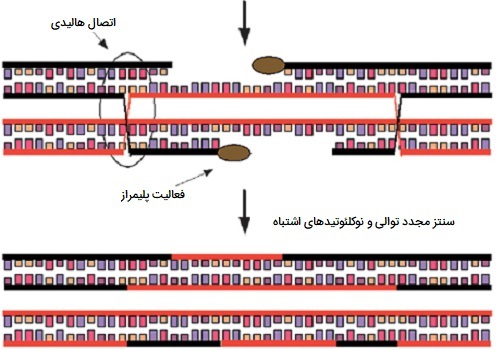
ادغام قطعات DNA باکتریایی
باکتریها به معنای واقعی تولید مثل جنسی ندارند، اما بسیاری یا اکثر آنها قادر به انتقال قطعات DNA از سلول به سلول توسط یکی از سه مکانیزم زیر هستند. (1) قطعاتی از ژنوم باکتری میتوانند به DNA پلاسمید متصل شده و از طریق ترکیب سلول با همان مکانیزمی که انتقال DNA پلاسمیدهای قابل انتقال را تضمین میکند، منتقل شوند. (2) قطعات ژنومی را میتوان از سلول به سلول دیگر در پوشش عفونی ویروسهای باکتریایی (فاژها) منتقل کرد، این فرآیند «انتقال» (Transduction) نامیده میشود. (3) بسیاری از باکتریها توانایی جذب قطعات DNA از محلول را دارند و بنابراین ممکن است ژنهای سلولهای تخریب شده را جذب کنند.
قطعات DNA به دست آمده توسط هر یک از این روشها میتوانند در DNA ژنوم جایگزین توالیهای همولوگ قبلی شوند. اگر DNA ورودی با سلول گیرنده همخوانی نداشته باشد، معمولاً نمیتواند یکپارچه شود و به دلیل عدم توانایی تکثیر به صورت خودکار از بین میرود. ادغام همولوگ در باکتریها، از نظر ماهیت غیر متقابل و شاید هم از نظر مکانیسم، با تبدیل ژنی در ارگانیسمهای یوکاریوتی مشابه است.
نوترکیبی اختصاصی سایت
باکتریوفاژها، پلاسمیدها، باکتریها و یوکاریوتهای تک سلولی نمونههای زیادی از تمایز را از طریق نوترکیبی کنترل شده و «اختصاصی جایگاه» (Site-specific) قطعات DNA ارائه میدهند. بی مهرگان، یک سری حذف کنترل شده منجر به ایجاد تنوع زیادی از توالیهای ژنی کد کننده آنتی بادیها و گیرندههای سلول T دارند که برای دفاع ایمنی در برابر عوامل بیماریزا لازم میشود. همه این فرایندها به تعامل و نوترکیبی بین توالیهای خاص DNA بستگی دارد، به طور کلی اما نه همیشه این فرایند با برخی از توالیهای شبیه، توسط آنزیمهای «ریکامبیناز» (recombinase) اختصاصی جایگاه کاتالیز میشود. مکانیسمهای مولکولی ممکن است برخی از شباهتها را با نوترکیبی میوز کلی داشته باشند، با این تفاوت که دومی به هیچ توالی خاصی بستگی ندارد، فقط به شباهت (همسانی) توالی ترکیب شده بستگی دارد.
نوترکیبی خاص سایت موقعیت نسبی توالیهای نوکلئوتیدی را در کروموزوم تغییر میدهد. واکنش جفت شدن بازها به پروتئین تشخیص دهنده دو توالی DNA بستگی دارد و در آن توالی همولوگ بسیار طولانی مورد نیاز نیست. برخلاف نوترکیبی عمومی، نوترکیبی خاص سایت توسط آنزیم نوترکیبی هدایت میشود که توالیهای نوکلئوتیدی خاصی را که در یکی از دو مولکول DNA وجود دارد، تشخیص میدهد. در این روش جفت شدن بازها درگیر نیست بلکه در صورتی که در هترودابلکس اتفاق بیفتد فقط به اندازه چند جفت باز طول دارد. این روش اولین بار در فاژ λ کشف شد که توسط آن ژنوم فاژ به داخل و خارج از کروموزوم E. coli حرکت میکند. فاژ نفوذی کد کننده یک آنزیم بوده که لامبدا اینتگراز است و روند نوترکیبی را کاتالیز میکند. لامبدا اینتگراز به یک محل اتصال خاص از توالی DNA در هر کروموزوم متصل میشود.
برشهایی ایجاد میکند و توالیهای DNA همولوگ کوتاه را میشکند. اینتگراز رشتههای همراه را تغییر داده و دوباره به آنها متصل میشود و یک اتصال هترو دابلکس به طول 7 جفت باز ایجاد میکند. اینتگراز در اتصال مجدد رشتههایی که قبلاً شکسته شده اند شبیه توپوایزومراز DNA است. ۲ نوع نوترکیبی اختصاصی جایگاه وجود دارد که شامل موارد زیر هستند:
- نوترکیبی اختصاصی جایگاه حفاظت شده. تولید یک هترودابلکس بسیار کوتاه با نیاز به برخی از توالیهای DNA که در دو مولکول DNA یکسان است، به عنوان «نوترکیبی اختصاصی جایگاه حفاظت شده» (Conservative site-specific recombination) شناخته میشود.
- نوترکیبی اختصاصی جایگاه فرا موضعی. نوع دیگری از سیستم نوترکیبی وجود دارد که به عنوان «نوترکیبی اختصاصی جایگاه فرا موضعی» (Trans-positional site-specific recombination) (TSS) شناخته میشود. نوترکیبی TSS هترودابلکس تولید نمیکند و نیازی به توالی خاصی در بزرگترین DNA نیست. چندین توالی DNA متحرک وجود دارد که شامل بسیاری از ویروسها و عناصر قابل انتقال است که ادغام شدن را رمزگذاری میکنند. این امر باعث میشود توالی DNA ویروسی در کروموزوم هدف وارد شود و دو شکاف کوتاه رشتهای در هر طرف از مولکول DNA ترکیبی باقی بماند. این شکافها بعداً با فرآیند ترمیم DNA (به عنوان مثال توسط DNA پلیمراز) پر میشوند تا روند نوترکیبی تکمیل شود. این مکانیسم منجر به تشکیل تکرارهای کوتاه حدود 3 تا 12 نوکلئوتیدی از توالی DNA هدف مجاور میشود. شکل گیری تکرارهای کوتاه از مشخصههای یک نوترکیبی TSS است.
نوترکیبی غیر همولوگ
از قوانین اصلی ژنتیک این است که دو والد مقادیر ژنی مساوی باهم را به فرزندان انتقال دهند. این بدان معناست که فرزندان نیمی از مجموعه کامل ژنها را از جنس نر و نیمی را از ماده به ارث میبرند. یک سلول دیپلوئید تحت میوز چهار سلول هاپلوئید را تولید میکند. بنابراین، تعداد نصف ژنهای آن مشترک با نر و نصف دیگر آن مشترک با ماده خواهد بود. در موجودات پیشرفتهتر مانند انسان، تجزیه و تحلیل این ژنها با استفاده از یک سلول امکان پذیر نیست. با این حال، در ارگانیسمهای خاصی مانند قارچها میتوان چهار سلول دختری تولید شده از یک سلول از طریق میوز را بازیابی و تجزیه و تحلیل کرد.
گاهی اوقات، سه نسخه از آلل مادر و تنها یک نسخه از آلل پدر توسط میوز تشکیل میشود. این نشان میدهد که یکی از دو نسخه از آللهای والدین به آلل مادر تغییر یافته است. این تغییر ژن از نوع غیر متقابل است و «تبدیل ژنی» (Gene Conversion) نامیده میشود. تصور میشود که تبدیل ژنی یک رویداد مهم در تکامل ژنهای خاص است و در نتیجه مکانیسم نوترکیبی عمومی و ترمیم DNA رخ میدهد. این فرآیند از زمانی شروع میشود که یک شکاف در یکی از رشتههای DNA ساخته میشود. از این مرحله DNA پلیمراز یک کپی اضافی از یک رشته را سنتز میکند و نسخه اصلی را به صورت یک رشته جابجا میکند. این رشته واحد مانند دابلکس پایین مولکول DNA با منطقه همولوگ جفت میشود. رشته جفت نشده کوتاه تولید شده در مرحله قبلی با تکمیل انتقال توالی نوکلئوتید تخریب میشود. نتایج وقتی (در چرخه بعدی) مشاهده میشود که تکثیر DNA دو رشته غیر همسان را از هم جدا کرده است.
نوترکیبی همولوگ چیست؟
نوترکیبی همولوگ نوعی نوترکیبی است که در آن اطلاعات ژنتیکی بین دو مولکول مشابه یا یکسان از اسیدهای نوکلئیک دو رشته یا تک رشته مبادله میشود. به طور گستردهای توسط سلولها برای ترمیم شکستهای مضر که در هر دو رشته DNA معروف به شکست دو رشته (DSB) ایجاد میشود و در فرآیندی به نام ترمیم ترکیبی همولوگ (HRR) استفاده میشود. نوترکیبی همولوگ همچنین ترکیبات جدیدی از توالی DNA را در طی میوز تولید میکند، فرایندی که یوکاریوتها سلولهای گامت را مانند سلولهای اسپرم و تخمک در حیوانات ایجاد میکنند.
این ترکیبات جدید DNA بیانگر تنوع ژنتیکی در فرزندان است، که به نوبه خود جمعیت را قادر میسازد تا در طول تکامل سازگار شوند. از نوترکیبی همولوگ در انتقال افقی ژن برای تبادل مواد ژنتیکی بین سویهها و گونههای مختلف باکتریها و ویروسها نیز استفاده میشود. اگرچه نوترکیبی همولوگ به طور گستردهای در بین ارگانیسمها و انواع سلولهای مختلف متفاوت است، اما برای DNA دو رشتهای (dsDNA) اکثر اشکال همان مراحل اساسی را شامل میشوند.
نوترکیبی در میتوز چگونه است؟
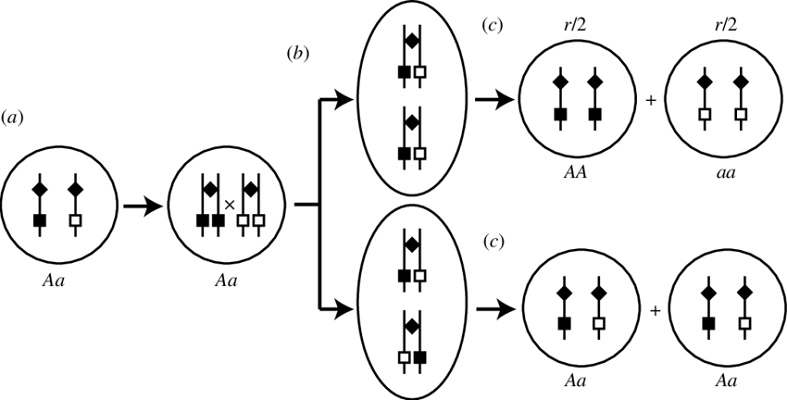
کراسینگ اور بین جفتهای کروموزوم همولوگ نیز میتواند در طول پروفاز تقسیم هستهای میتوزی رخ دهد. فرکانس آن بسیار پایینتر از میوز است، احتمالاً به این دلیل که سلول میتوزی دستگاه جفت سازی را برای جفت شدن کارآمد کروموزومهای هومولوگ تشکیل نمیدهد. کراسینگ اور میتوزی در در «مگس سرکه» (Drosophila melanogaster) در قارچهای رشتهای مانند «آسپرژیلوس نیدولانس» (Aspergillus nidulans) و مخمر ساکارومیسز مطالعه شده است. در این گونهها از طریق تشکیل کلونهای هموزیگوت سلول در یک دیپلوئید هتروزیگوت ابتدایی تشخیص داده میشود. هر زمان که تلاقی بین کروماتیدها در فاصله بین نشانگر و سانترومر رخ دهد، 50 درصد احتمال هموزیگوسیتی در سلولهای دختر در جایگاه اتصال کروموزومها به دوک میتوزی وجود دارد. فرکانس کراسینگ اور میتوزی توسط اشعه بسیار افزایش مییابد.
نوترکیبی در باکتری ها و پروکاریوت ها
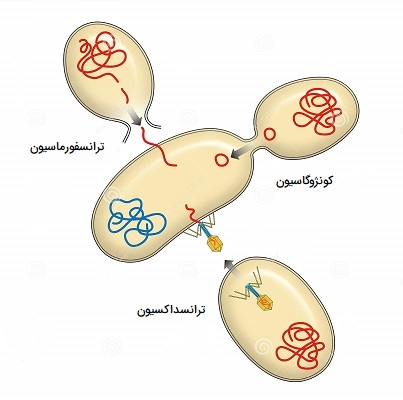
نوترکیبی باکتری نوعی ترکیب ژنتیکی در باکتریها است که با انتقال DNA از یک ارگانیسم به نام اهدا کننده به ارگانیسم دیگر به عنوان گیرنده مشخص میشود. این فرایند به سه روش اصلی اتفاق میافتد شامل «تبدیل» (Transformation) یا جذب DNA برونزا از محیط اطراف. «انتقال» (Transduction) یا انتقال DNA با واسطه ویروس بین باکتریها. «هم یوغی» (Conjugation) یا انتقال DNA از یک باکتری به باکتری دیگر از طریق تماس سلول به سلول. نتیجه نهایی این فرایند تولید ترکیبات جدید ژنتیکی در افرادی که نه تنها ژنهایی را که از سلولهای اصلی خود به ارث بردهاند، دارند بلکه ژنهایی را نیز که از طریق نوترکیبی به ژنوم آنها وارد میشود، حمل میکنند. نوترکیبی در باکتریها بطور معمول توسط یک نوع آنزیم RecA کاتالیز میشود. این آنزیمهای ریکامبیناز باعث ترمیم آسیبهای DNA توسط نوترکیبی همولوگ میشوند.
توانایی ترانسفورماسیون طبیعی حداقل در 67 گونه باکتری وجود دارد، ترانسفورماسیون طبیعی در بین گونههای باکتریایی بیماریزا رایج است. در برخی موارد، توانایی ترمیم DNA فراهم شده توسط نوترکیبی در طی تحول، بقای پاتوژن باکتریایی عفونتزا را تسهیل میکند. ترانسفورماسیون باکتریایی توسط محصولات ژن باکتریایی متقابل متعددی انجام میشود. تکامل در باکتریها قبلاً در نتیجه جهش یا رانش ژنتیکی مشاهده میشد. امروزه تبادل ژنتیکی یا انتقال ژن به عنوان یک نیروی محرکه اصلی در تکامل پروکاریوتها تلقی میشود. این نیروی محرکه به طور گستردهای در موجوداتی مانند E. coli مورد مطالعه قرار گرفته است.
پروکاریوتها علاوه بر اتکا به جهشهای نسبتاً نادر، روشهای دیگری برای تکامل ژنوم خود دارند. از طریق نوترکیبی ژنتیکی، سلولهای پروکاریوتی میتوانند DNA را با سلولهای جداگانه دیگری تقسیم کنندکه لزوما متعلق به همان گونه نیستند. این میتواند به گسترش ژنهای مفیدی کمک کند که ارگانیسمهای سازگارتر تولید میکنند. به عنوان مثال، ظاهر ژنی که مقاومت آنتی بیوتیکی را ایجاد میکند، ممکن است یک نوع ویروس با میزبان باکتری ایجاد کند. سلولها ممکن است از طریق نوترکیبی ژنتیکی ژن مفید را گسترش دهند و به اطمینان از زنده ماندن گونه کمک کنند. در ادامه به بررسی انواع فرایندهای نوترکیبی در پروکاریوتها میپردازیم.
ترانسداکسیون
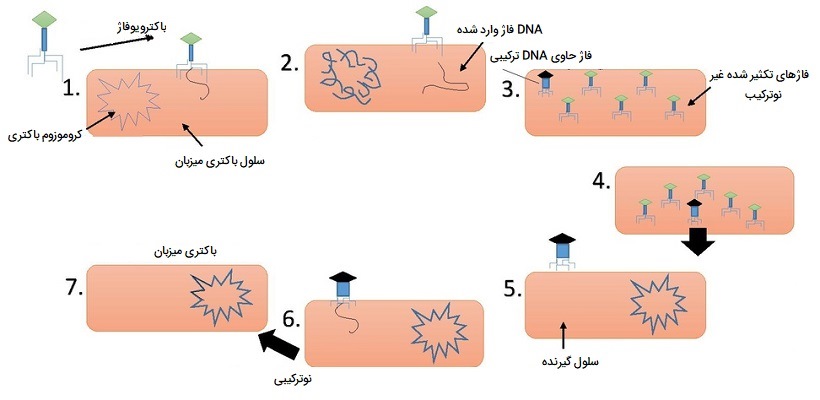
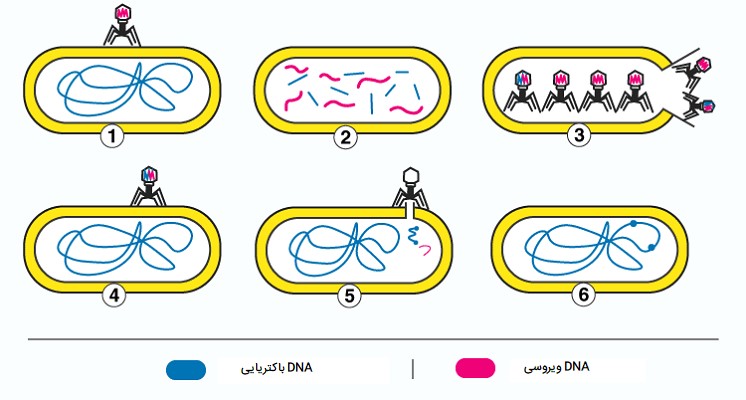
«ترانسداکشن یا ترانسداکسیون» (Transduction)، انتقال DNA از یک باکتری به باکتری دیگر از طریق عملکرد ویروسها است. وقتی ویروس یک باکتری را آلوده میکند، مواد ژنتیکی خود را به قربانی تزریق میکند و تجهیزات داخل سلول باکتری را برای سنتز DNA ، RNA و پروتئینها با سرعت زیاد تسخیر میکند. گاهی اوقات، ماده ژنتیکی ویروسی با DNA میزبان میپیوندد. سپس، DNA ویروسی خود را از کروموزوم باکتری خارج میکند، که در این فرایند، ژنهای باکتری ممکن است در DNA ویروسی تازه آزاد شده گنجانده شود. ویروس باعث میشود که باکتری میزبان نسخههای زیادی از ژنوم ویروس را به همراه ژنهای خود تکثیر کند. سپس ویروس باعث پاره شدن سلول شده و ذرات ویروسی جدید آزاد میشود که هر کدام چرخه را تکرار میکنند. به این ترتیب، ژنهای یک میزبان با ژنهای میزبان دیگر، شاید از گونه دیگری ترکیب شوند.
ترانسداکشن میتواند به سرعت ترکیب ژنتیکی جمعیت باکتریها را تغییر دهد حتی اگر آنها به صورت غیرجنسی تولید مثل کنند. این نوع انتقال ژن میتواند تأثیرات عمیقی روی باکتریها و زیستگاههای آنها بگذارد. به عنوان مثال، بسیاری از گونههای باکتری شناخته شده اند که باعث آلوده شدن انسان و موجودات دیگر و ایجاد بیماری میشوند. آنتی بیوتیکها درمانهایی بوده که معمولاً برای مقابله با عفونتهای باکتریایی بالقوه خطرناک یا حتی کشنده موثر هستند. ریشه کن کردن برخی سویههای باکتریایی دشوار است و به آنتی بیوتیکهای بسیار خاصی نیاز دارند. بنابراین هنگامی که باکتریها به آنتی بیوتیک مقاومت پیدا میکنند، بسیار نگران کننده است زیرا استفاده نکردن از آنتی بیوتیک، میتواند منجر به عفونتهایی شود که بدون کنترل در بدن پخش میشوند.
ترانسداکشن در مقاومت به آنتی بیوتیک نقش دارد. برخی از سلولهای باکتریایی مقاومت طبیعی در برابر آنتی بیوتیکها بر روی غشای سلول خود دارند که باعث میشود اتصال آنتی بیوتیک در آنجا دشوار باشد. البته این پدیده میتواند به دلیل یک جهش تصادفی باشد و بر اثربخشی کلی آنتی بیوتیک تأثیر نگذارد. با این حال، اگر یک باکتریوفاژ یک سلول باکتریایی مقاوم در برابر آنتی بیوتیک را آلوده کند و سپس ژن جهش یافته را با انتقال به سلولهای دیگر باکتریایی منتقل کند، سلولهای بیشتری در برابر آنتی بیوتیک مقاوم خواهند بود و همانطور که با شکافت دوتایی تولید مثل میکنند، تعداد سلولهای باکتریایی مقاوم در برابر آنتی بیوتیک میتواند به طور تصاعدی افزایش یابد.
ترانسفورماسیون
گونههای خاصی از باکتریها میتوانند بخشهای DNA را که به عنوان پلاسمید شناخته میشوند یا قطعات ژنی خارجی را، از محیط اطراف خود بلعیده و این قطعات جدید را در کروموزومهای خود قرار دهند. ابتدا باکتری باید وارد حالت خاصی شود، به نام «مستعد شدن» (Competence)، که امکان «ترانسفورماسیون یا ترانسفورمیشن» (Transformation) را فراهم کند. برای دستیابی به این صلاحیت، باکتری باید تعدادی از ژنهای بیان کننده پروتئینهای مورد نیاز را فعال کند. باکتریها معمولاً ترانسفورماسیون را در یک گونه انجام میدهند. با استفاده از این امکانات در باکتریها، دانشمندان با قرار دادن DNA در محیط رشد، DNA مورد نظر خود را وارد سلولهای پروکاریوتی میکنند و به این ترتیب سویههایی با ویژگیهای دلخواه ایجاد کنند.
کونژوگاسیون
«کونژوگاسیون یا کانجوگیشن» (Conjugation) معادل آمیزش در باکتریها است که شامل تماس فیزیکی بین دو سلول بوده و از طریق یک سازه پل مانند به نام پیلوس صورت میگیرد. سلولهای دهنده باید دارای یک بخش کوچک DNA به نام F - پلاسمید باشند که سلول گیرنده فاقد آن است. سلول دهنده یک رشته DNA از F - پلاسمید را فراهم و آن را به گیرنده منتقل میکند. سپس آنزیم DNA پلیمراز گیرنده یک رشته مکمل را برای تولید ساختار DNA دو رشتهای معمول تولید کرده و گیرنده DNA دهنده را با ژنوم خود ترکیب میکند.
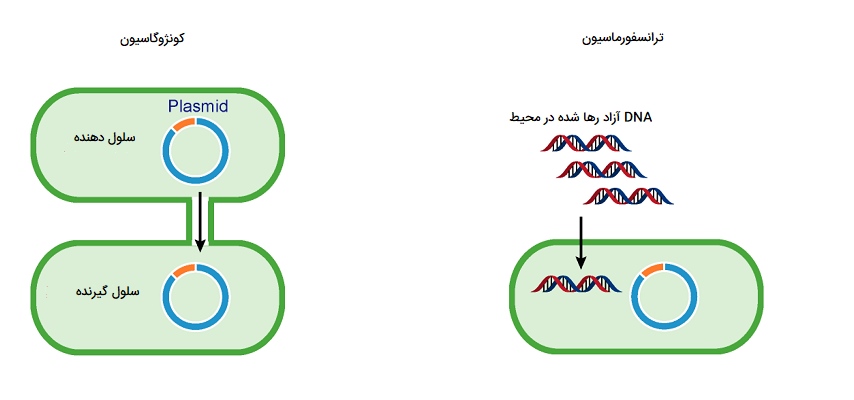
مکانیسم هایی برای شکست دو رشته ای
همانطور که بیان شد، باکتریها به صورت غیر جنسی تولید مثل میکنند، جایی که سلولهای دختری از والدین کلون میشوند. این نوع تولید مثل منجر به جهشهای تصادفی میشود که در طی همانند سازی DNA رخ میدهند و به طور بالقوه به تکامل باکتریها کمک میکنند. در مقابل، باکتریها نیز در فرآیندی به نام نوترکیبی همولوگ، که برای اولین بار با مشاهده ژنهای موزاییکی در مکانهای مقاومت در برابر آنتی بیوتیک کشف شد، ژن جدید وارد ژنوم خود میکنند. کشف نوترکیبی همولوگ بر درک تکامل باکتری تأثیر داشته است.
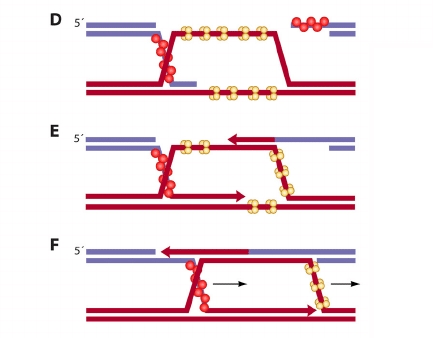
مسیر RecBCD در نوترکیبی همولوگ شکافهای دو رشته DNA را که در باکتریها تجزیه شده است را ترمیم میکند. جفت بازها در محل اتصال هالیدی (محل اتصال هالیدی یک ساختار اسید نوکلئیک منشعب است که شامل چهار بازوی دو رشتهای است که بهم متصل شده اند) به رشتههای DNA متصل میشوند. در مرحله دوم نوترکیبی باکتریها، مهاجرت شاخهای (فرآیندی که طی آن جفت بازها و رد و بدل شدن آنها در رشتههای DNA همولوگ به طور متوالی در محل اتصال هالیدی صورت گرفته و حرکت شاخه به سمت بالا یا پایین توالی DNA رخ میدهد) رخ میدهد و منجر به تشکیل دو دوبلکس DNA میشود.
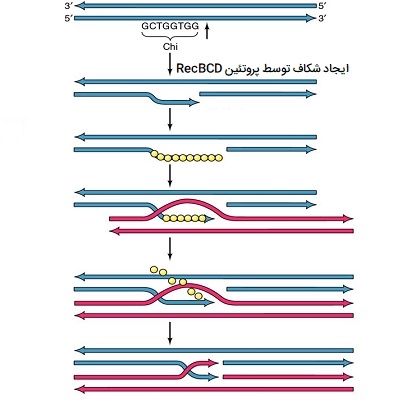
مسیر RecBCD با باز کردن زیپ دوبلکس DNA تحت فعالیت هلیکاز قرار میگیرد و وقتی توالی نوکلئوتید به ’5GCTGGTGG3 برسد متوقف میشود. این توالی نوکلئوتیدی به عنوان جایگاه Chi شناخته میشود. آنزیمهای RecBCD پس از رسیدن توالی نوکلئوتید به محل Chi تغییر خواهند کرد. مسیر RecF تخریب رشتههای DNA را ترمیم میکند.

نوترکیبی در ویروس ها
نوترکیبی یک مکانیسم فراگیر است که باعث ایجاد تنوع در بیشتر ویروسها میشود. این فرایند به طور طبیعی در ویروسها رخ میدهد که به طور مستقل در همان مولکول بوجود میآیند و فرصتهای جدیدی را برای ویروسها فراهم میکند تا از فشارهای انتخابی محیط عبور کرده و با محیطها و میزبانهای جدید سازگار شوند. ویروسها طیف گستردهای از ساختارهای ژنومی را در بر میگیرند.
اکثر ویروسهای طبقه بندی شده دارای ژنوم RNA هستند، اما بسیاری از آنها دارای ژنوم DNA هستند و حتی برخی ممکن است در مراحل مختلف چرخه زندگی خود دارای DNA و RNA باشند. آنها می توانند تک رشتهای (ss) یا دو رشتهای (ds) باشند و برخی از خانوادههای ویروس حاوی ژنوم دو رشتهای با مناطق تک رشتهای هستند.
ویروسها توسط مکانیسمهای مختلف، از جمله جهش نقطهای (منبع نهایی تغییر ژنتیکی) و نوترکیبی، دچار تغییر ژنتیکی میشوند. به طور کلی، ویروسهای RNA دار احتمالاً به دلیل نرخ جهش بالاتر ژنوم کوچکتری نسبت به ویروسهای DNA دار دارند. دلیل این رابطه معکوس بین اندازه ژنوم و میزان جهش این است که ویروسهای با RNA بزرگتر توانایی تکثیر ماده ژنتیکی خود را بدون جهش کشنده ندارند. در مقابل ویروسهای DNA دار به طور کلی ژنومهای بزرگتری داشته زیرا آنزیمهای همانند سازی بیشتری دارند. ویروسهای با DNA تک رشتهای از این قاعده مستثنی هستند، زیرا نرخ جهش ژنوم آنها میتواند به همان اندازهای باشد که در ژنوم ویروسهای RNA دار تک رشتهای دیده میشود.
نوترکیبی هنگامی اتفاق میافتد که حداقل دو ژنوم ویروسی، سلول میزبان یکسانی را آلوده کرده و بخشهای ژنتیکی را مبادله کنند. انواع مختلف نوترکیبی ویروسی بر اساس ساختار محل تقاطع قطعات ژنی شناخته میشود. نوترکیبی همولوگ در یک محل در هر دو رشته والدینی اتفاق میافتد، در حالی که نوترکیبی غیر همولوگ در مکانهای مختلف قطعات ژنتیکی درگیر رخ میدهد. علاوه بر این، تبادل مواد ژنتیکی بین ویروسها معمولاً غیر متقابل است، به این معنی که گیرنده بخشی از ژنوم به عنوان اهدا کننده قسمت جایگزین شده در منبع اصلی عمل نمیکند. از این نظر، اصطلاح نوترکیبی در ویروسها با نوترکیبی در موجودات دیپلوئید که در آن طی تولید مثل جنسی تبادل ماده ژنتیکی بین کروماتیدها در بخش میوز اول رخ میدهد متفاوت است. در واقع، نوترکیبی با گسترش دامنه میزبان ویروسی، ظهور ویروسهای جدید، تغییر خصوصیات ناقل، افزایش پاتوژنزی، فرار از مصونیت میزبان و مقاومت در برابر ضد ویروسها همراه خواهد بود.
مکانیسم نوترکیبی در ویروس ها
بسته به منشا رشتههای والدین، میتوان بین نوترکیبی درون ژنومی (که رشتههای نوترکیب مربوط به واحد ژنتیکی یکسان هستند) و نوترکیبی بین ژنومی (که در آن قطعات ریشههای مختلف دارند) تفاوت قائل شد. نوترکیبی داخل ژنومی مربوط به تنظیم بیان ژن است که این ویژگی خاصی از ویروسهای هرپس است، مانند ویروس هرپس - 1 انسان (HSV-1)، بهترین ویروس DNA دار مورد مطالعه. نوترکیبی بین ژنومی یک استراتژی برای ایجاد تنوع ژنتیکی و به طور متناقض برای حفظ یکپارچگی کروموزومی است. نوتركيبی بين ژنومی مناسب ترين فرم برای هر دو ويروس DNA و RNA دار است زيرا قادر به توليد انواع جديد با ويژگیهای بيولوژيكی متفاوت هستند.
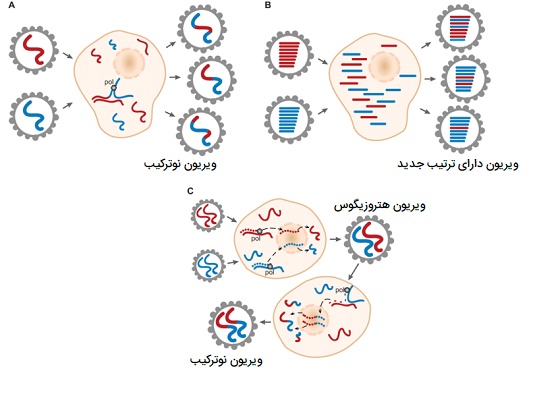
در تصویر بالا نوترکیبی و مرتب سازی مجدد ژنوم ویروس نشان داده شده است. قسمت A سادهترین مدل را برای نوترکیبی دو سویه ویروس دارای ژنومهای غیر خطی نشان میدهد. تغییر شکل الگو ممکن است زمانی اتفاق بیفتد که یک پلیمراز ویروسی در حال تکثیر دو ژنوم ویروس در یک سلول میزبان آلوده به ویروس باشد در این شرایط میتوان یک ژنوم نوترکیب از دو سویه ویروس تولید کرد. قسمت B مدل نوترتیبی (طبقه بندی جدید) در ویروس RNA با ژنوم قطعه قطعه شده مانند آنفلوانزا را نشان میدهد. ویروسهای آنفلوانزا حاوی ژنوم RNA هستند که به هشت بخش تقسیم شدهاند. هر بخش میتواند با یک بخش متناظر از ویروس سویهای دیگر مبادله شود، به طوری که ویروسهای حاصل از این پروسه میتوانند ترکیبی از پروتئینهای اهدا شده توسط هر دو ویروس مادر را بیان کنند. قسمت C مکانیسم نوترکیبی را همانطور که در HIV رخ میدهد، نشان میدهد. اچ آی وی یک ویروس دیپلوئید است که وقتی سلول میزبان به طور همزمان (یا به طور پی در پی) به دو سویه HIV آلوده میشود، دو ویروس متفاوت را در خود جای میدهد. هنگامی که این ویروس متعاقباً یک سلول جدید را آلوده میکند و در حین رونویسی معکوس تعویض الگو رخ میدهد، توالی DNA ویروسی نوترکیبی ایجاد میشود و همه ویروسهای نسل بعدی از این ژنوتیپ نوترکیب خواهند بود.
نوترکیبی در ویروس های DNA دار
اعتقاد بر این است که نوترکیبی در بسیاری از ویروسهای DNA دار توسط فعالیتهای آنزیمی سلولی انجام میشود. دو نوع کلی از نوترکیبیِ DNA ژنتیکی در سلول وجود دارد: نوترکیبی همولوگ (نوترکیبی عمومی) و نوترکیبی غیر همولوگ. نوترکیبی غیر همولوگ یا اختصاصی جایگاه نسبتاً به ندرت اتفاق میافتد و به پروتئینهای خاصی نیاز دارد که توالی DNA مشخصی را برای ترویج نوترکیبی، تشخیص میدهند. نوترکیبی همولوگ بین دو توالی DNA اتفاق میافتد که در منطقه کراس اوورها یکسان یا بسیار مشابه هستند. نوترکیبی همولوگ احتمالاً در هر ارگانیسم مبتنی بر DNA رخ میدهد و خیلی بیشتر از ترکیب غیر همولوگ اتفاق میافتد.
اطلاعات زیادی در مورد مسیرهای بیوشیمیایی مسئول کراس اور در DNA وجود دارد. علاوه بر شناسایی توالی، نیازهای ترکیبی عمومی شامل جفت شدن بازهای مکمل بین مولکولهای DNA دو رشتهای، آنزیمهای نوترکیبی و تشکیل هترودابلکس در مناطق جفت باز تکمیلی بین دو مولکول DNA است. برخی از ویروسهای DNA دار پروتئینهای خود را رمزگذاری کرده که در طی فرآیندهای نوترکیبی کار میکنند. به عنوان مثال، برخی از باکتریوفاژها مسیرهای نوترکیبی را رمزگذاری میکنند تا از وابستگی به سیستمهای میزبان جلوگیری کنند. از چنین نوترکیبی میتوان برای ترمیم DNA فاژ آسیب دیده و برای مبادله DNA بین فاژهای مرتبط استفاده کرد تا تنوع آنها افزایش یابد.
بسیاری از فعالیتهای نوترکیبی فاژی مشابه آنهایی است که در باکتری میزبان وجود دارد و مطالعات روی سیستمهای نوترکیبی باکتری تحت تأثیر مطالعات روی سیستمهای ویروسی صورت گرفته است. این مسیرها شامل پروتئینهای Rec فاژهای T4 و T7 (مشابه پروتئینهای میزبان RecA ، RecG ، RuvC یا RecBCD) ، مسیر RecE در پیش فاژ E. coli K-12 یا سیستم قرمز 1 فاژی است. نوترکیبی بین DNA ویروسی و ژنهای میزبان اولین بار در ترانسداکشن باکتریوفاژها در پروکاریوتها و رترو ویروسها (مانند HIV) در یوکاریوتها مشاهده شد. در بعضی موارد، این یک روش مفید برای به دست آوردن ژنهای سلولی برای ویروسهای DNA دار است. از جمله مثالهای جالبِ کسب ژنهای سلولی توسط ویروسهای DNA دار، ژنهای tRNA موجود در باکتریوفاژ T4 است. این ژنها حاوی اینترون (قسمت غیرخواندنی ژن) هستند که نشان میدهد باکتریوفاژ T4 باید در طی تکامل از یک میزبان یوکاریوتی عبور کرده باشد.
ویروسهای هرپس یک مدل مکانیکی شبیه با باکتریوفاژها دارند که در آن نوترکیبی و همانندسازی DNA به هم پیوسته یک مکانیسم اجدادی را نشان میدهد. همه ویروسهای هرپس یک مجموعه تکثیری مشترک دارند که با گروههای بسیار محافظت شده از پروتئینهای مخصوص همانند سازی و نوترکیبی مشخص میشوند. در ویروسهای DNA دار، نوترکیبی، نقش مهمی در ترمیم DNA آسیب دیده، دارد. پس از اتمام عفونت سلولی توسط HSV، بحثهای قابل توجهی در مورد شروع همانند سازی وجود دارد.
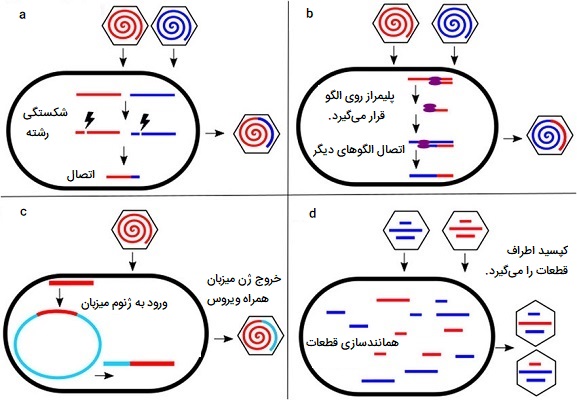
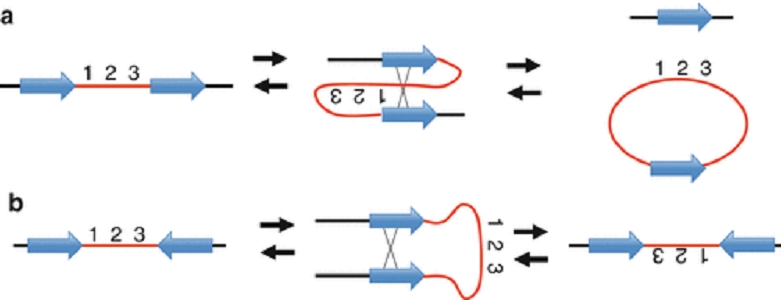
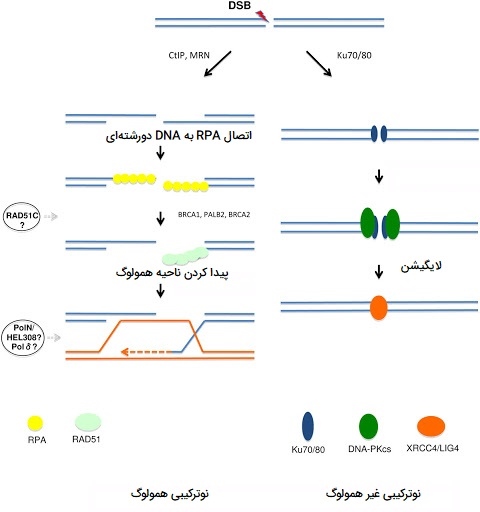
در تصویر بالا مکانیسمهای اصلی نوترکیبی ویروسهای DNA دار نشان داده شده اند. قسمت a در نوترکیبی مستقل از همانندسازی، شکستگی و ترمیم رشته نوکلئیک اسید باعث ترکیبی از مواد ژنتیکی از منابع مختلف به همان ژنوم ویروسی میشود. نوترکیبی میتواند بین توالی همولوگ یا غیرهمولوگ و بین ویروسهای عفونی کننده همزمان یا بین رشتههای اسید نوکلئیک ویروس و قطعات خارجی DNA رخ دهد. قسمت b در نوترکیبی همانندسازی یا تعویض الگو، یک مولکول پلی مراز الگو را در طی فرآیند تکثیر رشته اسید نوکلئیک تغییر میدهد. اگر الگوها از منابع مختلف مشتق شده باشند، میتوان مواد ژنتیکی جدیدی را به ژنوم ویروس وارد کرد. قسمت c، در طی فرآیند ادغام ویروس و برداشتن آن از ژنوم میزبان، ویروسها میتوانند مواد ژنتیکی را از میزبان بدست آورند. این ژنها میتوانند عفونت را افزایش دهند یا به سرکوب میزبان کمک کنند. در قسمت d تجدید ترتیب (نوترتیبی) به دنبال عفونت همزمان سلول میزبان توسط چندین ویروس تقسیم شده رخ میدهد. بخشهای ژنوم تکثیر شده صرف نظر از مبدأ، در كپسیدها بسته بندی میشوند. به این ترتیب، بخشهایی از دو یا چند والد را میتوان در یک کپسید یکسان بسته بندی کرد و سویه جدیدی ایجاد میکند که از نظر ژنتیکی با هر یک از والدین متفاوت است.
نوترکیبی در ویروس های RNA دار
ویروسهای RNA دار از RNA به عنوان ماده ژنتیکی خود استفاده میکنند. پتانسیل تغییر ژنوم RNA به دلیل سرعت جهش بالا (در هنگام کپی برداری توسط RNA پلیمراز وابسته به RNA) و نوترکیبی بسیار زیاد است. فرآیندهای ترکیب ژنتیکی در ویروسهای RNA دار دو رشتهای احتمالاً در سطح RNA رخ میدهد، زیرا این ویروسها به احتمال زیاد مراحل DNA را در چرخههای تکثیر خود طی نمیکنند. فرآیندهای نوترکیبی RNA معمولاً به صورت همولوگ یا غیر همولوگ دسته بندی میشوند. در سال 1992 ، Lai فرض کرد سه کلاس از نوترکیبی در RNA وجود دارد شامل: همولوگ، همولوگ منحرف شده و غیر همولوگ.
نوترکیبی همولوگ بین دو مولکول RNA مرتبط در مکانهای مربوطه اتفاق میافتد، اگرچه نوترکیبی RNA همولوگ نیز میتواند در یک منطقه مشترک اتفاق بیفتد که توالیهای RNA در غیر این صورت غیر متناظر هستند. نوترکیبی همولوگ منحرف شامل تلاقی بین RNA های مرتبط است، اما در جایگاههای متناظر رخ نمیدهد و منجر به درج یا حذف توالی میشود. نوترکیبی غیر همولوگ بین مولکولهای RNA غیر مرتبط رخ میدهد. نوترکیبی، در ویروسهای RNA دار مانند ویروس آنفلوانزا و ویروس فلج اطفال مشاهده شده است.
برای ویروسهای کرونا یعنی ویروسهای RNA دار حیوانی حاوی یک ژنوم بزرگ RNA، نوترکیبی بین ژنوم ویروس کرونا و RNA های معیوب تداخلی نشان داده است که ماهیت غیر پردازشی RNA پلیمراز کرونا ویروس ممکن است مسئول نوترکیبی باشد. به همین ترتیب، نوترکیبی RNA در نوداویروسها (ویروسهای RNA دو بخشی) بین بخشهای RNA در یک مکان، جایی که رشته نوپا میتواند یک منطقه جفت باز با الگوی گیرنده ایجاد کند، رخ میدهد. به نظر می رسد عواملی مانند ساختار ثانویه الگو و شباهت سایتهای متقاطع با مبدأ همانند سازی در انتخاب سایت نوترکیبی تأثیرگذار باشد. مدل ترکیبی که در آن پلیمراز به طور مستقیم با RNA ویروس پذیرنده ارتباط دارد.
نوترکیبی RNA ژنتیکی در رترو ویروسها هم مشاهده شده است. در اینجا، پرشهای نوترکیب کارآمد توسط رونویسی معکوس ایمن میشوند. در واقع، سیستم رترو ویروس نشان دهنده مدلی کاملاً ثابت از واکنشهای تغییر شکل پلیمراز / الگو است که هم در داخل بدن و هم در شرایط in vitro وجود دارد. رونویسیهای معکوس ویروسی رمزگذاری شده از نظر تکاملی برای اطمینان از پریدن در هنگام واکنشهای رونویسی معکوس انتخاب میشوند. پرشهای نوترکیب هم عوض کننده الگوهای درون مولکولی و هم بین مولکولی هستند و به علاوه تشکیل ژنومهای معیوب رترو ویروسی را نیز بر عهده دارند. آنها به طور قابل توجهی به تنوع ژنتیکی رترو ویروسها کمک میکنند.
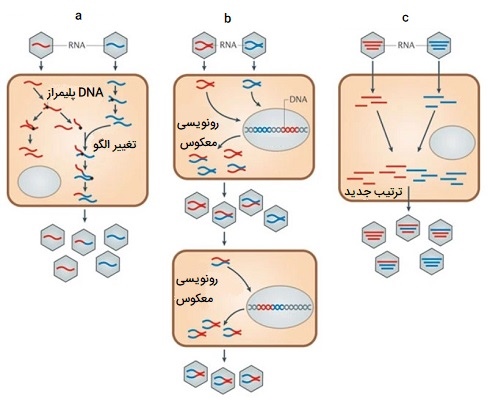
در تصویر بالا نوترکیبی در ویروسهای RNA دار نشان داده شده است. در قسمت a عفونت همزمان سلول توسط سویههای ویروسی متمایز از نظر ژنتیکی میتواند منجر به تولید ویروسهای نوترکیب شود. این روند میتواند در هر دو ویروس غیر قطعه قطعه شده (همانطور که در اینجا نشان داده شده است) یا در بخشی از ویروس قطعه قطعه شده رخ دهد. قسمت b عفونت همزمان سلول توسط سویههای ویروس متمایز از لحاظ ژنتیکی میتواند منجر به تولید ذرات ویروس هتروزیگوت شود، پس از آن یک رویداد تغییر شکل الگو میتواند منجر به ایجاد یک ویروس نوترکیب شود. در قسمت c عفونت همزمان سلول توسط سویههای ژنتیکی متمایز ویروسهای قطعه قطعه شده میتواند ترکیبات مختلفی از نسلهای جدید را ایجاد کنند.
نوترکیبی مصنوعی
در قرن گذشته، فناوری DNA نوترکیب فقط تصوری بود که میتوان با کنترل بیان ژنهای هدف، خصوصیات مطلوب را در موجود زنده بهبود بخشید. با این حال، در سالهای اخیر، این تکنیک تأثیرات منحصر به فردی را در پیشرفت زندگی بشر نشان داده است. به موجب این فناوری، پروتئینهای مهم مورد نیاز برای مشکلات بالینی و اهداف غذایی میتوانند با خیال راحت، مقرون به صرفه و کافی تولید شوند. این فناوری کاربردهای چند رشتهای و پتانسیلی برای مقابله با جنبههای مهم زندگی دارد، به عنوان مثال، بهبود سلامت، افزایش منابع غذایی و مقاومت در برابر اثرات نامطلوب زیست محیطی.
تکنیکهایی برای انتقال مصنوعی قطعات DNA از هر منبع به سلولهای گونههای مختلف ابداع شده است، بنابراین ویژگیهای جدیدی به آنها اعطا میشود. در باکتریها و مخمر (به عنوان مثال ساکارومیسز سرویزیه)، ادغام چنین DNA در ژنوم (که که ثبات تحول به طور کلی به آن بستگی دارد) به تشابه توالی قابل توجهی بین DNA ورودی و محل گیرنده نیاز دارد. با این حال، سلولهای سایر قارچها، گیاهان پیشرفتهتر و حیوانات قادرند DNA خارجی را با شباهت توالی کمی یا بدون شباهت توالی در کروموزومهای خود ادغام کنند. به نظر میرسد که این ارگانیسمها دارای یک سیستم ناشناخته هستند که انتهای آزاد قطعات DNA را بدون توجه به توالی آنها با کروموزومها ترکیب میکند.
به ویژه در کشاورزی، میتوان گفت گیاهان اصلاح شده ژنتیکی مقاومت بیشتری در برابر عوامل مضر دارند، عملکرد محصول را افزایش میدهند و برای بقا سازگاری بهتری نشان میدهند. علاوه بر این، داروهای نوترکیب اکنون با اطمینان و به سرعت در حال کسب مجوزهای تجاری هستند. تکنیکهای فن آوری DNA نوترکیب، ژن درمانی، و اصلاحات ژنتیکی نیز به طور گستردهای برای اهداف زیست پالایی و درمان بیماریهای جدی استفاده میشوند. انواع تکنیکهایی که امروزه برای نوترکیبی و ایجاد موجودات با ترکیبات ژنتیکی جدید استفاده میشوند در ادامه توضیح داده شده اند.

نوترکیبی درج پلاسمید
تکنیکی که از طریق آن از یک پلاسمید برای وارد کردن DNA نوترکیب به سلول میزبان برای شبیه سازی استفاده میشود. هم پلاسمید حامل ژن مقاومت به آنتی بیوتیک و هم رشته DNA که حاوی ژن مورد نظر است با یک آنزیم اندونوکلئاز محدود کننده برش داده میشود. پلاسمید باز شده و ژن از رشته DNA اصلی خود آزاد میشود، آنها انتهای چسبنده (ناشی از برش با یک آنزیم محدودکننده) مکمل هم دارند. سپس پلاسمید باز و ژن آزاد شده با آنزیم DNA لیگاز مخلوط میشوند، که این آنزیم آنها را به هم متصل میکند. این پلاسمید حاوی ژن، اکنون آماده انتقال به باکتری است و بعد از آن در معرض آنتی بیوتیک قرار میگیرد. تمام سلولها به جز سلولهایی که توسط DNA پلاسمید رمزگذاری شده اند، از بین میروند و سلولهای حاوی DNA نوترکیب مورد نظر باقی میمانند.
نوترکیبی از طریق تفنگ ژنی
تفنگ ژنی یک روش عالی برای مهندسی ژنتیک گیاهان فراهم میکند. این کار بر اساس این اصل انجام میشود که اگر مولکولهای DNA پوشانده شده روی ذرات طلا به سلولهای زنده بمباران شوند، این محلول DNA میتواند در DNA سلول قرار گیرد. یک تفنگ ژنی این محلول DNA را به صورت جریان تندرو با نیروی کافی برای نفوذ به ژنوم ارگانیسم هدف ارائه میدهد.
نوترکیبی تکثیر ویروس ها
ویروسها با حمله به یک سلول میزبان و تحت فرمان در آوردن سلول، در صدها نسخه از DNA ویروسی، تکثیر میشوند. ویروس خود را به خارج سلول میزبان متصل کرده و DNA خود را به سلول تزریق میکند. ژنهای ویروسی توسط آنزیمها و ریبوزومهای سلول رونویسی و ترجمه میشوند. سلول بین DNA تزریق شده توسط ویروس و DNA خود تمایز قائل نمیشود و فقط دستورالعملهای ژنتیکی داخلی خود را دنبال میکند. به این ترتیب ویروس تولیدات سلول را به عهده میگیرد. اکنون، سلول به جای تولید مواد سلولی جدید، به یک کارخانه تولید ویروس تبدیل شده است. ذرات جدید ویروس سرانجام برای یافتن سلولهای میزبان جدید از سلول آزاد میشوند.
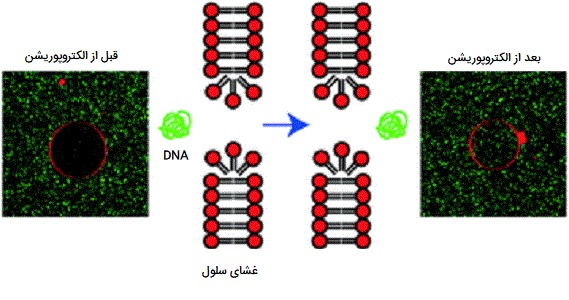
نوترکیبی از طریق الکتروپوریشن
DNA خارجی با تکنیک جدیدی به نام الکتروپوریشن (استفاده از پالس الکتریکی) به سلولهای گیاهان وارد میشود. این تکنیک شامل استفاده از پالسهای الکتریکی برای نفوذپذیری غشاهای پلاسمایی گیاه به مولکولهای DNA پلاسمید است. نشان داده شده است که DNA پلاسمیدی که از این طریق گرفته میشود، به طور پایدارتر به ارث میرسد و بیان میشود. این روش همچنین برای نوترکیبی سلولهای حیوانی استفاده شده است. پالسهای میدان الکتریکی با دقت کنترل شده به سلولهای حیوانی وارد میشوند. این امر باعث میشود که منافذ در غشای سلول باز شده و ژنها به داخل سلول دسترسی پیدا کنند.
کاربرد فناوری DNA نوترکیب
سه عامل زندگی انسان را بسیار تحت تأثیر قرار میدهد: کمبود غذا، مشکلات بهداشتی و مسائل زیست محیطی. غذا و سلامتی از نیازهای اساسی انسان در کنار یک محیط پاک و ایمن است. با افزایش جمعیت جهان با سرعت بیشتر، نیازهای انسان برای غذا به سرعت در حال افزایش است. به علاوه چندین مسئله بهداشتی مرتبط با انسان در سراسر جهان باعث مرگ و میر زیادی میشود. تقریباً هر ساله 36 میلیون نفر به دلیل بیماریهای واگیر و غیرواگیر مانند بیماریهای قلبی عروقی، سرطان، دیابت، ایدز، سل و مالاریا میمیرند. علی رغم تلاشهای گسترده، تولید مواد غذایی فعلی در جهان بسیار کمتر از نیاز انسان است و امکانات بهداشتی در کشورهای جهان سوم حتی کمتر از حد استاندارد است.
افزایش سریع صنعتی سازی باعث افزایش آلودگی محیط زیست شده و پسماندهای صنعتی به طور مستقیم اجازه مخلوط شدن با آب را دارند که این امر بر جانوران آبزی و به طور غیرمستقیم بر انسان تأثیر گذاشته است. برخلاف رویکردهای سنتی برای غلبه بر کشاورزی، بهداشت و مسائل زیست محیطی از طریق اصلاح نژاد، داروهای سنتی و تخریب آلایندهها از طریق تکنیکهای معمول، مهندسی ژنتیک فقط یک قطعه کوچک از ژنهای مورد نظر را از طریق روشهای مختلف مانند تحول بیولوژیک و ناقل آگروباکتریوم به هدف منتقل میکند. تغییر در ژنومهای گیاهی یا با هدف قرار دادن ژن وابسته به نوترکیبی همولوگ یا با اصلاح ژنوم اختصاصی جایگاه به واسطه نوکلئاز به وجود میآید.
فناوری DNA نوترکیب با تولید واکسنها و داروهای جدید در بهبود شرایط سلامتی نقش اساسی دارند. استراتژیهای درمان نیز با ایجاد کیتهای تشخیصی، دستگاههای نظارتی و رویکردهای درمانی جدید بهبود مییابند. سنتز انسولین انسانی و اریتروپویتین که یک نوع فاکتور رشد است توسط باکتریهای اصلاح شده ژنتیکی و تولید انواع جدید موشهای جهش یافته آزمایشی برای اهداف تحقیقاتی یکی از نمونههای برجسته مهندسی ژنتیک در سلامت است. به همین ترتیب، استراتژیهای مهندسی ژنتیک برای مقابله با مسائل زیست محیطی مانند تبدیل مواد زائد به سوختهای زیستی و اتانول زیستی، تمیز کردن نشت روغن، کربن و سایر مواد زائد سمی و شناسایی آرسنیک و سایر آلایندهها در آب آشامیدنی استفاده شده است. میکروبهای اصلاح شده ژنتیکی نیز به طور موثری در استخراج بیولوژیک و پالایش زیستی استفاده میشوند.
فناوری DNA نوترکیب یک زمینه با رشد سریع است و محققان در سراسر جهان در حال توسعه رویکردها، دستگاهها و محصولات مهندسی جدید برای کاربرد در بخشهای مختلف از جمله کشاورزی، بهداشت و محیط زیست هستند. به عنوان مثال، لیسپرو (هومالوگ)، در مقایسه با انسولین انسانی قدیمی، یک انسولین نوترکیب موثر بوده و سریع عمل میکند. به طور مشابه، Epoetin alfa یک پروتئین نوترکیب جدید و شناخته شده است که میتواند به طور موثری در بهبود کم خونی استفاده شود. در ادامه به نقش مهم تکنولوژی DNA نوترکیب در انواع کاربردهای مختلف زندگی بشر پرداخته ایم.
نقش نوترکیبی DNA در غذا و کشاورزی
فناوری DNA نوترکیب دارای موارد عمدهای است که تولید آنزیمهای جدید را که در شرایط لازم برای فرآوری مواد غذایی مناسب هستند، ممکن میسازد. چندین آنزیم مهم از جمله لیپازها و آمیلازها به دلیل نقشها و کاربردهای خاص آنها در صنایع غذایی، برای تولیدات خاص در دسترس هستند. تولید سویههای میکروبی نیز دستاورد عظیم دیگری است که با کمک فناوری DNA نوترکیب امکان پذیر شد. تعدادی از سویههای میکروبی تولید شده اند که از طریق مهندسی برای تولید آنزیمهای پروتئاز اختصاص یافته اند. سویههای خاصی از قارچها اصلاح شده اند تا بتوانند توانایی تولید مواد سمی را کاهش دهند.
لیزوزیمها عوامل موثری برای از بین بردن باکتریها در صنایع غذایی هستند. آنها از گسترش موجودات میکروبی جلوگیری میکنند. این ماده برای نگهداری مواد غذایی از جمله میوهها، سبزیجات، پنیر و گوشت مناسب است زیرا باعث افزایش ماندگاری آنها میشود. مهار میکروارگانیسمهای مضر غذا را میتوان از طریق لیزوزیم تثبیت شده روی فیلمهای الکل پلی وینیل و سلولز انجام داد. همچنین بیوفیلمهای مربوط به صنایع غذایی را میتوان با ترکیب فعالیت پروتئینازهای سرین و آمیلازها از بین برد. طیف گستردهای از پروتئینهای نوترکیب در گونههای مختلف گیاهی بیان شده است تا به عنوان آنزیم در صنایع مورد استفاده قرار گیرد، برخی از پروتئینهای عمده مورد استفاده در تحقیقات، پروتئینهای موجود در شیر هستند که در تغذیه نقش دارند.
تجزیه و تحلیل تولید سنتی و منبع کمی تجارت (QTL) در شناسایی انواع برنج با پروتئین کیناز معروف به PSTOL1 (تحمل کبود فسفر 1) به افزایش رشد ریشه در مراحل اولیه کمک میکند و کمبود فسفر را تحمل میکند. بیان بیش از حد این آنزیم باعث میشود ریشه بتواند مواد مغذی را به مقدار کافی در خاک با کمبود فسفر جذب کند که در نهایت عملکرد دانه را افزایش میدهد. توالی ژن کلروپلاست در تکامل و فیلوژنی گیاه مهم است. در نظر گرفته میشود که Rpl22 از کلروپلاست به ژنوم هستهای منتقل میشود. این ژن حاوی یک پپتید است که در انتقال پروتئین از سیتوزول به کلروپلاست نقش دارد. تعدادی از ژنهای مهم حذف شده از کلروپلاست به جز ycf1 و ycf2، مشاهده شده اند که به منظور جلوگیری از ایجاد اختلال در فتوسنتز و سایر فرایندهای لازم به هسته منتقل میشوند.

ترانس ژنیک کردن کلروپلاست گیاه حالتی پایدار در نظر گرفته میشود زیرا گیاهان دارای هسته تراریخته، با مشکلاتی مانند بیان پایینتر و فرار تراریخته از طریق گرده افشانی روبرو هستند. تقریباً ده هزار نسخه از تراریختهها در ژنوم کلروپلاست گنجانده شده اند. بیان تراریخته وابسته به توالیهای نظارتی ناهمگن است اما مستقل از کنترل سلولی است. درج ژن γ-tmt در ژنوم کلروپلاست منجر به تشکیل چند لایه از پوشش داخلی کلروپلاست میشود. معرفی ژنهای لیکوپن β-سیکلاز به ژنوم پلاستید (اندامک داخل سلولی دارای DNA حلقوی) گوجه فرنگی، تبدیل لیکوپن به پرو ویتامین A را افزایش میدهد.
شناسایی ژنهای خاص اندام یا بافت از طریق پروفایل بیان ژنی انجام میشود. نوسان بیان ژن و پویایی رونویسی از طریق دادههای رونوشت سنجی قابل پیش بینی است. این فرآیندها و پیش بینیها برای بهبود تولید محصولات و مقاومت در برابر تنشهای محیطی یا میکروبی مفید هستند. مقاومت در برابر عفونتهای قارچی و باکتریایی میتواند توسط ژن WRKY45 موجود در برنج که توسط گیاه فعال کننده بنزوتیادیازول که سیستم ایمنی ذاتی گیاه را فعال میکند، افزایش یابد. همچنین با قرار دادن ژن qSW5 میتوان به اندازه دانه بزرگتر دست یافت. qSH1 نیز با تشکیل لایه فرسایشی باعث جلوگیری از خرد شدن بذر میشود. ژن Kala4 مسئول رنگ سیاه برنج است که باعث مقاومت برنج در برابر عوامل بیماریزا میشود.
اصلاح ژنتیکی نیازمند ساده کردن کار با ژن از طریق معرفی ویژگیهای شناخته شده ژن است. این کار اجازه میدهد تا به طیف گستردهای از ژنهای موجود زنده دسترسی داشته باشید. سیب زمینی، لوبیا، بادمجان، چغندر قند، کدو و بسیاری از گیاهان دیگر با ویژگیهای مطلوبی به عنوان مثال، تحمل علف کش گلیفوسات، مقاومت در برابر حشرات، مقاومت به خشکی، بیماری و تحمل نمک در حال تولید هستند. مصرف نیتروژن بهتر، رسیدن محصول و سازگاری گیاهان نیز از طریق نوترکیبی افزایش یافته است.
نقش نوترکیبی DNA در درمان بیماری ها
فناوری DNA نوترکیب طیف گستردهای از کاربردها را در درمان بیماریها و بهبود شرایط سلامتی جامعه دارد. از جمله استفاده از نوترکیبی در صنایع داروسازی و همچنین تولید واکسن یا درمان بیماریهای خاص به روشهای مختلفی مانند ژن درمانی صورت گرفته و همچنان در حال رشد است. در بخشهای زیر موفقیتهای فناوری DNA نوترکیب برای بهبود سلامت انسان را توضیح داده ایم.
نوترکیبی و ژن درمانی
ژن درمانی یک تکنیک پیشرفته با پتانسیل درمانی در خدمات بهداشتی است. اولین گزارش موفقیت آمیز در زمینه ژن درمانی برای درمان یک بیماری ژنتیکی شرایط ایمنتری را به سمت درمان کشنده ترین بیماریهای ژنتیکی فراهم میکند. به عنوان مثال این استراتژی در ارائه درمان کمبود آدنوزین دآمیناز (ADA-SCID)، که یک نقص ایمنی اولیه است، پاسخ خوبی نشان میدهد. در ابتدای این فناوری، چالشهای متعددی از جمله نگهداری بیماران در PEGylated ADA (PEG-ADA) در طول ژن درمانی و هدف قرار دادن انتقال ژن به لنفوسیتهای T دلیل عدم موفقیت در نتایج بود. با این حال، بعداً نتایج موفقیت آمیز با هدف قرار دادن سلولهای بنیادی خونساز (HSC) با استفاده از یک پروتکل انتقال ژن بهبود یافته و یک رژیم تهویه myeloablative بدست آمد.
نوترکیبی و درمان بیماری های ژنتیکی
استفاده از ناقل ویروسی برای اولین بار در درمان بیماری ژنتیکی انسان موفقیت آمیز بود. ملانوم (سرطان پوست) متاستاتیک از طریق ایمونوتراپی با افزایش بیان پروتئینهای خاص طی سال 2006 تحت درمان قرار گرفت. این موفقیت در زمینه علوم بهداشتی دریچههای جدیدی برای گسترش تحقیقات جهت درمان مرگ بیماران ناشی از ایمونوتراپی باز کرد. سطوح بسیار پایدار سلولهایی که برای شناسایی تومور در خون با استفاده از رترو ویروس رمزگذار گیرنده سلول T در دو بیمار ساخته شده اند تا 1 سال پس از تزریق منجر به پسروی ضایعات ملانومای متاستاتیک شد. این استراتژی بعداً برای درمان بیماران مبتلا به کارسینوم سلول سینوویال متاستاتیک استفاده شد. سلولهای T اتولوگ برای بیان گیرندههای آنتی ژن Chimeric (CAR) با ویژگی آنتی ژن CD19 لنفوسیتهای B برای درمان سرطان خون لنفوسیتیک مزمن اصلاح ژنتیکی شدند.
انتقال ژن به تعداد کمی از سلولها در مکانهای گسسته آناتومیکی، یک استراتژی هدفمند است که توانایی ایجاد مزایای درمانی را دارد. این نتایج چشمگیر برای دیستروفی اتوزومال مغلوب غیرقابل درمان مانند کوری مادرزادی و آموروز مادرزادی لبر (LCA) نشان داد. آزمایش بالینی ژن درمانی فاز I / II کشورهای سوئیس و آلمان با هدف درمان بیماری گرانولوماتوز مزمن در آوریل 2006 با موفقیت همراه بود.
نوترکیبی و درمان سرطان
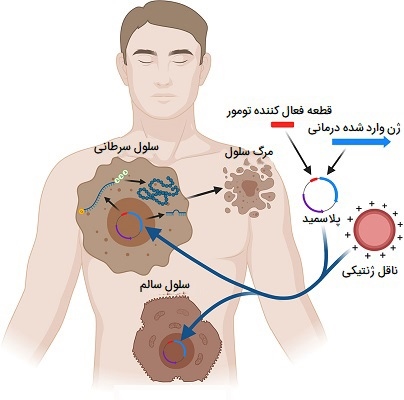
بسیاری از سرطانهای مختلف از جمله تومورهای ریه، زنان، پوستی، اورولوژی، عصبی و دستگاه گوارش و همچنین بدخیمیهای خون و تومورهای کودکان از طریق ژن درمانی مورد هدف قرار گرفته اند. قرار دادن ژنهای سرکوب کننده تومور در ایمونوتراپی، ویروس درمانی آنکولیتیک و آنزیم درمانی پیش دارو از طریق ژنها استراتژیهای مختلفی هستند که برای درمان انواع مختلف سرطانها استفاده شده است. p53، یک ژن سرکوبگر تومور که معمولاً منتقل میشود، یک بازیگر اصلی در تلاش برای درمان سرطان است.
در برخی از استراتژیها، انتقال ژن p53 با شیمی درمانی یا رادیوتراپی ترکیب میشود. مهمترین استراتژیهایی که تاکنون استفاده شده اند، واکسیناسیون با سلولهای تومور مهندسی شده برای بیان مولکولهای تحریک کننده سیستم ایمنی است. باید گفت که ژن درمانی سرطان پیشرفتهتر شده و کارایی آن در سالهای اخیر بهبود یافته است.
نوترکیبی و بیماری های قلبی
درمان بیماریهای قلبی عروقی توسط ژن درمانی یک استراتژی مهم در علوم بهداشتی است. در زمینه قلب و عروق، ژن درمانی راهی جدید برای آنژیوژنز درمانی، محافظت از قلب، بازسازی و ترمیم، پیشگیری از تنگی مجدد بدنبال آنژیوپلاستی، جلوگیری از شکست پیوند بای پس و مدیریت فاکتورهای خطر است.
نوترکیبی و تولید آنتی بادی
اخیراً از سیستمهای گیاهی برای بیان و تولید آنتی بادیهای مختلف و مشتقات آنها استفاده شده است و از بین بسیاری از آنتی بادیها و مشتقات آنتی بادی، هفت مورد به مراحل رضایت بخش مورد نیاز رسیده اند. از گیاهان توتون تراریخته میتوان برای تولید IgA / G ترشحی کایمریک معروف به CaroRx ، CaroRx استفاده کرد. پاتوژن دهانی مسئول پوسیدگی دندان معروف به جهش یافتههای استرپتوکوک توسط این آنتی بادی قابل تشخیص است.
یک آنتی بادی مونوکلونال به نام T84.66 میتواند به طور موثری برای شناسایی آنتی ژن کارسینوآمبریک، که هنوز هم به عنوان یک مارکر مشخص شده در سرطانهای بافت پوششی بدن شناخته میشود، عمل کند. تولید تستوسترون توسط hCG تحریک شده میتواند توسط هر یک از این آنتی بادیها در سلولهای کشت شده توسط LEYDIG مهار شود و افزایش وزن رحم در موشها که از طریق آن فعالیت hCG بررسی میشود به تأخیر بیفتد. تشخیص و درمان تومورها میتواند با کمک آنتی بادی انجام شود.
نوترکیبی و بررسی متابولیسم دارو
سیستم پیچیده آنزیمهای متابولیزه کننده دارو که در متابولیسم دارو نقش دارند، برای بررسی اثربخشی مناسب و اثرات داروها بسیار مهم است. رویکردهای DNA نوترکیب اخیراً از طریق بیان ناهمگن نقش آن را ایفا کرده اند، جایی که در آن اطلاعات ژنتیکی آنزیم از طریق انتقال ژن به صورت in vitro یا in vivo بیان میشود.
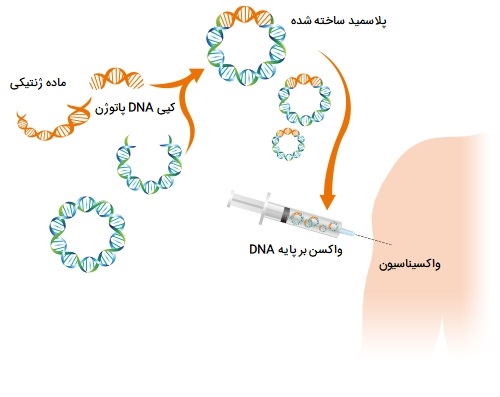
نوترکیبی و تولید واکسن و هورمون های نوترکیب
واکسنهای سنتی مقایسهای دارای کارایی و اختصاصیت کمتری نسبت به واکسنهای نوترکیب هستند. یک روش بدون ترس و بدون درد برای انتقال ناقلین آدنوویروسی که آنتی ژنهای پاتوژن را رمزگذاری میکنند، از طریق انتقال از بینی افراد است که همچنین یک روش سریع و محافظت کننده در برابر عوامل بیماریزای مخاطی است. این به عنوان یک واکسن دارویی عمل میکند که در آن یک حالت ضد آنفلوانزا از طریق بیان ژن در مجاری هوایی ایجاد میشود.
در حال حاضر تولید آزمایشگاهی هورمون محرک فولیکول انسان (FSH) از طریق فناوری DNA نوترکیب امکان پذیر است. FSH بطور قابل توجهی یک پروتئین هترودایمری پیچیده است و رده سلولی مشخص شده از یوکاریوتها برای بیان آن انتخاب شده است. درمان کمک باروری از طریق تحریک رشد فولیکولی دستاورد فناوری DNA نوترکیب است. تعداد زیادی از بیماران از طریق r-FSH تحت درمان هستند.
نوترکیبی و محیط زیست
مهندسی ژنتیک و نوترکیبی DNA کاربردهای گستردهای در حل مسائل زیست محیطی دارند. آزادسازی میکروبهای مهندسی ژنتیک، به عنوان مثال، سویه سودوموناس فلورسانس تعیین شده HK44 برای اهداف زیست پالایی در این زمینه برای اولین بار توسط دانشگاه تنسی و آزمایشگاه ملی اوک ریج با همکاری هم صورت گرفت. سویه مهندسی شده حاوی پلاسمید کاتابولیک نفتالین pUTK21 و یک ژن lux تولید کننده «بیولومینسانس» (Bioluminescence) مبتنی بر ترانسپوزون است که در یک پروموتر ذوب شده است و منجر به بهبود تخریب نفتالین و یک پاسخ همزمان «بیولومینسنت» (Bioluminescent) میشود.
ژن HK44 به عنوان «گزارشگر» (Reporter) برای فراهمی زیستی و تجزیه بیولوژیکی نفتالین عمل میکند در حالی که توانایی سیگنالینگ بیولومینسانس آن را قادر میسازد به عنوان ابزاری آنلاین برای نظارت درجا از فرایندهای تصفیه زیست محیطی مورد استفاده قرار گیرد. تولید سیگنال بیولومینسنت با استفاده از فیبرهای نوری و ماژولهای شمارش فوتون قابل تشخیص است.
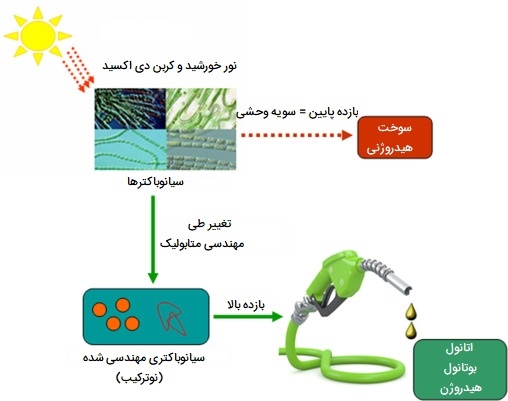
کاربرد نوترکیبی در تولید انرژی
چندین میکروارگانیسم، به ویژه سیانوباکتریومها، تولید هیدروژن که یک منبع انرژی دوستدار محیط زیست است، را هدایت میکنند. تولید یک ماده خاص با استفاده درست از آنزیمهای مورد نیاز حفظ میشود زیرا این آنزیمها نقشی اساسی در تشکیل محصول دارند. اما رویکردهای پیشرفته مانند مهندسی ژنتیک، تغییر در مواد مغذی و شرایط رشد، محیط کشتهای ترکیبی، مهندسی متابولیک و فناوری بدون سلول نتایج مثبتی را برای افزایش تولید هیدروژن در سیانوباکتریها و سایر سوختهای زیستی نشان داده اند. تجاری سازی این منبع انرژی، محیط را تمیز نگه میدارد که با استفاده از منابع متداول انرژی آزاد کننده CO2 و سایر مواد شیمیایی خطرناک، این امر ممکن نیست.
فناوری DNA نوترکیب یک پیشرفت مهم در علم است که زندگی انسان را بسیار آسانتر کرده است. در سالهای اخیر، این تکنولوژی استراتژیهای پیشرفتهای برای کاربردهای زیست پزشکی مانند درمان سرطان، بیماریهای ژنتیکی، دیابت و چندین بیماری گیاهی به ویژه مقاومت در برابر ویروس و قارچ دارد. نقش فن آوری DNA نوترکیب در تمیز کردن محیط زیست (گیاه درمانی و اصلاح میکروبی) و افزایش مقاومت گیاهان در برابر عوامل مختلف نامطلوب (خشکسالی، آفات و نمک) به طور گستردهای شناخته شده است. چالشهای موجود در زمینه بهبود محصولات در سطح ژن، گاهی اوقات با مشکلات جدی روبرو است که برای بهتر شدن آینده فناوری نوترکیب DNA باید مورد بررسی قرار گیرد. با توجه به مسائل بهداشتی، فناوری نوترکیب به درمان چندین بیماری کمک میکند که در شرایط طبیعی قابل درمان نیستند، اگرچه پاسخهای ایمنی مانع دستیابی به نتایج خوب میشوند.
نگرانیهای زیادی در مورد تولید گیاهان مهندسی ژنتیک و سایر محصولات وجود دارد. به عنوان مثال، بدیهی است که گیاهان مهندسی ژنتیکی میتوانند با گیاهان وحشی هم نژاد شوند، بنابراین ژنهای مهندسی شده خود را در محیط پخش میکنند و تنوع زیستی ما را آلوده میکنند. بعلاوه، این نگرانی وجود دارد که مهندسی ژنتیک پیامدهای سلامتی خطرناکی داشته باشد. بنابراین، برای غلبه بر چنین موضوعاتی و رفع نگرانیهای افراد جامعه، تحقیقات گسترده دیگری در این زمینه لازم است.












