سیکل ترمودینامیکی اتو (Otto Cycle) و موتور احتراق داخلی – یادگیری با مثال
در راستای معرفی و تشریح سیکلهای ترمودینامیکی در این قسمت، قصد داریم تا در مورد روابط حاکم بر سیکل اتو صحبت کنیم.

در ابتدا دکتر Nikolaus August Otto، دانشمند آلمانی بود که مفاهیم سیکل اتو را ارائه کرد. همچنین او بود که برای اولین بار موتور چهار مرحلهای درونسوز را ساخت. البته برای اولین بار Alphonse Beau de Rochas، مهندس فرانسوی بود که توانست موتور احتراق داخلی چهار مرحلهای را ثبت اختراع کند.
سیکل اتو به مجموعه فرآیندهایی ایدهآلی اتلاق میشود که مبنای کاری موتورهای احتراق داخلی هستند. در حقیقت در اکثر وسایل نقلیه عمومی از این سیکل استفاده میشود. گفتنی است که در سیکل اتو از گاز به عنوان سیال کاری استفاده میشود. البته همچون سیکل رانکین و یا سیکل یخچال، سیال کاری در حالت واقعی یک چرخه را طی نمیکند و تنها به منظور مدلسازی راحتتر است که فرآیندها به صورت یک چرخه در نظر گرفته میشوند. در ادامه در مورد نحوه کارکرد و چرخهای بودن سیکل اتو بیشتر صحبت خواهیم کرد. در سیکل اتو گاز موجود در سیلندر را به عنوان سیستم در نظر میگیرند.
فرآیندهای سیکل اتو
پیشتر در وبلاگ فرادرس در مورد سیکل برایتون بحث شد. در آنجا گفتیم که این سیکل از ۲ فرآیند فشار ثابت و دو فرآیند آیزنتروپیک تشکیل شده است. اگر در همان سیکل، به جای دو فرآیند فشار ثابت، از دو فرآیند حجم ثابت استفاده شود، سیکل بدست آمده همان سیکل اتو است.
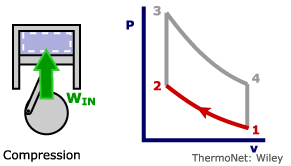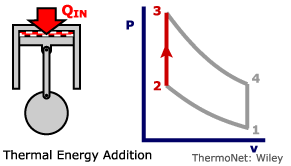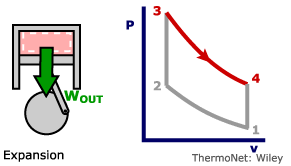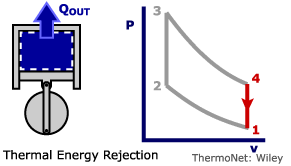
بهمنظور تشریح فرآیندهای رخ داده در سیکل اتو در ابتدا نمودار زیر را در نظر بگیرید. این نمودار نشان دهنده تغییرات فشار بر حسب حجم سیلندر در هر مرحله از سیکل است.
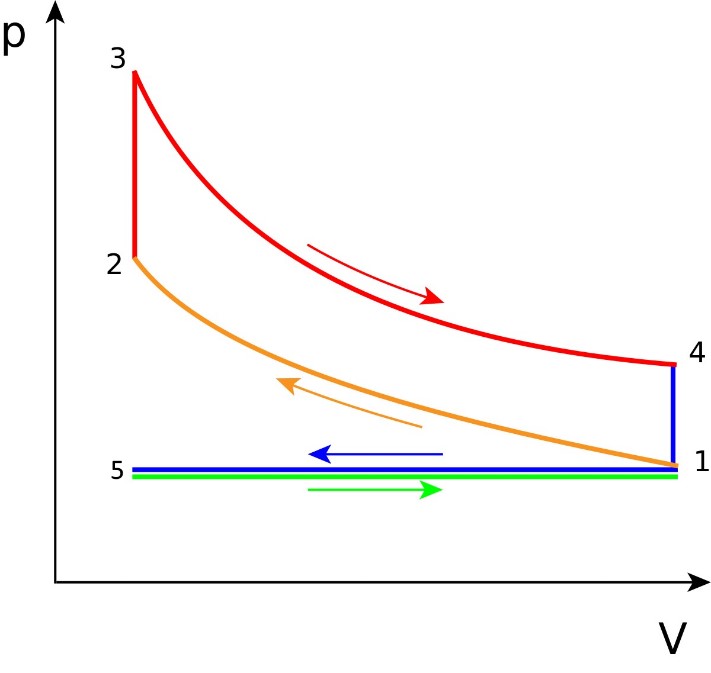
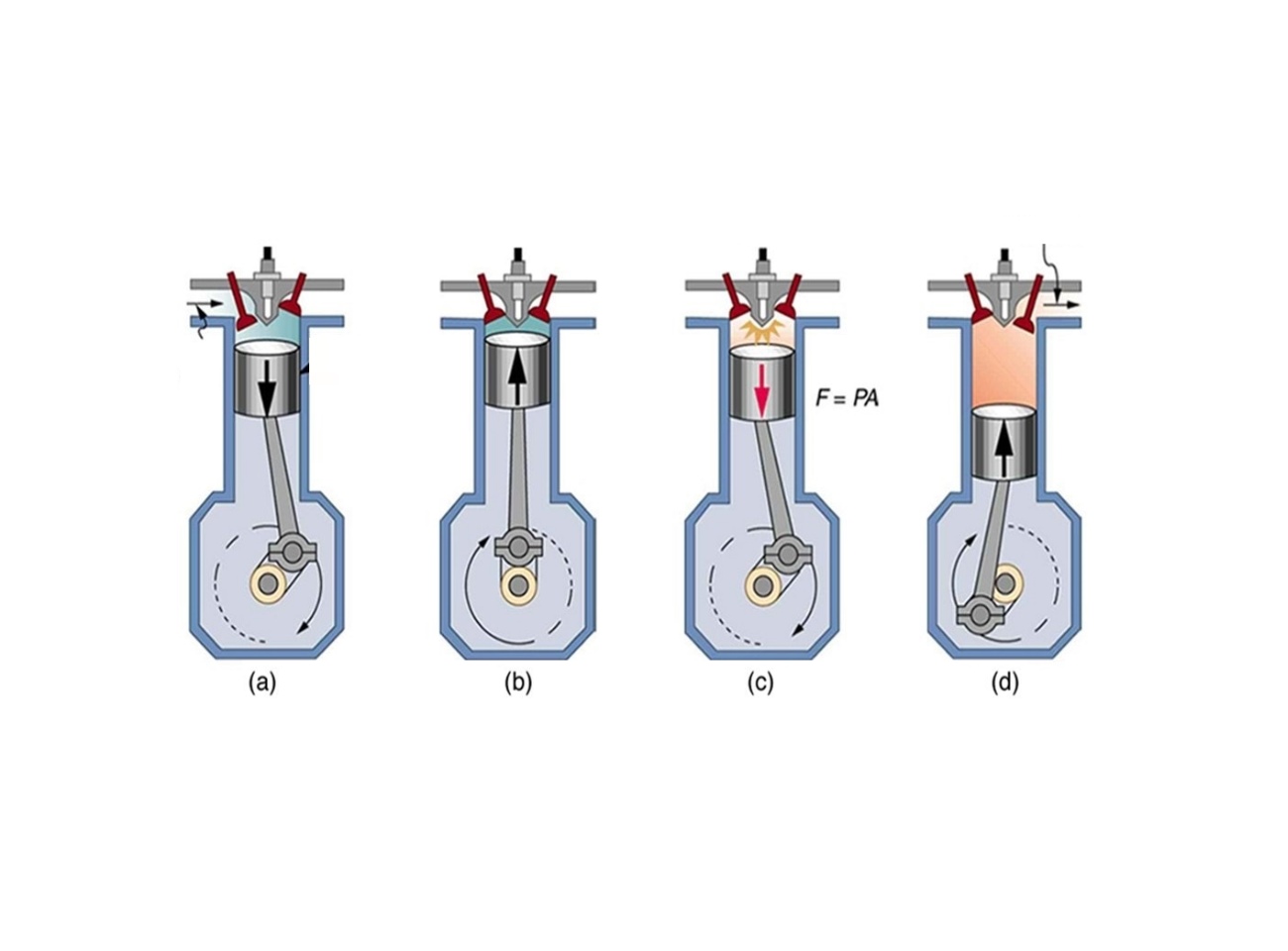
در سیکل اتو در ابتدا مخلوط هوا و سوخت به شکل فشار ثابت به سیلندر تزریق میشود [این فرآیند را مکش نیز مینامند]. پس از آن گاز به صورت آیزنتروپیک فشرده شده و دمای آن افزایش مییابد. در مرحله بعد، زمانی که پیستون به بالاترین نقطه میرسد (اصطلاحاً به این نقطه، «مرگ بالا» گفته میشود)، احتراق رخ داده و منجر به پایین آمدن پیستون و در نتیجه تولید کار میشود. در مرحله آخر دما و فشار گاز به صورت آیزنتروپیک کاهش مییابد. پس از آن دوباره مخلوط سوخت و هوا مکیده میشود و همین مراحل تکرار خواهند شد. شکل زیر فرآیندهای رخ داده در سیکل اتو را نشان میدهد.
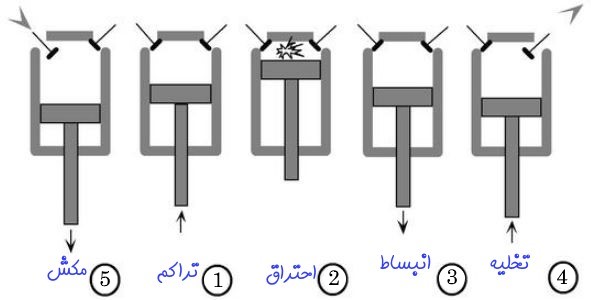
به طور خلاصه و با توجه به شکل ۱ فرآیندها را میتوان به شرح زیر بیان کرد:
- : مکش سوخت و هوا به صورت فشار ثابت
- : افزایش فشارِ مخلوطِ گاز به صورت آیزنتروپیک
- : فرآیند احتراق و دریافت گرما در حجم ثابت
- : انبساط و تولید کار به صورت آیزنتروپیک
- : دفع حرارت به بیرون
- : تخلیه مخلوط هوا و گاز به محیط
همچنین انیمیشن زیر مراحل مختلف سیکل اتو را که در موتور احتراق داخلی مورد استفاده قرار گرفته، نشان میدهد.
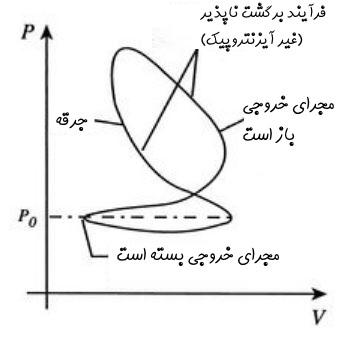
سیکل واقعی اتو، تغییرات ناگهانی سیکل ایدهآل را تجربه نمیکند. شکل زیر نمودار فشار-حجم مربوط به یک سیکل واقعی را نشان میدهد. همانطور که در آن میبینید، ارتباط میان فرآیندها به شکلی پیوسته و به نسبت سیکل ایدهآل، آرامتر اتفاق میافتد.
راندمان سیکل ایدهآل اتو
در مبحث سیکلهای ترمودینامیکی بیان کردیم که راندمان یک سیکل ایدهآل معادل با نسبت کار خالص خروجی به گرمای ورودی به سیستم است. در حقیقت راندمان یک سیکل را میتوان مطابق با رابطه زیر بیان کرد:
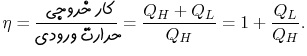
در این سیکل نیز همانند بقیه سیکلهای ترمودینامیکی گرمای ورودی به سیستم مثبت و گرمای خروجی از آن منفی در نظر گرفته میشود. در سیکل اتو گرمای دریافتی در طی فرآیند احتراق و در حجم ثابت اتفاق میافتد. در حقیقت با توجه به نمودار شکل ۱ این گرما در فرآیند ۲-۳ رخ میدهد. از این رو میتوان تغییرات انرژی درونی در این فرآیندها را برابر با گرمای ورودی به سیستم در نظر گرفت. در نتیجه میتوان گفت:
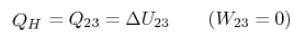
با توجه به اینکه این فرآیند به صورت حجم ثابت در نظر گرفته شده، بنابراین میتوان تغییرات انرژی درونی را به شکل زیر و وابسته به دمای اولیه و نهایی نوشت.
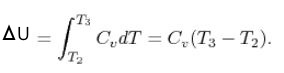
روابط مربوط به دفع حرارت نیز همانند بالا قابل بیان است. از آنجایی که دفع حرارت در فرآیند ۱→۴ اتفاق میافتد، میتوان نوشت:
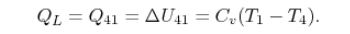
با توجه به مقادیر بدست آمده راندمان سیکل برابر است با:
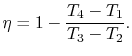
با توجه به آیزنتروپیک بودن فرآیند ۱-۲ و ۳-۴، نسبت دمایی سمت چپ رابطه بالا را به شکل زیر و بر حسب نسبت حجم در این دو نقطه بیان میکنیم.
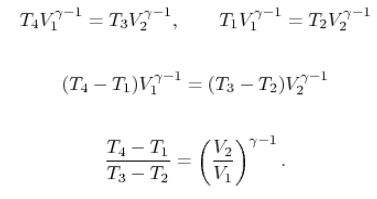
مقدار v2/v1 را نسبت تراکم مینامند و آن را با r نمایش میدهند. با توجه به فرضهای صورت گرفته، راندمان سیکل بر حسب r، به صورت زیر بدست میآید.
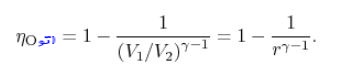
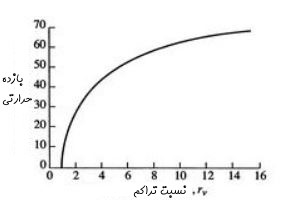
همچنین در نمودار زیر راندمان سیکل بر حسب نسبت فشار، نشان داده شده است. با توجه به این نمودار میتوان فهمید که با افزایش مقدار r، راندمان سیکل نیز افزایش مییابد اما مشکل آن است که دمای T۲ نیز افزایش یافته که منجر به احتراق زود هنگام خواهد شد. در حقیقت تلاش ما بر این است که احتراق را با استفاده از جرقه ایجاد کنیم تا به این شکل زمان دقیق احتراق برای ما قابل کنترل باشد.
نرخ کار انجام شده بر واحد آنتالپی ورودی به سیستم
با استفاده از مقادیر حرارت ورودی و خروجی محاسبه شده برای سیکل اتو، نسبت توان خروجی به آنتالپی ورودی به سیستم را میتوان مطابق با رابطه زیر محاسبه کرد.
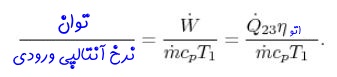
معمولا مهندسان علاقهمند هستند تا این عدد را افزایش دهند. دلیل این امر تولید توان مشابه، با حجم کمتری از سیلندر در نسبتهای بالاتر است. حرارت ورودی به موتور را میتوان مطابق با رابطه زیر محاسبه کرد:
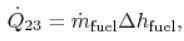
در رابطه بالا Δhfuel حرارت ناشی از واکنش است. این حرارت در حقیقت میزان انرژی آزاد شده بر واحد جرم مخلوط هوا و سوخت است. همچنین دبی جریان ورودی به موتور است. از طرفی توان بیبعد را میتوان به صورت نسبت کار خروجی به آنتالپی جریان ورودی در نظر گرفت. با توجه به تعریف، این عدد بیبعد به شکل زیر قابل تعریف است.
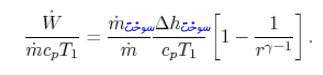
معمولا نسبت سوخت به هوا برابر با ۱/۱۵ در نظر گرفته میشود []. همچنین نسبت انرژی آزاد شده ناشی از واکنش به آنتالپی سوخت ورودی، برابر است با:
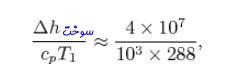
با توجه به این دو مقدار ثابت در نظر گرفته شده، نسبت توان خروجی به آنتالپی ورودی به موتور برابر است با:
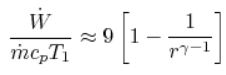
مثال
سیکل اتویی را فرض کنید که در آن نسبت تراکم - یا ضریب تراکم - برابر با r=9 باشد. همچنین فرض کنید که هوا در فشار ۱۰۰ کیلوپاسکال و دمای ۲۰ درجه به محفظه 500 سانتی متر مکعب وارد میشود. همچنین دمای مخلوط را پس از احتراق برابر با ۸۰۰ کلوین در نظر بگیرید. خواص گاز به ترتیب زیر هستند.
- ظرفیت گرمایی ویژه هوا در فشار ثابت را برابر با در نظر بگیرید.
- ظرفیت گرمایی ویژه مخلوط در حجم ثابت برابر با است.
- ظرفیت حرارتی مخلوط را نیز برابر با k= cp/cv= 1.4 در نظر بگیرید.
با توجه به فرضیات در نظر گرفته شده، موارد زیر مطلوب است.
- جرم هوای وارد شده به سیلندر در طی یک سیکل
- دمای T3
- فشار p3
- میزان حرارت اضافه شده به سیستم پس از سوختن مخلوط
- راندمان حرارتی سیکل
۱. جرم هوای وارد شده
بهمنظور انجام محاسبات مربوط به سیکل اتو در ابتدا بایستی جرم وارد شده به سیلندر را قبل از تراکم بدست آورد. با استفاده از قانون گاز ایدهآل میتوان گفت:
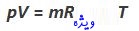
اجزاء رابطه بالا به ترتیب زیر هستند:
- p: فشار مطلق گاز
- m: جرم گاز وارد شده به سیستم
- V: حجم سیستم
Rspecific ثابت ویژه گازها است که برابر با نسبت ثابت جهانی گازها به جرم مولکولی مخلوط گاز در نظر گرفته میشود. برای هوای خشک این مقدار برابر با محاسبه شده است. با توجه به ثوابت بیان شده برای این مسئله مقدار جرم ورودی به سیلندر را میتوان با استفاده از قانون گاز ایدهآل و به صورت زیر بیان کرد:
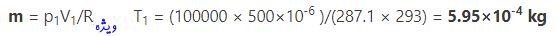
۲. دمای T3
با توجه به اینکه فرآیند انبساط به شکلی آدیاباتیک اتفاق میافتد از این رو میتوان رابطه زیر را بین دما و حجم نوشت.
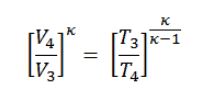
با استفاده از رابطه بالا، T3 به صورت زیر بدست میآید.
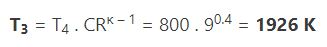
۳. فشار p3
دوباره میتوان از قانون گاز ایدهآل بهمنظور محاسبه فشار در ابتدای فرآیند انبساط استفاده کرد [منظور فشار در نقطه ۳ است]. فشار در نقطه ۳ برابر است با:
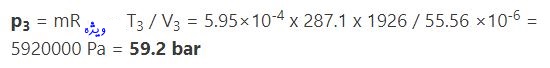
۴. مقدار حرارت اضافه شده
بهمنظور محاسبه میزان حرارت اضافه شده ناشی از سوختن مخلوط گازی، میتوان از قانون اول ترمودینامیک - یا همان قانون پایستگی انرژی - در یک فرآیند حجم ثابت استفاده کرد. این قانون میگوید که میزان انرژی داخلی زیاد شده برای گاز و مقدار حرارت اضافه شده به آن با یکدیگر برابر هستند. بنابراین میتوان نوشت:
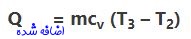
دمای نهایی پس از فرآیند تراکم را میتوان با استفاده رابطه حجم - فشار - دما، برای یک فرآیند آدیاباتیک به شکل زیر نوشت. توجه داشته باشید که این رابطه در فرآیند ۱ به ۲ نوشته شده است.
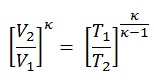
در نتیجه دمای T2 برابر با مقدار زیر بدست میآید.
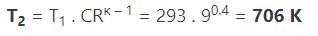
از این رو با بدست آمدن دمای T2 تغییرات انرژی درونی و نهایتا مقدار حرارت اضافه شده به سیستم نیز به شکل زیر بدست میآید.
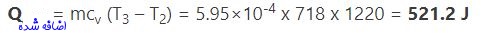
۵. راندمان حرارتی
همانطور که در بالا نیز بیان شد، میتوان با تقسیم مقدار کار خالص انجام شده به حرارت ورودی به سیستم، راندمان سیکل را یافت. اما در حالتی که نسبت تراکم معلوم است، راحتتر است که از رابطه زیر استفاده شود.
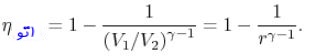
با جایگذاری ۹ به جای r و ۱.۴ به جای γ در رابطه بالا، راندمان حرارتی سیکل برابر با مقدار زیر بدست میآید.
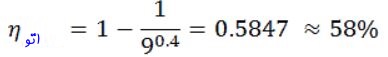
مثال بالا نمونه مناسبی جهت تحلیل یک سیکل اتو است. از این رو لازم است که آن را چندین بار مطالعه بفرمایید؛ همچنین در صورت علاقهمندی به مباحث مرتبط در زمینه مهندسی مکانیک آموزشهای زیر به شما پیشنهاد میشود:
- سیکل رانکین چیست؟ -- یادگیری با مثال
- سیکل ترمودینامیکی چیست؟ — به زبان ساده
- ترمودینامیک — از صفر تا صد
- تعریف گرما و دما در ترمودینامیک — به زبان ساده
^^













سلام
مطالب مفید بودن ای کاش مطالبی هم در رابطه با
راندمان حداکثری موتور های درون سوز در حالت های مختلف هم توضیح میدادین و همچنین آنتالپی بازگشت انرژی حرارتی اتلاف شده توسط بدنه سیلندر به چرخه
با سلام خدمت شما همراه گرامی؛
در این زمینهها پیشنهاد میکنیم مطلب «موتورهای درونسوز و هر آنچه باید درباره آنها بدانید» از مجله فرادرس را مطالعه کنید. همچنین مشاهده فیلم آموزش «آموزش موتورهای درون سوز و احتراق داخلی ICE – بخش یکم + گواهینامه» فرادرس نیز به شما کمک خواهد کرد.
از همراهی شما با مجله فرادرس سپاسگزاریم.
در فرمول به دست آوردنQ23 یکای دبی جریان ورودی به موتور چیست یکای حرارت ناشی از احتراق چیست
در قسمت جرم هوای وارد شده، واحد ثابت گاز هوا رو اشتباه نوشتید.
باید بنویسید j/Kg.K
از توجه شما سپاسگزاریم؛
متن مورد نظر اصلاح شد.
با تشکر
ممنون بابت مطالب مفیدتون
یسوال داشتم
توی مثال و قسمت p3 برای حجمv3 مقدار 6-^10*55.56 را از کجا بدست آوردید؟؟
زبان از بیان مفید و علمی بودن مطلبتون غاصره مرسی