گروه عاملی در شیمی – به زبان ساده
در این مطلب از مجله فرادرس در مورد گروه عاملی در شیمی صحبت میکنیم. در حال حاضر بیش از ۱۶ میلیون ترکیب آلی در دنیا کشف شده است که هرکدام خواص فیزیکی و شیمیایی ویژهای دارند. بدون داشتن روشی مشخص، نمیتوان ارتباط بین ساختار این مواد و خواص آنها را بررسی کرد. از جمله اصلیترین راهها برای بررسی مولکولهای آلی، دستهبندی آنها به دو بخش است: چهارچوبی از اتمهای کربن و گروههای اتمی ویژهای موسوم به گروه عاملی. با تقسیمبندی ترکیبات آلی به کمک گروه عاملی میتوان آنها را در دستههای کوچکتری مورد بررسی قرار داد.
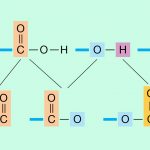
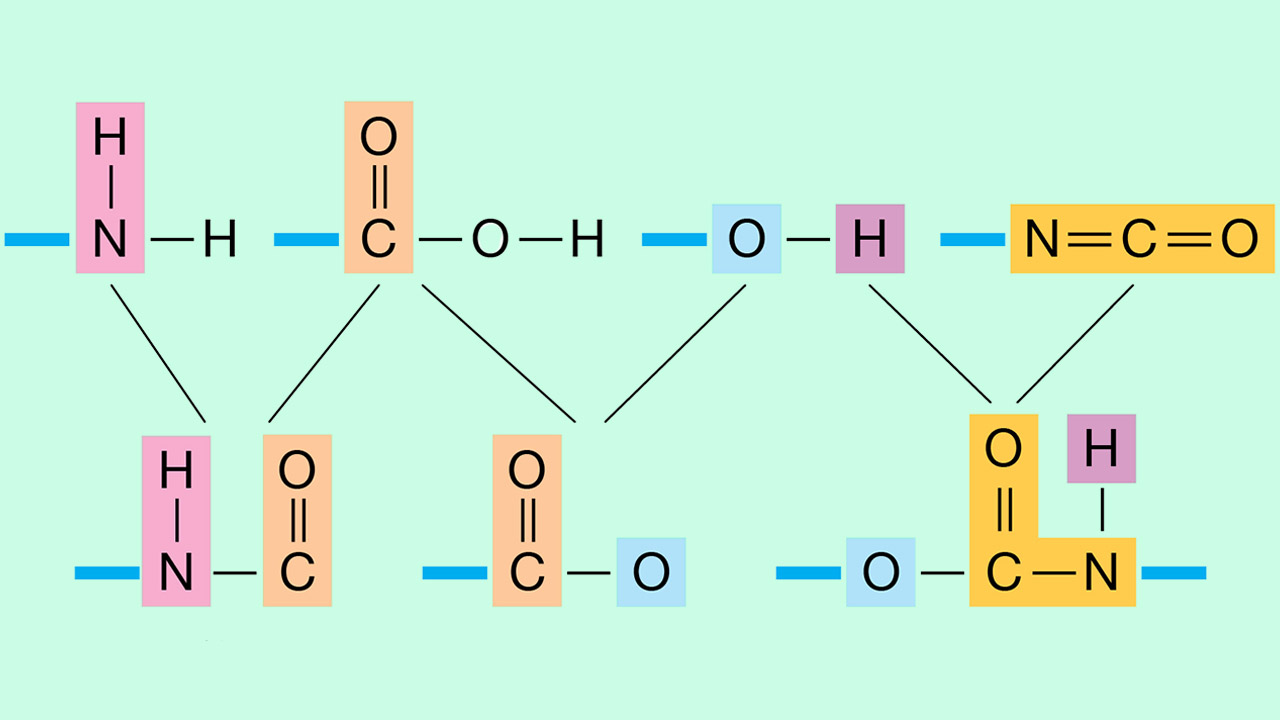
گروه عاملی به شدت بر خواص فیزیکی و شیمیایی مولکولهای خود تاثیرگذار است. به عبارت دیگر، گروههای عاملی، محلی از انجام واکنشهای شیمیایی در ترکیبات آلی به شمار میآیند. با بررسی گروه عاملی در یک مولکول، خواص فیزیکی و شیمیایی آن قابل پیشبینی خواهد بود.
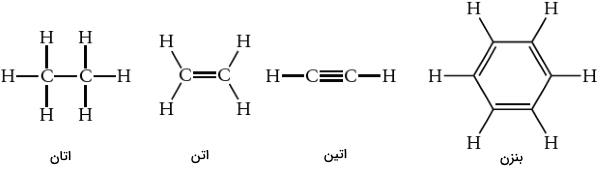
گروههای عاملی، میتوانند شامل عناصر زیادی باشند اما اصلیترین آنها اکسیژن و نیتروژن است. گوگرد و هالوژنها کمتر در این گروهها دخیل هستند. برخی از گروههای عاملی، بخشی از چهارچوب مولکول به شمار میآیند و شامل پیوندهای چندگانه بین ساختار اتم کربن در ترکیبات آلی همچون اتن، اتین و بنزن میشوند.
هیدروکربنها و هالوآلکانها
همانطور که از نام هیدروکربنها مشخص است، این مواد در ساختار خود شامل اتمهای کربن و هیدروژن هستند. بسته به نوع پیوندی که بین اتمهای کربن و هیدروژن وجود دارد، هیدروکربنها را میتوان به آلکانها، آلکنها و آلکینها دستهبندی کرد.
همچنین، اگر هیدروکربنها دارای حلقه بنزنی باشند، در دسته «آرن» (Arene) جای میگیرند.
ترکیباتی که پیوند دوگانه یا سهگانه کربن-کربن داشته باشند، در واکنش با گاز هیدروژن، ترکیب آلی با پیوند یگانه کربن تشکیل میدهند. به طور مثال، اتن به هنگام واکنش با گاز هیدروژن و در حضور کاتالیزور پلاتین، اتان تولید میکند. بسیاری از ترکیباتی که پیوند دوگانه کربن-کربن دارند، در چنین واکنشهایی شرکت میکنند.
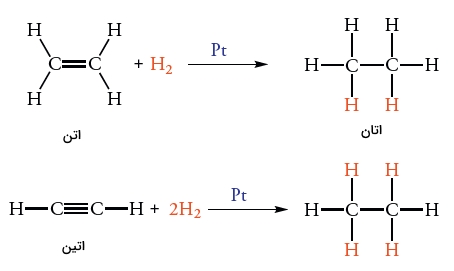
پیوندهای دوگانه یا سهگانه، در ساختارهای پیچیدهای حضور دارند. بسیاری از این ترکیبات کربنی، در واکنشهایی همانند بالا شرکت میکنند. البته در این خصوص باید ترکیبات آروماتیک و واکنشهای آنها را به طور جداگانه بررسی کرد.
مثال
براساس واکنش هیدروژن با اتن، ساختار فرآورده واکنش بین گاز هیدروژن اضافی با مولکول ۱و۳-بوتادین را رسم کنید.
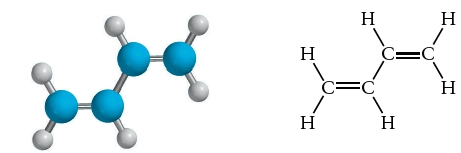
ساختار مولکول، شامل دو پیوند دوگانه است که هرکدام با هیدروژن وارد واکنش میشوند. در اثر این واکنش، اتم دیگری از هیدروژن در محل پیوندهای دوگانه قرار میگیرد و پیوندهای دوگانه را به یگانه تبدیل میکند. این واکنش با دو مول گاز هیدروژن برای هر مول از مولکول ۱و۳-بوتادین انجام میشود. در نهایت، ساختار مولکولی فرآورده واکنش (بوتان) به صورت زیر خواهد بود:
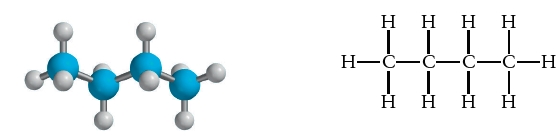
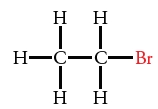
هالوآلکانها
در یک «هالوآلکان» (Haloalkane)، یکی از اتمهای هیدروژن یا بیشتر، با یک یا چند هالوژن جایگزین شده است.
گروه عاملی شامل اکسیژن
بعد از کربن و هیدروژن، معمولترین عنصر در ترکیبات آلی، اکسیژن است. اکسیژن، اتمی «دوظرفیتی» (Divalent) محسوب میشود و در نتیجه، پیوندهای یگانه یا دوگانه کربن-اکسیژن را در ترکیبات کربن شاهد هستیم.
پیوند یگانه کربن-اکسیژن در الکلها و اترها
پیوند یگانه کربن اکسیژن در الکلها و اترها دیده میشود. الکلها، شامل پیوند یگانه و پیوند یگانه هستند. واحد ساختاری ، به گروه هیدروکسیل موسوم است و گروه عاملی الکلها را تشکیل میدهد.
گروه عاملی اترها نیز، اتم اکسیژن متصل به دو اتم کربن با پیوند یگانه است. اتم اکسیژن الکلها و اترها، دو جفتالکترون ناپیوندی را شامل میشود.
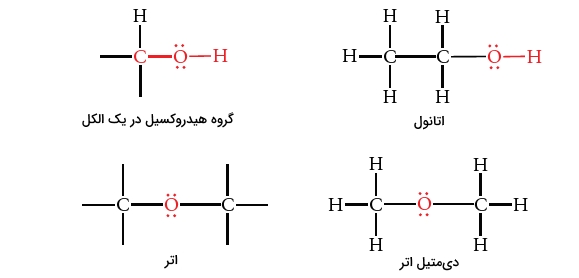
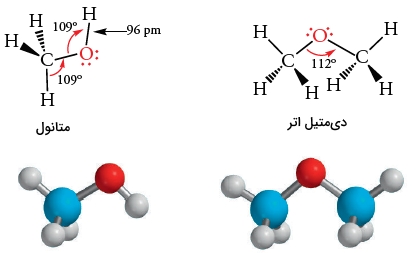
زاویه پیوندی در الکلها و در اترها، طبق تصویر زیر، برابر با 109 درجه است. طول پیوند کوتاهتر از ذکر میشود چراکه اکسیژن، الکترونگاتیوی بیشتری نسبت به کربن دارد. در نگاهی دیگر، با توجه به اینکه شعاع اتمی اکسیژن، از کربن کوچکتر است، طول پیوند کربن-اکسیژن، کوتاهتر از پیوند کربن-کربن خواهد بود.
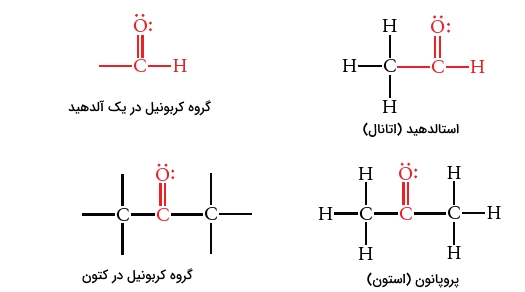
پیوند دوگانه کربن-اکسیژن در آلدهیدها و کتونها
پیوند دوگانه بین کربن و اکسیژن را با نام گروه عاملی کربونیل میشناسند. اتم کربن در گروه کربونیل، موسوم به «کربن کربونیل» (Carbonyl Carbon) و اتم اکسیژن، «اکسیژن کربونیل» (Carbonyl Oxygen) است. آلدهیدها و کتونها، هردو شامل گروه کربونیل هستند. گروه کربونیل در آلدهیدها، حداقل با یک اتم هیدروژن پیوند تشکیل داده است. در کتونها، کربن کربونیل با دو اتم کربن دیگر پیوند پیوند دارد.
اتم کربن کربونیل از نوع هیبرید شده است و شکلی به صورت سهضلعی مسطح دارد. پیوندهای سیگما در اتم کربن، نتیجه همپوشانی هرکدام از اوربیتالهای هیبریدشده کربن با اوربیتال اتم دیگر ذکر میشود.
پیوندهای کربن-اکسیژن در اسیدها و استرها
گروه کربونیل در کربوکسیلیک اسیدها و استرها نیز دیده میشود. در یک کربوکسیلیک اسید، اتم کربن کربونیل با گروه هیدروکسیل نیز پیوند دارد. در یک استر، کربن کربونیل، به یک گروه آلکوکسی، مانند متصل شده است.
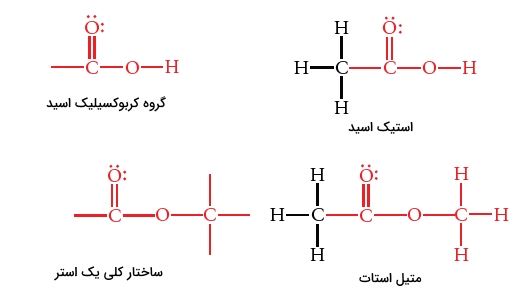
کربوکسیلیک اسیدها و استرها شامل یک پیوند دوگانه کربن-اکسیژن و یک پیوند یگانه کربن-اکسیژن هستند. در اتم اکسیژن، پیوند از نوع هیبرید شده خواهد بود و بنابراین، شکل گروهِ شامل اکسیژن، به الکلها و اترها شباهت دارد.
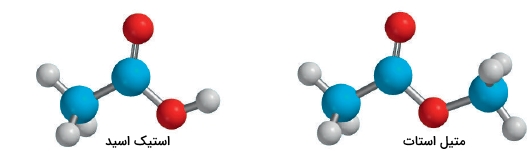
پیشنهاد میکنیم برای درک بهتر این گروه عاملی، مطلب جمع بندی فصل دوم شیمی یازدهم را مطالعه کنید.
گروه عاملی شامل نیتروژن
گروههای عاملی بسیاری وجود دارند که شامل نیتروژن هستند. یک اتم نیتروژن میتواند پیوندهای یگانه، دوگانه یا سهگانه با اتم کربن تشکیل دهد. در آمینها حداقل یک پیوند کربن-نیتروژن از نوع سیگما وجود دارد. دو پیوند دیگر سیگما مربوط به پیوند هیدروژن یا اتم کربن خواهد بود. ترکیبهایی که پیوند دوگانه کربن-نیتروژن دارند، «ایمین» (Imine) و ترکیبات با پیوند سهگانه کربن-نیتروژن، «نیتریل» (Nitirile) نام دارند.
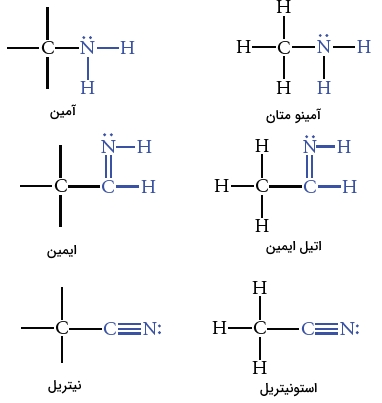
پیوند کربن-نیتروژن در آمین، به دلیل همپوشانی اوربیتالهای هیبرید نیتروژن و کربن بوجود میآید. توجه داشته باشید که طول پیوند کربن-نیتروژن از طول پیوند کربن-کربن در مولکول متان کمتر است. زاویه پیوندی در حدود 107 درجه است که مقداری نزدیک به زاویه چهاروجهی 109/5 درجه دارد.
در ایمینها، اتم کربن و نیتروژن، هردو به صورت هیبرید شده هستند. پیوندهای آنها نیز از نوع سیگما و «پای» است. در نیتریلها، اتمهای نیتروژن و کربن به صورت هیبرید شده هستند. پیوندهای سهگانه بین آنها نیز شامل یک پیوند سیگما و دو پیوند پای است.
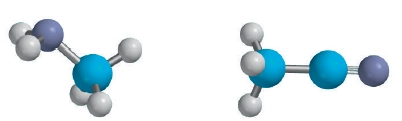
همچنین، نیتروژن در آمیدها نیز دیده میشود. در آمیدها، اتم نیتروژن با پیوند یگانه به کربن کربونیل متصل شده است. اتم نیتروژن در آمید، دو پیوند دیگر با اتمهای هیدروژن یا کربن تشکیل میدهد. ساختار آمیدها نیز همچون کربوکسیلیکاسیدها و استرها است.
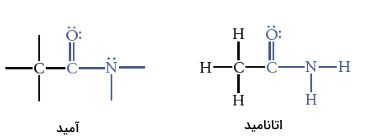
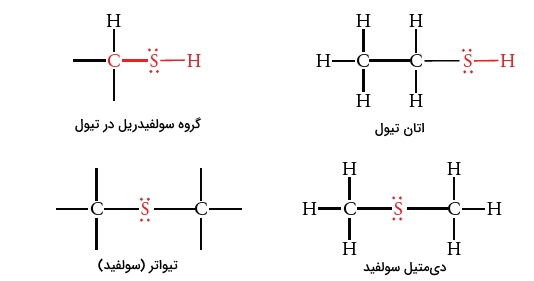
گوگرد، پیوندهایی یگانه در دو دسته از ترکیبات تشکیل میدهد: «تیولها» (Thiols) یا مرکاپتانها و «تیواترها» (Thioethers) یا سولفیدها. به گروه در تیولها، گروه سولفیدیریل میگویند. از آنجایی که گوگرد هم مانند اکسیژن، عنصری از گروه ۶ جدول تناوبی است، ساختار تیولها در ترکیبات آن مشابه الکلها است و تیواترها ساختاری همانند اترها دارند.
در جدول زیر، آنچه که در خصوص گروه عاملی گفته شد به طور خلاصه آورده شده است:
| ترکیبات آلی | گروه عاملی |
| الکلها | |
| اترها | |
| تیول | |
| آمینها | |
| آلدهیدها | |
| کتونها | |
| کربوکسیلیک اسید | |
| استر | |
| آمید | |
| هالوآلکانها |
معرفی فیلم آموزش شیمی عمومی
سینتیک شیمیایی از جمله مباحث اصلی در شیمی عمومی به شمار میرود و هم در دوره متوسطه و هم در دانشگاه به عنوان دروس پایهای به آن نگاه میشود. به همین منظور، «فرادرس» دوره آموزشی را در ۱۴ درس و بیش از ۸ ساعت تدوین کرده است که در ادامه به توضیح درسهای آن خواهیم پرداخت.
درس اول این آموزش به ساختار اتم اختصاص دارد و از جمله دروس مهم آن میتوان به ایزوتوپها، انرژی یونش، الکترونخواهی و الکترونگاتیوی اشاره کرد. در درس دوم پیوندهای شیمیایی از جمله پیوندهای یونی، کووالانسی و فلزی مورد بررسی قرار میگیرند و قاعده هشتتایی نیز در همین درس بررسی خواهد شد. ساختار هندسی مولکولها و مباحثی همچون ممان دوقطبی و هیبریداسیون در درس سوم بررسی میشوند. رفتار گازها و معادلات مربوط به گاز کامل و گازهای واقعی از مباحث مهم درس چهارم به شمار میآیند.
درس پنجم از این آموزش به فازهای مایع و جامد اختصاص دارد و محلولها در درس ششم بررسی میشوند. مباحث مربوط به ترمودینامیک از جمله قانون هس و قوانین ترمودینامیک در درس هفتم مرور خواهند شد. درس هشتم به طور ویژه به سینتیک شیمیایی میپردازد و انواع واکنشهای درجه ۱ و ۲ و قوانین دیفرانسیلی سرعت در این درس مطرح میشوند. انواع شناساگرهای اسید و باز و همچنین مباحث مربوط به اسید و باز از جمله اسیدهای قوی در درس نهم آموزش داده خواهند شد. درس دهم به تعادلهای آبی اشاره دارد و از مباحث مهم این درس باید به تیتراسیون و محلولهای بافر اشاره کرد.
از جمله مباحث مهم در شیمی، الکتروشیمی است که درس یازدهم این آموزش را شامل میشود انواع پیلهای گالوانی، سلولهای الکترولیتی و همچنین پتانسیل استاندارد الکترود در این درس مورد بررسی قرار میگیرند. روندهای تناوبی و آشنایی با هالوژنها و گازهای نجیب، سرفصلهای مهم در درس دوازدهم آموزش شیمی عمومی هستند و درس سیزدهم و چهاردهم نیز به شیمی فلزات از جمله فلزات قلیایی، واسطه و قلیایی خاکی اختصاص دارد. ساختارهای ایزومری همچون ایزومرهای فضایی و نامگذاری آنها نیز در درس چهاردم بررسی خواهند شد.
مهمترین گروههای عاملی
در شیمی آلی، 14 گروه عاملی بسیار مهم هستند که نقشی کلیدی در ترکیبات دارند. در زیر، تصویر ۱۴ گروه عاملی مهم در شیمی آلی آورده شده است:
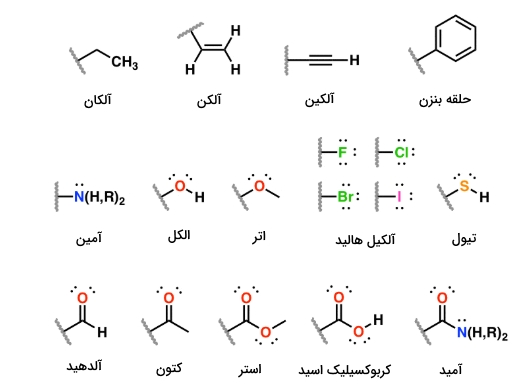
همچنین، ۸ گروه عاملی دیگر نیز وجود دارند که نسبت به ۱۴ گروه قبلی کمتر دیده میشوند اما نمیتوان از آنها چشمپوشی کرد:
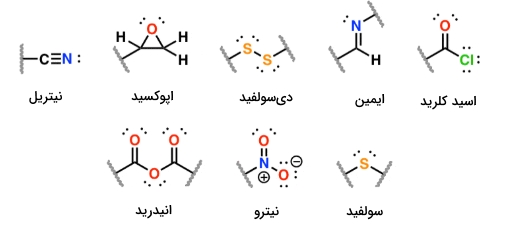
اگر این مطلب برای شما مفید بوده است، آموزشها و مطالب زیر از سایت و مجله فرادرس نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای نرمافزارهای مهندسی شیمی
- آموزش شیمی آلی ۲
- شیمی فضایی — به زبان ساده
- تبلور مواد چیست؟ — از صفر تا صد
^^











سلام اکثر گروه های عاملی که در اینجا بیان شده: تیول و بنزن و آلکیل و آلکان و آلکیل و… اصلا در کنکور مطرح نیست و اگه شکل ترکیب رو داده باشند اصلا اونهارو جز گروه های عاملی حساب نمیکنیم!
اتر.آمین.آمید.کربوکسیل.استر.کتون.آلدهید.الکل فکر میکنم کامل باشه، همینارو یاد بگیریم بسه.
با سلام؛
از ارائه بازخورد شما بسیار سپاسگزاریم. سعی بر این است که مطالب علمی را تا حد ممکن به صورت ساده اما کامل پوشش دهیم.
با تشکر از همراهی شما با مجله فرادرس
بهترین سایت در زمینه علمی، واقعا ب من کمک کرده مطالب سایت
عالی:)
ممنون
خیلی ممنون از شما. مطالب برای جمع بندی امتحانات عالی بود.