مولکول های زیستی | تعریف، انواع، ساختار و عملکرد
«مولکول زیستی» (Biomolecule) مادهای ضروری برای ادامه حیات ارگانیسمهای زنده و فعالیتهایی همچون تقسیم سلولی و فرایندهای زیستی است. در این مطلب به انواع مولکول های زیستی و ساختار و عملکرد آنها پرداختهایم.

مولکول زیستی چیست؟
موجودات زنده اغلب مولکول های زیستی مورد نیاز خود را میسازند اما برخی از انواع ضروری آنها نیز باید از طریق تغذیه دریافت شوند. بیشتر درشت مولکولها ترکیبات آلی هستند و برای ساخته شدن در بدن انسان نیاز به مواد معدنی اولیه مانند اکسیژن، کربن، هیدروژن و نیتروژن و برخی عناصر دیگر مانند دارند. درشت مولکولهای زیستی ۹۶ درصد از بدن انسان را تشکیل میدهند و نقشهای بسیار مهمی مانند تشکیل ساختارهای زیستی، ذخیره انرژی و انتقال سیگنالهایی همچون پیام عصبی را در سلولهای مختلف بر عهده دارند.
انواع مولکول های زیستی
همه موجودات زنده برای عملکردهای بیولوژیکی خود به سه بیوپلیمر (پلمیر زیستی) ضروری وابسته هستند: مولکول RNA، مولکول DNA و پروتئین. این مولکولها برای حیات ضروری هستند چون هریک از آنها نقش متمایز و ضروری را در سلول بازی میکنند. از نظر اندازه مولکول های زیستی به دستههای زیر تقسیمبندی میشوند:
- ریز مولکول یا کوچک مولکولها
- مونومرها: از یک واحد مولکولی تشکیل شده است.
- اولیگومرها: ازا تصال یک تا چند مونومر به وجود میآید.
- درشتمولکولها (ماکرومولکولها)
- پلیمرها: حاصل اتصال تعداد زیادی مونومر یکسان هستند.
- درشتمولکولهای غیر پلیمریزه: دارای وزن مولکولی بالایی هستند اما از مونومرهای یکسان تشکیل نمیشوند.
بر اساس اجزای سازنده، کوچک مولکولها عبارتند از:
- اسیدهای چرب
- گلیکولیپیدها
- استرولها
- مونوساکاریدها
- ویتامینها
- هورمونها
- نوروترانسمیترها
- متابولیتها
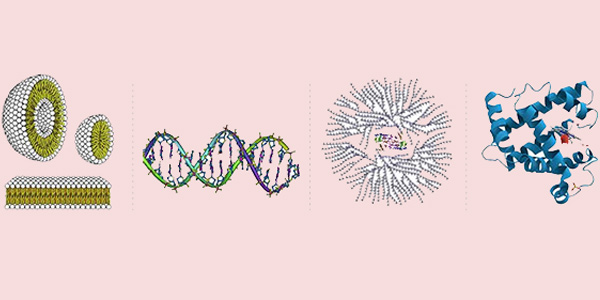
درشت مولکول چیست؟
«درشت مولکول» (Macromolecule)، یک مولکول بسیار بزرگ است که به طور معمول از پلیمریزاسیون زیرواحدهای کوچکتری به نام مونومر تشکیل شده است. درشت مولکولها از هزاران اتم یا بیشتر تشکیل شدهاند.
متداولترین درشت مولکولهای بیوشیمیایی، بیوپلیمرهایی مانند اسیدهای نوکلئیک، پروتئینها و کربوهیدراتها و مولکولهای بزرگ غیر پلیمری مانند لیپیدها و ماکروسیکلها، الیاف مصنوعی و مواد سنتتیک مثل نانولولههای کربنی هستند. بزرگ مولکولهای زیستی را میتوان به انواع مولکولهای زیر تقسیمبندی کرد:
- پروتئینها
- کربوهیدراتها
- لیپیدها
- نوکلئید اسیدها
تفاوت پلیمر و درشت مولکول چیست؟
انواع پلیمرها در واقع یکی از زیرگروههای درشت مولکول محسوب میشوند. در علم شیمی به هر مولکولی که تعداد اتمهای تشکیل دهنده، وزن مولکولی و جرم مولکولی بالایی داشته باشد درشتمولکول گفته میشود که بر اساس نوع واحدهای تشکیل دهنده آن، میتواند پلیمریزه مانند سلولز یا غیر پلیمریزه مانند لیپیدها باشد.

ویژگی درشت مولکول ها چیست؟
درشت مولکولها خصوصیات فیزیکی غیرمعمولی دارند که در مولکولهای کوچکتر دیده نمیشود. یکی دیگر از خصوصیات رایج درشت مولکولها، عدم حلالیت نسبی آنها در آب و حلالهای مشابه است اما کلوئید تشکیل میدهند. بسیاری از آنها برای حل شدن در آب به نمک یا یونهای خاص احتیاج دارند.
غلظت زیاد درشت مولکولها در یک محلول میتواند از طریق تاثیری که به عنوان ازدحام درشت مولکولی شناخته میشود سرعت و ثابت تعادل واکنشهای دیگر را تغییر دهد چون به دلیل اندازه بزرگ، مولکولهای دیگر را از قسمت زیادی از حجم محلول حذف میکنند در نتیجه غلظت موثر این مولکولها افزایش مییابد.
نوکلئوزیدها و نوکلئوتیدها
نوکلئوزیدها مولکولهای زیستی هستند که از اتصال نوکلئوبازها به یک قند ریبوز یا دئوکسی ریبوز تشکیل میشوند. برخی از آنها عبارتند از:
- «سیتیدین» (Cytidine)
- «یوریدین» (Uridine)
- «آدنوزین» (Adenosine)
- «گوانوزین» (Guanosine)
- «تیمیدین» (Thymidine)
نوکلئوزیدها را میتوان با کینازهای خاص در سلول فسفریله و نوکلئوتید تولید کرد. DNA و RNA هر دو پلیمر هستند و از مولکولهای خطی با طول بلند و توسط آنزیمهای پلیمراز از واحدهای ساختاری تکرار شده یا مونومرهای مونونوکلئوتیدها تشکیل شدهاند. DNA از دیاُکسینوکلئوتیدهای C ،G ،A و T استفاده میکند، در حالی که RNA از ریبونوکلئوتیدها (که یک گروه اضافی هیدروکسیل (OH) روی حلقه پنتوز دارند) C ،G ،A و U استفاده میکند.
بازهای اصلاح شده به نسبت رایج هستند (مانند با گروههای متیل روی حلقه پایه)، همانطور که در RNA ریبوزومی یا RNAهای انتقال یافته یا برای تمایز رشتههای جدید DNA از رشتههای DNA پس از تکثیر، یافت میشود. هر نوکلئوتید از یک باز نیتروژنی حلقوی، یک قند پنتوز و ۳ گروه فسفات تشکیل شده است. این ساختارها دارای عناصر کربن، نیتروژن، اکسیژن، هیدروژن و فسفر هستند.
این ترکیبات در غالب آدنوزین تریفسفات و گوانوزین تریفسفات، به عنوان منبع انرژی، در انتقال پیام یا سیگنالینگ به عنوان گواتنوزین مونوفسفات حلقوی (GMP) و آدنوزین مونوفسفات حلقوی (AMP) عمل میکنند. همچنین، کوفاکتورهای مهمی در عملکرد آنزیمهای شرکت دارند که از آن جمله میتوان به موارد زیر اشاره کرد:
- کوآنزیم آ
- فلاوین آدنین دینوکئوتید (FAD)
- فلاوین مونونوکلئوتید (FMN)
- نیکوتین آمید آدنین دینوکلئوتید فسفات (NADPH)
ساختار RNA و DNA
ساختار DNA از یک مارپیچ دوتایی تشکیل شده است که با اتصال بازها بر اساس قانون «واتسون-کریک» (Watson-Crick)، به صورت اتصال باز C با G و باز A با T شکل میگیرد. این نوع ساختار به عنوان DNA شکل B شناخته میشود و مطلوبترین و رایجترین حالت DNA است. چهارچوب خاص و پایدار آن اساس ذخیره اطلاعات ژنتیکی محافظت شده هستند.
DNA میتواند به صورت تکرشتهای (که غالباً نیاز به تثبیت پروتئینهای متصل به یک رشته دارد) یا به صورت مارپیچهای A یا Z و گاهی اوقات در ساختارهای سه بعدی پیچیدهتر و ناشی از فرایندی به نام «کراسینگاور» (Crossing Over) در اتصالات هالیدی هنگام تکثیر و همانندسازی DNA وجود داشته باشد. کراسینگاور فرایندی است که حین تقسیم میوز رخ میدهد و طی آن دو کروموزوم هومولوگ (همسان) با یکدیگر ادغام میشوند و حاصل آن تنوع زیستی است.
در مقابل، RNAها ساختارهای بزرگ و پیچیده سه بعدی و مشابه پروتئینها و رشتههای منفرد با مناطق تا شده محلی هستند که مولکولهای RNA پیامرسان (mRNA) را تشکیل میدهند. این نوع RNA حاوی بخشهای زیادی از مارپیچ A است که توسط حلقه های تک رشتهای، لوپها و اتصالات به آرایش سهبعدی مشخص متصل میشوند. به عنوان مثال میتوان به tRNA، ریبوزوم، ریبوزیم و ریبوسویچ اشاره کرد. این ساختارهای پیچیده با این واقعیت تسهیل میشوند.
ساختار RNA دارای انعطافپذیری موضعی کمتری نسبت به DNA است اما یک مجموعه بزرگ از ساختارهای مشخص، ظاهرا به دلیل فعل و انفعالات مثبت و منفی گروه هیدروکسیل اضافی روی قند ریبوز است. مولکولهای ساختاریافته RNA میتوانند اتصال بسیار خاصی از سایر مولکولها را انجام دهند و به طور خاص شناخته شوند. علاوه بر این، تجزیه و تحلیل آنزیمی را هم انجام میدهند (زمانی که به عنوان ریبوزیم شناخته میشوند، همانطور که در ابتدا توسط تام چک و همکارانش کشف شد).

ساکاریدها
ساکاریدها (Saccharides) ساکاریدها ترکیبات آلی هستند که از سه عنصر کربن، هیدروژن و اکسیژن تشکیل شدهاند. از نظر ساختار شیمیایی، پلیمر کربوهیدراتها از پلی هیدروکسی آلدئیدها، کتونها یا پلیمرهای آنها ساخته میشوند. ساکاریدها بر اساس تعداد واحدهای به کار رفته در آنها، به سه دسته مونوساکاریدها، اولیگوساکاریدها و پلیساکاریدها تقسیم میشوند که در ادامه انواع آنها را توضیح دادهایم. کربوهیدراتها سه عملکرد دارند:
- تولیدکننده انرژی: مانند گلوکز و ATP
- نقش ذخیرهای: مانند گلیکوژن
- عملکرد ساختاری: مانند سلولز و پکتین
مونوساکارید چیست؟
مونوساکاریدها فقط با یک قند ساده و منفرد و از سادهترین نوع کربوهیدرات هستند و در ساختار خود یک گروه آلدهید یا کتون دارند. حضور یک گروه آلدهید در یک مونوساکارید با پیشوند «آلدو» نشان داده و به همین ترتیب، یک گروه کتونی با پیشوند «کتو» نشان داده می شود.
مونوساکاریدها بر اساس تعداد کربن به کار رفته در آنها انواع مختلفی دارند به عنوان مثال میتوان به هگزوزها، گلوکز، فروکتوز، تریوزها، تتروزها، هپتوزها، گالاکتوز، پنتوزها، ریبوز و دئوکسیریبوز اشاره کرد. فروکتوز و گلوکز مصرفی میزان تخلیه معده متفاوتی دارند، به طرز متفاوتی جذب میشوند و سرنوشت متابولیکی متفاوتی دارند و فرصتهای مختلفی را برای دو ساکارید مختلف فراهم میکند تا تأثیر متفاوتی بر مصرف غذا بگذارد. بیشتر ساکاریدها سرانجام سوخت را برای تنفس سلولی تأمین میکنند.
دی ساکارید چیست؟
دیساکاریدها از اتصال دو مونوساکاریدها مانند دو قند ساده با حذف و آزاد شدن یک مولکول آب، تشکیل میشوند. برای تجزیه دیساکاریدها به واحدهای سازنده آنها، میتوان از جوشاندن آنها در اسید رقیق یا واکنش آنها با آنزیمهای تجزیه کننده، استفاده کرد. نمونههایی از دیساکاریدها شامل ساکارز، مالتوز و لاکتوز هستند.
پلی ساکارید چیست؟
پلی ساکاریدها پلیمرهای ساخته شده از واحدهای مونوساکاریدی و کربوهیدراتهای پیچیدهای هستند. آنها چندین قند ساده دارند که به عنوان مثالی از پلیساکاریدها میتوان نشاسته، سلولز و گلیکوژن را نام برد. این ترکیبات آلی اندازه بزرگی دارند و اغلب دارای انشعابات پیچیده شاخهای هستند. به دلیل اندازه بزرگ، پلیساکاریدها در آب محلول نیستند اما گروههای جانبی آنها در صورت باردار بودن، طوری جهت گرفتهاند که در تماس با مولکولهای آب قرار بگیرند.
به طور مثال، گروههای هیدروکسی و آبدوست پلیساکاریدها هیدراته میشوند و برخی از پلی ساکاریدها در هنگام گرم شدن در آب نیز پراکندگی کلوئیدی ضخیمی ایجاد میکنند. پلیساکاریدهای کوچکتر، با 3 تا 10 مونومر، الیگوساکارید نامیده میشوند. یک مولکول جایگزیتشده با نشانگر فلوئورسنت برای تمایز ساکاریدها ساخته شده است که توانست سه نوع محلول ساخته شده از سه نوع مونوساکارید مختلف را شناسایی کند. تغییر در شدت فلورسانس فیلمهای سنجشی حاصل، با غلظت ساکارید مورد بررسی ارتباط مستقیم دارد.
لیگنین چیست؟
«لیگنین» (Lignin) بعد از سلولز، رایجترین ماده موجود در گیاهان چوبی و غیر چوبی است که در دیواره سلول گیاهی قرار دارد. این پلیمر بین سلولز، همیسلولز و پکتین بیشترین نقش را در تحکیم دیواره سلولی ایفا میکند و از واحدهای مولکولی فنیلپروپان ساخته شده است. لیگنین از نظر ساختار شیمیایی یک درشت مولکول پلیفنلی پیچیده است. ترکیب تشکیلدهنده لیگنین از گونهای به گونه دیگر تفاوت دارد.
به طور مثال در ترکیبات موجود در نمونه درخت صنوبر، دارای 63/4 درصد کربن، 5/9 درصد هیدروژن، 0/7 درصد خاکستر (اجزای معدنی) و 30٪ اکسیژن دارد. لیگنین به عنوان یک پلیمر، به دلیل ناهمگنی و نداشتن ساختار اولیه مشخص غیرمعمول است. این ماده حاوی زیرواحدهای مشتق شده از الکل p-کوکرامیل، کنیفریل الکل (Coniferyl Alcohol) و سیناپیل الکل (Sinapyl Alcohol) است. عدم فعالیت نوری به دلیل پلیمریزاسیون لیگنین است که از طریق واکنشهای اتصال رادیکالهای آزاد رخ میدهد و در آن هیچ ارجحیتی برای دو پیکربندی، در مرکز کایرال وجود ندارد.
عملکرد اصلی لیگنین، پشتیبانی از طریق تقویت چوب (سلولهای آوند چوبی و الیاف اسکلرانشیم) در گیاهان عروقی است. لیگنین نقش مهمی در هدایت آب در ساقه های گیاه دارد. اجزای پلی ساکارید دیواره سلولهای گیاهی بسیار آبدوست بوده و در نتیجه به آب نفوذ میکنند، در حالی که لیگنین بیشتر آبگریز است. اتصال عرضی پلیساکاریدها توسط لیگنین مانعی برای جذب آب در دیواره سلول است. بنابراین این امکان را برای بافت آوندی فراهم میکند که بتواند آب را به طور موثر هدایت کند.
لیگنین در همه گیاهان عروقی به جز بریوفیتها (خزهها) وجود دارد که نشان میدهد عملکرد اصلی لیگنین به حمل و نقل آب محدود شده است. بریوفیتها گیاهان فاقد گل، برگ، ساقه و ریشه هستند که با اسپور تولید مثل میکنند. به نظر میرسد که در جد مشترک گیاهان و جلبکهای قرمز نیز لیگنین سنتز میشده و این نشان میدهد که عملکرد آن ساختاری بوده است.

لیپیدها
لیپیدها عموما استرهای اسید چرب و عناصر اصلی سازنده غشاهای بیولوژیک هستند. نقش بیولوژیکی دیگر آنها، به عنوان مثال در مورد تریگلیسیریدها، ذخیره انرژی در سلول است. بیشتر لیپیدها از یک سر قطبی یا آبدوست (هیدروفوب) که به طور معمول گلیسرول است و یک تا سه دم اسید چرب غیر قطبی یا آبگریز تشکیل شدهاند و بنابراین آمفیفیلیک هستند.
اسیدهای چرب متشکل دو نوع زنجیرههای غیر منشعب کربنی هستند که با پیوندهای منفرد (در اسیدهای چرب اشباع) یا پیوندهای یگانه و دوگانه (در اسیدهای چرب اشباع نشده) به هم متصل میشوند. این زنجیرهها به طور معمول 14 تا 24 کربن دارند و تعداد کربن در آنها همیشه یک عدد زوج است. سرهای آبدوست چربیهای موجود در غشاهای بیولوژیکی، در سه شکل سازمان یافته اند:
- گلیکولیپیدها: که سر آنها حاوی یک الیگوساکارید با 1 تا 15 باقیمانده ساکاریدی است.
- فسفولیپیدها: که آنها گروهی با بار مثبت دارد و توسط یک گروه فسفات با بار منفی به دم مرتبط میشود.
- استرولها: سر دارای یک حلقه استروئیدی مسطح است. به عنوان مثال، کلسترول از جمله استرولها به حساب میآید.
- پروستاگلاندینها و لکوترینها: هر دو واحد استیل چرب آنها 20 کربنی هستند و از اسید آراشیدونیک ساخته شدهاند. این چربیها همچنین به عنوان اسیدهای چرب هم شناخته میشوند.
پروتئین ها
توالی اسیدهای آمینه سازنده پروتئین، ساختار اولیه پروتئین است که با کدهای ژنتیکی تعیین میشود. این ترتیب گروههای زنجیرهای جانبی را در امتداد ستون فقرات پلیپپتیدی و خطی مشخص میکند. پروتئینها دارای دو نوع ساختار طبقهبندی شده و غالباً متشکل از ساختار محلی هستند که توسط الگوی خاصی از پیوندهای هیدروژنی در امتداد توالی اسیدآمینهای تعریف شدهاند. تعداد و سازمانیابی ساختارهای اولیه در کنار یکدیگر، ساختار ثانویه پروتئین را میسازند و دو نوع دارند:
- مارپیچ آلفا: مارپیچی منظم است که توسط پیوندهای هیدروژنی بین گروه کربونیل (CO) یک باقیمانده اسید آمینه و گروه آمید (NH) باقیمانده شماره «i + 4» تثبیت میشود. مارپیچ آلفا در هر ردیف حدود ۳/۶ آمینو اسید دارد و زنجیرههای جانبی اسیدهای آمینه از استوانه مارپیچ بیرون زدهاند.
- صفحات بتا: ورقهای چیندار بتا، توسط پیوندهای هیدروژنی ستون فقرات بین رشتههای بتای منفرد تشکیل میشوند که هرکدام از آنها در یک ساختار گسترش یافته یا کاملاً کشیده قرار دارند. رشتهها به موازات یکدیگر یا در جهت مخالف قرار میگیرند و جهت زنجیره جانبی در بالا و پایین ورق متناوب باشد. یکی از پروتئینها با ساختار بتا، فقط مارپیچ آلفا دارد. ابریشم طبیعی از ورقهای چیندار بتا تشکیل میشود و بسیاری از آنزیمها هم مارپیچهای متناوب و هم رشتههای بتا دارند. ساختارهای ثانویه توسط لوپها یا مارپیچها با ترکیب غیر تکراری یکدیگر متصل میشوند که گاهی اوقات کاملاً بینظم هستند اما به طور معمول ترتیب پایدار و مشخصی دارند.
ساختار کلی، فشرده و سه بعدی پروتئین، ساختار سوم آن نامیده میشود. ساختار سهبعدی در نتیجه نیروهای مختلف مانند پیوند هیدروژنی، پلهای دی سولفیدی، فعل و انفعالات آبگریز و آبدوست، نیروهای واندروالس ایجاد میشود. هنگامی که دو یا چند زنجیره پلیپپتیدی (با توالی یکسان یا متفاوت) با یکدیگر مرتبط باشند، ساختار چهارم پروتئین تشکیل میشود. یکی مثال از پروتئینی با ساختار چهارم، هموگلوبین با دو زنجیره پلیپپتیدی آلفا و دو ساختار بتا است. به دلیل وجود ۲۱ اسید آمینه مختلف و تنوعی که در اتصال این اسیدآمینهها وجود دارد، پروتئینهای مختلف و پیچیدهای وجود دارند.
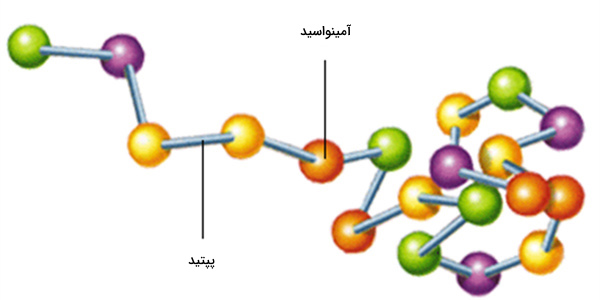
آمینواسید چیست؟
اسیدهای آمینه یا آمینواسیدها، مولکول های زیستی حاوی دو گروه عملکردی اسید آمینه و کربوکسیلیک اسید هستند. در بیوشیمی، اصطلاح اسید آمینه، هنگام اشاره به اسیدهای آمینهای گفته میشود که در آنها گروههای عملکردیِ آمین و کربوکسیلات به کربن یکسانی متصل شده باشند همچنین به پرولین که در واقع یک اسید آمینه نیست. اسیدهای آمینه تغییریافته نیز در پروتئیینها مشاهده میشوند که ایجاد آنها نتیجه اصلاح آنزیمی پس از ترجمه (سنتز پروتئین) است.
به عنوان مثال، فسفوریلاسیون اسیدآمینه سرین توسط کینازها و دفسفریلاسیون آنها توسط فسفاتازها که یک مکانیسم کنترلی مهم در چرخه سلولی است. در برخی موجودات دو اسید آمینه غیر از 20 اسید آمینه استاندارد، هنگام ترجمه در ساختار پروتئینها وجود دارند که عبارتند از:
- سلنوسیستئین: در برخی از پروتئینها کدون UGA، که به طور معمول کدون توقف است، وجود دارد.
- پیرولیزین: در کدون «UAG» برخی پروتئینها، به عنوان مثال در برخی از متانوژنها (آنزیمهای دخیل در تولید متان) دیده میشود.
علاوه بر اسید آمینههای استاندارد، سایر آمینواسیدهای مهم بیولوژیکی شامل موارد زیر هستند:
- کارنیتین: در انتقال لیپید در سلول نقش دارد.
- اورنیتین: از اسیدآمینه آرژنین سنتز میشود و در چرخه اوره دخیل است.
- GABA: گاما آمینو بوتیریک اسید، مهمترین انتقال دهند عصبی مهاری در سیستم عصبی مرکزی است و نقش مهمی در هماهنگی شبکههای عصبی موضعی و عملکرد نواحی مغزی دارد.
- تورین: تورین یا تائورین از متابولیتهای لوسین است.
آپوآنزیم چیست؟
«آپوآنزیم» (Apoenzyme) یا به طور کلی آپوپروتئین، پروتئینی بدون هیچ کوفاکتور، سوبسترا یا مهارکننده است که غالباً به عنوان ماده ذخیرهای، انتقالی یا شکل ترشحی و غیر فعال پروتئین عمل میکند. این مورد برای مثال برای محافظت از سلول ترشحی در برابر فعالیت آن پروتئین لازم است.
آپوآنزیمها با افزودن یک فاکتور به آنزیمهای فعال تبدیل میشوند. کوفاکتورها میتوانند از جمله مولکولهای غیرآلی مانند یونهای فلزی و خوشههای گوگرد، آهن یا ترکیبات آلی مانند گروه فلاوین باشند. کوفاکتورهای آلی میتوانند گروههای مصنوعی باشند که به آنزیم متصل شدهاند یا کوآنزیمهایی که در طی واکنش از جایگاه فعال آنزیم آزاد میشوند.
ایزوآنزیم چیست؟
ایزوآنزیمها یا ایزوزیمها، اشکال از آنزیمها با توالی پروتئینی کمی متفاوت و عملکردهای مشابه هستند. این مولکول های زیستی یا محصولاتی از چند ژن مختلف هستند یا حاصل پردازش متفاوت پس از رونویسی هستند. آنها ممکن است در اندامهای مختلف یا سلولهای مختلف برای انجام عملکرد یکسان تولید شوند یا چندین نوع ایزو آنزیم تحت تنظیمات متناسب با نیازهای رشدی یا محیط در همان نوع سلول تولید شوند.
LDH (لاکتات دهیدروژناز) دارای چندین ایزوآنزیم است، در حالی که هموگلوبین جنینی، مثالی از ایزوفرم تنظیم شده بر رشد از پروتئین غیر آنزیمی است. از سطح نسبی ایزوآنزیمها در خون میتوان برای تشخیص مشکلات موجود در اندام استفاده کرد.
مولکول های زیستی سنتتیک
بیومولکولهای مصنوعی برای سنتز پپتیدهای ویژه و اختصاصی به کار میروند. با تقریباً دو دهه تجربه تولید و استفاده از پپتیدها، بیومولکولهای مصنوعی میتوانند به سرعت پپتیدهای مصنوعی را با ارزشی که در صنعت بینظیر است تولید کنند و در اختیار به مصرفکنندگان بگذارند. پلیمرهای مصنوعی باید با بدن ما سازگار باشند که به آن «زیستسازگاری» گفته میشود به این معنی که بدون آسیب رساندن به بافت زنده یا ایجاد واکنشهای آلرژیک یا عوارض جانبی ناخواسته قابل استفاده باشند.

مدل سازی مولکول های زیستی
مدلسازی چند حالته از بیومولکولها به مجموعه تکنیکهایی گفته میشود که برای نشان دادن و محاسبه رفتار مولکول های زیستی یا کمپلکسهای مولکولی استفاده میشوند که میتوانند تعداد زیادی از حالتهای عملکردی ممکن آنها را داشته باشند. سیستمهای سیگنالینگ بیولوژیکی غالباً به مجموعهای از درشت مولکولها متکی هستند که چندین عملکرد مهم را به صورت همراستا انجام دهند و با یکدیگر سازگار هستند، بنابراین حالتهای مختلف عملکردی دارند. مدلسازی چنین سیستمهای چند حالته دو مشکل ایجاد میکند:
- نحوه توصیف و مشخص کردن یک سیستم چند حالته
- نحوه استفاده از رایانه برای شبیهسازی پیشرفت سیستم در طول زمان
در سلولهای زنده، سیگنالها توسط شبکه پروتئینی پردازش میشوند و میتوانند به عنوان دستگاههای محاسباتی پیچیده عمل کنند. این شبکهها، برای وجود حالتهای مختلف عملکردی که از طریق مکانیزمهای متعدد از جمله تغییرات پس از ترجمه، اتصال لیگاند، تغییر ساختار و یا تشکیل مجتمعهای جدید متکی هستند، ٰبه توانایی پروتئینها نیازمند هستند. به همین ترتیب، اسیدهای نوکلئیک میتوانند تحت تحولات مختلفی از جمله موارد زیر قرار بگیرند:
- اتصال پروتئین
- اتصال به اسیدهای نوکلئیک
- تغییر ساختار
- متیلاسیون DNA
علاوه بر این، امکان وجود انواع تغییرات وجود دارد که در هر زمان تأثیر متفاوتی بر درشت مولکول بیولوژیکی اعمال میکنند. بنابراین، مجموعهای از مولکول های زیستی اغلب میتوانند عملکردهای بسیار متنوع و متفاوتی داشته باشند. تعداد حالات به طور نمایی با تعداد تغییرات ممکن قابل قیاس است که به عنوان «انفجار ترکیبی» شناخته میشود. این موضوع باعث نگرانی محققان است که چنین مولکول های زیستی را مدلسازی یا شبیهسازی میکنند و این سؤال مطرح است که چه تعداد از این حالتها قابل شبیهسازی هستند.
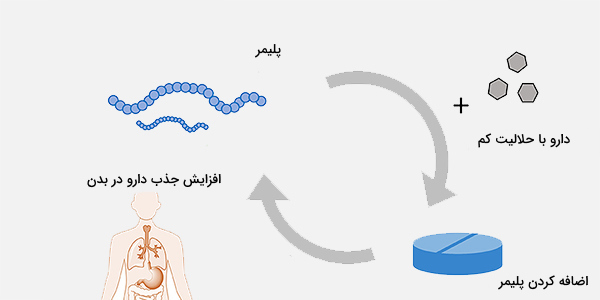
استفاده از پلیمرها در داروسازی
پلیمرها به عنوان یکی از انواع مولکول های زیستی میتوانند به جذب بهتر داروها کمک کنند. به طور مثال، برخی داروها به راحتی حل نمیشوند اما با پوشانده شدن در پلیمرهای ویژه، به حل شدن دارو در بدن بیمار کمک میکنند. از طرف دیگر برخی داروها به سرعت با اسید معده یا بزاق دهان تجزیه و جذب میشوند، اما در صورت استفاده از پلیمرها به عنوان پوشش، دارو با سرعت مناسبی جذب و در جریان خون آزاد خواهد شد.
به عنوان مثال، دارویی به نام نیفدیپین برای درمان فشار خون بالا برای حدود 1 میلیارد نفر از افراد مبتلا به این بیماری در سراسر جهان کاربرد دارد اما خبر بد این است که نیفدیپین معمولاً زمان کافی برای حل شدن در معده ندارد و قبل از جذب کامل، از بدن دفع میشود. از پلیمری به نام «پلی وینیل پیرولیدون» برای تقویت توانایی حل شدن نیفدیپین در معده استفاده میشود که جذب و ورود دارو به خون را سرعت میبخشد. این فقط یک نمونه از اثرات مثبت استفاده از مولکول های زیستی بر سلامت انسان است.
پلیمرهای مصنوعی که در کاشت استخوانهای شکسته یا داروها استفاده میشوند، به گونهای طراحی شدهاند که به مرور در بدن به قطعات کوچکتری تقسیم شوند و سلولها بتوانند آنها را به صورت طبیعی پردازش کنند و به همین دلیل پلیمرهای تجزیهپذیر نام دارند. یک کلاس از پلیمرهای قابل تجزیه، پلی استرهایی هستند که در موارد بیشماری پزشکی مانند مفاصل مصنوعی، پیچها، پینها و صفحات به کار رفته برای پشتیبانی از ترمیم استخوانهای شکسته و نگه داشتن آنها به کار میروند.













عالی و جامع
خیلی ممنون!:)
خوبه ولی به آسانی در دسترس نیست.