ویژگی خطوط رامان – تفسیر طیف + مثال – به زبان ساده
ویژگی خطوط رامان به دست آمده از این روش طیف سنجی، در مورد ترکیبات شیمیایی معدنی و آلی اطلاعات مفیدی ارائه میدهد. اطلاعات بهدست آمده از خطوط رامان این امکان را میدهد که طیفسنجی رامان نسبت به طیفبینی فروسرخ، تفکیک فضایی بهتر و آنالیز ابعاد کوچکتری را داشته باشد. از ویژگی خطوط رامان برای تأیید ساختار و شناسایی مولکولها استفاده میشود. در این تکنیک ارتعاشات مولکولی شامل کششی، خمشی و چرخشی ثبت و بررسی میشود. طیفسنجی رامان و فروسرخ دو تکنیک مکمل در شناسایی ترکیبات هستند. در ادامه مطلب با طیف ترکیبات گوناگون در طیفسنجی رامان آشنا خواهید شد.
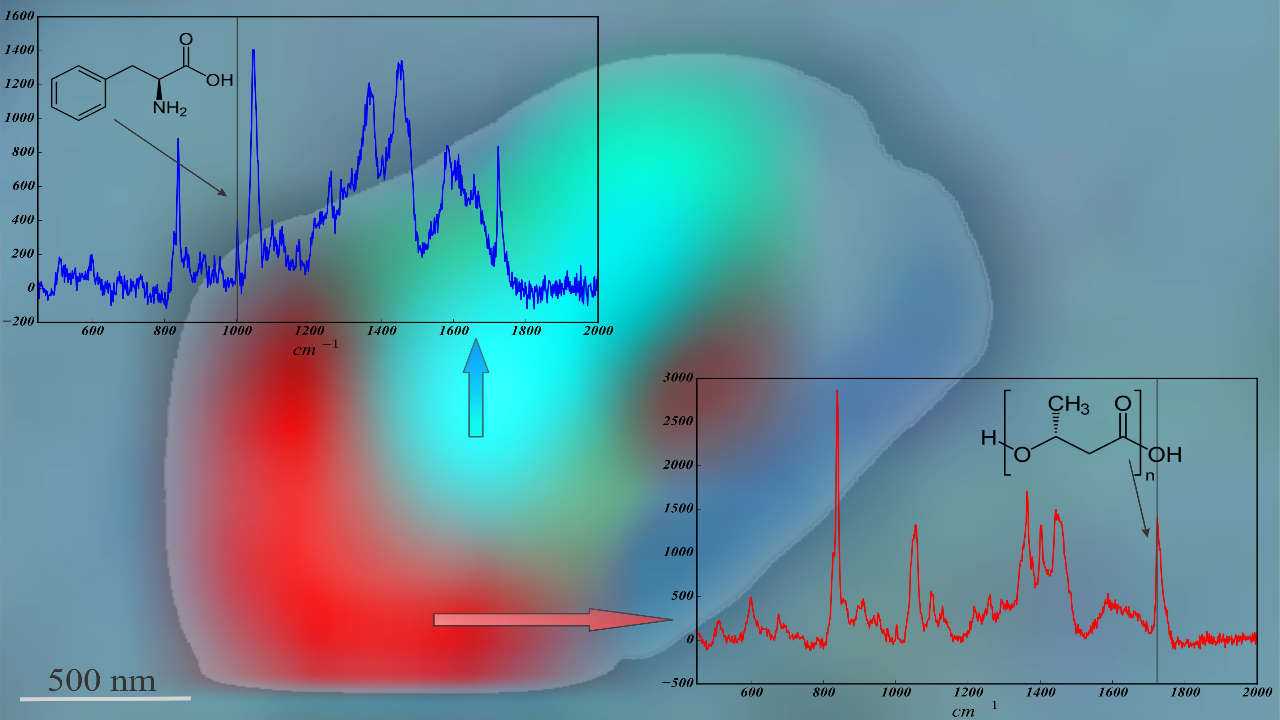
ویژگی خطوط رامان چیست ؟
شدت و نوع خطوط و همچنین چگونگی و شرایط ایجاد آنها ازجمله ویژگی خطوط رامان هستند. از این ویژگی خطوط رامان و اطلاعاتی که از اندازهگیری نمونه بهدست میآید میتوان خواص شیمیایی، ساختاری و فیزیکی ترکیبات مختلف را تعیین کرد.
وقتی منبع نور قدرتمندی مانند لیزر به نمونهای برخورد میکند، در نتیجه برخوردهای ذرات تشکیلدهنده پرتوهای نور و نمونه، یعنی فوتونها با مولکولها، پرتوهای نور به روشهای مختلفی بازتابیده و پراکنده میشوند. بهطور معمول، بیشتر پرتوهای نور بازتابی بدون تغییر انرژی و طول موج به صورت کشسان پراکنده میشوند که به آنها پراکندگی رایلی گفته میشود. پراکندگی رایلی بدون تغییر انرژی در مولکولها همراه است. به همین دلیل در طیفسنجی رامان حذف میشود.
تخمین زده شده است که از میان هر یک میلیون پرتو پراکنده شده، تنها یک پرتو، انرژی و طول موجی متفاوت دارد. به این دسته از پرتوها که نتیجه برخوردهای ناکشان فوتونها و مولکولهای نمونه هستند، پراکندگی رامان میگویند که به دو دسته «استوکس» (Stokes) و «آنتیاستوکس» (anti-Stokes) تقسیم میشود.
با دریافت انرژیِ فوتون، مولکول مدت بسیار کوتاهی به سطح بالاتر انرژی منتقل میشود و در بازگشت به سطح پایدار، انرژی آزاد میکند. به این حالت بالاتر انرژی، حالت مجازی میگویند. حالت مجازی انرژی حالتی ناپایدار است و مولکول بلافاصله به حالت پایدار خود باز میگردد. انرژی مولکول میتواند به شکلهای زیر باشد.
- حرکت الکترونها در مولکول
- ارتعاشات اتمهای تشکیلدهنده مولکول
- چرخش مولکول
فرایند پراکندگی را میتوان به صورت جذب و پراکنده شدن فوتون در نظر گرفت. مراحل پراکندگی فوتونهایِ نور توسط مولکول به شرح زیر است.
- سیستم از حالت الکترونی و ارتعاشیِ پایه به سطح مجازی منتقل میشود.
- سیستم میتواند از سطح مجازی به حالت پایه انرژی ارتعاشی بازگردد. بازگشت سیستم به این سطح با تابش فوتون همراه است و فرکانس فرودی و تابشی برابر خواهد بود که خطوط رایلی را ایجاد میکنند.
- سیستم میتواند از سطح مجازی به اولین حالت انرژی ارتعاشی بازگردد، در این حالت فرکانسِ پرتو تابشی برابر با خواهد بود که خطوط استوکس را ایجاد میکنند.
- اگر مولکول از اولین حالت انرژیِ ارتعاشی به حالت مجازی منتقل شود و به حالت ارتعاشی پایه بازگردد، فرکانسِ پرتو تابشی برابر با خواهد بود که خطوط آنتیاستوکس را ایجاد میکنند.
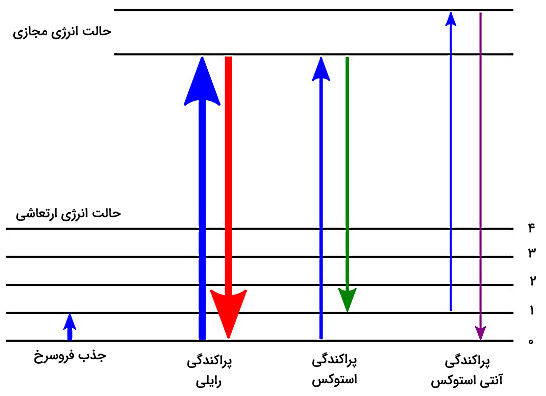
در این حالت مولکول یا انرژی جذب میکند یا انرژی از دست میدهد که نتیجه این تبادل انرژی به صورت خطوط رامان زیر است:
- استوکس: اگر مولکول انرژی جذب کند؛ انرژی فوتونِ بازتابی کاهش پیدا می کند، پس فرکانس کمتر و طول موج بیشتری دارد.
- آنتیاستوکس: اگر مولکول انرژی آزاد کند؛ انرژی فوتونِ بازتابی افزایش پیدا می کند، پس فرکانس بیشتر و طول موج کمتری دارد.
پراکندگی رامان استوکس
پراکندگی رامان استوکس زمانی رخ میدهد که مولکول هنگام پراکندگی و برخورد با فوتون، انرژی دریافت کند. در این حالت مولکول به سطح ارتعاشی بالاتر میرود و فوتون پراکنده شده با از دست دادن انرژی همراه است. با کاهش انرژیِ فوتون طول موج آن افزایش و فرکانس کاهش پیدا میکند. مقداری انرژی که از فوتون به مولکول منتقل میشود دقیقاً با انرژی مورد نیاز برای برانگیختگیِ یکی از ارتعاشات مولکولی برابر است. به همین دلیل نور پراکنده شده به نوع دقیق مولکول بستگی دارد.
پراکندگی رامان آنتی استوکس
پراکندگی رامان آنتیاستوکس مانند رامان استوکس از فرآیندهای پراکندگی غیر کشسان است. در این پراکندگی هنگام برخورد فوتونها با مولکول، مقدار مشخصی از انرژیِ ارتعاشی مولکول به فوتون منتقل میشود. با افزایش انرژی فوتون طول موج کاهش و فرکانس آن افزایش پیدا میکند. احتمال رخ دادن این فرایند زیاد نیست و معمولاً در طیفسنجی رامان خیلی کمتر استفاده میشود.
قطبشپذیری در پراکندگی رامان
در پراکندگی رامان، برخورد فوتونهای نور و تعامل میدان الکتریکی این ذرات امواج الکترومغناطیسی با ابر الکترونی مولکول باعث جابهجایی و تغییر شکل آنها میشود. نتیجه این جابهجایی الکترونها، القای گشتاور دوقطبی در مولکول است. این حالت که تنها حدود ثانیه طول میکشید ساختار هندسی مولکول را تغییر نمیدهد و تنها موجب ایجاد تغییر شکل و قطبش در ابر الکترونی مولکول میشود.
میزان گشتاور دوقطبی به انرژی میدان الکتریکی فوتون و قطبش ایجاد شده رابطهای مستقیم دارد که از معادله زیر بهدست میآید.
- : گشتاور دوقطبی القا شده
- : انرژی میدان الکتریکی
- : ثابت قطبشپذیری پیوند
در واقع، تغییر قطبشپذیری پیوند، شرط فعال بودن پیوندی در طیفسنجی رامان و معیاری از میزان شکلپذیری پیوند در میدان الکتریکی است. به همین دلیل طیفسنجی رامان نسبت به ساختار مولکولی حساسیت بیشتری دارد.
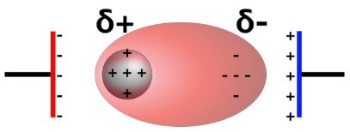
برای مثال؛ گشتاور دوقطبی الکتریکی مولکول دواتمی که از دو اتم یکسان تشکیل شده و هسته در موقعیتی متعادل قرار دارد برابر صفر است. اگر به این مولکول میدانی الکتریکی اعمال شود، ابر الکترونی و هستهها در جهت مخالف حرکت میکنند و مولکول دچار خمیدگی یا پیچش میشود. در حقیقت جابهجایی بار موجب ایجاد گشتاور دوقطبی الکتریکی در مولکول میشود که با شدت میدان الکتریکی متناسب است.
ثابت تناسب یا ، قطبشپذیری مولکول نام دارد که بهطور کیفی انحراف ابر الکترونی مولکول را نشان میدهد. در ریاضی بین بردار گشتاور دوقطبی القایی و بردار میدان الکتریکی به دلیل تأثیر جهت پیوندهای شیمیایی بر قطبش مولکول و بررسی تغییرات ابر الکترونی در جهات مختلف فضا تناسب سادهای ندارد.
جابه جایی رامان چیست ؟
برخورد فوتونها و مولکولها با تبادل انرژی بین آنها همراه است و در نتیجه آن، طول موجِ فوتونهای پراکنده شده تغییر میکند. «جابهجایی رامان» (Raman Shift) تفاوت انرژی نور تابیده شده و نور پراکنده شده است. این جابهجایی به شکل استوکس و آنتیاستوکس است.
در طیفسنجی رامان، جابهجایی به جای طول موج به صورت عدد موج گزارش میشود. عدد موج ارتباط خطی با انرژی دارد و از طول موج منبعِ برانگیختهکننده مستقل است. برای مثال؛ « قله یا پیک» (Peak) طیف رامان متعلق به الماس همیشه در ناحیه ظاهر میشود و به طول موج منبع بستگی ندارد. منحصربهفرد بودن طیف رامان برای هر مادهای جهت شناسایی آن به کاربرد میرود.
شدت خطوط رامان
میزان شدت پراکندگی رامان به جمعیت ذرات حالت اولیه مولکول بستگی دارد. بر اساس «توزیع ماکسول-بولتزمن» (Maxwell–Boltzmann Distribution) میتوان نسبت جمعیت را از رابطه زیر بهدست آورد. در این رابطه و اختلاف انرژی بین دو حالت ارتعاشی است.
- : ثابت پلانک
- : ثابت بولتزمن
- : دمای کلوین
- : جمعیت ذرات حالت پایه که تعیینکننده شدت خطوط استوکس هستند.
- : جمعیت ذرات اولین سطح برانگیخته انرژی ارتعاشی که تعیینکننده شدت خطوط آنتیاستوکس هستند.
نسبتِ شدت خطوط آنتیاستوکس به استوکس نیز از رابطه زیر بهدست میآید.
از ویژگی خطوط رامان این است که نتایج تجربی نشان دادهاند که خطوط آنتیاستوکس رامان نسبت به خطوط استوکس شدت کمتری دارند و ضعیفتر هستند و شدت پیکها با انرژی ارتعاشی بهطور تصاعدی تغییر میکنند. با استفاده از رفتار کوانتومی فرایند پراکندگی رامان میتوان نسبت صحیح بین این خطوط و میزان وابستگی آنها به دما را پیشبینی کرد.
همچنین با استفاده از رابطه بالا در مواردی که اندازهگیری مستقیم ممکن نباشد، میتوان از ویژگی خطوط رامان برای اندازهگیریِ نوری دما استفاده کرد. با وارونه کردن رابطه بالا، دمای نمونه از سایر مقادیر بهدست آمده از طیف رامان محاسبه میشود.
رامان فعال
در طیفسنجی رامان تنها ارتعاشاتی تشخیص داده شده و اندازهگیری میشوند که رامان فعال باشند. این حالت زمانی رخ میدهد که مولکول هنگام ارتعاش با تغییر قطبشپذیری همراه باشد. برای مثال ارتعاش کششی متقارن، موجب افزایش اندازه ابر الکترونی و تغییر قطبشپذیری مولکول میشود. در شکل زیر ارتعاش کششی متقارن کربن دیاکسید نمایش داده شده که رامان فعال است.
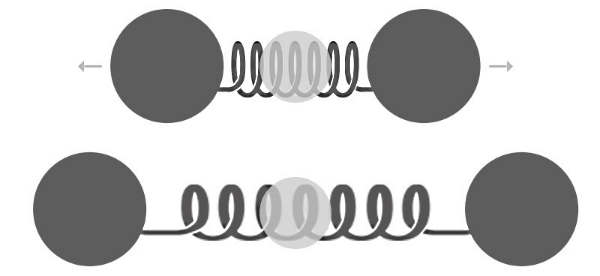
رسم طیف رامان
طیف رامان به شکل استاندارد و رایج به صورت نرخ شمارش یا شدت در مقابل جابهجایی رامان رسم میشود. جابهجایی رامان نشاندهنده تفاوت انرژی بین فوتونهای پرتو لیزر و فوتونهای پرتو پراکنده شده است و تنها به ویژگی انرژی ارتعاشی مولکول بستگی دارد. نرخ شمارش، تعداد دفعات ثبت آشکارساز برای رامان شیفت یا جابهجایی رامان در هر ثانیه است.
شکل زیر طیف رامان «سیستئین» ( | Cysteine) را نشان میدهد که با طول موج ۶۳۳ نانومتر بهدست آمده است.
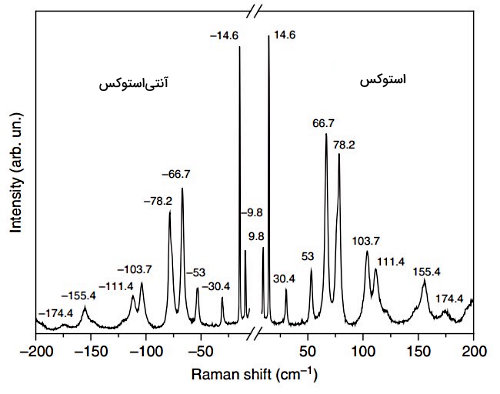
محور افقی طیف، جابجایی رامان و محور عمودی آن شدت خطوط است. الگوی جابهجایی خطوط رامان در هر طرف خط رایلی یکسان است. یکسانی جابهجایی به این دلیل است که در هر صورت انرژی یا جذب و یا آزاد میشود و تنها میزان یا شدت آن تفاوت دارد. تنها مولکولهایی که پیش از تابش نور تکفام لیزر، به صورت ارتعاشی برانگیخته شده باشند خطوط آنتیاستوکس را ایجاد میکنند به همین دلیل شدت این خطوط نسبت به رامان استوکس کمتر است.
به دلیل شدت پایین خطوط آنتیاستوکس معمولا از آن برای آنالیز استفاده نمیشود و تنها بخش استوکس طیف تفسیر میشود. هرچند در مواردی این خطها مفید هستند. برای نمونههای فلورسنت، ویژگی خطوط رامان استوکس ممکن است با فلورسانس تداخل ایجاد کند، به همین دلیل از ویژگی خطوط رامان آنتیاستوکس استفاده میشود. خطوط رامان آنتیاستوکس به دلیل انرژي بالاتری از انتشار فلورسانس تداخلی ایجاد نمیکنند.
ارتعاش مولکولی
ارتعاشات مولکولی نتیجه حرکتهای اتمهای مولکول نسبت به یکدیگر هستند. در مولکول ارتعاشات به شکلهای مختلفی مانند کششی، خمشی و چرخشی انجام میشود. طیفسنجیهای ارتعاشی، طیفِ ارتعاشات گوناگونی را ثبت و شناسایی میکنند. طیفسنجهای رامان و از رایجترین روشهای مکمل در این زمینه هستند.
ارتعاشات مولکولی به نوع و آرایش اتمها و همچنین ساختار دقیق مولکول وابسته است و به همین علت طیفهای ارتعاشی بیمانند هستند. در واقع بخشی از طیف ارتعاشی نقش اثر انگشت ترکیبات شیمیایی را دارد. از این ویژگی بینظیر برای شناسایی مواد استفاده میشود. تعداد حالتهای ارتعاشی مولکولی با اتم به صورت زیر است.
- مولکول غیرخطی: حالت
- مولکول خطی: حالت
چرخش حول محور مولکولهای خطی قابل مشاهده نیست و مولکول دواتمی تنها میتواند فشرده یا کشیده شود و یک حالت ارتعاشی دارد. در جدول زیر انواع ارتعاش مولکولی نشان داده شده است.
| خمشی
(Bending) | کششی نامتقارن
(Asymmetrical Stretching) | کششی متقارن
(Symmetrical Stretching) |
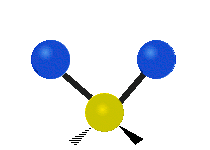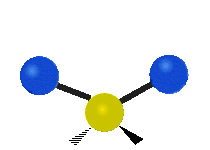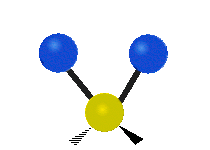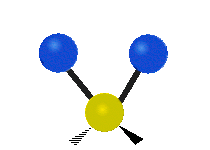 |
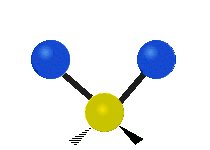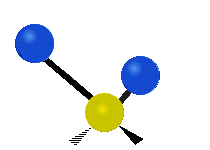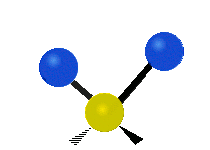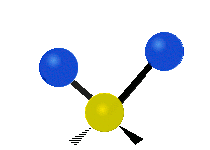 |
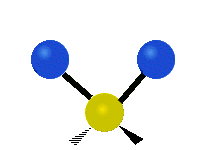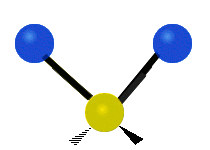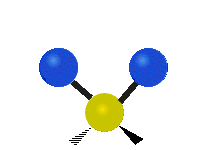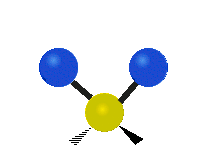 |
| چرخشی خارج از صفحه
(Wagging) | چرخشی داخل صفحه
(Twisting) | گهوارهای
(Rocking) |
 |
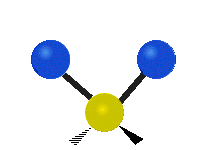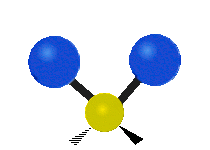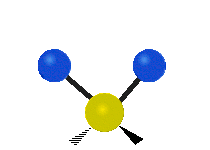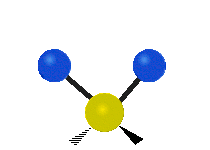 |
 |
شکل زیر طیف رامان نمونهای از تتراکلرید کربن است. تتراکلرید کربن مولکولی چهاروجهی با سه حالت ارتعاشی فعال رامان در ناحیه تا است.
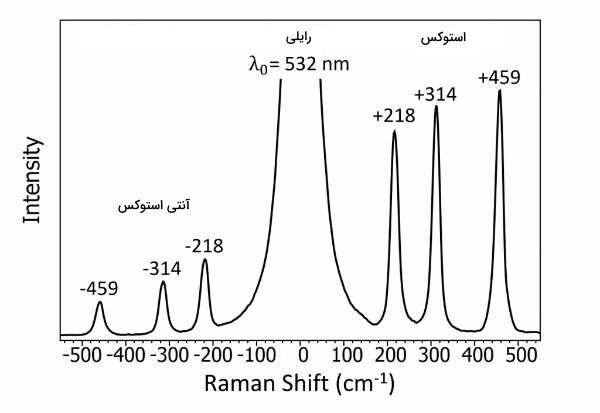
مرکز طیف رامان، پیک پراکندگی ریلی در طول موج لیزر قابل مشاهده است. این پیک از پراکندگی رامان میلیونها بار شدیدتر است و توسط فیلتر از در طیفسنج رامان حذف میشود. در دو طرف پراکندگی ریلی به شکل متقارن، سه پیک استوکس و سه پیک آنتیاستوکس وجود دارند. این سه پیک مربوط به سه ارتعاش است.
تفسیر طیف رامان
تفسیر طیف، تشخیص و شناسایی طیفهای بهدست آمده از طیفسنج است. با استفاده از اطلاعاتی که از طیفی حاصل میشود میتوان وجود آلایندهای که در فرایند تولید ایجاد مزاحمت میکند را تشخیص داد. ویژگی خطوط طیف رامانِ مواد آلی و معدنی متفاوت است. هر طیف از تعدادی پیک تشکیل شده که شدت و موقعیت طول موج پرتوهای نور پراکنده شده را نشان میدهند.
در طیف رامان، هر ارتعاش پیوند مولکولی پیک خاص خود را دارد، پیوندهایی را مانند و و و یا ارتعاشات زنجیره پلیمری، حالتهای شبکه یا گروههایی از پیوندها در حلقه بنزن که حالت «تنفس حلقه» (Ring Breathing) ایجاد میکنند.
برای تفسیر و تشخیص طیف رامان، روشها و راهکارهای متفاوتی وجود دارد. در زیر برخی از این راهها توضیح داده شده است.
- تعیین گروههای عاملی
- استفاده از ناحیه اثر انگشت طیف
- نرمافزارهای آنالیز طیف
- کتابهای مرجع
گروه های عاملی
گروه عاملی، گروهی از اتمها در مولکول هستند که ویژگی خاصی به مولکولهایی با گروه عاملی مشابه میدهند. این گروه از اتمها در رامان ارتعاشات، طیف و جایگاه مخصوصی دارند و برای مولکولهای مختلف با گروه عاملی مشابه به صورت یکسان ظاهر میشود. طیف ارتعاشی گروههای عاملی در نتیجه کارهای «ویلیام کوبلنتز» (William Coblentz) شناسایی شدند.
طیف این گروهها اندازهگیری مستقیم پیشرفت در طول واکنش را نشان میدهند که برای نظارت بر واکنشهایی شامل گروههای عاملی مفید هستند. با استفاده از طیف چنین گروههایی میتوان تشحیص داد که ترکیب نامشخصی به چه گروهی از ترکیبات شیمیایی مرتبط است. برای مثال ارتعاشات کششی گروه کربونیل در آلدهید همیشه در تا است.
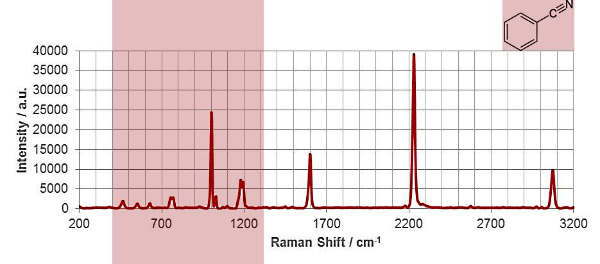
در شکل زیر که طیف رامان ترکیب «بنزونیتریل» ( | Benzonitrile) است، پیک مربوط به گروه عاملی آن با رنگ قرمز مشخص شده است. ارتعاش کششی گروه عاملی نیتریل در بنزونیتریل با مقدار قرار دارد.
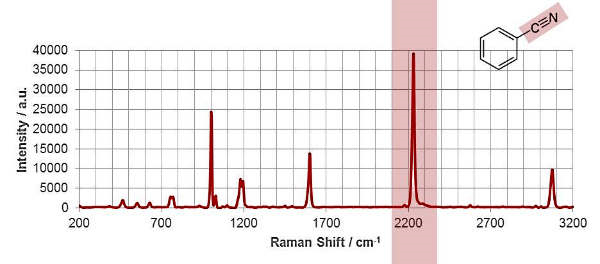
نمونههایی از گروههای عاملی که به راحتی قابل شناسایی هستند در جدول زیر فهرست شدهاند.
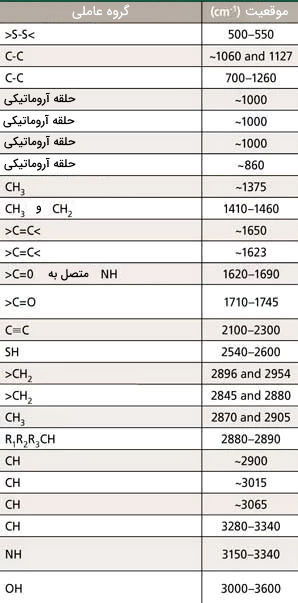
پیوندهایی مانند ، و از نظر هندسی در ترکیبات پیچیده به هم نزدیک هستند و انرژیهای مشابهی دارند. شناسایی بخش زیادی از طیف ماده که در محدوده کمتر از قرار دارد با استفاده از گروههای عاملی بهسختی قابل تفسیر است.
ناحیه اثر انگشتی
هر ساختار مولکولی ارتعاشات مخصوص به خود را دارد که در رامان قابل تشخیص است. ارتعاشات مربوط به ساختار مولکولی ترکیبات معمولاً در جابهجایی رامان کمتر ظاهر میشوند که ویژه همان ساختار هستند. به همین دلیل این بخش از ناحیه طیفی به عنوان «ناحیه اثر انگشتی» نامیده میشود و مهمترین بخش طیف رامان با هدف شناسایی ترکیبات ناشناس است.
نرمافزار آنالیز طیف رامان
همچنین آنالیز طیفهای رامان توسط نرمافزار نیز انجام میشود. این نرمافزارها با استفاده از الگوریتم و پایگاه دادهای از طیف ترکیبات گوناگون، طیف مورد نظر را با سایر طیفها مقایسه میکنند. نتیجه مقایسه با «شاخص کیفیت همخوان» (Hit Quality Index | HQI) نشان داده میشود که میزان همخوانی یا مطابقت طیف ناشناس با طیفهای موجود در پایگاه داده است. شاخص کیفیت در بازه ۰ تا ۱۰۰ متغیر است. شناسایی ماده با استفاده از نرمافزار و تنظیمات بیشتر برای آنالیز طیف تنها در چند ثانیه انجام میشود.
- عدد «۰» یعنی: کمترین میزان مطابقت یا عدم مطابقت
- عدد «۱۰۰» یعنی: بالاترین همخوانی، همخوانی دقیق یا مطابقت کامل،
«الگوریتم» (Algorithm) نرمافزار طیف را بهصورت بردار در نظر میگیرد و با استفاده از ضرب نقطهای بین طیفهای پایگاه داده و طیف ناشناس را مشخص میکند. در واقع این شاخص مقدار ضرب نقطهای شدت در هر نقطه از طیف است و هرچه نتیجه حاصلضرب بالاتر باشد به این معنی است که دو نقطه شباهت بیشتری به یکدیگر دارند. این روش محاسبه به «الگوریتم همبستگی» (Correlation Algorithm) معروف است. در شکل زیر محیط نرمافزار آنالیز طیف رامان برای طیفی ناشناس و موارد همخوان با آن را نشان میدهد.
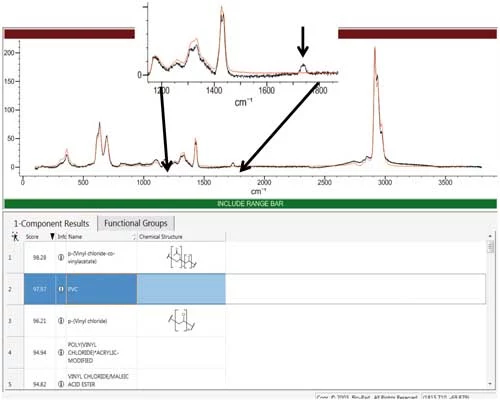
همچنین با استفاده از نرمافزارها و روشهای «ماتریس جی» (G matrix) میتوان طیف فرکانسهای ارتعاشی ترکیبات را پیشبینی کرد. در این نرمافزار مختصات جابجایی برای همه اتمهای مولکول توصیف شده است.
انواع طیف رامان
نمونههایی از ویژگی فرکانسی برخی از گروههای شیمیایی در این بخش بررسی شده است. در شکلها، طیف بالایی مربوط به طیفهای فروسرخ (IR) و طیفهای پایین هر نمودار مربوط به طیفهای رامان است. همچنین محورهای عمودی در IR برحسب «عبور» (Transmittance) و در رامان برحسب «شدت» (Intensity) است.
ویژگی خطوط رامان باند کششی گروه X-H
مقدار است. تفاوت در فرکانسهای کششی بیشتر به دلیل تفاوت در نوع پیوند است. برخی از طیفها مانند ارتعاش کششی در IR نسبت به طیف رامان شدت بیشتری دارند. شکل زیر طیف IR و رامانِ پیوندهای کششی عنصرهای اکسیژن، گوگرد، فسفر، نیتروژن و سیلیسیم متصل به هیدروژن هستند.
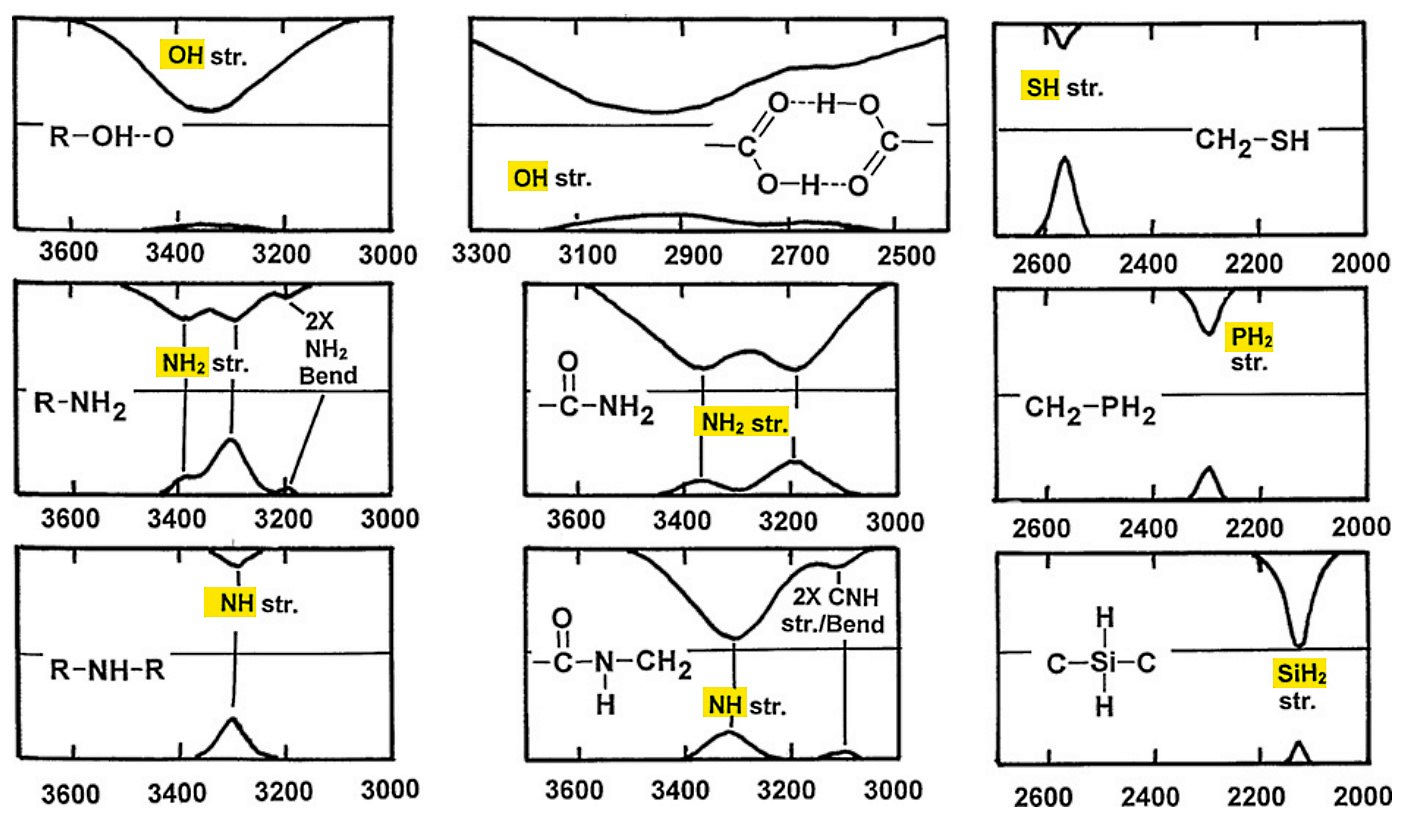
- ردیف اول
- چپ: ارتعاش کششی مربوط به پیوند هیدروژنی الکلی در باند بزرگی در IR میدهد در حالیکه در رامان بسیار ضعیف است.
- وسط: ارتعاش کششی پیوند هیدروژنی دیمر کربوکسیلیک اسید طیف گستردهای در IR دارد که مرکز آن در است.
- راست: گروه متعلق به تیول یا «مرکاپتان» (Mercaptan) برخلاف باند ظعیفی در IR دارد و باند قوی رامان در ظاهر شده است.
- ردیف دوم
- چپ: آمینهای آلیفاتیک نوع اول در ساختار خود، گروه دارند که در IR نزدیک به و ظاهر شدهاند. این ارتعاشات به ترتیب متعلق به ارتعاش کششی نامتقارن (خارج از صفحه) و متقارن (داخل صفحه) هستند. بهطور معمول، کشش درون صفحه در طیف رامان قویتر از کشش خارج از صفحه است.
- وسط: در آمیدهای نوع یک باندهای کششی در و ظاهر میشوند و معمولاً در IR نسبت به طیفهای رامان قویتر هستند.
- راست: گروه در IR و رامان طیف یکسانی نزدیک به دارد.
- ردیف سوم
- چپ: در آمینهای آلیفاتیک نوع دوم باند کششی نزدیک به ظاهر میشود که در IR بسیار ضعیف است اما در طیف رامان قویتر است.
- وسط: آمیدهای تک استخلافی باندی قوی در IR نزدیکی دارد که از ارتعاش کششی ناشی میشود. این ترکیبات در در طیف IR باند ضعیفی دارند که مربوط به جذب اورتون است.
- راست: گروه نیز در IR نزدیک باندی قوی دارد ولی در رامان بسیار ضعیف ظاهر میشود.
همچنین ترکیبات و که در شکل بالا نشان داده نشدهاند، باندهای کششی متوسط تا قوی در IR دارند. باندهای رامان این ترکیبات نیز ضعیف است.
برای مقایسه، طیف کامل IR و رامان چند ترکیب در زیر آورده شده است.
- بنزوئیک اسید : سادهترین کربوکسیلیک اسید آروماتیک است. این ترکیب همانند سایر کربوکسیلیک اسیدها ارتعاش کششی در IR دارد که مرکز آن در است.
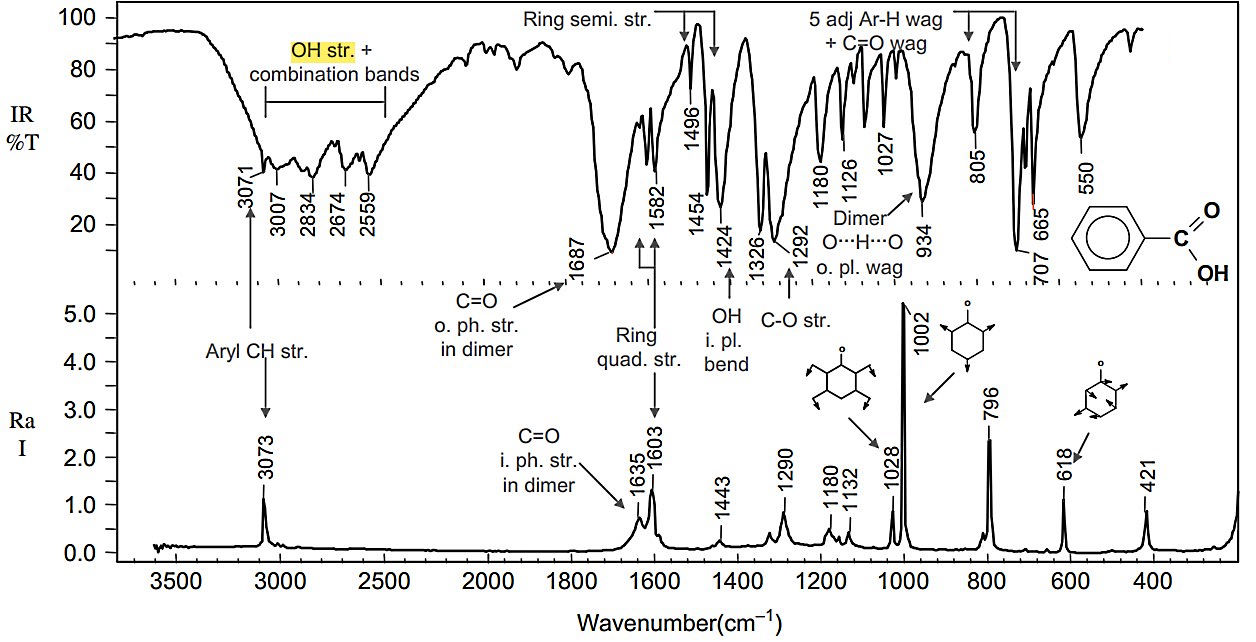
- استامید : سادهترین نوع آمید است که از استیک اسید ساخته میشود. آمیدهای نوع یک باندهای کششی قویتری در IR نسبت به رامان دارند.
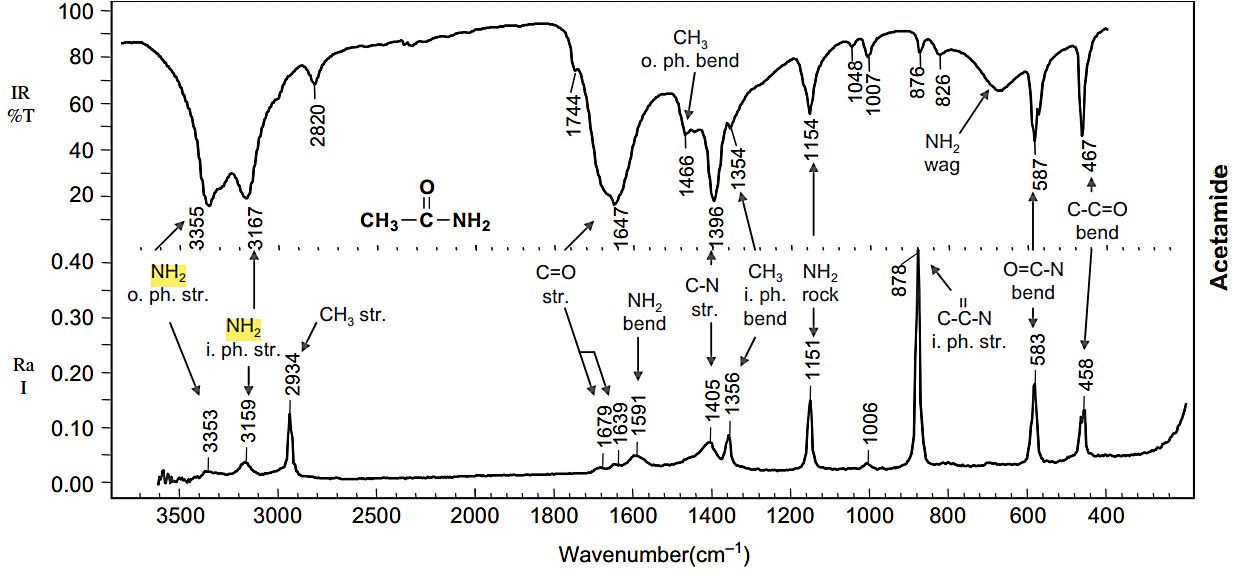
- متانول : سادهترین نوع الکل است که کشش در رامان ضعیف اما در IR قوی است.
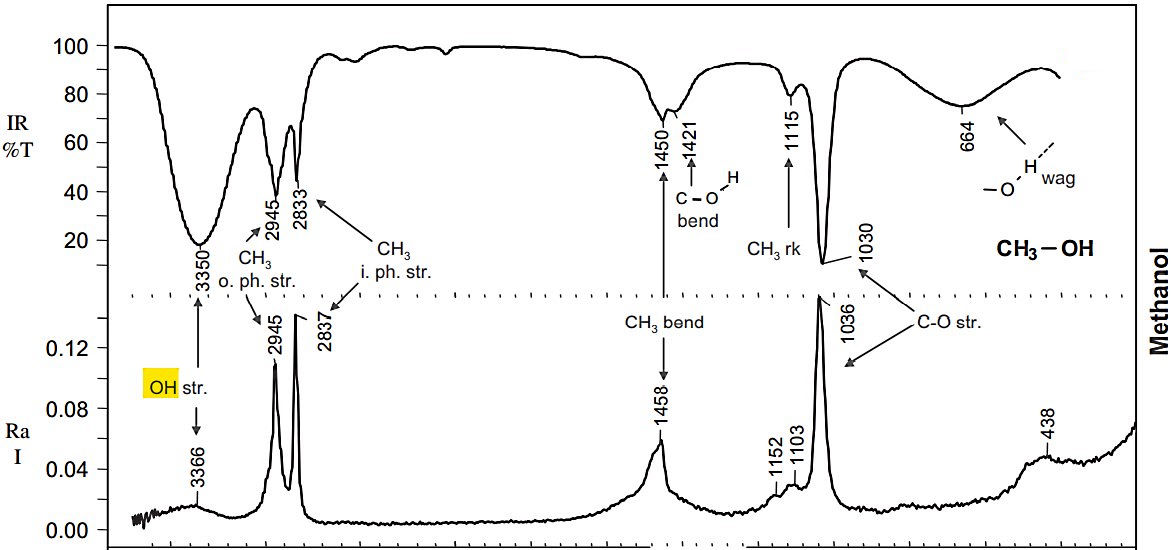
ویژگی خطوط رامان گروه های آلیفاتیک
در زیر بخشهای گزینش شدهای از طیف گروههای آلکان در رامان و IR نشان داده شده است.
گروه متیلن
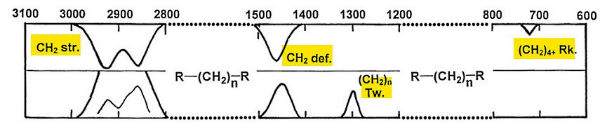
- ارتعاش کششی: برای زنجیره غیرحلقوی، باندهای کششی خارج و داخل صفحه به ترتیب نزدیک در و ظاهر میشوند.
- ارتعاش خمشی: باند خَمشی نیز نزدیک به ظاهر میشود.
- ارتعاش چرخشی: باند پیچشی درون صفحهای تنها در رامان و در نزدیکی و ارتعاش گهوارهای آن تنها در IR و نزدیک ظاهر میشود.
گروه متیل
- ارتعاش کششی: باندهای کششی روی کربن آلکان خارج و داخل صفحه به ترتیب نزدیک در و ظاهر میشوند.
- ارتعاش خمشی: باند خمشی گروه متیل خارج از صفحه نزدیک به در IR ظاهر میشود. ارتعاش خمشی درون صفحهای متیل روی کربن آلکان، نزدیک در IR دیده میشود ولی در رامان طیفی ندارد.
وجود گروههای مانند اتم N یا O مجاور اتم مرکزی میتوانند فرکانس ارتعاش کششی متیل را به فرکانسهای پایینترین بین و انتقال دهد.
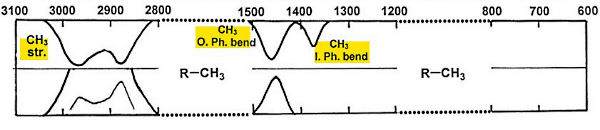
آلکانهای شاخه دار
در IR، اگر دو گروه متیل روی کربن باشد، دو باند قوی نزدیک و ظاهر میشود. اگر سه گروه متیل روی کربن باشد، یک باند ضعیف نزدیک و باندی قوی نزدیک خواهد داشت.
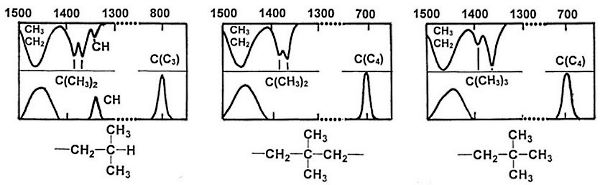
در رامان، ارتعاش کششی درون صفحهای باندی قوی در دارد. همچنین باند قوی کشش درون صفحه نیز در ظاهر خواهد شد.
تفاوت باند کششی درون صفحهای برخی ترکیبات در جدول زیر نمایش داده شده است. در این ترکیبات کربن، نیتروژن، اکسیژن و گوگرد است.
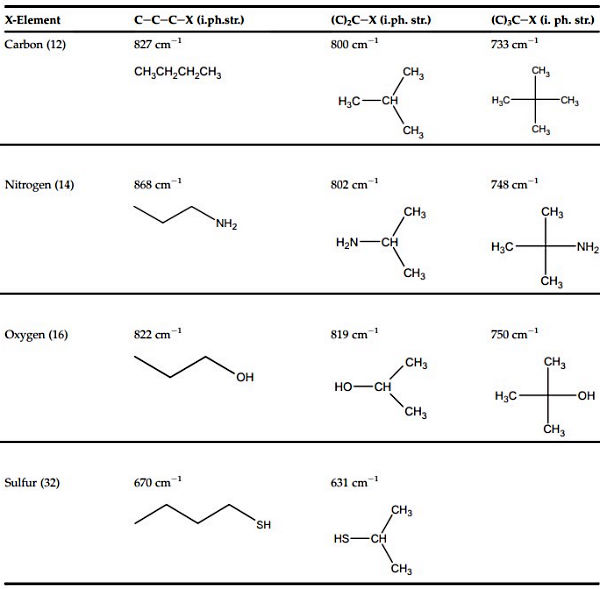
در شکل زیر طیف کامل IR و رامانِ هپتان جهت مقایسه نشان داده شده است.
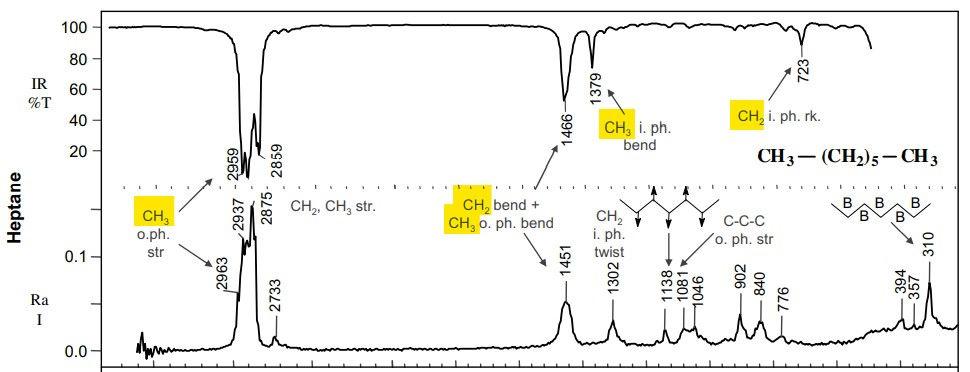
در شکل زیر طیف IR و رامان در ناحیه کششی برای n-پنتان، n-هگزان، n-هپتان، n-اکتان و سیکلوهگزان نشان داده شده است. ارتعاشات مربوط به کششهای متیل و متیلن (۳۰۰۰ تا ) باعث ایجاد باندهایی میشود که در هر دو طیف فروسرخ و رامان قوی و مشخص هستند.
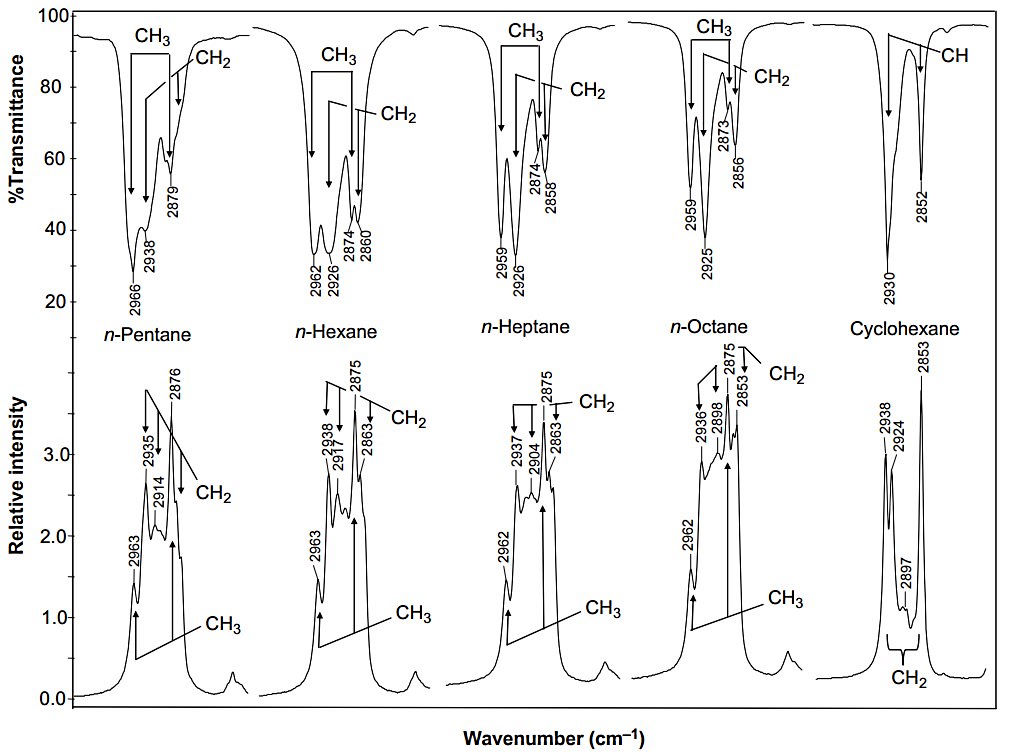
پیچیدگی و برخی باندهای بیشتر در رامان به دلیل اثرات رزونانس فرمی است.
طیف رامان ترکیبات S=O، Si-O و P=O
ترکیبات در رامان و IR باندهای قوی دارند. در شکل زیر ویژگی خطوط رامان و IR برخی از فرکانسهای گروههای و و و نشان داده شده است.
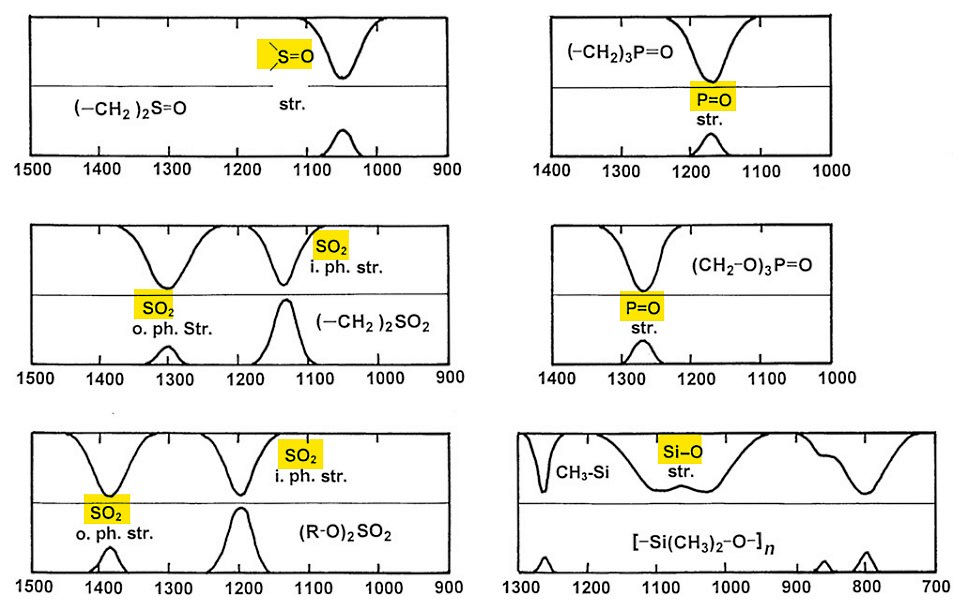
ستون چپ
ستون سمت چپ ویژگی خطوط رامان و IR مربوط به ترکیبات سولفوکسید ، سولفون و دیآلکیل سولفات است. فرکانس باند این ترکیبات را میتوان با «الکترونگاتیوی جانشینی، استخلافی یا گروهی» (Substituent Electronegativity) مرتبط دانست. در شیمی آلی، الکترونگاتیوی بیشتر با گروههای عاملی وابسته است. به همین دلیل از اصطلاح الکترونگاتیوی گروهی یا الکترونگاتیوی جایگزین استفاده میشود.
ارتعاش کششی که در نزدیکی ظاهر شده است در IR نسبت به رامان شدت بیشتری دارد. گروه در سولفونها و دیآلکیل سولفاتها به دلیل ارتعاشهای کششی متقارن و نامتقارن دو باند مجزا دارد که ارتعاش خارج از صفحه در IR و ارتعاش درون صفحهای در رامان شدت بیشتری دارد.
ستون راست
ستون سمت راست ویژگی خطوط رامان و فروسرخ مرتبط با فسفین اکسید ، فسفر استر و پلیمر «سیلوکسان» (Siloxane) است. طیف IR این ترکیبات نسبت به طیف رامان شدت بیشتری دارد. فرکانس گروهای مهم فسفر به ترتیب زیر است.
- ارتعاش کششی در ۲۴۵۰ تا ۲۲۷۰
- ارتعاش کششی متعلق به گروه در ۲۸۰۰ تا ۲۱۰۰
- ارتعاش کششی متعلق به گروه در ۱۰۵۰ تا ۹۷۰
همچنین گروه فنیلی دو باند کششی فنوکسی و را به ترتیب از ۱۲۴۰ تا ۱۱۶۰ و ۹۹۵ تا ۸۵۵ ایجاد میکند. طیف رامان برای سیلیکونها بسیار ضعیف است و طیف IR کارکرد بسیار بهتری دارد.
ترکیبات معدنی
طیفسنجی رامان و IR برای بسیاری از ترکیبات معدنی، اطلاعات ساختاری مهمی ارائه میدهند. هر دو روش به شکل بلوری ترکیبها حساس هستند. در جدول زیر باند رامان و فروسرخ چند ترکیب معدنی پرکاربرد فهرست شده است.
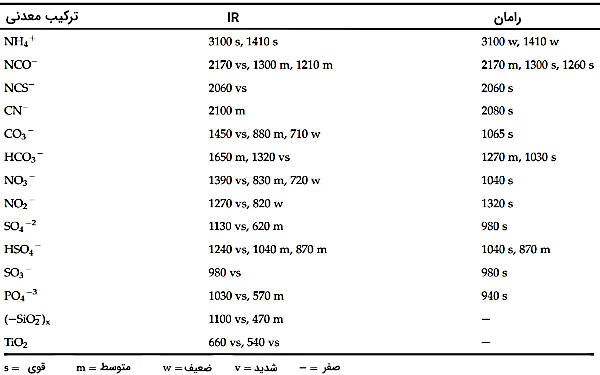
برای مثال طیف کامل رامان و IR دو ترکیب معدنی پتاسیم نیترات و سدیم سولفات برای مقایسه در زیر آمده است.
طیف رامان پتاسیم نیترات
شکل زیر طیف کامل رامان و IR پتاسیم نیترات است. طیف رامان برای ارتعاش کششی در ظاهر شده است. همچنین در طیف فروسرخ پتاسیم نیترات باند قوی ارتعاش کششی در قابل مشاهده است.
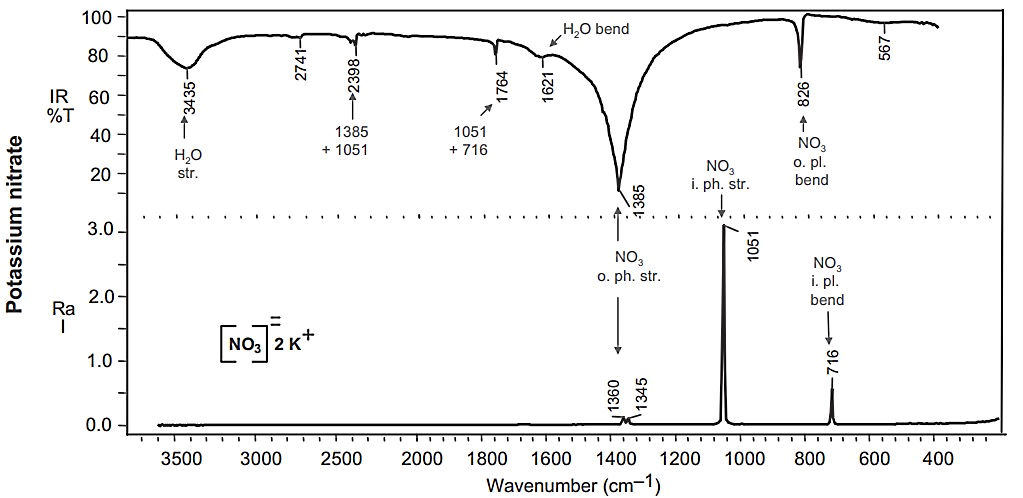
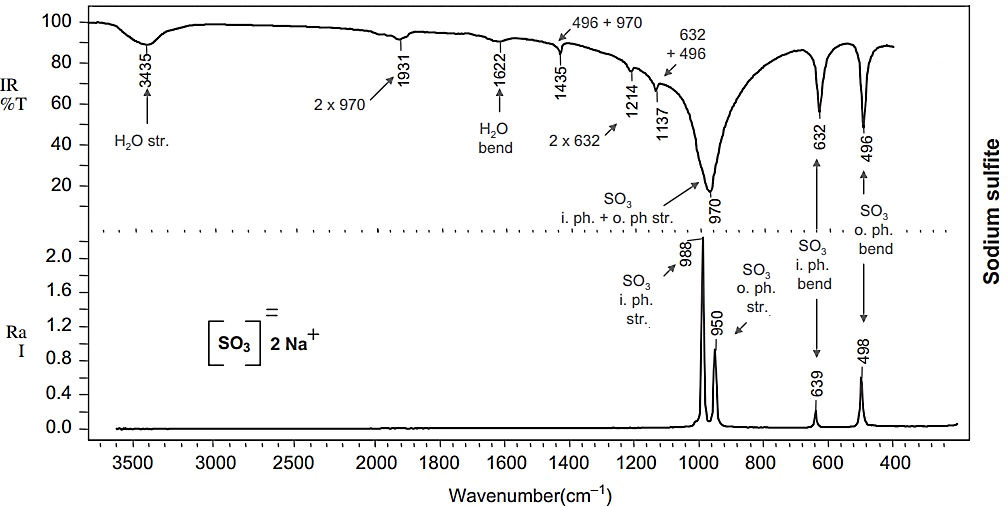
طیف رامان سدیم سولفات
در زیر طیف کامل رامان و IR سدیم سولفات آورده شده است. سدیم سولفات در داروسازی، صنعت رنگ و تولید مواد پاککننده کاربرد دارد. بهطور معمول یون چنداتمی در رامان در ناحیه نزدیک به باند کششی قوی دارد. در شکل زیر این باند در ظاهر شده است. همچنین در IR در شدت متوسط و در شدت آن قوی است.











آقا واقعا عالی بود ؛ دستتون درد نکنه