دناتوره شدن چیست؟ – انواع و عوامل – به زبان ساده
دناتوره شدن فرایندی در ماکرومولکولها است که باعث بههم ریختگی ساختار سهبعدی و تغییر عملکرد آنها میشود. یکی از ملموسترین مثالهای دناتوره شدن، پخت غذا است که در آن گرما باعث تغییر ساختار پروتئین و نرم شدن موادی مثل گوشت میشود. دناتوره شدن در فرایندهای داخل بدن و تکنیکهای سنجش مولکولهای زیستی در آزمایشگاه نیز انجام میشود. این فرایند منحصر به پروتئینها نیست و DNA و RNA را نیز تحت تاثیر قرار میدهد. در این مطلب از دناتوراسیون مولکولهای زیستی و عوامل ایجاد آن صحبت میکنیم.

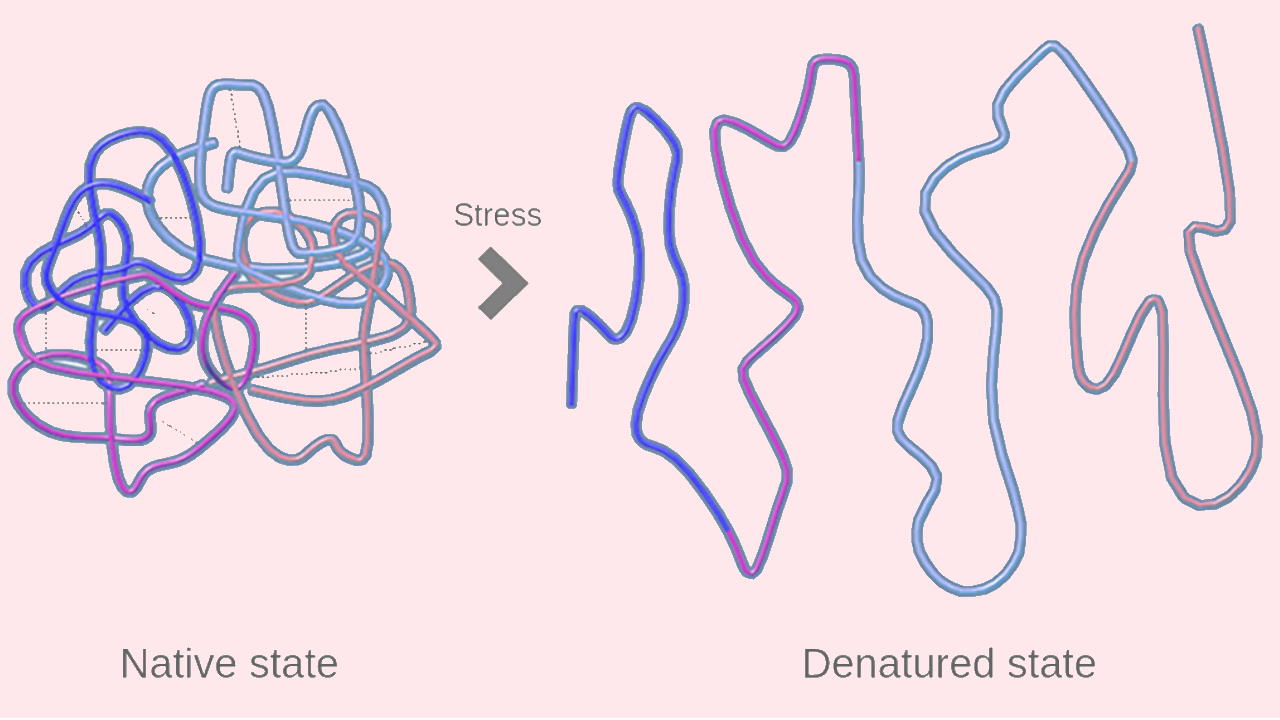
دناتوره شدن چیست ؟
دناتوره شدن یا «دناتوراسیون» (Denaturation) مولکول زیستی، به معنی از دست دادن ساختار سهبعدی آن است. ازآنجاکه عملکرد بیومولکولهایی مانند پروتئین و نوکلئیکاسید، مربوط به ساختار سهبعدی آنها است، دناتوره شدن عملکرد ماکرومولکول را از بین میبرد اما بر توالی مونومرهای سازنده آن اثری ندارد.
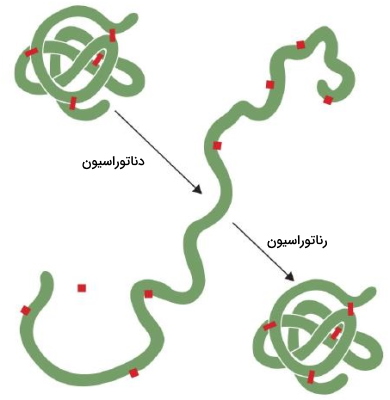
دناتوره شدن پروتئین
پروتئین از زیرواحدهای اسیدآمینه تشکیل شده است و چهار سطح ساختاری دارد.
- ساختار اول: ساختار خطی پلیمر که از کنار هم قرارگرفتن آمینواسیدها تشکیل میشود.
- ساختار دوم: تاخوردگیهای اولیه و تشکیل موتیفهای آلفاهلیکس و صفحات بتا که بهکمک پیوندهای هیدروژنی درونمولکولی بهوجود میآیند.
- ساختار سوم: جهتگیری آمینواسیدهای لازم برای ساخت واحدهای عملکردی (دومین) ازجمله جایگاه فعال آنزیم در این ساختار انجام میگیرد.
- ساختار چهارم: برهمکنش زیرواحدها در این ساختار، تعیینکننده ساختار سهبعدی پروتئین و کنفورماسیونهای عملکردی آن است.
غیر از ساختار اول، بقیه ساختارهای پروتئین بهوسیله برهمکنشهای غیرکووالانسی دوقطبی-دوقطبی یا پیوند هیدروژنی تشکیل میشوند. بههمین دلیل نسبت به تغییرات دما، pH و غلظت نمک محیط حساس هستند و حتی تغییرات ملایم این پارامترها هم ممکن است بر ساختار سهبعدی پروتئین تاثیر داشته باشد.
عوامل دناتوره کننده پروتئین
عوامل دناتورهکننده پروتئین را میتوان بر اساس ماهیت به دو نوع فیزیکی و شیمیایی تقسیم کرد.
- عوامل فیزیکی: این گروه شامل عواملی مانند گرما، تغییرات pH و اشعه ماورابنفش میشوند.
- عوامل شیمیایی یا «دناتورانتها» (Denaturant) : این گروه شامل اسیدها، ترکیبات قلیایی، نمکهای فلزات سنگین، اوره، اتانول و دترجنتهای مختلف میشوند.
عوامل دناتورهکننده، موادی هستند که با ایجاد تغییر در برهمکنشهای واندروالسی، یونی، هیدروژنی و آبگریز در ساختارهای چهارگانه پروتئین تغییر ایجاد میکنند.
انواع دناتوره شدن پروتئین
دناتوراسیون پروتئین بر اساس نوع عامل دناتورهکننده به سه دسته کلی تقسیم میشود.
- دناتوره شدن با تغییر pH
- دناتوره شدن شیمیایی
- دناتوره شدن بهوسیله گرما و اشعه UV
دناتوره شدن با تغییر pH
تغییرات pH محیط بر تعداد پیوندهای هیدروژنی بین اسیدهای آمینه تاثیر میگذارد و ساختار سهبعدی پروتئین را تغییر میدهد. در pH فیزیولوژیک، بار کلی اسکلت پروتئین صفر است ولی زنجیرههای جانبی آمینواسیدها به دلیل از دست دادن یا جذب هیدروژن بار منفی یا مثبت دارند. تغییرات pH محیط، بار کلی مولکول، برهمکنش آمینواسیدها با هم و در نتیجه ساختار سهبعدی پروتئین را تحت تاثیر قرار میدهد.
برای نمونه، آسپارژین، تیروزین و سیستئین، اسیدآمینههای با زنجیره جانبی قطبی هستند. این مولکولها با توجه به جهتگیری فضایی و جایگاهی که در توالی آمینواسیدی پروتئین دارند، با یکدیگر پیوند هیدروژنی تشکیل میدهند. تغییرات pH محیط، باعث پروتونه یا دپروتونه شدن آنها و تغییر توانایی تشکیل این پیوند میشود. به علاوه، تغییرات pH، با تغییر بار کلی پروتئین، انحلالپذیری آن را تغییر میدهد. صفر شدن بار کلی پروتئین، «سبب تجمع» (Aggregation) یا «رسوب» (Precipitation) خواهد شد.
دناتوره شدن شیمیایی
بخشهای آبگریز پروتئین برای رسیدن به حداقل انتروپی و پایداری بیشتر، در مناطق دور از آب و در تاخوردگیهای داخلی پنهان شدهاند. اما برخی مواد معدنی و آلی از جمله اتانول و بنزن این ساختار را برعکس میکنند. در این حالت، بخشهای آبگریز در تماس با مولکولهای قطبی آب قرار میگیرند و برهمکنش این دوبخش، ساختار پروتئین را بهم میریزد.
دترجنتها
«دترجنتها» (Detergents) دستهای از ترکیبات شیمایی هستند که دناتوراسیون پروتئین را تسهیل میکنند. این ترکیبات «دوگانهدوست» (Amphipathic) با برهمزدن ساختار بخشهای آبگریز و ایجاد تغییر در غلظت یونها و فلزات سنگین محیط، بیومولکول را دناتوره میکنند. این ترکیبات از یک سر قطبی و یک دنباله آبگریز تشکیل میشوند.
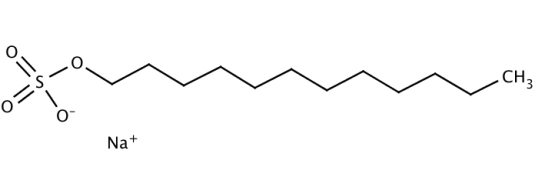
«سدیم دودسیل سولفات» (SDS) یکی از متداولترین دترجنتهای پروتئین است. این مولکول با دم هیدروکربنی خود به ساختار اصلی پروتئین متصل میشود، مناطق آبگریز پروتئین را در معرض قرار میدهد و زنجیره پروتئینی را بهطور کامل میپوشاند. سرقطبی این مولکول، پیوندهای یونی را میشکند و در نهایت بار کلی پروتئین منفی و دناتوره میشود.
اوره
ترکیبات «بینظمی دوست» (Chaotropic) بر پیوندهای غیرکوالان اثر میگذارند و پروتئین را به صورت برگشتپذیر دناتوره میکنند. اوره یکی از ترکیبات بینظمیدوست معمول است که در آمادهکردن پروتئین برای الکتروفورز دوبعدی استفاده میشود. در استفاده از اوره باید توجه داشت دمای بالاتر از ۳۷ درجه باعث «کربامیله شدن» (Carbamylation) پروتئین میشود.
دناتوره شدن با گرما یا اشعه
افزایش دما در یک نمونه زیستی، افزایش انرژی سینتیکی هر اتم و انتروپی را به دنبال خواهد داشت. در این شرایط انرژی جنبشی و ارتعاشی اتمها بیشتر میشود و قدرت پیوند هیدروژنی کاهش مییابد. اشعه طولانیمدت خورشید و سایر منابع ازجمله دستگاههای X-Ray نیز ساختار پروتئين را تغییر میدهند. آبمروارید و آفتابسوختگی نمونههایی از اثر اشعه خورشید بر ساختارهای پروتئینی هستند.
تفاوت دناتوراسیون و تخریب پروتئین
تفاوت دناتوراسیون و «تخریب» (Degradation) پروتئین را در جدول زیر توضیح میدهیم.
| دناتوراسیون پروتئین | تخریب پروتئین |
| ساختار دوم، سوم و چهارم پروتئین از بین میرود. | ساختارهای دوم، سوم و چهارم بدون تغییر میمانند. |
| ساختار اول تغییری نمیکند. | ساختار اول از بین میرود. |
| مولکول عملکرد خود را از دست میدهد. | ممکن است مولکول بعضی عملکردها را حفظ کند. |
دناتوره شدن آنزیم
هر آنزیم برای فعالیت بهینه خود نیاز به دما و pH خاصی دارد، تغییر در این دو فاکتور باعث دناتوره شدن آنزیم، تغییر در کنفورماسیون جایگاه فعال آن و کاهش یا از بین رفتن کامل فعالیت میشود. برای نمونه اگر دمای بدن انسان از ۴۰ درجه سانتیگراد بالاتر رود امکان دناتوره شدن آنزیمها و بهم خوردن هومئوستاز بدن وجود دارد.
اثر تغییرات pH، بر فعالیت و ساختار آنزیمها بستگی زیادی به نوع آنزیم دارد. برای نمونه، پپسین آنزیمی است که در محیط کاملا اسیدی معده، بهترین عملکرد را دارد و بازی شدن محیط سبب دپروتونه شدن اسیدهای آمینه آن، کاهش پیوندهای هیدروژنی و تغییر در جایگاه فعال آنزیم میشود.
دناتوره شدن DNA
دناتوره شدن DNA یا «ذوب» (Annealing) به معنی بازشدن دو رشته مولکول از هم است. در سلول برای اینکه فرایندهای همانندسازی و رونویسی انجام گیرند، ابتدا نیاز است مولکول دناتوره شود و این عمل را آنزیم هلیکاز انجام میدهد. هلیکاز در طول چنگال همانندسازی حرکت و با مصرف ATP دو رشته را از هم جدا ميکند.
برای سنجش DNA در محیط آزمایشگاه و انجام برخی تکنیکها ازجمله توالییابی و «ساتِرن بلات» (Southern Blot) نیز مولکول دناتوره میشود. در ادامه ۴ روش اصلی دناتوره شدن پروتئین در آزمایشگاه را توضیح میدهیم که اساس همه آنها شکستن پیوند هیدروژنی بین دو رشته است.
- افزایش دما
- استفاده از
- تغییر غلظت نمک
- تغییر pH محیط
دناتوراسیون DNA به کمک افزایش دما
DNA در فرایندی که بسیار شبیه به ذوب است، دناتوره میشود. در این فرایند دمای مولکول تا زمان بازشدن پیچخوردگیها و جداشدن کامل دو رشته از هم ادامه دارد. سپس دما را پایین میآوریم تا مولکول در وضعیتی پایدار قرار بگیرد. از این فرایند بیشتر در مقایسه DNA گونهها با هم استفاده میشود اما برای مواقعی که دقت مهم است کاربرد چندانی ندارد چراکه احتمال ایجاد دورشتههای غیردلخواه، در مرحله کاهش دما زیاد است. واکنش زنجیره پلیمراز (PCR) ازجمله تکنیکهایی است که از این روش برای دناتوراسیون استفاده میکند.
دناتوراسیون DNA به کمک استفاده از
با بهکارگیری غلظت مشخصی از میتوان DNA را در کمتر از ۱ دقیقه دناتوره کرد. یکی از مزایای استفاده از این روش امکان رناتوراسیون مولکول با استفاده از بافر فسفات است. از این روش میتوان برای دناتوراسیون حجم بالای این مولکول در فرایندهایی استفاده کرد که به دقت زیادی نیاز ندارند.
دناتوراسیون DNA به کمک تغییر غلظت نمک
غلظت بالای نمک، DNA را دناتوره میکند. برای دناتوراسیون کامل ممکن است این روش همراه افزایش دما یا اسید انجام شود و غیرقابل برگشت است.
دناتوراسیون DNA به کمک تغییر pH محیط
در pH بالای ۱۱، حضور ، باعث باز شدن پیوندهای هیدروژرنی بین بازها در ۲ رشته DNA، دناتوراسیون مولکول میشود.
عوامل دناتوره شدن DNA
عوامل دناتوره شدن DNA را میتوان بر اساس ماهیت به دو نوع فیزیکی و شیمیایی تقسیم کرد.
- عوامل فیزیکی: این گروه شامل عواملی مانند گرما، اشعه UV، امواج مافوق صوت و فشار زیاد میشوند.
- عوامل شیمیایی: این گروه شامل اسیدها، ترکیبات قلیایی، نمکهای فلزات سنگین، اوره، اتانول و دترجنتهای گوانیدین میشوند. ترکیبات اسیدی و قلیایی مستقیما به پیوند هیدروژنی حمله میکنند اما اوره و دترجنتهای گوانیدین با این پیوندها تداخل پیدا میکنند.
اندازهگیری میزان دناتوراسیون DNA
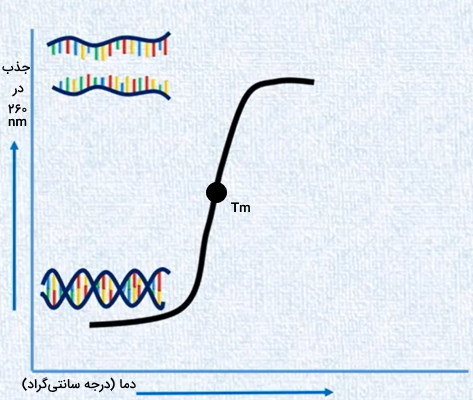
ساختار مولکول DNA از بازهای آلی تشکیل شده است که اشعه UV را در طول موج ۲۶۰ نانومتر جذب میکنند. بههمین دلیل، برای اندازهگیری میزان دناتوره شدن این مولکول از «اسپکتروفوتومتر» (Spectrophotometer) استفاده میکنیم. میزان جذب اشعه UV در DNA تکرشتهای بهدلیل در معرض بودن بازهای آلی بیشتر است. میزان دناتوره شدن مولکول را میتوان به کمک میزان جذب بازها و پیدا کردن دمای ذوب () اندازه گرفت. دمای ذوب DNA دمایی است که در آن نیمی از مولکولهای DNA کاملا دناتوره شدهاند و وابسته به سه عامل است.
- محتوای نوکلئوتیدی مولکول: نوکلئوتیدهای گوانین (G) و سیتوزین (C) با سه پیوند هیدروژنی و نوکلئوتیدهای آدنین (A) و تیمین (T) با دو پیوند هیدروژنی به هم متصل هستند. بههمین دلیل هر چه محتوای G-C در DNA بیشتر باشد دمای ذوب نیز بالاتر میرود.
- طول مولکول: هر چه طول DNA بیشتر باشد انرژی بیشتری برای باز کردن دو رشته از هم نیاز است و دمای ذوب بالاتر میرود.
- قدرت یونی محلول حاوی DNA: قدرت یونی محلول، به معنی غلظت کل یونهای موجود در محلول است. هر چه میزان غلظت یونها در محلول بیشتر باشد، به دلیل وجود کاتیونهای بیشتر، پایداری DNA و دمای ذوب مولکول افزایش مییابد.
تفاوت دناتوراسیون و رناتوراسیون DNA
دناتوراسیون و رناتوراسیون DNA دو فرایند معکوس هستند که هم در بدن موجود زنده و هم در آزمایشگاه، برای انجام تکنیکهای شناسایی، مقایسه و تعیین توالی انجام میگیرند. تفاوتهای این دو فرایند در جدول زیر آمده است.
| دناتوراسیون DNA | رناتوراسیون DNA |
| DNA تکرشتهای است. | DNA دورشتهای است. |
| در دمای بالا انجام میشود. | در دمای پایین انجام میشود. |
| پیوندهای هیدروژنی بین بازها از بین میروند. | پیوندهای هیدروژنی بین بازها تشکیل میشوند. |
| جذب UV افزایش مییابد. | جذب UV کاهش مییابد. |
| ویسکوزیتی کاهش مییابد. | ویسکوزیتی افزایش مییابد. |
دناتوراسیون RNA
با وجود اینکه RNA یک مولکول تکرشتهای است، ساختارهای دوم و سومی دارد که بهوسیله پیوندهای درونمولکولی ایجاد میشوند. برای انجام تکنیکهای آزمایشگاهی، ابتدا نیاز است که این مولکول دناتوره شود.
دناتوراسیون برگشت پذیر
در بعضی از موارد، با خارج کردن دناتورانت، پروتئین به ساختار عملکردی برمیگردد. به این نوع دناتوراسیون، برگشتپذیر میگویند. اگرچه در مواردی مثل پختن تخممرغ که دناتوراسیون شدید است، حتی با برداشت دناتورانت ساختار عملکردی پروتئین احیا نمیشود. دناتوراسیون اسیدهای نوکلئوئیک نیز در مواردی مثل همانندسازی، برگشتپذیر است.
پرسشهای متداول
هنگام مطالعه در مورد دناتوره شدن پروتئین و اسیدهای نوکلئوئیک ممکن است پرسشهایی برای شما پیش بیاید که در این بخش به آنها میپردازیم.
رناتوراسیون چیست؟
بازسازی شکل اولیه ماکرومولکول پس از دناتوره شدن «رناتوراسیون» (Renaturation) نام دارد.
واسرشت چیست ؟
واسرشت همان دناتوره شدن پروتئین یا DNA است.
الکل دناتوره چیست ؟
«الکل دناتوره» (Denatured Alcohol)، اتانولی است که به کمک مواد افزودنی، خاصیتی سمی و تلخمزه پیدا کرده است. به دلیل تداخل ترکیبات افزودنی با ساختار DNA، از این الکل نباید برای دناتورهکردن مولکول DNA، در آزمایشگاه استفاده کنیم.
تفاوت دناتوراسیون و انعقاد پروتئین
دناتوراسیون از دست دادن ساختار عملکردی پروتئین است. اما «انعقاد» (Coagulation) به حالتی گفته میشود که پروتئین بهدلیل تغییر ساختار در اثر افزایش دما، اسید یا عوامل مکانیکی، رسوب میکند. در واقع دناتوراسیون مرحله اول انعقاد است.
دلیل قدرت دناتوره کنندگی اوره چیست ؟
اوره مولکولی با دو گروه عاملی آمید و یک کربونیل است و تمایل بالایی به ایجاد پیوند هیدروژنی دارد. دو مکانیسم متفاوت برای دناتوره شدن پروتئین توسط اوره پیشنهاد میشود. یکی از آنها اثر مستقیم بر مولکول پروتئین دارد و دیگری با بههمریختن نظم مولکولی اطراف، باعث دناتوره شدن این بیومولکول میشود.
- روش مستقیم: اوره با اتصال به گروه های پپتیدی بهوسیله پیوند هیدروژنی یا الکترواستاتیک باعث ضعیف شدن پیوندهای هیدروژنی درونمولکولی و سبب دناتوراسیون پروتئین میشود.
- روش غیرمستقیم: اوره بین مولکولهای آبی که اطراف بخشهاغی آبگریز هستند قرار میگیرد و در شبکه پیوندی تغییر ایجاد میکند. این کار منجر به انحلالپذیری بیشتر، تضعیف اثرات آبگریزی و در نهایت دناتوراسیون پروتئین میشود.













سلام وقت بخیر مطالب بسیار عالی و با زبان ساده بیان شده بود. با سپاس
عالی کامل و خیلی بدرد بخور بود.
خدا امواتتون رو بیامرزه و خیرتون بده