زیست شناسی مصنوعی چیست؟ – به زبان ساده
زیست شناسی علمی برای بررسی حیات است. شاخههای این علم ساختارهای مختلف سلولی، مولکولی و بیوشیمیایی را در سلولهای یوکاریوتی و پروکاریوتی بررسی میکند. زیست شناسی مصنوعی یکی از شاخههای این علم است که از رشتههای مختلف و تکنولوژی برای درک بهتر فرایندهای زیستی و تولید ابزارها و روشهای درمانی جدید کمک میگیرد. در این مطلب تعریف زیست شناسی مصنوعی و کاربردهای آن را با مثال توضیح میدهیم.
- یاد میگیرید زیستشناسی مصنوعی چیست و چه رویکردهایی دارد.
- با فناوریها و کاربردهای نوین زیستشناسی مصنوعی در پزشکی و صنعت آشنا میشوید.
- توانایی تشخیص و مقایسه سیستمهای دارورسانی و سلولهای مصنوعی را بهدست میآورید.
- تفاوتهای اصلی زیستشناسی مصنوعی و زیستشناسی سامانهای را خواهید آموخت.
- یاد میگیرید بیوسنسورها و سیستمهای بدون سلول چگونه کار میکنند.
- میآموزید زیستشناسی مصنوعی چه نقشی در کشاورزی و کامپیوترهای زیستی دارد.

زیست شناسی مصنوعی چیست ؟
زیست شناسی مصنوعی شاخهای از علم است که از ترکیب کردن رشتههای مختلف مهندسی و زیست شناسی برای تولید ابزارها و سیستمهای زیستی استفاده میکند. تعریفهای متفاوتی برای این علم وجود دارد.
- علمی که از ترکیب مهندسی فیزیک و ژنتیک برای خلق شکلهای جدید حیات استفاده میکند.
- علم نوظهوری که تلاش میکند با ترکیب دانش و روشهای زیستشناسی، مهندسی و رشتههای مرتبط در زمینه سنتز شیمیایی DNA، ارگانیسمهای جدید با ویژگیهای منحصربهفرد یا بهبودیافته خلق کند.
- علمی که برای طراحی و ساخت سیستمها، ماشینها و مدلهای زیستی جدید یا طراحی مجدد سیستمهای زیستی موجود برای اهداف مشخص، کاربرد دارد.
- استفاده از الگوی مهندسی ساخت سیستمها برای طراحی سیستمهای قابل پیشبینی و قوی با ویژگیهای جدیدی که در طبیعت وجود ندارد.
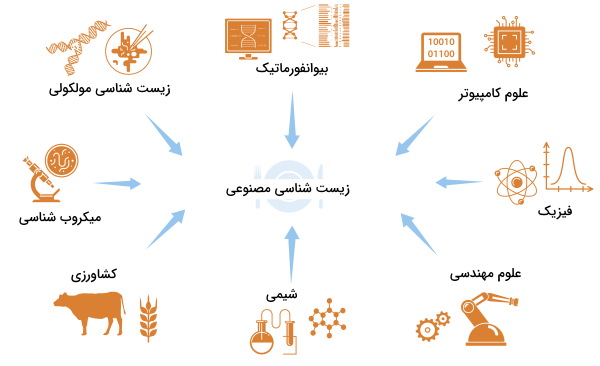
زیست شناسی مصنوعی را میتوان مثل سایر سیستمهای مهندسی به دو روش «بالا به پایین» (Top Down) و «پایین به بالا» (Bottom Up) تقسیمبندی کرد.
- در روش بالا به پایین از روشهای متابولیک و مهندسی ژنتیک برای ایجاد یک ویژگی جدید در سلولهای زنده استفاده میشود.
- در روش پایین به بالا از مولکولها و پلیمرهای غیرزنده در محیط آزمایشگاه (in vitro) برای ایجاد یک سلول زنده جدید استفاده میشود.
تاریخچه زیست شناسی مصنوعی
این واژه اولین بار در سال ۱۹۱۰ و در یکی از مقالات زیستشناس فرانسوی، استفان لدوس (Stéphane Leduc) مطرح شد. لدوس معتقد بود بررسی سیستمهای زیستی و موجودات زنده بهوسیله علم فیزیک و شیمی، علاوه بر اینکه به فهم بهتر این سیستمها کمک میکند، امکان سنتز سیستمهای «زیستتقلید» (Biomimic) را برای انسان فراهم خواهد کرد.

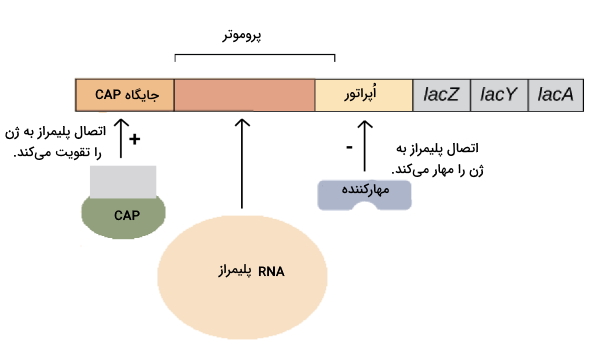
در سال ۱۹۶۱ جاکوب و مونود با بررسی اپران lac در ژنوم باکتری ای. کولی تنظیم مولکولی سیستمهای زیستی را بررسی کردند. تحقیق آنها تصویری جدید از ویژگیهای مولکول در سلولهای زنده ایجاد کرد و پایه بسیاری از اطلاعات امروز ما از رونویسی، ترجمه و تنظیم ژنها است.
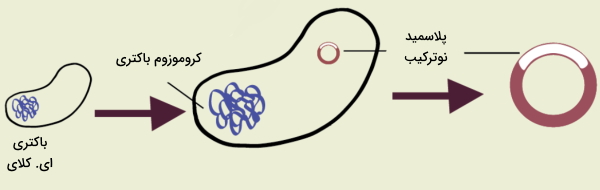
اولین «کلونینگ» (Cloning) و تکثیر DNA در سال ۱۹۷۳ توسط کوهن و همکارانش با استفاده از پلاسمید انجام شد. تحقیقات این دانشمندان اولین قدم در زیست شناسی مصنوعی و مکانیسم خلق سلولهای زنده مشابه بود. کوهن و بویر موفق شدند پلاسمیدهای موجود در سیتوپلاسم باکتری ای. کلای را استخراج و به سلول زنده دیگر منتقل کنند. تحقیقات آنها مفهوم جدید از علم ژنتیک و زیست شناسی به نام DNA نوترکیب را به دنیا معرفی کرد. کوهن و بوهر برای این کار بخشی از DNA ریبوزومی قورباغه را با پلاسمید باکتری ترکیب و بهوسیله سیستم مولکولی باکتری تکثیر کردند.
پنج سال پس از تحقیقات کوهمن و بویر، جایزه نوبل پزشکی برای کشف «آنزیمهای محدودکننده» (Restriction Enzymes) به آربر، ناتان و اسمیث اهدا شد. این آنزیمها قیچیهای دئوکسی ریبواسید نوکلئیک هستند که بهوسیله آنها میتوان بخشهای مختلف یک DNA یا DNA گونههای مختلف را برای بررسی مولکولی برش داد. این آنزیمها علاو بر تسهیل سنتز DNA نوترکیب، امکان سنتز ژنهای جدید بهوسیله زیست شناسی مصنوعی را فراهم میکنند.
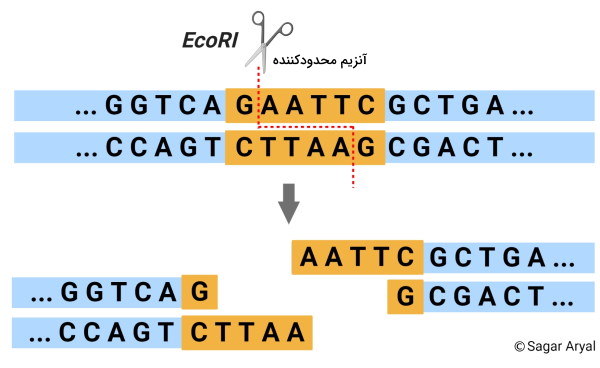
با انجام اولین PCR در سال ۱۹۸۸ بهوسیله مولیس و همکارانش، قدم بعدی در پیشرفت زیست شناسی مصنوعی برداشته شد. واکنش زنجیره پلیمراز یا PCR مجموعهای از چرخههای تکثیر DNA بهوسیله یک DNA پلیمراز مقاوم به گرما در مدت زمان بسیار کوتاه است. کشف این واکنش نه تنها امکان تکثیر DNA، بلکه بررسی جهشها و توالییابی ژنوم گونههای مختلف را فراهم کرد.
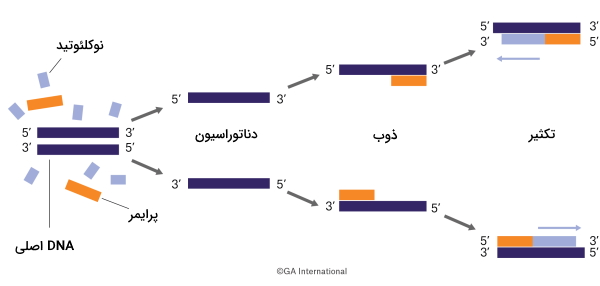
در سالهای اول قرن ۲۱ زیست شناسی مصنوعی قدمهای بسیاری در ساخت سلولهای زنده مهندسی شده برداشت. اولین کنفرانس بین المللی زیست شناسی مصنوعی، نخستین داروهای پروتئینی سنتز شده در ای. کلی، مدارهای الکتریکی که سرعت حمله باکتریایی به سلولهای سرطانی را افزایش میدهند، سنتز اولین ژنوم مصنوعی باکتری بهوسیله روشهای شیمیایی و ژنوم مخمر، و مهندسی بازوهای کروموزمی عملکردی در مخمر از دست آوردهای مختلف این سالها بود.
در سال ۲۰۲۰ میلادی اولین «زنوبوتها» (Xenobots) ساخته شدند. این ساختارهای زنده مصنوعی بهوسیله الگوریتمهای کامپیوتری و بافتهای زنده مختلف طراحی شدهاند تا عملکرد مشخصی برای مثال جمعآوری ذرات پلاستیک اقیانوس، را انجام دهند.
کاربرد زیست شناسی مصنوعی
زیست شناسی مصنوعی علاوه بر اینکه شناخت ما از فرایندهای زیستی و موجودات زنده را افزایش میدهد، مسیر جدید برای ساخت ابزارهای مختلف در صنایع مختلف ازجمله کشاورزی، پزشکی، داروسازی، محیط زیست و صنایع غذایی در اختیار ما قرار میدهد. زیستتقلید بودن این ابزارها احتمال آلودگیهای محیطزیستی و ایجاد خطرات جانبی برای انسان را کاهش خواهد داد. به علاوه در سیستمهای بر پایه سبلول معمولا نیاز است ژنوم سلول توالییابی شود و بهوسیله وکتور مناسب وارد سلول میزبان شود. این فرایند سرعت روشهای زیست شناسی مصنوعی را کاهش و درصد خطا را افزایش میدهد. به همین دلیل ایده زیست شناسی مصنوعی بدون سلول شکل گرفت.
حسگرهای زیستی کدامند ؟
حسگرهای زیستی یا بیوسنسورها ساختارهای زیستی-الکترونی هستند که تغییرات زیستی محیط برای مثال حضور توکسینها یا فلزات سنگین در آب را تشخیص میدهند. انواع بسیار زیادی از این سیستمها وجود دارد که بر اساس برهمکنش آنتیبادی-آنتیژن، تولید محصول جدید بهوسیله واکنشهای آنزیمی، برهمکنش رسپتور-لیگاند و فعالیت باکتریها عمل میکند. تمام این سیستمها از یک بخش «شناساگر» (Detector)، «مبدل» (Transducer) و «آشکارساز» (Reader) تشکیل میشوند.
- شناساگر: این بخش ساختاری زیستی است که با آنالیت برهمکنش میکند. این بخش ممکن است آنتیبادی، آنزیم یا رسپتور استخرج شده از یک سلول زنده یا ساختارهای زیستی سنتز شده با کمک مهندسی ژنتیک یا ساختارهای زیستتقلید باشد.
- مبدل: مبدل بخشی از بیوسنسور است که برهمکنش شناساگر با آنالیت را به تغییر شیمیایی یا الکتریکی قابل اندازهگیری تبدیل میکند. مکانیسمهای «نوری» (Optical)، «پیزوالکتریک» (Piezoelectric)، «الکتروشیمیایی» (Electrochemical) و «الکترولومینسانس» (Electrochemiluminescence) ازجمله مکانیسمهایی هستند که در حسگرهای زیستی مختلف کاربرد دارند.
- آشکارساز: آشکارساز بخشی الکتریکی این سیستمها است که پیام مبدل را به شکل اعداد و نمودار برای کاربر نمایش میدهد.
انواع شناساگر بیوسنسور
آنتیبادیها مولکولهای پروتئینی بسیار تخصصی هستند که تنها به یک نوع آنتیژن متصل میشوند. به همین دلیل یکی از گزینههای مناسب برای شناساگر بیوسنسورهای تخصصی به حساب میآیند. اتصال این دو مولکول به هم تغییرات کنفورماسیونی به وجود میآورد که میتوان آن را به کمک مولکولهای شناساگر (رنگ فلوئورسنت، آنزیم یا رادیوایزوتوپها) به سیگنال قابل اندازهگیری تبدیل کرد. یکی از معایب مهم این شناساگرها حساسیت زیاد برهمکنش به pH و ترکیبات محیط است. به علاوه این پروتئین ها وزن مولکولی بالایی دارند و تولید آنها فرایندی هزینهبر است. زیست شناسی مصنوعی با سنتز قطعات (Fab، Fv و scFv) و دومینهای (VH و VHH) اتصالی نوترکیب به کمک بیوسنسور آمد.
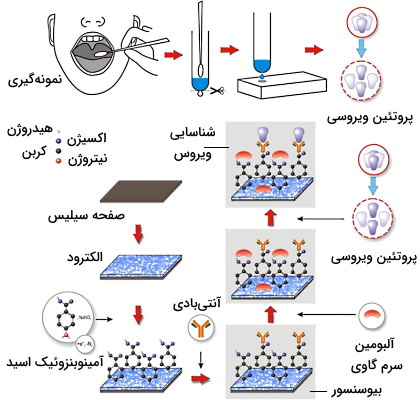
پروتئینهای متصل شونده به آنتیژن (AgBP) گروهی دیگر از پروتئینهای مهندسی شده و جایگزین آنتیبادیها هستند که وزن بسیار کمتری (کمتر از ۱۰۰ آمینواسید) دارند. نبود پیوند دیسولفیدی در ساختار این پروتئینها، پایداری ساختار را افزایش میدهد.
شناساگرهای آنزیمی تعداد زیادی از واکنشهای متفاوت را کاتالیز میکنند و آنالیتهایی که میتوان بهوسیله آنها بررسی کرد بسیار متنوعتر از شناساگرهای آنتیبادی است. استفاده از آن راحتتر است و از آنزیم میتوان بارها استفاده کرد. عامل محدودکننده طول عمر این سنسورها، پایداری آنزیم است. این شناساگرها از مکانیسمهای مختلفی برای شناسایی ترکیبات زیستی استفاده میکنند.
- آنالیت را به مولکولی قابل شناسایی بهوسیله بیوسنسور تبدیل میکنند.
- آنالیت مهارکننده یا فعالکننده آنزیم است.
- تغییرات کنفورماسیونی آنزیم پس از اتصال به سوبسترا بهوسیله شناساگر تشخیص داده میشود.
گروه دیگر شناساگرهای بیوسنسورها، اسیدهای نوکلئوئیکی هستند. در این بیوسنسورها، شناساگر توالی اسید نوکلئوئیکی یا آپتامر (اسید نوکلئیک بر پایه آنتیبادی) است. در نوع اول این شناساگر، تغییر نوری ایجاد شده بهوسیله اتصال جفت بازهای مکمل بین شناساگر و آنالیت بهوسیله سنسور تشخیص داده میشود. آپتامرها توالی نوکلئوتیدی تکرشتهای و کوچکی هستند که علاوه بر اسید نوکلئیک، پروتئینها، پپتیدها، توکسینها و سلولهای زنده را شناسایی میکنند.
در بعضی از بیوسنسورها از بافت، سلولها یا یکی از اندامکهای مشخص درون سلولی ازجمله لیزوزوم، میتوکندری و کلروپلاست برای شناسایی آنالیتها استفاده میشود. برای مثال میتوکندری یکی از اندامکهای فعال در متابولیسم یون کلسیم است. به همین دلیل میتوان از آن در بیوسنسورهای تشخیص کلسیم استفاده کرد.
مبدل های بیوسنسور
در ابتدای بخش بیوسنسور توضیح دادیم که انواع مختلفی از مبدلها، برهمکنش شناساگر-آنالیت را به پیام قابل اندازهگیری تبدیل میکنند. مبدلهای الکتروشیمیایی معمولا در سنسورهایی استفاده میشوند که واکنش آنزیمی بهوسیله انتقال الکترون (اکسایش-کاهش) انجام میشود. کانالهای یونی، دسته دیگری از مبدلها هستند که اتصال شناساگر-آنالیت سبب تغییر کنفورماسیون آنها باز شدن کانال و جریان یونها خواهد شد. پارامتر قابل اندازهگیری در این بیوسنسورها، تغییر الکتریکی حاصل از جریان یون است.
مبدلهای فلوئورسنت یکی از پرکاربردترین انواع مبدل در حسگرهای زیستی هستند. تغییر تابش نور این مولکولها پس از برهمکنش آنالیت-شناساگر، سیگنال قابل اندازهگیری بخش الکتریکی است. استفاده از مولکولهای فلوئورسانسی که طیف نشری آنها با آمینواسیدهای آروماتیک ازجمله تریپتوفان تفاوت دارد، حساسیت، دقت و کاربرد بیوسنسور را افزایش میدهد.
مبدلها میدان مغناظیسی و پیزوالکتریک، گروه آخر مبدلهای حسگرهای زیستی هستند. مبدلهای مغناطیسی ذرات یا بلورهای پارامغناطیس یا فرومغناطیسی هستند که شناساگر در سطح آنها قرار میگیرد. اتصال شناساگر-آنالیت این بار ویژگیهای مغناطیسی این مواد را تغییر میدهد که آشکارساز آن را تبدیل به سیگنال قابل اندازهگیری تبدیل خواهد کرد. مبدلهای پیزوالکتریک، بلورهای جامدی هستند که شکل آنها با تغییر پتانسیل الکتریکی به شکل برگشتپذیر تغییر میکند. بلور کوارتز یکی از این مبدلها است.
صنایع غذایی
«کشاورزی سلولی» (Cellular Agriculture) از ترکیب مهندسی بافت، بیوتکنولوژی، زیست شناسی مولکولی و زیست شناسی مصنوعی برای طراحی و ایجاد روشهای جدید برای سنتز چربیها، پروتئینها بافتهای مختلف استفاده میکند. تمرکز این بخش بیشتر بر تولید محصولات جانوری ازجمله لبنیات گوشت در محیط آزمایشگاه و بهوسیله کشت سلولی است تا پرورش و کشتار حیوانات را کاهش دهد. برای سنتز این محصولات از دو روش زیست شناسی مصنوعی بدون سلول و باکتریهای مهندسی شده استفاده میشود. شکل زیر تصویر استیکی را نشان میدهد که دانشمندان در سال ۲۰۲۱ با استفاده از با استفاده از روش چابگر سهبعدی و سلولهای گاوی ساختند.
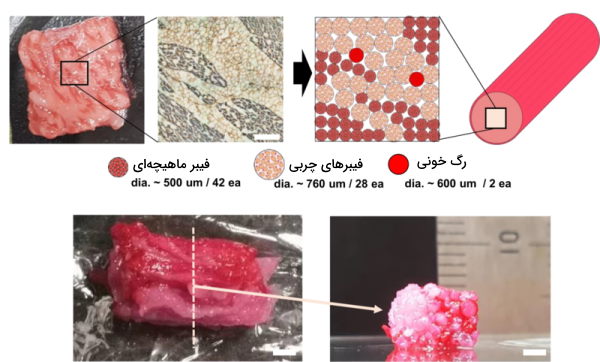
کامپیوتر های زیستی
مغز کامپیوتر زیستی بسیار پیچیدهای است که تمام فعالیتهای انسان را کنترل میکند. کامپیوترهای زیستی یا آلی از مولکولهای زیستی به جای مدارهای الکتریکی برای انجام معادلات محاسباتی استفاده میکنند. این کامپیوترهای آلی دقیقا مثل کامپیوترهای الکتریکی، دیتاهای مختلف را دریافت و تحلیل میکنند. برای بهتر عملکرد این کامپیوترها، سنتز پروتئین را در نظر بگیرید. اطلاعات حیاتی در DNA ذخیره شده است (ورودی). این اطلاعات بهوسیله واکنشهای آنزیمی و استفاده از آمینواسیدها، RNA و ریبوزوم (معادلات محاسباتی) به پروتئین (خروجی) تبدیل میشود. برای ساخت این مدار در این کامپیوترها میتوان از ترکیب مواد آلی طبیعی یا سنتزی، DNA دستکاری شده برای ذخیره و تحلیل دیتا یا ساخت ژنوم عملکردی جدید بهوسیله زیست شناسی مصنوعی استفاده کرد. کامپیوترهای بیوشیمیایی، بیومکانیکی و بیوالکتریکی سه گروه اصلی این سیستمها هستند.
کامپیوترهای بیوشیمیایی
این کامپیوترها از لوپهای بازخوردی فراوانی که ویژگی واکنشهای بیوشیمیایی است برای انجام محاسبات بهره میبرند. بازخورد مثبت و منفی دو مکانیسم واکنشهای بیوشیمیایی هستند که افزایش یا کاهش خروجی مسیرهای بیوشیمیایی را تنظیم میکنند. تعداد آنزیمهای شرکتکننده در واکنشها، غلظت واکنشدهندهها و مولکولهای تنظیمی ازجمله کوفاکتورها و کوآنزیمها در این بازخوردها نقش دارند. بررسی و شناسایی دقیق این مسیرها و مولکولهای موثر در تنظیم آنها این امکان را فراهم میکند که بتوان این سیستم را بهوسیله یک ورودی دیگر تغییر داد.
کامپیوترهای بیومکانیکی
تفاوت این کامپیوترها با انواع بیوشیمیایی در این است که در کامپیوترهای بیوشیمیایی غلظت شیمیایی مواد داده ورودی سیستم است. اما در کامپیوترهای مکانیکی، ویژگیهای مکانیکی یک مولکول مشخص یا مجموعهای از مولکولها به عنوان ورودی و تغییر آن خروجی سیستم در نظر گرفته میشود. ساختار مکانیکی و سهبعدی محصول در این نوع کامپیوترها به عنوان خروجی محاسباتی شناسایی و تفسیر میشود.
کامپیوترهای بیوالکتریکی
در این کامپیوترها، تغییر رسانایی الکتریکی طبیعی خروجی است که اندازهگیری میشود. خروجی از مولکولهایی تشکیل شده است که به طور تخصصی برای انتقال جریان الکتریکی در یک مسیر بسیار تخصصی و بر اساس شرایط اولیه طراحی شدهاند.
ترانسفورماسیون سلولی
در زیستشناسی مولکولی و ژنتیک ترانسفورماسیون ایجاد تغییر در ژنوم یک سلو.ل برای ایجاد پروتئینهایی با ویژگی های ساختاری و عملکردی دلخواه است. سلولها برای پاسخ به سیگنالهای محیط، برقراری ارتباط با سایر سلولها و محافظت از خود از برهمکنش ژنوم و پروتئینهای مختلف استفاده میکنند. از دیدگاه مهندسی، میتوان ارتباط بین ژنها و پروتئینها را مدار الکتریکی یک وسیله الکترونی در نظر گرفت. با ترکیب زیست شناسی مصنوعی و علم مواد میتوان از مدار ژنتیکی سلولهای مختلف برای سنتز مولکولهای زیستی با ویژگیهای دلخواه استفاده کرد. سنتز پیشماده داروی «آرتمیسین» (Artemisinin) با استفاده از پلاسمیدهای باکتری ای. کلی یکی از مثالهای ثابت شده این کاربرد زیست شناسی مصنوعی است. این لاکتون، دارویی است که برای درمان مالاریا استفاده میشود.
طراحی پروتئین
مهندسی پروتئینهای طبیعی بدن امکان استفاده از پروتئينها در صنایع داروسازی، آرایشی، غذایی و حتی چرمسازی را افزایش میدهد. این ترکیبات سازگاری بیشتری با بدن دارند و عوارض جانبی کمتری ایجاد میکنند. به علاوه به کمک آنها میتوان مکانیسمهای مولکولی داخل بدن موجود زنده را دقیقتر بررسی کرد یا کارایی پروتئینهای طبیعی را افزایش داد. برای مثال گروهی از دانشمندان با ایجاد تغییر در آلفا هلیکسهای هموگلوبین، مولکول نوترکیبی سنتز کردند که توانایی اتصال به اکسیژن را دارد اما به دیاکسید کربن متصل نمیشود.
تولید آنزیمهای صنعتی با فعالیت بالا، بازده بهینه و اثربخشی زیاد، یکی از پر طرفدارترین کاربردهای طراحی پروتئین بهوسیله زیست شناسی مصنوعی است. از این روش میتوان برای سنتز دترجنتها و محصولات لبنی فاقد لاکتوز استفاده کرد.
سلول های مصنوعی
سلولهای مصنوعی ساختارهای غشایی هستند که مولکولهای زیستی را محصور میکنند. یکی از اهداف زیست شناسی مصنوعی فهمیدن منشا حیات، مسیرهای زیستی و تولید موجود زنده جدید به کمک مولکولهای زیستی و آلی در آزمایشگاه است. دانشمندان تلاش میکنند سلولهایی جدید با عملکردهای متنوع از تولید داروها تا پاکسازی آلودگیهای محیطی ایجاد کنند. لیپوزومهای دارای مولکولهای زیستی ازجمله سلولهای مصنوعی هستند. اولین سلول زنده با DNA مصنوعی در سال ۲۰۱۴ تولید شد که دانشمندان ژنوم باکتری ای. کلای را با ژنومی جدید جایگزین کردند.
به علاوه، این سلولها را میتوان به شکل ساختارهای دوبعدی حالت جامد سنتز کرد. سلولهای مصنوعی و دوبعدی سنتز شده از سلیکون، توانایی انجام متابولیسمهای ساده، فعالیت ساده مدار ژنتیکی و ارتباط بین بخشهای مختلف را دارند.
طراحی سیستم های دارورسانی
داروها دامنه وسیعی از مولکولهای شیمیایی و زیستی هستند که با انجام یک عملکرد مشخص در بدن یا مهار یک فرایند زیستی در بهبود وضعیت سلامت فرد نقش دارند. بلع، استنشاق، جذب پوستی و تزریق، چهار مسر اصلی برای ورود این مواد به بدن هستند. اما ممکن است دارویی که از راه دهان وارد معده میشود و باید ترشح صفرا را مهار کند، بهوسیله پپسین یا اسید معده غیرفعال شود یا فعالیت آن کاهش یابد. به همین دلیل نیاز به سیستمهای پیشرفتهتری است تا دارو مستقیم به بافت هدف برسد و با کمترین عوارض جانبی بیشترین اثر را برای بیمار داشته باشد. زیست شناسی مصنوعی با طراحی سیستمهای دارورسانی در به نتیجه رسیدن این مسیر نقش فراوانی دارد. در این بخش سیستمهای دارورسانی بر پایه سلولهای مهندسی شده و نانوذرات را بررسی میکنیم.
سیستمهای بر پایه سلول باکتری
از این سیستمها معمولا برای انتقال داروهای پروتئینی استفاده میشود. برای مثال ژن پپتیدی که یک نوع خاص گیرنده یا پروتئین سطح سلولهای سرطانی را شناسایی میکند وارد DNA باکتری میشود. رونویسی و ترجمه ژن باکتریایی، انتقال پپتید به سطح غشای پلاسمایی را به دنبال خواهد داشت. پس از ورود باکتری به بدن، پپتید سطحی آن فقط با گیرنده اختصاصی خود برهمکنش میدهد و کل باکتری یا مولکول دارو وارد سلول میشود.
به علاوه میتوان تغییراتی در سلول باکتریایی ایجاد کرد که تغییرات محیط اطراف تومور (برای مثال کاهش غلظت اکسیژن) را تشخیص دهد و با لیز شدن یا سیستم ترشحی خود، مولکول دارو را به سلول هدف منتقل کند. به علاوه میتوان رهایش دارو را بهوسیله سیگنالهای خارج سلولی (مواد شیمیایی، امواج الکترومغناطیس و امواج نوری) القا کرد. سالمونلا تیفیموریوم ( Salmonella typhimurium)، ای. کلای ( Escherichia Coli)، بیفیدوباکتریا (Bifidobacteria)، استرپتوکوکوس (Streptococcus)، لاکتوباسیلوس (Lactobacillus)، لیستریا ( Listeria) و باسیلوس سابتیلیس (Bacillus subtilis) انواع باکتریهستند که در این سیستم دارورسانی میتوان از آنها بهره برد.
سیستمهای بر پایه سلول یوکاریوتی
سیستم ایمنی نقش بسیار مهمی در مهار سرطان دارد و میتوان با دستکاری سلولهای آن، توانایی حمله به تومورها را افزایش داد. بخشی از سلول درمانی برپایه ایمنی درمانی و کمک سلولهای T مهندسی شده انجام میشود. در این روش مهندسی ژنتیک و تغییر رسپتورهای سطحی سلولهای T امکان شناسایی آنتیژنهای سطح سلولهای توموری را افزایش میدهد. این روش درمانی در پنج مرحله کلی انجام میشود.
- سلول T از بدن بیمار استخراج میشود.
- ژن کدکننده رسپتور کایمریک وارد ژن سلول T میشود.
- بیان ژن جدید، سلول T را به رسپتور اختصاصی نوع خاصی از آنتیزن سلولهای توموری تبدیل میکند.
- سلول T نوترکیب در محیط کشت مناسب تکثیر میود.
- سلول T به بیمار منتقل میشود. تا با فعال کردن سیستم ایمنی تومور را از بین ببرد.
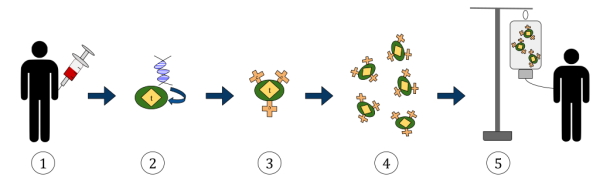
رسپتورهای کایمریک آنتیژن (Chimeric antigen receptors| CARs) از یک قطعه آنتیبادی تشکیل میشود که به دومین داخل سلولی و شرکتکننده در مسیرهای پیامرسانی رسپتور T متصل شده است. سلولهای T، و برای درمان به روش CAR T Cell استفاده میشوند. این سلولها داروی زنده در بدن هستند. زمانی که رسپتور سطحی این سلولها به آنتیزن هدف در سطح سلولهای تومور متصل شود، مسیر تکثیر و سیتوتاکسیسیتی سلولهای T فعال میشود. استفاده از این روش درمانی در سال ۲۰۱۷ به وسیله FAD تایید شد.
علاوه بر درمان سرطان، میتوان از این روش درمانی برای بیماریهای خودایمنی بهره برد. با ترکیب سلولهای T تنظیمی با آنتیژنهای CAR میتوان مقاومت سیستم ایمنی بدن به یک نوع آنتیژن را افزایش داد. با کمک این روش میتوان واکنشهای ایمنی پس از پیوند عضو و بیماریهای خودایمنی ازجمله روماتیسم را کنترل کرد. مثل هر روش درمانی دیگر استفاده از CAR T CELL ها عوارض جانبی دارد و سندروم رهایش سیتوکین یکی از عوارض متداول استفاده از این روش درمانی است که منجر به ترشح تعداد زیادی سیتوکین التهابی از سلولهای ایمنی میشود. این حالت علائمی شبیه عفونت خونی ازجمله تب بالا، بیحالی، احساس تهوع، گرفتگی و درد ماهیچه، تاکیکاردی (افزایش ضربان قلب)، از کارافتادگی کبد و کلیه نشان میدهد. این علائم نشان میدهد درمان CAR T CELL موفق بوده و سیستم ایمنی در حال مبارزه با سلولهای توموری است.
نوروتاکسیسیتی یکی دیگر از عوارض روش درمانی CAR T Cell است. هذیان، تشنج و کاهش هوشیاری ازجمله علائم این اختلال است. در این وضعیت توانایی صحیح صحبت کردن بیمار کاهش مییابد، اما هنوزر توانایی فهمیدن کلمات دیگران را دارد.
ساختار CAR
ساختارهای CARs از چهار بخش دومین شناسایی آنتیژن، لولای خارج سلولی، دومین عرض غشایی و دومین داخل سلولی تشکیل میشود.
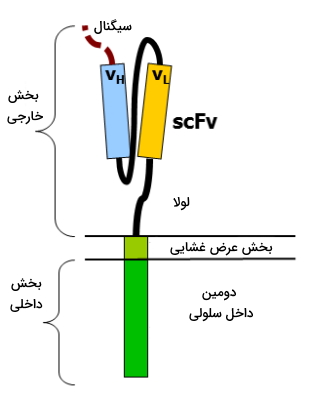
- دومین شناساییکننده آنتیژن: خارج غشای سلولهای T قرار میگیرد و بخش اصلی است که با آنتیژن برهمکنش میدهد. این بخش معمولا از ناحیه متغیر آنتیبادی مونوکلونال مشتق میشود و پروتئین کایمری است که از اتصال یک زنجیره سبک () و زنجیره سنگین () بهوسیله یک زنجیره پلیپپتیدی به هم تشکیل میشود (scFv). زنجیره پپتیدی بین دو جایگاه شناسایی آنتیژن، از آمینواسیدهای هیدروفیل گلایسن و سرین با انعطافپذیری زیاد و گلوتامات و لیزین برای افزایش انحلالپذیری تشکیل شده است.
- لولا یا جداکننده: بخش کوچکی است که دومین خارج سلولی را به دومین عرض غشایی و داخل سلولی متصل میکند. این بخش از CAR انعطافپذیر ناحیه خارج سلولی را افزایش و مقاومت فضایی بین ناحیه حارجی و داخلی را کاهش میدهد. توالی آمینواسیدهای این بخش معمولا بر اساس ناحیه عرض غشایی IgG، CD8 و CD28 است.
- ناحیه عرض غشایی: از چند آلفا هلیکس هیدروفوب تشکیل میشود که بخش شناساگر را به غشای پلاسمایی سلول T قلاب میکند و در پایداری رسپتور نقش بسیار مهمی دارد.
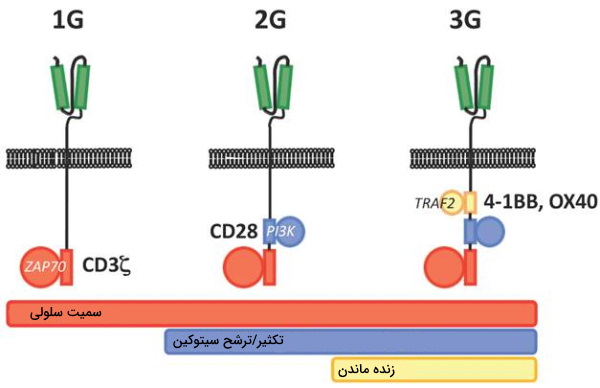
- دومین انتقال پیام داخل سلولی: این بخش معمولا دومین داخل سلولی رسپتورهای زتا CD3 است که بهوسیله مسیر تیروزین کینازی تکثیر و فعال شدن سلولهای T را تنظیم میکند. سه نسل از این دومین وجود دارد.
- نسل اول: این دومینها تنها از دومین داخل سلولی زتا CD3 تشکیل میشود.
- نسل دوم: در این دومینها یک بخش کمکی برای تحریک بهینهتر مسیرهای سیگنالینگ سلول اضافه شد. CD28 و ۴۱BB ازجمله دومینهای کمک تحریکی این نسل بودند.
- نسل سوم: بیش از یک دومین کمک تحریکی برای افزایش پیامرسانی به دومین داخل سلولی اضافه شد.
به علاوه برای افزایش کارایی این روش درمانی، مسیرهای تنظیمی مختلف به سلول T اضافه شده است تا عوارض جانبی و احتمال آسیب به سلولهای سالم را کاهش دهد.
- کلید خاموشکننده: یک یا دو ژن مسیر آپوپتوز که بهوسیله محرکهای خارجی فعال میشوند، به ژنوم سلولهای T اضافه خواهد شد. تیمیدین کیناز ویروس هرپس سیمپلکس (HSV-TK) و کاسپاز ۹ دو ژن آپوپتوزی هستند که میتوان از آنها برای تنظیم این سلولها بهره برد.
- رسپتور دوگانه آنتیژن: در این روش دومین اتصالی به آنتیزن برای دو آنتیزن سطحی طراحی میشود. به همین دلیل احتمال اتصال رسپتور به سلولهای سالم کاهش میباید.
- کلید روشنکننده: در این روش سلولهای T تنها در حضور دو آنتیژن توموری و مولکول غیر سرطانی خارجی فعال میشود. در این روش رسپتور اتصالی به آنتيژن، دو بخش پروتئینی جدا است که برای فعال شدن باید به هم متصل شوند. یکی از این دومینهای پروتئینی شامل بخش متصل شونده به آنتیژن است و دومینهای شرکتکننده در پیامرسانی و کمک تحریکی در بخش پروتئینی دیگر قرار دارند. در حضور یک مولکول خارجی ازجمله آنالوگهای رمپامایسین، دیمری شدن این پروتئينها سبب فعال شدن و اتصال CAR T Cell به تومور میشود.
- کلیدهای دو میزبانه: در این نوع تنظیم رسپتورهای CAR برای آنتیژن توموری و مولکول CD3 طراحی میشوند. در نتیجه بدون حضور یکی از این پروتئینهای سطح سلولی اتصال رسپتور-لیگاند و فعال شدن سلولهای T انجام نمیشود.
دارورسانی بهوسیله ساختارهای نانو
با استفاده از ترکیب زیستشناسی، مهندسی مواد، فیزیک و شیمی میتوان نانو ذراتی سنتز کرد که به دارورسانی و تشخیص بیماریها کمک فراوانی میکنند. برای مثال استفاده از این ذرات در شیمیدرمانی، کمک میکند دارو فقط بر سلول تومور اثر داشته باشد و عوارض جانبی درمان را کاهش میدهد. انواع مختلفی از این ساختارها در دارورسانی استفاده میشوند.
نانوذرات لیپیدی
نانوذرات لیپیدی ساختارهای کروی هستند که حداقل از یک لایه لیپیدی تشکیل میشوند. زیستتخریبپذیری، زیستسازگاری، فراهمیزیستی، امکان انتقال مولکولهای بزرگ، امکان ایجاد تغییرات سطحی و روشهای سنتز سادهتر این نانوذرات را به ساختارهای مناسبی برای انتقال دارو تبدیل کرده است. این نانوذرات اولین ساختارهایی بودند که کاربرد بالینی آنها بهوسیله FAD تایید شد. لیپوزومها انواعی از نانوذرات لیپیدی پرکاربرد در صنایع داروسازی هستند.
نانوذرات پلیمری
این نانوذرات بهوسیله پلیمرهای طبیعی (آلژینات، کیتوزان) و سنتزی (اتیلن آمین و آمیدو آمین) و با استفاده از روشهای متفاوتی ازجمله تهیه امولسیون، رسوبگذاری، ژلی شدن یونی و میکروجریانها (microfluidics) سنتز میشوند. در این روش مولکول دارو بهوسیله پلیمر کپسوله میشود، بین ماترکیس پلیمری قرار میگیرد یا بهوسیله روشهای شیمیایی به سطح مولکول متصل (Conjugated) میشود. به همین دلیل امکان انتقال همزمان چند دارو یا سنتز ناوذرات تشخیصی-درمانی (Theranostics) بهوسیله این پلیمرها وجود دارد.
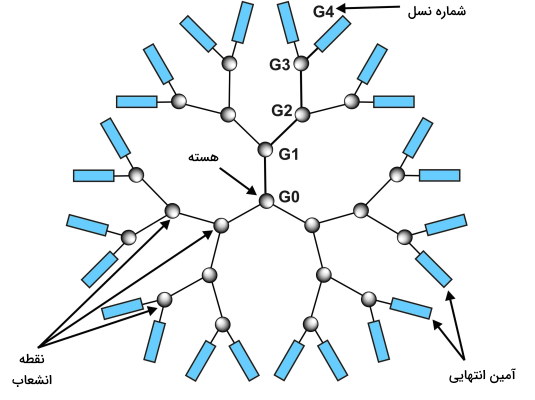
دندریمرها دسته دیگری از نانوذرات پلیمری هستند. این ذرات از یک هسته مرکزی و تعداد زیادی انشعاب پلیمری تشکیل میشوند. مولکول دارو بین شاخهها، در هسته پلیمری یا سطح شاخهها قرار میگیرد. برای سنتز این نانوذرات از پلیمرهای آمینی استفاده میشود و بر اساس تعداد گروههای عاملی آمین سطحی به چهار نسل ، (۳ گروه آمین) ،(۶ گروه آمین) (۱۲ گروه آمین) و (۲۴ گروه آمین) تقسیم میشوند.
نانوذرات معدنی
از نانوذرات معدنی سیلیکا، طلا و آهن در تصویربرداری پزشکی، درمان و تشخیص بیماریها استفاده میشود. این ذرات بر اساس روش سننتز و نقشی که در بدن دارند در شکلها و اندازههای مختلف سنتز میشوند. نانوذرات طلا از پرکاربردترین انواع این ناوذرات هستند که در شکلهای کروی (nanospheres)، میلهای (nanorods)، ستارهای (nanostars)، پوسته (nanoshells) و قفس (nanocages) ساخته میشوند. برای مثال میتوان آنتیبادی پروتئینهای سطحی سلولهای سرطانی را روی این نانوذرات قرار داد. تابش پرتو لیزر پس از اتصال آنتیبادی-لیگاند، سبب گرم شدن نانوذره و از بین رفتن سلول سرطانی میشود.
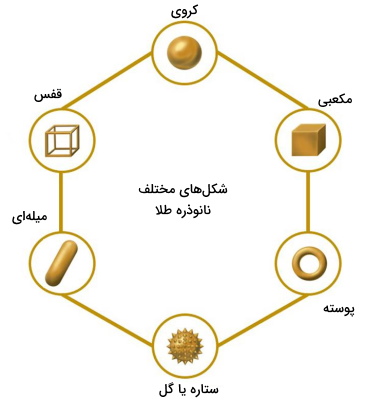
ساختارهای نانو بر پایه کربن
فورلرنها، نانولولههای کربنی و گرافن ازجمله نانوساختارهای بر پایه کربن هستند که در مهندسی بافت، دارورسانی، بیوسنسورها و ژنرسانی از آنها استفاده میشود. یکی از مزیتهای این ساختارها توانایی رسانایی و توانایی انتقال جریان در آنها است که سبب میشود کاندید مناسبی برای داربستهای مهندسی بافت عصبی باشند. نانولولههای کربنی به دو شکل تکلایه و چندلایه سنتز میشوند. این ساختارها را میتوان بهراحتی و با پیوند کوالانسی به پپتیدها، مولکولها دارو، اسید نوکلئوئیک یا پروتئینهای مختلف متصل و برای دارورسانی هدفمند استفاده کرد.
زیست شناسی مصنوعی بدون سلول
زیست شناسی مصنوعی با طراحی سیستمهای بر پایه سلولهای مهندسی شده شروع شد. بسیاری از بیوسنسورها، پروتئينهای نوترکیب، مهندسی بافت و درمان به کمک سلولهای T مهندسی شده (CAR T Cell) همه تکنولوژیهای وابسته به سلول در زیستشناسی هستند. اما استفاده از آنها با محدودیتهایی همراه است. برای مثال توانایی تکثیر سلول بهوسیله میتوز، شرایط نگهداری این سامانهها در محیط آزمایشگاه را دشوار میکند و احتمال آلودگیهای مضر برای انسان را افزایش میدهد.
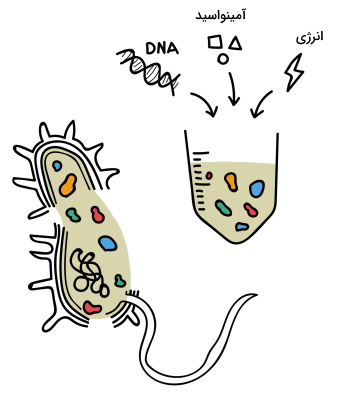
سیستمهای زیست شناسی مصنوعی بدون سلول، از مجموعه آنزیمها و مولکولهای زیستی تشکیل میشوند که فرایند زیستی اصلی (همانندسازی، رونویسی و ترجمه) را بدون نیاز به سلول انجام میدهند. این سیستمها از سلولهای یوکاریوتی (مهرهداران، گیاهان، مخمرها، حشرات و قارچها)، پروکاریوت یا مولکولهای آلی آزمایشگاهی تشکیل میشوند. سیستمهای زیست شناسی مصنوعی بدون سلول را میتوان در آزمایشگاه فیلتر و آلودگیهای مضر برای سلامت انسان را از آن حذف کرد. به علاوه نگهداری این سیستمها از سیستمهای بر پایه سلول بسیار راحتتر است. میتوان از فریزدرای برای نگهداری سیستمهای بدون سلول بهره برد و در زمان مورد نیاز با اضافه کردن آب به سیستم، از آن استفاده کرد.
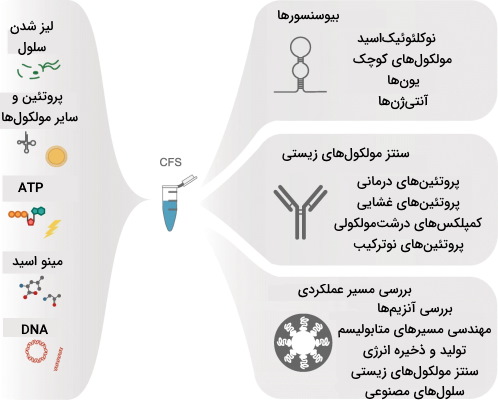
تفاوت زیست شناسی مصنوعی و سامانه ای چیست ؟
«زیست شناسی سامانهای» (System Biology) شاخهای از این علم است که اجزای مختلف یک موجود زنده را به شکل یک شبکه یکپارچه بررسی میکند. هدف این علم ایجاد روشهای جدی برای مطالعه سیستمهای زیستی به عنوان یک واحد کلی است. برای مثال زیست شناسی سامانهای در بررسی میکروبها، نه تنها روشهای سازگاری، تکامل و برقراری ارتباط با محیط و گونههای دیگر را نظر میگیریم بلکه پروفایل و پویایی RNA، پروتئين و متابولیتها را مشخص میکند. به علاوه مکانیسمهای برهمکنش و شبکه تنظیمی این مولکولهای زیستی را بررسی میکند.
تمرکز دانشمندان زیست شناسی سامانهای بر جمعآوری، طبقهبندی و آنالیز مجموعه دیتاهای بزرگ ازجمله اطلاعات ژنومیک (جمعآوری و آنالیز ژنوم موجود زنده) و پروتئومیک (جمعآوری و آنالیز کل محتوای پروتئینی یک موجود زنده) است.
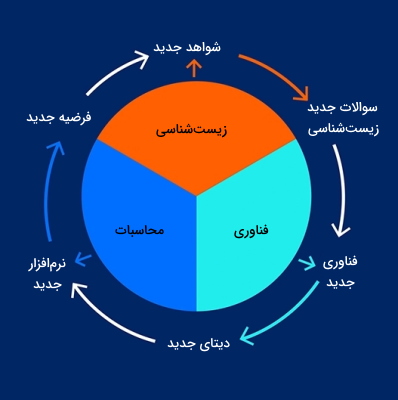
اما تمرکز دانشمندان زیستشناسی مصنوعی بر ساخت ابزارها، بخشی از موجود زنده یا مسیرهای زیستی جدید برای انجام عملکردی متفاوت است. سلولهای باکتری یکی از پرکاربردترین سامانهها در این شاخه از زیستشناسی هستند و میتوان آنها را کارخانهی تولید پروتئینها، آنزیمهای صنعتی، داروها، سوخت زیستی و مولکولهای شیمیایی نامید.
برای مثال زیستشناسی سامانهای با بررسی توالی نوکلئوتیدی در ژنوم هر موجود زنده، اطلاعات کاربردی در مورد ژنهای ساختاری، عملکردی و تکاملی در اختیار دانشمندان قرار میدهد. زیستشناسی مصنوعی از این اطلاعات طبقهبندی شده برای دستکاری و مهندسی ژنوم جاندار استفاده میکند تا رسپتوری بساز که به یک نوع آنتیژن خاص در سطح سلول سرطانی متصل میشود.
جمع بندی
در این مطلب توضیح دادیم که زیست شناسی مصنوعی بهوسیله ترکیب کردن زیستشناسی و رشتههای فیزیک، شیمی و مهندسی ابزارها یا سیستمهای جدیدی برای تولید داروها، سیستمهای محاسباتی، آنزیمهای صنعتی و سلولهای مصنوعی ایجاد میکند. به کمک این علم و استفاده از دارورسانی هدفمند میتوان عوارض جانبی دراوهای شیمیایی و درصد بهبوبد بیماران را افزایش داد. به علاوه حسگرهای زیستی که به کمک مهندسی ساختارهای زیستی تولید میشود، اممکان تشخیص سریعتر را برای پزشکان فراهم میکند. اما در نظر داشته باشید این علم جدید مسیر طولانی پیش رو دارد.












