تبرید چیست؟ – با مثال و تمرین
گرما و سرما دو چهره مختلف دما هستند که در زندگی خود آنها را حس میکنیم. «گرمسازی» (Heating) فرآیندی است که در آن تلاش میکنیم تا دما را بالا ببریم و در نقطه مقابل آن، «تبرید یا سردسازی» (Refrigeration) فرآیندی است که در آن تلاش میکنیم با حذف گرما، فضا یا ماده موردنظر خود را سرد کنیم. «یخچال» (Refrigerator)، کولرگازی یا چیلر وسایلی هستند که این کار را انجام میدهند. در این مطلب از مجله فرادرس میخواهیم توضیح دهیم تبرید چیست، اصول ترمودینامیکی آن چه هستند و چگونه ایجاد میشود. همچنین در ادامه با ارائه چند مثال از کاربرد سیکل تبرید و تهیه سوالاتی بهعنوان آزمون، به شما کمک میکنیم تا درک عمیقتری از مفهوم تبرید بهدست آورید.
- با مفهوم تبرید و اهمیت آن در صنایع مختلف آشنا میشوید.
- میتوانید اصول عملکرد سیکل تبرید تراکمی و اجزای آن را درک کنید.
- مفهوم مبردها، کمپرسور، کندانسور، شیر انبساط و اواپراتور را میآموزید.
- رابطه بین دما، آنتروپی، فشار و آنتالپی را درک میکنید.
- با انواع سیکل تبرید مانند جذبی، گازی و ترموالکتریکی آشنا میشوید.
- میتوانید تفاوت مفاهیمی مانند سوپرهیت، سابکول و قانون دوم ترمودینامیک را تشخیص دهید.


تبرید چیست؟
به فرآیند حذف گرما از یک ماده، فضا یا سیستم و سردسازی آن تا دمایی کمتر از دمای واقعی آن، تبرید، سرمایش، سردسازی یا چگالش گفته میشود. طی فرآیند تبرید، انرژی گرمایی از محیطی با دمای کم حذف شده و به محیطی با دمای بالاتر دفع میشود. معمولا در سیستمهای تبرید از مواد خاصی به نام «مبرد» (Refrigerant) جهت جذب گرما از محیط موردنظر و دفع آن در محیط دیگر استفاده میشود.
برای اینکه مفهوم تبرید را بهتر متوجه شوید، یک مثال ساده میزنیم. یک لیوان آب یخ را در نظر بگیرید. با گذشت زمان و جذب گرما از محیط اطراف، دمای آب و یخ داخل لیوان زیاد میشود. در حالی که دمای محیط اطراف کاهش خواهد یافت. این مبادله گرما تا زمانی که آب و یخ داخل لیوان با محیط اطراف همدما شوند، ادامه مییابد. اساس کار تبرید نیز شبیه این مثال است.

چنین فرآیندهای انتقال گرمایی پیشتر توسط ابزارهای مکانیکی مثل یخ یا ماشینهای الکترومکانیکی انجام میشد. در دوران روم و یونان باستان، از یخهای کوهها بهعنوان سردکننده غذا استفاده میشد. بنابراین میتوانیم بگوییم نگهداری و حفظ غذا، چالشی بود که در نهایت منجر به توسعه فرآیند تبرید شد. امروز میدانیم میتوان این فرآیند را توسط گرما، مغناطیس، الکتریسیته و لیزر نیز انجام داد. تبرید کاربردهای خیلی گستردهای دارد، از یخچالهای خانگی تا فریزرهای صنعتی، سیستمهای تهویه هوا و «صنعت کرایوژنیک یا برودتی» (Cryogenic). همچنین از گرمای خروجی طی فرآیند تبرید، در پمپهای گرمایی استفاده میشود.
اصول تبرید
در بخش قبل تا حدی متوجه شدیم که تعریف تبرید چیست. در این بخش میخواهیم یک سری اصول مقدماتی در مورد این موضوع را توضیح دهیم تا درک دقیقتری از تبرید داشته باشیم. اولین مفهومی که در مواجه با تبرید یا سردسازی با آن سروکار داریم، گرما است. اگر دانشآموز دهم هستید و به دنبال یادگیری بیشتر از طریق حل مثال و تمرین در مورد مباحث ترمودینامیکی و گرما، میتوانید فیلم آموزشی فیزیک پایه دهم - مرور و حل تمرین فرادرس را مشاهده کنید:
گرما نوعی انرژی است که به واسطه اختلاف دما منتقل میشود. پس چون انرژی است، نمیتواند خود به خود از بین برود یا ایجاد شود، بلکه به شکل دیگری از انرژی تبدیل خواهد شد. البته معمولا این انواع دیگر انرژی هستند که به گرما تبدیل میشوند.
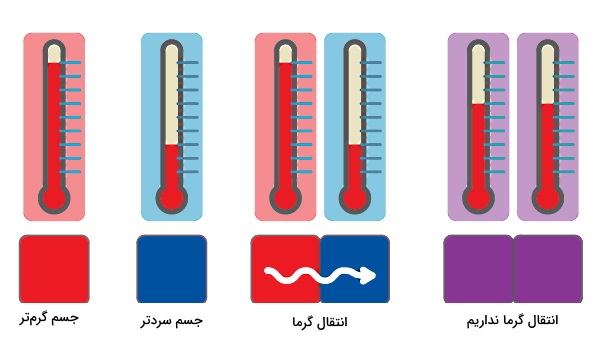
نکته مهم در مورد گرما این است که به یاد داشته باشیم گرما همیشه در یک جهت مشخص جاری میشود و آن جهت، از ماده یا فضایی با دمای بالاتر به ماده یا فضایی با دمای پایینتر است. مفهوم مقابل گرما، سرما است. سرما کمبود گرما است و لزوما به معنای حذف کامل گرما از یک ماده نیست. حالا میتوانیم سردسازی یا تبرید را به این صورت تعریف کنیم، فرآیندی که در آن گرمای ناخواسته از یک ماده حذف و به ماده دیگری منتقل میشود. حذف گرما دمای ماده را کاهش خواهد داد.

چرخه یا سیکل تبرید بر مبنای این اصل مهم کار میکند که وقتی مایعی به گاز تبدیل میشود (تبخیر)، از محیط اطراف خود گرما دریافت میکند. یک آزمایش ساده این اصل مهم را بهخوبی توصیف میکند. یکی از انگشتان دست خود را خیس کنید. اگر آن را به سمت بالا و در مقابل جریان هوا بگیرید، در این انگشت نسبت به سایر انگشتان دست خود، احساس سرما خواهید کرد. علت این است که با قرار دادن این انگشت در مقابل جریان هوا، عمل تبخیر آب انجام میشود که همراه با دریافت گرما از پوست انگشت شما و هوای اطراف است. بنابراین در این انگشت احساس سرما میکنید.
مبرد چیست؟
پیش از اینکه ببینیم اجزای یک سیکل تبرید چیست، در این بخش کمی در مورد مبرد بیشتر توضیح میدهیم. ماده مهمی که بهعنوان سردکن در سیستمهای تبرید بکار میرود، مبرد نام دارد. مبرد یک ترکیب شیمیایی است که به شکل مایع متراکم شده است و زمانی که با استفاده از تجهیزات مکانیکی خاصی برای چرخش در سیستم تبرید پمپ شود، قابلیت انبساط به شکل گاز یا بخار را دارد. این ماده از مواد غذایی داخل یخچال گرما میگیرد و این گرما را به محیط منتقل میکند.

در شکل بالا چند نمونه گاز مبرد متداول نشان داده شده است که برای مثال R134A نوعی گاز مبرد بدون کلرید است و در حال حاضر از آن زیاد استفاده میشود. میتوان از یک ماده طبیعی یا یک ترکیب شیمیایی ساخته شده بهعنوان مبرد استفاده کرد. مهم این است که روی این ماده یک سری فرآیندهای ترمودینامیکی انجام شود و در انتقال گرما نیز کمک کند. مبرد با جذب گرما از ماده دیگر، مانند یک محیط سردکننده در اواپراتور عمل میکند.
یادگیری تبرید با فرادرس برای دانشآموزان
در بخش قبل متوجه شدیم که اصول اولیه برای یادگیری تبرید چیست. اگر دانشآموز هستید و تمایل دارید به مباحث ترمودینامیک در مقطع متوسطه کاملا مسلط شوید، پیشنهاد میکنیم این فیلمهای آموزشی فرادرس را مشاهده کنید:
- فیلم آموزش فیزیک پایه دهم فرادرس
- فیلم آموزش فیزیک دهم – مرور و حل تمرین فرادرس
- فیلم آموزش رایگان دما و گرما در فیزیک پایه دهم فرادرس
اجزای یک سیکل تبرید
گفتیم که اصول تبرید چیست و با مفهوم اساسی چرخه تبرید یعنی فرآیند تبخیر آشنا شدیم. در سیکل تبرید هدف این است گرمای ناخواسته از یک ماده حذف شود و در جای دیگری تخلیه شود. برای اینکه چنین عملکردی داشته باشیم، لازم است مبرد در یک سیستم بسته پمپ شود. اگر سیستم بسته نباشد، مقدار خیلی زیادی مبرد لازم است، چون در هر سیکل، مبرد به محیط بیرون دفع میشود. اما در یک سیستم بسته، همان مقدار مبرد را بارها و بارها میتوان بکار گرفت.
سیکل تبرید بر اساس چهار فرآیند فیزیکی مهم کار میکند که بهترتیب شروع در سیکل عبارتاند از:
- «تراکم» (Compression)
- «میعان» (Condensation)
- «انبساط» (Expansion)
- «تبخیر» (Evaporation)
تراکم یا انقباض به معنای کاهش حجم ماده، میعان نوعی تغییر حالت ماده از گاز به مایع، انبساط افزایش حجم ماده و تبخیر هم نوعی تغییر حالت ماده از مایع به گاز است. پس در این چهار فرآیند، فقط دو تغییر حالت داریم. این چهار فرآیند به ترتیب در چهار بخش مهم به نامهای «کمپرسور» (Compressor)، «کندانسور» (Condenser)، «شیر انبساط» (Expansion Valve) و «تبخیرکننده یا اواپراتور» (Evaporator) انجام میشود.
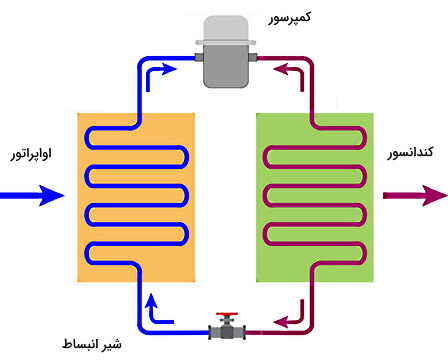
در شکل بالا دو پیکان بنفش و آبی در سمت چپ و راست شکل مشخص شدهاند که کل فرآیند تبرید را توضیح میدهند. در یک سیکل تبرید، در بخش اواپراتور اصل فرآیند سردسازی یا تبرید انجام میشود. به این ترتیب که با دریافت گرما از محیط، مبرد در این قسمت تبخیر میشود و سپس در بخش کندانسور، گرمایی که توسط مبرد از محیط دریافت شده بود، تخلیه یا دفع میشود.
بهتر است پیش از اینکه این چهار فرآیند را در سیکل بررسی کنیم، ابتدا «دما یا نقطه اشباع» (Saturation Temperature) را نیز توضیح دهیم. نقطه اشباع، دمایی است که در آن ماده طی یک فرآیند فشار ثابت تغییر فاز یا تغییر حالت میدهد. در واقع دو تغییر حالت این سیکل، یعنی میعان و تبخیر هر دو در دمای اشباع مبرد رخ میدهند و طی فرآیند تغییر حالت، دمای مبرد ثابت و برابر با دمای اشباع آن است.
شکل زیر شماتیکی از یک سیکل تبرید را بر اساس چهار فرآیندی که گفتیم نشان میدهد. در سمت راست شکل، «لولههای مارپیچی یا پیچههای» (Coils) مربوط به کندانسور قرار دارند و در سمت چپ پیچههای اواپراتور یا تبخیرکننده. جزئیات اجزای سیکل تبرید خیلی گسترده است. برای مثال انواع مختلفی کمپرسور وجود دارد اما اصول عملکرد همه آنها یکی است.
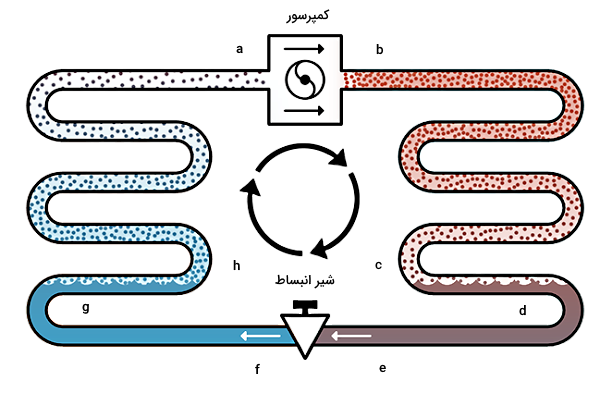
اصول عملکرد سیکلی که در ادامه توضیح میدهیم، برای انواع سردکننده شامل یخچال، فریزر، سیستمهای تهویه هوا و چیلرهای صنعتی یکسان است. اما مبرد یا اندازه تجهیزات بسته به نوع کاربرد متفاوت است. در بخشهای بعد بر اساس تصویر بالا و نقاطی که روی آن مشخص کردهایم، جزئیات هر کدام از فرآیندهای مهم این سیکل را شرح میدهیم.
تراکم و کمپرسور
بخش قبل تا حدودی معرفی کرد که اجزای یک سیکل تبرید چیست. بر اساس آخرین شکل بخش قبل، سیکل تبرید از نقطه a شروع میشود. مبرد که در حالت بخار است، توسط کمپرسور مکش و سپس متراکم میشود. در نتیجه فشار، دما و انرژی بخار متراکم شده به سرعت افزایش مییابد، در حالی که حجم آن کم میشود. فرآیند تراکم در نقطه b تمام میشود. در کل سیکل تبرید، در نقطه b دما و انرژی بخار مبرد بالاترین مقدار خود را دارد. در شکل زیر نمونه سادهای از یک فرآیند تراکم برای مولکولهای گاز داخل یک بطری را مشاهده میکنید.
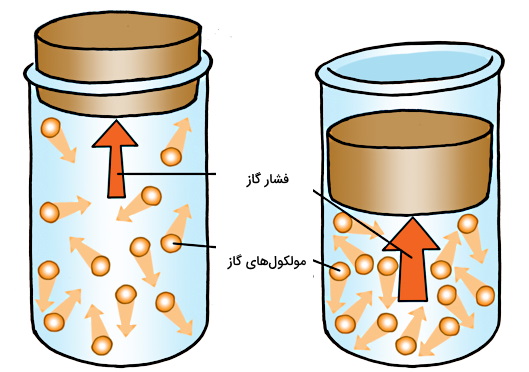
پس کمپرسور بخاری با دما و فشار پایین که از اواپراتور خارج شده است را به بخاری با دما و فشار بالا تبدیل میکند تا برای تغییر حالت میعان آماده شود. کمپرسور یک وسیله مکانیکی محسوب میشود و به گونهای طراحی شده است تا فشار گاز را با کاهش حجماش، زیاد کند. معمولا کمپرسور را قلب یک چرخه تبرید در نظر میگیرند و مهمترین بخش این سیستم است. به کمپرسور موتور یخچال هم گفته میشود. این قطعه در سیکل تبرید مانند یک پمپ کار میکند و همزمان چرخش مبرد در سیکل را نیز کنترل میکند.

پارامتری که مشخصه عملکرد کمپرسور در یک سیکل تبرید است، نسبت تراکم نام دارد که با نشان داده میشود. نسبت تراکم برابر است با نسبت فشار گاز در خروجی کمپرسور (بخش تخلیه کمپرسور) () به فشار آن در ورودی (بخش مکش کمپرسور) ():
بسته به اینکه در ساخت کمپرسور از چه تکنولوژی استفاده شده باشد، فرآیند تراکم در جزئیات متفاوت انجام خواهد شد. معمولا مقدار گرمای مشخصی طی این فرآیند در کمپرسور تولید میشود که حتما لازم است خارج شود تا عملکرد و بازدهی کمپرسور را دچار مشکل نکند. نکته مهم دیگر این است که کمپرسور برای متراکمسازی بخار طراحی شده است و ورود مایع به کمپرسور، موجب اختلال در عملکرد آن خواهد شد. انواع مختلف کمپرسورها به شکل زیر طبقهبندی میشوند:
| انواع کمپرسور | ||||
| دینامیکی | جابجایی مثبت | |||
| جریان مخلوط | گریز از مرکز | جریان محوری | دورانی | رفت و برگشتی |
میعان و کندانسور
در بخش قبل توضیح دادیم که کمپرسور در سیکل تبرید چیست و چه کاری انجام میدهد. پیش از اینکه به فرآیند میعان در سیکل برسیم، نقطه b را در نظر بگیرید. فاصله بین نقطه b و c، فرآیند سرد شدن این بخار داغ با فشار بالا را نشان میدهد. این سرد شدن تا رسیدن به شرایطی که بخار شروع به میعان کند، ادامه خواهد داشت و انرژی و حجم بخار نیز به تدریج کم میشود. در نقطه c، بخار نه تنها دیگر خیلی داغ نیست، بلکه کاملا سرد شده است.
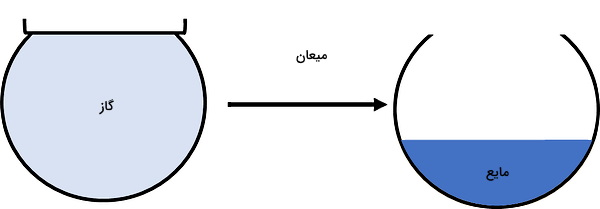
حالا فرآیند تغییر حالت میعان بین نقاط c و d اتفاق میافتد. در این تغییر حالت، بخار اشباع به مایع اشباع تبدیل خواهد شد. در نتیجه، انرژی خیلی زیادی به شکل گرما آزاد میشود که لازم است دفع یا تخلیه شود. فرآیند میعان در دما و فشار ثابت رخ میدهد و در نقطه d تمام میشود. بنابراین کندانسور با استخراج گرما، بخار را به مایع تبدیل میکند. در واقع چون دمای میعان مبرد از دمای هوای محیط بالاتر است، طی فرآیند انتقال گرما، مبرد از بخار فشار بالا به مایع اشباع شده فشار بالا تبدیل میشود.

ظرفیت کندانسور به اختلاف بین دمای محیط و دمای میعان مبرد بستگی دارد. اگر دمای محیط کم شود، این اختلاف دما زیاد خواهد شد که منجر به افزایش ظرفیت کندانسور نیز میشود. شکل زیر عملکرد کندانسور را با جزئیات بیشتری نشان میدهد. از قسمت پایین شکل، مبرد در فاز بخار با دما و فشار بالا وارد لولههای مارپیچی کندانسور میشود که به علت دمای بالای مبرد، لولهها در این قسمت با رنگ نارنجی نشان داده شدهاند.
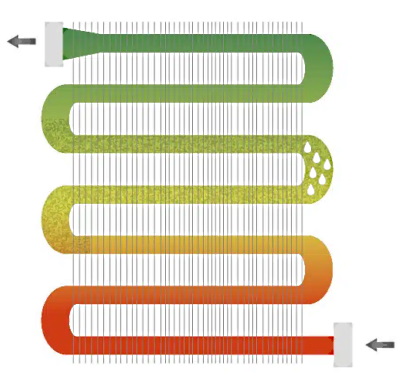
با چرخش هوای بیرون در اطراف لولهها، میعان اتفاق میافتد و بخار به مایع تبدیل میشود. تغییر حالت بخار به مایع با چند قطره در شکل نمایش داده شده است. مایع اشباع شده و تا حد کمی سابکول شده در قسمت بالای لولهها، کندانسور را ترک میکند و به سمت شیر انبساط جاری میشود.
سابکول چیست؟
گفتیم که کندانسور در سیکل تبرید چیست و چگونه عمل میکند. از نقطه d تا e فرآیند «سابکول» (Subcooling) یا به اختصار SC اتفاق میافتد. اشاره شد که پیش از مرحله میعان مبرد سرد میشود تا به دمای اشباع خود برسد. سپس تغییر حالت انجام میشود. اما سرد شدن مبرد در نقطه d متوقف نمیشود، بلکه باز هم سردتر میشود. به مرحله سرد شدن مبرد پس از میعان، سابکول گفته میشود. پس سردسازی مبرد در مرحله سابکول نیز همچنان توسط کندانسور انجام میشود.

سابکول باعث میشود مبردی که میخواهد وارد بخش شیر انبساط شود، دمای کمتری داشته باشد. در نتیجه پس از انبساط، حجم کمتری از مبرد تبخیر میشود و به دنبال آن، گرمای بیشتری برای تبخیر بیشتر مبرد از محیط جذب خواهد شد. پس سابکول با جذب گرمای بیشتر، موجب افزایش بازدهی شده است.
اگر بخواهیم سابکول را دقیقتر معرفی کنیم، برابر است با اختلاف بین دمای میعان مبرد با دمایی که مبرد در ابتدای ورود به شیر انبساط دارد. برای محاسبه این اختلاف، میتوانیم دمای مبرد در ابتدای ورود به شیر انبساط و فشار بخش تخلیه در قسمت کمپرسور را اندازهگیری کنیم. به این ترتیب دمای میعان مبرد بهدست خواهد آمد و در نتیجه، اختلاف دما قابل محاسبه است. البته اگر فرض کنیم در مرحله تخلیه یا در بخش کمپرسور اتلاف فشار نداریم.
افزایش سابکول به معنای افزایش ظرفیت سردسازی تجهیزات سیستم است. بهعنوان یک قانون کلی، برای هر ۲ درجه سابکول مایع مبرد، حدود ۱ درصد افزایش ظرفیت سردسازی بهدست آمده است. همین مسئله باعث شده است که در طراحی کندانسورها نحوه سابکول نیز در نظر گرفته شود.
شیر انبساط
در بخش قبل یاد گرفتیم که فرآیند میعان و سابکول در چرخه تبرید چیست و چه اهمیتی دارند. در نقطه e، مبرد بهصورت یک مایع سابکول شده وارد بخش شیر انبساط میشود. سپس در نقطه f، مبرد به شکل مخلوطی از مایع و بخار از شیر انبساط خارج میشود. در واقع یک علت سابکول کردن مبرد در مرحله قبل این است که مطمئن باشیم زمانی که به شیر انبساط میرسد، حاوی هیچ گونه فاز بخاری نیست.

تبخیر و اواپراتور
در بخشهای قبل آموختیم که سه فرآیند اول در یک سیکل تبرید چیست و چگونه انجام میشوند. در این بخش به آخرین فرآیندهای چرخه تبرید یعنی تبخیر و «سوپرهیت» (Superheating) میپردازیم تا چرخه را کامل کنیم. در فاصله نقطه f تا g، گرمای دریافت شده از محیط خنک توسط اواپرتور یا تبخیرکننده به مبرد منتقل میشود. بنابراین انرژی مبرد تا حد زیادی بالا میرود. سپس تبخیر در فاصله نقطه g تا h طی یک فرآیند دما و فشار ثابت انجام میشود و در نتیجه، مبرد مایع به بخار تبدیل خواهد شد.
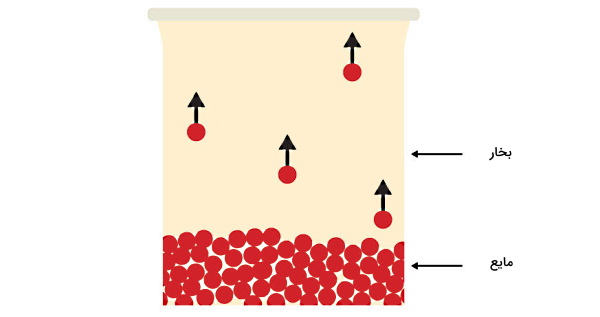
پس در نقطه h تمام مبرد به بخار تبدیل شده است و البته که بخار مبرد در دمای اشباع خود قرار دارد. به یاد داریم که هدف از یک سیکل تبرید این بود که گرمای اضافی یا موردنظر ما را از محیط یا ماده حذف کند. بنابراین این اواپراتور است که این گرما را در نهایت حذف میکند. زمانی که مایع مبرد با یک فشار کاهش یافته بهعلت عبور از شیر انبساط به اواپراتور میرسد، خیلی از هوای اطرافش سردتر است. این مسئله باعث میشود مبرد بتواند گرما را از محیط گرمتر اطراف خود جذب کند و سریعتر به به نقطه جوش نسبتا پایین خود برسد. به این ترتیب با جذب بیشترین مقدار گرما، مبرد تبخیر میشود.
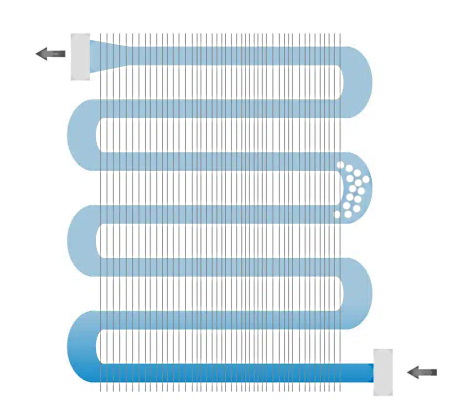
این گرما توسط مبرد به عنوان یک گاز فشار پایین، به بخش پایین کمپرسور (شکل کمپرسور در بخش تراکم و کمپرسور را نگاه کنید) منتقل میشود تا سیکل تبرید تکرار شود. در کاربردهای سیکل تبرید به منظور تهویه هوا، نیاز است فضای خیلی بزرگتری خنک شود. بنابراین لازم است حجم خیلی بیشتری از هوا از طریق پیچههای اواپراتور منتقل شود تا تهویه هوا بهخوبی انجام شود. در شکل بالا شماتیکی از یک اواپراتور را مشاهده میکنید.
از قسمت پایین، مبرد پس از عبور از شیر انبساط با فشار و دمای پایین وارد اواپراتور میشود. سپس با گرمایی که از محیط دریافت میکند، به جوش آمده و به بخار تبدیل خواهد شد. این بخش در لولههای مارپیچی شکل اواپراتور شکل بالا با مولکولهای دایرهای شکل بخار نشان داده شده است. در نهایت از قسمت بالای لولهها، مبرد اواپراتور را بهعنوان یک بخار اشباع شده و تا حدی سوپرهیت شده با فشار و دمای پایینی ترک میکند.
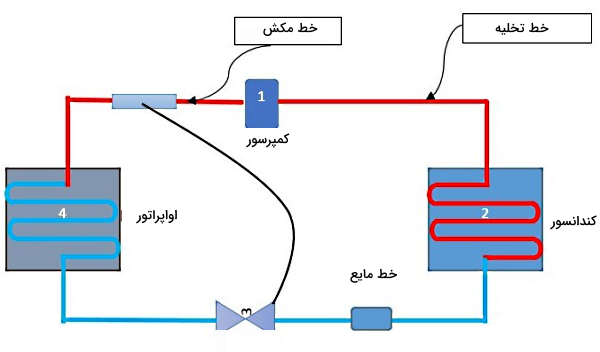
در انتهای سیکل تبرید، میخواهیم خطوط مختلفی که در این سیستم وجود دارند را معرفی کنیم. خط ارتباطی اواپراتور یا پیچههای خنککننده به کمپرسور، «خط مکش» و خط ارتباطی کمپرسور به کندانسور، «خط تخلیه یا خط گاز داغ» نامیده میشود. همچنین لولههای ارتباطی بین کندانسور و دستگاه اندازهگیری مثل شیر انبساط، «خط مایع» نام دارد.
در برخی از سیستمهای تبرید در خط مایع بین کندانسور و شیر انبساط، محفظهای برای ذخیرهسازی مبرد قرار دارد تا در صورت نیاز توسط اواپراتور استفاده شود. بنابراین یک سیکل تبرید را در نقطه شروع یعنی a، تمام کردیم. در این نقطه همانطور که گفتیم، مبرد سوپرهیت شده در بالاترین میزان حجم مشخصه خود قرار دارد و آماده است که وارد کمپرسور و مرحله تراکم شود.
سوپرهیت چیست؟
در ادامه یادگیری اینکه مراحل تبرید چیست، یک مرحله مهم و شبیه به سابکول، مرحله سوپرهیت است. از نقطه h تا a، بخار اشباع مبرد از طریق لولههای مکش جریان مییابد، در حالی که مرحله سوپرهیت هم انجام میشود. سوپرهیت به این معنا است که بخار حاصل شده با گرفتن گرمای بیشتر در دمایی بالاتر از دمای تبخیر خود قرار داشته باشد. سوپرهیت به معنای مقدار گرمایی است که مبرد پس از تبخیر دریافت میکند. محاسبه دمای لازم برای سوپرهیت مشابه با روندی است که برای سابکول گفتیم.

اگر دمای بخش مکش در ورودی کمپرسور و نقطه تبخیر در فشار داده شده برای مبرد را بدانیم، میتوانیم دمای سوپرهیت را محاسبه کنیم. با استفاده از یک فشارسنج برای اندازهگیری فشار مکش، دمای بخار سوپرهیت را بهدست خواهیم آورد. دمای تبخیر نیز با استفاده از یک دماسنج قابل اندازهگیری است.
یک نکته مهم در مورد سوپرهیت این است که ممکن است در اواپراتور یا در لوله مکش کمپرسور اتفاق بیفتد. اگر سوپرهیت داخل اواپراتور رخ دهد، سرمای مفیدی را تولید میکند. چون گرما را از محیطی که قرار بوده است سرد شود، جذب کرده است. در این شرایط سوپرهیت باعث افزایش ظرفیت یا بازدهی سیستم سردکننده خواهد شد. از طرفی، همزمان با افزایش سوپرهیت چگالی بخار مبرد نیز کم میشودو این مسئله باعث کاهش بازدهی خواهد شد. بنابراین نتیجه این دو فرآیند مخالف هم باید بررسی شود تا بتوان گفت آیا سوپرهیت در یک سیکل تبرید فرضی اثر مثبت دارد یا نه.
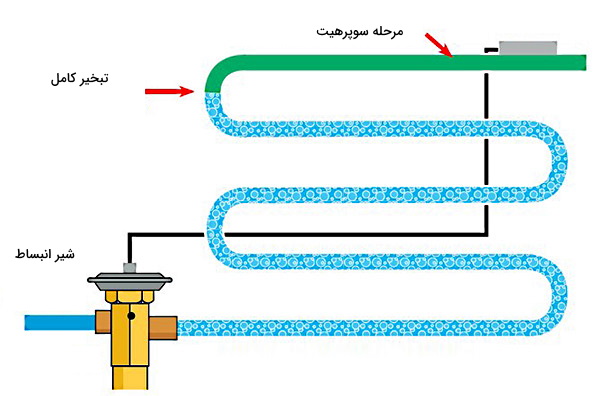
برای درک بهتر مفهوم سوپرهیت یا مفهوم عکس آن سابکول، فرض کنید یک مایع مبرد در دمای ۱۰۰ درجه در اواپراتور تبخیر میشود. میدانیم در مرحله تبخیر دما در ۱۰۰ ثابت خواهد بود. پس از اینکه تبخیر کامل انجام شد، در مرحله سوپرهیت بهطور مداوم دمای بخار مبرد افزایش داده میشود تا برای مثال به ۱۱۰ درجه برسد. علت انجام مرحله سوپرهیت مشابه چیزی است که در مورد سابکول گفتیم، میخواهیم مطمئن شویم وقتی مبرد به کمپرسور میرسد، هیچگونه فاز مایعی نداشته باشد.
ترمودینامیک سیکل تبرید
اگر بخواهیم بدانیم مهمترین روش ایجاد تبرید چیست و چگونه کار میکند، باید با جزئیات روش تبرید چرخهای بهخوبی آشنا شویم. تبرید چرخهای یا همان سیکل تبرید فرآیندی است که در آن گرما از یک ماده یا فضا با دمای پایینتر حذف میشود و به منبعی با دمای بالاتر تخلیه میشود. چنین فرآیندی به کمک انجام یک کار خارجی انجامپذیر است. در بخش «اجزای یک سیکل تبرید» عملکرد این روش را توضیح دادیم. در این بخش میخواهیم روابط ترمودینامیکی سیکل تبرید را بیان کنیم.
اصول عملکرد یک سیکل تبرید توسط «سعدی کارنو» (Sadi Carnot) در سال ۱۸۲۴ برای یک «ماشین گرمایی» (Heat Engine) یا همان پمپ گرمایی بیان شد. معکوس سیکل تبرید، چرخه توان ترمودینامیکی است. در سیکل توانی، گرما از یک منبع دما بالا برای موتور فراهم میشود، بخشی از آن صرف انجام کار میشود و باقی گرما نیز به مخزنی با دمای پایینتر تخلیه میشود. به این ترتیب، قانون دوم ترمودینامیک برقرار میماند.

بنابراین اگر شرایط مخالف توضیح بالا را در نظر بگیریم، یک سیکل تبرید خواهیم داشت. طبق شکل زیر در یک سیکل تبرید، گرما از مادهای با دمای کمتر (TL یا QL) گرفته میشود و به ماده یا در محیطی با دمای بالاتر (TH یا QH) تخلیه میشود. همانطور که گفتیم برای داشتن چنین روندی لازم است کار خارجی (Wnet,in) روی سیستم انجام شود. برای یخچال، این کار خارجی در کمپرسور انجام میشود.
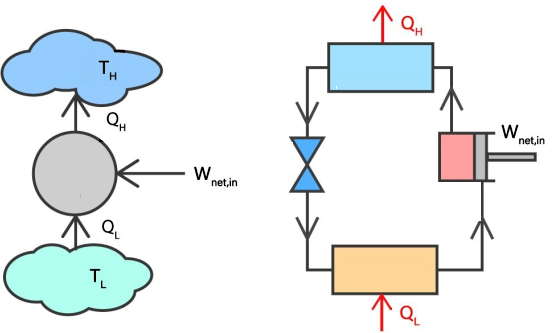
چون ماهیت گرما این است که از ماده داغ به ماده سرد جاری شود، بنابراین برای اینکه بتوانیم در یک سیکل تبرید یک فضا یا منبع را سرد کنیم، لازم است کار انجام دهیم تا گرما از منبع گرمایی با دمای کمتر به مخزن گرما با دمای بیشتر پمپ شود. همچنین عایقسازی راهحل مناسبی است که برای کاهش کار انجام شده و انرژی موردنیاز جهت حفظ دمای پایین در منبع سرد، میتوان بکار گرفت.
در شکل بالا اگر بخواهیم «ضریب عملکرد» (Coefficient of Performance) یا به اختصار COP را برای سیکل تبرید در یخچال محاسبه کنیم، فرمول زیر را بکار میبریم:
اما دقت کنید ضریب عملکرد پمپ گرمایی به شکل زیر محاسبه میشود:
در واقع اختلاف فرمول برای این دو سیستم به این برمیگردد که هدف از هر کدام چیست. برای یخچال هدف ایجاد اثر سرمایش است. پس در صورت کسر اثر سرمایشی یا دمای کمتر در نظر گرفته میشود، در حالی که برای پمپ گرمایی با هدف گرمایش در صورت کسر دمای بالاتر قرار داده میشود. مقادیر COP برای هر دو سیستم میتوانند بیشتر از یک باشند ولی رابطه بین آنها همیشه طبق فرمول بالا است.
معمولترین سیستمهای تبرید از «سیکل تبرید تراکم-بخار معکوس رانکین» (Reverse-Rankine Vapor-Compression Refrigeration Cycle) استفاده میکنند، اما بهطور کلی سیکلهای تبرید را میتوانیم در دو گروه دستهبندی کنیم:
- چرخه بخار
- چرخه گاز
همچنین تبرید چرخه بخار شامل گروهبندی زیر میشود که در زیربخشهای بعد راجعبه این دو مورد نیز توضیح خواهیم داد:
- «سیکل تراکم-بخار» (Vapor-compression Cycle)
- سیکل تبرید جذبی (تبرید جذب-بخار و تبرید جذب سطحی)
قانون دوم ترمودینامیک
برای اینکه بهتر متوجه شویم ترمودینامیک سیکل تبرید چیست، لازم است مروری داشته باشیم بر قانون دوم ترمودینامیک و مفهوم «آنتروپی» (Entropy). آنتروپی به معنای بینظمی یا آشفتگی است و به میزان انرژی گرمایی سیستم گفته میشود که برای انجام کار مفید در دسترس نیست. بنابراین هرچه آنتروپی یک سیستم بالاتر باشد، بینظمی و آشفتگی آن سیستم هم بالاتر است. آنتروپی یک خاصیت فیزیکی غیرقابلاندازهگیری است که با نماد S نشان داده میشود و واحد آن ژول بر کلوین () است.
طبق قانون دوم ترمودینامیک، تغییرات در آنتروپی با انتقال گرما معادل است. اگر تغییرات آنتروپی را با ، تغییرات گرما را با و دما را با نشان دهیم، خواهیم داشت:
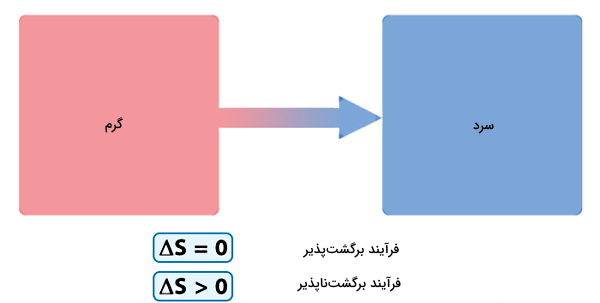
بنابراین اگر فرآیند فیزیکی «برگشتپذیر» (Reversible) باشد، انتظار داریم آنتروپی سیستم و محیط ثابت بماند. یعنی اگر آنتروپی اولیه سیستم و محیط را با و آنتروپی نهایی سیستم و محیط را با نشان دهیم، برای یک فرآیند برگشتپذیر خواهیم داشت:
همچنین قانون دوم ترمودینامیک که به قانون آنتروپی هم معروف است، بیان میکند که اگر یک فرآیند فیزیکی «برگشتناپذیر» (Irreversible) باشد، آنتروپی سیستم و محیط باید افزایش پیدا کند، یعنی آنتروپی نهایی سیستم و محیط باید از آنتروپی اولیه بیشتر باشد:
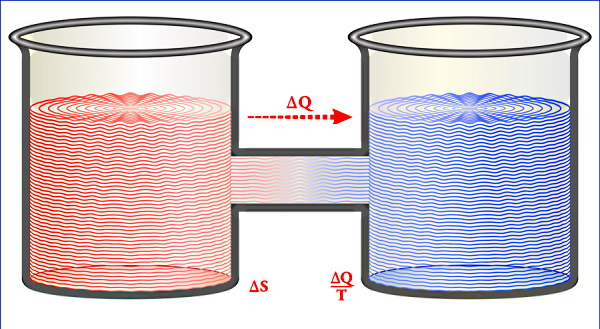
بنابراین قانون دوم ترمودینامیک توضیح میدهد که چرا گرما از مادهای با دمای بالاتر به مادهی با دمای پایینتر منتقل میشود. فرض کنید که گرما از مادهای با دمای بالاتر به نام ماده 1 در دمای به مادهای با دمای کمتر به نام ماده 2 با دمای منتقل شود. همچنین مقدار گرمای انتقال داده شده برابر با و دمای نهایی که هر دو ماده در آن دما به تعادل میرسند، برابر با باشد.
حالا اگر بخواهیم برای ماده 1 دمای میانگین یا طی این فرآیند را محاسبه کنیم، خواهیم داشت:
بهطور مشابه برای ماده 2، دمای میانگین از میانگینگیری دو دمای اولیه و نهایی برای این ماده حاصل خواهد شد:
چون در ابتدا فرض کرده بودیم که ، بنابراین انتظار داریم که . حالا اگر تغییرات آنتروپی را برای دو ماده طبق فرمول ابتدای بخش بنویسیم، خواهیم داشت:
به علامت منفی برای ماده اول توجه کنید. چون این ماده گرمتر بود و انتقال حرارت از این ماده به ماده دوم انجام شد، پس گرمای منتقل شده برای ماده اول منفی است. به همان میزانی که ماده اول گرما از دست داده است، ماده دوم گرما بهدست آورده است. پس گرمای منتقل شده برای ماده دوم مثبت است. پس تغییرات کل آنتروپی برای سیستم خواهد شد:
در رابطه بالا چون گفتیم که ، بنابراین با توجه به یکسان بودن گرمای تبادل شده بین دو ماده داریم . پس در رابطه بالا طبق پیشبینی قانون دوم ترمودینامیک، برقرار است.
رابطه دما و آنتروپی
پس از مرور قانون دوم ترمودینامیک و مفهوم آنتروپی، حالا میخواهیم ببینیم رابطه دما و آنتروپی در سیکل تبرید چیست. با توجه به چهار فرآیندی که برای سیکل تبرید شرح دادیم و فرمول آنتروپی برحسب دما در بخش قبل، نمودار دما برحسب آنتروپی برای یک سیکل تبرید به شکل زیر میشود:
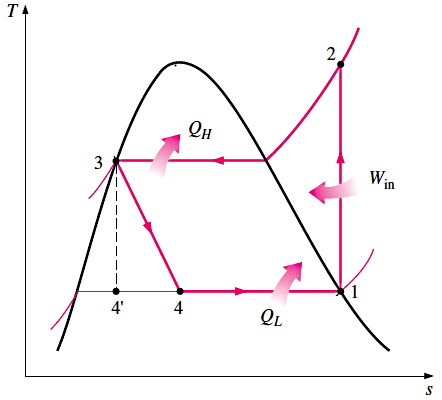
- ۱ تا ۲: تراکم بیدرردو برگشتپذیر
- ۲ تا ۳: تخلیه گرما در فشار ثابت
- ۳ تا ۴: انبساط برگشتناپذیر
- ۴ تا ۱: دریافت گرما در فشار ثابت
رابطه فشار و آنتالپی
نمودار مهم دیگری که برای یک سیکل تبرید رسم میشود، نمودار تغییرات فشار برحسب «آنتالپی» (Enthalpy) است. آنتالپی یک سیستم برابر است با مجموع انرژی درونی سیستم و حاصلضرب حجم در فشار آن. نمودار فشار برحسب آنتالپی برای یک سیکل تبرید به شکل زیر است:
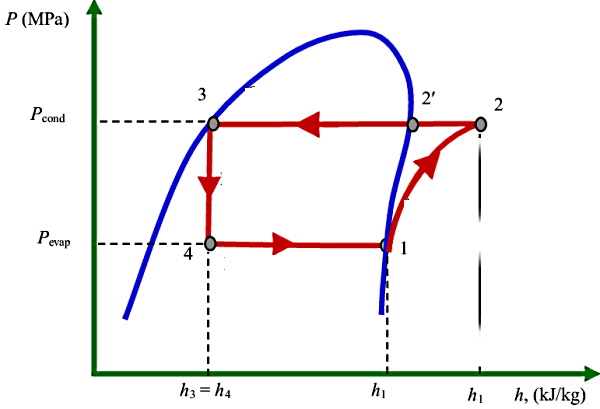
ترتیب و نوع فرآیندها در نمودار دقیقا مانند بخش قبل است. آنتالپی را با h نشان میدهند. اگر h1 آنتالپی در ورودی کمپرسور، h2 آنتالپی در خروجی کمپرسور و h۴ آنتالپی در ورودی اواپراتور باشد، تعاریف زیر را خواهیم داشت:
- اثر تبرید: اختلاف آنتالپی در نقاط ۱ و ۴ ()
- کار کمپرسور: اختلاف آنتالپی در نقاط ۱ و ۲ ()
حالا اگر بخواهیم COP را برای یک پمپ گرمایی یا یخچال محاسبه کنیم، خواهیم داشت:
بهصورت مشابه میتوانیم از رابطه زیر هم برای محاسبه COP استفاده کنیم:
سیکل تبرید تراکم-بخار
در این قسمت میخواهیم توضیح دهیم مهمترین نوع سیکل تبرید چیست. تمام توضیحاتی که برای اجزای یک سیکل تبرید و فرمولهایی که در بخشهای گذشته بیان کردیم، برای سیکل تبرید تراکم-بخار محسوب میشدند. در این بخش توضیحات دیگری در مورد این سیکل میدهیم تا تفاوتهای آن با سایر سیکلهای تبرید مشخص شود. در این نوع چرخه تبرید، مبرد دچار تغییر فاز میشود و از آن در سیستمهای تهویه، یخچالهای خانگی، سردخانههای بزرگ و پالایشگاهها زیاد استفاده میشود. شکل زیر اجزای یک سیکل تبرید تراکم-بخار را نشان میدهد که قبلا جزئیات هر کدام را توضیح دادهایم.
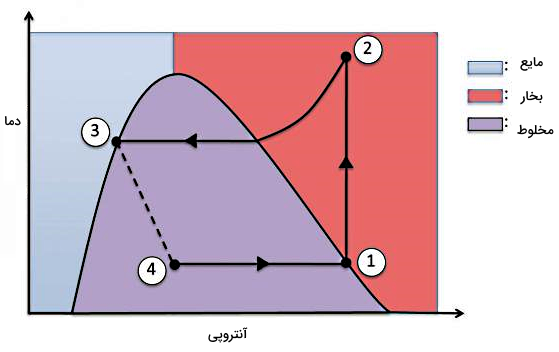
ترمودینامیک چنین سیستمی در شکل زیر قابل تحلیل و بررسی است. در این چرخه، یک ماده مبرد در حال گردش داخل این سیستم مثل یک هیدروکربن دارای نقطه جوش پایین، بهعنوان بخار وارد کمپرسور میشود:
- از نقطه ۱ تا نقطه ۲: بخار وارد شده طی یک فرآیند آنتروپی ثابت، متراکم میشود و در نهایت کمپرسور را به شکل بخاری با دمای بالاتر ترک میکند.
- از نقطه ۲ تا نقطه ۳: کندانسور بخار مرحله قبل را جابهجا و خنک میکند تا زمانی که بخار شروع کند به میعان شدن. با تبدیل بخار به مایع، گرمای اضافی آن در یک فرآیند فشار و دما ثابت حذف میشود.
- از نقطه ۳ تا نقطه ۴: مایع مبرد از طریق لولههای انبساط حرکت میکند و در این فرآیند به شدت فشار آن کم میشود، به صورتی که تبخیر ناگهانی و تبرید خودکار بخشی از مایع مبرد در این مرحله اتفاق میافتد.
- از نقطه ۴ تا نقطه ۱: پس مخلوطی از مایع و گاز با فشار و دمای پایینتر در نقطه ۴ خواهیم داشت. این مخلوط سرد شده توسط لولهها به گردش خود ادامه میدهد. در نهایت با خنکسازی هوای گرم، کاملا تبخیر میشود. بخار مبرد نهایی به کمپرسور در نقطه ۱ باز می گردد تا چرخه ترمودینامیکی کامل شود.
چرخهای که در این بخش توصیف کردیم، یک چرخه ایدهآل است. در عمل به علت وجود اصطکاک یا رفتار گازهای غیرایدهآل در سیستم، معمولا افت فشار در این چرخهها مشاهده میشود.
سیکل تبرید جذبی
تا اینجا دیدیم که برخی روشهای ایجاد تبرید چیست و چگونه کار میکنند. یکی دیگر از روشهای بر پایه چرخه یا سیکل ترمودینامیکی جهت ایجاد تبرید، «چرخه جذبی» (Absorption Cycle) است. اوایل قرن بیستم، تبرید جذبی روشی مرسوم و پرکاربرد محسوب میشد. اما پس از توسعه تبرید تراکم-بخار، این روش به علت بازدهی خیلی کمترش در مقایسه با تبرید تراکم-بخار کاربرد گسترده خود را از دست داد. در حال حاضر از تبرید جذبی در موقعیتهایی استفاده میشود که سوخت کافی برای ایجاد گرما موجود است، اما الکتریسیته کافی نه، مثلا در کامیونهای کمپر.
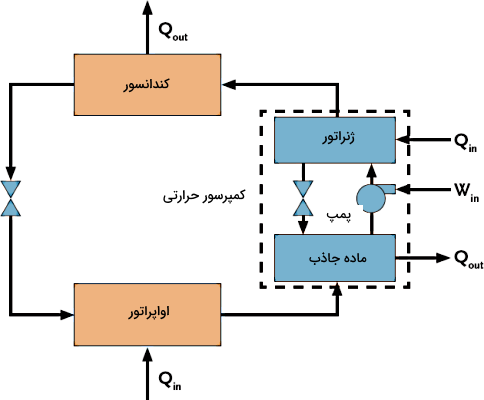
چرخه جذبی شبیه چرخه تراکم است، فقط روش افزایش فشار بخار مبرد در این چرخه متفاوت است. در چرخه جذبی، کمپرسور توسط یک ماده جذبکننده جایگزین میشود. این ماده، مبرد را در یک مایع مناسب حل میکند. همچنین یک پمپ مایع در این سیستم وجود دارد که فشار را بالا میبرد. به علاوه، یک ژنراتور هم در این سیستم هست که با افزایش گرما، بخار مبرد را از مایع فشار بالا جدا میکند.
برای اینکه پمپ مایع عملکرد خوبی داشته باشد، لازم است کار انجام شود که معمولا این مقدار کار از کار مورد نیاز توسط کمپرسور در سیستم تراکمی کمتر است. در یک یخچال جذبی، باید یک ترکیب مناسب از مبرد و ماده جذبکننده بکار رود. معمولترین ترکیبات مورد استفاده در یخچالهای جذبی عبارتاند از «آمونیاک» (Ammonia) (مبرد) با آب (جاذب) یا آب (مبرد) با «برمید لیتیوم» (Lithium Bromide) (جاذب).
سیکل تبرید جذب سطحی
در ابتدای بخش گفتیم که نوع دیگری از تبرید جذبی بر پایه چرخه جذب سطحی یا Adsorption Cycle است. در این روش هم مادهای که جذب سطح میشود یا همان مبرد میتواند آب، آمونیاک، «متانول» (Methanol) یا ... باشد. اما سطحی که ماده مبرد را جذب میکند، یک جامد است. جامداتی مانند «سیلیکا ژل» (Silica Gel) یا «کربن فعال» (Activated Carbon) و «زئولیت یا سنگ جوشان» (Zeolite) معمولا در این چرخهها استفاده میشوند.
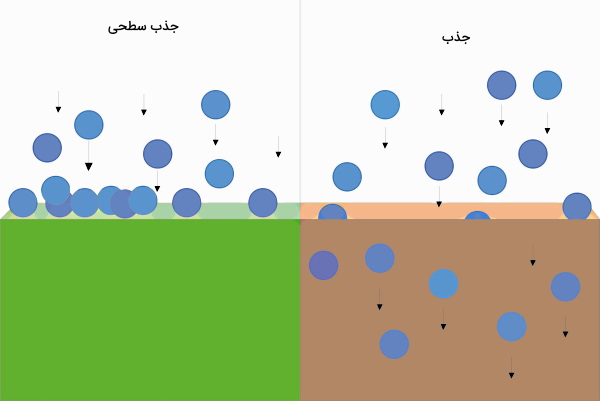
پس تفاوت اساسی چرخه جذبی و چرخه جذب سطحی، در حالت مادهای است که مبرد را جذب میکند. در چرخه جذب این ماده هم مانند مبرد مایع است، در حالی که در چرخه جذب سطحی، این ماده یک جامد است. این روش طی ۳۰ سال اخیر بسیار موردتوجه و مطالعه قرار گرفته است، چون سردسازی جذب سطحی معمولا صدا و خوردگی کمتری دارد و با محیط زیست هم سازگارتر است.
سیکل تبرید گازی
میخواهیم ببینیم روش دیگر برای ایجاد تبرید چیست. فرض کنید که شاره یا سیال در حال چرخش داخل یک سردساز، گازی باشد که با تراکم و انبساط تغییر فاز نداشته باشد. چنین چرخهای، چرخه گازی نامیده میشود. هوا ماده معمول مورداستفاده در این چرخه است. از آنجایی که در چرخه گازی تبخیر و میعان در نظر گرفته نشده است، اجزای مربوط به کندانسور و تبخیرکننده در چرخه تراکم-بخار در این چرخه با مبدلهای حرارتی گاز به گاز گرم و سرد معادل هستند.
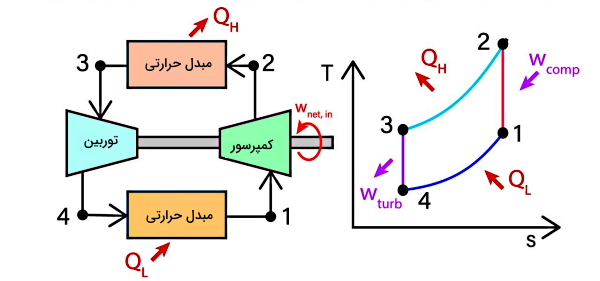
چرخه گازی از چرخه بخار بازدهی کمتری دارد. این چرخه عکس «چرخه برایتون» (Brayton Cycle) کار میکند. اگر به خاطر داشته باشید گفتیم که عملکرد چرخه بخار، عکس چرخه رانکین است. دو مطلب «سیکل رانکین (Rankine Cycle) — یادگیری با مثال» و «سیکل برایتون (Brayton Cycle) و محاسبات مربوط به آن — از صفر تا صد» از مجله فرادرس، اطلاعات کاملی در مورد این دو نوع سیکل در اختیار شما قرار میدهند.
بنابراین سیال در حال چرخش در چنین چرخهای طی یک فرآیند دما ثابت، گرما را جذب یا دفع نمیکند و اگر بخواهیم میزان سردسازی مشابهی از دو چرخه گازی و بخار دریافت کنیم، یک سیکل تبرید گازی به دبی جرم بالاتری نیاز دارد که نتیجه آن حجیمتر شدن سیستم نیز هست. از این نوع سیکل به خاطر بازدهی کمتر و حجم بالاتر، در حال حاضر چندان استفاده نمیشود. از جمله کاربردهای این سیکل در دستگاه تهویه هوایی است که در توربینهای گازی به منظور سردسازی قرار داده میشوند.
روشهای دیگر ایجاد تبرید
پس از اینکه کاملا با اجزای یک سیکل تبرید آشنا شدیم و متوجه شدیم اصول تبرید چیست، لازم است بدانیم با چه روشهایی میتوانیم تبرید را ایجاد کنیم. روشهای ایجاد تبرید را میتوانیم به چهار گروه کلی غیرچرخهای، چرخهای، ترموالکتریکی و مغناطیسی تقسیمبندی کنیم. اساس نامگذاری روش اول و دوم این است که آیا در ایجاد تبرید از یک چرخه ترمودینامیکی استفاده شده است یا خیر. با تبرید چرخهای یا همان سیکل تبرید و روابط ترمودینامیکی حاکم بر آن در بخش گذشته بهطور کامل آشنا شدیم. در زیربخشهای بعدی، روشهای دیگر ایجاد تبرید را توضیح میدهیم.
تبرید غیرچرخهای
یکی از روشهایی که کمک میکند تا ببینیم تبرید چیست و چگونه ایجاد میشود، روش تبرید غیرچرخهای است. در این روش یک ناحیه محدود توسط یخ در حال ذوب شدن یا یخ خشک در حال تصعید، سرد میشود. در واقع در این روش هیچ چرخه ترمودینامیکی برای ایجاد تبرید در سیستم وجود ندارد.
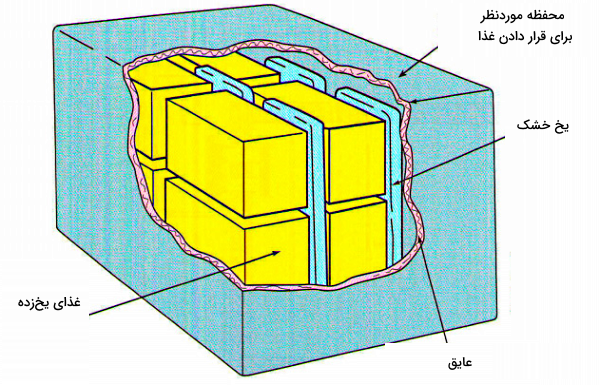
شاید ملموسترین مثالی که برای این روش میتوانیم بزنیم، استفاده از یک سیستم سردکننده قابل حمل معمولی است که در آن داخل یک محفظه عایق حرارتی مقادیری یخ جهت سردسازی قرار داده میشود و اجزای موردنظر زیر یخها قرار داده میشوند تا سرد بمانند. این یخها میتوانند دمای محیط را نزدیک صفر نگه دارند، اما دمای زیر صفر ایجاد نمیکنند. البته اگر از نمک استفاده شود، ممکن است دما به زیر صفر هم برسد. استفاده از نمک، ترفندی بود که در بستنیسازهای سنتی از آن استفاده میشد. همچنین کاربرد یخ خشک هم میتواند دما را تا زیر نقطه انجماد آب برساند.
تبرید ترموالکتریکی
در این بخش میخواهیم ببینیم روش دیگر سردسازی یا تبرید چیست. مبنای سردسازی ترموالکتریکی، «اثر پلیته» (Peltier Effect) است. در این روش بر اساس اثر پلیته، یک شار حرارتی در محل اتصال دو نوع ماده ایجاد میشود. معمولا از چنین سیستمی در سردکنندههای قابلحمل جهت کمپ کردن یا به منظور سرد کردن قطعات الکترونیکی کوچک استفاده میشود. سردکنندههای پلیته معمولا در موقعیتهایی که سیکل تبرید تراکم-بخار عملا قابل اجرا کردن نباشد یا فضای زیادی را اشغال کند، بکار میروند.
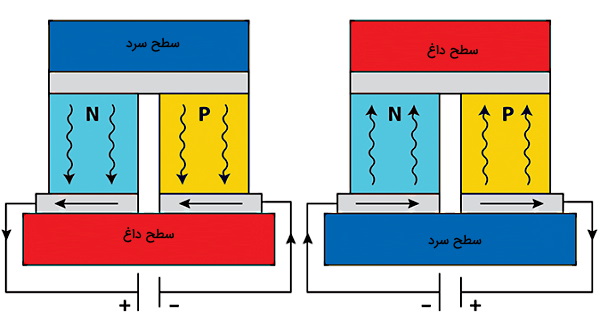
در شکل بالا مشاهده میکنید که اثر پلیته همان اختلاف دمایی است که با اعمال ولتاژ بین دو الکترود متصل به یک نمونه، ایجاد میشود. از این روش برای انتقال گرما از یک محیط به محیط دیگر در مقیاس کوچک میتوان استفاده کرد. بازدهی سیستم تبرید ترمودینامیکی نسبت به چرخه تبرید تراکم-بخار کمتر است و گرمای زیادی را تولید میکند.
تبرید مغناطیسی
پس از اینکه یاد گرفتیم سه روش عمده ایجاد تبرید چیست، در این بخش آخرین روش تبرید را توضیح میدهیم که بر پایه مغناطیس است. این روش به «دیمغناطیس شدن آدیاباتیک یا مغناطیسزدایی بیدررو» (Adiabatic Demagnetization) هم معروف است. اساس کار در این نوع سردسازی، «اثر مغناطوگرمایی» (Magnetocaloric Effect) است که یک خاصیت ذاتی در جامدات مغناطیسی محسوب میشود. ماده مبرد در این روش، یک نمک پارامغناطیسی است.
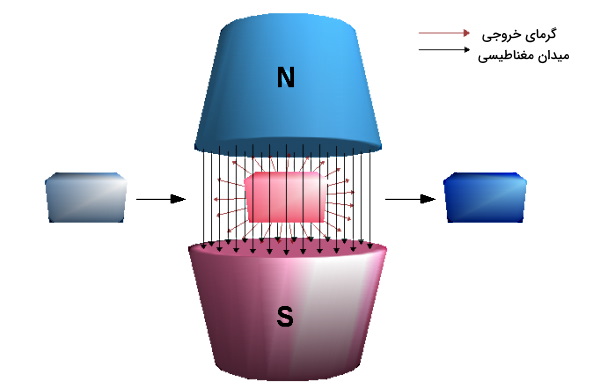
با اعمال یک میدان قوی مغناطیسی به ماده پارامغناطیس، دوقطبیها در پوسته الکترونی بیرونی اتمهای این ماده همجهت میشوند. در نتیجه، آنتروپی ماده مبرد کم خواهد شد. چون مواد مغناطیسی کمی در دمای اتاق میتوانند خواص موردنیاز برای چنین سیستمی را فراهم کنند، کابرد این روش تبرید محدود به بخش تحقیقات و سیستمهای برودتی یا کرایوژنیک است.
حل مثال و تمرین تبرید
پس از اینکه کاملا یاد گرفتیم تبرید چیست و چگونه ایجاد میشود، در این بخش با حل مثالهای مختلف و استفاده از روابط ترمودینامیکی به شما آموزش میدهیم که مسائل مربوط به تبرید را چگونه حل کنید.
مثال ۱
یک پمپ گرمایی بین دو دمای ۲۷ و ۳۲۷ درجه سانتیگراد کار میکند. COP آن را محاسبه کنید:
پاسخ
با توجه به فرمول ، باید بهجای TL دمای پایینتر یعنی ۲۷ درجه و بهجای TH دمای بالاتر یعنی ۳۲۷ درجه را قرار دهیم. اما نکته مهم این است که این دو دما برحسب درجه سانتیگراد هستند و باید به کلوین تبدیل شوند. رابطه تبدیل دما بهصورت تقریبی برابر است با:
مثال ۲
اگر مقادیر آنتالپی در ابتدای ورود به کمپرسور، هنگام خروج از آن و در انتهای فرآیند میعان بهترتیب برابر با مقادیر زیر باشند، COP این سیستم تبرید تراکم-بخار چقدر است؟
پاسخ
همانطور که توضیح دادیم، COP یک سیکل تبرید تراکم-بخار ایدهآل برابر است با نسبت اثر تبرید () به کار انجام شده توسط کمپرسور ():
برای اینکه بتوانیم مقادیر آنتالپی بالا را در فرمول قرار دهیم باید چرخه فشار - آنتالپی را در نظر داشته باشیم. طبق شکل زیر نقطه ۱ تا ۲ معادل کار انجام شده در کمپرسور است. پس آنتالپی در نقطه ورود کمپرسور همان h1 و در نقطه خروج برابر با h2 است. انتهای میعان نیز معادل نقطه ۳ است. فرآیند ۳ تا ۴ انبساط در آنتالپی ثابت است. بنابراین آنتالپی در نقطه ۳ و ۴ یکی است.
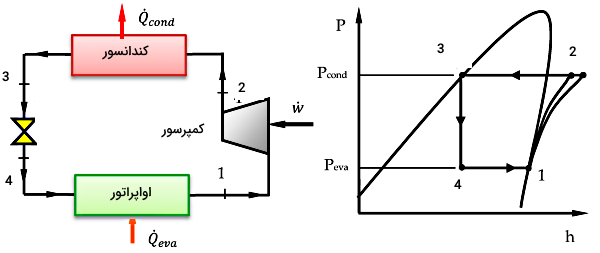
مثال ۳
در یک چرخه تبرید تراکم-بخار ایدهآل اثر تبرید و COP برابر با ۴ است. اگر نرخ جریان مبرد باشد، گرمای خروجی در کندانسور چقدر است؟
پاسخ
در بخش وابستگی فشار و آنتالپی، گفته بودیم COP برابر است با نسبت اثر تبرید به کار انجام شده توسط کمپرسور:
در این رابطه اثر تبرید برابر است با . بنابراین میتوانیم کار کمپرسور را به شکل زیر محاسبه کنیم:
در رابطه آخر کل گرمای خروجی را با q نشان دادهایم.
تکمیل یادگیری تبرید با فرادرس
در بخش گذشته با حل مثال کاملا متوجه شدهاید که تبرید چیست و مسائل مربوط به آن چگونه است. اگر علاقهمند به یادگیری مباحث پیشرفتهتری در ترمودینامیک هستید، فیلمهای آموزشی فرادرس که در ادامه لینک آنها قرار داده شده است را به ترتیب بررسی کنید:
- فیلم آموزش فیزیک ۱ دانشگاهی حل مساله فرادرس
- فیلم آموزش فیزیک پایه ۳ فرادرس
- فیلم آموزش فیزیک ۳ حل تمرین فرادرس
- فیلم آموزش فیزیک پایه ۳ مرور و حل تست کنکور ارشد فرادرس
- فیلم آموزش رایگان مبانی ترمودینامیک فرادرس
- فیلم آموزش رایگان کار و گرما در ترمودینامیک ۱ فرادرس
- فیلم آموزش رایگان سیستم های تبرید تراکمی فرادرس
- فیلم آموزش ترمودینامیک ۱ فرادرس
- فیلم آموزش ترمودینامیک ۲ مرور و تست کنکور ارشد فرادرس
- فیلم آموزش سیستم های تبرید و سردخانه ای فرادرس
آزمون تبرید
پس از اینکه یاد گرفتید تبرید چیست، اگر میخواهید آنچه که در این مطلب از مجله فرادرس آموختهاید را بیازمایید، میتوانید به سوالات آزمون زیر که برای شما تهیه شده است پاسخ دهید. پس از انتهای آزمون، با کلیک بر روی بخش «دریافت نتیجه آزمون» نمره نهایی شما نمایش داده خواهد شد.
تمرین و آزمون
یخچالها بر اساس کدام قانون ترمودینامیک کار میکنند؟
قانون صفرم
قانون اول
قانون دوم
قانون سوم
پاسخ صحیح گزینه سوم است. اساس کار یخچال، قانون دوم ترمودینامیک است.
اجزای یک سیکل تبرید در یخچال در کدام گزینه با ترتیب درستی قرار گرفتهاند؟
کمپرسور-کندانسور-اواپراتور-شیر انبساط
کمپرسور-اواپراتور-کندانسور-شیر انبساط
اواپراتور-کندانسور-کمپرسور-شیر انبساط
اواپراتور-کمپرسور-کندانسور-شیر انبساط
گزینه آخر درست است. در گزینه اول پس از کندانسور، اواپراتور قرار داده شده است. در حالی که ابتدا مبرد وارد شیر انبساط میشود و سپس در اواپراتور قرار میگیرد. گزینه دوم هم پس از کمپرسور، اواپراتور را قرار داده است که اشتباه است و باید کندانسور نوشته میشد. در گزینه سوم پس از اواپراتور باید کمپرسور قرار بگیرد.
کار اصلی یک شیر انبساط در یخچال این است که باعث ... مبرد ... از فشار ... به فشار ... شود.
انبساط، مایع، اواپراتور، کندانسور
میعان، گازی، اواپراتور، کندانسور
میعان، گازی، کندانسور، اواپراتور
انبساط، مایع، کندانسور، اواپراتور
گزینه آخر صحیح است. میدانیم مبرد به شکل مایع وارد اواپراتور میشود و با جذب گرما، تبدیل به بخار خواهد شد. سپس به کمک کندانسور و کمپرسور این بخار مجددا به مابع تبدیل خواهد شد. بنابراین مایع مبرد پس از خروج از کندانسور، وارد شیر انبساط میشود و بهسرعت نیز منبسط میشود، طوری که دما و فشار آن هر دو افت میکند تا برای ورود به اواپراتور آماده شود.
اگر در یک پمپ گرمایی دمای پیچههای کندانسور و اواپراتور به ترتیب برابر با ۲۷ C و -۲۳ C باشد، برای کار ورودی به میزان ،۱ kW چه مقدار گرما پمپ میشود؟
گزینه سوم درست است. ابتدا رابطه COP برای یک پمپ گرمایی را مینویسیم:
در رابطه بالا و . لازم است این دو دما را به کلوین تبدیل کنیم:
در نهایت میدانیم رابطه کار ورودی با گرمای پمپ شده خروجی برای پمپ گرمایی به شکل زیر است:
کمترین دمای مبرد در یک چرخه تبرید تراکم-بخار پس از کدام فرآیند ایجاد میشود؟
تراکم
انبساط
میعان
تبخیر
کدام گزینه خاصیت مطلوبی برای یک مبرد است؟
سمی بودن
قابلیت انفجار
نقطه جوش پایین
نقطه انجماد بالا
برای اینکه مطمئن باشیم زمانی که مبرد به کمپرسور میرسد هیچ فاز مایعی ندارد، ... پس از ... انجام میشود.
سوپرهیت-تبخیر
سابکول-تبخیر
سوپرهیت-میعان
سوپرهیت-انبساط
اساس ایجاد تبرید به روش مغناطیسی و ترموالکتریکی کدام گزینه است؟
قانون دوم ترمودینامیک - چرخه کارنو
اثر پلیته - اثر مغناطوگرمایی
اثر مغناطوگرمایی - اثر پلیته
اثر مغناطوگرمایی - جذب سطحی
در کدام بخش یخچال کار لازم برای سردسازی انجام میشود؟
کندانسور
شیر انبساط
لولههای انتقالدهنده مبرد
کمپرسور
مراحل تخلیه و دریافت گرما در یک سیکل تراکم-بخار چگونه فرآیندهایی هستند؟
دما ثابت - فشار ثابت
هر دو فشار ثابت
فشار ثابت - دما ثابت
هر دو دما ثابت












سلام، وقت بخیر
ممنون از مطالب مفیدتون
من این قسمت (طی فرآیند تبرید، انرژی گرمایی از محیطی با دمای کم حذف میشود و به محیطی با دمای بالاتر منتقل یا دفع میشود) رو متوجه نشدم
مگه گرما از محیط با دمای بالاتر منتقل نمیشه؟
با سلام خدمت شما؛
بیان صحیحتر این است که بگوییم گرما از محیطی با دمای کم جذب شده و به محیطی با دمای بالاتر دفع میشود. منظور از کلمه انتقال در این جمله چنین فرآیندی است که توسط مادهای به نام مبرد انجام میشود. با توجه به اینکه میدانیم گرما از ماده یا محیطی گرمتر به ماده یا محیط سردتر منتقل میشود، پس در اینجا نیاز داریم برای این انتقال حرارت، «کار» انجام شود و مبرد در یک سیستم بسته پمپ شود.
از همراهی شما با مجله فرادرس سپاسگزاریم.
ممنون از مطالب مفید وکامل شما 🙏🙏