آلکیلاسیون چیست؟ – شرح فرایند به زبان ساده
آلکیلاسیون واکنشی شیمیایی است که طی آن یک گروه آلکیلی به زنجیرهای هیدروکربنی متصل میشود و هیدروکربنی جدید با جرم مولکولی بیشتری را تولید میکند. واکنش فریدل کرافتس یکی از مهمترین واکنشهای آلکیلاسیونی است که در شیمی آلی به آن پرداخته میشود. به دلیل اهمیت این واکنش و مکانیسم انجام آن، دانشجویان شیمی و افراد فعال در این حوزه باید با آن آشنایی کافی داشته باشند.
- میآموزید که آلکیلاسیون چیست و چه کاربردهایی دارد.
- یاد خواهید گرفت که چطور گروههای آلکیل را شناسایی و نامگذاری کنید.
- انواع عاملهای آلکیلاسیون و نقش هریک را خواهید آموخت.
- خواهید توانست مکانیسم واکنش فریدل کرافتس را تحلیل کنید.
- با کاربرد آلکیلاسیون در صنایع نفت و شیمی آشنا میشوید.
- تمایز واکنش جانشینی و حذفی را در آلکیلاسیون آلکینها یاد میگیرید.


در این مطلب از مجله فرادرس میخواهیم بدانیم آلکیلاسیون چیست و با چه مکانیسمی انجام میشود. سپس به بررسی انواع آلکیلاسیون، مانند آلکیلاسیون آلکن و آلکین و آلکیلاسیون فریدل کرافتس میپردازیم و در هر مورد نحوه انجام آنها را بررسی خواهیم کرد. آلکیلاسیون محدودیتهایی نیز دارد که به آنها نیز اشاره میکنیم. در نهایت نیز برای درک بهتر به تعدادی مثال و تمرین چندگزینهای پاسخ میدهیم.
آلکیلاسیون چیست؟
«آلکیلاسیون» (Alkylation) فرآیندی است که طی آن گروه آلکیلی با روشهای افزایشی یا جانشینی به مولکولی آلی متصل میشود. گروه آلکیل، آلکانی است که یکی از هیدروژنهای خود را از دست داده باشد و سادهترین عضو این خانواده متیل نام دارد که از متان به وجود میآید. در گروه متیل تنها ۱ اتم کربن و ۳ هیدروژن وجود دارد.
فرآیند آلکیلاسیون در حضور اسید قوی معدنی یا اسید لوویس و به کمک عامل آلکیلاسیونی مانند اولفین یا آلکیل هالید انجام میشود. در آلکیلاسیون هیدروکربنهای آروماتیک، زنجیرههای ساده هیدروکربنی با واکنش افزایشی به حلقه بنزن متصل میشوند.
دآلکیلاسیون چیست؟
به فرآیند عکس آلکیلاسیون، «دآلکیلاسیون» (Dealkylation) گفته میشود. در این فرآیند گروه آلکیلی از زنجیره اصلی هیدروکربنی پایه جدا خواهد شد و در نهایت یک گروه آلکیل و یک هیدروکربن به دست میآید.

فرآیند آلکیلاسیون به روشهای متفاوتی انجام میشود که هر کدام عامل آلکیلاسیون ویژهای را به کار میبرند و موارد مصرف آنها نیز متفاوت است. برای مثال علاوه بر شیمی آلی در رشته زیستشناسی نیز از این فرآیند استفاده میشود. در ادامه ابتدا میخواهیم کمی بیشتر با گروه آلکیل آشنا شویم و سپس انواع روشهای انجام فرآیند آلکیلاسیون را فرا گیریم.
گروه آلکیل چیست؟
یک «گروه آلکیلی» (Alkyl Group) از حذف ۱ عدد اتم هیدروژن از زنجیره آلکانی به وجود میآید. بنابراین هر آلکیل از آلکان همتای خود ۱ عدد هیدروژن کمتر دارد و از همان موضع میتواند پیوند شیمیایی جدیدی را ایجاد کند و بهصورت استخلاف روی زنجیره هیدروکربنی دیگری قرار بگیرد.
حذف این هیدروژن به جایگزینی پسوند «ان» در آلکان به «یل» در آلکیل میانجامد. برای مثال در صورتی که متان یکی از هیدروژنهای خود را از دست بدهد به گروه آلکیلی متیل تبدیل میشود. به همین صورت با حذف یک هیدروژن از اتان، گروه آلکیلی اتیل به وجود خواهد آمد. در جدول زیر میتوانید نام ۶ عضو ابتدایی آلکیلها را مشاهده کنید.
| نام آلکان | نام آلکیل | فرمول شیمیایی آلکیل |
| متان | متیل | |
| اتان | اتیل | |
| پروپان | پروپیل | |
| بوتان | بوتیل | |
| پنتان | پنتیل | |
| هگزان | هگزیل |
آلکیلها انواع متفاوتی دارند که در ادامه میخواهیم با آنها آشنا شویم.
آلکیل نرمال
از پیشوند برای مشخص کردن آلکیلهای نرمال استفاده میشود که از آلکانهای «راستزنجیر» (Open Chain) به وجود میآیند. در مواردی که از پیشوند نرمال یا استفاده نمیشود، منظور همان آلکیل نرمال است و در تصویر زیر تعدادی از ساختارهای آن را مشاهده میکنید.
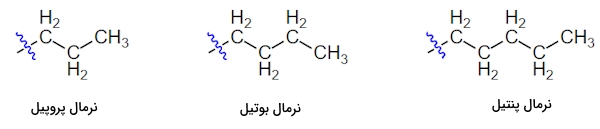
آلکیل ایزو
در صورتی که آلکیلی از نوع ایزو باشد، در انتها به گروه ختم میشود. برای نامگذاری این دسته از آلکیلها از پیشوند ایزو پیش از نام گروه آلکیلی استفاده میشود که به تعدادی از آنها در گروه زیر اشاره کردهایم.
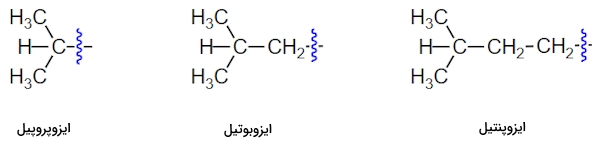
آلکیل سک
در گروه آلکیلی راستزنجیر بوتیل این امکان وجود دارد که اتصال از دومین کربن در زنجیره به گروه اصلی صورت بگیرد و برای نامگذاری آن از پیشوند «سک» (Sec) استفاده میشود. آلکیل سک در گروههای پنتیل و هگزیل وجود ندارد زیرا بیش از یک ساختار غیرمشابه وجود دارد که میتوان آن را به این دسته متعلق دانست. برای درک بهتر به تصویر زیر توجه کنید.
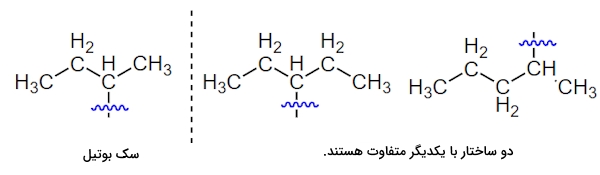
آلکیل ترت
در آلکیل ترت نقطه اتصال کربنی از نوع سوم است و برای نامگذاری آنها از پیشوند ترت یا استفاده میشود که تعدادی از آنها را در تصویر زیر مشاهده میکنید.
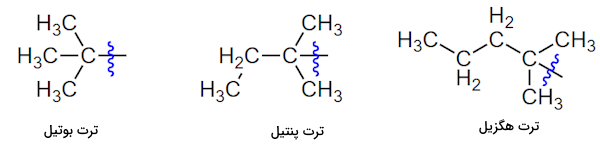
انواع عامل آلکیلاسیون
در این بخش میخواهیم با ترکیباتی که در آلکیلاسیون از آنها استفاده میشود، آشنا شویم و نحوه کاربرد آنها را فرا گیریم. انواع عامل آلکیلاسیون را در فهرست زیر مشاهده میکنید.
- «عامل آلکیلاسیون هستهدوست» (Nucleophilic Alkylating Agent)
- «عامل آلکیلاسیون الکتروندوست» (Electrophilic Alkylating Agent)
عامل آلکیلاسیون هسته دوست چیست؟
عامل آلکیلاسیون هستهدوست گونهای «کربانیون» (Carbanion) را به وجود میآورد و استخلافهای هالیدی را روی اتم کربن مورد نظر از طریق مکانیسم مینشاند.
یکی از رایجترین مثالها از واکنشهای عامل آلکیلاسیون هستهدوست، «جفت شدن سوزوکی» (Suzuki Coupling) است که در آن گروههای هالیدی جایگزین میشوند. «واکنشدهنده گرینیارد» (Grignard Reagent) و ترکیبات آلی فلزی مثالهایی از عوامل آلکیلاسیون هستهدوست به شمار میروند.
عامل آلکیلاسیون الکترون دوست چیست؟
این عامل آلکیلاسیون گونههای «کربوکاتیونی» (Carbocation) را به وجود میآورد که همارز کاتیون آلکیلها هستند. این دسته از عوامل آلکیلاسیون شامل آلکیل هالیدهایی مانند تریمتیل اگزونیوم و تترافلوئورو بورات میشوند که دارای بار الکتریکی مثبت هستند و گروههای ترککننده خوبی به حساب میآیند.
کاتالیزوری که به همراه این عوامل به کار میرود شامل اسید لوییس و اسید برونستد لوری میشود. از جمله اسیدهای لوییس مورد استفاده میتوان به آلومینیوم تریکلرید اشاره کرد که معمولا در حضور آلکیل هالیدها به کار میروند. همچنین از اسید برونستد لوری در زمانی استفاده میشود که فرآیند آلکیلاسیون توسط اولفین صورت بگیرد. از رایجترین کاتالیزورها میتوان به زئولیت اشاره کرد.
استفاده از عامل آلکیلاسیون الکتروندوست خطراتی را در پی دارد زیرا این دسته از ترکیبات سمی هستند و میتوانند عامل ایجاد سرطان باشند زیرا باعث آلکیلاسیون میشوند. پرکاربرترین واکنش آلکیلاسیون، واکنش فریدل کرافتنس است که در ادامه به معرفی آن خواهیم پرداخت.
انواع آلکیلاسیون
در این بخش میخواهیم به انواع واکنشهای آلکیلاسیون موجود بپردازیم و در هر مورد نحوه انجام و جزئیات آن را مورد بررسی قرار دهیم.
واکنش فریدل کرافتس چیست؟
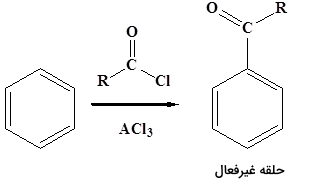
واکنش «آلکیلاسیون فریدل کرافتس» (Friedel Crafts Alkylation) توسط دانشمند فرانسوی «چارلز فریدل» (Charles Friedel) و همکار آمریکایی او، «جیمز کرافتس» (James Crafts) در سال ۱۸۷۷ میلادی معرفی شد. در این واکنش میتوان از آلکیل هالیدها برای تولید آلکیل بنزنها استفاده کرد اما در آن عواملی وجود دارد که میتواند روی مقدار کارآمدی تاثیر منفی بگذارد.
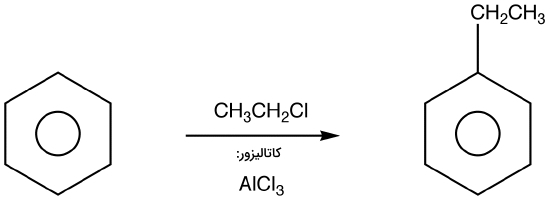
صورت کلی این واکنش را در تصویر بالا مشاهده میکنید. در ادامه میخواهیم مکانیسم انجام آن را در هر مرحله مورد بررسی قرار دهیم.
مرحله اول
در مرحله اول آلکیلاسیون فریدل کرافتس کربوکاتیونی تولید میشود که نقش الکتروندوست را در واکنش ایفا خواهد کرد. در این مرحله هالوآلکان فعال میشود و هالیدهای نوع دوم و سوم توانایی تشکیل کربوکاتیون را در این مرحله دارند. نحوه انجام این مرحله را میتوانید در تصویر زیر مشاهده کنید.
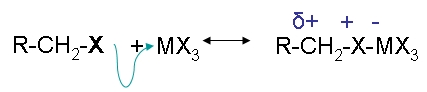
مرحله دوم و سوم
در مرحله دوم زوج الکترونی از حلقه آروماتیک به کربوکاتیون حمله میکنید و پیوند کربن کربن جدیدی را به وجود میآورد. حد واسط یون آرونیومی در نتیجه پایدار شدن فرمهای رزونانسی به وجود میآید. سپس از دست دادن پروتون به تولید محصول آلکیله خنثی میانجامد. روند انجام این مرحله را میتوانید در تصویر زیر مشاهده کنید.
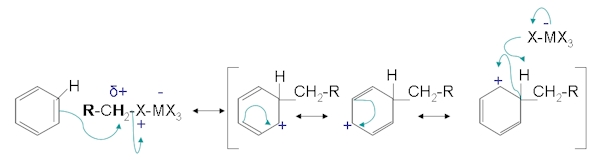
مرحله پایانی
واکنشپذیری هالوآلکانها با حرکت به سمت بالای جدول تناوبی و افزایش مقدار قطبیت، افزایش پیدا میکند. بنابراین میتوان با اطمینان گفت که هالوآلکان واکنشپذیرترین است و بعد از آن و سپس قرار دارند.
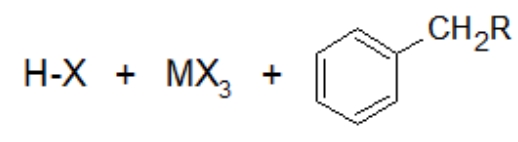
کمترین واکنشپذیری نیز مربوط به است. در این صورت اسیدهای لوییس مورد استفاده در واکنش آلکیلاسیون فریدل کرافتس ترکیب هالوژنی مشابهی دارند و میتوان به موارد زیر اشاره کرد.
محدودیتهای واکنش فریدل کرافتس
در صورتی که زنجیره آلکیلی دارای بیش از یک کربن باشد، احتمال بازآرایی آن در زمان واکنش وجود دارد. این بازآرایی در اثر انتقال هیدروژن و متیل صورت میگیرد. برای مثال در افزودن آلکیل با ۳ اتم کربن در محصول شاهد بازآرایی خواهیم بود که در تصویر زیر آن را مشاهده میکنید. یکی از روشهای حل این مشکل «آسیلاسیون فریدل کرافتس» (Friedel Crafts Acylation) است.
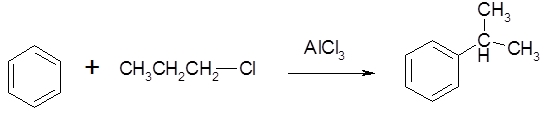
برای درک بهتر میخواهیم نحوه این بازآرایی را با مکانیسم آن بهصورت مرحله به مرحله مورد مطالعه قرار دهیم. ابتدا به واکنش تصویر زیر توجه کنید.
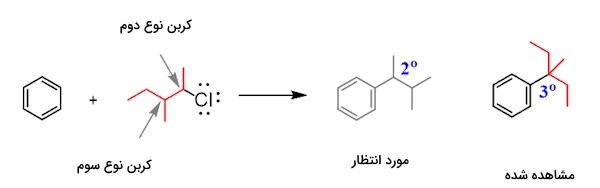
همانطور که مشاهده میکنید، در سمت چپ واکنش، کلر روی کربن نوع دوم قرار دارد اما در سمت راست محصولی مشاهده میشود که آلکیل آن از نوع سوم است. بنابراین میتوان اینطور جمعبندی کرد که در این واکنش بازآرایی صورت گرفته است. در تصویر زیر مکانیسم بازآرایی کربوکاتیون نوع دوم و تبدیل آن به کربوکاتیون پایداتر نوع سوم را مشاهده میکنید.
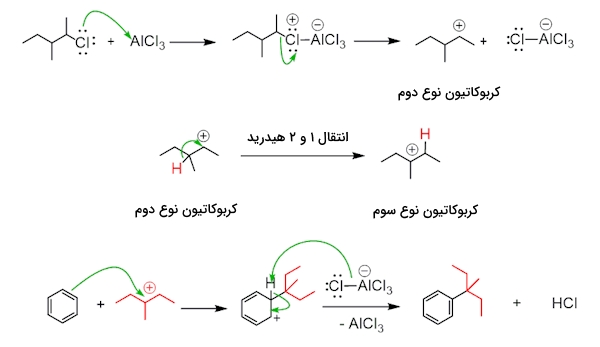
بازآرایی حتی در صورت وجود آلکیل هالید نوع اول نیز روی آلکیلاسیون فریدل کرافتس تاثیر میگذارد. در تصویر زیر نمونهای از یک آلکیل هالید نوع اول را مشاهده میکنید اما در محصول آلکیله شده، آلکیل بازآرایی شده است و محصولی غیر از آنچه انتظار داریم به دست داده است.
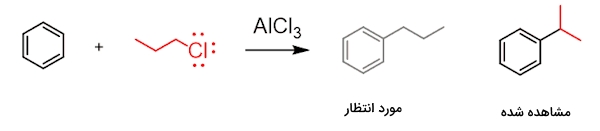
بازآرایی کربوکاتیونهای نوع اول تعجبآور است زیرا بر اساس انتظار توانایی تشکیل ندارند. در واقعیت در واکنش اسید لوییس و باز کمپلکسی تشکیل میشود که کربنی با الکتروندوستی بالا متصل به کلر دارد و متحمل انتقال ۱ و ۲ هیدرید میشود که میتوانید آن را در تصویر زیر مشاهده کنید. در نتیجه این انتقال کربوکاتیون نوع دوم تشکیل و با حلقه بنزنی وارد واکنش میشود.
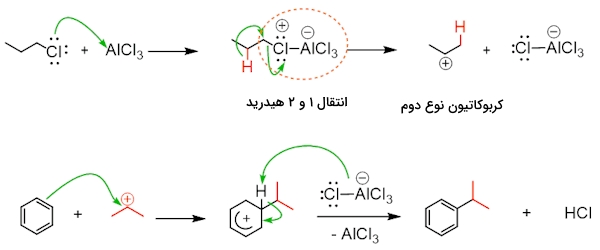
از دیگر محدودیتهای واکنش آلکیلاسیون فریدل کرافتس میتوان به این نکته اشاره کرد که در صورت وجود استخلاف یا گروه غیرفعالکننده روی حلقه بنزنی انجام نخواهد شد. بنابراین در صورتی که این واکنش روی حلقه بنزن با استخلافی مانند نیتروبنزن انجام شود، محصولی به دست نخواهد آمد که میتوانید آن را در تصویر زیر مشاهده کنید.
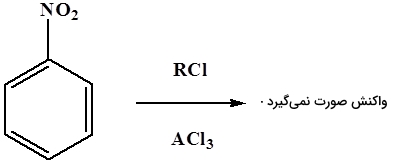
همچنین در صورتی که حلقه بنزنی شامل استخلافهای و و باشد، انجام نخواهد شد. زوجالکترون تنها روی این آمینها با اسید لوییس واکنش میدهد و باعث ایجاد یک بار مثبت در مجاورت حلقه بنزنی میشود. وجود این بار مثبت حلقه را غیرفعال میکند و واکنش فریدل کرافتس صورت نخواهد گرفت. این نکته را در تصویر زیر آوردهایم.
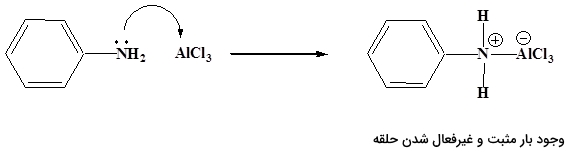
فریدل کرافتس میتواند چندین واکنش آلکیلاسیون را انجام دهد. در این واکنش الکترونی به گروه آلکیل داده میشود که حلقه بنزن را فعال میکند و برای آلکیلاسیونهای بعدی آماده میشود. در زیر نمونهای از ایجاد دو آلکیل روی یک حلقه بنزنی را مشاهده میکنید که به تولید دو محصول متفاوت میانجامد.
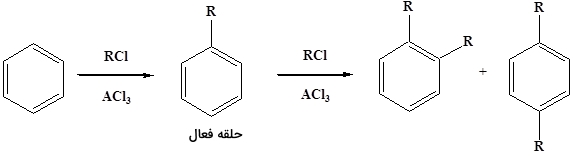
این مشکل در آسیلاسیون فریدل کرافتس بروز پیدا نمیکند زیرا گروه آسیل غیرفعالکننده است و از ایجاد آسیلاسیونهای بعدی پیشگیری میکند. در واکنش زیر یک آسیلاسیون فریدل کرافتس را مشاهده میکنید.
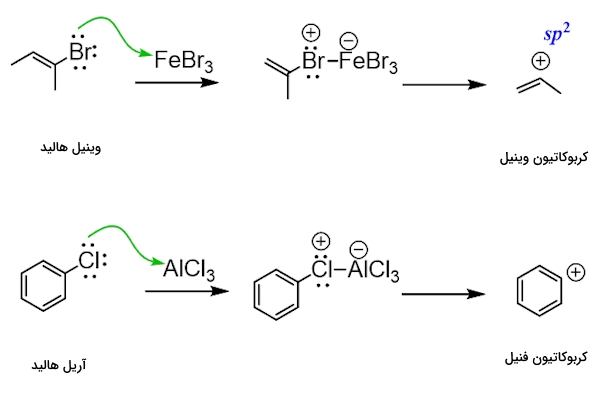
برای انجام واکنش فریدل کرافتس، هالوژن آلکیل هالید باید به اتم کربنی با هیبریداسیون متصل باشد زیرا کربوکاتیون با بار مثبت روی کربن ناپایدار است و به راحتی تشکیل نمیشود. بنابراین وینیل هالیدها و آریل هالیدها در واکنش آلکیلاسیون فریدل کرافتس شرکت نمیکنند. کربوکاتیون حاصل از هر کدام آنها را میتوانید در تصویر زیر مشاهده کنید که ناپایدار هستند.
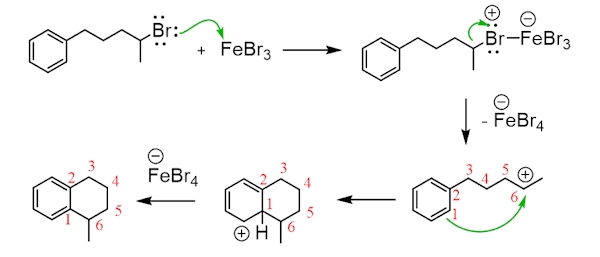
آلکیلاسیون درون مولکولی فریدل کرافتس
ترکیبات آروماتیکی که داری گروه عاملی با قابلیت تبدیل به الکتروندوست باشند، میتوانند آلکیلاسیون فریدل کرافتسی را انجام دهند که درون مولکولی نامیده میشود. در تصویر زیر میتوانید نمونهای از این نوع واکنش را مشاهده کنید.
آلکیلاسیون فریدل کرافتس در گروههای عاملی دیگر
تا اینجا با روشهای متعددی برای انجام آلکیلاسیون فریدل کرافتس آشنا شدیم. در این بخش میخواهیم به دیگر ترکیباتی بپردازیم که میتوانند وارد این واکنش جانشینی شوند. از لحاظ نظری تمامی گروههای عاملی در صورتی که قابلیت تبدیل به الکتروندوستی قوی را داشته باشند، میتوانند در واکنش آلکیلاسیون فریدل کرافتس شرکت کنند.
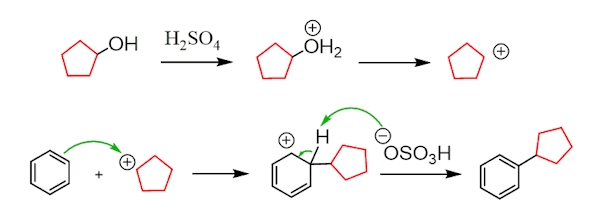
برای مثال الکلها در حضور سولفوریک اسید به کربوکاتیون تبدیل میشوند. درست مانند آنچه در واکنشهای حذفی با مکانیسم اتفاق میافتد که میتوانید نمونهای از آن را در تصویر بالا مشاهده کنید.
آلکیلاسیون آلکنها
در آلکیلاسیون آلکنها، گروه آلکیلی را به آلکن اضافه میکنند و نتیجه به دست آمدن هیدروکربنی اشباع است که جرم مولکولی بالاتری نیز دارد. در تصویر زیر نمونهای کلی از این نوع واکنش را مشاهده میکنید.
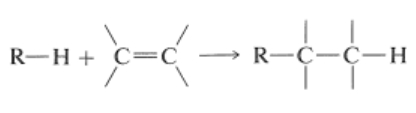
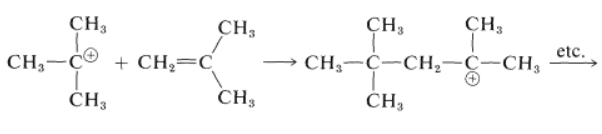
از این واکنش در صنعت نفت و گاز برای به دست آوردن هیدروکربنهایی با جرم مولکولی متوسط از مولکولهای کوچکتر استفاده میشود. یکی از مهمترین مثالها در این مورد افزودن ۲-متیل پروپان به ۲-متیل پروپن در حضور سولفوریک اسید یا هیدروژن فلوئورید بیآب است که به تولید محصول ۲و۲و۴-تریمتیل پنتان میانجامد. نحوه انجام این واکنش را در تصویر زیر مشاهده میکنید که گروه آلکیل در آن ۲-متیل پروپیل است.
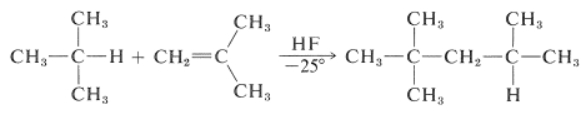
در ادامه مکانیسم این واکنش را مورد بررسی قرار خواهیم داد. نکته مهم در مورد این مکانیسم این است که یک کربوکاتیون میتواند به سرعت با هیدروکربن دارای کربن نوع سوم وارد واکنش شود و کربوکاتیون و هیدروکربنی جدید را به عنوان محصول به دست دهد.
برخی از انتقالهای هیدروژن به شدت سریع و در کمتر از یک ثانیه صورت میگیرند. برای نمونه به انتقال هیدروژن در واکنش زیر توجه کنید.

با دانستن این نکته که انتقال هیدروژن به سرعت انجام میشود، اولین مرحله این مکانیسم را پلیمریزاسیون سریع دو مولکول ۲-متیل پروپان در حضور کاتالیزور سولفوریک اسید میدانیم که کاتیون اکتیل را به دست میدهد.
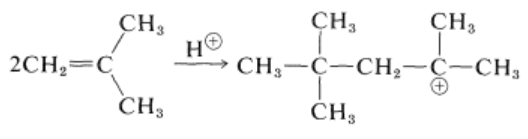
سپس کاتیون اکتیل انتقال هیدروژنی را با ۲-متیل پروپان تجربه میکنید و محصول کاتیون ترت-بوتیل و ۲و۲و۴-تریمتیل پنتان خواهد بود که آنها را در تصویر زیر مشاهده میکنید.
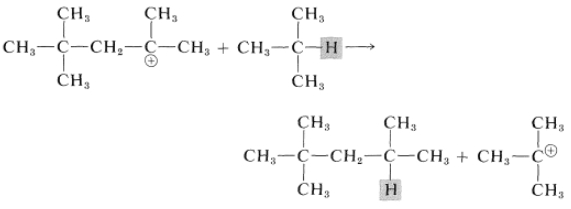
حمله کاتیون ترت-بوتیل به یک مولکول دیگر ۲-متیل پروپن به تولید کاتیون هشت کربنی از نوع سوم میانجامد که خود میتواند آغازگر واکنش آلکیلاسیون دیگری باشد.
آلکیلاسیون آنیون استیلید
وجود بار منفی و زوجالکترون تنها روی کربن آنیون استیلید، آن را هستهدوستی قوی میکنید. بنابراین آنیون استیلید میتواند با الکتروندوستهایی مانند آلکیل هالیدها وارد واکنش شود که در اثر آن آلکینی جدید به وجود میآید. نحوه انجام این واکنش را در تصویر زیر نشان دادهایم.
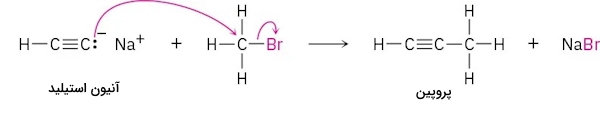
در این واکنش یون هستهدوست استیلید از زوجالکترون برای تشکیل پیوند کربن الکتروندوست قطبی در مولکول برمومتان استفاده میکند. با تشکیل پیوند کربن کربن جدید، مولکول را ترک میکند و الکترون پیوند بین کربن و برم را نیز با خود میبرد که در این صورت پروپین به عنوان محصول به جا خواهد ماند. از آنجا که در این واکنش گروه آلکیلی جدیدی به مولکول اولیه متصل شده است آن را آلکیلاسیون میدانیم.
آلکیلاسیون آلکین به استیلن محدود نمیشود. تمامی آلکینهای انتهایی میتوانند به آنیون مربوطهشان تبدیل شوند و سپس در واکنش با یک آلکیل هالید، محصول آلکین انتهایی را طی فرآيند آلکیلاسیون به دست دهند. برای مثال به مولکول ۱-هگزین توجه کنید که از زنجیرهای با ۶ اتم کربن تشکیل شده است و پیوند سهگانه آن انتهایی است.
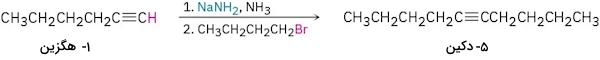
در صورتی که این مولکول ابتدا در مجاورت و سپس ۱-برمو بوتان قرار بگیرد، محصول آلکیلاسیون ۵-دکین را با بازدهی ۷۶٪ به دست میدهد. واکنش این آلکیلاسیون را در تصویر بالا مشاهده میکنید.
استفاده از آلکیلاسیون استیلید روشی مناسب برای تولید آلکینهای استخلافدار از مولکولهای سادهتر به شمار میرود. یک آلکین انتهایی را میتوان با آلکیلاسیون استیلن ایجاد کرد. همچنین میتوان از آلکین انتهایی به کمک آلکیلاسیون به آلکین میانی رسید. نحوه انجام این دو واکنش را در تصویر زیر مشاهده میکنید.
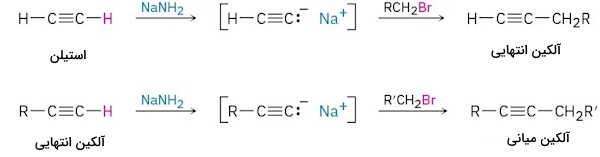
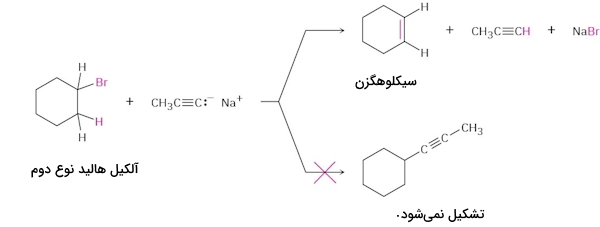
تنها محدودیت واکنش آلکیلاسیون این است که در آن باید از آلکیل برمید و آلکیل یدیدهای نوع اول استفاده کرد. دلیل این نکته این است یون استیلید بازی قوی است و میتواند با آلکیل هالیدهای نوع دوم و سوم وارد واکنش شود و واکنش حذفی را به جای واکنش جانشینی به انجام برساند.
برای مثال واکنش برمو سیکلو هگزان با آنیون پروپین به تولید محصول حذفی سیکلوهگزن میانجامد و محصول ناشی از آلکیلاسیون یعنی ۱-پروپینیل سیکلوهگزان را به دست نمیدهد. این دو واکنش حذفی و جانشینی را میتوانید در تصویر زیر مشاهده کنید.
مثال و حل تمرین
حال که میدانیم آلکیلاسیون چیست و چگونه انجام میشود، میخواهیم در این بخش به حل تعدادی مثال و تمرین بپردازیم.
مثال
در این بخش به حل تعدادی مثال میپردازیم و در هر مورد پاسخ تشریحی آنها را نیز میآوریم. با دقت به این پاسخهای تشریحی میتوان به پرسشهای مشابه پاسخ داد.
مثال اول
در تصویر زیر ۵ مولکول آلی را مشاهده میکنید. با توجه به نکات گفته شده، کدام یک از آنها در واکنش آلکیلاسیون فریدل کرافتس دستخوش بازآیی نمیشود.
پاسخ
مولکول شماره ۲، ۳ و ۴ در انجام واکنش آلکیلاسیون فریدل کرافتس بازآرایی را تجربه خواهند کرد و تنها مولکولهای شماره ۱ و ۵ بازآرایی نخواهند کرد.
مثال دوم
کدام یک از محصولاتی که بهصورت روزمره توسط انسان مورد استفاده قرار میگیرد از واکنش آلکیلاسیون استفاده میشود؟
پاسخ
دترجنتها و شویندهها از جمله ترکیباتی هستند که در تولید آنها واکنش آلکیلاسیون نقش بهسزایی را ایفا میکند.
مثال سوم
فرآیند آلکیلاسیون حلقه بنزن به چه روشی انجام میشود؟
پاسخ
همانطور که پیشتر گفتیم در واکنش آلکیلاسیون اتم یا گروهی با گروه آلکیل جایگزین میشود که در این مورد همان هیدروژن روی حلقه بنزن است. در آلکیلاسیون بنزن، هیدروژن آن توسط آلکیلی مانند متیل یا اتیل جایگزین میشود. در این واکش از کاتالیزور آلومینیوم کلرید و عامل آلکیلاسیون کلروآلکان بهره میبرند.
تمرین
در این بخش به مرور تعدادی تمرین چندگزینهای پیرامون آلکیلاسیون میپردازیم.
تمرین اول
تمرین دوم
تمرین سوم
تمرین چهارم
تمرین پنجم
سوالات متداول
حال که میدانیم واکنش آلکیلاسیون چیست و با انواع آن نیز آشنا شدیم، در این بخش به تعدادی از سوالهای متداول و پرتکرار پیرامون آن پاسخ میدهیم.
دآلکیلاسیون چیست؟
به فرآیند عکس آلکیلاسیون، دآلکیلاسیون گفته میشود که در آن گروه آلکیلی از زنجیره اصلی هیدروکربنی پایه جدا خواهد شد و در نهایت یک گروه آلکیل و یک هیدروکربن به دست میآید.
واکنش فریدل کرافتس چیست؟
در واکنش فریدل کرافتس یک گروه آلکیل به کمک واکنش جانشینی هستهدوستی آروماتیک، به حلقه بنزن افزوده میشود.
انواع گروههای آلکیلی را نام ببرید
آلکیلها با توجه به ساختار خود انواع مختلفی دارند که از این بین میتوان به آلکیل نرمال، ایزو آلکیل، سک آلکیل و ترت آلکیل اشاره کرد.
در واکنش آلکیلاسیون از چه اسیدهای لوییسی استفاده میشود؟
از جمله اسیدهای لوییس مورد استفاده در واکنش آلکیلاسیون میتوان به ترکیبات زیر اشاره کرد.
جمعبندی
هدف از این مطلب مجله فرادرس آشنایی با مفهوم آلکیلاسیون و چگونگی انجام در آن در شیمی آلی بود. آلکیلاسیون واکنشی است که طی آن یک گروه آلکیل به زنجیره هیدروکربنی متصل میشود و محصول آلکیله شده را به وجود میآورد.
در این مطلب ابتدا به بررسی آلکیلاسیون و نحوه انجام آن پرداختهایم و سپس انواع آن را مرور کردهایم. در نهایت نیز با محدودیتهای این روش شیمیایی آشنا شدیم و تعدادی مثال و تمرین را حل کردیم تا درک خود از این مفهوم را عمق ببخشیم.