کروماتوگرافی HPLC – به زبان ساده
کروماتوگرافی HPLC یا «کروماتوگرافی مایع با عملکرد بالا» (High Performance Liquid Chromatography) روشی در شیمی تجزیه برای جدا کردن اجزای یک مخلوط، شناسایی و اندازهگیری هر جزء است. این روش در اوایل قرن بیستم کشف شد و برای اولین بار بمنظور جدا کردن ترکیبات رنگی مورد استفاده قرار گرفت. واژه کروماتوگرافی به معنای «رنگنگاری» (Color Writing) است.


مخترع این روش، گیاهشناس روسی «میخاییل تسوت» (Mikhail Tsvet) بود که برای مطالعه رنگ برگها از آن بهره گرفت. در سال 1906، تسوت دو مقاله در توصیف جنبههای مخلتف «کروماتوگرافی جذب مایع» (Liquid Adsorption Chromatography) به چاپ رساند. او همچنین بیان کرد که فارغ از نوع نام این روش، میتوان از کروماتوگرافی برای جداسازی سایر مواد نیز بهره گرفت.
مقدمه
کروماتوگرافی مایع با عملکرد (کارایی) بالا از جمله روشهای کروماتوگرافی برای جداسازی مواد به شمار میآید. این جدایش بر اساس برهمکنش نمونه با فازهای ساکن و متحرک انجام میگیرد. از آنجایی که ترکیبهای مختلفی را میتوان برای فازهای ساکن و متحرک به هنگام جدا کردن یک مخلوط بکار برد، روشهای مختلف کروماتوگرافی نیز وجود دارند که بر مبنای حالت فیزیکی این فازها بنا شدهاند.
کروماتوگرافی مایع و کروماتوگرافی ستونی مایع-جامد، معمولترین روشهای کروماتوگرافی هستند که از فاز متحرک مایع استفاده میکنند که این فاز، به آرامی با عبور از یک فاز ساکن جامد، با عمل فیلتراسیون، اجزا مختلف را از یکدیگر تفکیک میکند. کروماتوگرافی مایع با علمکرد بالا یا کروماتوگرافی HPLC را میتوان نوع پیشرفته کروماتوگرافی مایع با بازده، سرعت و کارایی بیشتر دانست.

شمای کلی از کروماتوگرافی مایع
اجزای یک مخلوط، بر اساس تمایل هر جزء به فایل مایع، در ستون، جداسازی میشوند. بنابراین، اگر اجزا، قطبیت متفاوتی داشته باشند و فاز ساکنی با قطبیت شدید از میان ستون عبور کند، یکی از اجزا نسبت به بقیه، با سرعت بیشتری از داخل ستون عبور خواهد کرد. از آنجایی که مولکولهای یک ترکیب، به صورت گروهی حرکت میکنند، ترکیبات به صورت باندهایی جداگانه و مشخص در ستون از یکدیگر متمایز هستند.
اگر اجزای جدا شونده، رنگی باشند، در زمان کروماتوگرافی، باندهای رنگی متناظر با هر گروه قابل تشخیص خواهند بود. در غیر اینصورت، همچون «کروماتوگرافی مایع با عملکرد بالا» (High Performance Liquid Chromatography)، حضور باندهای متناظر هر گروه را به کمک سایر روشها مانند استفاده از انواع طیف سنجی همچون طیفسنجی ماورابنفش-مرئی شناسایی میکنند.
نحوه جدایش اجزا در کروماتوگرافی مایع
در یک مخلوط دو جزئی با عبور فاز ساکن از میان ستون، هر دو جزء به صورت باندهایی مجزا از یکدیگر جدا میشوند. زمانی که هر جزء از ستون، شویش شود، هر کدام را میتوان بسته به نوع روش مورد نظر، جداسازی و بررسی کرد. بر اساس نوع قطبیت فازهای ساکن و متحرک، قطبیتهای نسبی هر دو جزء قابل تعیین است.
آمادهسازی ستون کروماتوگرافی مایع
در این بخش، توضیحات کوتاهی در خصوص آمادهسازی ستون در یک کروماتوگرافی مایع داده میشود و در ادامه متن، به طور دقیقتر، کروماتوگرافی HPLC مورد بررسی قرار میگیرد. فاز ساکن در «کروماتوگرافی ستونی» (Column Chromatography)، به طور معمول، یک جاذب جامد است. این جامد میتواند اجزای مایع و گازی را در سطح خارجی خود حفظ کند. ستونی که به طور معمول در کروماتوگرافی ستونی از آن بهره میگیرند همانند پیپت پاستور است که در کروماتوگرافی ستونی با مقیاس پایین مورد استفاده قرار میگیرد. بخش نازک خروجی را با پشم شیشه یا صفحهای متخلخل پر می کنند تا مواد پرشده داخل ستون را حفظ کند. در ادامه، جامد جاذب (به طور معمول سیلیکا) را به صورت فشرده به داخل لوله شیشهای میفرستند تا ستون را تکمیل کند. پر کردن ستون با فاز ساکن باید با دقت کافی انجام شود تا توزیع یکنواختی از مواد در داخل ستون صورت بگیرد.
این توزیع یکنواخت برای جلوگیری از ایجاد حباب یا کانالیشدن در ستون انجام میشود. در انتهای آمادهسازی ستون، حلال مورد استفاده در فاز متحرک را از میان ستون خشک عبور میدهند. چنین ستونی را «تَرشده» (Wetted) مینامند. زمانی که ستون، به خوبی آماده شد، نمونه را در بالای ستون قرار میدهند.
اساس کروماتوگرافی HPLC
اجزای مولکولی در کروماتوگرافی HPLC، دو دسته مهم را به نام آنالیت و ماتریکس تشکیل میدهند. آنالیت، اجزای مولکولی مورد نظر و ماتریکس، سایر اجزای نمونه هستند. بمنظور انجام کروماتوگرافی HPLC نمونه را به یک فاز متحرک وارد میکنند تا از میان فاز ساکن عبور کند. فاز متحرک را با شاخصههای مختلفی همچون ترکیب اجزا، انحلالپذیری، خواص فرابنفش، ویسکوزیته و امتزاجپذیری با سایر حلالها توصیف میکنند.
فاز ساکن میتواند تودهای از مایع متراکم، لایهای مایع بر سطحی جامد یا یک لایه «بین سطحی» (InterFacial) بین مایع و جامد باشد. در کروماتوگرافی HPLC فاز ساکن به طور معمول به صورت یک ستون پرشده با اجزای کوچک متخلخل است که فاز متحرک مایع، به کمک یک پمپ از میان آن عبور میکند. در حقیقت، توسعه کروماتوگرافی HPLC با توسعه ستونهای جدید همراه بود که این امر نیازمند اجزای جدید، فازهای ساکن جدید و دستورالعملهای بهبودیافته برای پرکردن ستون است. تصویری از یک دستگاه کروماتوگرافی HPLC در زیر نشان داده شده است.

شرح دستگاه کروماتوگرافی HPLC
اجزای اصلی یک دستگاه کروماتوگرافی HPLC در زیر نشان داده شده است. نقش پمپ در این دستگاه، حرکت دادن فاز متحرک با یک نرخ جریانی مشخص بر حسب میلیلیتر بر دقیقه است. وظیفه «انژکتور» (Injector)، تزریق نمونه مایع به جریان فاز متحرک است. ستون دستگاه، مهمترین بخش دستگاه کروماتوگرافی با عملکرد بالا را تشکیل میدهد. فاز ساکن در ستون نیز اجزای نمونه مورد نظر را از یکدیگر جدا میکند. از آشکارساز بمنظور شناسایی مولکولهای شویش شده از ستون بهره میگیرند. همچنین، از یک کامپیوتر برای تحلیل و ارزیابی دادهها استفاده میکنند. در حقیقت، از کامپیوتر نه تنها برای کنترل پارامترهای دستگاه بلکه برای ارزیابی «زمان بازداری» (Retention Time)، اجزای نمونه و آنالیز مقداری بهره میگیرند.
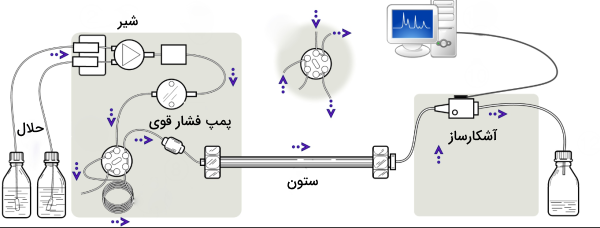
ستون کروماتوگرافی
بر اساس خواص فاز ساکن در ستون، از مکانیسمهای جدایش مختلفی در کروماتوگرافی استفاده میشود که از آن جمله میتوان به «کروماتوگرافی فاز نرمال» (Normal Phase Chromatography)، «کروماتوگرافی فاز معکوس» (Reverse Phase Chromatography)، «کروماتوگرافی تبادل یونی» (Ion Exchange Chromatography)، «کروماتوگرافی اندازه طردی» (Size Exclusion Chromatography) و «کروماتوگرافی میل ترکیبی» (Affinity Chromatography) اشاره کرد.
کروماتوگرافی فاز نرمال
در این روش، ستون را با ذرات قطبی معدنی پر و از یک فاز متحرک ناقطبی برای عبور از میان فاز قطبی استفاده میکنند. از کروماتوگرافی فاز نرمال به طور عمده برای خالصسازی نمونههای خام، جداسازی نمونههای به شدت قطبی یا جداسازی تحلیلی با کروماتوگرافی لایه نازک بهره میگیرند. یکی از مشکلات استفاده از این روش این است که آب، حلالی قوی برای کروماتوگرافی فاز نرمال به شمار میآید و وجود آب در فاز متحرک به طور محسوسی بر بازداری نمونه تاثیر گذار است. در جدول زیر، نوع فازهای متحرک و ساکن در کروماتوگرافی فاز نرمال و معکوس آورده شده است.
| فاز ساکن | فاز متحرک | |
| فاز نرمال | قطبی | ناقطبی |
| فاز معکوس | ناقطبی | قطبی |
کروماتوگرافی فاز معکوس
در کروماتوگرافی فاز معکوس، فاز ساکن، دارای خاصیت «آبگریز» (Hydrophobic) است درحالیکه فاز متحرک خاصیتی قطبی دارد. همانطور که در جدول بالا نیز نشان داده شده، نوع قطبیت فازها، عکس کروماتوگرافی فاز نرمال است. نوع برهمکنشها در کروماتوگرافی HPLC با فاز معکوس (RP-HPLC) را به صورت نیروهای آبگریز در نظر میگیرند. این نیروها نتیجه انرژی حاصل از تغییر در ساختارهای دوقطبی حلال است. جدایش مواد به طور عمده ناشی از تقسیم شدن آنالیت بین فاز ساکن و متحرک ذکر میشود.
مولکولهای حلشونده در تعادل بین فاز ساکن آبگریز و فاز متحرک با قطبیت جزئی هستند. هر قدر مولکول آبگریز (ناقطبی) باشد، زمان بازداری طولانیتری خواهد داشت درحالیکه ترکیبات معدنی یونیزه شده، یونهای معدنی و مولکولهای فلزی قطبی، زمان بازداری کمی دارند.
کروماتوگرافی تبادل یونی
مکانیسم تبادل یونی، بر اساس برهمکنش الکترواستاتیک بین یونهای آبدار از نمونه و گروههای عاملی با بار مخالف فاز ساکن بنا شده است. دو مکانیسم برای جداسازی مورد استفاده قرار میگیرد. در یک مکانیسم، به هنگام شویش، از فاز متحرک با یونهایی استفاده می شود که با یونهای آنالیت جایگزین شوند و این یونها را به خارج از ستون هدایت میکنند.
مکانیسم دیگر، شامل اضافه کردن ریجنت کمپلکس کننده به فاز ساکن برای تغییر اجزای نمونه از حالت اولیه خود است. با انجام چنین فرآیندی بر روی مولکولها، عمل شویش انجام میشود. علاوه بر تبادل یونها، تبادل یونی فاز ساکن میتواند برخی از مولکولها را به صورت خنثی نگهدارد. این فرآیند با میزن بازداری در تشکیل کمپلکسها مرتبط میشود. یونهای ویژهای همچون فلزات واسطه میتوانند بر رزینهای تبادل کاتیونی قرار بگیرند و با پذیرفتن جفتالکترونهای ناپیوندی، لیگاندهای «دهنده» (Donor) را بپذیرند.
کروماتوگرافیهای تبادل یونی امروزی، امکان تحلیلهای مقداری در غلظتهای پایین حلشونده را دارند. از آنها میتوان بمنظور آنالیز نمونههای محلول در آب آنیونهای معدنی استفاده کرد. کاتیونهای فلزی و آنیونهای معدنی به طور عمده توسط برهمکنشهای یونی با رزینهای تبادل یونی، از یکدیگر جدا میشوند.
یکی از کاربردهای صنعتی کروماتوگرافی تبادل یونی، در صنایع غذایی است که برای تعیین اجزای شامل نیتروژن، گوگرد، فسفر و یونهای هالید از آن بهره میگیرند. همچنین، این روش میتواند برای تعیین یونهای معدنی و آلی در آبها استفاده شود.
کروماتوگرافی اندازه طردی
«کروماتوگرافی اندازه طردی» (Size Exclusion Chromatography)، روشی برای جداسازی مولکولها بر اساس اندازه است. از این روش به طور معمول برای جداسازی درشتمولکولها از مولکولهای کوچکتر استفاده میشود. بعد از تزریق آنالیت به ستون، مولکولهایی که از اندازه حفرات فاز ساکن کوچکتر باشند، به داخل ذرات متخلخل وارد میشوند در بین کانالهای تودرتوی فاز ساکن جریان پیدا میکنند اما مولکولهای بزرگتر، مسیر طولانیتری را برای خروج باید طی کنند و در نتیجه، دیرتر از ستون خارج میشوند.
با توجه به اینکه حجم مولکولی با جرم مولکولی مرتبط است، انتظار میرود که زمان بازداری، به نحوی با جرم مولکولی مواد پلیمری مرتبط باشد. ارتباط بین زمان بازداری و جرم مولکولی در تصویر زیر نشان داده شده است:
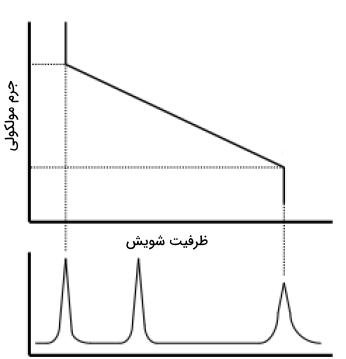
به طور معمول، نوع روش کروماتوگرافی HPLC به طبیعت شیمیایی و پارامترهای فیزیکوشیمیایی نمونه بستگی دارد. در تصویر زیر، فلوچارتی برای تuیین روش کروماتوگرافی HPLC نمایش داده شده است.
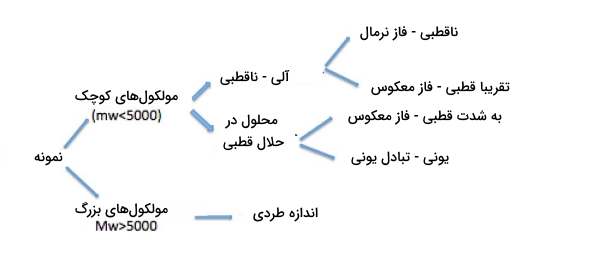
آشکارسازها در کروماتوگرافی HPLC
آشکارسازهایی که در کروماتوگرافی مایع مورد استفاده قرار میگیرند، بیشتر شامل آشکارسازیهای ماوربنفش-مرئی هستند. شاخصههای اساسی آشکارسازها در کروماتوگرافی مایع عبارتند از:
- «گستره دینامیکی» (Dynamic Range)
- «شاخص پاسخ» (Response Index)
- گسترده دینامیکی خطی
- پاسخ آشکارساز
- حساسیت
در میان این آشکارسازها، معروفترین و اقتصادیترین روش، استفاده از آشکارسازهای ماورابنفش (UV) و ضریب شکست نور (RI) است. این آشکارسازها محدوده شناسایی منطقی گستردهای دارند.
آشکارساز RI
آشکارسازهای RI از اولین آشکارسازهای تجاری بودند که مورد استفاده قرار گرفتند. این روش به طور ویژه در کروماتوگرافی HPLC بر اساس اندازه کاربرد دارد و اندازهگیری آن به طور مستقیم به غلظت پلیمر وابسته و مستقل از جرم مولکولی است. برخی از شاخصههای RI در زیر آورده شده است:
- حساسیت:
- گسترده دینامیکی خطی:
- شاخص پاسخ: 0/97-1/3
آشکارساز UV
آشکارسازهای ماورابنفش تنها برای موادی کاربرد دارند که نور ماورا بنفش را در طول موج منبع نوری جذب میکنند. لازم به ذکر است که بسیاری از ترکیبات، نور را در دامنه ماورا بنفش (180-350 نانومتر) جذب میکنند که از آنجمله میتوان به مواد پیوندهای یگانه یا موادی با الکترون غیراشتراکی اشاره کرد. رابطه بین شدت نور ماورابنفش گذرنده از سلول و غلظت حلشونده را بوسیله «قانون بیر» (Beer's Law) میتوان بیان کرد:
- : شدت نور ورودی به سلول
- : نور گذرنده از سلول
- : طول مسیر سلول
- : غلظت حلشونده
- : ضریب جذب مولی حلشونده
از آشکارسازهای ماورابنفش به طور موثر در کروماتوگرافی فاز معکوس و تبادل یونی بهره میگیرند. آشکارسازهای ماورا بنفش، حساسیت بالا و قیمت مناسبی دارند و کار کردن با آنها ساده است. به همین دلیل، آشکارسازهای ماورا بنفش، بیشترین استفاده را در کروماتوگرافی HPLC دارند.
طیفسنجی جرمی
روش دیگری موسوم به طیفسنجی جرمی، مزایایی خاصی نسبت به سایر روشها دارد. طیف جرمی را میتوان به سرعت بدست آورد و تنها مقادیر کمی از ماده برای نمونهگیری و تحلیل لازم است. علاوه بر این، دادهای که از این روش بدست میآید، اطلاعات مفیدی را در خصوص ساختار مولکول در اختیار ما قرار میدهد. از ترکیب کروماتوگرافی HPLC و طیفسنج جرمی بمنظور شناسایی ویژه و تعیین مواد شیمیایی استفاده میشود. ذکر این نکته لازم است که ترکیب کروماتوگرافی مایع با طیفسنج جرمی قدری دشوار است چراکه در ابتدا باید تمامی حلال خارج شود.

اصطلاحات مرتبط با HPLC
در ادامه قصد داریم تا پارامترها و اصطلاحات مرتبط با HPLC را بیان کنیم. این پارمترها عبارتند از:
- نرخ جریان
- زمان بازداری
- حجم بازداری
- «سرعت مهاجرت» (Migration Rate)
- فاکتور ظرفیت
- ثابت تعادل و نسبت فاز
دبی جریان
نرخ جریان یا «دبی جریان» (Flow Rate)، بیانگر سرعت حرکت فاز متحرک در داخل ستون است و به منظور محاسبه مقدار مصرف فاز متحرک در بازه زمانی مشخص، مورد استفاده قرار میگیرد. در این خصوص، عبارات دبی حجمی جریان (U) و دبی خطی جریان (u) را میتوان بکار گرفت که در روابط زیر نشان داده شدهاند. در این روابط، بیانگر مساحت مسیر (کانال) جریان است.
زمان بازداری
«زمان بازداری» (Retention Time) را با نشان میدهند و به صورت زمان تزریق نمونه تا زمان «شویش» (Elution) تعریف میشود که برای اندازهگیری آن از نوک قله (پیک) مرتبط با جزء مولکولی بهره میگیرند. زمان بازداری به عوامل مختلفی همچون ساختار مولکول، دبی (سرعت) جریان فاز متحرک و ابعاد ستون بستگی دارد. همچنین، زمانی موسوم به «زمان مرده» (Dead Time) را با نماد برای ذرات مولکولی «بازداری نشده» (non-Retained)، در شویش از ستون در نظر میگیرند.
حجم بازداری
حجم بازداری را به صورت حجم فاز متحرک، از زمان تزریق تا زمان بازداری متناظر با مولکول مورد نظر تعریف میکنند که رابطه آن در زیر آورده شده است. حجم بازداری متناظر با زمان مرده نیز با نام «حجم مرده» (Dead Volume) و با نماد بیان میشود.
سرعت مهاجرت
سرعت مهاجرت عبارتست از سرعت حرکت ذرات از میان ستون که مقدار را به صورت زیر تعریف میکنند:
فاکتور ظرفیت
«فاکتور ظرفیت» (Capacity Factor)، نسبت زمان کاهش یافته به زمان مرده است که با رابطه زیر نشان داده میشود:
ثابت تعادل و نسبت فاز
به هنگام جداسازی مواد، مولکولهایی که در داخل ستون حرکت میکنند را میتوان در تعادل بین فاز متحرک و فاز ساکن در نظر گرفت. این تعادلِ پیوسته، متأثر از ثابت تعادل است و روابط آن را در زیر ملاحظه میکنید. در این روابط، ، غلظت مولی مولکولهای فاز متحرک و ، غلظت مولی مولکولها در فاز ساکن است.

مزایای استفاده از کروماتوگرافی HPLC
مهمترین جنبه بهرهگیری از کروماتوگرافی HPLC امکان «تجزیه و تحلیل دستهای» (Batch Analysis) مواد چندجزئی است. حتی در صورتیکه نمونه مورد نظر، شامل مخلوط هم باشد، از این روش میتوان برای جداسازی، شناسایی و اندازهگیری ماده مطلوب استفاده کرد. در ادامه قصد داریم تا با سه مورد از مزایای کروماتوگرافی HPLC آشنا شویم.
امکان آزمایش نمونههای متنوع
از مزایای کروماتوگرافی با عملکرد بالا این است که میتوان نمونههای متنوعی را از مولکولهای زیستی تا یونها، به کمک آن مورد آزمایش قرار داد. تنوع استفاده از نمونهها و دقت بالای این روش به آزمایشگاهها این امکان را میدهد تا نمونههای مختلف را با صرف هزینه کمتر و دقت بالا، مورد آزمایش قرار دهند.
شرایط آزمایش قابل تنظیم
یکی از دلایلی که میتوان از کروماتوگرافی HPLC برای بررسی نمونههای مختلف استفاده کرد، امکان تنظیم آن برای شرایط مختلف است. همانطور که در متن به آن اشاره شد، جدایش مواد به کمک فاز ساکن انجام میشود. این فاز، در ستون کروماتوگرافی دستگاه قرار دارد و به طور معمول، ۴ نوع مختلف و تجاری از آن وجود دارد که بسته به نوع آزمایش، میتوان از این فازها کمک گرفت.
معمولترین فاز ساکن، جداسازی به کمک فاز معکوس است. اما یک کارشناس کروماتوگرافی ممکن است از سایر روشها همچون فاز نرمال، تبادل یونی یا اندازه طردی بهره بگیرد که شرایط استفاده از هرکدام را در این آموزش بیان کردیم.
کارایی بالا در کروماتوگرافی HPLC
پیش از رونق استفاده از این روش، کروماتوگرافی لایه نازک (TLC) رواج داشت. کروماتوگرافی لایه نازک بر پایه حرکت مواد از طریق گرانش بنا شده بود در حالیکه در HPLC، فشار پمپ برای حرکت سیال بکار گرفته میشود که همین مورد سبب میشود مواد در بازه زمانی ۱۰-۳۰ دقیقه و با دقت بالا، آزمایش شوند. علاوه بر این، بیشتر دستگاههای کروماتوگرافی HPLC به صورت خودکار عمل میکنند. به عبارت دیگر، زمانی که نمونه به دستگاه وارد شود، سایر عملیات به طور خودکار انجام خواهد شد. این امر به کارشناس کروماتوگرافی کمک میکند تا سریعتر و سادهتر، نتایج مورد نظر را تحت بررسی قرار دهد.
اگر این مطلب برای شما مفید بوده است، آموزشها و مطالب زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای مهندسی شیمی
- ٰآموزش کاربرد ریاضیات در مهندسی شیمی
- کروماتوگرافی گازی - از صفر تا صد
- تعیین گروه عاملی به کمک طیفسنجی مادون قرمز -- از صفر تا صد
^^













خیلی عالی بود ممنونم
با عرض سلام و خسته نباشید سوالی داشتم در مورد کروماتوگرام که چرا در برخی مواقع پیک تشکیل شده از یک ماده خود به دو پیک مجزا تقسیم میشود.
با تشکر
اگه منظورتون دو قله ای بودن یک ماده هست. دوتا احتمال داره یا نمونه شما غلظه و باید رقیقش کنید و بعدا این رقت رو در فرمولتون بیارید یا دستگاهتون در قسمت بازدارندگی مشکل داره
با سلام
پاسخ این سوال بستگی به
1- نوع ماده ای که در حال آنالیزش هستید.
2- ستون مورد استفاده دارد.(البته در این مورد جای بحث و اطلاعات بیشتر هست چون بستگی به این دارد هر دو پیک کامل مجزا هست یا دو شاخه شده و سطح زیر هر پیک نیز مهم هست.)
خیلی خوب و مفید بود. برای گزارشکارم دنبال یه چیز تر و تمیز و کامل میگشتم. عالی. ممنون ازتون
عالی