مولکول دو اتمی ناجور هسته چیست؟ – به زبان ساده + ساختار، انواع و کاربردها
مولکول دو اتمی ناجور هسته مولکولی است که از دو اتم متفاوت تشکیل شده است. این مولکولها میتوانند از ترکیب دو اتم با پیوند کووالانسی قطبی تشکیل شوند. برای مثال، هیدروژن کلرید و کربن مونوکسید دو نمونه مولکول دو اتمی ناجور هسته هستند. در این ترکیبات توزیع بار الکترونی نامتقارن بوده و چگالی بار الکترونی در نزدیکی اتم الکترونگاتیوتر، بیشتر است. در این مطلب از مجله فرادرس میآموزیم مولکول دو اتمی ناجور هسته چیست و چه ویژگیهایی دارد.
- میآموزید مولکول دو اتمی ناجور هسته چیست.
- با خصوصیات ساختاری مولکول دو اتمی ناجور هسته آشنا میشوید.
- میتوانید انواع پیوند در مولکول دو اتمی ناجور هسته را تشخیص دهید.
- اوربیتال مولکولی مولکول دو اتمی ناجور هسته را میشناسید.
- با کاربردها و اهمیت مولکول دو اتمی ناجور هسته آشنا میشوید.
- انواع مولکولهای دواتمی و خواص آنها را بررسی کرده و میشناسید.

در ابتدای این مطلب میآموزیم مولکول دو اتمی ناجور هسته چیست. سپس به بررسی مثالهای مولکول دو اتمی ناجور هسته پرداخته و خصوصیات ساختاری آنها را میشناسیم. پس از آن اوربیتال مولکولی را در این مولکولها بررسی کرده و رایجترین ترکیبات دو اتمی ناجور هسته را بررسی میکنیم. در نهایت، کاربردها و اهمیت این مواد را میآموزیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید مولکول دو اتمی ناجور هسته چیست.
مولکول دو اتمی ناجور هسته چیست؟
مولکول دو اتمی ناجور هسته (Heteronuclear Diatomic Molecule) مولکولی است که تنها از دو اتم تشکیل شده و این اتمها با هم متفاوت هستند. پیوند شیمیایی بین اتمهای این مولکولها اغلب از نوع کووالانسی قطبی است. بسیاری از عناصر میتوانند با هم ترکیب شده و مولکول دو اتمی ناجور هسته تشکیل دهند. تشکیل این مولکولها به فشار و دمای موجود بستگی دارد. برای مثال، مولکولهای کربن مونوکسید، نیتریک مونواکسید و هیدروژن کلرید از انواع این مولکولها هستند.
همچنین باید توجه داشت که برخی از ترکیبات دوتایی مانند منیزیم اکسید و سیلیسیم اکسید اغلب به عنوان مولکول دو اتمی شناخته نمیشوند زیرا این ترکیبات در دمای اتاق ساختاری پلیمری خواهند داشت. این نوع ترکیبات تنها در صورت تبخیر شدن و در حالت گازی مولکولهای دو اتمی هستند.
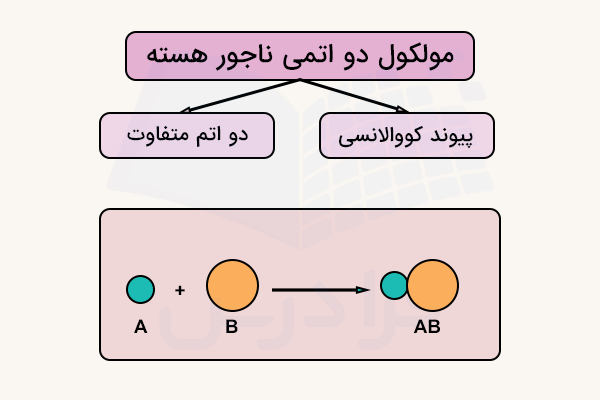
مولکول دو اتمی چیست؟
مولکولهای دو اتمی به طور کلی به مولکولهایی گفته میشود که فرمول واحد شیمیایی آنها از دو اتم تشکیل شده باشد. اگر این دو اتم از یک نوع عنصر باشند، ترکیب «جور هسته» (Homonuclear) و اگر از عناصر مختلف باشند ترکیب «ناجور هسته» (Heteronuclear) تشکیل میدهند.
اگر تا این قسمت از مطلب را مطالعه کردهاید، با مفهوم مولکول دواتمی ناجور هسته آشنا شدهاید. در ادامه مطلب نیز به بررسی بیشتر این مولکولها میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
برخی از مثالهای مولکول دو اتمی جور هسته ترکیباتی مانند مولکول هیدروژن، نیتروژن، فلوئور، کلر، ید، برم، لیتیم و هلیم هستند. هر دو نوع جور هسته و ناجور هسته ترکیبات مولکولی دوتایی، با یک پیوند مستقیم بین دو اتم به هم متصل میشوند. ساختار هندسی تمامی این ترکیبات مشابه است و زاویه پیوندی بین اتمها ۱۸۰ درجه است. پیوند بین اتمها در ترکیبات دو اتمی میتواند از نوع دوگانه (مانند مولکول اکسیژن) و سهگانه (مانند کربن مونوکسید) نیز باشد.
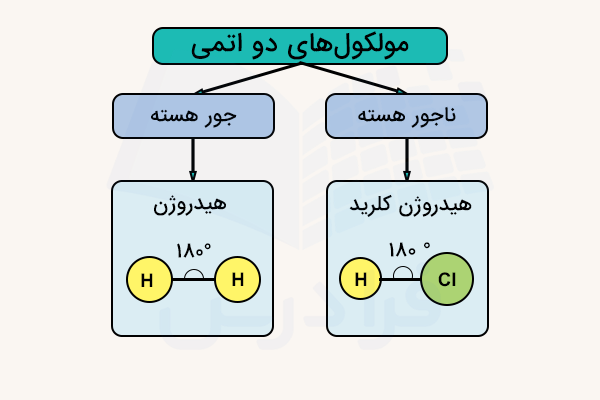
مولکول دو اتمی جور هسته چیست؟
تنها عناصری که در شرایط استاندارد دما و فشار (STP) یا شرایط معمول آزمایشگاهی (۱ بار و ۲۵ درجه سانتیگراد) بهصورت پایدار به شکل مولکولهای دو اتمی جور هسته وجود دارند، در جدول زیر معرفی شدهاند.
| نام مولکول دو اتمی جور هسته | فرمول شیمیایی |
| کلر (گاز) | |
| فلوئور (گاز) | |
| اکسیژن (گاز) | |
| نیتروژن (گاز) | |
| هیدروژن (گاز) | |
| برم (مایع) |
گازهای نجیب (هلیم، نئون، آرگون، کریپتون، زنون و رادون) نیز در این شرایط گازی هستند، اما بهصورت تکاتمی وجود دارند. گازهای دو اتمی جور هسته و گازهای نجیب را در مجموع «گازهای عنصری» یا «گازهای مولکولی» مینامند تا از سایر گازها که ترکیبات شیمیایی هستند، متمایز شوند.
در دماهای کمی بالاتر، هالوژنهایی مانند و نیز بهصورت گاز دو اتمی در میآیند. همه هالوژنها بهصورت دو اتمی مشاهده شدهاند، بهجز استاتین و تنسین که وضعیت آنها نامشخص است. این مواد عموما در دسته عناصر مولکولی قرار گرفته و بررسی میشوند. پیشنهاد میکنیم برای آشنایی بیشتر با این مواد، مطلب عنصر مولکولی مجله فرادرس را مطالعه کنید.
یادگیری شیمی دوازدهم با فرادرس
برای درک بهتر این موضوع که مولکول دو اتمی ناجور هسته چیست، ابتدا باید با مفاهیمی چون پیوند شیمیایی، ساختار اتم، نیروهای بین مولکولی، تعیین قطبیت مواد و مواد مولکولی و کووالانسی آشنا شویم. پیشنهاد میکنیم برای درک بهتر این مفاهیم، به مجموعه فیلم آموزش دروس پایه دوازدهم بخش شیمی مراجعه کنید که با زبانی ساده به بررسی این مباحث میپردازد.
همچنین با مشاهده فیلمهای آموزش فرادرس که لینک آنها در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه مولکول دو اتمی ناجور هسته دسترسی داشته باشید.
- فیلم آموزش فیزیک پایه دوازدهم فرادرس
- فیلم آموزش شیمی ۱ پایه دهم فرادرس
- فیلم آموزش الکتروشیمی کاربردی جامع و با مفاهیم کلیدی فرادرس
جدول مثال مولکول دو اتمی ناجور هسته
در قسمت قبل آموختیم مولکول دو اتمی ناجور هسته چیست. شناخت مولکولهای دو اتمی ناجور هسته اهمیت زیادی در شیمی دارد، زیرا این مولکولها سادهترین نمونهها برای درک مفاهیم بنیادی مانند قطبیت، گشتاور دوقطبی و نظریه اوربیتال مولکولی هستند. با بررسی این مولکولها میتوان فهمید که چگونه اختلاف الکترونگاتیوی باعث توزیع نامتقارن الکترونها میشود و چگونه این موضوع بر خواصی مانند حلالیت، نقطه جوش، واکنشپذیری و برهمکنشهای بینمولکولی تاثیر میگذارد.
علاوه بر این، بسیاری از این مولکولها مانند ، و در فرایندهای صنعتی، زیستی و محیطی نقش مهمی دارند. در جدول زیر، نام و نماد شیمیایی رایجترین مولکولهای دو اتمی ناجور هسته آورده شده است.
| نام مولکول | فرمول شیمیایی |
| هیدروژن فلوئورید | |
| هیدروژن کلرید | |
| هیدروژن برومید | |
| هیدروژن یدید | |
| کربن مونوکسید | |
| نیتروژن مونوکسید | |
| فسفر مونوکسید | |
| گوگرد مونوکسید | |
| کلر مونوکسید | |
| سیلیسیم مونوکسید | |
| هیدروژن سیانید |
خصوصیات ساختاری مولکول دو اتمی ناجور هسته
در مولکولهای دو اتمی ناجور هسته اغلب اختلاف الکترونگاتیوی وجود دارد. این اختلاف بدین معنی است که یکی از این دو اتم تمایل بیشتری به جذب الکترونهای پیوندی به سمت هسته خود دارد. این تمایل بیشتر باعث به وجود آمدن یک گشتاور دوقطبی در مولکول شده و ماهیت پیوند و مولکول را قطبی میکند.
اختلاف الکترونگاتیویته باعث ایجاد پیوند کووالانسی قطبی میشود. در نتیجه، یک ممان دوقطبی به وجود میآید که در آن یک سر مولکول دارای بار جزئی منفی و سر دیگر دارای بار جزئی مثبت است. بنابراین، این مولکولها نسبت به میدانهای الکتریکی و مواد قطبی دیگر رفتار متفاوتی نسبت به مولکولهای دو اتمی جور هستهای دارند. در تصویر زیر، قطبیت و الکترونگاتیوی را در ترکیب هیدروژن فلوئورید مشاهده میکنید.
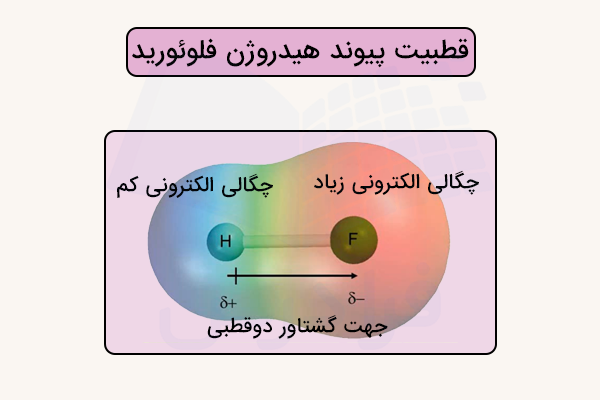
مثال اختلاف الکترونگاتیوی
در مولکولهای دو اتمی ناجور هسته، مانند یا ، تفاوت در الکترونگاتیوی دو اتم باعث میشود پیوند کووالانسی به صورت نامتقارن شکل بگیرد. الکترونگاتیوی تمایل یک اتم برای جذب الکترونهای پیوندی به سمت خود است. بنابراین هرچه اختلاف الکترونگاتیوی بین دو اتم بیشتر باشد، ابر الکترونی پیوند بیشتر به سمت اتم با الکترونگاتیوی بالاتر کشیده میشود. این پدیده باعث ایجاد بار جزئی منفی روی اتم الکترونگاتیوتر و بار جزئی مثبت روی اتم دیگر میشود و در نتیجه مولکول خاصیت قطبی پیدا میکند.
برای درک بهتر اثر اختلاف الکترونگاتیوی در مولکولهای ناجور هسته، به مثالهای زیر دقت کنید. این برهمکنشها در مولکولهای دو اتمی ناجور هسته هیدروژن کلرید، کربن مونوکسید، نیتروژن مونوکسید و ... بررسی شده است. در این موارد، با مقایسه مقدار الکترونگاتیوی عناصر بر اساس مقیاس پاولینگ در جدول تناوبی، اختلاف الکترونگاتیوی به دست میآید.
هیدروژن کلرید
در مولکول هیدروژن کلرید ()، کلر الکترونگاتیوتر از هیدروژن است، بنابراین چگالی الکترونی به سمت کلر کشیده میشود. در نتیجه کلر دارای بار جزئی منفی و هیدروژن دارای بار جزئی مثبت است و جهت گشتاور دوقطبی از هیدروژن به سمت کلر خواهد بود. اختلاف الکترونگاتیوی در این مولکول نسبتا زیاد است و باعث قطبیت قابل توجهی میشود. الکترونگاتیوی کلربرابر با ۳٫۱۶ و الکترونگاتیوی هیدروژن ۲٫۲۰ است، پس اختلاف الکترونگاتیوی برابر ۰٫۹۶ خواهد بود. این مقدار نشاندهنده یک پیوند قطبی قابل توجه است.
هیدروژن فلوئورید
در مولکول هیدروژن فلوئورید ()، الکترونگاتیوی فلوئور ۳٫۹۸ و هیدروژن ۲٫۲۰ است، بنابراین اختلاف الکترونگاتیوی برابر ۱٫۷۸ میشود. این مقدار بسیار بزرگ است و نشان میدهد که الکترونها به شدت به سمت فلوئور کشیده میشوند. در نتیجه فلوئور دارای بار جزئی منفی و هیدروژن دارای بار جزئی مثبت است و جهت گشتاور دوقطبی از هیدروژن به سمت فلوئور خواهد بود و این مولکول یکی از قطبیترین مولکولهای دو اتمی است.
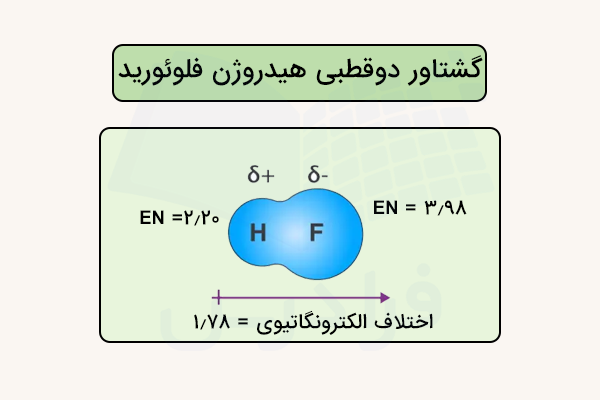
کربن مونوکسید
در مولکول کربن مونوکسید ()، اگرچه کربن و اکسیژن هر دو نافلز هستند، اما اکسیژن الکترونگاتیوتر است و انتظار میرود چگالی الکترونی به سمت اکسیژن کشیده شود. با این حال، به دلیل ساختار الکترونی خاص این مولکول، توزیع بار کمی پیچیدهتر است، ولی در حالت کلی اکسیژن تمایل بیشتری به جذب الکترون دارد و نقش قطب منفی را ایفا میکند، هرچند گشتاور دوقطبی آن نسبت به و کمتر است.
الکترونگاتیوی اکسیژن ۳٫۴۴ و کربن ۲٫۵۵ است، بنابراین اختلاف الکترونگاتیوی برابر ۰٫۸۹ میشود. این مقدار نشان میدهد که پیوند قطبی متوسطی وجود دارد. در حالت کلی الکترونها به سمت اکسیژن کشیده میشوند.
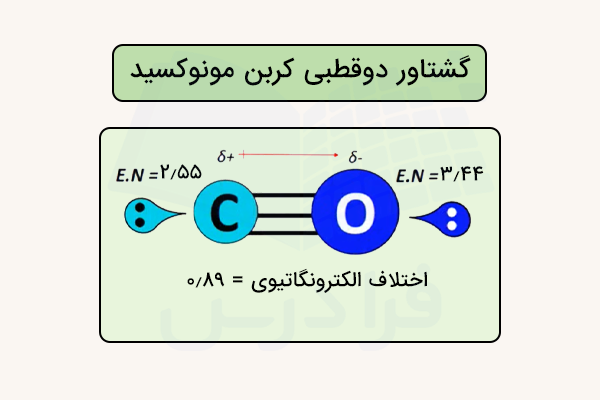
نیتروژن مونوکسید
در مولکول نیتروژن مونوکسید ()، الکترونگاتیوی اکسیژن ۳٫۴۴ و نیتروژن ۳٫۰۴ است و اختلاف آنها برابر ۰٫۴۰ است. این اختلاف کم است و در نتیجه گشتاور دوقطبی ضعیفتری ایجاد میشود. با این حال همچنان اکسیژن الکترونگاتیوتر است و جهت گشتاور دوقطبی از نیتروژن به سمت اکسیژن خواهد بود.
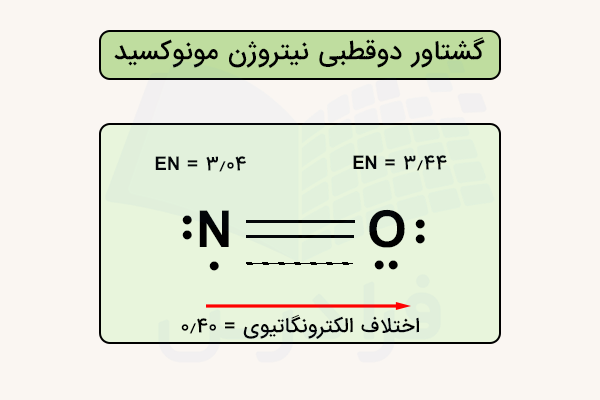
به طور کلی میتوان نتیجه گرفت که هرچه اختلاف الکترونگاتیوی بیشتر باشد، گشتاور دوقطبی بزرگتر و مولکول قطبیتر خواهد بود، و جهت گشتاور دوقطبی همواره به سمت اتمی است که الکترونگاتیوی بیشتری دارد.
پیوند در مولکول دو اتمی ناجور هسته
پیوند شیمیایی بین مولکولهای دو اتمی ناجور هسته پیوند کووالانسی قطبی است. در این ترکیبات اغلب دو اتم نافلزی به هم متصل میشوند. اتصال این اتمها با به اشتراک گذاری اتم با استفاده از پیوند کووالانسی انجام میشود. به دلیل متفاوت بودن نوع اتمها در مولکول دو اتمی ناجور هسته، معمولا بین اتمها اختلاف الکترونگاتیوی وجود دارد.
این بدین معنی است که اتم الکترونگاتیوتر با جذب الکترونهای پیوند به سوی خود دارای بار جزئی منفی شده و اتم دیگر بار جزئی مثبت میگیرد. در نتیجه، نوع پیوند از نوع کووالانسی قطبی و مولکول از نوع مولکول قطبی خواهد بود. برای تشخیص نوع پیوند با استفاده از اختلاف الکترونگاتیوی میتوانیم از جدول زیر استفاده کنیم.
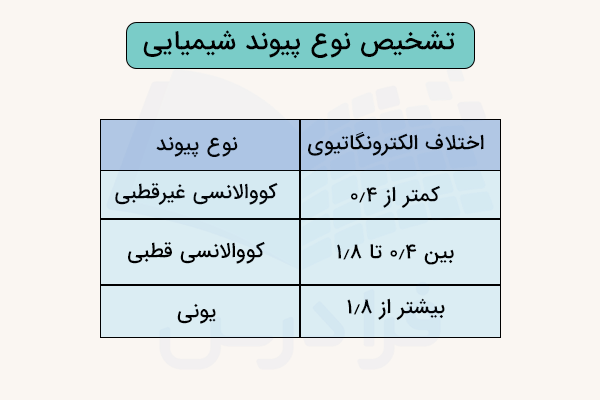
پیوند یونی
با به هم پیونستن یک یون مثبت (کاتیون) و یک یون منفی (آنیون) یک ترکیب یونی تشکیل میشود. پیوند بین دو یون مثبت و منفی، از نوع یونی است. پیوند یونی با انتقال کامل الکترونها از یک یون به یون دیگر تشکیل میشود.
برای مثال، ترکیب دو اتمی سدیم کلرید، از نوع یونی است. معمولا ترکیبات یونی دوتایی جزو دسته مولکول دو اتمی ناجور هسته قرار نمیگیرند. پیشنهاد میکنیم برای اشنایی بیشتر با انواع پیوند در شیمی، فیلم آموزش پیوند شیمیایی فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
اوربیتال مولکولی مولکول دو اتمی ناجور هسته
در تئوری اوربیتال مولکولی، از ترکیب اوربیتالهای اتمی اتمهای مختلف، اوربیتالهای مولکولی پیوندی و ضد پیوندی به وجود میآید. میزان سطوح انرژی اوربیتالهای مولکولی در ترکیبات دو اتمی ناجور هسته، بسته به نوع اتمها و میزان الکترونگاتیوی آنها مختلف است. بنابراین میزان پایداری این اوربیتالها نیز بسته به این عوامل تغییر میکند.
به طور کلی، میزان پایداری اوربیتالهای پیوندی بیشتر و میزان انرژی آنها کمتر است. به همین ترتیب، میزان پایداری اوربیتالهای ضدپیوندی کمتر و میزان انرژی آنها بیشتر است. در تصویر زیر، انواع کل اوربیتالهای پیوندی و ضدپیوندی مشخص شده است.
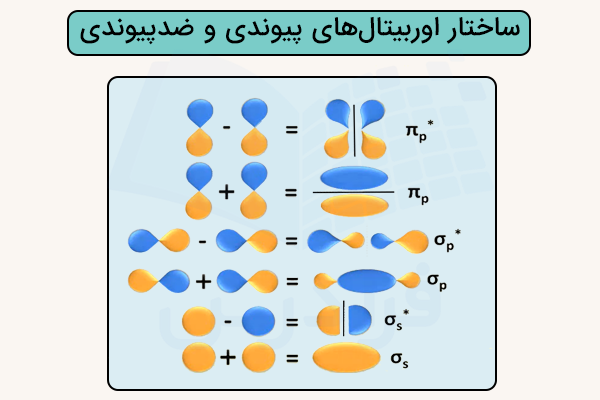
بررسی انرژی اوربیتالهای مولکولی
در مولکولهای دو اتمی ناجور هسته، اغلب میزان انرژی اوربیتال اتم الکترونگاتیوتر پایینتر و پایدارتر است. برای تشخیص بهتر برهمکنش اوربیتالهای اتمی و تشکیل اوربیتالهای مولکولی در این مولکولها بهتر است این موارد را به صورت هندسی بررسی کرده و الکترونگاتیوی را نیز در مولکول برررسی کنیم.
برای مثال، مولکول کربن مونوکسید را در نظر بگیرید. در این مولکول، یک اتم کربن با الکترونگاتیوی کمتر به یک اتم اکسیژن با الکترونگاتیوی بیشتر متصل شده است. پیوند بین این دو اتم از نوع سهگانه بوده در نتیجه از یک پیوند سیگما و دو پیوند پای تشکیل شده است که هر کدام ۲ الکترون داشته و در مجموع ۶ الکترون به صورت پیوندی در این پیوند وجود دارند.
در این دو اتم، دو اوربیتال s با هم ترکیب شده و یک پیوند سیگما را به وجود آورده اند و ۴ اوربیتال p با هم ترکیب شده و دو پیوند پای را تشکیل دادهاند. این پیوندها و اوربیتالها در تصویر زیر مشخص شده است.
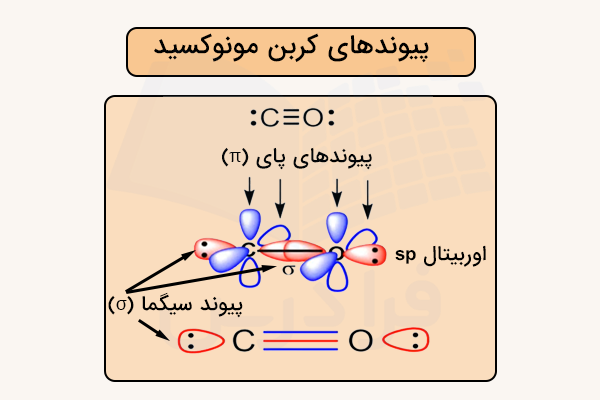
هر جفت از این اوربیتالها با هم ترکیب شده و دو اوربیتال مولکولی تشکیل میدهند که یکی از جمع ریاضی و یکی از تفاضل ریاضی این اوربیتالها به وجود میآید. جمع این برهمکنشهای جانبی باعث افزایش چگالی احتمال الکترون در نواحی بالا و پایین محور بینهستهای میشود. بنابراین یک اوربیتال مولکولی پیوندی تشکیل میشود که به آن اوربیتال گفته میشود. در مقابل، تفاضل این اوربیتالها باعث همپوشانی لوبهایی با علامت مخالف میشود و یک صفحه گرهای عمود بر محور بینهستهای ایجاد میکند. بنابراین این حالت یک اوربیتال ضدپیوندی است.
تراز انرژی اوربیتال ها
نظریه اوربیتال مولکولی نشان میدهد که هنگام تشکیل مولکولهای دو اتمی ناجور هسته، اوربیتالهای اتمی از اتمهای مختلف با هم ترکیب میشوند و اوربیتالهای مولکولی خاصی را ایجاد میکنند. برخلاف مولکولهای جور هسته که در آنها اوربیتالهای اتمی انرژی و شکل مشابهی دارند، در مولکولهای ناجور هسته تفاوت در ویژگیهای اتمی باعث میشود سهم اتمها در اوربیتالهای پیوندی و ضدپیوندی برابر نباشد.
این موضوع منجر به ترازهای انرژی متفاوت و آرایش الکترونی خاصی میشود که بر خواص شیمیایی تاثیر میگذارد. این اوربیتالها بسته به نوی پیوند و مرتبه آن و همچنین میزان الکترونگاتیوی اتمهای مولکول ناجور هسته تغییر میکند. این تغییرات در تصویر زیر نمایش داده شده است.
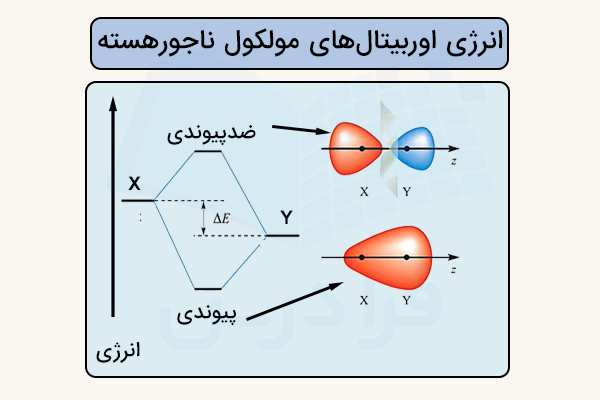
بررسی مولکولهای دو اتمی ناجور هسته
در بررسی اوربیتالهای مولکولی در مولکولهای دو اتمی ناجور هسته، باید توجه داشت که به دلیل تفاوت در الکترونگاتیوی، انرژی اوربیتالهای اتمی دو اتم برابر نیست. اتم الکترونگاتیوتر اوربیتالهای با انرژی پایینتری دارد و بنابراین در تشکیل اوربیتالهای مولکولی، سهم بیشتری در اوربیتالهای پیوندی خواهد داشت. در مقابل، اوربیتالهای ضدپیوندی بیشتر به اتم با الکترونگاتیوی کمتر نزدیک هستند. این عدم تقارن باعث میشود اوربیتالهای مولکولی در این نوع مولکولها نامتقارن باشند.
برای درک بهتر مفاهیم قسمت قبل، نحوه تشکیل پیوند و همپوشانی اوربیتالهای اتمی را در مولکولهای دو اتمی ناجور هسته رایج بررسی میکنیم.
هیدروژن فلوئورید
در مولکول HF، اوربیتال ۱s هیدروژن با یکی از اوربیتالهای ۲p فلوئور که در راستای محور بین دو هسته قرار دارد همپوشانی میکند و یک پیوند سیگما تشکیل میدهد. به دلیل اختلاف الکترونگاتیوی زیاد، اوربیتال ۲p فلوئور انرژی پایینتری دارد، بنابراین اوربیتال مولکولی پیوندی بسیار شبیه به اوربیتال فلوئور است و الکترونها بیشتر در اطراف فلوئور حضور دارند.
در عین حال، دو اوربیتال ۲p دیگر فلوئور که عمود بر محور پیوند هستند، در همپوشانی شرکت نمیکنند و به صورت اوربیتالهای ناپیوندی باقی میمانند. اوربیتال ضدپیوندی سیگما استار نیز بیشتر به هیدروژن نزدیک است و انرژی بالاتری دارد، به همین دلیل در حالت پایه اشغال نمیشود.
هیدروژن کلرید
در مولکول هیدروژن کلرید ()، اوربیتال ۱s هیدروژن با اوربیتال ۳p کلر در راستای محور پیوند همپوشانی کرده و پیوند سیگما تشکیل میدهد. از آنجا که اختلاف الکترونگاتیوی کمتر از HF است، اوربیتال مولکولی پیوندی هنوز به سمت کلر متمایل است اما نه به شدت HF. کلر نیز مانند فلوئور دارای اوربیتالهای p ناپیوندی است که در تشکیل پیوند شرکت نمیکنند. بنابراین در این مولکول هم یک پیوند سیگما داریم و چند جفت الکترون ناپیوندی روی کلر باقی میماند.
هیدروژن یدید
در مولکول هیدروژن یدید ()، اوربیتال ۱s هیدروژن با اوربیتال ۵p ید همپوشانی میکند و پیوند سیگما تشکیل میشود. به دلیل بزرگ بودن اتم ید و پخش بودن اوربیتالهای آن، همپوشانی ضعیفتر است و در نتیجه پیوند نسبت به و ضعیفتر میشود. همچنین اختلاف الکترونگاتیوی کمتر است، بنابراین اوربیتال مولکولی پیوندی نسبت به دو حالت قبلی متقارنتر است، هرچند هنوز کمی به سمت ید متمایل است. اوربیتالهای دیگر ید نیز عمدتا به صورت ناپیوندی باقی میمانند.
کربن مونوکسید
در مولکول کربن مونوکسید ()، هر دو اتم دارای اوربیتالهای ۲s و ۲p هستند و این اوربیتالها با هم ترکیبهای پیچیدهتری ایجاد میکنند. اوربیتالهای ۲s با هم اوربیتالهای سیگما و سیگما استار میسازند و اوربیتالهای ۲p نیز بسته به جهتگیری خود، اوربیتالهای سیگما و پای و پای استار تشکیل میدهند. در راستای محور بین دو هسته، همپوشانی ۲p باعث تشکیل پیوند سیگما میشود و در جهتهای عمود، دو پیوند پای شکل میگیرد، بنابراین در مجموع یک پیوند سهگانه شامل یک سیگما و دو پای وجود دارد.
به دلیل اختلاف الکترونگاتیوی، اوربیتالهای پیوندی بیشتر به سمت اکسیژن متمایل هستند، اما به علت پدیده اختلاط اوربیتالهای s و p، ترتیب انرژی اوربیتالها کمی پیچیدهتر از حالت ساده است و همین موضوع باعث برخی ویژگیهای خاص این مولکول میشود.
نیتروژن مونوکسید
در مولکول نیتروژن مونوکسید ()، وضعیت مشابه CO است با این تفاوت که یک الکترون فرد وجود دارد. اوربیتالهای ۲s و ۲p نیتروژن و اکسیژن با هم ترکیب شده و مجموعهای از اوربیتالهای سیگما، پی، سیگما استار و پای استار تشکیل میدهند. در اینجا نیز یک پیوند سیگما و پیوندهای پای وجود دارد، اما یکی از اوربیتالهای پای استار دارای یک الکترون جفتنشده است. این موضوع باعث میشود مرتبه پیوند برابر ۲.۵ باشد و مولکول خاصیت پارامغناطیسی پیدا کند. به دلیل الکترونگاتیوی بیشتر اکسیژن، اوربیتالهای پیوندی بیشتر به سمت آن متمایل هستند.
کاربردها و اهمیت مولکول دو اتمی ناجور هسته
در این مطلب از مجله فرادرس آموختیم مولکول دو اتمی ناجور هسته چیست. درک مولکول دو اتمی ناجور هسته نشان میدهد که چگونه تفاوت در ویژگیهای اتمی بر واکنشپذیری شیمیایی تاثیر میگذارد. وجود پیوندهای قطبی باعث ایجاد برهمکنشهای خاص با ترکیبات قطبی یا یونی میشود که میتواند بر حلالیت، نقطه جوش و الگوهای واکنشپذیری اثر بگذارد.
همچنین بررسی ساختار اوربیتالهای مولکولی آنها کمک میکند پیشبینی کنیم این مولکولها چگونه در واکنشهای شیمیایی شرکت میکنند و درک جامعتری از رفتار شیمیایی به دست آوریم. در ادامه، کاربردها و اهمیت مولکول دو اتمی ناجور هسته را بررسی میکنیم.
درک پیوند شیمیایی
ترکیبات دو اتمی ناجور هسته مولکولهای سادهای با دو اتم هستند و به همین دلیل مدل مناسبی برای درک پدیدههای شیمیایی مانند قطبیت پیوند، اوربیتالهای مولکولی، برهمکنشهای الکترومغناطیسی اتمها، روش تشکیل پیوند شیمیایی و ... هستند.
شیمی فیزیک و طیف سنجی
از مولکولهای دو اتمی ناجور هسته در علوم شیمی فیزیک و طیف سنجی برای بررسی و مطالعه فعالیتها و انرژیهای ارتعاشی، چرخشی و الکترونی استفاده میشوند.
شیمی نجوم و کیهان شناسی
بسیاری از مولکولهای دو اتمی ناجور هسته در فضاهای میان استارهای و کیهان وجود دارند. برای مثال مولکولهای OH، CN، CH و ... در این فضا وجود دارند.
شیمی صنعتی و کاتالیست ها
بسیاری از مولکولهای دو اتمی ناجور هسته مانند NO یاCN میتوانند مانند یک لیگاند عمل کرده و با متصل شدن به اتمهای فلزی واسطه، ترکیبات کمپلکس یا کاتالیستها را تشکیل دهند. این مواد همچنین میتوانند به عنوان پیش ماده برای تولید و سنتز سایر مواد نیز استفاده شوند.












