انواع مولکول ها در شیمی – به زبان ساده
مولکولها گروهی از اتمهای به هم متصل هستند که یک ساختار شیمیایی واحد را تشکیل میدهند. این ساختارهای شیمیایی خواص فیزیکی و شیمیایی منحصر به فردی دارند که بسته به نوع و تعداد اتمها و پیوندهای شیمیایی متفاوت است. انواع مولکول ها در شیمی بسته به تعداد اتم و نوع اتمها میتوانند به مولکولهای تک اتمی و چند اتمی، آلی و معدنی، مولکولهای کوچک و بزرگ، قطبی و غیرقطبی و زیستی تقسیم شوند. در این مطلب از مجله فرادرس میآموزیم انواع مولکولها در شیمی چیست. در ابتدای این مطلب میآموزیم انواع مولکول ها در حوزههای مختلف بررسی چیست. سپس تعریف مولکول و نمایش و نام گذاری آنها آشنا میشویم. در ادامه مثالها و انواع مولکول را از نظر تعداد اتم، تفاوت اتمها، نوع اتمها، اندازه و قطبیت بررسی میکنیم. در نهایت خواص انواع مولکول ها را میآموزیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید انواع مولکول چیست.
- با انواع مولکولها از نظر شکل، اندازه، پیوند و ... آشنا میشوید.
- با روش نمایش انواع مولکولها آشنا میشوید.
- مثالهای مختلف انواع مولکول ها را بررسی میکنید.
- با شکل انواع مولکولها آشنا میشوید.
- پیوند و اندازه مولکولهای مختلف را میشناسید.
- با ویژگیها و خواص فیزیکی و شیمیایی مولکول آشنا میشوید.

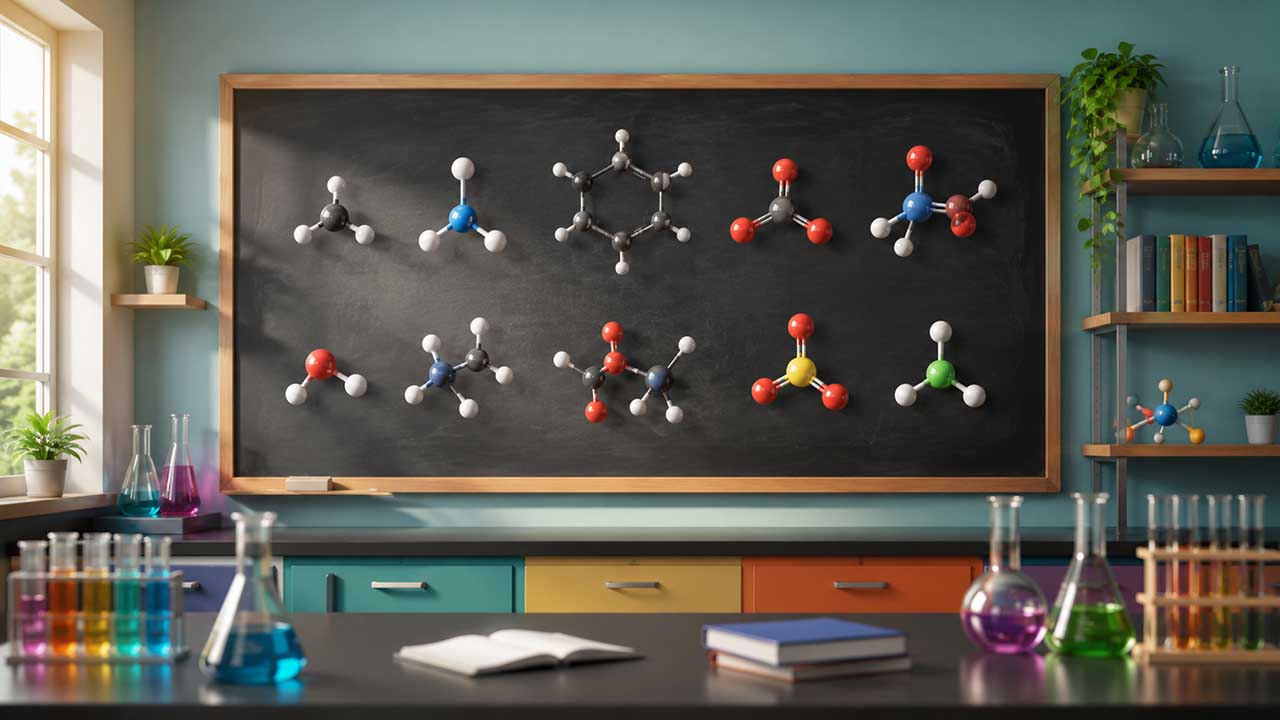
انواع مولکول ها
انواع مولکول ها در شیمی به نوع و تعداد اتمها و همچنین پیوندهای شیمیایی بستگی دارند. در ادامه دستهبندی انواع مولکول ها را به صورت مختصر معرفی میکنیم.
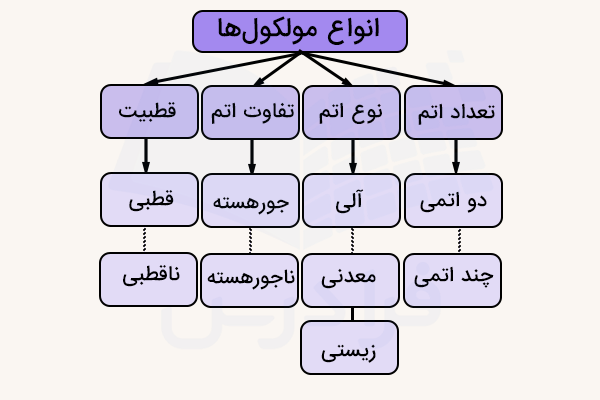
انواع مولکول ها از نظر تعداد اتم
مولکولها میتوانند از یک یا چند اتم تشکیل شده باشند. مولکولهای تک اتمی گاهی به نام مولکول عنصری نیز شناخته میشوند و بسیار نادرند. مولکولهای دو اتمی از دو اتم تشکیل شدهاند و به همین ترتیب مولکولهای سه و چند اتمی نیز وجود دارند.
انواع مولکولها از نظر تعداد اتم به دستههای زیر تقسیم میشوند.
- مولکول دو اتمی
- مولکول سه اتمی
- مولکول چند اتمی
انواع مولکول از نظر تفاوت اتم ها
مولکولها میتوانند از اتمهای یکسان یا از اتمهای متفاوت تشکیل شده باشند. بدین ترتیب مولکولها از نظر تفاوت اتمها به دو نوع جورهسته (همونوکلیر) و ناجورهسته (هترونوکلیر) تقسیم میشوند.
اگر تا این قسمت از مطلب را مطالعه کردهاید با انواع مولکول ها از نظر تفاوت اتمها و تعداد اتمها آشنا شدهاید. در ادامه این مطلب نیز به بررسی سایر انواع مولکول ها میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
انواع مولکول ها از نظر نوع اتم
در شیمی و بررسی مولکولها و واکنشهای شیمیایی معمولا اتمها و مواد به دو دسته آلی و معدنی تقسیم میشوند. به همین ترتیب مولکولها نیز از نظر نوع اتمها میتوانند از نوع مولکول آلی یا مولکول معدنی باشند. مولکولهای آلی غالبا از اتمهای کربن و مولکولهای معدنی از مواد معدنی و فلزی تشکیل شدهاند.
انواع مولکول ها از نظر اندازه
مولکولها میتوانند با تعداد اتمهای بسیار کم (دو یا سه) یا تعداد بسیار زیاد اتم (پلیمرها) اندازههای متفاوتی داشته باشند. برخی از مولکولهای آلی مانند تفلون بسیار بزرگ بوده و برخی از مولکولها مانند مولکول آب کوچک هستند. بدین ترتیب انواع مولکول ها از نظر اندازه به دستههای زیر تقسیم میشوند.
- ریز مولکولها
- درشت مولکولها
انواع مولکول ها از نظر پیوند
نوع پیوند بین اتمهای سازنده مولکول نیز میتوانند تعیین کننده نوع مولکول باشد. در مولکولهایی که پیوند بین آنها اغلب از نوع پیوند اشتراکی کووالانسی است، این پیوند میتواند انواع قطبی و ناقطبی داشته باشد. بدین ترتیب انواع مولکول ها از نظر نوع پیوند میتوانند به دو نوع مولکول قطبی و مولکول ناقطبی تقسیم شوند.
نکته: ترکیباتی که از پیوندهای یونی تشکیل شده باشند، ترکیب یونی هستند و اغلب به عنوان ترکیب مولکولی در نظر گرفته نمیشوند. انواع مولکولهای ذکر شده در قسمتهای بعدی توضیح داده خواهند شد.
یادگیری علوم هفتم با فرادرس
برای درک بهتر انواع مولکول ها نیاز است ابتدا با مفاهیمی چون اتم، ترکیب، مولکول، پیوند شیمیایی، انواع مواد و ... آشنا شویم. پیشنهاد میکنیم برای یادگیری بهتر این مفاهیم، به مجموعه فیلم آموزش دروس پایه هفتم فرادرس، بخش علوم تجربی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این موارد میپردازد.
همچنین با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه انواع مولکول ها دسترسی داشته باشید.
- فیلم آموزش شیمی ۱ پایه دهم و گواهینامه فرادرس
- فیلم آموزش علوم تجربی پایه نهم بخش شیمی فرادرس
- فیلم آموزش علوم تجربی پایه هشتم بخش شیمی فرادرس
مولکول چیست؟
برای درک بهتر انواع مولکول بهتر است ابتدا مروری بر تعریف مولکول داشته باشیم. مولکولها ترکیبات شیمیایی هستند که از به هم پیوستن اتمهای مختلف با استفاده از پیوند شیمیایی تشکیل شدهاند. برخی از مولکولها از چندین اتم و برخی از آنها از یک یا دو اتم تشکیل شدهاند.
تقریبا تمامی اجسام و موجوداتی که در اطراف ما وجو دارند، از اتمها و مولکولها تشکیل شدهاند. برای مثال، آب از مولکول هیدروژن اکسید و قند از مولکول گلوکز تشکیل شده است. مولکولهای مختلف میتوانند اندازهها، انواع، ساختار و پیچیدگیهای بسیار متفاوتی داشته باشند. بسیاری از مولکولها در طبیعت وجود دارند و بسیاری از مولکولها در آزمایشگاه و فرآیندهای شیمیایی به صورت مصنوعی تولید میشوند.
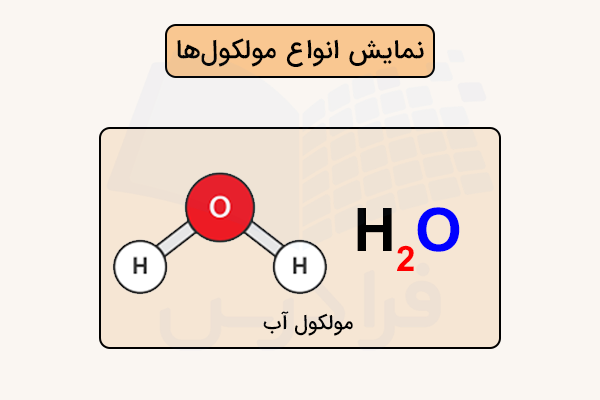
نمایش انواع مولکول ها
برای نشان دادن نوع و تعداد اتمهای موجود در یک مولکول، از فرمول مولکولی استفاده میشود. در این فرمول، عددی که پایین نماد عنصر نوشته میشود تعداد اتمهای آن عنصر را نشان میدهد. اگر عددی وجود نداشته باشد، یعنی فقط یک اتم از آن عنصر در مولکول حضور دارد.
برخی عنصرها بهصورت مولکولهای بزرگتر نیز وجود دارند. برای مثال، گوگرد معمولا بهصورت مولکول هشت اتمی و فسفر بهصورت مولکول چهار اتمی دیده میشود. در نمایش شکل مولکولها، هر اتم معمولا بهصورت یک کره کوچک نشان داده میشود که محل هسته اتم را مشخص میکند. خطهایی که میان این کرهها کشیده میشوند، اتصال بین اتمها را نشان میدهند. این اتصال را پیوند شیمیایی مینامند.
فرمول مولکولی
فرمول مولکولی برای نمایش ساختار یک مولکول به کار میرود. این فرمول تعداد دقیق و نوع اتمهای سازنده مولکول را با استفاده از نماد شیمیایی و اعداد مشخص میکند. فرمول مولکولی با نمایش دقیق ساختار مولکول به دانشمندان این امکان را میدهد تا مواد مختلف را شناسایی کرده و خواص آنها را درک کنند و رفتار آنها را در واکنشهای شیمیایی پیشبینی کنند.
نام گذاری انواع مولکول ها
در ترکیبهای دوتایی، یعنی ترکیبهایی که فقط از دو عنصر تشکیل شدهاند، برای نامگذاری این مراحل انجام میشود.
- ابتدا عنصرهای موجود در مولکول مشخص میشوند.
- نام عنصر اول بدون تغییر نوشته میشود. اگر تعداد اتمهای آن بیشتر از یک باشد، از پیشوند عددی استفاده میشود.
- برای عنصر دوم، پیشوند عددی به همراه ریشه نام عنصر و پسوند «-ید» بهکار میرود.
- سپس دو بخش کنار هم قرار میگیرند و نام کامل ترکیب ساخته میشود.
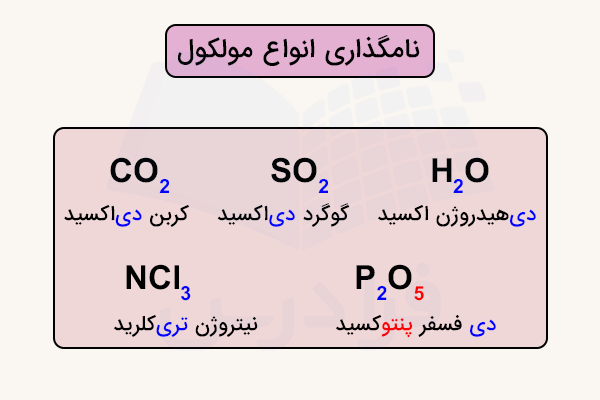
برای نشان دادن تعداد اتمها از پیشوندهای عددی استفاده میشود. برای مثال پیشوند مونو برای یک، دی برای دو، تری برای سه، تترا برای چهار، پنتا برای پنج، هگزا برای شش و به همین ترتیب استفاده میشوند. برای مثال، اگر مولکولی از یک اتم گوگرد و دو اتم اکسیژن تشکیل شده باشد، نام آن دیاکسید گوگرد خواهد بود.
نکته مهم این است که این سیستم نامگذاری دوطرفه است. یعنی هم از روی فرمول میتوان نام ترکیب را نوشت و هم از روی نام میتوان فرمول را به دست آورد. برای مثال، از نام نیتروژن تریکلرید فرمول بهدست میآید که نشان میدهد یک اتم نیتروژن و سه اتم کلر وجود دارد. همچنین از نام دیفسفر پنتوکسید میتوان فرمولی بهدست آورد که شامل دو اتم فسفر و پنج اتم اکسیژن است.
نام گذاری مولکولهای چندتایی
اگر در یک ترکیب مولکولی بیش از دو عنصر وجود داشته باشد، معمولا یک یون چنداتمی در ساختار ترکیب وجود دارد. این ترکیبات در مجموع یونی بوده اما بین اتمهای یون چند اتمی پیوند کووالانسی وجود دارد. در چنین موارد، ابتدا نام کاتیون و سپس نام یون چند اتمی مانند (نیترات، کربنات، سولفات و ...) نوشته میشود. برای مثال، نام و فرمول مولکولی برخی از عناصر در جدول زیر آورده شده است.
| فرمول مولکولی | نام موکلول |
| سدیم نیترات | |
| منیزیم هیدروکسید | |
| پتاسیم کربنات | |
| سدیم سولفات | |
| سدیم پرکلرات | |
| منیزیم کرومات | |
| پتاسیم نیترات | |
| کلسیم کربنات |
نامگذاری مولکولهای آلی
مولکولهای آلی و هیدروکربنها به شیوه متفاوتی نامگذری میشوند. این ترکیبات که از تعداد بیشتری اتم نسبت به ترکیبات دوتایی تشکیل شدهاند، با شمارهگذاری اتمهای کربن نامگذاری میشوند. همچنین، پیشوندها و پسوندهای مختلفی برای نامگذاری این ترکیبات با توجه به نوع آنها (آلکان، آلکن، آلکین، ترکیبات حلقوی و ...) استفاده میشوند.
برای مثال، نام برخی از هیدروکربنها در تصویر زیر آورده شده است.
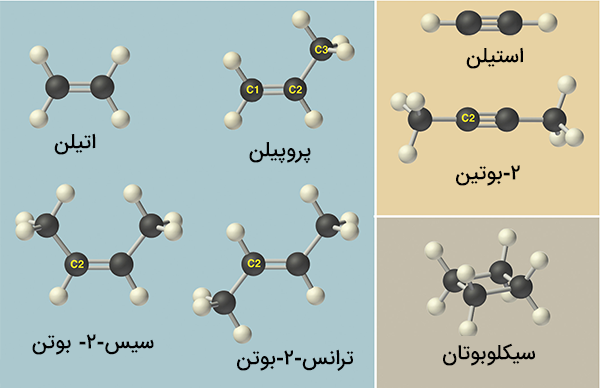
پیشنهاد میکنیم برای آشنایی با شیوه نامگذاری این ترکیبات به شکل کامل، مطلب نام گذاری هیدروکربن ها را در مجله فرادرس را مطالعه کنید.
نام رایج مولکول ها
برخی ترکیبات نامهای رایج و پذیرفته شده تری دارند. برای مثال معمولا آب نامیده میشود نه دی هیدروژن مونوکسید، و بیشتر آمونیاک نام دارد تا نیتروژن تری هیدرید. در جدول زیر نام رایج برخی از مولکولها آورده شده است.
| نام رایج مولکول | فرمول مولکولی |
| آب | |
| آمونیاک | |
| هیدروژن پراکسید | |
| گلوکز | |
| کافئین | |
| گچ | |
| آهک زنده | |
| اوزون | |
| نمک |
مثال انواع مولکول
همانطور که در قسمتهای قبل توضیح دادیم، تقریبا تمامی موادی که در اطراف ما وجود دارند، از مولکولها تشکیل شدهاند. این مولکولها میتوانند انواع مختلفی داشته باشند و هر یک در دستهبندیهای مختلف قرار گیرد. در ادامه برخی از مثالهای انواع مولکول ها را بررسی میکنیم.
مولکول آب
مولکول آب در شیمی از هیدروژن و اکسیژن تشکیل شده است. این مولکول یک مولکول غیر آلی، سه اتمی و قطبی است. فرمول مولکول آب به شکل است.
مولکول کربن دی اکسید
کربن دی اکسید یکی از فراوانترین مولکولهای روی زمین است. این مولکول یک مولکول آلی، خطی، غیرقطبی و سه اتمی است. این مولکول توسط تنفس و واکنش سوختن مواد آلی تولید شده و در فتوسنتز مصرف میشود. فرمول مولکولی کربن دی اکسید به شکل است.
مولکول اکسیژن
مولکول اکسیژن یک مولکول دو اتمی گازی و خطی است. این مولکول کوچک از دو اتم اکسیژن مشابه تشکیل شده و از نوع جورهسته است. فرمول مولکولی اکسیژن به شکل است.
مولکول گلوکز
گلوکز نوعی قند است که در بسیاری از مواد یافت میشود. این مولکول یک مولکول آلی متشکل از کربن و هیدروژن و اکسیژن است و ساختاری غیرقطبی دارد. فرمول مولکولی این مولکول به شکل است.
مولکول اتانول
مولکول اتانول یک مولکول کوچک آلی است که ساختاری الکلی دارد این مولکول قطبی بوده و از اتمهای کربن، هیدروژن و اکسیژن تشکیل شده است. فرمول مولکولی مولکول اتانول به شکل است.
مولکول متان
مولکول متان که گازی متشکل از کربن و هیدروژن است، مولکولی آلی و غیرقطبی است. این مولکول در گاز شهری وجود داشته و برای سوختن و تولید گرما استفاده میشود و فرمول مولکولی آن به شکل است.
مولکول استیک اسید
استیک اسید یک مولکول آلی قطبی است که ساختار اسیدی داشته و در واقع همان سرکه است. از این مولکول در بسیاری از موارد استفاده شده و فرمول مولکولی آن به شکل است.
مولکول DNA
مولکول DNA (دیانای) یا اسید دئوکسیریبونوکلئیک یک ماکرومولکول زیستی است که اطلاعات ژنتیکی موجودات زنده را ذخیره، نگهداری و منتقل میکند. مولکول DNA یک ماکرومولکول زیستی آلی، بسیار بزرگ و قطبی است که از پیوندهای کووالانسی در ستون قندی-فسفاتی و پیوندهای هیدروژنی بین بازهای نیتروژنی تشکیل شده است.
انواع مولکول ها از نظر تعداد اتم
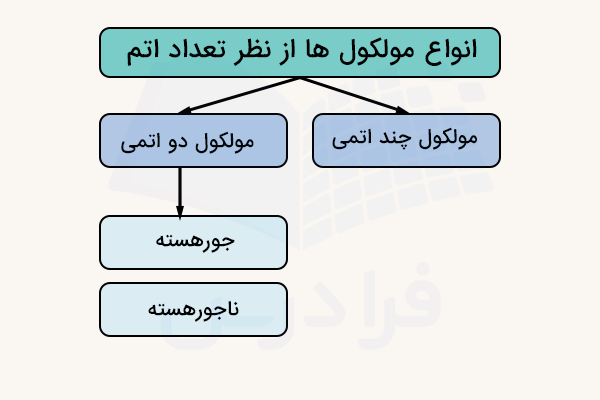
در قسمتهای قبل اشاره کردیم که موکلولها از نظر تعداد اتمی به مولکولهای دو اتمی، سه اتمی و چند اتمی تقسیم میشوند. در ادامه این انواع را توضیح میدهیم.
مولکول دو اتمی
مولکولهای دو اتمی تنها از دو اتم تشکیل شدهاند. این نوع مولکولها میتوانند جورهسته یا ناجورهسته باشند.
مولکول دواتمی جور هسته
این نوع مولکولها از به هم پیوستن دو اتم یکسان تشکیل شدهاند. بسیاری از گازها به این شکل در طبیعت وجود دارند. از مولکولهای دواتمی جورهسته میتوان به مولکول هیدروژن، مولکول اکسیژن، مولکول گوگرد، مولکول نیتروژن و مولکولهای هالوژنهایی مانند فلوئور، ید و برم اشاره کرد.
این مولکولها ساختاری خطی دارند، زاویه پیوندی آنها ۱۸۰ درجه است و کاملا ناقطبی هستند. برای مثال مولکولهای هیدروژن ()، نیتروژن ()، اکسیژن ()، فلوئور ()، کلر ()، برم ()، ید () از مولکولهای دو اتمی جورهسته هستند.
مولکول دواتمی ناجورهسته
این مولکولها از به هم پیوستن دو اتم متفاوت تشکیل شدهاند. این نوع از مولکول عموما قطبی است و ساختاری خطی دارد. مولکولهای مونوکسید کربن ()، مونوکسید نیتروژن ()، هیدروژن کلرید ()، هیدروژن فلورید ()، برمید هیدروژن ()، یدید هیدروژن () از مولکولهای دو اتمی ناجورهسته هستند.
مولکولهای چند اتمی
مولکولهای چند اتمی از به هم پیوستن چند اتم متفاوت تشکیل شدهاند. این مولکولها انواع و تنوع بسیاری دارند. برای مثال، مولکولهای آب، کربن دی اکسید و ... مولکولهای چند اتمی هستند. این نوع مولکولها به دلیل وجود اتمهای مختلف و تعداد متفاوت آنها میتوانند قطبی یا غیرقطبی، با شکل هندسی متفاوت و اندازه متفاوت باشند. در جدول زیر چند مثال از این مولکول ها آورده شده است.
| فرمول مولکولی | نام مولکول |
| آب | |
| کربن دی اکسید | |
| آمونیاک | |
| متان | |
| اوزون | |
| اسید سولفوریک | |
| اسید نیتریک | |
| اتانول | |
| گلوکز | |
| سدیم کربنات |
انواع مولکول از نظر تفاوت اتمها
همانطور که در قسمتهای قبل اشاره کردیم، مولکولها از نظر تفاوت نوع اتمها میتوانند به دو نوع جور هسته و ناجور هسته تقسیم شوند. در ادامه این انواع را توضیح میدهیم.
مولکول جورهسته
مولکولهای جور هسته مولکولهایی هستند که تنها از یک نوع اتم تشکیل شده باشند. این نوع مولکولها میتوانند دو یا تعداد بیشتری اتم داشته باشند. برای مثال مولکول اکسیژن یک مولکول جورهسته با دو اتم، مولکول اوزون یک مولکول جورهسته با سه اتم و مولکول گوگرد یک مولکول جورهسته با ۸ اتم است.
در جدول زیر برخی از این نوع مولکولها آورده شده است.
| نام مولکول | فرمول مولکولی |
| هیدروژن | |
| اوزون | |
| گوگرد حلقوی | |
| فسفر سفید | |
| اکسیژن | |
| کلر |
مولکول ناجورهسته
مولکولهای ناجور هسته مولکولهایی هستند که از انواع مختلفی از اتمها تشکیل شدهاند. این نوع دستهبندی بیشتر برای مولکولهای دواتمی مورد استفاده قرار میگیرد. برای مثال مولکولهای کربن مونوکسید و نیتروژن مونوکسید از این نوع هستند.
انواع مولکول ها از نظر نوع اتم ها
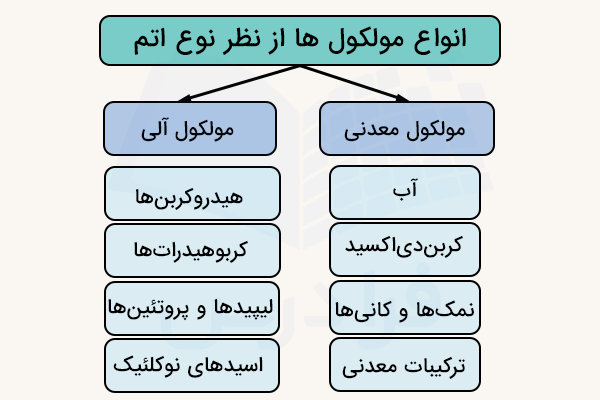
انواع مولکول ها از نظر نوع اتمها را میتوان به دو دسته مولکولهای آلی و معدنی تقسیم کرد. مولکولهای آلی مولکولهایی هستند که قسمت عمده ساختار آنها را اتمهای کربن و هیدروژن تشکیل داده است. بالعکس، در مولکولهای معدنی، سایر اتمها بخش عمده ساختار مولکول را تشکیل میهد.
مولکول آلی چیست؟
مولکولهای آلی مولکولهایی هستند که بخش عمده ساختار آنها را مولکولهای کربن و هیدروژن تشکیل داده باشند. در واقع مولکولهای آأی باید دارای پیوند کربن هیدروژن باشند. برای مثال مولکولهای هیدروکربن از نوع مولکولهای آلی هستند. بسیاری از مواد و مولکولهای زیستی، مواد سوختی، پلاستیکها و ... از مولکولهای آلی تشکیل شدهاند.
مولکولهای آلی زیستی
مولکولهای آلی زیستی مولکولهایی هستند که در موجودات زنده یافت میشوند. از این مولکولها میتوان به کربوهیدراتها، لیپیدها، پروتئینها و اسید نوکلئیکها اشاره کرد. پیشنهاد میکنیم برای آشنایی بیشتر با انواع مولکول ها در زیست شناسی، فیلم آموزش مولکول زیستی چیست فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
کربوهیدرات ها
کربوهیدراتها اولین گروه از مولکولهای آلی هستند و بیشتر برای تامین و ذخیره انرژی در بدن استفاده میشوند. سادهترین نوع آنها قندهای ساده هستند که میتوانند به هم وصل شوند و زنجیرههای بزرگتر بسازند.
لیپیدها
لیپیدها شامل چربیها و روغنها هستند و ساختار آنها از گلیسرول و اسیدهای چرب تشکیل شده است. آنها میتوانند اشباع یا غیراشباع باشند و به طور کلی در آب حل نمی شوند و نقش مهمی در ذخیره انرژی و ساخت غشای سلولی دارند.
پروتئین ها
پروتئینها زنجیرههایی از آمینو اسیدها هستند که در چند سطح ساختاری تاخورده و شکل سه بعدی پیدا میکنند و در عملکردهای مهم سلولی نقش دارند.
اسیدهای نوکلئیک
اسیدهای نوکلئیک مانند DNA و RNA از واحدهایی به نام بازهای نیتروژنی ساخته شدهاند. DNA اطلاعات ژنتیکی را ذخیره میکند و دستور ساخت پروتئینها را در سلول کنترل میکند.
مولکولهای معدنی
مولکولهای معدنی (غیرآلی) ترکیباتی هستنند که قسمت عمده ساختار آنها را کربن و هیدروژن تشکیل نداده باشد. این ترکیبات پیوند کربن-هیدروژن در ساختار خود ندارند. این مولکولها میتوانند شامل عناصر فلزی یا غیرفلزی باشند. برای مثال، مولکولهایی مانند آب، کربن دی اکسید، بسیاری از کانیها، نمک خوراکی و .... از مولکولهای غیرآلی هستند.
انواع مولکول ها از نظر اندازه
مولکولها میتوانند اندازههای متفاوتی داشته باشند. برخی از مولکولها بسیار ریز و برخی بسیار درشت هستند. برای مثال، مولکولهای زیستی مانند DNA و پروتئین در دسته مولکولهای درشت جای میگیرند. معمولا دستهبندی انواع مولکول ها از نظر اندازه در مولکولهای زیستی و آلی استفاده میشود. بدین ترتیب مولکولها میتوانند کوچک (میکرومولکولها) یا بزرگ (ماکرومولکولها) باشند.
اندازه یک مولکول بر قدرت کلی نیروهای بین مولکولی تاثیر میگذارد. قدرت این نیروها نیز بر ویژگیهای یک مولکول اثرگذار است.
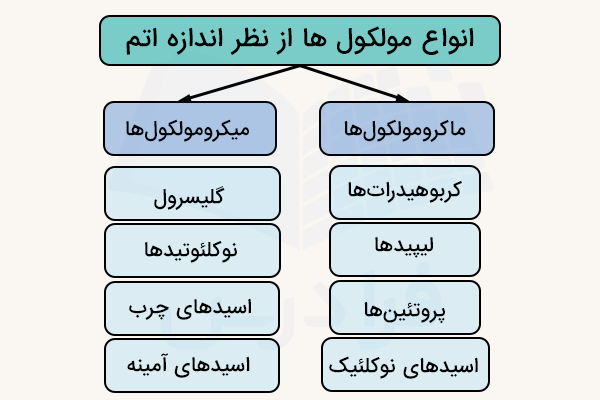
میکرومولکول ها
مولکولهای کوچک دارای نیروهای بین مولکولی ضعیف هستند. این موضوع باعث میشود که نقطه ذوب و جوش پایینی داشته باشند. به همین دلیل، اغلب در دمای اتاق به صورت مایع یا گاز هستند. میکرومولکولها، همان طور که از نامشان پیداست، مولکولهای کوچکی هستند که جرم مولکولی پایینی دارند و به همین دلیل به عنوان مونومر شناخته میشوند. آنها نقش بسیار مهمی در واکنشهای زیستی مختلف ایفا میکنند. در یک واکنش، اتصال مونومرها منجر به تشکیل یک ماکرومولکول یا پلیمر میشود.
گلیسرول، نوکلئوتیدها، اسیدهای آمینه، اسیدهای چرب و مونوساکاریدها از مهمترین میکرومولکولها هستند. آب و مواد معدنی نیز میکرومولکولهای غیرآلی مهمی به شمار میروند. میکرومولکولها میتوانند یا به صورت آزاد مانند آب وجود داشته باشند یا با اتصال به یکدیگر ماکرومولکول تشکیل دهند. در واکنشها، این مولکولها یکی پس از دیگری به هم متصل میشوند.
ماکرومولکول ها
ماکرومولکولها مولکولهای بسیار بزرگی هستند که از پلیمریزه شدن مولکولهای کوچکتر به نام مونومرها تشکیل میشوند. یک مولکول آلی بزرگ مانند کربوهیدراتها، لیپیدها، پروتئینها و اسیدهای نوکلئیک که دارای شکل و عملکرد مشخصی است، ماکرومولکول نامیده میشود. به دلیل اندازه بسیار بزرگ، ماکرومولکولها از بیش از ده هزار اتم یا حتی بیشتر تشکیل شدهاند.
ماکرومولکولها ماهیتی قطبی دارند و سر و انتهای آنها دارای ویژگیهای فیزیکی و شیمیایی متفاوتی است. انواع ماکرومولکولها پروتئینها، اسیدهای نوکلئیک و لیپیدها هستند. مولکولهای بزرگتر با نیروهای بین مولکولی قویتری یکدیگر را جذب میکنند. این موضوع باعث میشود که نسبت به مولکولهای کوچک، نقطه ذوب و جوش بالاتری داشته باشند.
انواع مولکول ها از نظر قطبیت
پیوند بین اتمهای مولکولها نیز یکی از روشهای دستهبندی انواع مولکول به شمار میرود. پیوند بین اتمها در مولکول و قطبیت آن، یکی از مهمترین خواص مولکول است که رفتار آن را در مواردی مانند واکنشهای شیمیایی، پایداری، حلالیت و ... تعیین میکند.
در قسمتهای قبل آموختیم که ترکیباتی که با پیوند یونی به هم متصل شده باشند عموما در دستهبندی انواع مولکول ها قرار نمیگیرند بنابراین انواع مولکول ها بر اساس نوع پیوند بین اتمها را میتوان به دو دسته مولکول کووالانسی قطبی و غیرقطبی دستهبندی کرد.
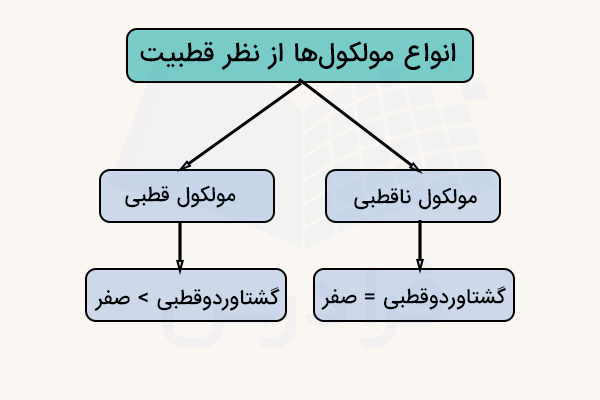
مولکول قطبی
مولکولهای قطبی مولکولهایی هستند که از پیوند کووالانسی قطبی تشکیل شده باشند و هندسه مولکول به شکلی باشد که برایند ممان دوقطبی پیوندهای بین اتمهای آن برابر صفر نباشد. در مولکولهایی که از اتمهای مختلف (ناجورهسته) تشکیل شدهاند، اختلاف الکترونگاتیوی اتمهای دو سر پیوند، باعث میشود که یک ممان دوقطبی لحظهای به وجود آمده و دوسر پیوند، دارای بارهای جزئی مثبت و منفی شوند. بدین ترتیب با بررسی تمامی پیوندها و شکل موکول میتوان قطبی یا ناقطبی بودن آن را تعیین کرد.
مولکول ناقطبی
مولکول ناقطبی مولکولی است که پیوند بین اتمهای آن از نوع قطبی نبوده یا اینکه هندسه مولکول به شکلی باشد که برآیند بردارهای ممان دوقطبی مولکول یکدیگر را خنثی کنند. برای مثال کربن دی اکسید یکی از این موارد است.
بسیاری از مولکولهای آلی بلند زنجیر و مولکولهای درشت از نوع مولکولهای غیر قطبی هستند.
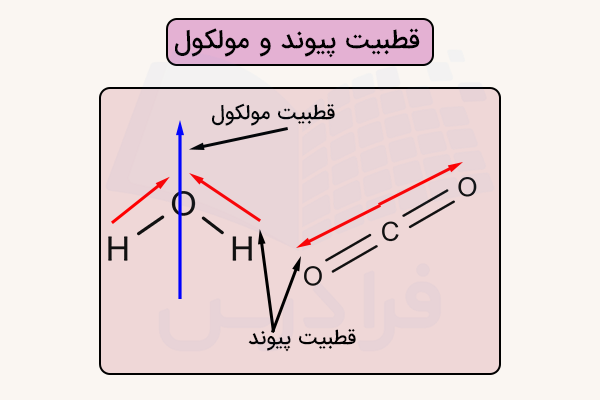
قطبیت مولکول و قطبیت پیوند
قطبیت بین اتمها (قطبیت پیوندها) با استفاده از اختلاف الکترونگاتیوی بین دو اتم به دست میآید. به این صورت که با مقایسه الکترونگاتیوی عناصر دو سر پیوند میتوانیم اختلاف الکترونگاتیوی آن را به دست آوریم. اگر این اختلاف کمتر از ۰٫۴ باشد، پیوند ناقطبی و اگر بزرگتر باشد، قطبی است. نکته مهم این است که اگر اختلاف الکترونگاتیوی بیشتر از ۱٫۷ باشد، آن پیوند یونی بوده و ترکیب حاصل دیگر ترکیبی مولکولی نیست، بلکه یک ترکیب یونی محسوب میشود.
قطبیت مولکولها با بررسی قطبیت تمامی پیوندهای یک واحد مولکول تعیین میشود. اگر بردار ممان دو قطبی پیوندها صفر باشد، مولکول ناقطبی و اگر صفر نباشد، مولکول قطبی خواهد بود. برای درک بهتر و تشخیص نوع مولکولهای مختلف، نیاز است با خواصی مانند هندسه مولکول و نوع پیوندهای بین مولکولی آشنا شویم. در ادامه این موارد را توضیح میدهیم.
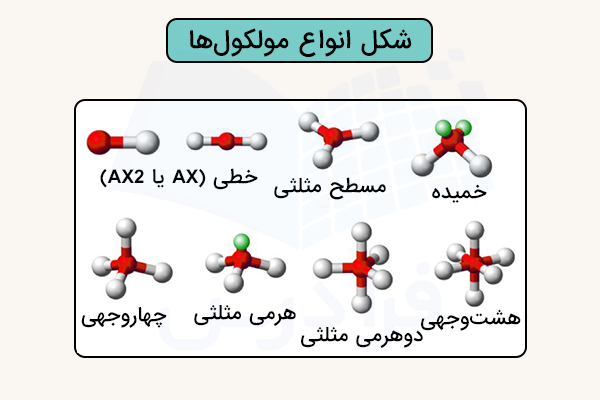
شکل انواع مولکول ها
شکل مولکولها نحوه قرارگیری سهبعدی اتمها در یک مولکول را مشخص میکنند و بر خواص شیمیایی و واکنشهای آن تاثیر میگذارند. شکل هر مولکول به دلیل دافعه بین جفتالکترونهای اطراف اتم مرکزی ایجاد میشود که این موضوع با نظریه دافعه جفتالکترونهای لایه ظرفیت (VSEPR) توضیح داده میشود.
دانستن و بررسی شکل مولکولها به ما این امکان را میدهد که خواص آن مانند پیوندها، هیبریداسیون، قطبیت و برهمکنشهای مولکول با نور را درک کنیم. شکل مولکولی در تعیین نحوه برهمکنش و واکنش آن با سایر مولکولها بسیار مهم است. شکل مولکولی همچنین بر نقطه جوش و ذوب مولکولها تاثیر میگذارد. اگر همه مولکولها خطی بودند، حیات به شکلی که میشناسیم وجود نداشت. بسیاری از ویژگیهای مولکولها ناشی از شکل خاص آنها است. برای مثال، اگر مولکول آب خطی بود، غیرقطبی میشد و در نتیجه ویژگیهای خاص فعلی خود را نداشت. در ادامه انواع شکل مولکول را توضیح میدهیم.
تعیین شکل مولکول
برای پیشبینی شکل یک مولکول کووالانسی، ابتدا باید ساختار لوویس مولکول را رسم کرده و همه الکترونهای ظرفیت اطراف اتم مرکزی را نشان دهیم. سپس، تعداد جفتهای الکترونی اطراف اتم مرکزی و پیوندها را شمرده و با استفاده از این اطلاعات، شکل هندسی مولکول را تعیین کنیم. اتم مرکزی اتمی است که سایر اتمها در اطراف آن قرار گرفتهاند. برای مثال در اتم مرکزی اکسیژن و در اتم مرکزی نیتروژن است.
در جدول زیر، انواع شکل مولکول با توجه به تعداد الکترونهای پیوندی و غیرپیوندی مشخص شده است.
| تعداد پیوند | تعداد جفت الکترون غیر پیوندی اتم مرکزی | شکل مولکول |
| ۱ یا ۲ | صفر | خطی (AX یا AX2) |
| ۲ | ۲ | خمیده (AX2E2) |
| ۳ | صفر | مسطح مثلثی (AX3) |
| ۳ | ۱ | هرمی مثلثی (AX3E) |
| ۴ | صفر | چهاروجهی (AX4) |
| ۵ | صفر | دوهرمی مثلثی (AX5) |
| ۶ | صفر | هشت وجهی (AX6) |
در این نمادگذاری، A اتم مرکزی، X اتمهای اطراف و E جفتهای الکترون ناپیوندی را نشان میدهد.
ساختار رزونانسی انواع مولکول ها
گاهی خواص شیمیایی یک مولکول را نمی توان فقط با یک ساختار ساده توضیح داد. در این شرایط، مولکول را میتوان به چند شکل مختلف رسم کرد که در همه آنها جای اتمها ثابت است، اما محل قرار گرفتن الکترونها و پیوندها تغییر میکند. به این شکلهای مختلف، ساختارهای رزونانسی گفته میشود. ساختار واقعی مولکول در حقیقت هیچ کدام از این شکلها به تنهایی نیست، بلکه ترکیبی از همه آنها است که به آن هیبرید رزونانسی میگویند. این حالت باعث میشود مولکول پایدارتر باشد، چون الکترونها در بخشهای مختلف مولکول پخش میشوند و در یک نقطه متمرکز نیستند.
رزونانس نشان میدهد که الکترونها میتوانند بین چند اتم جابه جا شوند و بعضی پیوندها حالتی بین پیوند یگانه و دوگانه پیدا میکنند. این موضوع نقش مهمی در تعیین پایداری، واکنش پذیری و خواص شیمیایی مولکولها دارد. برای مثال، ترکیبات حلقوی آروماتیک آلی، اغلب ساختاری رزونانسی دارند.
هیبریداسیون انواع مولکول ها
در شیمی، هیبریداسیون فرایندی است که در آن اوربیتالهای خالص اتمی با یکدیگر ترکیب میشوند و اوربیتالهای جدیدی به نام اوربیتالهای هیبریدی را تشکیل میدهند. این اوربیتالهای جدید در تشکیل پیوندهای شیمیایی نقش دارند. برای مثال، اتم کربن در مولکول متان دارای هیبریداسیون sp3 است.
پیوند انواع مولکول ها
پیوند بین انواع مولکول ها یکی از مهمترین مباحث بررسی شده در شیمی است که توضیح میدهد اتمها و مولکولها چگونه در کنار یکدیگر قرار میگیرند. در ادامه انواع پیوندهای مولکولها را بررسی میکنیم.
پیوندهای درون مولکولی
پیوندهای درون مولکولی پیوندهایی هستند که بین اتمهای تشکیلدهنده یک مولکول وجود داشته و آنها در کنار یکدیگر نگه میدارند. در ترکیبات مولکولی، پیوندهای درون مولکولی از نوع کووالانسی قطبی یا غیرقطبی هستند. این نوع پیوند در ترکیبات یونی از نوع پیوند یونی، در ترکیبت فلزی از نوع پیوند فلزی و در ترکیبات کوئوردیناسی از نوع پیوند داتیو است.
پیوند کووالانسی
پیوند کووالانسی از به اشتراک گذاری الکترون بین اتمهای مختلف به وجود میآید. در این نوع پیوند، اتمها با این به اشتراکگذاری، ظرفیت خود را کامل کرده و به آرایش پایدارتری (مانند آرایش اکتت) میرسند. همانطور که در قسمتهای قبل آموختیم، پیوند کووالانسی میتواند از نوع قطبی یا غیر قطبی باشد.
پیوندهای بین مولکولی
پیوندهای بین مولکولی پیوندهایی هستند که مولکولها را در یک ترکیب مولکولی به هم متصل میکنند. برای مثال، ترکیب مولکولی قند ممکن است از هزاران مولکول تشکیل شده باد که این مولکولها با پیوندهای بین مولکولی در کنار یکدیگر قرار گرفتهاند.
پیوندهای بین مولکولی از پیوندهای بین اتمی ضعیفتر بوده و راحتتر میشکنند. این پیوندهای میتوانند از نوع پیوند هیدروژنی یا نیروهای ضعیف واندروالسی باشند.
پیوند هیدروژنی
پیوند هیدروژنی پیوندی بین مولکولی است. این پیوند زمانی شکل میگیرد که اتم هیدروژن متصل به یک اتم الکترونگاتیو مانند اکسیژن یا نیتروژن، درمجاورت یک اتم الکترونگاتیو دیگر قرار بگیرد. این نوع پیوند از پیوند کووالانسی ضعیفتر بوه و عامل به هم پیوستن مولکولهای مختلف در بسیاری از ترکیبات مانند آب و DNA است.
نیروهای واندروالس
نیروهای واندروالس شامل نیروهای جاذبه بین مولکولهای مختلف به دیل وجود دوقطبیهای موقت است. این نوع نیروهای از ضعیفترین نوع نیروهای بین مولکولی بوده و نقش مهمی را در خواص فیزیکی انواع مولکول مانند نقطه ذوب و جوش آنها ایفا میکنند.
اندازه مولکول ها
اندازه مولکولهای مختلف به عواملی مانند تعداد اتمها، نوع اتمها و نحوه ارایش و قرارگیری آنها در مولکول بستگی دارد. مولکولها میتوانند اندازههای مختلف و متفاوتی داشته باشند. برای مثال مولکول آب مولکولی کوچک با سه اتم و پروتئینها مولکولهای بزرگ هستند که میتوانند هزاران اتم داشته باشند.
اندازه مولکولها بر خواص فیزیکی و شیمیایی آنها اثر میگذارد. برای مثال، نقطه ذوب و جوش، حلالیت و فعالیت شیمیایی همگی خواصی هستند که میتوانند به اندازه مولکول وابسته باشند. دانشمندان برای اندازهگیری و بررسی اندازه مولکولهای مختلف از تکنیکهایی منند کریستالوگرافی اشعه ایکس و میکروسکوپهای الکترونی استفاده میکنند.
کوچکترین مولکول شناخته شده مولکول هیدروژن است که از دو اتم هیدروژن تشکیل شده است.
ویژگیهای انواع مولکول ها
انواع مولکول ها به عنوان یکی از کوچکترین واحدهای سازنده ماده، ویژگیهای مشخصی دارند که آنها را از یکدیگر متمایز میکند. از این ویژگیها میتوان به ساختار انواع مولکول، پیوندهای شیمیایی، فرمول ساختاری، وزن مولکولی، خواص فیزیکی و شیمیایی مختلف مانند ایزومری، برهکمنش نوری و فعالیت شیمیایی اشاره کرد.
در ادامه این ویژگیهای انواع مولکولها را بررسی میکنیم.
ساختار مولکول
مولکولها از دو یا چند اتم تشکیل شدهاند که توسط پیوندهای شیمیایی به هم متصل هستند. در قسمتهای قبل آموختیم مولکولها میتوانند از یک یا چند نوع اتم تشکیل شده باشند. در واقع نوع و تعداد اتمهای سازنده مولکول و نحوه اتصال آنها به یکدیگر ساختار مولکول را تشکیل میدهند و ویژگیهای فیزیکی و شیمیایی مختلفی را برای هر مولکول تعیین میکنند.
فرمول ساختاری
فرمول ساختاری یک مولکول نشان میدهد که اتمها در مولکول چگونه به هم متصل شده و با چه ترتیبی در کنارهم قرار گرفتهاند. فرمول ساختاری یکی از مهمترین ابزارها برای درک هندسه مولکول و برهمکنشهای شیمیایی آن است.
وزن مولکولی
وزن مولکولی (یا جرم مولکولی) از جمع جرم تمامی اتمهای موجود در یک مولکول به دست میآید. وزن مولکولی برای انجام بسیاری از محاسبات شیمیایی مانند مسائل استوکیومتری و محاسبات غلظت محلولها پارامتری ضروری است.
سنگین ترین مولکولها معمولا پروتئینهای بزرگ یا پلیمرهای مصنوعی هستند که میتوانند میلیونها واحد جرم اتمی داشته باشند.
خواص فیزیکی و شیمیایی مولکول ها
در این مطلب از مجله فرادرس آموختیم انواع مولکول ها کدامند. هر مولکول، خواص فیزیکی و شیمیایی منحصر به فردی دارد که آن را از سایر مولکولها متمایز میکند. برای مثال، نقطه ذوب و جوش، حلالیت و واکنشپذیری از جمله این خواص مولکولها هستند. این خواص از نوع اتمها و نحوه اتصال و تعداد اتمها در مولکول ناشی میشوند. برای مثال، قطبیت یک مولکول بر میزان حلالیت آن در حلالهای قطبی و غیرقطبی اثر میگذارد.
در ادامه، سه خاصیت ایزومری، برهمکنش با نور و واکنشپذیری مولکول را بررسی میکنیم.
ایزومری
ایزومری پدیدهای است که در آن مولکولهایی با فرمول مولکلی یکسان، ساختار شیمیایی متفاوتی از اتمها را داشته باشند. ایزومرها میتوانند از نوع ساختاری فضایی، نوری و .... باشند. ایزومرها خواص و رفتار شیمیایی متفاوتی دارند که از اتصال متفاوت اتمها در مولکولها ناشی میشود.
برهمکنش با نور
مولکولها میتوانند به شکلهای مختلفی با نور برهم کنش داشته باشند. برای مثال جذب نور، بازتاب نور و فلورسانس از این برهمکنشها هستند. این رفتارها به ساختار و ترکیب مولکول بستگی دارد و اساس بسیاری از روشهای شناسایی مواد در شیمی مانند طیفسنجی است.
واکنش پذیری
واکنشپذیری یک مولکول به ترکیب، ساختار و نوع پیوندهای شیمیایی آن بستگی دارد. این ویژگی تعیین میکند که یک مولکول چگونه در واکنشهای شیمیایی شرکت میکند و چه نوع واکنشهایی میتواند انجام دهد.












