غنی سازی ایزوتوپی چیست؟ – به زبان ساده
به فرایندی که طی آن غلظت ایزوتوپی خاص از یک عنصر افزایش پیدا کند غنیسازی میگوییم. بسیاری از عنصرها در طبیعت به صورت مخلوطی از چند ایزوتوپ متفاوت خود حضور دارند اما برای برخی کاربردهای ویژه مثلا در صنایع نظامی و پزشکی نیاز به ایزوتوپی خاص به صورت خالص داریم و این لزوم غنیسازی را برای ما روشن میکند. روشهای گوناگونی برای جدا کردن و غنیسازی ایزوتوپ عنصرها به کار گرفته میشود. در این مطلب میخواهیم بدانیم غنی سازی ایزوتوپی چیست و سپس به روشهای انجام آن بهخصوص در مورد عنصر اورانیوم خواهیم پرداخت.
- یاد میگیرید ایزوتوپ چیست و اهمیت تفاوت عدد جرمی را درک میکنید.
- میآموزید چگونه ایزوتوپها برای مصارف صنعتی، پزشکی و هستهای غنیسازی میشوند.
- با روشهای عمده جداسازی ایزوتوپها و عملکرد هرکدام آشنا میشوید.
- خواهید آموخت مزایا و چالشهای سانتریفیوژ گازی، انتشار گازی و غنیسازی لیزری را مقایسه کنید.
- یاد میگیرید غنیسازی اورانیوم چه نقشی در صنایع هستهای دارد.
- خطرات زیستی اورانیوم غنیشده و اهمیت رعایت نکات ایمنی را فرا میگیرید.


غنی سازی ایزوتوپی چیست ؟
غنیسازی ایزوتوپی به مجموعه فعالیتهایی گفته میشود که طی آنها غلظت یک ایزوتوپ خاص در مخلوطی از ایزوتوپها افزایش مییابد و در نتیجه غلظت باقی ایزوتوپها کم میشود. در حالی که ایزوتوپهای برخی عنصرها را میتوان جداسازی کرد، عنصرهایی نیز وجود دارند که ایزوتوپهای آنها به دلیل داشتن ویژگیهای شیمیایی بسیار مشابه که پایه و اساس روشهای جداسازی هستند، قابلیت غنیسازی ندارند. در این مورد ایزوتوپ دوتریم () عنصر هیدروژن استثنا است.
ایزوتوپ چیست ؟
برای فهم بهتر مطلب و درک اینکه غنی سازی ایزوتوپی چیست، در این قسمت میخواهیم تعریفی دقیق از چیستی ایزوتوپ ارائه دهیم. ایزوتوپهای یک عنصر اتمهایی با تعداد پروتون برابر (عدد اتمی) در هسته اتم خود هستند، به همین دلیل در یک خانه از جدول تناوبی عناصر گنجانده میشوند. تفاوت آنها در تعداد نوترونهای هسته اتم (عدد جرمی) است. ایزوتوپها در بیشتر ویژگیهای شیمیایی با یکدیگر برابر هستند اما جرم اتمی و ویژگیهای فیزیکی متفاوتی دارند. بنابراین با داشتن عدد اتمی متوجه میشویم که مربوط به چه عنصری است اما در مورد اینکه کدام ایزوتوپ آن عنصر هست نمیتوانیم حدسی بزنیم و نیاز به دانستن عدد جرمی آن داریم. ایزوتوپها به دو حالت ایزوتوپ پایدار و ایزوتوپ ناپایدار وجود دارند.
مثلا کربن عنصری با عدد اتمی ۱۲ است یعنی در هسته خود ۶ عدد پرتون و ۶ عدد نوترون دارد اما ایزوتوپی از کربن وجود دارد که ۷ عدد نوترون دارد. توجه داشته باشید که این یعنی عدد جرمی آن به جای ۱۲، ۱۳ است. در تصویر زیر ایزوتوپهای متفاوت عنصر کربن را مشاهده میکنید. پس با دانستن عدد اتمی نمیتوان پیبرد که در مورد کدام ایزوتوپ کربن صحبت میکنیم زیرا هر دو برابر با ۱۲ هستند اما با در دست داشتن عدد جرمی این دو قابل تشخیص از هم هستند.
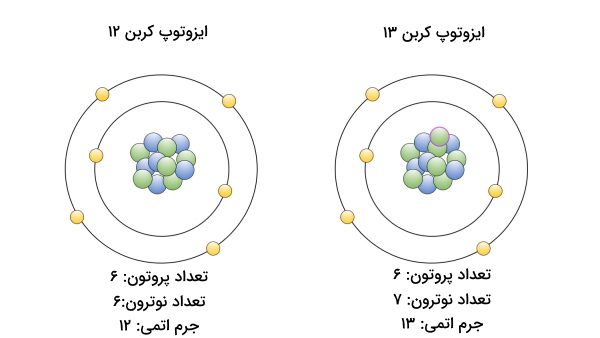
کاربرد ایزوتوپ های غنی شده
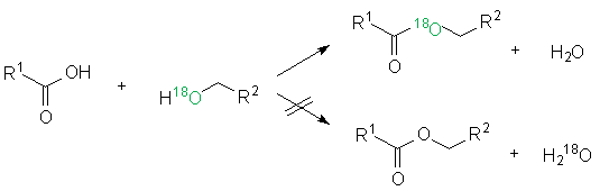
از ایزوتوپهای خالص در موارد متنوعی استفاده میشود. یکی از این کاربردها در مطالعات علمی است به صورتی از از اتم ایزوتوپ عنصری خاص برای برچسب زدن (Labeling) به مولکول استفاده میشود و سپس با وارد کردن آن مولکول در واکنش شیمیایی روند پیشرفت و مسیر آن را مورد مطالعه و پیگیری قرار میدهند. از پلوتونیوم غنی شده در این راکتورهای هستهای برای ساخت سلاحهای هستهای استفاده میشود. خروجی این راکتور باید به صورتی باشد که پلوتونیوم ترکیب مطلوبی از ایزوتوپها را از نظر غلظت و در نتیجه کارایی داشته باشند.
کاربرد اورانیوم غنی شده
پرکاربردترین عنصری که توسط غنیسازی ایزوتوپی به غلظت موردنظر میرسد اورانیوم است. اورانیوم سالانه در تناژ بسیار بالایی تولید و مصرف میشود. از این ماده در نیروگاههای هستهای به عنوان سوخت استفاده میشود. همچنین این ماده نقش بسیار مهمی را در تولید سلاحهای هستهای ایفا میکند.

روش های غنی سازی
برای جدا کردن ایزوتوپی خاص از یک عنصر از ایزوتوپهای دیگر، روشهای بسیاری در نظر گرفته شده است. این روشهای گاهی با یکدیگر تفاوتهای زیادی دارند و گاهی مبنای جداسازی ایزوتوپهای از یکدیگر تفاوت جزئی در ویژگیهای فیزیکی و شیمیایی آنها است. در حالت کلی از سه روش برای جداسازی ایزوتوپها از یکدیگر استفاده میشود که شامل موارد زیر هستند.
- روشهایی که بر مبنای تفاوت ایزوتوپهای یک عنصر در تعداد نوترونها (جرم اتمی) انجام میشوند.
- روشهایی که مبنای خود را تفاوت جزئی سرعت انجام واکنشهای شیمیایی توسط عنصرها میگذارند.
- روشهایی که به ویژگیهای که مرتبط با جرم اتمی ایزوتوپ نیستند، مانند مبنا قرار دادن رزونانس هستهای آنها، تکیه دارند.
روش سوم همچنان نوپا است و دانشمندان در حال گسترش آن هستند. باید این نکته را ذکر کنیم که تمام این روشها به نحوی به تفاوت در عدد جرمی بستگی دارند. بنابراین هرچه دو ایزوتوپهای یک عنصر تفاوت عدد جرمی بیشتر باشد غنیسازی راحتتر و بهتر خواهد بود.
به مثال زیر توجه کنید:
جداسازی ایزوتوپ دوتریم از آنجا که جرمی دو برابر هیدروژن معمولی دارد بسیار سادهتر از جداسازی اورانیوم-۲۳۵ از اورانیوم-۲۳۸ است. یکی از نامطلوبترین شرایط غنیسازی مربوط به عنصر پلوتونیوم است. جداسازی پلوتونیوم-۲۳۹ از پلوتونیوم-۲۴۰ با ۱ واحد تفاوت در عدد جرمی تقریبا ناممکن است.
روش طیف سنجی جرمی
گرچه از این روش بیشتر برای تجزیههای کیفی استفاده میشود اما به دلیل سهولت کار با آن در جداسازی نیز میتواند کاربرد داشته باشد.
طیف سنجی جرمی چیست ؟
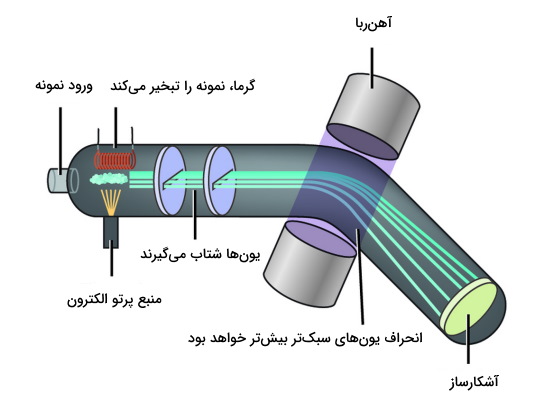
طیف سنجی جرمی (Mass Spectrometry) یکی از انواع طیف سنجی در شیمی تجزیه است که در آن نسبت جرم به بار الکتریکی یونها اندازهگیری میشود. نتایج این روش را با نموداری به نام طیف جرمی نشان میدهند. از این روش در زمینههای گوناگونی استفاده میشود و هم برای مواد خالص هم مخلوطی از مواد، نتایج خوبی به دست میدهد.
با استفاده از این روش میتوان ساختار یک ماده شیمیایی را حدس زد. از ویژگیهای بسیار مفید این روش امکان داشتن ماده به هر سه حالت فیزیکی جامد، مایع و گاز است که همه در نهایت برای پیشبرد مسیر باید تبدیل به یون شوند.

طیف سنجی جرمی در غنی سازی
اولین بمب اتمی که در آن از اورانیوم-۲۳۵ استفاده شد، به کمک طیفسنجی جرمی به دست آمد. البته این روش محدودیتی دارد که باعث میشود تنها زمانی که نیاز به محصول در حد چند میلیگرم یا چند گرم است، از آن استفاده شود. این محدودیت هزینه بالای انجام طیفسنجی جرمی است.
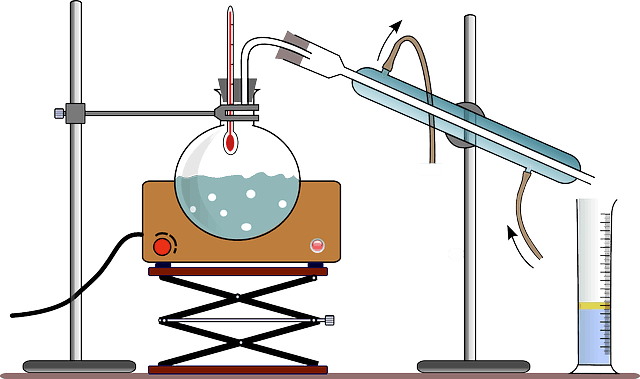
روش تقطیر
همانطور که میتوان از این روش برای افزایش خلوص الکل از ترکیب آب و الکل استفاده کرد، برای غنیسازی ایزوتوپ نیز کاربرد دارد. در این قسمت مثالی از این نوع جداسازی را بررسی میکنیم.
تقطیر چیست ؟
در این قسمت با بررسی مثالی ساده میخواهیم به ماهیت روش تقطیر پی ببریم. در دمای پایین ۲۲۰ درجه سانتیگراد، آب سبک که شامل هیدروژن است ، نسبت به آب سنگین که شامل دوتریوم است ، مقدار تبخیر بیشتری دارد. تقطیر آب معمولی که شامل هر دو مولکول آب سبک و سنگین است، بخاری به دست میدهد که بیشتر شامل آب سبک است. بنابراین در مایعی که باقی میماند میزان آب سنگین بیشتر خواهد بود.
تقطیر در غنی سازی
با توجه به مثال قسمت قبل میتوانیم بگوییم که معمولا و نه لزوما همیشه، آن ایزوتوپی که سبکتر است زودتر تبدیل به بخار میشود. در ادامه مثال دیگری را در این مورد بررسی میکنیم. مولکول کربن دیاکسید را در نظر بگیرید. این مولکول میتواند شامل کربنهایی با تعداد متفاوت نوترون باشد.
از روش تقطیر برای جداسازی مولکولهای کربن دیاکسید با ایزوتوپهای متفاوت کربن استفاده میشود. تقطیر کربن دیاکسید مایع در لولههای طویل باعث میشود باقیمانده مایع، بیشتر حاوی کربن-۱۳ که ایزوتوپ سنگینتر به حساب میآید، باشد. ترکیبات کربندار غنی از کربن-۱۳ در آزمایشهای پزشکی برای تشخیص زخم معده ناشی از هلیکوباکتر پیلوری استفاده میشوند.
روش های شیمیایی
گرچه ویژگیهای شیمیایی ایزوتوپهای یک عنصر را عموما یکسان در نظر میگیریم اما در این مورد استثناهایی نیز وجود دارد. در ادامه به بررسی روشهای شیمیایی که میتوان از آنها برای جداسازی ایزتوپهای عنصرها استفاده کرد میپردازیم.
سرعت واکنش شیمیایی
سرعت واکنشهای شیمیایی به جرم اتمی بستگی دارد. از این روش بیشتر برای ایزوتوپها عنصرهای سبک مانند هیدروژن استفاده میشود. ایزوتوپها سبکتر سریعتر وارد واکنش میشوند و همچین زمان کمتری برای تبخیر نیاز دارند. این ویژگیها به آنها امکان جداسازی میدهد. از این روش برای تولید آب سنگین تجاری استفاده میشود.
در ادامه سرعت اکسیداسیون آنیون فرمات تریتیله شده و تبدیل آن به را بررسی خواهیم کرد.
روش واکنش تبادلی
تفاوتهای جزئی در عملکرد ایزوتوپها نسبت به یکدیگر میتواند مبنایی برای جداسازی باشد. مثالی از این مورد تهیه نیتروژن غنی از با کمک روشهای تعویض یون است.
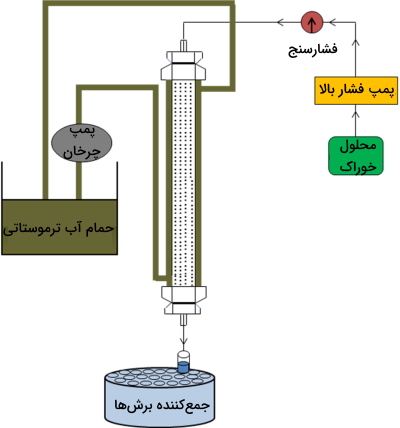
در این روش آمونیاک محلول به رزینهای تبادل یون متصل میشود. به این صورت که ابتدا آمونیاک را در ستونی از رزین سررریز میکنند تا در بالای ستون تجمعی از آن به وجود بیاید. سپس با اضافه کردن سدیم هیدروکسید تجمع آمونیاک به انتهای ستون رانده میشود. در این مرحله رزین با شدت نیروی بیشتری اتمهای آمونیاک را نسبت به به خود جذب میکند و نگه میدارد. در نتیجه در بالای ستون آمونیاک به فرم و در پایین به فرم است سپس با شستشوی برشهای مختلف ستون جداسازی انجام میشود.
روش انتشار گازی
گازها به دلیل ماهیت خود میتوانند از کوچکترین حفره مواد هم عبور کنند و بعد از برخورد به دیواره منتشر شوند. میانگین زمانی که هر مولکول گاز برای عبور از این روزنه نیاز دارد بستگی به سرعت و برخی ویژگیهای دیگر آن دارد. با توجه به نظریه جنبشی گازها در دمایی مشخص هرچه مولکولی سبکتر باشد با سرعت بیشتری مسیر را طی خواهد کرد. این نظریه به قانون پخش گراهام مشهور است و در قسمت بعدی بررسی خواهد شد. به علاوه همیشه حرکت گاز از محفظهای با فشار بیشتر به محفظهای با فشار کمتر خواهد بود.
قانون پخش گراهام
شیمیدان اسکاتلندی، توماس گراهام در مطالعات خود به نتیجه جالبی رسید. او متوجه شد که سرعت انتشار گاز از حفرهای در مانع پیش رو نسبت عکس با ریشه توان ۲ جرم آن دارد. در معادله زیر مقدار گاز و با یکدیگر برابر است. سرعت انتشار آنها را میتوان به صورت زیر نشان داد. در این معادله منظور از rate سرعت انتشار گاز و منظور از molar lass جرم مولی هر مولکول گازی است.
انتشار گاز در غنی سازی
در قسمت قبل در مورد تفاوت سرعت مولکولهای گاز با توجه به اندازه آنها توضیح دادیم. این تفاوت میتواند مبنایی برای جداسازی ایزوتوپها از یکدیگر باشد. این روش برای جداسازی ایزوتوپ شکافتپذیر اورانیوم-۲۳۵ مورد استفاده در راکتورهای هستهای و سلاح هستهای به کار گرفته میشود. اورانیوم موجود در طبیعت تنها شامل ۰٫۷٪ از این ایزوتوپ است و باقیمانده را اورانیوم-۲۳۸ تشکیل میدهد.
روش سانتریفیوژ گازی
زمانی که ترکیبی از چند مولکول گازی با سرعت بالا در محفظهای بسته چرخانده میشوند، سنگینترین مولکول نزدیک به دیوارهها و سبکترین مولکول نزدیکتر به مرکز محفظه تجمع میکنند. این روش اولین بار در سال ۱۹۳۶ توسط فیزیکدان آمریکایی برای جداسازی ایزوتوپهای کلر به کار گرفته شد. امروزه نیز مقادیر متفاوتی از ایزوتوپهای عنصرها از گرم تا کیلوگرم از این روش به دست میآید.
روش های غنی سازی فتوشیمیایی
مبنای این روش تفاوت در فرکانس جذب نور توسط هر ایزوتوپ است. زمانی که اتمی اشعهای را جذب کند و به حالت برانگیختگی برسد، این احتمال وجود دارد که ویژگیهای شیمیایی آن با حالت پایه کاملا متفاوت باشد. همچنین اتم برانگیخته درگیر فرایندهای فیزیکی و شیمیایی میشود که از اتم پایه انتظار نمیرود، مثلا اتم برانگیخته میتواند الکترون خود را از دست بدهد. این نکته، اصل اساسی در استفاده از این روش برای جداسازی ایزوتوپها است. با تابیدن اشعهای خاص به مخلوطی از ایزوتوپهای یک عنصر تنها یکی از آنها برانگیخته میشود و قابل جداسازی خواهد بود.
غنی سازی لیزری
از لیزر برای دو مدل غنیساز استفاده میشود. در اولی ماده اولیه عنصر است و به آن جداسازی ایزوتوپ لیزر بخار اتمی () گفته میشود. در روش دوم که به جداسازی ایزوتوپ لیزر مولکولی () مشهور است، ماده اولیه مولکول حاوی ایزوتوپ موردنظر خواهد بود.
منابع معمول نور برای این روش مناسب نیستند زیرا نوری که میتابانند طیف وسیعی از فرکانسها را دارد و ممکن است تمام ایزوتوپهای یک عنصر را برانگیخته کند که برای جداسازی مطلوب نیست. به همین دلیل از منابع لیزری با فرکانسهای محدودی استفاده میشود. آزمایشگاههای دولتی و خصوصی همزمان در حال گسترش این روش برای جداسازی ایزوتوپهای مورد استفاده در پزشکی و تحقیقات هستند.

غنی سازی آبشاری
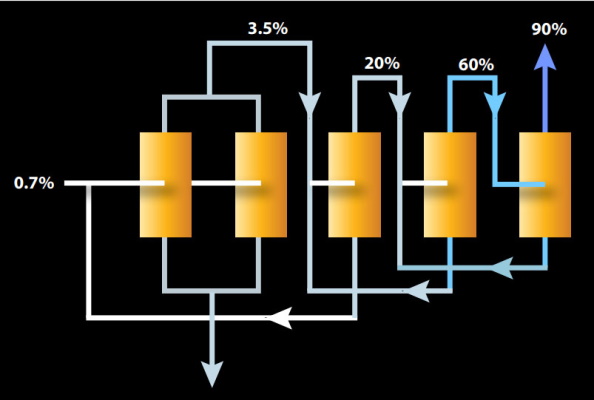
غنیسازی آبشاری روشی مجزا در جداسازی ایزوتوپهای یک عنصر از یکدیگر نیست. تمام روشهایی که پیش از این بررسی کردیم در هر مرحله به مقدار مشخصی کارایی دارند و جداسازی را انجام میدهند اما برای داشتن غنای کافی از یک ایزوتوپ ممکن است نیاز داشته باشیم از این روشها بیش از یکبار استفاده کنیم. به فرایندی که در آن از یک روش به تناوب و دفعات زیاد، در حد صد یا هزار، استفاده میشود، غنیسازی آبشاری میگوییم. این مسئله دلیل نیاز سایتهای غنیسازی به فضایی بسیار بزرگ را توجیه میکند.
در هر مرحله از این فرایند غلظت ایزوتوپ مد نظر اندکی افزایش پیدا میکند. خروجی غنی از ایزوتوپ مد نظر، ورودی مرحله بعد غنیسازی خواهد بود. همچنین ماده اولیه که بعد از هر فرایند حاوی مقدار کمتری از ایزوتوپ مد نظر است دوباره از ابتدا وارد چرخه میشود.
غنی سازی اورانیوم چیست ؟
اورانیوم از پرکاربردترین رادیو ایزوتوپ یا ایزوتوپ ناپایدار مورد استفاده در صنایع است. به همین دلیل غنی سازی آن از اهمیت ویژهای برخوردار است. تا اینجا به بررسی این مطلب پرداختیم که بهطور کلی غنی سازی ایزوتوپی چیست و در قسمتهای پیشرو در مورد روشهای جداسازی عنصر اورانیوم صحبت خواهیم کرد.

غنی سازی اورانیوم به روش طیف سنجی جرمی
مبنای این روش جداسازی الکترومغناطیسی ایزوتوپها است که اینطور بیان میشود:
ذره باردار در عبور از میدان مغناطیسی مشخص مسیری دایرهای را با توجه به جرم خود طی میکند. بنابراین اورانیوم--۲۳۵ و اورانیوم-۲۳۸ کمی در مسیر از یکدیگر انحراف خواهند داشت. شعاعی که اورانیوم-۲۳۸ طی میکند کمی از شعاع اورانیوم-۲۳۵ بزرگتر است که این امکان جداسازی این دو ایزوتوپ را میدهد و غنیسازی اورانیوم انجام میشود. منبع اورانیوم مورد استفاده در این روش، جامد اورانیوم تتراکلرید () است.
غنی سازی اورانیوم به روش انتشار گازی
از آنجایی که بیشتر اورانیوم موجود در طبیعت از نوع ایزوتوپ اورانیوم-۲۳۸ است نیاز به غنیسازی آن برای داشتن اورانیوم-۲۳۵ داریم. در فرایند جداسازی اورانیوم طبیعی به فرم هگزافلوریدی () محافظی متخلخل در بین دو محفظه عبور داده میشود. مولکول حاوی اورانیوم-۲۳۸ سنگینتر از مولکول حاوی اورانیوم-۲۳۵ است و در نتیجه کندتر حرکت میکند. بنابراین انتقال مولکول حاوی اورانیوم-۲۳۵ سریعتر وارد محفظه دوم میشوند.
در هر مرحله از این فرایند غلظت مولکول حاوی اورانیوم-۲۳۵ در محفظه دوم بیشتر از قبل میشود اما چون این روند افزایشی کند است نیاز به تکرار چندباره آن برای دستیابی به غلظت موردنظر است.
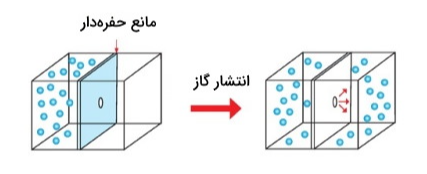
مانع متخلخل در این روش از اهمیت بسیار زیادی برخوردار است. این مانع باید دارای حفرههای هم اندازهای در حدود یک میلیونم اینچ باشد. به علاوه جنس آن باید طوری انتخاب شود که با گاز بسیار خورنده اورانیوم هگزافلورید وارد واکنش نشود. در نهایت معلوم شد که استفاده از نیکل و آلومینیوم اکسید بهترین نتیجه را رقم میزند.
باید توجه داشت که محیط انجام این فرایند باید کاملا عایق باشد به طوری که هوایی به آن وارد نشود. همچنین اورانیوم هگزافلورید نباید نشتی داشته باشد.
قانون پخش گراهام در غنی سازی اورانیوم
گفتیم که طبق این قانون سرعت انتشار هر گاز با جرم آن رابطه عکس دارد. میخواهیم معادله این قانون را برای غنیسازی اورانیوم از ماده اولیه اورانیوم هگزافلورید بنویسیم. از آنجا که فلوئور تنها یک ایزوتوپ متدوال با عدد جرمی ۱۹ دارد برای محاسبه جرم ماده اولیه میتوانیم به طریق زیر عمل کنیم.
جرم اورانیوم هگزافلورید حاوی اورانیوم-۲۳۵:
جرم اورانیوم هگزافلورید حاوی اورانیوم-۲۳۸:
سپس این اعداد را در معادله قانون پخش گراهام جاگذاری میکنیم.
همانطور که میبینید تفاوت سرعت این دو ایزوتوپ با یکدیگر بسیار ناچیز است، بنابراین این فرایند باید بارها و بارها انجام شود تا بتوان به ایزوتوپ اورانیوم-۲۳۵ غنی شده رسید. به همین دلیل مراکز غنیسازی اورانیوم نیاز به خط تولید بسیار طولانی دارند.

غنی سازی اورانیوم به روش سانتریفیوژ گازی
از روش سانتزیفیوژ گازی نیز برای جداسازی ایزوتوپهای اورانیوم استفاده میشود که باعث صرفهجویی زیادی در مصرف انرژی شده است. امروزه چیزی حدود ۵٪ از اورانیوم غنی شده مورد نیاز از این روش به دست میآید. در این روش اورانیوم هگزافلورید شامل اتم اورانیوم-۲۳۸ به دلیل وزن بیشتر نزدیکتر به دیوارههای محفظه و اورانیوم هگزافلورید شامل اتم اورانیوم-۲۳۵ نزدیکتر به مرکز محفظه تجمع میکنند و قابل جداسازی هستند.
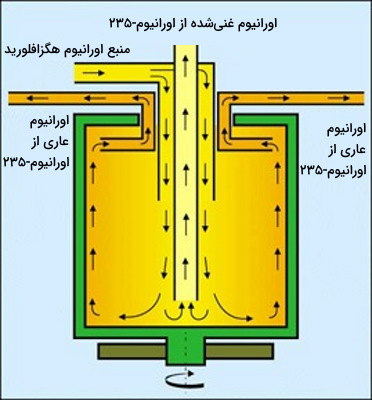
تفاوت انتشار گازی و سانتریفیوژ گازی
مقدار غنیسازی حاصل از یک سانتریفیوژ گازی بسیار بیشتر از مقدار به دست آمده از روش انتشار گازی است با این حال این روش را نیز باید به دفعات تکرار کرد تا مقدار اورانیوم غنی شده قابل ملاحظه باشد. به سانتریفیوژهای گازی که در یک سری متصل به هم قرار میگیرند اصطلاحا سانتریفیوژ آبشار گازی میگوییم. به این روش در هر مرحله خلوص ایزوتوپ اورانیوم-۲۳۵ موردنظر اندکی افزایش پیدا میکند. خروجی هر سانتریفیوژ که شامل مقدار کمتری از اورانیوم-۲۳۵ است دوباره از ابتدا برای غنیسازی وارد چرخه میشود. آبشارهای سانتریفیوژ گازی به صدها و گاهی هزاران عدد سانتریفیوژ متوالی میرسند.

غنی سازی اورانیوم به روش فتوشیمیایی
استفاده از روشهایی غنیسازی اورانیومی که در آنها با کمک لیزر اتم ایزوتوپ خاص برانگیخته میشود در سالهای پایانی قرن بیستم با استقبال بسیاری مواجه شده است. طرفداران استفاده از این روش دو دلیل برتری این روش به نسبت روشهای دیگر مانند انتشار گازی بیان میکنند.
- مصرف انرژی کمتر
- دورریز ماده اولیه کمتر
غنی سازی اورانیوم به کمک لیزر
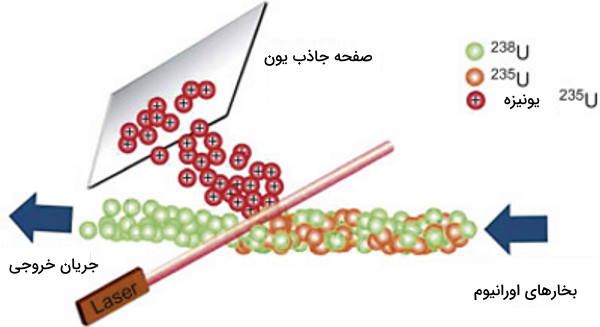
در کشورهایی که دولتها در برنامه غنیسازی اورانیوم سرمایهگذاری میکنند از اورانیوم فلزی به عنوان ماده اولیه استفاده میشود. این اورانیوم فلزی در اثر گرم شدن در کوره، تبخیر شده و تبدیل به پرتوهایی از اتم شده و از حفرهای کوچک میگریزند. سپس منابعی بسیار قوی از لیزر با فرکانس مشخص به صورتی به آن تابانده میشوند که تنها اورانیوم-۲۳۵ الکترون از دست بدهد. اتمهای اورانیوم یونیزه شده در این مرحله به صفحهای باردار میچسبند. به نظر میآید که با گسترش و پیشرفت این روش بتوان از آن به عنوان منبعی برای تولید سوخت هستهای استفاده کرد.
تاثیر اورانیوم غنی شده بر بدن
هر ذره رادیواکتیو یک یا چند پرتوی خاص را از خود ساطع میکند و تاثیر آن بر بدن به قدرت نفوذ و قدرت یونیزاسیون آن تابش بستگی دارد. پس برای بررسی احتمال خطر اورانیوم بر بدن ابتدا باید بدانیم تابش ساطعشده از این اتم از چه نوعی است.
اتم اورانیوم رادیو اکتیو از خود تابش آلفا را ساطع میکند. از آنجا که قدرت یونیزاسیون آلفا بسیار زیاد و قدرت نفوذ آن بسیار کم است مواجهه با آن برای بدن خطرناک نیست زیرا این پرتو در برخورد با پوست بدن انسان به دلیل قدرت نفوذ پایین خود از حرکت باز میماند. اما اگر اورانیوم به هر طریقی وارد بدن انسان شود از آنجا که مانعی برای جلوگیری از نفوذ آن وجود ندارد بسیار خطرناک است و میتواند باعث ایجاد سرطان کبد و استخوان شود.

روش جایگزین غنی سازی
تنها روشی که میتوان از آن به عنوان جایگزینی بر روشهای پردردسر و زمانبر غنیسازی در نظر گرفت، تولید ایزوتوپ مد نظر به فرم خالص آن است. این کار را میتوان با ایجاد تابش روی منابعی خاص از آن عنصر به انجام رساند اما در تمامی مراحل باید پیشرفت مسیر کنترل شود تا فقط همان ایزوتوپ مدنظر به وجود بیاید و ناخالصی نداشته باشد.
این روش برای داشتن ایزوتوپ پلوتونیوم-۲۳۹ کاربرد دارد زیرا همانطور که پیشتر بررسی کردیم امکان جداسازی آن از ایزوتوپهای دیگر، پلوتونیوم-۲۴۰ و پلوتونیوم-۲۴۱، به دلیل نزدیک بسیار زیاد جرم اتمی آنها وجود ندارد.

پیشرفت غنی سازی در جهان
امروزه بسیاری از کشورهای جهان به تکنولوژی غنیسازی دسترسی دارند اما ذکر این نکته خالی از لطف نیست که بیشتر تلاشها و مطالعات بر روی جداسازی ۳ ایزوتوپ متمرکز بوده است. یعنی تنها این موارد هستند که در مقدار بسیار بالا جداسازی میشوند. در زیر به این ۳ مورد اشاره میکنیم.
- اورانیوم: این عنصر بیشتر از همه در معرض توجه قرار گرفته است و از آن به عنوان سوخت راکتور هستهای و در تهیه سلاح هستهای استفاده میشود.
- هیدروژن: این عنصرر ۳ ایزوتوپ متفاوت دارد. از ایزوتوپ غنی شده آن به عنوان ماده ناظر در راکتورهای هستهای استفاده میشود. از آنجا که وجود ایزوتوپ تریتیوم در آب مورد استفاده در راکتورها ایجاد مزاحمت میکند در این مورد استفاده، آن را جدا میکنند.
- لیتیم: ایزوتوپ غنی شده آن در تولید سلاح گرماهستهای کاربرد دارد. در واقع تیرتیوم حاصل از این لیتیم با ایجاد انفجار و شکافت هستهای هدف این سلاح را به سرانجام میرساند.

برخی ایزوتوپهای دیگر نیز وجود دارند که در مقیاس بسیار کوچکتر غنی میشوند و کاربرد دارند. مثلا از کربن غنی شده برای افزایش هدایت گرمایی الماس استفاده میشود.
سوال های متدوال
در این قسمت به بررسی چند موردی میپردازیم که باید در مورد غنیسازی ایزوتوپها بدانیم.
از چه روشی برای پی بردن به درصد هر ایزوتوپ در نمونه استفاده می شود؟
برای اینکه بدانیم در نمونه از هر ایزوتوپ چه مقداری حضور دارد از طیفسنجی جرمی استفاده میکنیم. در این روش ذرات بر اساس جرمی که دارند از یکدیگر قابل تشخیص هستند بنابراین در مورد ایزوتوپها که در تعداد نوترون و در نتیجه جرم اتمی با یکدیگر اختلاف دارند، کارکرد دارد.
آیا ایزوتوپ ها ویژگیهای شیمیایی یکسانی دارند ؟
از آنجا که ایزوتوپهای مختلف یک عنصر تعداد الکترون و در نتیجه آرایش الکترونی مشابهی دارند میتوان گفت که در ویژگیهای شیمیایی با هم برابر هستند. اما باید به این نکته توجه داشت که تفاوت آنها در تعداد نوترون که منجر به تفاوت در عدد جرمی میشود روی برخی ویژگیهای شیمیایی آنها تاثیرگذار است. در واقع همین تفاوتهای مبنای چند روش جداسازی نیز هستند.
چرا ایزوتوپ ها از نظر بار الکتریکی خنثی هستند ؟
ایزوتوپها تنها در تعداد نوترون با یکدیگر تفاوت دارند و میدانیم که نوترون ذرهای بدون بار است. پس تفاوت در تعداد نوترون باعث افزایش یا کاهش بار الکتریکی اتمها نمیشود.
کارامدترین روش غنی سازی اورانیوم کدام است ؟
روش سانتریفیوژ گازی که به صورت آبشاری به کار گرفته میشود بهترین روش برای جداسازی اورانیوم-۲۳۵ از اورانیوم-۲۳۸ است.
اورانیوم غنی شده چه مدتی باقی میماند؟
نیمهعمر اورانیوم بسیار طولانی و درم نتیجه واپاشی پرتوزای بسیار آهستهای ار. نیمهعمر اتم اورانیوم-۲۳۸، ۴٫۵ میلیارد سال و نیمهعمر اورانیوم-۲۳۵ ۷۰۰ میلون سال است. بنابراین برای مدتی بسیار طولانی سالم و دستنخورده باقی میماند.
جمع بندی
هدف در این مطلب این بود که بدانیم غنی سازی ایزوتوپی چیست و چه کاربردهایی دارد. غنیسازی به فرایندی گفته میشود که طی آن ایزوتوپهای مختلف یک عنصر از یکدیگر جدا میشوند زیرا این ایزوتوپهای مختلف کاربردهای متفاوتی نیز دارند. مبنای این جداسازی تفاوتهایی است که ایزوتوپهای یک عنصر در شرایط خاص از آن برخوردارند. برای این منظور از روشهای متفاوتی استفاده میشود که سانتریفیوژ گازی و انتشار گاز مثالهایی از آن هستند. این روشهای جداسازی بهخصوص برای غنیسازی اورانیوم مورد استفاده قرار میگیرد.








بسیار عالی
مثلا برای تبدیل اوارنیوم به ۲۳۵ از همون ایزوتوم های خودش استفاده میکنه یا ایزوتوپ های عنصرهای دیگه؟
لطفا سریع جواب بدیددد.