سیستم کمپلمان چیست؟ – به زبان ساده + اجزا و مکانیسم ایمنی
سیستم ایمنی انسان از مجموعه سلولها، پروتئینها و مولکولهای شیمیایی تشکیل شده است که از ورود میکروبهای بیماریزا به بدن و تکثیر آنها جلوگیری میکند. مکانیسمهای این سیستم بر اساس شناسایی انواع آنتیژن فعال میشود. پاسخ ایمنی ایجاد شده فقط یک آنتیژن خاص را از بین میبرد یا در حضور هر عامل خارجی فعال میشود. سیستم کمپلمان بخشی از دستگاه ایمنی انسان است که با همکاری سلولهای ایمنی ذاتی و اکتسابی پاتوژنها را از بین میبرد. در این مطلب از مجله فرادرس اجزای سیستم کمپلکان را به همراه مکانیسمهای ایمنی آن توضیح میدهیم.
- یاد میگیرید که سیستم کمپلمان چگونه کارکرد ایمنی بدن را تقویت میکند.
- خواهید آموخت کدام پروتئینها و گیرندهها اجزای اصلی کمپلمان را میسازند.
- میآموزید مسیرهای کلاسیک، لکتین و جایگزین چگونه کمپلمان را فعال میکنند.
- نقش کمپلکس حمله به غشا و فرآیند اوپسونیزاسیون را یاد میگیرید.
- با مهمترین پیامدهای نقص کمپلمان و روشهای تشخیص آن آشنا میشوید.
- اهمیت تنظیم دقیق کمپلمان برای پیشگیری از آسیب به سلولهای خودی را میآموزید.
سیستم کمپلمکان چیست ؟
سیستم کمپلمان بخشی از سیستم ایمنی بدن است که به ایمنی ذاتی و اکتسابی در حذف میکروبهای بیماریزا کمک میکند. پروتئینهای این سیستم با آنتیژنهای غشایی، آنتیژنهای محلول و گیرندههای سلولهای ایمنی برهمکنش میدهند و با افزایش پاسخ ایمنی اختصاصی یا مستقل پاتوژن را از بین میبرد.
اجزای سیستم کمپلکان
سیستم کمپلمان مجموعهای از پروتئینهای دفاعی، پروتئینهای تنظیمی و گیرنده غشایی سلولهای ایمنی است. بخش دفاعی این سیستم از ۱۲ پروتئین کوچک (پروتئینهای C1-C9، فاکتور B، فاکتور D و فاکتور P) تشکیل شده است که در کبد سنتز شده و به شکل غیرفعال وارد جریان خون میشوند. پروتئین C1 از سه زیرواحد Cq، Cr و Cs تشکیل شده است. زیرواحد Cr و Cs این پروتئین سرین پروتئازهایی هستند که پروتئینهای دیگر سیستم کمپلکمان را فعال میکنند.
زیرواحد Cq از ۱۸ زنجیره پلیپپتیدی تشکیل شده است که ۶ هلیکس ساختار C1 را تشکیل میدهند. سر این هلیکس ها دومین اتصالی به کمپلکس آنتیژن-آنتیبادی است. پروتئینهای C4 و C8 از سه، پروتئینهای C3 و C5 از یک و پروتئینهای C2، C6، C7 و C9 از یک زنجیره پلیپپتدی تشکیل شده است. فاکتورهای F و D پروتئینهای آنزیمی و تکزنجیرهای سیستم کمپلمان هستند.
گیرنده های سیستم کمپلمان
گیرندههای سیستم کمپلمان پروتئینهای عرض غشایی سلولهای ایمنی هستند. CR1 یا CD35 یکی از گیرندههای فاگوسیتها است که به کمپلکس C3-آنتیژن سطحی متصل میشود. گیرنده CR2 یا CD21 به C3dg متصل شده و فعال شدن مسیر جایگزین را کنترل میکند.
گیرنده CR3 و CR4 اینتگرینهای غشایی هستند. اتصال C3b به CR3 غشای نوتروفیل آزاد شدن رادیکالهای آزاد و گرانولهای آنزیمی را تحریک میکند. اتصال این پروتئین به CR4 به گیرنده گلبولهای سفید، فاگوسیت و مهاجرت لوکوسیتها از مویرگ را تحریک میکند. گیرنده C3aR و C5aR پروتئینهای عرض غشایی لوکوسیتها و لنفوسیتهای T عملکننده هستند. اتصال C3a به C3aR و C5a به C5aR، پروتئین G همراه گیرنده و این پروتئین آنزیم فسفولیپاز C را فعال میکند. در نتیجه آبشار واکنشهای فسفوریلاسیون در سلول ایمنی و افزایش غلظت یون کلسیم، کموتاکسی، آزاد شدن گرانولهای آنزیمی و پاسخ التهابی تحریک میشود.
cC1qR و C1qRp سه گیرنده C1q هستند که کموتاکسی لوکوسیتها، فاگوسیتوز، مهاجرت لوکوسیت از خون و تجمع پلاکتها را تحریک میکنند. gC1qR گیرنده Cq در غشای سلولهای B است که در فعال شدن این سلولها نقش دارد.
مکانیسم ایمنی سیستم کمپلمان
پروتئینهای سیستم کمپلمان از سه مسیر کلاسیک، جایگزین و لکتین به پروتئینهای سطحی پاتوژنها متصل میشوند. این مسیرها با روشهای متفاوتی فعال میشوند اما در نهایت با افزایش التهاب، فعالسازی فاگوسیتها پاتوژنها را از بین میبرند.
مسیر کلاسیک
مسیر کلاسیک سیستم کمپلمان با اتصال پروتئینهای C1 به آنتیبادیهای محلول یا کمپلکس آنتیبادی-آنتیژن سطحی (ویروسی، انگلی، باکتریایی و قارچی) شروع میشود. اتصال آنتیبادی (IgGو IgM) به آنتیژن با تغییر کنفورماسیون آنتیبادی و آزاد شدن جایگاه Fc همراه است.برای فعال شدن مسیر کلاسیک حداقل ۳ مولکول C1 باید به جایگاه ثابت (Fc) آنتیبادی پنتامر M متصل شود. مولکول C1 به مونومرها و هگزامرهای IgG متصل میشود. اما تمایل اتصال پروتئین-آنتیبادی به هگزامرهای آنتیبادی بیشتر از مونومرها است.
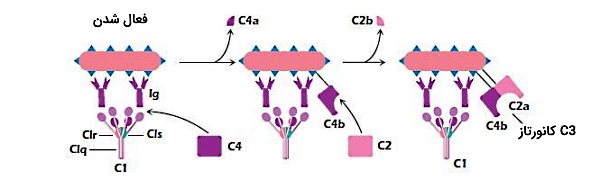
پس از اتصال پروتئین C1 به آنتیبادی پروتئینهای مکمل دیگر به آن متصل میشوند.
- اتصال C1 به کمپلکس آنتیبادی-آنتیژن با تغییر کنفورماسیون، سرین پروتئاز C1r را فعال میکند. C1r فعال از کمپلکس جدا شده و سرین پروتئاز C1s را فعال میکند.
- فعالیت پروتئازی C1s بخشی از توالی آمینواسید (C4a) در انتهای آمین پروتئنهای C4 را جدا میکند. C4b بخش باقیمانده C4 با تشکیل پیونداستری با پروتئینها یا کربوهیدراتها به غشای پاتوژن متصل میشود.
- در مرحله بعدی پروتئین C2 به C4b متصل میشود. C2 بهوسیله سرین پروتئاز C1s به دو زیرواحد C2a و C2b تقسیم میشود. C2b از کمپلکس جدا شده و واکنشهای التهایبی را فعال میکند.
- C2a آنزیمی است که پس از اتصال به C4b فعال میشود. این کمپلکس آنزیمی پروتئین C3 را فعال و به دو زیرواحد C3a و C3b تبدیل میکند. زیرواحد C3a یکی دیگر از پروتئینهای مکمل فعالکننده پاسخ التهابی است.
- پروتئین C3b از سه مکانیسم متفاوت به سیستم ایمنی کمک میکند. اتصال این مولکول با پیوند کوالانسی به پروتئینها یا کربوهیدراتهای غشای پلاسمایی پاتوژن شناسایی این سلول بهوسیله فاگوسیتها را افزایش میدهد. C3b با اتصال به دومین Fc آنتیبادیهای محلول منجر به رسوب کمپلکس آنتیژن-آنتیبادی، انتقال آن به کبد و تجزیه آنتیژن میشود. اتصال C3b به C4b2a آنزیم جدیدی میسازد که پروتئین C5 را فعال میکند. این مجموعه کانال غشایی تشکیل میدهد که با تغییر جریان یونی و فشار اسمزی منجر به لیز شدن پاتوژن خواهد شد.
مسیر لکتین
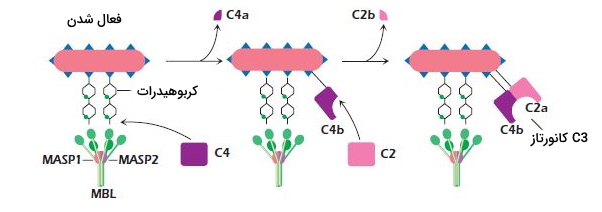
لکتینها پروتئینها محلول در پلاسما هستند که در کبد سنتز میشوند این پروتئینها به کربوهیدراتهای غشای پاتوژن متصل شده و پروتئینهای سیستم کمپلمان را فعال میکنند. لکتین اتصالی به مانوز (MBL) همراه پروتئازهای اتصالی به لکتین (MASP) به بخشهای مختلف بدن منتقل میشود. این پروتئازها ساختار و عملکردی شبیه C1s دارند و پس از اتصال لکتین به مولکول مانوز، C2 و C4 را به زیرواحدهای a و B تقسیم میکند. در نتیجه C3 فعال شده و با مکانیسمهای مشابه مسیر کلاسیک پاتوژنها را از بین میبرد.
مسیر جایگزین
مسیر جایگزین مثل مسیر لکتین مستقل از آنتیبادی است. این مسیر با فعال شدن پروتئینهای C3، فاکتور B، فاکتور D و پروپردین (فاکتور P) شروع میشود. در این مسیر پیوند تیواستری بین آمینواسیدهای پروتئین C3 تولیز و به C3(H2O) تبدیل میشود. کنفورماسیون C3(H2O) با C3 فرق دارد. این مولکول در حضور یون منیزیوم پلاسما با فاکتور B کمپلکس تشکیل میدهد. در این حالت فاکتور B بهوسیله فاکتور D به زیرواحدهای کوچکتر تجزیه میشود. زیرواحد Bb به پروتئین C3(H2O) متصل شده و کمپلکس آنزیمی C3 کانورتاز را تشکیل میدهد. این آنزیم پروتئینهای C3 بیشتری در پلاسما را فعال و فعالیت سیستم کمپلمان را افزایش میدهد.
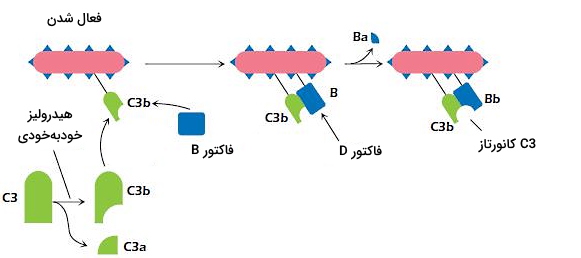
به علاوه فاکتور به به پروتئینهای C3b متصل شده به غشای هدف وصل میشود. فعالیت آنزیمی فاکتور D روی این مولکول، کمپلکس آنزیمی C3 کانورتاز غشایی ایجاد میکند. C3 کانورتاز محلول در پلاسما شروعکننده مسیر جایگزین سیستم کمپلمان و نوع غشایی این آنزیم افزایشدهنده پاسخ ایمنی است. پروپدرین پروتئینی است که با اتنصال به کانورتاز غشایی پایداری این آنزیم را افزایش میدهد. بنابراین کمپلکس آنزیمی C5 کانورتاز در این مسیر از C3bBbC3b تشکیل میشود. فعال شدن کانورتاز C5 با تشکیل کانالهای غشایی و مرگ سلول هدف همراه است.
کمپلکس حمله به غشا چگونه تشکیل می شود؟
«کمپلکس حمله به غشا» (Membrane Attack Complex | MAC) کانالی است که ساختار غشای سلول هدف را به هم ریخته و لیز شدن سلول را تحریک میکند. C5b در اثر فعالیت کانورتاز در غشا ایجاد میشود. این پروتئین بهوسیله پیوندهای غیرکوالانسی به غشا متصل شده و جایگاهی برای اتصال سایر پروتئینهای کمپلکس حمله به غشا دارد. اتصال پروتئین C6 به C5 سبب پایداری این مولکول در غشا میشود. سپس مولکول C7 به کمپلکس C5bC6 متصل شده و کنفورماسیون آن تغییر میکند. در نتیجه تغییر کنفورماسیون توالی هیدروفوب پروتئین وارد غشای پاتوژن می شود.
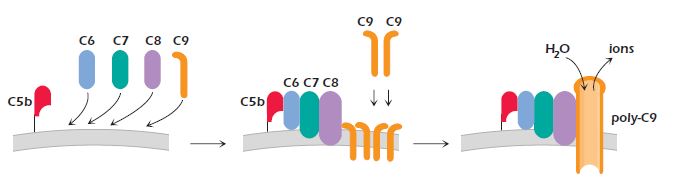
اتصال زنجیره بتای پروتئین C8 به کمپلکس C5b67 کنفورماسیون زنجیره آلفا-گاما را تغییر داده و بخش هیدروفوب پروتئین وارد غشای پاتوژن خواهد شد. در ادامه این واکنشهای آبشاری ۱۰ تا ۱۹ پروتئین C9 به مجموعه قبلی اضافه شده و کانالی به قطر ۷۰ تا ۱۰۰ آنگستروم در غشا ایجاد میشود. به هم ریختگی ساختار غشا و تعادل اسمزی با مرگ سلول همراه است.
اوپسونیزاسیون
در اپسونیزاسیون آنتیبادیهای محلول در پلاسما یا پروتئینهای سیستم کمپلمان به آنتیژنهای سطحی سلول مهاجم متصل میشوند. اتصال این پروتئینها به آنتیژنهای ویروسی از ورود ویروسها به سلولهای سالم جلوگیری میکند. در غشای فاگوسیتها گیرندهای برای بخش Fc آنتیبادیها و پروتئینها C1q، CEb و MBL وجود دارد. در نتیجه اتصال این مولکولها به گیرندههای CD35، SHGN-R1 و C1qRp فاگوسیتوز را فعال میکند. گیرنده پروتئینهای مکمل در غشای گلبولهای قرمز نیز وجود دارد. در نتیجه پاتوژن متصل به پروتئین مکمل به کبد منتقل شده و بهوسله ماکروفاژهای کبدی حذف میشود.
به علاوه ترشح سیتوکینها از سلولهای آسیبدیده و نکروزی سبب فعال شدن سیستم کمپلمان، اتصال پروتئین های C4b و C3b، برهمکنش پروتئینها با گیرندههای فاگوسیتی (CR1 یا CR3) و فاگوسیتوز سلول آسیبدیده میشود. اتصال پروتئین فاز حاد و سیتوکینهای التهابی به گیرندههای سلولهای آسیبدیده مسیر کلاسیک کمپلمان را فعال میکند.
پاسخ التهابی
C3a و C5a زیرواحدهای کوچک پروتئینهای سیتم کمپلمان هستند که به گیرندههای غشایی گرانولوسیتها، مونوسیتها، ماکروفاژها، ماستسلها و سلولهای اندوتلیال متصل شده و ترشح فاکتورهای پیشالتهابی ازجمله IL6 و TNF را تحریک میکنند. فاکتورهای پیشالتهابی لوکوسیتهای بیشتری را به محل عفونت جذب میکنند و سرعت پاسخ ایمنی افزایش مییابد.
افزایش فعالیت سلول B
پروتئین C3dg یکی از زیرواحدهایی است که پس از تجزیه C3 ایجاد میشود. این پروتئین همزمان به آنتیژن متصل به گیرنده غشای سلول B (IgG) و گیرنده CR2 یا CD21 آستانه تحریک سلول را کاهش و فعالیت آن را افزایش میدهد. گیرنده CR2 در غشای سلولهای دندریتی در فولیکولهای گره لنفاوی به C3dg و گیرنده CR1 به C3b متصل میشود. اتصال کمپلکس گیرنده-پروتئین کمپلمان به گیرنده سلولهای B تشکیل سلولهای B خاطره را تحریک میکند. به علاوه سلولهای B وابسته به لنفوسیت T در حضور CR2-C3dg سریعتر فعال میشود.
تنظیم سیستم کمپلمان
تمام مکانیسمهای ایمنی بدن برای پیشگیری از آسیب به سلولهای سالم تنظیم میشوند. نیمهعمر کوتاه پروتئینهای سیستم کمپلمان اولین عامل تنظیمکننده این سیستم است. برای مثال نیمهعمر کمپلکس تنها ۵ دقیقه است! تفاوت کربوهیدراتهای غشای سلولهای بدن انسان و پاتوژنها عامل دیگری است که از اتصال پروتئینهای مکمل به غشای سلولی و فعال شدن واکنشهای ایمنی آن جلوگیری میکند. به علاوه پروتئینهای تنظیمی محلول در پلاسما و غشای سلولهای ایمنی، با مهار تشکیل کمپلکلسها، تجزیه یا غیرفعال کردن فاکتورهای التهابی سیستم کمپلمان و مهار MAC سیستم کمپلمان را تنظیم میکند. عملکرد این پروتئینها در جدول زیر خلاصه شده است.
| نوع پروتئین | مسیر تنظیمی | فعالیت |
|
مهارکننده C1 (محلول در پلاسما) | کلاسیک و لکتین | مهار فعالیت سرین پروتئازی و جدا شدن C1s و C1r |
|
پروتئین DAF (غشایی) | کلاسیک و لکتین | تحریک جدا شدن C3 کانورتازها |
|
CD35 (غشایی) | جایگزین | مهار تشکیل کمپلکسهای C3 کانورتاز و افزایش سرعت جدا شدن زیرواحدها
پروتئین کمکی فاکتور I برای تجزیه C4b و C3b |
|
C4BP (محلول در پلاسما) | همه مسیرها | مهار تشکیل کمپلکسهای C3 کانورتاز و افزایش سرعت جدا شدن زیرواحدها
پروتئین کمکی فاکتور I برای تجزیه C4b |
|
فاکتور H (محلول در پلاسما) | همه مسیرها | مهار تشکیل کمپلکسهای C3 کانورتاز و افزایش سرعت جدا شدن زیرواحدها
پروتئین کمکی فاکتور I برای تجزیه C3b |
|
فاکتور I (محلول در پلاسما) | همه مسیرها | سرین پروتئاز تجزیه C3b و C4b |
|
کوفاکتورهای پروتئولیز (CD46) (غشایی) | همه مسیرها | پروتئین کمکی فاکتور I برای تجزیه C4b و C3b |
|
پروتئین S (ویترونکتین) (محلول در پلاسما) | همه مسیرها | مهار ورود کمپلکلس C5b67 به غشای سلولی |
|
پروتکتین (CD59) (غشایی) | همه مسیرها | بلاک جایگاه اتصال C9 به کمپلکس C5b67 |
|
کربوکسیپپتیدازها (N، B و R) (محلول در پلاسما) | فاکتورهای التهابی | مهار پاسخ التهابی بهوسیله تجزیه باقیماندههای آرژنین از انتهای C پروتئینهای C5a و C3a |
مکانیسم دفاعی پاتوژن در برابر سیستم کمپلمان چیست؟
میکروبها برای دفاع از خود در برابر سیستم کمپلمان مکانیسمهای متفاوتی دارند. دیواره سلولی ضخیم در باکتریهای گرم مثبت، کپسول، ترشح پروتئاز پروتئینهای مکمل و واکوئلهای درون سلولی مکانیسمهایی است که از باکتریها در برابر سیستم کمپلمان محافظت میکند. گلیکوپروتئینهای ویروسی و آلکالین پروتئاز ترشح شده بهوسیله بعضی قارچها (Aspergillus Fumigatus) با اتصال به جایگاه Fc آنتیبادی (مهار اتصال C1 و C3) و تجزیه پروتئینهای مکمل شروع پاسخ ایمنی را مهار میکنند.
نقص سیستم کمپلمان و اهمیت تشخیص
در بخشهای قبلی این مطلب از مجله فرادرس نقش دفاعی سیستم کمپلمان در برابر انواع پاتوژنهای باکتریایی، قارچی و ویروسی را توضیح دادیم. این سیستم نقش مهمی در از بین بردن باکتریهای کپسولدار و عفونتزا (پیوژنیک) ازجمله گونههای نایسریا (Neisseria | پاتوژنهای ایجاد مننژیت و بیماریهای مقاربتی)، «استافیلوکوکوس نومونیا» (Streptococcus pneumoniae)، «اچ. آنفولانزا» ( H. influenzae) و «استافیکوکوس اورئوس» (Staphylococcus aureus) دارد.
پاسخ ایمنی ایجاد شده در سیستم هومورال در پاسخ به این باکتریها، با افزایش تولید ترشح آنتیبادی جی (IgG) همراه است. اتصال این آنتیبادی به آنتیژنهای پاتوژن فعال شدن سیستم کمپلمان، اوپسونیزاسیون، فاگوسیتوز و مرگ سلولی را به همراه دارد. به همین دلیل نقص ژنتیکی یا اکتسابی در سیستم کمپلمان یا تولید آنتیبادی احتمال به این بیماریها را افزایش میدهد.
به علاوه پروتئینهای این سیستم نقش مهمی در رسوب کمپلکسهای آنتیژن-آنتیبادی و حذف آنها از بدن دارند. نقص این سیستم تجمع آنتیژن-آنتیبادی در بافت و پاسخ التهابی را افزایش میدهد. نقص سیتم کامپلمان را میتوان بهوسیله شمارش کامل سلولهای خون (CBC)، آنالیز ادرار، تست سرولوژی آنتیهسته لوپوس، تست جایگزین کمپلمان همولیتیک و تست کامل کمپلمانهای همولیتیک سرم تشخیص داد.
اگرچه جهش ژنتیکی یکی از پروتئینهای مسیر کمپلمان بسیار نادر و معمولا بدون علائم بالینی است اما بررسی این نقصها در تشخیص نوع عفونت اهمیت دارد. جدول زیر نقصهای ژنتیکی اجزای (پروتئینها ایمنی و تنظیمی) مختلف سیستم کمپلمان و نتیجه آن خلاصه شده است.
| پروتئین جهشیافته | تغییر سیستم کمپلمان | علائم بالینی |
| C3 | مهار مسیر جایگزین کمپلمان، التهاب ایجاد شده بهوسیله C3b و تشکیل MAC | عفونت چرکی شدید و علائم لوپوس سیستمی (SLE) |
| C1، C4 و C2 | مهار مسیر کلاسیک | عفونت چرکی شدید و علائم لوپوس سیستمی (SLE) |
| پروپردین، فاکتور B یا فاکتور D | مهار مسیر جایگزین | عفونت چرکی شدید |
| لکتین اتصالی به مانوز | مهار مسیر لکتین | عفونت باکتریایی مکرر |
| C5، C6، C7، C8 و C9 | مهار تشکیل MAC | عفونت نایسریایی (باکتری گرم مثبت) مکرر |
| مهارکننده C1 | بههم ریختگی تنظیم تمام مسیرهای ایمنی کمپلمان | ادم رگها |
| CD59 و DAF | بههمریختگی سیستم تنظیمی: حمله MAC به سلولهای سالم | همولیز و ترومبوزیس |
| فاکتور H و فاکتور I | بههمریختگی فعال شدن C3 | التهاب گلومرول نفرون و سندروم اورمیک همولیتیک غیرمعمول |
| تغییرات فاکتور H و پروتئینهای دیگر مسیر جایگزین | کاهش تنظیم مسیر جایگزین | تحلیل عضلانی وابسته به سن |
| گیرنده کامپلمان ۳ (CR3) | نقص اتصال و مهاجرت لوکوسیتها | عفونت باکتریایی مکرر |
جمع بندی
در این مطلب از مجله فرادرس توضیح دادیم که سیستم کمپلمان بخشی از سیستم دفاعی بدن است که بهوسیله برهمکنش پروتئین با پاتوژن، آنتیبادی و گیرندههای سلول ایمنی از بدن دفاع میکند. اتصال پروتئینهای مکمل این سیستم به آنتیزنهای محلول یا غشایی فاگوسیتوز پاتوژنها را افزایش میدهد. تعدادی از پروتسینهای این سیستم فاکتورهای پیشالتهابی هستند که با تحریک پاسخ التهابی به حذف پاتوژنها کمک میکنند و تعدادی از این پروتئینها با تشکیل کانال غشایی سبب لیز شدن پاتوژن میشوند.













زیات تشکر از همکاری همه جانبه شما