تبخیر چیست؟ – به زبان ساده
تبخیر به فرآیند تبدیل مایع به بخار (گاز) میگویند. در نتیجه افزایش دما، انرژی جنبشی مولکولها افزایش پیدا میکند. به دلیل این افزایش، نیروی جاذبه بین مولکولها کاهش مییابد و در نهایت، این مولکولها به شکل بخار به محیط اطراف روانه میشوند. این فرآیند با تغییر حالت ماده و مصرف گرما همراه است.


در این مطلب از مجله فرادرس میآموزیم تبخیر چیست و عوامل تاثیرگذار بر آن کدامند. در ادامه مثالهایی را از انواع تبخیر بررسی کرده و رابطه تبخیر و فشار بخار را بررسی میکنیم. با مطالعه این مطلب از مجله فرادرس میتوانید به شکلی کامل بیاموزید تبخیر چیست.
تبخیر چیست؟
تبخیر فرآیندی است که در آن مولکولهای یک ماده مایع، انرژی گرمایی دریافت کرده و به سبب آن به بخار (گاز) تبدیل میشوند. در این فرآیند، انرژی جنبشی ذرات سازنده مایع افزایش یافته و فاصله بین مولکولها زیاد میشود. نیروهای بین مولکولی تضعیف میشوند و در نهایت مایع به گاز تبدیل میشود.
عکس فرآیند تبخیر، چگالش نام دارد که در آن گاز به مایع تبدیل میشود.
انواع تبخیر
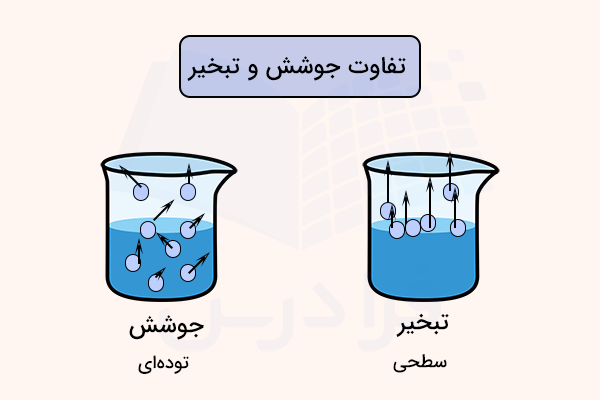
تبخیر را میتوان به دو نوع زیر تقسیم کرد:
- «تبخیر» (Vaporization)
- «جوشش» (Boiling)
تبخیر نوع پدیده سطحی (وابسته به سطح) به شمار میآید حال آنکه جوشش به عنوان پدیدهای تودهای - اتفاق افتاده در توده ماده - در نظر گرفته میشود.
عوامل موثر بر تبخیر
عوامل مختلفی سبب میشوند که فرآیند تبخیر سرعت بیشتر یا کمتری داشته باشد که در ادامه به این عوامل اشاره خواهیم کرد.
- دما: تبخیر به طور مستقیم به دما وابسته است. با افزایش دما، انرژی جنبشی مولکول افزایش و نیروی جاذبه بین مولکولها کاهش پیدا میکند. در نتیجه، با افزایش دما، سرعت تبخیر افزایش مییابد.
- سطح: با افزایش سطح تماس مایع با اتمسفر یا منبع گرما، سرعت این فرآیند افزایش خواهد یافت چراکه در این شرایط تعداد ذرات بیشتری در معرض تغییر دما قرار میگیرند.
- فشار: فشار رابطه معکوس با بخار شدن دارد. با افزایش فشار، انرژی جنبشی ذرات به سادگی قبل افزایش پیدا نمیکند.
- سرعت باد: با افزایش سرعت باد، به دلیل نقش روبشی باد در جابجایی مولکولها، سرعت این فرآیند نیز افزایش پیدا خواهد کرد.

نمونه های از تبخیر در زندگی روزمره
در زندگی روزمره به وفور شاهد فرآیند تبخیر هستیم. به همین دلیل در ادامه متن، مثالهایی از تبخیر آورده شدهاند.
در فرآیند صنعتی تولید نمک، این ماده را از طریق تبخیر آب شور دریا بدست میآورند. برای خشک کردن لباسهای شسته شده از این پدیده بهره میگیرند. علاوه بر این، برای جداسازی اجزای مخلوطها نیز میتوان از این پدیده استفاده کرد.
معرفی فیلم آموزش شیمی عمومی
پدیدههایی مانند تبخیر را میتوان در علم شیمی مورد بررسی قرار داد و به همین منظور، دورهای ۸ ساعت و ۲۴ دقیقهای در فرادرس تدوین شده است که در ادامه متن به توضیح این دروس خواهیم پرداخت.
در درس اول این آموزش، ساختار اتم مورد بررسی قرار میگیردو ایزوتوپها و مدلهای اتمی و الکترونخواهی از جمله مباحث مهم آن به شمار میآیند. در درس دوم، پیوندهای شیمیایی همچون پیوندهای یونی، کووالانسی و فلزی مرور میشوند و ساختار هندسی مولکولها در درس سوم بررسی خواهد شد. رفتار گازها مانند قوانین بویل و شارل در درس چهارم آموزش داده میشود. درس پنجم به مایعات و جامدات اختصاص دارد و فشار بخار و دمای ذوب و انجماد در این درس مورد بررسی قرار میگیرد.
انواع محلولها و عوامل موثر بر انحلالپذیری از مباحثی به شمار میآیند که به درس ششم اختصاص دارند و تقطیر نیز در همین درس بررسی میشود. تعادلهای شیمیایی و قوانینی همچون قوانین ترمودینامیک و قانون هس در درس هفتم مرور خواهد شد. بررسی سینتیک شیمیایی به درس هشتم اختصاص دارد و اسیدها و بازها و انواع شناساگرهای اسید و باز در درس نهم مورد بررسی قرار میگیرند. منحنیهای تیتراسیون و محلولهای بافر، مباحث مهم درس دهم را تشکیل میدهند.
در درس یازدهم الکتروشیمی به همراه واکنشهای اکسایش و کاهش آموزش داده میشود و شیمی عناصر فلزی و از جمله گازهای نجیب و هالوژنها و روندهای جدول تناوبی مباحث مهم درس دوازدهم را تشکیل میدهند. درس سیزدهم و چهاردهم نیز به شیمی فلزات مانند فلزات قلیایی و قلیایی خاکی میپردازد.
تبخیر و فشار بخار
همه ما زمانی که یک کتری آب را حرارت دادهایم بعد از مدتی صدای جوشش آب درون کتری را شنیدهایم. زمانی که به مایعی حرارت میدهیم، مولکولهای آن انرژی جنبشی مشخصی را کسب میکنند تا بر نیرویی غلبه شود که آنها را در حالت مایع نگه داشته است و در نهایت به فاز گاز منتقل خواهند شد. در اثر این اتفاق، مجموعهای از مولکولهای گازی در بالای مایع ایجاد میشوند و فشاری را ایجاد میکنند. اگر بخار ایجاد شده در محفظهای عایق تشکیل شده بود، به مرور این فشار ایجاد شده میتوانست شکل ظرف را تغییر دهد.

اما در یک کتری آب که عایقبندی نشده است، زمانیکه فشار بخار ایجاد شده با فشار هوا (در اینجا فشار اتمسفریک) برابر شود، آب شروع به جوشیدن میکند. این جوشش که با تبخیر آب همراه است، در نهایت سبب میشود که حجم آب مایع در ظرف به مرور زمان کاهش بیابد.
آزمون تبخیر
۱. کدام مورد زیر باعث افزایش سرعت تبخیر یک مایع میشود؟
افزایش دمای محیط اطراف مایع
افزایش فشار محیطی اطراف مایع
کاهش سرعت باد در اطراف مایع
کاهش سطح تماس مایع با هوا
افزایش دمای محیط اطراف مایع باعث میشود مولکولهای مایع انرژی بیشتری دریافت کرده و سریعتر از سطح مایع خارج شوند، در نتیجه سرعت تبخیر افزایش پیدا میکند.
۲. اگر فشار اتمسفریک محیط کاهش یابد، نقطه جوش یک مایع چه تغییری میکند و دلیل این تغییر چیست؟
مایع به راحتی تبخیر میشود ولی نقطه جوش ثابت میماند.
نقطه جوش تغییری نمیکند چون به فشار وابسته نیست.
نقطه جوش مایع کاهش مییابد چون تعادل راحتتر برقرار میشود.
نقطه جوش مایع افزایش مییابد چون فشار بخار باید بیشتر شود.
وقتی فشار محیط کاهش پیدا میکند، مایع زودتر به فشاری میرسد که با فشار بخارش برابر شود، بنابراین نقطه جوش آن پایین میآید. در نتیجه، کاهش فشار باعث میشود مایع آسانتر بجوشد و گزینههایی که افزایش یا عدم تغییر نقطه جوش را بیان میکنند نادرست هستند.