کبد، لوزالمعده و کیسه صفرا – از صفر تا صد
دستگاه گوارش انسان علاوه بر لولههای گوارشی دارای غددی است که آنزیمها و ترشحات گوارشی را برای هضم مواد غذایی و مایعات فراهم میکنند. از این غدد میتوان به کبد ، لوزالمعده و کیسه صفرا اشاره کرد. این بخشها هریک به طور مستقل عملکرد و وظایف خاص خود را دارند و در کنار این وظایف به هضم و جذب مواد غذایی در لوله گوارش کمک میکنند. در این مطلب به معرفی آناتومی و عملکرد این بخشها میپردازیم.
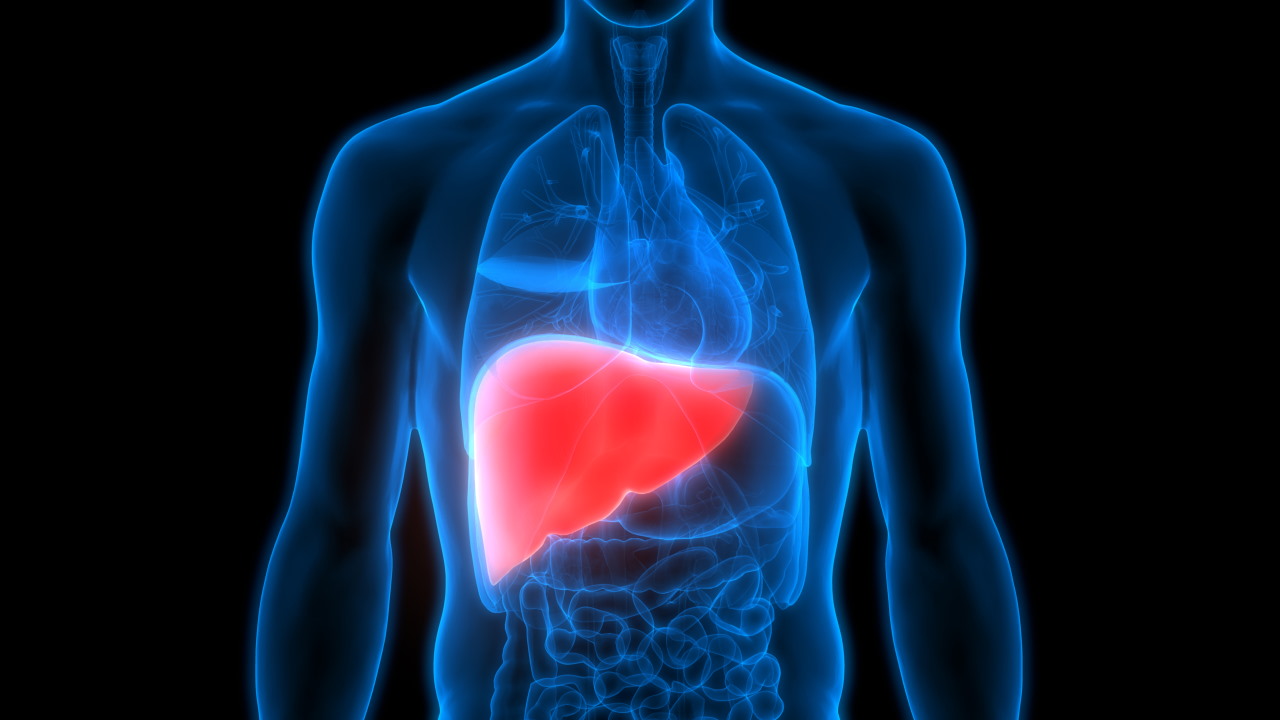
کبد
کبد نه تنها بزرگترین غده در بدن انسان است بلکه از نظر عملکرد، پیچیدهترین غده محسوب میشود.
عمده کارکردهای کبد شرکت در متابولیسم پروتئین، کربوهیدراتها و چربیها است. برخی از فعالیتهایی که کبد نقش اساسی در آنها دارد را میتوان به صورت زیر بیان کرد:
- سنتز کلسترول
- تولید اسیدهای صفراوی برای شروع تشکیل صفرا
- شرکت در حمل و نقل بیلی روبین
- سوخت و ساز و انتقال داروهای خاص
- کنترل حمل و نقل و ذخیره کربوهیدراتها
آناتومی کبد
کبد در زیر قفسه سینه و درسمت راست آن قرار دارد و قسمت اعظم ناحیه راست حفره شکم را به خود اختصاص داده است، بخشهای کوچکی از آن نیز به یک چهارم بخش فوقانی سمت چپ حفره شکم وارد شده است.
وزن این اندام از 1.2 تا 1.6 کیلوگرم (2.6 تا 3.5 پوند) است و در مردان تا حدودی بزرگتر از زنان است. بزرگترین بخش افقی آن در حدود 20 تا 22 سانتیمتر (تقریباً 8 اینچ) طول دارد. اندازه کبد به صورت عمودی، از 15 تا 18 سانتیمتر است و از ضخامت آن به 10 تا 13 سانتیمتر میرسد.
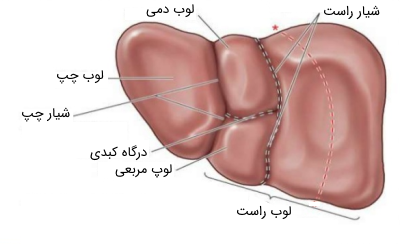
کبد به دو لوب (بخش) نابرابر تقسیم میشود: یک لوب بزرگ که در سمت راست قرار دارد و لوب چپ که کوچکتر است. لوب چپ از سطح قدامی کبد توسط رباطهای متراکم داسی شکل به سطح زیر دیافراگم متصل میشود. در سطح جلویی کبد، لوبهای راست و چپ از هم جدا میشوند، این امر با یک شیار (شکاف رباط گرد) که دارای رباطهایی است که تا قسمت ناف میرود، صورت میگیرد.
دو لوب کوچک دیگر به نامهای لوب «دمی» (Caudate) و «مربعی» (Quadrate)، قسمتی از سطح تحتانی لوب راست را اشغال میکنند. کل بخشهای کبد به جز قسمت کوچکی از سمت راست آن که به دیافراگم متصل است، در یک کپسول از بافت قرار دارد که در ادامه به پرده صفاقی میرسد و در این حالت به دیوارههای شکمی متصل میشود.
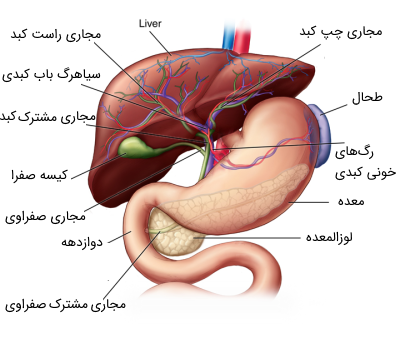
رگهای خونی اصلی در یک شیار مرکزی که به نام درگاه کبدی یا ناف کبدی (Porta Hepatis) شناخته میشود قرار میگیرند، این شیار تا سطح تحتانی کبد ادامه یافته و به صورت آناتومیکی لوبهای دمی و مربعی را از هم جدا میکند. خون مورد نیاز به کبد از دو منبع تامین میشود: خون کاملاً اکسیژن یافته رگ کبدی که از شاخه اصلی محور سلیاک (شریان اصلی که از شکم عبور میکند) منشعب میشود. منبع دوم، خونی که به میزان کمی دارای اکسیژن است و درون ورید پرتال بزرگ جریان دارد. خونی که از سیاهرگهای طحال، لوزالمعده، کیسه صفرا، مری و لولههای دستگاه گوارش اعم از معده، روده کوچک و روده بزرگ میآیند توسط ورید پرتال دریافت شده و بخشی از نیاز خونی کبد را مرتفع میکند.
سیاهرگ یا ورید پورتال از محل تقاطع ورید طحال با سیاهرگ رودهبند بالایی تشکیل میشود. سیاهرگ پرتال در ناحیه درگاه کبدی به دوشاخه اصلی تقسیم میشود که هریک به سمت یکی از لوبهای اصلی کبد میروند. درگاه کبدی همچنین محل خروج مجاری و کانالهای کبدی است. این کانالها مسیر نهایی برای شبکهای از مجرای صفراوی کوچکتر هستند که در سراسر کبد پراکنده شدهاند و برای انتقال صفرا تازه تشکیل شده از سلولهای کبدی به روده کوچک از طریق مجاری صفراوی فعالیت میکنند.
آناتومی میکروسکوپی
آناتومی میکروسکوپی کبد ساختار یکنواخت و خوشهای سلولهایی به نام لوبول را آشکار میکند، این سلولها محل اصلی انجام عملکردهای حیاتی کبد هستند. هر لوبول قطری در حدود یک میلیمتر دارد و از طنابهای بیشماری از سلولهای مستطیلی کبد یا هپاتوسیت تشکیل شده است. این طنابها از رگهای مرکزی و ونولها یا سیاهرگچههای کبدی منشا میگیرند. هر لوبول توسط یک لایه نازک از بافت همبند از سایر لوبولهای همسایه جدا میشود. طناب سلول کبدی یک سلول ضخیم است و از طریق چندین سطح توسط فضاهایی به نام سینوس کبدی یا سلولهای کپیلاری کبدی از یکدیگر جدا میشوند.
سینوسهای کبدی در کنار لایه نازکی از سلولهای اندوتلیال قرار دارند که دارای دهانههایی هستند که از طریق آنها میتوانند میکروویلیهای سلولهای کبدی را گسترش دهند و امکان دسترسی مستقیم سلولهای کبدی به جریان خون از راه سینوسها را فراهم کنند. از دیگر سلولهای اصلی کبد، «سلولهای کوپفر» (Kupffer Cell) است که به دیواره سینوسی میچسبند و به لومن آنها میروند. این سلولها به صورت فاگوسیت عمل میکنند (فاگوسیت سلولی است که مواد خارجی یا سلولهای دیگر را درون خود به دام میاندازد و از بین میبرد).
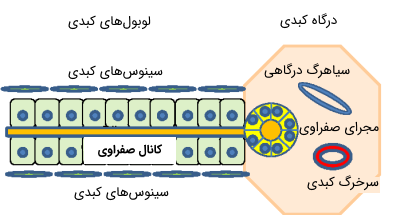
فضاهای کوچکی به نام «Disse Spaces» در مکانهایی بین سلولهای کبدی یا هپاتوسیتها و اندوتلیوم سینوسی وجود دارند. این فضاها احتمالاً برای انتقال لنف ایجاد شدهاند. در سطوح همجوار، سلولهای کبدی به وسیله اتصالات متراکم و محکم به یکدیگر متصل میشوند. این اتصالها توسط کانالهای کوچکی به نام «کانالیکولی» (Canaliculi) سوراخ میشوند که محل ورود و خروج مجاری صفراوی هستند و صفرا را از کبد دریافت میکنند. آنها سرانجام با کانالهای دیگر پیوند مییابند و مجاری صفراوی بزرگتر را تشکیل میدهند که در آخر از مجاری کبدی و درگاه کبدی خارج میشوند.
هپاتوسیتها یا سلولهای کبدی حدود 80 درصد از حجم کبد را اشغال میکنند و سیتوپلاسم آنها (منطقه اطراف هسته) حاوی میتوکندریهای زیادی است که انرژی مورد نیاز بسیاری از عملکردهای تولیدی و متابولیکی سلولهای کبد را تأمین میکنند. سیتوپلاسم همچنین حاوی چندین گروه از کیسهها و لولههای طولانی به نام شبکه آندوپلاسمی است که بسیاری از آنزیمهای ضروری برای فعالیتهای کبد را فراهم میکنند. بعضي از غشاهای شبکه آندوپلاسمی به دليل وجود ريبوزومها و دانههای رسوبی در سطح آنها به عنوان شبکه آندوپلاسمی خشن شناخته میشوند.
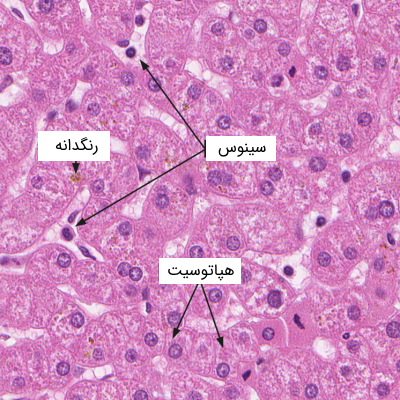
ریبوزومها اندامکهای سلولی هستند كه وظيفه تشكيل زنجيرههای اختصاصی پلی پپتيد (پروتئين) از روی رشتههای mRNA را با استفاده از جایگزینی اسیدهای آمینه بر عهده دارند. ریبوزومها این کار را با تبدیل گلیکوژن به گلوکوز طی فرایندی به نام «گلوکوژنز» (Gluconeogenesis) انجام میدهند. آمونیاک آزاد شده از گلوکونوژنز با استفاده از چرخه اوره در سلولهای کبدی به اوره تبدیل میشود.
شبکه آندوپلاسمی صاف، جایی است که سیتوکرومها (ترکیبی از هم (آهن) هموگلوبین با پروتئینهای مختلف) و آنزیمهای خاصی، عملکردهای مهم کبدی نظیر متابولیسمهای دارویی، هورمونی و همچنین سنتز کلسترول را انجام میدهند. هپاتوسیتها همچنین با ترکیبات کربوهیدراتی بیلیروبین و سایر ترکیبات متابولیک و خارجی محلول در چربی متصل میشوند و از این طریق آنها را در آب محلول میکنند.
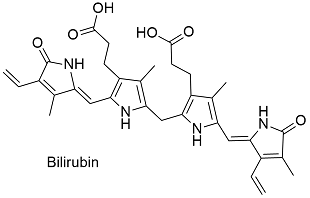
بیلیروبین محصول متابولیسم هموگلوبین است که در مغز استخوان و بافت لنفاوی تشکیل میشود و پس از اتصال به آلبومین پلاسما به کبد انتقال مییابد. بیلیروبین در غشای سینوسی سلولهای کبدی آزاد میشود و از آن جا به شبکه آندوپلاسمی صاف میرود، در شبکه آندوپلاسمی صاف، با یک یا دو مولکول اسید گلوکورونیک متصل شده و از این طریق در آب محلول میشود. در نتیجه بیلیروبین در صفرا به صورت قابل استفاده در میآید. دستگاه گلژی، مجموعهای از ساختارهای لولهای بین شبکه آندوپلاسمی و کانالهای آن است که به عنوان ایستگاه حمل و نقل برای پروتئینهای تازه ساخته شده و سایر محصولات کبدی قبل از انتقال به سایر قسمتهای سلول یا خارج از سلول عمل میکند.
لیزوزومها، یکی دیگر از ترکیبات مهم سیتوپلاسمی هستند که وظیفه ذخیره رنگدانههای داخل سلولی از قبیل آهن یا مس و هضم برخی از محتویات مانند گلیکوژن یا ذرات خارجی را بر عهده دارند. هسته سلولهای کبدی تکثیر سلول را کنترل میکنند و مواد ژنتیکی را به صورت رشته پیامرسان یا mRNA از DNA به اندامکهای مستقر در سیتوپلاسم انتقال میدهند. رشته پیامرسان یا mRNA در طی فرایند رونویسی از روی رشتههای DNA ساخته میشود و شامل کدهای اسید آمینههای تولید کننده پروتئین است.
مجاری صفراوی
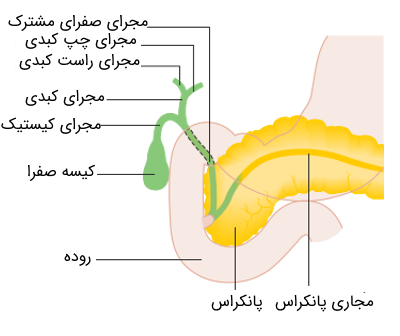
مجاری صفراوی با دو مجرای بزرگ شامل مجاری کبدی راست و چپ، از ناحیه درگاه کبدی (شیاری که دو لوب را در سمت راست کبد از هم جدا میکند) شروع میشوند. درست در زیر درگاه کبدی، این مجاری که 1 تا 2 سانتیمتر (تقریباً نیم اینچی) قطر دارند، برای تشکیل مجرای کبدی به هم متصل میشوند و در کل مجرایی به قطر 2 تا 3 سانتیمتر را تشکیل میدهند و در انتها به مجرای کیستیک که به کیسه صفرا متصل است، میپیوندند.
مجرای صفراوی مشترک ایجاد شده، از سر لوزالمعده به سمت پایین پیش میرود. این مجرا درون لوزالمعده معمولاً به مجرای اصلی آن به نام «ویرسونگ» (Wirsung) متصل میشود. مجرای ویرسونگ در ناحیه منبسط شدهای از مجرای صفراوی به نام آمپول کبدی (آمپول واتر) قرار دارد. آمپول کبدی در دیواره منحنی داخلی دوازدهه پایینرو قرار دارد. این مجرا در لومن دوازدهه (در قسمت 2 تا 3 سانتیمتری ابتدای آن به نام آمپول دوازدهه) خاتمه مییابد.
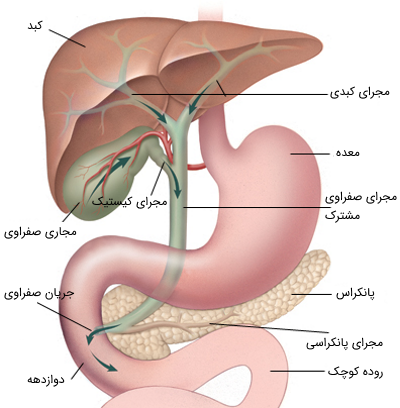
مجرای صفراوی مشترک به طور متوسط حدود 10 سانتیمتر طول دارد و جریان صفرا از انتهای پایین آن به سمت روده با عملکرد ماهیچههای اسفنکتر کبدی (اسفنکتر اوددی) واقع در پاپیلای دوازدهه کنترل میشود. مجرای کیستیک از طول 2 تا 3 سانتیمتر متغیر است و در کیسه صفرا پایان مییابد. مجرای کیستیک، یک ساختار کیسه مانند با ظرفیت حدود 50 میلی لیتر است. این مجرا در طول خود به صورت خطی در کنار سلولهای مارپیچ مخاطی به نام دریچههای مارپیچی قرار میگیرد. به طور معمول، کیسه صفرا تا حدی در زیر سطح لوب راست کبد تعبیه شده است.
صفرا
عملکرد اصلی صفرا هضمکنندگی آن است و به محلول کردن و هضم چربی در لومن روده کوچک کمک میکنند. ابتدا صفرا درون سلولهای کبدی یا هپاتوسیتها تشکیل میشود و میزان تشکیل آن در درجه اول به میزان سرعت اسیدهای صفراوی در مجاری صفرا یا کانالهای خون بستگی دارد. بخشی از جریان صفرا با عواملی غیر از ترشح اسیدهای صفراوی مرتبط است. به نظر می رسد جریان صفرا گاهی وابسته به ترشح سدیم از سلولهای کبدی است و همچنین تا حدی توسط عملکرد هورمونهای روده، مانند ترشح هورمون کولهسیستوکینین (CCK) و گاسترین کنترل میشود.
کل محتوای اسید صفراوی در هر زمان حدود 3 گرم اندازه گیری شده است، تقریباً همه این ۳ گرم در حالت استراحت کیسه صفرا، درون آن قرار دارد. در مسیر حرکت اسید صفراوی درون مجاری صفراوی کبد، حجم آن به یک دهم مقدار ابتدایی آن کاهش مییابد. این امر به دلیل جذب مجدد انتخابی آب، کلراید و بیکربنات ایجاد میشود. فرایند تغلیظ اسید صفرا عمدتاً در کیسه صفرا انجام میگیرد و در نتیجه، صفرا از کیسه صفرا با غلظت بیشتر و رنگ تیرهتر (به دلیل غلظت رنگدانههای آن) نسبت به صفرا قبل از ورود به آن، بیرون میآید. پر شدن دوازدهه، از غذا به ویژه با وعدههای غذایی حاوی چربی، ترشح CCK را تحریک میکند، این هورمون باعث انقباض لایه ماهیچهای در دیواره کیسه صفرا میشود.
علاوه بر یونهای معدنی (سدیم، پتاسیم، کلسیم، منیزیم، کلرید و بی کربنات)، صفرا حاوی پروتئین و بیلیروبین است. بیلیروبین رنگ طلایی در محلولهای رقیق و رنگ کهربایی تیره در محلولهای غلیظ را ایجاد میکند. این در حالی است که از نظر مقایسهای بیلیروبین از اسیدهای صفراوی (مشتق شده از کلسترول کبدی)، فسفولیپیدها (عمدتاً فسفاتیدیل کولین، یا لسیتین) و کلسترول غلظت بیشتری دارد. کلسترول یک استرول چهار حلقهای است که از رژیم غذایی جذب میشود، در حالیکه برخی از مواقع کبد و روده آن را میسازند. کلسترول به طور معمول در ترشحات آبی محلول نیست، این مولکول در محلولهای کلوئیدی در صفرا حمل میشود و به شکل ترکیبات متصل به هم از اسیدهای صفراوی و لسیتین قابل مشاهده است. در صورت عدم وجود مقادیر کافی لسیتین و اسیدهای صفراوی، کلسترول به حالت کریستالی در میآید.

کبد دو نوع اسید صفراوی اولیه را از کلسترول، به نام «اسید کنودئوکسیکولیک» (Chenodeoxycholic Acid) و «اسید کولیک» (Cholic Acid) تولید میکند. در اثر فعالیتهای باکتریایی روده تحتانی، یکی از گروههای هیدروکسیل (دهیدروکسیلاسیون) موجود در اسید کلولیک خارج شده و این ماده به «اسید دیئوکسیکولیک» (Deoxycholic Acid) تغییر مییابد. این اسید صفراوی ثانویه به دلیل اینکه از روده جذب میشود و به کبد باز میگردد، درون محتویات صفرا قابل مشاهده است. اسید کنودئوکسیکولیک نیز در روده، گروههای هیدروکسیل خود را از دست میدهد و به «لیتوکولیک اسید» (Lithocholic Acid) تبدیل میشود، مقدار کمی از آن نیز مجددا جذب شده و در صفرا ظاهر میشود.
پانکراس
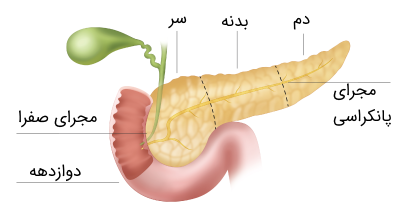
لوزالمعده یا پانکراس یک غده باریک و طویل است که به طور عرضی در قسمت فوقانی شکم، پشت معده و طحال قرار دارد. قسمت وسط لوزالمعده در مقابل ستون مهره، آئورت شکمی و بزرگ سیاهرگ زیرین قرار دارد. لوزالمعده غدهای است که هر دو حالت برونریز (دارای مجرا) و درونریز (بدون مجرای) را دارد. بافت برونریز آن از «سلولهای آکینار» (Acinar Cell) تشکیل شده است که وظیفه این بخش ساخت پیشسازهای مهمی از آنزیم گوارش غذا است و آنها را به روده کوچک منتقل میکند.
در حالی که بافت درونریز لوزالمعده (این بافت در جزایر لانگرهانس قرار دارد) حداقل دو هورمون «انسولین» (Insulin) و «گلوکاگون» (Glucagon) را تولید میکند که در تنظیمات متابولیسم کربوهیدرات اهمیت ویژهای دارند.
لوزالمعده دو هورمون دیگر را نیز تولید میکند، که شامل «پلی پپتید وازواکتیو روده» (Vasoactive Intestinal Polypeptide) و «سوماتوستاتین» (Somatostatin) هستند، این دو هورمون در کنترل ترشحات و انقباضات روده تاثیر میگذارند.
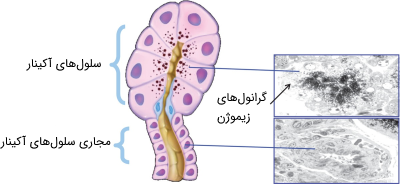
هر سلول آکینار به شکل یک هرم کوتاه است که به صورت گروههایی در اطراف یک کانال لومن مرکزی در کنار هم ردیف شدهاند. این مجاری مرکزی درون مجرای بزرگتری میریزند که در نهایت به مجرای اصلی لوزالمعده (ویرسونگ) میپیوندند. مجرای لوزالمعده به نوبه خود وارد آمپول کبدی (آمپول واتر) دوازدهه میشود، جایی که در حدود 80 درصد موارد، به مجرای صفراوی مشترک متصل میشود. گاهی اوقات اتصال مجرای اصلی لوزالمعده با مجرای صفراوی مشترک نزدیک به آمپول قرار دارد و در حالی که در مواردی، مجرای لوزالمعده و مجرای صفراوی مشترک به طور جداگانه به دوازدهه میروند.

سلولهای آکینار
سلولهای آکینار بیش از 95 درصد از جمعیت سلولی لوزالمعده برونریز را تشکیل میدهند. آنها پروتئینهای گوارشی یا آنزیمهایی تولید میکنند که عمدتاً در تخریب پروتئینهای رژیم غذایی (پروتئازها)، چربیها (لیپازها) و کربوهیدراتها (آمیلازها) در روده نقش دارند. ترشحات پروتئینی دیگر این سلولها شامل یک مهارکننده تریپسین است که به اصطلاح «پروتئین سنگی» (Stone Protein) نامیده میشود. این مهار کننده کلسیم و پروتئینهای مختلف سرمی از جمله آلبومین و ایمونوگلوبولینها را به صورت محلول نگه میدارد.
در سلولهای آکینار تقریباً تمام پروتئینهای آنزیمی بر روی ریبوزومها از اسیدهای آمینه منتقل شده به لوزالمعده توسط جریان خون ساخته میشوند. پیش سازهای آنزیمی در دستگاه گلژی با هم اتصال یافته و کمپلکسهای آنزیمی را میسازند و سپس درون گرانولهای زیموژن پوشیده از غشا که قبل از ترشح در سیتوپلاسم ذخیره شدهاند، تجمع مییابند. زیموژنها را پروآنزیمها نیز مینامند. این ترکیبات در واقع پروتئینهایی هستند که هیچ فعالیت کالیتیکی از خود نشان نمیدهند و درون سلولهای ارگانیسمهای مختلف با واکنشهای هیدرولیز پیوندی یا سایر واکنشها، به شکل فعال در میآیند. تریپسینوژن و کیموتریپسینوژن زیموژنهایی هستند که در پانکراس تولید شده و در روده به شکل فعال درآمده و تبدیل به تریپسین و کیموتریپسین میشوند.
تنظیم ترشح آنزیمی توسط محرکهایی مانند سکرین انجام میگیرد. سکرتین، هورمونی است که از دوازدهه با تحریک اسید معده آزاد میشود. کولهسیستوکینین (CCK) در صورت حضور چربی و اسیدهای آمینه در رژیم غذایی، از دوازدهه ترشح شده و در این حالت اسید هیدروکلریک و استیل کولین از پانکراس آزاد میشوند. تولیداستیل کولین و اسید هیدروکلریک در پاسخ به جنبههای حسی تغذیه و اثرات جسمی جویدن و بلع صورت میگیرد.
پس از اتصال CCK و یا استیل کولین به جایگاههای گیرنده خاص روی غشای سلولهای آکینار، گرانولهای زیموژن به نوک سلولهای آکینار مهاجرت میکنند، جایی که آنها به درون لومن مجرای مرکزی تخلیه میشوند. اتصال پلی پپتید وازواکتیو روده یا سکرتین به گیرندههای غشای سلولهای آکینار، تولید بیکربنات، سدیم، آب و آنزیمها در این سلولها و سلولهای کوچک مجرا را افزایش میدهند. بیکربنات در ازای کلرید ترشح میشود، سدیم برای هیدروژن رد و بدل می شود، در نتیجه اسیدیته خون افزایش یافته و باعث میشود که لوزالمعده به طور فعال به ترشحات خود ادامه دهد. اتصال CCK باعث تولید بیکربنات و آنزیمها توسط سلولهای آکینار میشود.
در صورت عدم وجود CCK و استیل کولین، همان شرایطی که در افراد روزهدار یا در بیمارانی که به صورت داخل وریدی تغذیه میکنند، ایجاد میشود. سنتز زیموژن توسط سلولهای آکینار به طور قابل توجهی کاهش مییابد.
آتروفی لوزالمعده نیز پس از برداشتن غده هیپوفیز رخ میدهد، این امر احتمالاً به دلیل عدم تولید هورمون رشد اتفاق میافتد. بنابراین CCK، استیل کولین و هورمونهای رشد، تغذیه کننده لوزالمعده هستند. همچنین به نظر میرسد که لوزالمعده هورمون ناشناختهای را ترشح میکند که کبد را تغذیه میکند.
سلولهای جزایر لانگرهانس
حداقل سه نوع سلول در جزایر لانگرهانس وجود دارند که به نامهای آلفای (یا A)، بتا (یا B) و دلتا (یا D) شناخته میشوند. این سلولها حدود 2 درصد از کل توده لوزالمعده را تشکیل میدهند. سلولهای این جزایر حدود 20 تا 35 درصد آلفا، 60 تا 75 درصد بتا و 5 درصد دلتا هستند. گرانولهای سلول آلفا فقط حاوی گلوکاگون هستند که ترشح آن منجر به شکسته شدن گلیکوژن در کبد و بالا رفتن سطح گلوکز خون میشود، در حالی که گرانولهای سلول بتا حاوی انسولین هستند که اثرات آن بر خلاف گلوکاگون است و قند خون را از گردش خون جمعآوری کرده و به کبد ارسال میکند تا به صورت گلیکوژن ذخیره شوند.
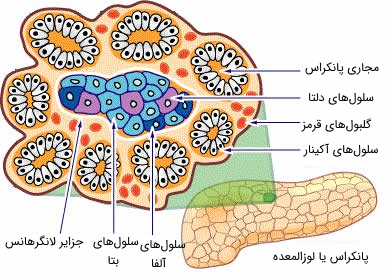
گرانولهای سلولهای دلتا حاوی سوماتوستاتین هستند که اثرات آن باعث مهار ترشح گلوکاگون و انسولین میشود. سوماتوستاتین هورمون پپتیدی است که فعالیتهای برخی از هورمونهای لوزالمعده و گوارشی را مهار میکند. این هورمون به دو شکل ۱۴ و ۲۸ اسید آمینهای در بدن مشاهده میشود. این هورمون به همراه انسولین و گلوکاگون گردش مواد مغذی سلولها را در بدن کنترل میکنند.
اگر مطلب بالا برای شما مفید بود، آموزشهای زیر به شما پیشنهاد میشود:
- مجموعه آموزشهای زیستشناسی
- آموزش فیزیولوژی جانوری ۱
- مجموعه آموزشهای علوم پزشکی
- DNA چیست؟ -- صفر تا صد
- با انواع پروتئین آشنا شوید
- کلوئید -- به زبان ساده
^^













من مطالعه نمودم خیلی عالی و آموزنده بود .ممنونم.
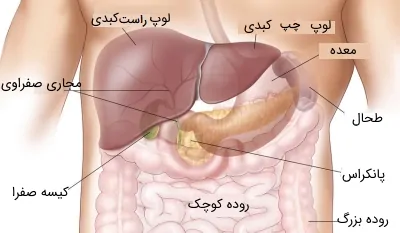
در شکل ١ لوپ چپ و راست جابجا نوشته شده
سلام، وقت شما بخیر؛
تصویر مورد نظر بازبینی و اصلاح شد، با سپاس از دقت نظر شما.
از اینکه با فرادرس همراه هستید بسیار خرسندیم.
معلومات شما خیلی عالی بود سپاس