ظرفیت گرمایی چیست؟ – به زبان ساده
ظرفیت گرمایی اصطلاحی در فیزیک است که بیان میکند چه مقدار گرما باید به ماده اضافه شود تا درجه حرارت آن یک درجه سانتیگراد افزایش یابد. این کمیت مربوط به گرمای ویژه است اما مفهومی متفاوت از این کمیت است. در این مطلب در مورد ظرفیت گرمایی و ویژگیهای این کمیت بحث و بررسی انجام میدهیم. اما در ابتدا مروری بر گرما، دما و برخی پارامترهای دیگر خواهیم داشت.


علم ترمودینامیک
قبل از شروع بحث در مورد ظرفیت گرمایی و گرمای ویژه لازم است که ابتدا اصول انتقال گرما در فیزیک و به طور کلی مفهوم گرما را بشناسید و با برخی از معادلات اساسی این زمینه آشنا شوید.
ترمودینامیک شاخهای از فیزیک است که با کار و انرژی یک سیستم سروکار دارد. کار، انرژی و گرما علیرغم داشتن معانی مختلف و کاربردهای مختلف واحدهای یکسانی در فیزیک دارند. واحد گرما در استاندارد بین المللی SI ژول است.
کار فیزیکی به عنوان حاصلضرب نیرو در فاصله تعریف میشود بنابراین با توجه به واحدهای SI برای هر یک از این مقادیر ژول همان نیوتن در متر است. واحدهای دیگری که احتمالاً برای گرما با آن روبرو میشوید عبارت از کالری (cal)، واحد انگلیسی حرارت (btu) و erg هستند.
رفتار گازها متفاوت از مایعات و جامدات است. بنابراین فیزیکدانان دنیای آیرودینامیک و رشتههای مرتبط که به طور طبیعی بسیار درگیر رفتار هوا و گازهای دیگر در کار خود با موتورهای پرسرعت و ماشینهای پرنده هستند، نگرانیهای ویژهای در مورد ظرفیت گرمایی و سایر پارامترهای قابل اندازهگیری فیزیکی مرتبط دارند که در این حالت مهم است.
یکی از این پارامترها آنتالپی است که شامل اندازهگیری گرمای داخلی سیستم بسته است. این کمیت برابر با حاصل جمع انرژی سیستم و حاصل ضرب فشار و حجم است و در حقیقت داریم:
به طور خاص تغییر در آنتالپی به معنای تغییر در حجم گاز است و داریم:
نماد یونانی یا دلتا به معنای تغییر یا تفاوت یک کمیت طبق قوانین در فیزیک و ریاضیات است. علاوه بر این میتوان گفت که حاصلضرب واحد فشار در حجم برابر با واحد کار میشود. واحد فشار برابر با نیوتن بر متر مربع است در حالی که واحد حجم متر مکعب است و حاصلضرب این دو واحد برابر با نیوتن در متر است. همچنین فشار و حجم گاز با معادله زیر به هم مربوط میشوند:
در رابطه بالا T دما و R ثابت گازها است که برای هر گاز مقدار متفاوتی دارد.
گرما چیست؟

گرما همان چیزی است که دانشمندان به آن نوعی انرژی میگویند که بین دو ماده با دمای مختلف منتقل میشود. این انتقال انرژی به دلیل تفاوت در میانگین انرژی جنبشی انتقالی برای هر مولکول در دو ماده رخ میدهد. تا رسیدن به تعادل گرمایی، گرما از ماده با درجه حرارت بالاتر به سمت ماده با درجه حرارت پایین جریان مییابد. واحد SI گرما ژول است و یک ژول برابر با یک نیوتن در متر است.
برای درک بهتر آنچه در هنگام وقوع این انتقال انرژی اتفاق میافتد سناریوی زیر را تصور کنید: دو ظرف مختلف پر از گلولههای کوچک پلاستیکی است که به اطراف پرش میکنند. در یکی از ظرفها سرعت متوسط توپها (و از این رو انرژی حرکتی متوسط آنها) بسیار بیشتر از سرعت متوسط توپهای موجود در ظرف دوم است (اگر چه سرعت هر توپ خاص در هر زمان ممکن است هر مقداری داشته باشد اما برخوردها باعث انتقال مداوم انرژی بین توپها میشوند).
اگر این ظروف را طوری قرار دهید که دیوارههای آنها یکدیگر را لمس کنند و سپس دیوارهای جدا کننده محتوای آنها را بردارید چه اتفاقی میافتد؟
توپهای ظرف اول تعامل با توپهای ظرف دوم را شروع میکنند. با بیشتر و بیشتر شدن برخورد بین توپها به تدریج سرعت متوسط توپها در هر دو ظرف یکسان میشود و مقداری از انرژی گلولههای ظرف اول تا رسیدن به این تعادل جدید به گلولههای ظرف دوم منتقل میشود.
این اساساً همان اتفاقی است که در برخورد دو جسم با دمای مختلف با یکدیگر در سطح میکروسکوپی اتفاق میافتد. در حقیقت در این فرآیند انرژی از جسم با دمای بالاتر به صورت گرما به جسم با درجه حرارت پایینتر منتقل میشود. برای مطالعه بیشتر در مورد گرما میتوانید مطلب انرژی گرمایی را مطالعه کنید.
دما چیست؟
دما اندازه میانگین انرژی جنبشی انتقالی در هر مولکول در یک ماده است. در قیاس با توپی در محفظه اندازهگیری میانگین انرژی جنبشی هر توپی در یک ظرف داده شده است. در سطح مولکولی اتمها و مولکولها همه به لرزش در میآیند و به هم میخورند. با این حال شما نمیتوانید این حرکت را ببینید زیرا در مقیاس بسیار کوچکی اتفاق میافتد.
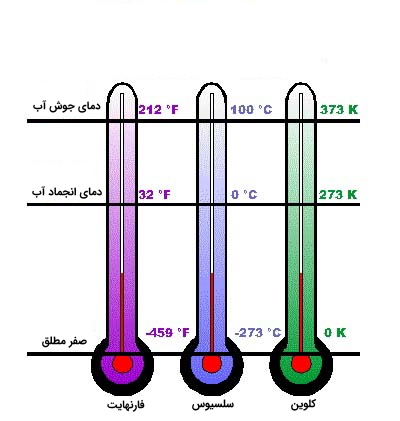
مقیاسهای معمول دما فارنهایت، سانتیگراد و کلوین هستند که کلوین استاندارد علمی است. مقیاس فارنهایت بیشتر در ایالات متحده دیده میشود. در این مقیاس آب در 32 درجه یخ میزند و در 212 درجه میجوشد. در مقیاس سانتیگراد که در اکثر نقاط دیگر دنیا رایج است آب در 0 درجه یخ میزند و در 100 درجه میجوشد. برای آشنایی بیشتر با نحوه تعریف واحدهای مختلف دما مطلب دماسنج چیست؟ را مطالعه کنید.

استاندارد علمی، مقیاس کلوین است. صفر در درجه کلوین برابر با درجه سانتیگراد است. چرا چنین گزینه عجیبی برای صفر کلوین وجود دارد؟ به نظر میرسد که این انتخاب عجیب که بسیار کمتر از مقدار صفر در مقیاس سانتیگراد است دمایی است که در آن تمام حرکات مولکولی متوقف میشود. صفر کلوین از نظر تئوری سردترین درجه حرارت ممکن است.
چگونه حرارت انتقال پیدا میکند؟
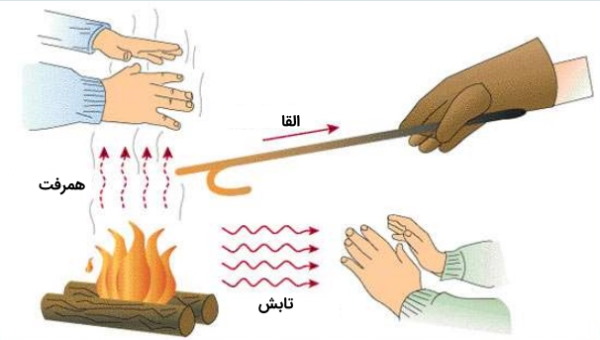
سه روش اصلی وجود دارد که با استفاده از آنها انرژی گرمایی از یک جسم به جسم دیگر منتقل میشود. این روشها عبارت از رسانایی، همرفت و تابش هستند.
هدایت هنگامی اتفاق میافتد که انرژی مستقیماً بین دو ماده در تماس حرارتی با یکدیگر منتقل شود. این نوع انتقال همان چیزی است که در مثال توپ پلاستیکی که بالاتر توضیح داده شد، اتفاق میافتد. هنگامی که دو جسم در تماس مستقیم هستند انرژی از طریق برخورد بین مولکولهای آنها منتقل میشود. این انرژی به آرامی از نقطه تماس با بقیه جسم که دمای کمتری دارند منتقل میشود تا تعادل گرمایی حاصل شود.
با این حال همه اشیا یا مواد از این طریق انرژی را به یک اندازه خوب هدایت نمیکنند. برخی از مواد به نام رساناهای حرارتی خوب، می توانند انرژی گرمایی را راحتتر نسبت به سایر مواد که عایقهای حرارتی خوبی هستند انتقال دهند.
شما در زندگی روزمره خود احتمالاً تجربه چنین رساناها و نارساناهای گرمایی را داشتهاید. در یک صبح سرد زمستانی، قدم گذاشتن با پای برهنه روی کف کاشی چگونه با قدم زدن با پای برهنه روی فرش مقایسه میشود؟ چیزی که شما تجربه میکنید این است که احتمالاً به نظر میرسد فرش به نوعی گرمتر است اما اینطور نیست. هر دو سطح احتمالاً دما یکسانی دارند اما کاشی رسانای حرارتی بسیار بهتری است. به همین دلیل باعث میشود که انرژی گرمایی خیلی سریعتر از بدن شما خارج شود.
همرفت نوعی انتقال گرما است که در گازها یا مایعات اتفاق میافتد. گازها و به میزان کمتری مایعات، با تغییر چگالی تغییرات دمایی را تجربه میکنند. سیالات معمولاً هرچه گرمتر باشند چگالی کمتری دارند.
به همین دلیل و به دلیل آزاد بودن حرکت مولکولهای موجود در گازها و مایعات، اگر قسمت پایین سیال گرم شود منبسط میشود و بنابراین به دلیل تراکم پایینتر مولکولها به سمت بالا میرود.
برای مثال اگر یک ظرف آب را روی اجاق گاز قرار دهید آب در ته دیگ گرم و منبسط میشود و با غرق کردن آب خنکتر به سمت بالا میآید. در ادامه این روند مجدداً آب خنک گرم و منبسط میشود و به سمت بالای ظرف حرکت میکند و این فرآیند متناوباً ادامه مییابد. در حقیقت در مثال ظرف روی اجاق گاز، جریانهای همرفت ایجاد میشوند که باعث میشود انرژی گرمایی از طریق مخلوط کردن مولکولهای درون سیستم در سیستم پراکنده شود، خلاف این حالت زمانی است که مولکولها در یک مکان باقی میمانند و تنها به جلو و عقب میروند.
به همین دلیل است که بخاریها اگر در کنار زمین قرار بگیرند برای گرم کردن خانه بهترین عملکرد را دارند. بخاریهایی که در نزدیکی سقف قرار میگیرند هوای نزدیک سقف را گرم میکنند و این هوا تقریباً در جای خود ثابت است.
شکل سوم انتقال گرما تابش است. تابش انتقال انرژی از طریق امواج الکترومغناطیسی است. اجسامی که گرم هستند میتوانند به صورت تابش الکترومغناطیسی انرژی بدهند، به عنوان مثال به همین صورت است که انرژی گرمایی خورشید به زمین میرسد. در حقیقت به محض تماس تابش خورشید با جسم دیگر، اتمهای آن جسم میتوانند این انرژی را جذب کنند.
برای مطالعه بیشتر در زمینه انتقال انرژی گرمایی و روشهای آن مطلب روشهای انتقال گرما را مطالعه کنید.
ظرفیت گرمایی ویژه یا گرمای ویژه
دو ماده مختلف با جرم یکسان با وجود اضافه شدن انرژی کل یکسان به دلیل تفاوت در مقداری به نام ظرفیت گرمایی ویژه یا گرمای ویژه، تغییرات دمایی متفاوتی را تجربه میکنند. ظرفیت گرمایی ویژه به ماده مورد نظر بستگی دارد و به طور معمول مقدار ظرفیت گرمایی ویژه یک ماده را توسط یک جدول ارائه میدهند.
به طور رسمی، ظرفیت گرمایی ویژه به عنوان مقدار انرژی گرمایی تعریف میشود که باید برای افزایش درجه حرارت تا یک درجه سانتیگراد در واحد جرم اضافه شود. واحدهای SI برای ظرفیت گرمایی ویژه، که معمولاً با c نشان داده میشود عبارت از است.
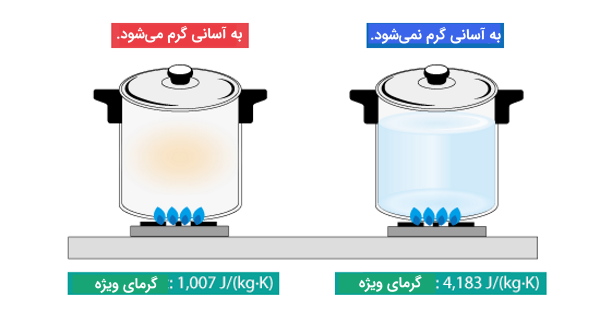
فرض کنید شما دو ماده مختلف دارید که وزن کاملاً یکسانی دارند و دقیقاً در یک دما هستند. ماده اول دارای ظرفیت گرمایی ویژه بالا و ماده دوم دارای ظرفیت گرمایی ویژه کم است. حال فرض کنید که شما به هر دوی آنها دقیقاً به یک میزان انرژی گرمایی بدهید. ماده اول، یعنی مادهای که ظرفیت گرمایی بالاتری دارد به اندازه ماده دوم افزایش دما نخواهد داشت.
ظرفیت گرمایی چیست؟
به مقدار گرمای لازم برای بالا بردن دمای جسمی به اندازه واحد، ظرفیت گرمایی میگوییم. به دست آوردن ظرفیت گرمایی ماده یا C از گرمای ویژه یعنی c بدین صورت است که گرمای ویژه را در جرم ضرب میکنیم و اطمینان حاصل کنیم که از واحدهای جرم مشابه در کل مسئله استفاده میشود. ظرفیت گرمایی به زبان ساده نشاندهنده توانایی جسم در برابر گرم شدن با افزودن انرژی گرمایی است. رابطه بین ظرفیت گرمایی و گرمای ویژه به صورت زیر بیان میشود:
ماده میتواند به صورت جامد، مایع یا گاز وجود داشته باشد. به عنوان مثال در گازها، ظرفیت گرمایی میتواند به فشار و دمای محیط بستگی داشته باشد. دانشمندان اغلب تمایل دارند که از ظرفیت گرمایی گاز در فشار ثابت مطلع شوند در حالی که سایر متغیرها مانند دما مجاز به تغییر هستند.
این کمیت به عنوان شناخته میشود. به همین ترتیب ممکن است تعیین ظرفیت گرمایی گاز در یک حجم ثابت یا مورد نیاز باشد. نسبت به اطلاعات خوبی در مورد خصوصیات ترمودینامیکی یک گاز ارائه میدهد.
ظرفیت گرمایی چه متغیری است؟
همانطور که گفته شد ظرفیت گرمایی و گرمای ویژه مقادیر مرتبط با یکدیگر هستند، اولی در واقع از دومی ناشی میشود. گرمای ویژه یک متغیر حالت است به این معنی که فقط مربوط به خصوصیات ذاتی یک ماده است و نه میزان جرم آن و بنابراین به صورت گرما در واحد جرم بیان میشود.
از طرف دیگر ظرفیت گرمایی بستگی به این دارد که چه مقدار از ماده مورد بحث تحت انتقال حرارت قرار میگیرد و یک متغیر حالت نیست.
همه مواد دارای درجه حرارتی مرتبط با ماده هستند. با این حال این کمیت ممکن است اولین چیزی نباشد که با مشاهده جسمی به ذهنتان خطور میکند اما در طول مسیر و آموزشهای علمی ممکن است یاد گرفته باشید که دانشمندان هرگز تحت هیچ شرایطی موفق به دستیابی به دمای صفر مطلق نشدهاند، هر چند به طرز عجیبی به آن نزدیک شدهاند.
حال سوال این است که چرا دانشمندان آنقدر در دستیابی به دمای صفر مطلق برای یک ماده تلاش میکنند. در حقیقت دلیل اینکه دانشمندان قصد رسیدن به چنین دمایی را دارند مربوط به خاصیت رسانایی بسیار بالای مواد بسیار سرد است. در حقیقت فقط به ارزش کاربردی یک هادی الکتریکی فیزیکی فکر کنید که عملاً هیچ مقاومتی ندارد.
دما به نوعی اندازهگیری حرکت مولکولهای یک جسم است . در مواد جامد مولکولها در یک شبکه یا ردیف مرتب شدهاند و حرکت مولکولها آزاد نیست. در مایع مولکولها آزادتر حرکت میکنند اما هنوز هم تا حد زیادی محدود هستند. در یک گاز مولکولها میتوانند بسیار آزادانه حرکت کنند. در هر صورت فقط این موضوع را به یاد داشته باشید که دمای پایین به معنای حرکت مولکولی کم در ماده است.
وقتی میخواهید جسمی از جمله خودتان را از مکانی فیزیکی به مکان دیگر منتقل کنید نیاز به صرف انرژی دارید و باید کار انجام دهید. شما باید بلند شوید و از اتاق عبور کنید، یا باید پدال گاز ماشین را فشار دهید تا سوخت را از طریق موتور آن جابهجا کرده و به ماشین نیرو وارد کند.
به همین ترتیب در سطحهای میکرو و خیلی کوچک نیز برای حرکت مولکولها نیاز است تا به سیستم انرژی وارد شود. اگر انرژی ورودی برای افزایش حرکت مولکولی کافی باشد بر اساس توضیحاتی که ارائه کردیم انرژی اضافی صرف افزایش دمای ماده میشود.
مواد متداول و مختلف دارای مقادیر مختلفی از گرمای ویژه هستند. به عنوان مثال در میان فلزات طلا گرمای ویژه طلا برابر با ژول بر گرم درجه سانتیگراد است. این کمیت به این معنی است که ژول گرما برای افزایش درجه حرارت 1 گرم طلا تا 1 درجه سانتیگراد نیاز است.
به یاد داشته باشید که این مقدار بر اساس مقدار طلا موجود تغییر نمیکند، زیرا جرم در مخرج واحد گرمای ویژه در نظر گرفته شده است. همان طور که در ادامه خواهید دید این موضوع در مورد ظرفیت گرمایی صدق نمیکند.
محاسبات مربوط به ظرفیت گرمایی
در اولین مواجهه ممکن است شگفت زده شوید که گرمای ویژه آب که مقدار آن ژول بر گرم درجه سانتی گراد یا است، به طور قابل توجهی بیشتر از فلزات معمولی است. همچنین ظرفیت گرمایی یخ نصف ظرفیت گرمایی آب است با اینکه فرمول شیمیایی هر دو است. این موضوع نشان میدهد که حالت یک ماده و نه تنها ترکیب مولکولی ماده، بر مقدار گرمای ویژه آن تأثیر میگذارد.
پرسش: مقدار گرمای مورد نیاز برای افزایش دمای ۵ درجه سلسیوس از 150 گرم آهن که گرمای ویژه دارد، چه قدر است؟
پاسخ: این محاسبه بسیار ساده است. گرمای ویژه c را در مقدار ماده و تغییر دما ضرب کنید و مقدار گرما به دست میآید. از آنجا که است، مقدار گرما برای این فرآیند برابر است با:
روش دیگر بیان این موضوع را میتوان بر حسب ظرفیت گرمایی بیان کرد. در حقیقت باید گفت که ظرفیت گرمایی 150 گرم آهن 67٫5 J است. این بیان چیزی بیشتر از این نیست که جرم ماده موجود را در گرمای ویژه ماده ضرب کرده و ظرفیت گرمایی را به دست میآوریم.
بدین ترتیب بدیهی است که حتی اگر ظرفیت گرمایی آب مایع در دمای مشخص ثابت باشد، برای گرم کردن یکی از دریاچههای بزرگ به اندازه یک دهم درجه، حرارت بسیار بیشتری تا گرم کردن یک پیمانه آب به میزان 1 یا 10 یا حتی 50 درجه لازم است.
نسبت بین به چیست؟
تا اینجا در مورد ظرفیت گرمایی شرطی یعنی مقدار گرمایی که در دما یا فشار ثابت به یک ماده خاص اعمال میشود، صحبت کردیم. همچنین دو معادله اساسی نیز به صورت و معرفی شدند.
از دو معادله اخیر میتوانید ببینید که روش دیگری که برای بیان تغییر در آنتالپی ممکن است به صورت زیر است:
اگرچه در این مطلب هیچ استدلالی برای این موضوع بیان نشده اما یکی از روشهای بیان اول قانون ترمودینامیک که در مورد سیستمهای بسته است و ممکن است به طور کلی شنیده باشید این است که انرژی نه ایجاد میشود و نه از بین میرود و این بیان به زبان ریاضی به صورت زیر نوشته میشود:
به زبان ساده این رابطه بدان معنی است که وقتی مقدار مشخصی از انرژی به یک سیستم از جمله گاز اضافه میشود و مجاز به تغییر حجم آن گاز نیست (ثابت بودن حجم توسط زیرنویس V در نشان داده شده است)، درجه حرارت آن باید به نسبت مستقیم و به مقدار ظرفیت گرمایی آن گاز افزایش یابد.
رابطه دیگری نیز در بین این متغیرها وجود دارد که استخراج ظرفیت گرمایی را در فشار ثابت به جای حجم ثابت امکان پذیر میکند. این رابطه روش دیگری برای توصیف آنتالپی است و داریم:
اگر در جبر مهارت داشته باشید میتوانید به یک رابطه مهم بین و برسید و داریم:
رابطه بالا نشان میدهد که ظرفیت گرمایی گاز در فشار ثابت بیشتر از ظرفیت گرمایی آن در حجم ثابت است و این فاصله توسط مقداری ثابت یعنی R که مربوط به خصوصیات خاص گاز مورد بررسی است نمایش داده میشود.
این کمیت یک حس شهودی دارد. اگر تصور کنید در پاسخ به افزایش فشار داخلی، گاز منبسط میشود احتمالاً میتوانید درک کنید که در پاسخ به یک انرژی اضافی معین، باید گرم شود تا اینکه در همان فضای محدود بماند.
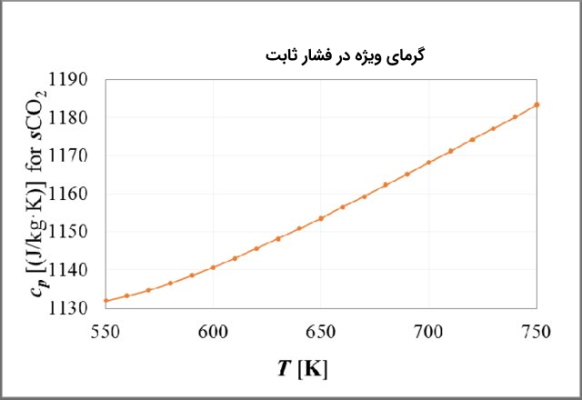
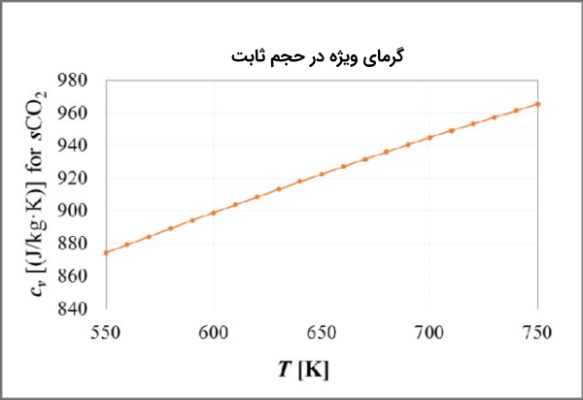
سرانجام میتوانید از تمام این اطلاعات برای تعریف متغیر خاص دیگری از ماده یعنی استفاده کنید که برابر با نسبت به است. از معادله قبلی میتوان دید که این نسبت برای گازهای با مقادیر بالاتر R افزایش مییابد.
و هوا
و هوا هر دو در مطالعه دینامیک سیالات مهم هستند زیرا هوا، متشکل از ازت و اکسیژن، متداولترین گازی است که انسان تجربه میکند. هر دو کمیت و وابسته به دما هستند ولی با این حال هر دو به یک اندازه به دما وابسته نیستند.
چیزی که اتفاق میافتد این است که با افزایش دما کمی سریعتر افزایش مییابد. این موضوع بدین معنی است که ثابت در واقع ثابت نیست، اما در طیف وسیعی از دماهای مورد بررسی مقدار نسبتاً ثابتی دارد.
به عنوان مثال در دمای 300 درجه کلوین که برابر با 27 درجه سانتیگراد است، مقدار برابر با 1٫400 است. همچنین در دمای 400 کلوین که برابر با 127 درجه سانتیگراد است و به طور قابل توجهی بالاتر از نقطه جوش آب است مقدار برابر با ۱٫۳۹۵ است.
ظرفیت گرمایی آب
سیستم آب و هوایی جهان بلافاصله و ناگهانی به تغییرات آب و هوایی واکنش نشان نمیدهد. این زمان و تأخیر باعث شده است که بحث در مورد تأثیر فعالیتهای انسانی بر آب و هوا بیشتر از آنچه که توسط نتایج آنی دیده میشود مورد بررسی قرار بگیرد.
به عنوان مثال وقتی مقدار مشخصی اضافی به اتمسفر اضافه شود اثرات گرم شدن هوا، زمین و اقیانوس مدتی طول میکشد تا کاملاً درک شود. حتی اگر راهی برای افزودن مستقیم گرما به زمین وجود داشته باشد، باز هم زمان لازم است تا دمایی که اندازه گیری میکنیم افزایش یابد. در این اینجا نشان میدهیم که چرا این تغییرات در سیستم آب و هوایی زمانی را نیاز دارند تا اثرات خود را نشان دهند.
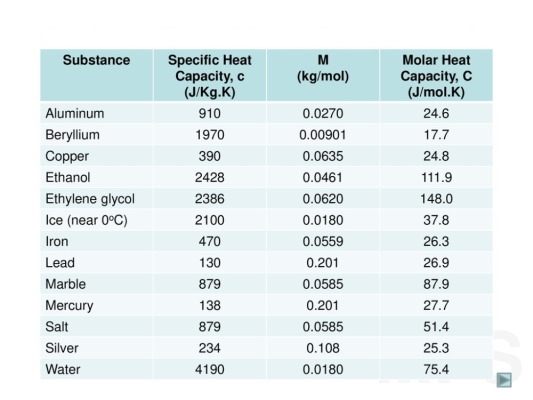
گرمای ویژه در فشار ثابت یعنی آب مایع در دما و فشار اتاق تقریباً 4/2 ژول بر گرم درجه سانتیگراد است. این بدان معنا است که برای بالا بردن 1 گرم یا 1 میلی لیتر آب به میزان 1 درجه سانتیگراد به 4/2 ژول انرژی نیاز است. این در واقع عددی بزرگ است. ظرفیت گرمایی ویژه بخار آب در دمای اتاق نیز از بیشتر مواد دیگر بالاتر است. در اینجا جدول ظرفیتهای ویژه گرمایی مواد مختلف روی زمین نشان داده شده است:
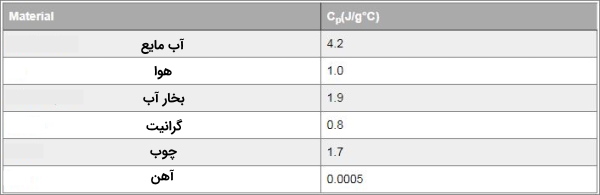
توجه داشته باشید که هیچ یک از مواد ذکر شده در جدول بالا در توانایی جذب گرما حتی نزدیک به آب نیستند.
بالای آب دلیل اصلی برای این موضوع است که تغییرات و دستکاری در جو با گذشت زمان نتایج مثبت یا منفی را نشان میدهند. در حقیقت گرمای ویژه بالای آب یک نکته مثبت است زیرا سبب میشود که اقیانوس توانایی جذب گرمای زیادی را قبل از افزایش قابل توجه دمای خود داشته باشد. نکته مهم این است که به محض حذف یک منبع خارجی انرژی، اقیانوس نیز به همان اندازه کند عمل میکند و دمای آن بلافاصله شروع به کاهش نمیکند.
ظرفیت گرمایی آب بر حسب کالری چه قدر است؟
ظرفیت گرمایی ویژه آب بر حسب کالری برابر با یک کالری بر گرم درجه سانتیگراد است. در حقیقت داریم:
رابطه ظرفیت گرمایی و انرژی سیستم
همان طور که میدانید انرژی گرمایی و تغییرات دمای یک جسم به صورت مستقیم با یکدیگر رابطه دارند و داریم:
که در این رابطه انرژی گرمایی، تغییرات دما، جرم و گرمای ویژه است. در قسمتهای قبل رابطه بین گرمای ویژه و ظرفیت گرمایی را بیان کردیم و نشان دادیم ظرفیت گرمایی برابر با حاصلضرب جرم در گرمای ویژه است. در نتیجه رابطه بین انرژی گرمایی و ظرفیت گرمایی به صورت زیر خواهد بود:
واحد ظرفیت گرمایی چیست؟
واحد گرمای ویژه ژول بر گرم درجه سانتیگراد است و با توجه به رابطه بین گرمای ویژه و ظرفیت گرمایی، واحد ظرفیت گرمایی ژول بر درجه سانتیگراد است.
ظرفیت گرمایی مواد مختلف چه قدر است؟
همان طور که گفتیم ظرفیت گرمایی ویژه مواد مختلف به ماهیت و حالت ماده بستگی دارد که در ادامه ما این کمیت را برای چند ماده مختلف معرفی میکنیم:
- ظرفیت گرمایی ویژه روغن زیتون:
- ظرفیت گرمایی ویژه اسید استیک:
- ظرفیت گرمایی آب دریا:
- ظرفیت گرمایی ویژه آب تازه:
- ظرفیت گرمایی ویژه روغن کنجد:
- ظرفیت گرمایی ویژه اسید سولفوریک:
- ظرفیت گرمایی ویژه جیوه:
- ظرفیت گرمایی ویژه مس:
- ظرفیت گرمایی ویژه بیسموت:
- ظرفیت گرمایی ویژه طلا:
جمعبندی
در این مطلب در مورد ظرفیت گرمایی صحبت کردیم. برای ورود به موضوع ظرفیت گرمایی ابتدا به صورت بسیار فشرده توضیحاتی در مورد گرما، دما، روشهای انتقال گرما و ظرفیت گرمایی ویژه بیان کردیم و سپس به تعریف ظرفیت گرمایی و ارتباط آن با ظرفیت ویژه گرمایی پرداختیم. همچنین در مورد ظرفیت گرمایی هوا و آب نیز توضیحاتی ارائه کردیم.




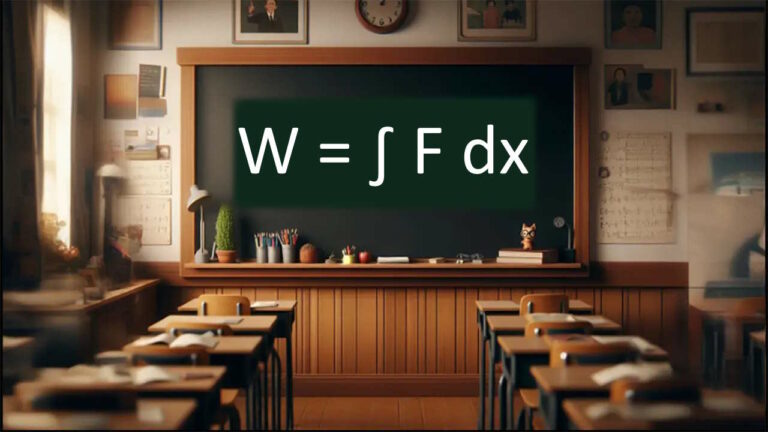



سلام ممکن است در مورد روابط انرژی گرمای محسوس و نهان توضیح دهید ؟
با سلام خدمت شما همراه گرامی؛
در این زمینه میتوانید مطلب «گرمای نهان چیست؟ – به زبان ساده» از مجله فرادرس یا فیلم آموزش رایگان «گرمای نهان چیست؟ + نحوه محاسبه با مثالهای کاربردی» را مشاهده نمایید.
از بازخورد و همراهی شما با مجله فرادرس سپاسگزاریم.
سلام و وقت بخیر.
نوشتید که ظرفبت گرمایی مقدار انرژی لازم برای بالا بردن دمای سیستم به اندازه درجه سلسیوس برای دقیقا یک گرم ماده است.
اما این توضیح گرمای ویژه است و جابه جا نوشتید.
با سلام،
متن بازبینی و اصلاح شد،
با تشکر از همراهی شما با مجله فرادرس
سپاسگزارم
سلام
میخواستم بدونم اگه چند مایع با ظرفیت گرمایی مختلف رو باهم مخلوط کنیم، ظرفیت گرمایی محلول نهایی چگونه محاسبه میشه
سلام وقت بخیر
عذر میخوام ، اگر در دو ظرف آب داشته باشیم که دمای متفاوتی دارن .میتونیم بگیم که ظرفیت گرمایی ویره دقیقا یکسانی دارند ؟
یعنی این جمله که” ظرفیت گرمایی ویژه به دما هم بستگی دارد” درست هست یا اشتباه؟
با سلام،
بر طبق آزمایشها انجام شده، ظرفیت گرمایی به سه عامل بستگی دارد:
۱. تغیرات دما
۲. جرم سیستم
۳. ماده و حالت آن
با تشکر از همراهی شما با مجله فرادرس
سلام تفاوت بين معادله Cp-Cv=nR , Cp-Cv=R چي هست و هدكدام در كجا استفاده ميشود ؟
سلام و روز شما به خیر؛
در پاسخ به سوال شما باید گفت که اگر Cp و Cv با حرف بزرگ یعنی C نمایش داده شوند، به ترتیب نمایش دهنده ظرفیت گرمایی ویژه مولی یک گاز ایده آل در حجم ثابت و ظرفیت گرمایی ویژه مولی یک گاز ایده آل در فشار ثابت هستند و داریم: (Cp−Cv=R). اما هنگامی که این دو کمیت با حرف کوچک یعنی c نوشته شوند، به ترتیب به ظرفیت گرمایی ویژه گاز در فشار ثابت و ظرفیت گرمایی ویژه گاز در حجم ثابت اشاره دارند و داریم: cp−cv=nR که n تعداد مول است.
از همراهی شما با فرادرس خرسندیم.
سلام. وقتتون بخیر. ببخشید من یه سوال در مورد ظرفیت گرمایی ویژه cp اکسید فلزاتی همچون اکسید آلومینیوم(آلومینا) و اکسید تیتانیوم(تیتانیا) همچنین شبه فلز سیلسیم دی اکسید(سیلیکا) داشتم. اعدادش رو نمیتونم پیدا کنم. میشه یه منبع برای پیدا کردن این اعداد در اختیار من قرار بدید؟ ظرفیت گرمایی ویژه فلزات بیشتره یا شبه فلزات؟