دیالیز در شیمی – به زبان ساده
دیالیز در شیمی، به جداسازی کلوییدها از یونهای محلول یا مولکولهای کوچک میگویند. همچنین این روش، از جمله روشهای جداسازی کریستالوئیدها در یک محلول به شمار میآید. کلوئید مادهای است که از ذرات بسیار ریزی درست شده و از اتمها بزرگتر باشد که اندازه این ذرات به طور معمول بین تا سانتیمتر است. یک کریستالوئید، مادهای است که به هنگام انحلال، یک محلول را میسازد و این محلول قادر است از میان غشاهای نیمهتراوا عبور کند. در نهایت، میتوان کریستالوئیدها را به کمک دیالیز از کلوئیدها جدا کرد.

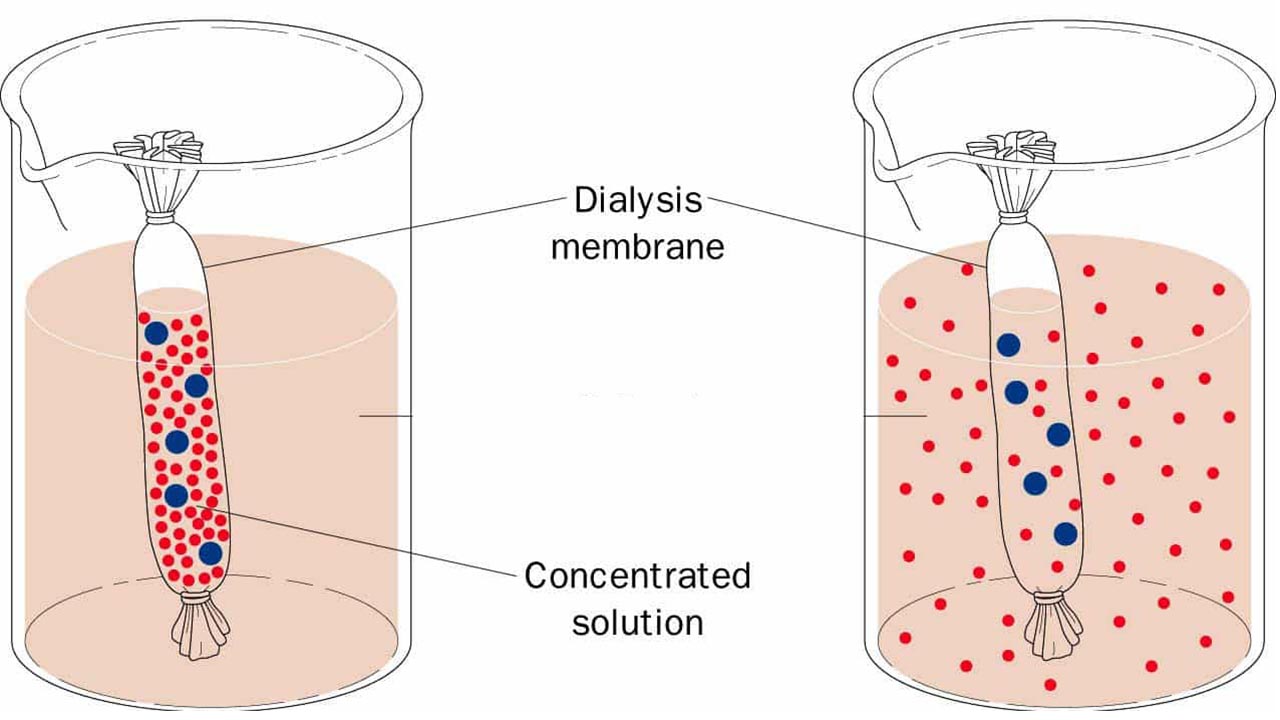
«دیالیز» (Dialysis)، یک روش آزمایشگاهی برای جداسازی مواد است که در پزشکی نیز کاربرد دارد. در متون علوم زیستی، بیشترین کاربرد دیالیز در حذف مولکولهای ناخواسته مانند نمکها، کاهندهها یا رنگها از مولکولهای بزرگتری همچون پروتئین، DNA یا پلیساکاریدها است.
مقدمه
در سال 1861، شیمیدانی به نام «توماس گراهام» (Thomas Graham)، از فرآیندی موسوم به دیالیز استفاده کرد. امکان انجام دیالیز به دلیل سرعت متفاوت «نفوذ» (Diffusion) از طریق یک غشای نیمهتراوا است. «غشای نیمهتراوا» (Semipermeable Membrane)، پوستهای است که اجازه عبور برخی از مولکولها را از میان خود میدهد.
برای اینکه تصور بهتری از یک غشای نیمهتراوا داشته باشید، میتوانید یک غربال (الک) را تصور کنید که اجازه عبور اجزای کوچکتر را از خود میدهد اما اجزای بزرگتر، اجازه عبور ندارند. زمانی که یک مخلوط کلوئیدی را داخل یک غشای نیمهتراوا بریزیم و سپس آنرا در داخل یک محلول آبی یا آب خالص قرار دهیم، یونهای محلول و مولکولهای کوچک، میتوانند از طریق این غشا عبور کنند. این کار سبب میشود تا اجزای کلوییدی داخل غشا باقی بمانند زیرا این اجزا امکان عبور از طریق حفرههای ریز داخل غشا را ندارند.

اساس دیالیز
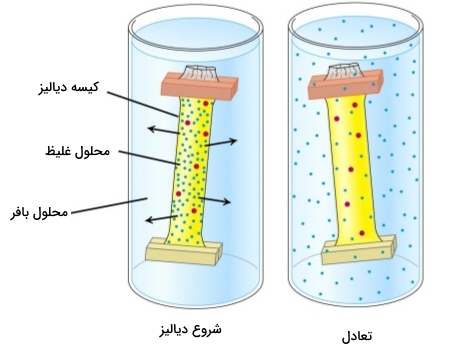
«نفوذ» (Diffusion)، حرکت تصادفی و «حرارتی» (Thermal) مولکولها در یک محلول است که به «حرکت براونی» (Brownian Motion)، موسوم است. این پدیده سبب میشود تا مولکولها از بخشی با غلظت بیشتر به بخشی با غلظت کمتر حرکت کنند. این حرکت تا زمان رسیدن به تعادل ادامه پیدا میکند. در فرآیند دیالیز، یک نمونه و یک محلول بافر موسوم به «دیالیزات» (Dialysate) به کمک یک غشای نیمهتراوا از یکدیگر جدا میشوند.
به دلیل «اندازه حفرات» (Pore Size) در غشا، مولکولهای درشت در نمونه، توانایی عبور از غشا را نخواهند داشت، در نتیجه، نفوذ آنها در محفظه نمونه محدود میشود. در مقابل، مولکولهای کوچک، آزادانه در طول غشا حرکت میکنند و در محلول به تعادل میرسند و غلظت کلی این مولکولها در دیالیزات و نمونه تغییر میکند. در حالت تعادلی، غلظت نهایی مولکول به حجم محلولهای نمونه و بافر وابسته است و اگر دیالیزات را با محلولی تازهتر عوض کنیم، عمل نفوذ به طور مجدد موجب کاهش غلظت مولکولهای کوچک در نمونه خواهد شد.
از این روش میتوان برای حذف یا اضافه کردن مولکولهای کوچک از نمونه بهره گرفت چراکه مولکولهای کوچک، آزادانه و در هر دو جهت در غشا حرکت میکنند. این امر سبب میشود تا دیالیز، کاربردهای بسیاری داشته باشد.
دستورالعمل انجام دیالیز در شیمی
جداسازی مولکولها در یک محلول و به کمک دیالیز، فرآیندی ساده است. به غیر از یک نمونه و محلول بافر (دیالیزات)، تمام آنچه که نیاز داریم عبارتست از:
- غشای دیالیزی در شکل مناسب مانند لوله، «کاست» (Cassette) و «کاتاف وزن مولکولی» (Molecular Weight Cut-off) مناسب
- محفظهای برای نگهداری دیالیزات
- امکانی برای همزدن محلول و کنترل دما
روش (دستورالعمل) کلی در دیالیز
دستورالعمل معمول دیالیز در نمونههای پروتئینی به صورت زیر است:
- آماده سازی غشا
- وارد کردن نمونه به لوله، کاست یا دستگاه
- قرار دادن نمونه در محفظه خارجی محلول بافر و همزدن آرام
- انجام دیالیز به مدت ۲ ساعت در دمای اتاق یا ۴ درجه سانتیگراد
- تعویض محلول بافر و انجام دیالیز برای دو ساعت دیگر
- تعویض مجدد محلول بافر و انجام دیالیز
حجم کلی نمونه و دیالیزات، غلظت تعادلی نهایی مولکولهای کوچک را در دو طرف غشا تعیین میکند. با استفاده از حجم مناسب دیالیزات و تغییرات متعدد محلول بافر، غلظت آلایندهها در نمونه را میتوان به یک مقدار قابل صرفنظر کاهش داد. به طور مثال، به هنگام دیالیز کردن ۱ میلیلیتر نمونه در برابر ۲۰۰ میلیلیتر دیالیزات، غلظت مواد دیالیزی به هنگام رسیدن به تعادل تا ۲۰۰ برابر کاهش مییابد. کافی است این دیالیز را دو مرحله دیگر انجام دهیم تا سطح آلایندگی به میزان برابر کاهش پیدا کند.
بهینهسازی فرآیند دیالیز
با اینکه دیالیز کردن یک نمونه به طور معمول، فرآیند سادهای است اما نمیتوان یک دستورالعمل کلی برای همه کاربردهای آن ارائه داد چراکه انجام این روش، وابسته به متغیرهایی است که در زیر آورده شدهاند:
- حجم نمونه
- اندازه مولکولهایی که باید جداسازی شوند.
- نوع غشا مورد استفاده
- هندسه غشا که بر «فاصله نفوذ» (Diffusion Distance) موثر است.
سرعت دیالیز
دیالیز، فرآیند سریعی نیست. سرعت دیالیز به سرعت متفاوت نفوذ بین کریستالوئیدها و کلوئیدها و اختلاف اندازه ذرات بستگی دارد. سرعت دیالیز را میتوان به کمک حرارت تغییر داد یا اینکه کریستالوئیدها را از طریق اعمال یک میدان الکتریکی، باردار کرد. به روش باردارکردن کریستالوئیدها، «الکترودیالیز» (Electrodialysis) میگویند. الکترودیالیز نوعی از دیالیز است که در آن، الکترودهایی در کنار غشای نیمهتراوا نصب میشوند. با این روش، یونهای مثبت از یک طرف غشا و یونهای منفی از طرف دیگر غشا عبور خواهند کرد که در نهایت موجب افزایش سرعت دیالیز میشود.
انواع دیالیز
آنچه که در خصوص دیالیز مطرح شد، استفاده از آن در علم شیمی بود اما این روش، کاربردهای بسیاری نیز در پزشکی دارد. از انواع دیالیز در پزشکی میتوان به همودیالیز، «دیالیز صفاقی» (Peritoneal Dialysis) و «هموفیلتراسیون» (Hemofiltration) اشاره کرد که در این بخش قصد داریم تا به صورت خلاصه، همودیالیز را توضیح دهیم.
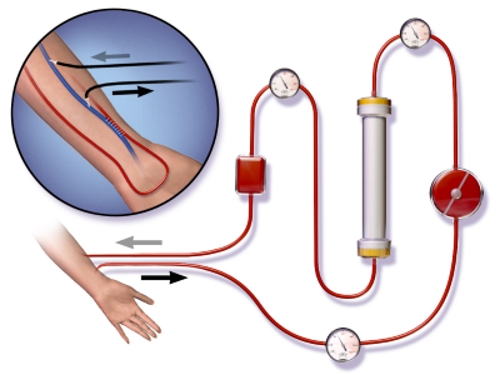
همودیالیز
همودیالیز روشی است که در درمان نارساییهای کلیه کاربرد دارد. در همودیالیز، خون را از بدن خارج، و پس از تصفیه به کمک دیالیز، آن را دوباره به بدن بازمیگردانند. در نارسائیهای کلیوی، نمکها، آب، اوره و اسیدهای متابولیکی از خون تصفیه نمیشوند. به طور معمول، بیمار را به یک دستگاه دیالیز متصل میکنند و خون از طریق کانالهای باریکی از غشاهای نیمهتراوا عبور میکند. مواد محلول مانند اوره و نمکها از میان یک محلول استریل عبور میکنند. ترکیباتی مانند شکر و آمینواسیدها را به این محلول استریل اضافه میکنند. محلول دیالیز، در طرف دیگر غشاها قرار دارند و مولکولها از طریق این غشاها جریان پیدا میکنند. این مولکولها از بخشی با غلظت پایینتر به بخشی با غلظت بالاتر نفوذ پیدا خواهند کرد. لازم به ذکر است در محلول دیالیز، غلظت مولکولهایی که باید از خون دفع شوند را صفر در نظر میگیرند.
اگر این مطلب برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای مهندسی شیمی
- آموزش مقدماتی غشا (Membrane) و فرآیندهای جداسازی غشایی
- فیلتراسیون در شیمی — از صفر تا صد
- الکترولیز — به زبان ساده
^^