تشکیل پیوند در ترکیبات کوئوردیناسیون – به زبان ساده
ترکیبات کوئوردیناسیون ترکیباتی هستند که در آنها لیگاند با جفت الکترون ناپیوندی به اتم مرکزی (معمولا فلزی) که دارای ظرفیت خالی است، متصل میشود. این ترکیبات که با نام کمپلکس نیز شناخته میشوند، میتوانند ترکیبات بسیار متعدد و کاربردی را با خواص فیزیکی و شیمیایی مختلف ایجاد کنند. تشکیل پیوند در ترکیبات کوئوردیناسیون از دو منظر نظریه پیوند والانس و نظریه میدان بلور با استفاده از ممان مغناطیسی لیگاند و شکافت اوربیتال اتم مرکزی بررسی میشود. در این مطلب از مجله فرادرس میآموزیم تشکیل پیوند در ترکیبات کوئوردیناسیون به چه شکل است.
- با روند تشکیل پیوند در ترکیبات کوئوردیناسیون آشنا میشوید.
- میآموزید نظریه پیوند والانس چیست و چگونه پیوند را تعریف میکند.
- می توانید انواع کمپلکس اوربیتال داخلی و خارجی را تعیین کنید.
- با نظریه میدان بلور و قوانین آن آشنا میشوید.
- روش شکافتگی اوربیتالهای d را در میدان هشتوجهی و چهاروجهی میشناسید.
- با هیبریداسیون انواع مختلف کمپلکس در فضای سهبعدی آشنا میشوید.


در ابتدای این مطلب، اصول اساسی تشکیل پیوند در ترکیبات کوئوردیناسیون را بررسی میکنیم. سپس این نحوه تشکیل پیوند را بر اساس نظریه پیوند والانس و نظریه میدان بلور بررسی میکنیم. در این مباحث، به بررسی ممان مغناطیسی لیگاندها، آرایش سه بعدی آنها، تغییرات هیبریداسیون کمپلکس و شکافتگی اوربیتالهای d اتم فلز مرکزی میپردازیم. در نهایت با بررسی بیشتر شکل و هیبریداسیون کمپلکسها، نحوه تشکیل پیوند در این ترکیبات را بهتر میآموزیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید تشکیل پیوند در ترکیبات کوئوردیناسیون به چه شکل است.
تشکیل پیوند در ترکیبات کوئوردیناسیون
ترکیبات کوئوردیناسیون در شیمی ترکیباتی هستند که در آنها یک اتم عموما فلزی به چند لیگاند متصل شده است. این نوع پیوند، که گاهی به آن پیوند داتیو یا پیوند لوئیس نیز گفته میشود، با پیوندهای یونی یا کووالانسی ساده متفاوت است و ویژگیهای فیزیکی و شیمیایی منحصر به فردی به کمپلکسها میدهد.
اتمهای فلزی عموما اوربیتالهای d نیمهپر در ساختار الکترونی خود دارند و این خاصیت، ظرفیت مناسب را برای اتصال لیگاندهایی که الکترون اضافی دارند، فراهم میکنند. ترکیباتی که دارای جفت الکترونهای غیرپیوندی هستند مانند هالوژنها، یون سیانید، گروه آمین و .. میتوانند به عنوان لیگاند عمل کنند. ساختار چهار نوع لیگاند در تصویر زیر رسم شده است.
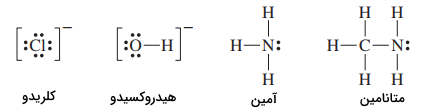
با نزدیک شدن لیگاندها به اتم مرکزی، تغییراتی در ساختار الکترونی اتم مرکزی به وجود میآید. این ساختارها معمولا تحت اثر میدان مغناطیسی لیگاند تغییر کرده و به سطوح انرژی مختلفی شکافته میشوند. همچنین، با اندازهگیری ممان مغناطیسی ترکیبات میتوان به نوع هیبریداسیون و تشکیل پیوند در آنها پی برد. بنابراین، تشکیل پیوند در ترکیبات کوئوردیناسیون معمولا از دو منظر نظریه پیوند والانس و نظریه میدان بلور برسی میشود. در ادامه این موارد را بررسی میکنیم.
عدد کوئوردیناسیون
عدد کوئوردیناسیون تعداد لیگاندهایی است که به اتم مرکزی متصل هستند. اعداد کوئوردیناسیون معمولا مقادیری بین ۲ تا ۹ دارند. تعداد لیگاندهای متصل به فلز بیشتر نیز در برخی از ترکیبات دیده شده است. تعداد لیگاندهای متصل به اتم فلز مرکزی به عواملی مانند اندازه، بار و آرایش الکترونی یون فلزی بستگی دارد. بیشتر یونهای فلزی بیشتر از یک عدد کوئوردیناسیون دارند.
فلز مرکزی و نقش آن
فلز مرکزی معمولا یک فلز واسطه است، که در بلوک d جدول تناوبی قرار دارد، هرچند برخی فلزات اصلی نیز میتوانند کمپلکس تشکیل دهند. ویژگیهای کلیدی فلز مرکزی عبارتاند از:
- ظرفیت پذیرش جفت الکترون آزاد (اکتت ناقص)
- چند ظرفیتی بودن، یعنی توانایی تشکیل پیوندهای متعدد با لیگاندها
- امکان ایجاد هندسههای مختلف (تتراهدرال، اکتاهدرال، مربعی مسطح و غیره)
فلز واسطه به دلیل داشتن اوربیتالهای d نیمهپر، ظرفیت بالایی برای جذب لیگاندها دارد و این مسئله اساس تشکیل کمپلکسهای پایدار است. همچنین، خواص مغناطیسی، رنگ و واکنشپذیری کمپلکسها عمدتا ناشی از فلز مرکزی و ترتیب اوربیتالهای d آن است.
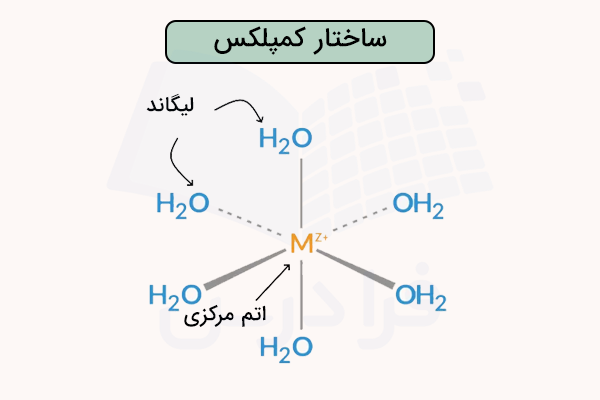
لیگاندها و انواع آن ها
لیگاندها مولکولها یا یونهایی هستند که یک یا چند جفت الکترون آزاد برای اهدا به فلز دارند. لیگاندها میتوانند ساده مانند آب، آمونیاک یا یون کلرید، یا پیچیده مانند اتیلندیآمین (en) و EDTA باشند.
اگر تا این قسمت از مطلب را مطالعه کردهاید با تشکیل پیوند در ترکیبات کوئوردیناسیون و مفاهیم پایه آن آشنا شدهاید. در ادامه نیز بیشتر این مفاهیم را بررسی میکنیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
لیگاندها بر اساس تعداد نقاط اتصال خود به فلز، به دستههای زیر تقسیم میشوند:
- تک دندانه: لیگاندهایی که یک جفت الکترون آزاد دارند و تنها یک پیوند با فلز تشکیل میدهند، مانند آمونیاک.
- دو دندانه: لیگاندهایی که دو جفت الکترون آزاد دارند و میتوانند دو پیوند همزمان با فلز برقرار کنند، مانند اتیلن دی آمین.
- چند دندانه: لیگاندهایی که چندین جفت الکترون آزاد دارند و میتوانند چند پیوند همزمان با فلز برقرار کنند، مانند EDTA.
نظریه پیوند والانس
نظریه پیوند والانس (Valence Bond Theory) که اولین بار توسط لینوس پاولینگ ارائه شد، بر اساس همپوشانی بین اوربیتالهای هیبریدی اتم مرکزی در کمپلکس و لیگاندهای آن تعریف میشود. نظریه پیوند والانس مکمل نظریه میدان بلور است و بر طبیعت کووالانسی پیوند فلز - لیگاند تمرکز دارد. این نظریه توضیح میدهد که چگونه اوربیتالهای فلز و لیگاندها همپوشانی پیدا میکنند و کمپلکس پایدار تشکیل میدهند. برای مثال اگر یک کمپلکس هشت وجهی داشته باشیم، ۶ اوربیتال هیبریدی در هیبریداسیون این ترکیب شرکت کرده است. هیبریداسیون چنین ترکیبی است.
در نظریه پیوند والانس، اگر بتوانیم ممان مغناطیسی یک کمپلکس را داشته باشیم، میتوانیم توزیع الکترون در اوربیتالهای d اتم مرکزی و نحوه تشکیل پیوند در ترکیب کوئوردیناسیون را داشته باشیم. پیشنهاد می کنیم برای درک بهتر شیمی ترکیبات کوئوردیناسیون و نظریههای مربوط به آنها، فیلم آموزش شیمی ترکیبات کوئوردینانسیون در شیمی معدنی ۲ که لینک آن در ادامه آورده شده است را مشاهده کنید.
برای درک بهتر این نظریه در تعیین نحوه تشکیل پیوند در ترکیات کوئوردسناسیون، به مراحل زیر دقت کنید.
مراحل تشکیل پیوند در نظریه پیوند والانس
روش تشکیل پیوند در ترکیبات کوئوردیناسیون بر پایه چهار اصل هیبریداسیون اوربیتالهای اتم فلز مرکزی، همپوشانی اوربیتالهای اتم مرکزی با لیگاند، تعیین هندسه مولکول بر اساس هیبریداسیون و پایداری کمپلکس تعریف میشود. این موارد در ادامه توضیح داده شده است.
- هیبریداسیون اوربیتالهای فلز: فلز مرکزی اوربیتالهای s, p و d خود را هیبرید میکند تا تعداد و شکل اوربیتالهای مناسب برای لیگاندها ایجاد شود.
- همپوشانی اوربیتالها با لیگاندها: هر لیگاند با جفت الکترون خود، با یک اوربیتال هیبرید فلز همپوشانی میکند و یک پیوند کوئوردیناسیون تشکیل میدهد.
- تعیین هندسه کمپلکس: نوع هیبریداسیون، هندسه کمپلکس را مشخص میکند.
- پایداری کمپلکسها: لیگاندهای چنددندانه (chelating) باعث افزایش همپوشانی و اثر چنگالی میشوند و لیگاندهای قوی (مثل CN یا CO) اوربیتالهای فلز را به خوبی پر میکنند و کمپلکس پایدارتر میشود.

مثال
ترکیب را در نظر بگیرید. عدد اتمی کبالت ۲۷ است و آرایش الکترونی آن به ختم میشود. کبالت ۳+ به آرایش الکترونی ختم میشود. بنابراین این ترکیب ۴ الکترون منفرد خواهد داشت.
اگر با این ۴ الکترون مقدار ممان مغناظیسی ترکیب را محسابه کنیم، عددی در حدود ۴٫۹ به دست میآید. بنابراین آرایش الکترونی با ممان مغناطیسی قابل پیشبینی است.
انواع کمپلکس بر اساس پیوند والانس
در قسمت قبل آموختیم که تشکیل پیوند در ترکیبات کوئوردیناسیون را میتوان با استفاده از محاسبه ممان مغناطیسی اتم مرکزی در ترکیبات کمپلکس پیشبینی کرد. بر اساس آرایش الکترونی اتم مرکزی و الکترونهای به اشتراک گذاشته شده در اوربیتالها میتوانیم دو نوع کمپلکس اوربیتال داخلی و خارج داشته باشیم.
این موارد به شکل زیر تعریف میشوند:
- کمپلکس اوربیتال داخلی: اگر اوربیتالهای d داخلی در هیبریداسون شرکت کرده باشند (مانند 3d)
- کمپلکس اوربیتال خارجی: اگر اوربیتالهای d خارجی در هیبریداسیون شرکت کرده باشند. (مانند 4d و 5d)
برای مثال، اگر آرایش 5d را در نظر بگیریم، دو حالت میتواند اتفاق بیافتد. حالت اول حالتی است که در آن کمپلکس کم اسپین بوده و ۵ الکترون اوربیتال d به صورت دو جفت الکترون و یک اتم تک در آن قرار دارند. اگر این آرایش مربوط به اتم مرکزی بوده و ۶ جفت الکترون لیگاند بخواهند به آن متصل شوند، از اوربیتالهای خالی 3d و 4s و 4p استفاده شده و هیبریداسیون آن خواهد بود. در این حالت از اوربیتال داخلی 3d استفاده شده است.
در حالت دوم، اگر کمپلکس یک کمپلکس پر اسپین باشد و ۵ الکترون اوربیتال d به شکل منفرد در اوربیتالهای d پخش شده باشند، ۶ لیگاند متصل شونده باید اوربیتالهای 4s و 4p و 4d اتم مرکزی را پر کنند. بدین ترتیب یک کمپلکس اوربیتال خارجی تشکیل خواهد شد. این دو حالت در تصویر زیر مشخص شدهاند.
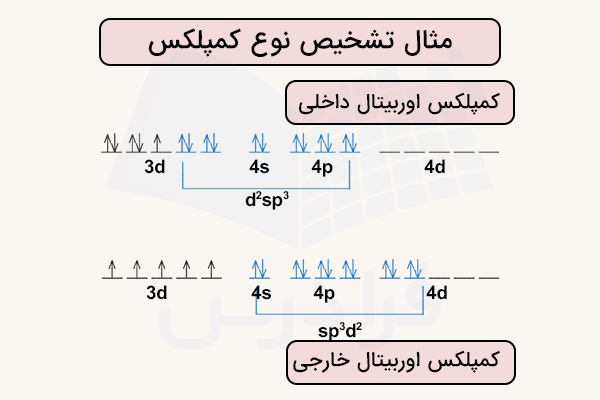
تشخیص نوع کمپلکس
با استفاده از آرایش الکترونی اتم مرکزی، میتوان نوع کمپلکس اوربیتال داخلی یا خارجی بودن آن را تشخیص داد. برای مثال در اتمی مانند اوربیتالهای 3d خالی وجود دارند که میتواند با الکترونهای لیگاند پر شود. بدین ترتیب یک کمپلکس اوربیتال داخلی تشکیل میدهد.
همچنین، اثر لیگاند نیز در نوع تشکیل پیوند در ترکیبات کوئوردیناسیون تاثیرگذار است. اگر لیگاند اتصلی یک لیگاند با میدان ضعیف باشد، الکترونهای اتم مرکزی به صورت جفت نشده باقی مانده و اوربیتالهای خارجیتر در دسترس لیگاندها خواهند بود. بدین ترتیب کمپلکسهای اوربیتال خارجی تشکیل میشوند.
در مقابل، اگر لیگاندها، میدان مغناطیسی قوی داشته باشند، الکترونهای ظرفیت اتم مرکزی جفت شده و اوربیتالهای داخلی ممکن است در دسترس لیگاندها قرار گیرند و کمپلکس یک کمپلکس اوربیتال داخلی را تشکیل دهد. دو مثال از این موارد را در تصویر زیر برای ترکیبات و نمایش داده شده است.
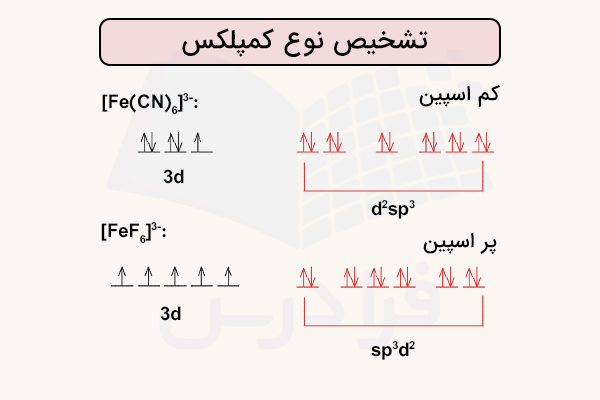
مثال نظریه پیوند والانس
برای درک بهتر نحوه تشکیل پیوند در ترکیبات کوئوردیناسیون طبق نظریه پیوند والانس، به دو ترکیب و دقت کنید. در این دو ترکیب ۴ لیگاند وجود داشته و اتم مرکزی از یک نوع است با این حال، سیانید یک لیگاند با میدان قوی بوده و الکترونهای اتم مرکزی را جفت میکند و بدین ترتیب کمپلکس یک مسطح مربع دیامغناطیسی با اوربیتالهای داخلی خواهد بود.
در مقابل کلر لیگاندی با میدان ضعیفتر است که میتواند الکترونهای نیکل را جفت کند. در نتیجه، لیگاندها از اوربیتالهای خارجی استفاده کرده و شکل کمپلکس یک چهاروجهی پارامغناطیسی خواهد بود. در ممان مغناطیسی برابر با ۲٫۸ است.
یادگیری شیمی معدنی با فرادرس
برای درک بهتر نحوه تشکیل پیوند در ترکیبات کوئوردیناسیون و کمپلکس، نیاز است ابتدا با مفاهیمی چون هیبریداسیون، آرایش الکترونی، اصل آفبا، میدان مغناطیسی، انواع پیوند و ساختار فلزات و بلورها آشنا شویم. پیشنهاد میکنیم برای درک بهتر این مفاهیم و مسائل، به مجموعه فیلم آموزش شیمی از دروس دانشگاهی تا کاربردی فرادرس مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است میتوانید به آموزشهای بیشتری در زمینه تشکیل پیوند در ترکیبات کوئوردیناسیون دسترسی داشته باشید.
- فیلم آموزش شیمی آلی فلزی جامع و کاربردی فرادرس
- فیلم آموزش شیمی تجزیه ۱ با نکات کاربردی فرادرس
- فیلم آموزش شیمی تجزیه پیشرفته با نکات کاربردی فرادرس
نظریه میدان بلور
نظریه میدان بلور (Crystale Field Therory) بر اساس در نظر گرفتن لیگاندها به عنوان نقاط باردار منفی و اتم مرکزی به عنوان نقطه باردار مثبت تعریف میشود. در این نظریه، نیروی بین لیگاندها و اتم مرکزی از نوع نیروی الکترواستاتیک (یونی) تعریف میشود. این نظریه انرژی اوربیتالهای d فلز را هنگام نزدیک شدن لیگاندها بررسی میکند. لیگاندها به عنوان بارهای منفی یا جفتهای الکترون، باعث شکاف انرژی در اوربیتالهای d میشوند که این شکاف تعیینکننده خواص مغناطیسی و رنگ کمپلکس است.
این نظریه بیان میکند که با نزدیک شدن لیگاندها به اتم مرکزی، یک دافعه الکترواستاتیکی بین الکترونهای لایه ظرفیت اتم مرکزی ایجاد میشود. به این نیروی وارد شده، نیروی میدان بلور گفته میشود. اگر میدان ایجاد شده طی نزدیک شدن لیگاندها به اتم مرکزی به شکل کروی باشد، سطح انرژی اوربیتالهای اتم مرکزی (به صورت همتراز) بالا رفته و در تقارنهایی پایینتر از کروی مانند میدان هشت وجهی، اوربیتالها در میدان بلوری شکافته میشوند.
این دو تغییر انرژی در تصویر زیر نمایش داده شده است.
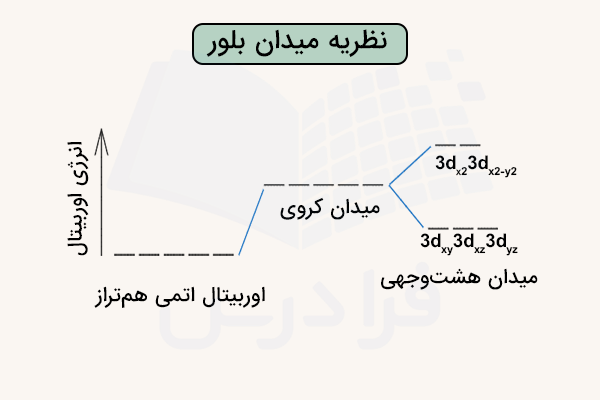
در نظریه میدان بلور، پیوند فلز و لیگاند به صورت الکترواستاتیک توضیح داده میشود و فرض میشود اوربیتالهای فلز پذیرنده و جفت الکترون لیگاند هیچ همپوشانی کووالانسی ندارند. اما این نظریه میتواند هندسه کمپلکس را پیشبینی کرده، تفاوت رنگ کمپلکسها را توضیح داده و اثر لیگاند و قدرت آن را مشخص کند.
شکافتگی اوربیتالها در میدان هشت وجهی
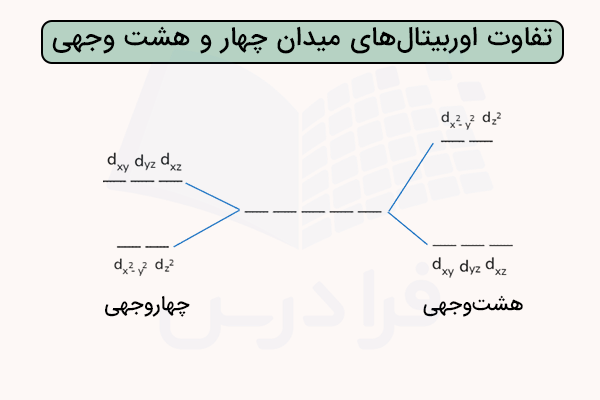
در قسمت قبل آموختیم که اگر میدان بلور به شکل کروی باشد، تنها انرژی اوربیتالهای همتراز بالا میرود. اما اگر اتم مرکزی تحت میدان هشتوجهی قرار بگیرد، اوربیتالهای اتمی هشتوجهی شکافته میشوند. در ساختار هشت وجهی به دلیل اینکه لیگاندها در راستای سه محور مختصات به اتم مرکزی نزدیک میشوند، دو اوربیتال و در تراز انرژی بالاتر و سه اوربیتال و و در تراز انرژی پایینتری قرار میگیرند.
اوربیتال دوتایی و با نام و اوربیتال سهتایی و و با نام شناخته میشود. فاصله بین این دوتراز انرژی برابر با (Dq) ۱۰ است. اوربیتال به اندازه (Dq) ۶ بالاتر و اوربیتال به اندازه (Dq) ۴ پایینتر از سطح انرژی اتم در میدان کروی قرار دارند. پیشنهاد میکنیم برای آشنایی بیشتر با انواع این ترکیبات و نوع میدان ایجاد شده توسط لیگاندها، مطلب ترکیبات کوئوردیناسی مجله فرادرس را مطالعه کنید.
شکل اوربیتالها در میدان هشت وجهی
در قسمت قبل آموختیم نحوه تشکیل پیوند در ترکیبات کوئوریناسیون طبق نظریه میدان بلور در میدان هشت وجهی به چه شکل است. درک دلیل شکافتگی اوربیتالهای d با مشاهده شکل این اوربیتالهای در فضای سه بعدی راحتتر انجام میشود. شکل اوربیتالهای d در فضای سه بعدی در تصویر زیر آورده شده است.
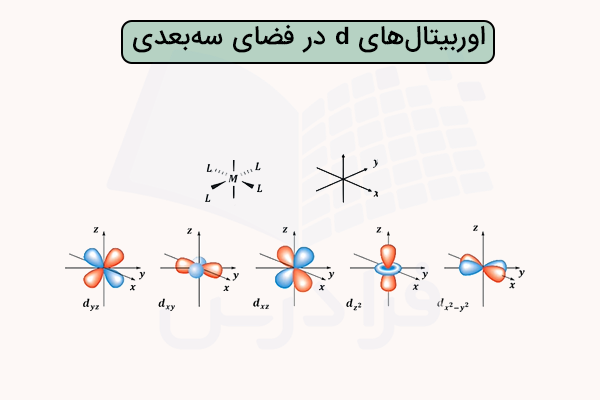
همانطور که مشاهده میکنید دو اوربیتال و در فضای سهبعدی، عمود و هم راستا با محور z مختصات قرار دارند. این اوربیتالها به دلیل دافعه الکترونی بیشتر در این راستا، در تراز انرژی بالاتری نسبت به سه اوربیتال d دیگر قرار میگیرند.
شکافتگی اوربیتالها در میدان چهار وجهی
در قسمتهای قبل آموختیم نحوه تشکیل پیوند در ترکیبات کوئوردیناسیون با آرایش هشت وجهی به چه شکل است. در کمپلکس چهاروجهی عدد کوئوردیناسیون برابر با ۴ است. تشکیل کمپلکس چهاروجهی به دلیل متفاوت بودن جهت نزدیک شدن لیگاندها به اتم مرکزی مقداری متفاوت است.
بر اساس نظریه میدان بلور، با نزدیک شدن لیگاندها به یون اتم مرکزی، یک شکافتگی در اوربیتالهای آن به وجود میآید و سطوح انرژی این اوربیتالها بسته به جهتگیری فضایی لیگاند تغییر میکند. در میدان چهار وجهی اوربیتالهای d به دو تراز e و شکافته میشوند. اوربیتالهای و به دلیل همجهت نبودن با لیگاندها، از انرژی پایینتری برخوردارند. مقدار فاصله این دو سطح انرژی در میدان چهاروجهی، برابر با میدان هشت وجهی است.
شکافتگی اوربیتالها در میدان مسطح مربع
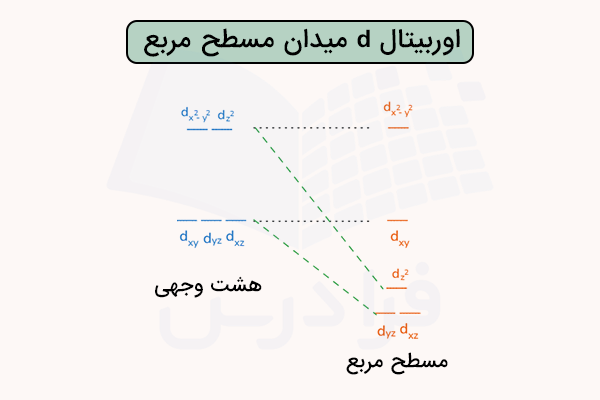
در میدان مسطح مربع، در راستای محور z لیگاندی به اتم مرکزی نزدیک نمیشود و اوربیتالها به ۴ سطح انرژی شکافته میشوند. در این میدان، لیگاندها در راستای مثبت و منفی محورهای x و y به اتم مرکزی نزدیک میشوند. به همین دلیل، سطح انرژی اوربیتال (با نام اوربیتال ) از سایر اوربیتالها بیشتر است. پس از آن اوربیتال (با نام اوربیتال ) بیشترین انرژی را دارد.
سپس اوربیتال (با نام اوربیتال ) بیشترین انرژی و در نهایت دو اوربیتال و (با نام اوربیتال ) پایینترین سطوح انرژی را دارند. این سطوح انرژی در تصویر زیر مشخص شدهاند.
نام گذاری اوربیتالها در میدان بلور
در قسمتهای قبل آموختیم نحوه تشکیل پیوند در ترکیبات کوئوردیناسیون در نظریه میدان بلور چگونه تعریف میشود. بر اساس شکل هندسی هر یک از اوربیتالهای اتمی موجود در اتم مرکزی، نامی به آنها اختصاص داده شده است تا بررسی و مطالعه انواع پیوند و هیبریداسیون آنها راحتتر باشد. در ادامه، نحوه نامگذاری این اوربیتالها معرفی شده است.
- اگر اوربیتال اتمی در نتیجه چرخش حول محور دوران اصلی متقارن بوده و به اوربیتال دیگری تبدیل نشود، با نام اوربیتال a نمایش داده میشود.
- اگر اوربیتال اتمی در نتیجه چرخش حول محور دوران اصلی ضدمتقارن بوده و به اوربیتال دیگری تبدیل نشود، با نام اوربیتال b نمایش داده میشود.
- اگر دو اوربیتال از نظر انرژی همتراز باشند با نام e مشخص میشوند.
- اگر سه اوربیتال از نظر انرژی با هم همتراز باشند با نام t نمایش داده میشوند.
همچنین بسته محور تقارن فرعی C2 نیز نامگذاری اوربیتال میتواند نمادهای دیگری نیز باشد که در ادامه توضیح داده میشود.
- اگر یک محور C2 بر محور اصلی عمود باشد، و اوربیتال نسبت به آن متقارن باشد، زیروند ۱ میگیرد.
- اگر محوی C2 بر محور اصلی عمود باشد، و اوربیتال نسبت به آن ضدمتقارن باشد، زیروند ۲ میگیرد.
- اگر اوربیتال نسبت به صفحه تقارن افقی متقارن باشد با علامت پرایم «'» مشخص میشود.
- اگر اوربیتال نسبت به صفحه تقارن افقی ضدمتقارن باشد با علامت دبلپرایم «''» مشخص میشود.
- اگر اوربیتال نسبت به مرکز تقارن اصلی متقارن باشد با علامت «g» مشخص میشود.
- اگر اوربیتال نسبت به مرکز تقارن اصلی ضدمتقارن باشد با علامت «u» مشخص میشود.
به همین دلیل است که اوربیتال دوتایی و با نام و اوربیتال سهتایی و و با نام شناخته میشود.
جدول هیبریداسیون ساختاری کمپلکس
برای درک بهتر نحوه تشکیل پیوند در ترکیبات کوئوردیناسیون، جدولی در ادامه برای نمایش هیبریداسیون، شکل هندسی، عدد کوئوردیناسیون، اوربیتالهای هیبریدی و مثالی از هر نوع ساختار ارائه شده است.
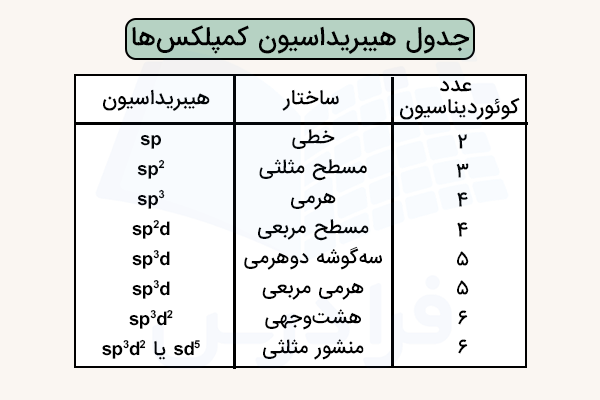
با تمرین و درک هر یک از این ساختارها و بررسی هیبریداسیون و ساختار آرایش الکترونی اتم مرکزی و لیگاندهای آنها میتوانید به شکلی عمیقتر بیاموزید تشکیل پیوند در ساختارهای کوئوردیناسیون چگونه انجام میشود.












