اصطلاحات کروماتوگرافی گازی – به زبان ساده
در آموزشهای قبلی، در خصوص روشهای جداسازی مواد از جمله کروماتوگرافی صحبت کردیم. علاوه بر این، به طور جداگانه، کروماتوگرافی گازی را مورد بررسی قرار داریم. اما آنچه که برای آشنایی پایهای با کروماتوگرافی گازی به آن نیاز داریم، دانشی در خصوص اصطلاحات کروماتوگرافی گازی و تعاریف پایه آن است. در این بخش با اصطلاحات کروماتوگرافی گازی آشنا خواهیم شد که به طور معمول برای درک مفاهیم این دانش کاربرد دارد.

لزوم آشنایی با اصطلاحات کروماتوگرافی گازی
همواره، درک مفاهیم پایه از جمله موارد ضروری برای بکارگیری موثر یک دانش عملی است. این امر در خصوص کروماتوگرافی گازی نیز صدق میکند چراکه با دانستن برخی مفاهیم پایه و اصلی، میتوان تحلیل بهتری از یک نمودار ارائه داد. آشنایی با اصطلاحات کروماتوگرافی گازی هم از جمله مواردی است که برای دانشجویان و افرادی که به تازگی با این علم آشنا شدهاند، میتواند بسیار مفید و در درک این علم تاثیرگذار باشد.
ثابت توزیع
از جمله اصطلاحات کروماتوگرافی گازی ثابت توزیع است. «ثابت توزیع» (Distribution Constant) را با نشان میدهند و به عنوان یک عامل کنترلی در تعادل بین حلشونده و فاز ساکن در نظر گرفته میشود. ثابت توزیع را به صورت غلظت حلشونده در فاز ساکن تقسیم بر غلظت آن در فاز متحرک تعریف میکنند و رابطه آن به شکل زیر است:
این ثابت، مقداری ترمودینامیکی و وابسته به دما است. ثابت توزیع، تمایل نسبی یک حلشونده برای توزیع خود بین دو فاز را بیان میکند. تفاوتها در ثابت توزیع موجب ایجاد سرعتهای حرکت (مهاجرت) دیفرانسیلی حلشونده از میان ستون کروماتوگرافی گازی میشود. هرقدر مقدار این عبارت، بزرگتر باشد، حلشونده بیشتری به فاز ساکن جذب میشود و عبور آن از ستون، دشوارتر خواهد بود.
تعادل و کروماتوگرافی گازی
با توجه به اینکه اصطلاحات کروماتوگرافی گازی شامل ثابت تعادل هم میشوند، ممکن است که این تصور پیش بیاید که کروماتوگرافی، نوعی فرآیند تعادلی است، در حالی که چنین چیزی صحت ندارد چراکه در حقیقت، مولکولهای حلشونده در طول ستون به کمک فاز متحرک، حرکت داده میشوند. البته در صورتیکه انتقال جرم سریعی داشته باشیم، یک سیستم کروماتوگرافی همانند یک سیستم تعادلی عمل خواهد کرد و ثابت توزیع نیز معنای بهتری پیدا میکند.
برهمکنش اجزا در کروماتوگرافی گازی
فرض دیگری که در خصوص کروماتوگرافی مطرح میشود آن است که حلشونده با خود برهمکنشی انجام نمیدهد یعنی مولکولهای حلشونده به گونهای از ستون کروماتوگرافی عبور میکنند که گویی هیچ حلشونده دیگری حضور ندارد. این فرض درستی است چراکه مواد با غلظتهای پایینی در ستون حضور پیدا میکنند و این مواد با گذر از داخل ستون، از یکدیگر به طور مداوم جدا خواهند شد. اگر این فرض محقق نشود، نتایج حاصل با نتایج نظری منطبق نمیشوند و این امر بر شکل پیکها و حجمهای بازداری تاثیرگذار خواهد بود.
نمودار کروماتوگرافی
برای بیان اصطلاحات کروماتوگرافی گازی بهتر است تا درک صحیحی از یک نمودار کروماتوگرافی گازی داشته باشیم. نمودار زیر، کروماتوگرامی کلی را برای حلشونده نشان میدهد که یک پیک اضافی در ابتدای آن ظاهر شده است. حرکت حلشوندههایی همچون A در ستون توسط «حجم بازداری» (Retention Volume) یا توصیف میشود. در نمودار زیر، به صورت فاصله از نقطه تزریق تا پیک ماکزیمم نشان داده شده است.
این مقدار، حجم گاز حاملی را نشان میهد که برای شویش حلشونده A نیاز داریم. درصورتیکه نرخ جریان در ستون ، ثابت باشد، را میتوان از طریق «زمان بازداری» (Retention Time) نیز توصیف کرد که رابطه آن به صورت زیر است:
با توجه به رابطه بالا، تا زمانی که نرخ جریان ثابت باشد، زمان بازداری را میتوان به طور مستقیم به حجم بازداری مرتبط کرد.
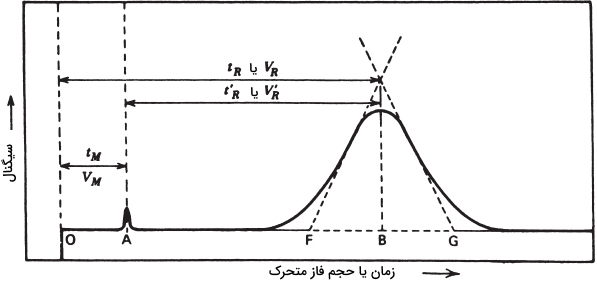
پیک (قله) کوچکی که در ابتدای نمودار وجود دارد، حلشوندهای را نشان میدهد که بدون جذب به فاز ساکن، به طور مستقیم و بدون مقاومت از میان ستون عبور کرده است. آیوپاک، این پدیده را «حجم هلدآپ» (Hold-up Volume) مینامد و آن را به صورت حجم مورد نیاز فاز متحرک (MP) جهت «شویش» (Elution) ترکیب «بازداری نشده» (Unretained) از ستون کروماتوگرافی تعریف میکند. همچنین، زمان مورد نیاز برای گذر MP از ستون کروماتوگرافی را نیز به نام «زمان هلدآپ» (Hold-up Time) یا تعریف میکنند. البته در تعریفهای جدیدتر به آن «پیک هوا» (Air Peak) نیز میگویند.
یکی از معادلات اساسی در کروماتوگرافی، معادلهای است که زمان بازداری را به ثابت بازداری نظری مرتبط میکند و به صورت زیر تعریف میشود:
- : حجم بازداری
- : حجم فاز متحرک
- : ثابت توزیع
- : حجم فاز ساکن
با نگاهی به معادله بالا در مییابیم که حجم کلی گاز حامل، در طول زمان شویشِ حلشونده به دو بخش تقسیم میشود:
- گازی که ستون را پر میکنید یا حجمی که حلشونده باید از میان آن در ستون عبور کند که آنرا با نشان میدهند.
- حجم گازی که به هنگام عدم حرکت حلشونده در ستون، جریان دارد.
بخش دوم، به کمک ثابت توزیع و مقدار فاز ساکن تعیین میشود. درنتیجه، دو حالت کلی برای حلشونده بوجود میآید: حرکت با جریان فاز متحرک یا جذب به فاز ساکن و عدم تحرک. مجموع این دو اثر را با نام حجم بازداری کلی میشناسند.
ضریب بازداری
برای اینکه بتوان از ثابت توزیع استفاده کرد، بهتر است آن را به دو عبارت تقسیم کنیم که در آن، ، نسبت حجم فاز و ضریب بازداری خواهد بود:
در یک ستون مویین، اگر مقدار ضخامت لایه را داشته باشیم، مقدار از رابطه زیر قابل محاسبه خواهد بود که در آن، شعاع ستون مویین است:
به طور معمول، مقدار شعاع ستون مویین بسیار بیشتر از «ضخامت لایه» (Film Thickness) است که در اینصورت، رابطه بالا به شکل زیر تبدیل خواهد شد:
ضریب بازداری (k)، نسبت مقدار حلشونده در فاز ساکن به مقدار آن در فاز متحرک است. توجه داشته باشید که در این رابطه، غلظت حلشونده مد نظر نیست:
هرقدر مقدار ضریب بازداری بیشتر باشد، مقدار حلشونده در فاز ساکن بیشتر خواهد بود و بنابراین، مدت زمان بیشتری در ستون باقی خواهد ماند. به عبارت دیگر، ضریب بازداری، میزان سختی عبور ماده از ستون کروماتوگرافی را مشخص میکند. به همین دلیل، از موارد مهمی که در اصطلاحات کروماتوگرافی مورد استفاده قرار میگیرد، ضریب بازداری است که به سادگی از روی کروماتوگرام قابل محاسبه است.
محاسبه ضریب بازداری از روی نمودار
رابطهای که در ابتدای بحث عنوان شد را به خاطر بیاورید. اگر این رابطه را به طور مجدد بازآرایی کنیم، به عبارت جدیدی موسوم به «حجم بازداری تعدیل شده» (Adjusted Retention Volume) خواهیم رسید:
در نهایت، با بازآرایی این رابطه و استفاده از آن در رابطه قبل، به معادله کاربردی برای محاسبه ضریب بازداری خواهیم رسید:
با توجه به اینکه هر دو عبارات و را میتوان به طور مستقیم از کروماتوگرام اندازهگیری کرد، میزان ضریب بازداری را برای هر ماده حلشونده، میتوان محاسبه کرد که در شکل زیر نشان داده شده است:
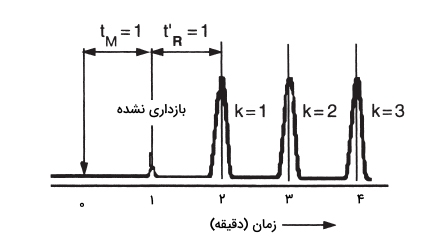
توجه داشته باشید که هرقدر فاز ساکن، تاثیر بیشتری روی ماده حلشونده داشته باشد، حجم بازداری و ضریب بازداری نیز بیشتر خواهد بود. بنابراین، حتی زمانی که مقدار ثابت توزیع را در اختیار نداشته باشیم، میتوانیم با اندازهگیری ضریب بازداری از روی کروماتوگرام، مقدار جذب یک ماده حلشونده را مشخص کنیم.
حجم بازداری تصحیح شده و خالص
عبارت دیگری نیز که در خصوص اصطلاحات کروماتوگرافی گازی مطرح میشود، میزان «حجم بازداری تصحیح شده» (Corrected Retention Volume) است که با نشان میدهیم و حجم تصحیح شدهای است که در خصوص تراکمپذیری گاز حامل درنظر میگیریم. در صورتی که بخواهیم حجم بازداری را از روی زمان بازداری محاسبه کنیم. باید از نرخ جریان متوسط استفاده کنیم که در نتیجه، حجم بازداری محاسبه شده موسوم به حجم بازداری تصحیح شده است که از رابطه زیر بدست میآید:
لازم به ذکر است که برای محاسبه ضریب تصحیح تراکمپذیری از رابطه زیر استفاده میکنیم که در آن، و به ترتیب فشار ورودی و خروجی ستون کروماتوگرافی هستند:
با تعریف حجمهای بازداری، به تعریف دیگری از اصطلاحات کروماتوگرافی گازی میرسیم و آن، «حجم بازداری خالص» (Net Retention Volume) است که به صورت زیر تعریف میشود:
به همین شکل، در خصوص کروماتوگرافی گازی، معادله فوق را میتوان به شکل زیر نوشت:
ضریب تاخیر
ضریب تاخیر نیز از جمله اصطلاحات کروماتوگرافی گازی است. راه دیگری که برای توصیف سختی حرکت یک حلشونده در ستون مطرح میشود، مقایسه سرعت آن در ستون با سرعت متوسط فاز گاز متحرک است. در اثر این مقایسه، پارامتر جدیدی تعریف میشود که به «ضریب تاخیر» (Retardation Factor) موسوم و رابطه آن در زیر آورده شده است:
به منظور تعریف یک رابطه محاسباتی، مقدار را میتوان از طریق تقسیم طول ستون به زمان بازداری یک ماده محسابه کرد که در این رابطه، واحد طول، سانتیمتر یا میلیمتر و واحد زمان، ثانیه است:
به طور مشابه، سرعت متوسط گازی که بدون ممانعت از ستون عبور میکند را نیز به کمک زمان بازداری آن میتوان محاسبه کرد:
با ادغام سه معادله اخیر، میتوان به یک تعریف محاسباتی برای ضریب تاخیر دست پیدا کرد:
در نهایت، همانطور که ضریب بازداری را از روی کروماتوگرام محسابه کردیم، ضریب تاخیر را هم به میتوان از روی کروماتوگرام محاسبه کرد. توجه داشته باشید که مقادیر R و k را هم میتوان به کمک رابطه زیر با یکدیگر مرتبط کرد. در حقیقت، این عبارت، میزان تاخیر ماده حلشونده در طول مسیر عبور خود از ستون را نشان میدهد:
این عبارت، همچنین کسر ماده حلشونده در فاز متحرک را برای هر زمان نشان میدهد. به طور مثال، حلشوندهای به نام A، ضریب بازداری برابر با ۵ دارد. این عبارت بدان معنی است که ماده A، پنج برابر بیشتر از «پیک هوا» (Air Peak) در ستون حضور دارد. ضریب تاخیر برای این ماده، با توجه به رابطه بالا برابر با 0/167 است که یعنی در هر لحظه، به هنگام عبور ماده از میان ستون، 16/7 درصد آن در فاز متحرک و 84/3 درصد آن در فاز ساکن حضور دارد. به همین شکل، برای ماده B که ضریب بازداری برابر با 9 داشته باشد، ۱۰ درصد آن در فاز متحرک و ۹۰ درصد آن در فاز ساکن قرار دارد.
ضریب تاخیری که در ستون کروماتوگرافی تعریف میشود، شباهت بسیاری با ضریب بازداری موجود در کروماتوگرافی لایه نازک دارد و به کمک آنها میتوان دادههای HPLC و TLC را با یکدیگر مقایسه کرد. در نهایت، با دریافت مفهوم ضریب بازداری، میتوان دریافت که این مفهوم، تشابهاتی با «استخراج مایع-مایع» (Liquid-Liquid Extraction) دارد.
شکل پیکها
در ادامه بحث در خصوص اصطلاحات کروماتوگرافی گازی باید به شکل پیکها در کروماتوگرافی اشاره کنیم. میدانیم که مولکولهای حلشونده، در طول فرآیند کروماتوگرافی، هر کدام رفتار متفاوتی دارند. در نتیجه این رفتارها، مولکولها، زمانهای بازداری تصادفی را به صورت تجمعی، بعد از فرآیندهای مختلف «جذب و دفع سطحی» ( Sorptions and Desorptions) تولید میکنند. برای یک ماده، مجموع این فرآیندها موجب توزیع آنها در ستون و ایجاد پیک میشود. از اصطلاحات کروماتوگرافی رایج میتوان به شکل این پیکها اشاره کرد که عموما به صورت یک توزیع «گاوسی» (Guassian) هستند. به طور معمول، یک پیک ایدهآل، شکلی گاوسی دارد. زمانی که پیک نامتقارنی را شاهد باشیم، یعنی برهمکنشی نامطلوب در طول فرآیند کروماتوگرافی روی داده است.
تصویر زیر، شکل پیکهای مختلف را در برخی نمونههای واقعی نشان میدهد. پیکهایی همچون پیک دوم که «پهن» (Broad) هستند را بیشتر در ستونهای «پرشده» (Packed) میبینیم و از روی آنها میتوان دریافت که انتقال جرم آهستهای داشتیم. هدف اصلی یک کروماتوگراف، تلاش برای هرچه باریکتر کردن پیک حاصل است. هر نوع پیک نامتقارن را بسته به محل عدم تقارن، میتوان به دستههای «دنبالهای» (Tailing) و «جبههای» (Fronting) تقسیمبندی کرد. مقدار عدم تقارن پیک، به کمک «ضریب دنبالهای» (Tailing Factor) قابل محاسبه است.
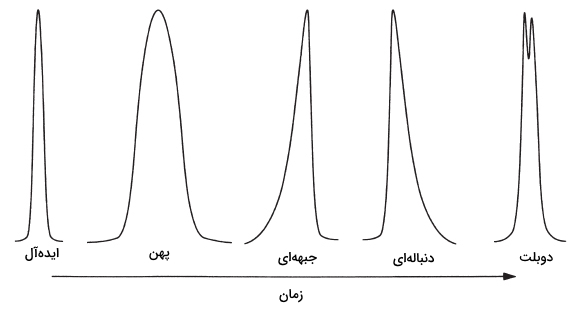
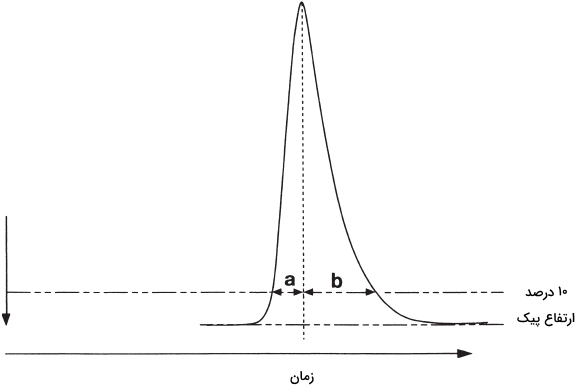
همانطور که در تصویر هم دیده میشود، مقادیر a و b را در ۱۰ درصد ارتفاع پیک محاسبه میکنند. به سادگی با محسابه مقدار درمییابیم که اگر این مقدار، عددی بیشتر از ۱ بود، شکل پیک، دنبالهای و اگر کمتر از ۱ بود، پیک جبههای داریم. پیک «دوبلت» (Doublet)، از چالشهای کارشناس هست و نشان میدهد که دو حلشونده به خوبی از یکدیگر جدا نشدهاند. عوامل مختلفی بر ایجاد پیک دوبلت دخیل هستند که در زیر آورده شدهاند:
- روش نامناسب تزریق
- مقدار زیاد از نمونه
- ستون معیوب
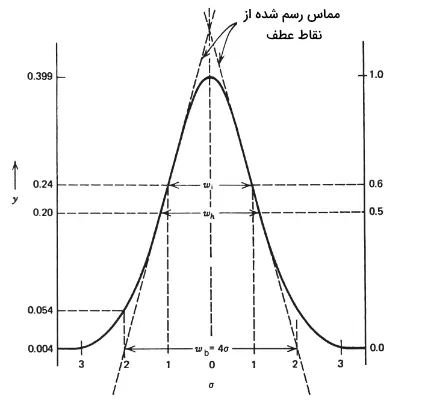
مشخصههای پیک ایدهآل
در این مقاله بیشتر بر پیک ایدهآل بحث خواهیم کرد که نمونهای از آن در تصویر زیر دیده میشود. مشخصههای یک پیک گاوسی را میتوان در این تصویر مشاهده کرد. نقاط عطف این پیک در محل 0/607 از ارتفاع آن وجود دارد که اگر بر این نقاط، مماسی رسم کنیم، مثلثی با قاعده تشکیل میشود که با انحراف معیار برابر است. در محل نقطه عطف، عرض این پیک برابر با خواهد بود. همچنین عرض پیک در نصف ارتفاع آن برابر با است. از این مشخصهها در اصطلاحات کروماتوگرافی گازی استفاده میشود تا بسیاری از پارامترها همچون «عدد سینی» (Plate Number) را بتوان تعریف کرد.
عدد سینی
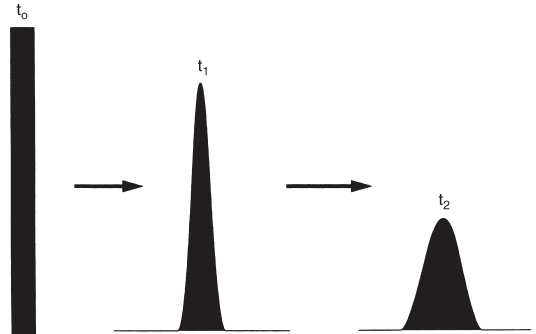
عدد سینی هم ازجمله اصطلاحات کروماتوگرافی گازی است. بمنظور توصیف بازده یک ستون کروماتوگرافی، باید معیاری از عرض پیک داشته باشیم اما این معیار باید با زمان بازداری متناسب باشد زیرا همانطور که دیدیم، پهنای پیک با زمان بازداری تناسب دارد که این مفهوم در تصویر زیر به خوبی دیده میشود:
متداولترین معیار برای اندازهگیری بازده یک ستون کروماتوگرافی، عدد سینی است که از رابطه زیر بدست میآید:
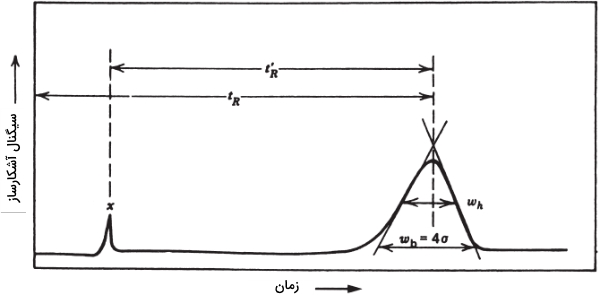
در تصویر زیر میتوانید پارامترهای قابل اندازهگیری برای محاسبه عدد سینی را ملاحظه کنید. فارغ از نوع پارامترها، واحدهای صورت و مخرج کسر باید یکسان باشند و در نتیجه، به عددی بدون بعد میرسیم. مقدار زیاد بیانگر ستون با بازده زیاد است.
ارتفاع سینی
پارامتر دیگری که در اصطلاحات کروماتوگرافی گازی و بیان بازده ستون استفاده میشود، ارتفاع سینی است که از رابطه زیر بدست میآید. در این رابطه، ، طول ستون را نشان میدهد. واحدی از جنس طول دارد و برای مقایسه بازده ستونها با طولهای مختلف، معیار بهتری بدست میدهد.
لبته به ، «ارتفاع معادل سینی نظری» (Height Equivalent to One Theoretical Plate) هم میگویند که آن را با نیز نشان میدهند. ستونی مناسب است که زیاد و پایینی داشته باشد.
تفکیک
در اصطلاحات کروماتوگرافی گازی یکی از معیارهای تعیین بازده ستون، «تفکیک» (Resolution) است که با نشان میدهند. همچون دیگر روشهای تحلیلی، از این واژه بمنظور توصیف میزان جدایش (تفکیک) پیکها بهره میگیرند. رابطه آن در کروماتوگرافی به صورت زیر نشان داده میشود و در آن، فاصله بین نقاط ماکزیمم دو ماده حلشونده است:
برای دستیابی به مقدار پهنای پیکها، خطوط مماسی از نقاط عطف مطابق تصویر زیر، رسم میکنیم. در حالت ایدهآل، پهنای دو پیک مجاور با یکدیگر یکسان هستند و بنابراین میزان با برابر خواهد بود و معادله به شکل زیر ساده میشود:
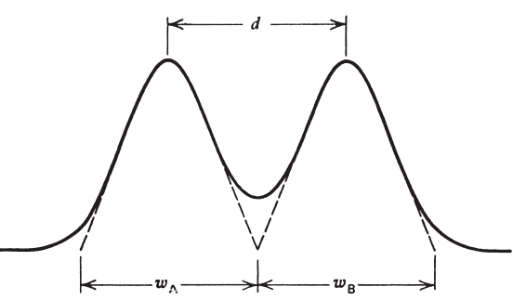
هرقدر میزان بیشتر باشد، جدایش بهتری خواهیم داشت. برای داشتن یک تفکیک مناسب، مقدار باید در حدود 1/5 باشد.
اگر این مطلب برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای مهندسی شیمی
- آموزش کاربرد ریاضیات در مهندسی شیمی
- کروماتوگرافی گازی — از صفر تا صد
- طیف سنجی مولکولی — به زبان ساده
^^