نمونه سوال موازنه شیمی دهم با جواب + آزمون سنجش
یکی از اولین قدمها برای درک یک واکنش شیمیایی و رفتار مواد شیمیایی در آن، موازنه واکنش است. موازنه واکنشهای شیمیایی، اطمینان حاصل کردن از برابر بودن تعداد هر اتم در هر دو سمت معادله واکنش است. بدین ترتیب، اصل پایستگی جرم در واکنش شیمیایی برقرار میشود. در این مطلب از مجله فرادرس با بررسی نمونه سوال موازنه شیمی دهم متوسطه و پاسخهای آنها، مسیری ساده و کاربردی برای درک موازنه معادله واکنش شیمیایی را ارائه میکنیم.
- با انواع نمونه سوال موازنه شیمی دهم آشنا میشوید.
- موازنه به روش وارسی و جمع جبری را میآموزید.
- با نمونه سوالات موازنه واکنش شیمیایی ساده آشنا میشوید.
- روش موازنه یونهای چنداتمی را میآموزید.
- یاد میگیرید موازنه واکنش اکسایش و کاهش چیست.
- هدف انجام موازنه واکنش شیمیایی را میشناسید.


در ابتدای این مطلب انواع نمونه سوال موازنه شیمی دهم را بررسی کرده و روشهای موازنه را مرور میکنیم. سپس نمونه سوال موازنه شیمی دهم را برای واکنشهای شیمیایی، واکنشهای اکسایش و کاهش، مولکولهای چند اتمی و مولکولهای باردار بررسی میکنیم. در نهایت اهمیت موازنه واکنش را آموخته و آزمونی برای سنجش یادگیری مطالب آموخته شده ارائه میدهیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل نمونه سوال موازنه شیمی دهم را بیاموزید.
نمونه سوال موازنه شیمی دهم
در این بخش، نمونه سوالات موازنه شیمی دهم را بررسی کرده و به آنها پاسخ میدهیم. برای موازنه واکنشهای شیمیایی، باید بتوانیم به خوبی و با دقت تعداد اتمهای هر سمت معادله واکنش را بشماریم. برای این کار ابتدا نیاز داریم تعداد هر اتم را با توجه به زیروند آن و ضریب استوکیومتری آن بررسی کنیم. سپس به مقایسه تعداد اتمها در هر سمت معادله و بررسی نحوه برابری آنها میپردازیم.
برای شروع هر نمونه سوال موازنه شیمی دهم ابتدا نیاز است جدولی مطابق جدول زیر برای شمارش تعداد اتمها رسم شود.
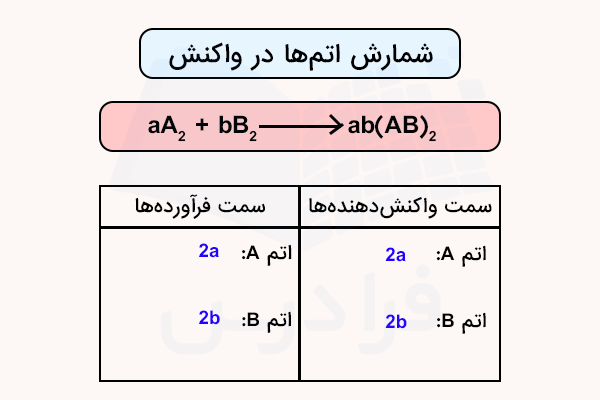
سپس با بررسی تعداد، به شروع موازنه با استفاده از روش وارسی یا روشهای دیگر میپردازیم. برای مرور و درک بهتر این دو روش موازنه، در ادامه این روشها را بررسی میکنیم. اصول کلی موازنه واکنشهای شیمیایی در ادامه آورده شده است.
- پیچیدهترین ماده از نظر فرمول شیمیایی باید ابتدا موازنه شود.
- سادهترین ماده از نظر فرمول شیمیایی باید در آخر موازنه شود.
- کوچکترین مضرب مشترک بین دو عدد میتواند برای تعیین ضرایب استفاده شود.
- یونهای چنداتمی (اگر در هر دو سمت معادله شیمیایی حضور داشته باشند) میتوانند بهعنوان یک واحد موازنه شوند.
- گاهی اوقات برای موازنه سادهترین ماده از نظر فرمول شیمیایی باقیمانده، استفاده از ضرایب کسری لازم است. اگر ضریب کسری استفاده شده باشد، برای بهدست آوردن ضرایب صحیح، هر دو سمت معادله را در مخرج ضرب کنید.
- تعداد اتمهای هر عنصر در هر سمت معادله را بشمارید تا اطمینان حاصل شود که معادله شیمیایی موازنه شده است.

انواع روش موازنه واکنش شیمیایی
برای حل نمونه سوال موازنه شیمی دهم، دو روش رایج وجود دارد. سادهترین روش، روش وارسی است و روش جبری برای معادلات پیچیده استفاده میشود. روش وارسی سادهتر و سریعتر است و بیشتر در سطح دبیرستان استفاده میشود، چون با امتحان کردن ضرایب میتوان به جواب رسید.
در مقابل، روش جبری دقیقتر و مرحلهای است و زمانی به کار میرود که موازنه با روش وارسی سخت باشد. آشنایی با هر دو روش به دانشآموز کمک میکند معادلات شیمیایی را بهتر و مطمئنتر موازنه کند. در ادامه این موارد را بررسی میکنیم.
موازنه به روش وارسی
یکی از سادهترین روشها برای موازنه واکنش شیمیایی، موازنه به روش وارسی است. در این روش، ابتدا تعداد عناصر در هر دو سمت معادله واکنش شمرده شده و سپس ترکیبی که بیشترین نوع عناصر را دارد به عنوان مرجع انتخاب میشود. سپس تعداد اتمهای هر دو سمت نسبت به این ترکیب شیمیایی شمارش و با استفاده از تغیین ضرایب استوکیومتری برابر میشوند.
اگر تا این قسمت از مطلب را مطالعه کردهاید با قدمهای کلی حل نمونه سوال موازنه شیمی دهم آشنا شدهاید. در ادامه نیز به بررسی بیشتر این سوالات میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
مراحل انجام موازنه به روش وارسی در ادامه آورده شده است.
- انتخاب پیچیدهترین ترکیب و در نظر گرفتن ضریب ۱ برای آن
- تعیین ضرایب سایر مواد بر اساس ترکیب اولیه
- حذف مخرج کسرها با ضرب کل واکنش در مخرج مناسب
- شمارش اتمها در دو طرف معادله و انجام موازنه نهایی واکنش

برای درک بهتر این روش به مثال زیر دقت کنید.
مثال
معادله واکنش شیمیایی زیر را موازنه کنید.
پاسخ
ابتدا تعداد اتمهای هر طرف را شمارش میکنیم و جدول را تشکیل میدهیم.
| سمت واکنشدهنده | سمت فرآورده |
| هیدروژن: ۲ عدد | هیدروژن: ۲ عدد |
| اکسیژن: ۲ عدد | اکسیژن ۱ عدد |
پس نیاز است برای موازنه واکنش تعداد اکسیژنها را برابر کنیم. آب را به عنوان ترکیب اصلی در نظر گرفته و به آن ضریب ۱ میدهیم. تعداد هیدروژنها برابر است و اکسیژن در سمت واکنشدهندهها باید ضریب بگیرد.
در نهایت برای از بین رفتن ضریب کسری کل معادله را در ۲ ضرب کرده و به واکنش موازنه شده زیر میرسیم.
موازنه به روش جمع جبری
روش جبری کمی پیچیده است و برای واکنشهایی به کار میرود که نمیتوان آنها را با روش وارسی موازنه کرد. این روش به شکل زیر انجام میشود.
- در گام نخست، بهجای ضرایب استوکیومتری هر مولکول از حروف انگلیسی مانند a، b، c، d، e و … استفاده میکنیم.
- سپس برای هر عنصر بهطور جداگانه، ضرایب را در تعداد اتمها ضرب کرده و مقادیر حاصل را در دو طرف معادله با هم برابر قرار میدهیم.
- در مرحله بعد، برای نخستین متغیر یعنی a مقدار ۱ در نظر گرفته میشود و با استفاده از آن دستگاه معادلات را حل میکنیم.
- در نهایت، اگر ضرایب به صورت کسری به دست آمده باشند، همه ضرایب را در بزرگترین مخرج مشترک ضرب میکنیم تا به اعداد صحیح تبدیل شوند.
پس از انجام این مراحل، معادله موازنهشده نوشته میشود و برای اطمینان، تعداد اتمهای هر عنصر در دو طرف واکنش دوباره شمارش میشود. به مثال زیر دقت کنید.
مثال
معادله واکنش زیر را موازنه کنید.
پاسخ
همانطور که در قسمت قبل اشاره شد برای موازنه واکنش با استفاده از روش جبری ابتدا به تمامی مواد بجای ضریب استوکیومتری، حروف انگلیسی را اختصاص میدهیم.
حال برای موازنه هر اتم، معادلات مورد نیاز ضراب استوکیومتری را مینویسیم.
| اتم | معادله |
| پتاسیم | |
| منگنز | |
| کلر | |
| اکسیژن | |
| هیدروژن |
حال معادلات را ساده میکنیم تا همگی بر حسب a نوشته شوند.
با در نظر گرفتن a=۱، معادله شیمیایی به شکل زیر در میآید.
حال با ضرب تمامی ضرایب در ۲، ضریب کسری از بین رفته و معادله واکنش موازنه میشود.
در ادامه مطلب نمونه سوال موازنه شیمی دهم را با توجه به نوع معادله واکنش شیمیایی بررسی میکنیم. به دلیل حذف روش جبری از کتاب شیمی دهم متوسطه، این روش در نمونه سوالات ادامه مطلب بررسی نخواهد شد. پینشهاد میکنیم برای یادگیری بیشتر در مورد این روش حل نمونه سوال موازنه شیمی دهم، به فیلم آموزش حل موازنه به روش معادله فرادرس که لینک آن در ادامه آورده شده است مراجعه کنید.
یادگیری شیمی دهم با فرادرس
برای درک بهتر و یافتن آسانتر پاسخ نمونه سوال موازنه شیمی دهم، ابتدا نیاز است با مفاهیمی چون واکنش شیمیایی، ترکیبات مولکولی، ترکیب یونی و نامگذاری ترکیبات شیمیایی آشنا شویم. پیشنهاد میکنیم برای درک بهتر این مفاهیم، به مجموعه فیلم آموزش دروس پایه دهم فرادرس بخش شیمی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مسائل میپردازد.
همچنین با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه نمونه سوال موازنه شیمی دهم دسترسی داشته باشید.
- فیلم آموزش شیمی ۲ پایه یازدهم رشته علوم تجربی و ریاضی و فیزیک فرادرس
- فیلم آموزش شیمی ۲ پایه یازدهم حل سوالات تشریحی امتحانات نهایی فرادرس
- فیلم آموزش شیمی عمومی ۱ و ۲ مرور و حل مساله فرادرس
نمونه سوال موازنه واکنش شیمیایی ساده
در ادامه این مطلب نمونه سوال موازنه شیمی دهم را برای معادله واکنشهای شیمیایی ساده بررسی میکنیم. در برخی از سوالات نیاز است معادله واکنش شیمیایی نیز نوشته شود. برای نوشتن معادله واکنش شیمیایی نیاز است نحوه نوشتن فرمول شیمیایی مواد را بدانیم. برای مرور و درک بهتر نحوه نوشتن واکنش شیمیایی، پیشنهاد میکنیم مطلب فرمول شیمیایی مجله فرادرس را مطالعه کنید. در ادامه این مثالها را بررسی میکنیم.
مثال ۱
معادله واکنش شیمیایی زیر را موازنه کنید.
پاسخ
ابتدا جدول شمارش اتمها را در دو سمت معادله رسم میکنیم.
| واکنشدهنده | فرآورده |
| آلومینیوم: ۲ عدد | آلومینیوم: ۱ عدد |
| اکسیژن: ۳ عدد | اکسیژن: ۲ عدد |
برای موازنه واکنش شیمیایی ساده که شامل یونهای چنداتمی و مواد باردار نیست، ابتدا پیچیدهترین ترکیب در معادله واکنش از نظر فرمول شیمیایی را انتخاب کرده و به آن ضریب ۱ میدهیم. در این معادله ترکیب آلومینیوم اکسید () پیچیدهترین ترکیب است. سپس یکی از اتمها را انتخاب کرده و آن را موازنه میکنیم.
برای موازنه کردن آلومینیوم، ترکیب آلومینیوم جامد در سمت واکنشدهندهها باید ضریب ۲ بگیرد.
سپس به سراغ اکسیژن رفته و تعداد آن را موازنه میکنیم. در سمت فرآوره ۳ اکسیژن و در سمت واکنشدهنده ۲ اکسیژن داریم. پس مولکول دو اتمی اکسیژن باید ضریب سه دوم بگیرد.
در نهایت تمامی ضرایب را در عدد ۲ ضرب میکنیم تا ضریب کسری از بین برود. بدین ترتیب معادله موازنه شده و در هر دو سمت واکنش تعداد برابری از اتمهای آلومینیوم (۴ عدد) و اکسیژن (۶ عدد) وجود دارد.
مثال ۲
معادله واکنش سوختن کامل بین بوتان مایع و گاز اکسیژن را نوشته و موازنه کنید.
پاسخ
برای نوشتن معادله واکنش باید بدانیم بوتان آلکانی است که ۴ اتم کربن و ۱ اتم اکسیژن دارد و از واکنش سوختن کامل این هیدروکربنها کربن دی اکسید و آب تولید میشود. بدین ترتیب معادله واکنش زیر را مینویسیم.
ابتدا تعداد اتمها را در دو سمت واکنش مقایسه میکنیم.
| سمت واکنشدهنده | سمت فرآورده |
| کربن: ۴ عدد | کربن: ۱ عدد |
| هیدروژن: ۱۰ عدد | هیدروژن: ۲ عدد |
| اکسیزن: ۲ عدد | اکسیژن: ۳ عدد |
سپس بوتان را به عنوان پیچیدهترین ماده انتخاب کرده و به آن ضریب ۱ میدهیم. برای انتخاب اتم اول برای موازنه بهتر است اتمی را انتخاب کنیم که در هر دو سمت تنها در ۱ ماده وجود دارد. پس اتم کربن را موازنه میکنیم و به کربن دی اکسید ضریب ۴ میدهیم.
سپس هیدروژن را موازنه میکنیم که در سمت فرآوردهها تنها در مولکول آب قرار دارد. برای این کار به آب ضریب ۵ میدهیم.
حال تنها اکسیژن باقی مانده است. در سمت فرآوردهها و پس از ضریبهایی که در نظر گرفتیم، ۱۳ عدد اکسیژن داریم. در سمت واکنشدهندهها تنها ترکیب ۲ اتمی اکسیژن را داریم. پس به آن ضریب را داده و سپس تمامی ضرایب را در ۲ ضرب میکنیم تا ضریب کسری از بین برود.
معادله موازنه شده:
مثال ۳
معادله واکنش زیر را موازنه کنید.
پاسخ
ابتدا تعداد اتمها را در دو سمت معادله واکنش بررسی میکنیم.
| سمت واکنشدهندهها | سمت فرآوردهها |
| فسفر: ۱ عدد | فسفر: ۱ عدد |
| کلر: ۵ عدد | کلر: ۴ عدد |
| هیدروژن: ۲ عدد | هیدروژن: ۱ عدد |
| اکسیژن: ۱ عدد | اکسیژن: ۱ عدد |
ابتدا ترکیب را به عنوان پیچیدهترین ترکیب انتخاب میکنیم. برای شروع موازنه میتوانیم از اتمهای فسفر و اکسیژن شروع کرده و به ترکیبات و آب ضریب ۱ بدهیم.
حال تنها اتمهای کلر و هیدروژن در ترکیب HCl موازنه نشده باقیماندهاند. اگر اتم هیدروژن را در نظر بگیریم، با ضریب ۲ دادن به این ترکیب تعداد کلرها نیز موازنه میشود. همچنین با در نظر گرفتن کلر نیز میتوانیم به همین ضریب برسیم. با ضریب ۲ دادن به این ترکیب تعداد اتمهای کلر در هر دو سمت معادله برابر ۵ خواهد بود. معادله واکنش موازنه شده به شکل زیر است.
مثال ۴
معادله واکنش شیمیایی زیر را موازنه کنید.
پاسخ
برای پاسخ به سوال ابتدا تعداد اتمها را در هر دو سمت معادله واکنش میشماریم.
| سمت واکنشدهندهها | سمت فرآوردهها |
| باریم: ۱ عدد | باریم: ۱ عدد |
| نیتروژن: ۲ عدد | نیتروژن: ۲ عدد |
| اکسیژن: ۶ عدد | اکسیژن: ۳ عدد |
برای موازنه واکنش میتوانیم ترکیب باریم نیترات را به عنوان ترکیب مرجع در نظر بگیریم. با ضریب ۱ دادن به این ترکیب، ترکیبات باریم اکسید و نیتروژن دو اتمی نیز ضریب ۱ میگیرند و تنها مولکول ۲ اتمی اکسیژن باقی میماند. در سمت واکنشدهندهها ۶ اتم اکسیژن داریم و در سمت فرآوردهها نیز یکی از اکسیژنها در ترکیب باریم اکسید قرار دارد. پس به ۵ اکسیژن دیگر نیاز داریم و به اکسیژن دو اتمی ضریب میدهیم.
در نهایت کل معادله را در ۲ ضرب میکنیم تا ضریب کسری از بین برود.
برای درک بهتر نمونه سوال موازنه شیمی دهم که در این بخش بررسی شد، به تمرینهای زیر پاسخ دهید.

تمرین ۱
تمرین ۲
نمونه سوال موازنه یونهای چند اتمی
در برخی از واکنشهای شیمیایی، برخی از یونهای چند اتمی مانند نیترات، فسفات، کربنات و ... در هر دو سمت واکنش دیده میشوند. در این موارد میتوانیم بهجای بررسی تک تک اتمها، آن یونهای چند اتمی را به عنوان یک واحد مجزا شمارش کنیم.
برای مثال، به واکنش شیمیایی زیر دقت کنید.
در این واکنش، گروه کربنات به صورت در هر دو سمت واکنش آورده شده است. پس میتوانیم آن را به صورت یک گروه مجرا شمارش کنیم. بنابراین میتوانیم جدول شمارش تعداد اتمها را به شکل زیر بنویسیم.
| سمت واکنشدهندهها | سمت فرآوردهها |
| آلومینیوم: ۱ عدد | آلومینیوم: ۲ عدد |
| اکسیژن: ۳ عدد | اکسیژن: ۱ عدد |
| هیدروژن: ۵ عدد | هیدروژن: ۲ عدد |
| کربنات: ۱ عدد | کربنات: ۳ عدد |
دقت داشته باشید که در شمارش بالا، اتمهای اکسیژن موجود در ترکیبات کربنات برای شمارش اتم هیدروژن لحاظ نشدهاند. در عوض، هر کروه کربنات به صورت جداگانه شمارش میشود. بدین ترتیب، برای شروع موازنه میتوانیم از ترکیب آلومینیوم کربنات () شروع کنیم. در این ترکیب ۲ اتم آلومینیوم و ۳ مولکول کربنات وجود دارد. بنابراین به ترکیب ضریب ۲ و به اسید کربنیک () ضریب ۳ میدهیم.
حال برای موازنه کربن هیدروژن و اکسیژن تعداد این اتمها را در دو طرف معادله (بجز آنهایی که در کربنات وجود دارند) را میشماریم. در سمت واکنشدهندهها ۱۲ اتم اکسیژن (در کربنیک اسید و آلومینیوم هیدروکسید) و ۶ اتم اکسیژن (در آلومینیوم هیدروکسید) وجود دارد. بنابراین با ضریب ۶ دادن به آب واکنش موازنه میشود.
معرفی یون چند اتمی
یونهای چند اتمی ترکیباتی هستند که از یک گروه مولکولی مشخص تشکیل شدهاند و همواره ترکیب مشخص و بار الکتریکی مشخص دارند. برای مثال، یون نیترات فرمول شیمیایی داشته و با یونهای یک بار مثبت ترکیب یونی تشکیل میدهد. بنابراین در موازنه واکنشهای شامل این یون، میتوان هر گروه () را به شرطی که در هر دو طرف معادله به همین شکل حضور داشته باشد، به عنوان یک واحد مجزا شمارش کرد.
در ادامه برخی از یونهای چند اتمی رایج و گروه مولکولی آنها (برای تشخیص بهتر در موازنه واکنش) معرفی شدهاند.
| نام یون چند اتمی | فرمول شیمیایی و گروه مولکولی |
| نیترات | و |
| سولفات | و |
| فسفات | و |
| آمونیوم | و |
| کربنات | و |
| هیدروکسید | و |
| کلرات | و |
| نیتریت | و |
| بیکربنات | و |
| سولفیت | و |
برای درک بهتر نمونه سوال موازنه شیمی دهم شامل یونهای چند اتمی، به مثالهای زیر دقت کنید.
مثال ۱
محلول آبی نیترات سرب (اا) و سدیم کلرید با هم مخلوط میشوند. فرآوردههای این واکنش، رسوب جامد کلرید سرب (اا) و محلول آبی سدیم نیترات است. معادله این واکنش را نوشته و موازنه کنید.
پاسخ
معادله این واکنش به شکل زیر نوشته میشود.
ابتدا جدول شمارش تعداد اتمها را رسم میکنیم. در این واکنش، یون چند اتمی نیترات میتواند به شکل یک واحد مجزا شمارش شود.
| سمت واکنشدهندهها | سمت فرآوردهها |
| یون نیترات: ۲ | یون نیترات: ۱ |
| سرب: ۱ | سرب: ۱ |
| سدیم: ۱ | سدیم: ۱ |
| کلر: ۱ | کلر: ۲ |
برای شروع موازنه از مولکول به عنوان پیچیدهترین ترکیب شروع کرده و به آن ضریب ۱ میدهیم. این ترکیب یک سرب و دو یون نیترات دارد. پس میتوانیم به سرب کلرید ضریب ۱ و سدیم نیترات ضریب ۱ بدهیم.
در نهایت اتم کلر و سدیم را موازنه میکنیم . این اتمها در سمت فرآوردهها ۲ عدد هستند پس نیاز است به سدیم کلرید ضریب ۲ بدهیم. بدین ترتیب واکنش موازنه میشود.
مثال ۲
واکنش محلول آلومینیوم نیترات و لیتیوم کربنات منجر به تولید آلومینیوم کربنات جامد و محلول مایع لیتیوم نیترات میشود. معادله این واکنش را نوشته و آن را موازنه کنید.
پاسخ
معادله شیمیایی این واکنش به شکل زیر نوشته میشود.
ابتدا تعداد اتمها را در هر سمت معادله شمارش میکنیم. در این واکنش، یونهای نیترات و کربنات میتوانند به عنوان یک واحد مجزا در هر دو سمت معادله شمارش شوند.
| سمت واکنشدهندهها | سمت فرآوردهها |
| یون نیترات: ۳ عدد | یون نیترات: ۱ عدد |
| یون کربنات: ۱ عدد | یون کربنات: ۳ عدد |
| آلومینیوم: ۱ عدد | آلومینیوم: ۲ عدد |
| لیتیوم: ۲ عدد | لیتیوم: ۱ عدد |
حال برای شروع موازنه یکی از ترکیبات پیچیده مانند آلومینیوم کربنات را در نظر گرفته و به آن ضریب ۱ میدهیم. در این ترکیب ۲ آلومینیوم و ۳ کربنات وجود دارد. پس میتوانیم به آلومینیوم نیترات ضریب ۲ داده و به لیتیوم کربنات ضریب ۳ بدهیم.
در نهایت یونهای نیترات و اتم لیتیوم موازنه نشده باقی میماند. در سمت واکنشدهندهها، ۶ اتم لیتیوم و ۶ یون نیترات وجود دارد. پس کافی است به ترکیب لیتیوم نیترات ضریب ۶ بدهیم. بدین ترتیب معادله واکنش موازنه میشود.
مثال ۳
از واکنش سدیم کلرید جامد و سولفوریک اسید محلول در آب، هیدروژن کلرید و سدیم سولفات محلول تولید میشود. معادله این واکنش را نوشته و موازنه کنید.
پاسخ
معادله این واکنش به شکل زیر نوشته میشود.
ابتدا تعداد اتمها را در هر سمت معادله شمارش میکنیم. در این واکنش، یون سولفات میتواند به شکل یک واحد مجزا شمارش شود.
| سمت واکنشدهندهها | سمت فرآوردهها |
| سدیم: ۱ عدد | سدیم: ۲ عدد |
| کلر: ۱ عدد | کلر: ۱ عدد |
| هیدروژن: ۲ عدد | هیدروژن: ۱ عدد |
| یون سولفات: ۱ عدد | یون سولفات: ۱ عدد |
برای موازنه این واکنش، ابتدا یک ترکیب پیچیده مانند سدیم سولفات را انتخاب میکنیم و به آن ضریب ۱ میدهیم. این ترکیب ۲ اتم سدیم و یک یون سولفات دارد. پس میتوانیم به ترکیب سدیم کلرید ضریب ۲ و به اسید سولفوریک ضریب ۱ بدهیم.
بدین ترتیب تنها هیدروژن و کلر موازنه نشده باقی میمانند. هیدروژن در سمت واکنشدهندهها ۲ عدد و کلر نیز ۲ عدد است. پس با در نظر گرفتن ضریب ۲ برای هیدروژن کلرید معادله واکنش موازنه میشود.
مثال ۴
از واکنش اسید فسفریک با منیزیم هیدروکسید، منیزیم فسفات و آب تولید میشود. معادله این واکنش را نوشته و آن را موازنه کنید.
پاسخ
معادله این واکنش به شکل زیر نوشته میشود.
برای آغاز موازنه، تعداد اتمها را شمرده و مقایسه میکنیم. در این واکنش، یون فسفات در هر دو سمت واکنش تکرار شده است اما گروه هیدروکسید تنها در سمت واکنشدهندهها وجود دارد. بنابراین گروه فسفات را میتوانیم به شکل یک واحد مجزا شمارش کنیم ولی این امکان برای گروه هیدروکسید وجود ندارد. جدول شمارش اتمهای موجود در واکنش به شکل زیر نوشته میشود.
| سمت واکنشدهندهها | سمت فرآوردهها |
| هیدروژن: ۵ عدد | هیدروژن: ۲ عدد |
| فسفات: ۱ عدد | فسفات: ۲ عدد |
| منیزیم: ۱ عدد | منیزیم: ۳ عدد |
| اکسیژن: ۲ عدد | اکسیژن: ۱ عدد |
دقت داشته باشید که تعداد اکسیژنهای شمارش شده در بالا مربوط به منیزیم هیدروکسید و آب بوده و اکسیژنهای موجود در گروههای فسفات را در آنها شمارش نمیکنیم. حال برای شروع موازنه واکنش از ترکیب آغاز کرده و به آن ضریب ۱ میدهیم. سپس برای موازنه کردن منیزیم، به منیزیم هیدروکسید ضریب ۳ و برای موازنه کردن فسفات، به اسید فسفریک ضریب ۲ میدهیم.
در نهایت برای تعیین ضریب آب، تعداد اکسیژنها و هیدروژنها را موازنه میکنیم. بدین ترتیب، معادله موازنه میشود.
مثال ۵
به معادله واکنش شیمیایی زیر دقت کرده و آن را موازنه کنید.
پاسخ
در معادله واکنش شیمیایی بالا، یون فسفات در سمت واکنشدهندهها وجود دارد اما این ترکیب به همین شکل در فرآوردهها تکرار نشده است. به همین دلیل نیاز است تا هر یک از اتمها را به صورت جداگانه شمارش کنیم. جدول شمارش اتمها به شکل زیر خواهد بود.
| سمت واکنشدهندهها | سمت فرآوردهها |
| کلسیم: ۳ عدد | کلسیم: ۱ عدد |
| فسفر: ۲ عدد | فسفر: ۱ عدد |
| اکسیژن: ۱۰ عدد | اکسیژن: ۴ عدد |
| سیلیسیم: ۱ عدد | سیلیسیم: ۱ عدد |
| کربن: ۱ عدد | کربن: ۱ عدد |
برای آغاز موازنه از مولکول آغاز کرده و به آن ضریب ۱ میدهیم. سپس برای موازنه کردن کلسیم ماده ضریب ۳ میگیرد. برای موازنه سیلیسیم به ضریب ۳ و برای موازنه فسفر به P ضریب ۲ میدهیم.
برای موازنه اکسیژن و پیدا کردن ضریب CO، تعداد اکسیژنهای هر دو طرف واکنش را میشماریم. در سمت واکنشدهندهها، ۸ اکسیژن در ترکیب کلسیم فسفات و ۶ اکسیژن در ترکیب اکسید سیلیسیم وجود دارد. در سمت فرآوردهها، ۹ اکسیژن در ترکیب وجود دارد و برای موازنه شدن اکسیژنها ترکیب CO باید ضریب ۵ بگیرد. در نهایت به C نیز در سمت واکنشدهندهها، ضریب ۵ میدهیم.
معادله موازنه شده به شکل زیر خواهد بود.
مثال ۶
معادله واکنش زیر را موازنه کنید.
پاسخ
این معادله واکنش شامل یونهای آمونیوم، فسفات، نیترات و اتم سرب است. با تشخیص این یونها و شمارش آنها در هر سمت معادله واکنش میتوانیم به راحتی معادله را موازنه کنیم.
| سمت واکنشدهندهها | سمت فرآوردهها |
| یون آمونیوم: ۳ عدد | یون آمونیوم: ۱ عدد |
| یون فسفات: ۱ عدد | یون فسفات: ۴ عدد |
| یون نیترات: ۴ عدد | یون نیترات: ۱ عدد |
| اتم سرب: ۱ عدد | اتم سرب: ۳ عدد |
حال برای شروع موازنه، مولکول سرب فسفات را در نظر گرفته و به آن ضریب ۱ میدهیم. سپس میتوانیم به ترکیبات آمونیوم فسفات و سرب نیترات مشابه زیر ضریب بدهیم.
حال تنها ماده آمونیوم نیترات بدون ضریب باقی مانده است. در سمت واکنشدهندهها، ۱۲ یون نیترات و ۱۲ یون آمونیوم وجود دارد. پس با در نظر گرفتن ضریب ۱۲ برای این ماده، معادله موازنه میشود.

برای درک بهتر روش پاسخ به نمونه سوال موازنه شیمی دهم ترکیبات چنداتمی، به تمرینهای زیر پاسخ دهید.
تمرین ۱
تمرین ۲
نمونه سوال موازنه ترکیبات باردار
در معادله واکنشهایی که در آنها ترکیباتی باردار وجود دارد، باید علاوه بر تعداد اتمهای موجود در هر سمت معادله واکنش، مقدار بار الکتریکی هر سمت نیز برابر باشد. برای مثال، اگر مجموع بارهای الکتریکی سمت واکنشدهندهها برابر با ۲- است، مجموع بار ترکیبات فرآورده نیز باید با ۲- برابر باشد. برای درک بهتر این موضوع به واکنش زیر دقت کنید.
در این واکنش اتمهای منگنز، اکسیژن، هیدروژن و آهن وجود دارد. برای محاسبه دقیقتر میتوانیم مقدار بار را نیز به جدول شمارش اتمهای دو سمت معادله اضافه کنیم.
| سمت واکنشدهندهها | سمت فرآوردهها |
| منگنز: ۱ عدد | منگنز: ۱ عدد |
| آهن: ۱ عدد | آهن: ۱ عدد |
| اکسیژن: ۴ عدد | اکسیژن: ۱ عدد |
| هیدروژن: ۱ عدد | هیدروژن: ۲ عدد |
| بار الکتریکی: ۲+ | بار الکتریکی: ۵+ |
برای موازنه این واکنش یکی ار ترکیبات پیچیده مانند را به عنوان مرجع انتخاب کرده و به منگنز و آب ضریب میدهیم.
حال اتمهای هیدروژن و آهن را موازنه میکنیم.
در نهایت برای اطمینان از موازنه بودن واکنش، باید مجددا مقدار بار الکتریکی را در دو سمت معادله بررسی کنیم. در سمت واکنشدهندهها مقدار بار الکتریکی برابر با ۹+ و در سمت فرآوردهها برابر با ۵+ است. بنابراین نیاز است ۴ بار مثبت به سمت فرآوردهها اضافه شود. برای این کار میتوانیم به اتمهای آهن ضریب ۵ بدهیم تا بارها موازنه شود.
برای پیدا کردن ضریب مناسب آهن برای موازنه بارها، نیاز است با مفهوم اکسایش و کاهش و موازنه واکنش اکسایش کاهش آشنا باشیم. در ادامه این روش را بررسی میکنیم.
موازنه واکنش اکسایش و کاهش
برای موازنه بالا، بهتر است از روش موازنه اکسایش و کاهش استفاده کنیم. برای این کار ابتدا واکنشهای اکسایش و کاهش را به صورت جداگانه مینویسیم.
واکنش اکسایش:
واکنش کاهش:
حال هر واکنش را به صورت جداگانه از نظر تعداد اتمها و بار الکتریکی موازنه میکنیم. واکنشهای موازنه شده به شکل زیر خواهند بود. در موازنه بار الکتریکی در هر سمت که تعداد الکترون کمتری داشت الکترون اضافه میکنیم.
واکنش اکسایش:
واکنش کاهش:
در نهایت این دو واکنش را با هم جمع میکنیم و برای برابر بودن تعداد اتمها و بارها در هر دو سمت ضریب مناسب را اعمال میکنیم.
در نمونه سوال موازنه شیمی دهم معمولا تنها روش وارسی بررسی شده و واکنشهای باردار و اکسایش و کاهش بررسی نمیشوند.
یادگیری شیمی دبیرستان با فرادرس
در این مطلب مجموعه نمونه سوال موازنه شیمی دهم را بررسی کردیم. برای آشنایی بیشتر با این روشها و سوالات نیاز است ابتدا با مفاهیمی چون انواع واکنشهای شیمیایی، کسر تبدیل استوکیومتری، مفهوم مول و نماد شیمیایی عناصر آشنا شوید. پیشنهاد میکنیم برای یادگیری بهتر این مفاهیم به مجموعه آموزش دروس متوسطه دوم و کنکور فرادرس، دروس شیمی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه نمونه سوال موازنه شیمی دهم دسترسی داشته باشید.
- فیلم آموزش شیمی دبیرستان نکته و حل تست کنکور
- فیلم آموزش شیمی ۳ پایه دوازدهم
- فیلم آموزش علوم تجربی پایه نهم بخش شیمی
هدف موازنه واکنش شیمیایی
هدف نهایی در موازنه معادلات شیمیایی این است که دو طرف واکنش، یعنی واکنشدهندهها و فرآوردهها، از نظر تعداد اتمهای هر عنصر برابر شوند. این موضوع از قانون جهانی پایستگی جرم ناشی میشود که بیان میکند ماده نه ایجاد میشود و نه از بین میرود.
بنابراین اگر پیش از واکنش با ده اتم اکسیژن شروع کنیم، باید پس از واکنش نیز به ده اتم اکسیژن برسیم. این یعنی واکنشهای شیمیایی اجزای سازنده اصلی ماده را تغییر نمیدهند، بلکه فقط آرایش این اجزا را تغییر میدهد.
آزمون سنجش یادگیری
برای درک بهتر آنچه در این مطلب از مجله فرادرس آموختیم، به سوالات زیر پاسخ دهید. همچنین، میتوانید پس از پاسخدهی به تمامی سوالات، با کیک بر روی گزینه «دریافت نتیجه آزمون» تعداد پاسخهای صحیح خود را مشاهده کنید.












