اتم خنثی چیست؟ – به زبان ساده + مثال
اتم خنثی اتمی است که در آن تعداد الکترونها و پروتونها برابر است. در تمامی عناصر جدول تناوبی، تعداد الکترونها و پروتونها برابر است بنابراین تمامی این عناصر در حالت پایه، خنثی هستند. اتم خنثی با از دست دادن الکترون میتواند به یون مثبت (کاتیون) و در صورت دریافت الکترون به یون منفی (آنیون) تبدیل شود. در این مطلب از مجله فرادرس میآموزیم اتم خنثی چیست و چگونه میتوان خنثی بودن اتم را تشخیص داد.
- میآموزید اتم خنثی چیست و کدام عناصر خنثی هستند.
- با روش تشخیص اتم خنثی آشنا میشوید.
- نماد شیمیایی اتم خنثی و ساختار اتم را میشناسید.
- یاد میگیرید بار الکتریکی اتم خنثی چیست.
- با کاربردهای اتم خنثی در علوم مختلف آشنا میشوید.


در ابتدای این مطلب میآموزیم اتم خنثی چیست و مثالهایی از آن را بررسی میکنیم. سپس روش تشخیص اتم خنثی را آموخته و با نماد شیمیایی اتم خنثی آشنا میشویم. در ادامه ساختار اتم را بررسی کرده و مفهوم اتم را بررسی میکنیم. پس از آن، بار الکتریکی اتم خنثی را آموخته و تفاوت یون و اتم خنثی را میآموزیم. با مطالعه این مطلب تا انتها به شکلی کامل میآموزید اتم خنثی چیست.
اتم خنثی چیست؟
اتم خنثی اتمی است که بار الکتریکی آن صفر (خنثی) است. این بدین معنی است که تعداد ذرات منفی الکترون با تعداد ذرات مثبت پروتون برابر است. اتم خنثی در بار الکتریکی ذرات با یون تفاوت دارد و مقدار بار آن خنثی است. تمامی عناصر ذکر شده در جدول تناوبی، فرم خنثی اتمها هستند. برای مثال، اتم سدیم با عدد اتمی ۱۱ دارای ۱۱ الکترون و ۱۱ پروتون است. این اتم با از دست دادن یک الکترون و تولید یون مثبت سدیم، دیگر خنثی نیست و بار الکتریکی ۱+ دارد.
اتم خنثی با استفاده از دریافت الکترون یا از دست دادن الکترون به دست نمیآید. تمامی اتمهایی که در حالت پایه خود بدون دریافت یا دادن الکترون قرار دارند، اتم خنثی هستند. در تصویر زیر، مشاهده میکنید شکل اتم خنثی چیست.
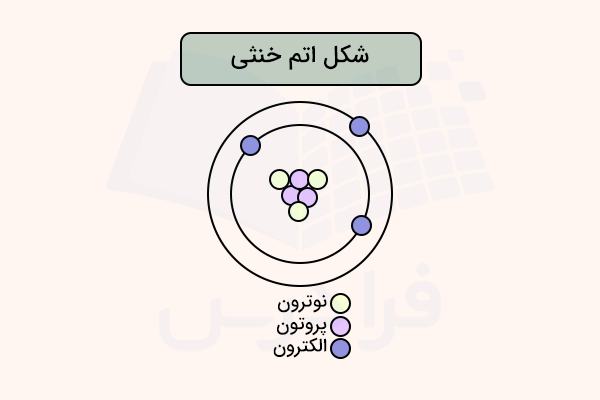
مثال اتم خنثی
هنگامی که اتم تعداد برابری الکترون و پروتون دارد، مقدار بار مثبت و منفی آن برابر خواهد بود. در نتیجه، مقدار بار الکتریکی کلی اتم برابر با صفر خواهد بود. بنابراین، تمامی عناصر موجود در جدول تناوبی عناصر در حالت خنثی قرار دارند زیرا در تمامی آنها تعداد پروتون و الکترون با هم برابر است.
روش تشخیص اتم خنثی چیست؟
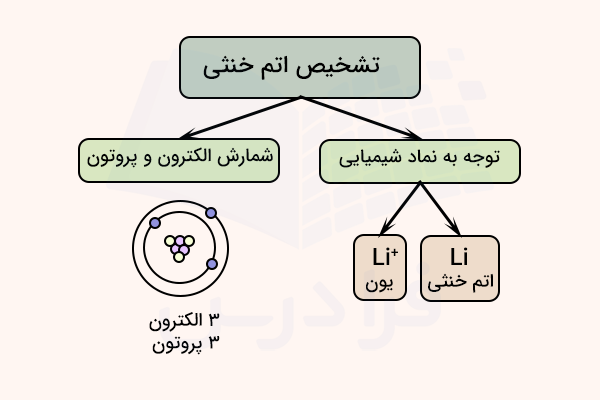
در قسمت قبل آموختیم مفهوم اتم خنثی چیست. سادهترین روش تشخیص اتم خنثی، توجه به نماد شیمیایی آن است. اتمهای خنثی بدون علامت بار در کنارشان نمایش داده میشوند. این در حالی است که مقدار بار الکتریکی یونها و ذرات باردار در کنار نماد شیمیایی آنها نمایش داده میشود.
یک روش دیگر برای تشخیص خنثی بودن اتم، شمارش تعداد الکترون و پروتونهای آن است. اگر تعداد پروتون و الکترون برابر باشد، اتم خنثی است. عدد اتمی تعداد الکترونها و پروتونهای اتم خنثی را مشخص میکند.
یادگیری علوم هشتم با فرادرس
برای درک بهتر اینکه اتم خنثی چیست، ابتدا باید با مفاهیمی چون ساختار اتم، هسته اتم، بار الکتریکی، عدد اتمی و مولکول آشنا شویم. پیشنهاد میکنیم برای آشنایی بیشتر با این مفاهیم، به مجموعه فیلم آموزش دروس پایه هشتم، بخش شیمی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه اتم خنثی دسترسی داشته باشید.
- فیلم آموزش علوم تجربی پایه هشتم بخش فیزیک فرادرس
- فیلم آموزش علوم تجربی پایه نهم بخش شیمی فرادرس
- فیلم آموزش شیمی ۱ پایه دهم + گواهینامه فرادرس
نماد شیمیایی اتم خنثی
اتم خنثی با استفاده از نماد شیمیایی عنصر و بدون مشخص کردن بار آن نمایش داده میشود. بر خلاف یونها که مقدار بار الکتریکی آنها در بالا و سمت راست نماد شیمیایی آنها نوشته میشود، اتمهای خنثی هیچ علامت یا باری در کنار نماد شیمیایی خود ندارند.
ساختار اتم
در قسمتهای قبل آموختیم مفهوم اتم خنثی چیست. برای درک بهتر این مفهوم، نیاز است ساختار اتم و اجزای آن را مرور کنیم. اتمها از الکترون، پروتون و نوترون تشکیل شدهاند. نوترونها و پروتونها در هسته اتم متراکم هستند و الکترونها در مکانهای مشخصی اطراف هسته اتم حرکت میکنند. همچنین، تمامی این ذرات از ذرات کوچکتر زیراتمی نیز تشکیل شدهاند. نیروهای الکترواستاتیک بین نوترونها و پروتونها، هسته را پایدار نگه میدارد.
اگر تا اینجای مطلب را مطالعه کردهاید، با مفهوم اتم خنثی و ویژگیهای آن آشنا شدهاید. در ادامه این مطلب نیز به بررسی بیشتر ساختار این اتمها میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی ریگان و همیشگی به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همواره به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
همچنین، هسته اتم که باری مثبت دارد، باعث پایدار ماندن الکترونها و خارج نشدن آنها از اتم در حالت پایه میشود. بدین ترتیب، برای تعادل انرژیهای الکترواستاتیک اتم، تعداد الکترون و پروتون باید برابر باشد.
پیشنهاد میکنیم برای درک بهتر این پدیده، فیلم آموزش عدد جرمی، عدد اتمی و بار اتمی فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
تشکیل یون
اگر الکترون به اتم اضافه شده یا از آن کم شود، دیگر خنثی نیست و ناپایدار میشود و تمایل دارد با اتمها یا یونهای دیگر واکنش دهد و ترکیبات شیمیایی را تولید کند. مقدار بار الکتریکی و جرم اتمی این ذرات در جدول زیر مشخص شده است.
| ذره | بار | جرم (amu) |
| الکترون | ۱- | ۰ |
| پروتون | ۱+ | ۱ |
| نوترون | ۰ | ۱ |
نوترونها نقشی در خنثی بودن اتم و تعادل بار الکتریکی اتم را ندارند. در واقع تعداد نوترونهای یک اتم با تعداد نوترونهای آنیون یا کاتیون آن برابر است. اما نوترونها نقش پایدار نگه داشتن هسته اتم و کنار هم نگه داشتن پروتونها را در هسته دارند. اگر تعداد نوترونهای یک اتم تغییر کند، واکنش هستهای رخ داده و آن اتم، به اتم جدید دیگری تبدیل میشود.
اتم چیست؟
اتم کوچکترین ساختار سازنده ماده است که خود از ذرات زیراتمی مانند الکترون، پروتون و نوترون تشکیل شده است. هر اتم عدد اتمی و تعداد پروتون منحصر به فردی دارد که آن را از سایر اتمها مجزا میکند. اتمها معمولا به صورت تکی وجود ندارند (بجز گازهای نجیب) و همواره به صورت ترکیب با سایر اتمها و ترکیبات یافت میشوند.
بار الکتریکی اتم خنثی چیست؟
بار الکتریکی اتم خنثی برابر با صفر است. زیرا در اتم خنثی، تعداد الکترونها و پروتونها برابر است. بنابراین، به ازای هر بار منفی، یک بار مثبت نیز وجود دارد که همدیگر را خنثی میکنند. در نتیجه بار کلی اتم خنثی برابر با صفر است.
اگر این تعادل با از دست دادن یا گرفتن الکترون بهم بخورد، اتم دیگر خنثی نبوده و به یون تبدیل میشود. پیشنهاد میکنیم برای درک بهتر بار این عناصر و یونهایی که میتوانند تشکیل دهند، مطلب بارهای جدول تناوبی مجله فرادرس را مطالعه کنید. برای مثال، به اتم لیتیوم و یون لیتیوم در شکل زیر دقت کنید.
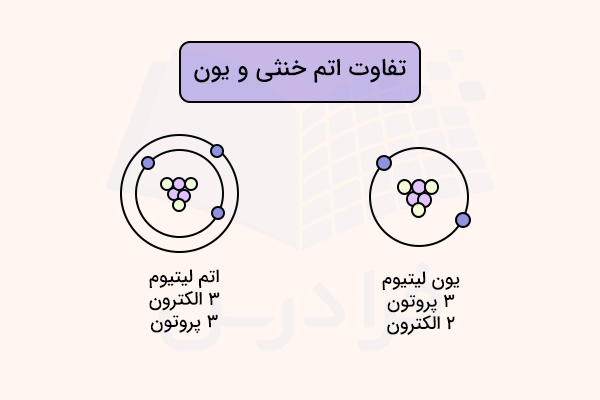
تفاوت یون و اتم خنثی چیست؟
اتم خنثی بار الکتریکی متعادلی دارد. بدین معنی که تعداد بارهای مثبت اتم خنثی برابر با تعداد بارهای منفی آن است. اما در یون، تعداد بارهای مثبت و منفی برابر نیستند. اگر تعداد الکترونهای یک یون از تعداد پروتونهای آن کمتر باشد، یون مثبت (کاتیون) تولید میشود.
در مقابل، اگر تعداد الکترونهای یک یون بیشتر از تعداد پروتونهای آن باشد، یون منفی ( آنیون) تولید میشود. آنیون و کاتیون ناپایدار هستند و به شدت تمایل دارند با یونهای دیگر پیوند یونی تشکیل داده و به تعادل بار برسند. در حالی که اتمهای خنثی معمولا پایدار هستند و پیوندهای ضعیفتری (پیوند کووالانسی) برقرار میکنند.
تفاوت اندازه اتم خنثی و یون
آنیونها از اتم خنثی بزرگتر و کاتیونها از اتم خنثی کوچکتر هستند. زیرا، آنیون نسبت به اتم خنثی الکترون بیشتری دارد. این الکترونهای بیشتر میتوانند در لایههای الکترونی بالاتر قرار گرفته و شعاع آنیون را نسبت به اتم خنثی افزایش دهند. همچنین، وجود الکترونهای بیشتر در آنیونها، باعث افزایش نیروی دافعه بین آنها شده و مقداری بیشتر از الکترونهای اتم خنثی از هم فاصله میگیرند. در نتیجه شعاع آنیون بیشتر از شعاع اتم خنثی خواهد بود. این پدیده در تصویر زیر برای اتم مشخص شده است.
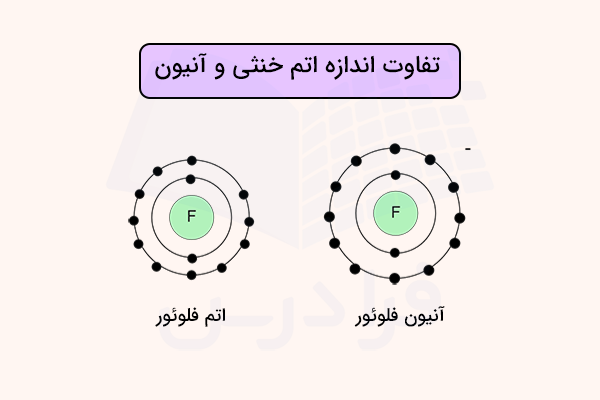
در مقابل، کاتیون، تعداد الکترون کمتری نسبت به اتم خنثی دارد. الکترون از دست رفته، میتواند تعداد لایههای الکترونی را کاهش داده و باعث کوچکتر شدن شعاع کاتیون نسبت به اتم خنثی شود. همچین، تعداد الکترون کمتر کاتیون باعث کاهش اثر دافعه بین الکترونها شده و همچنین، اثر بار مثبت هسته بر الکترونهای باقی مانده افزایش مییابد. در نتیجه، الکترونهای باقی مانده جمعتر شده و شعاع کاتیون نسبت به اتم خنثی کمتر خواهد بود. این پدیده در تصویر زیر برای اتم مشخص شده است.
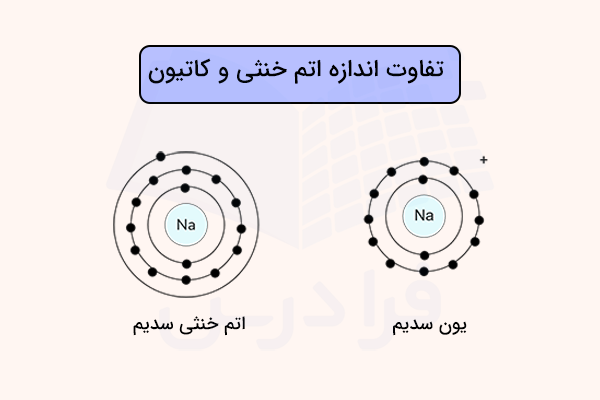
کاربرد اتم خنثی
در این مطلب از مجله فرادرس آموختیم اتم خنثی چیست. اتمهای خنثی به صورت عمده در دستکاری و نمایش کیوبیتها در اطلاعات کوانتومی کاربرد دارند. این اطلاعات در مواردی مانند کامپیوتر کوانتومی و رمزنگاری کوانتومی کاربرد دارند. کیوبیت (کوانتوم بیت) یا بیت کوانتومی، یک واحد از اطلاعات کوانتومی است. اتم خنثی با استفاده از سطوح انرژی درونی آنها مانند حالت ریدبرگ، به عنوان کیوبیت استفاده میشوند.
محاسبات کوانتومی بر پایه استفاده از اتم خنثی، در بسیاری از زمینههای تحقیقاتی و پژوهشی استفاده میشود و در شبیهسازی کوانتومی، بهینهسازی، کریپتوگرافی و ... کاربرد دارد.