کروماتوگرافی چیست؟ – به زبان ساده
کروماتوگرافی یک روش تحلیلی است که به طور معمول برای جداسازی اجزای تشکیل دهنده یک مخلوط شیمیایی بکار میرود. در نتیجه، با روش «کروماتوگرافی» (Chromatography)، به خوبی میتوان اجزای تشکیل دهنده مخلوطها را تحلیل و بررسی کرد. روشهای مختلفی در کروماتوگرافی وجود دارند که عبارتند از: کروماتوگرافی مایع، کروماتوگرافی گازی، «کروماتوگرافی تبادل یونی» (Ion-Exchange Chromatography) و «کروماتوگرافی میل ترکیبی» (Affinity Chromatography) که همه این روشها اساس یکسانی دارند.
مقدمه
کروماتوگرافی یک روش جداسازی است که هر شیمیدان و بیوشیمیست با آن آشنایی دارد. فرض کنید که دو واکنشدهنده A و B داشته باشیم و آنها را با یکدیگر وارد واکنش کنیم تا فرآوردهی C را تولید کنند. در پایان واکنش، مخلوطی از فرآورده C و واکنشدهندههای A و B داریم که در واکنش شرکت نکردهاند.
کروماتوگرافی به ما کمک میکند تا واکنشدهندهها و فرآوردهها را در مخلوط از یکدیگر جدا کنیم و به خوبی بتوانیم فرآورده C را مورد بررسی قرار دهیم.
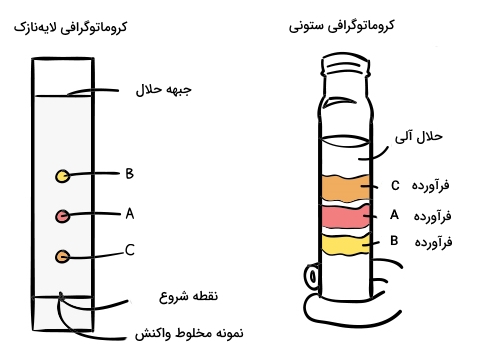
تصویر سمت چپ، یک کروماتوگرافی لایه نازک را نشان میدهد. کافی است تا چند قطره از مخلوط را در پایین این ورقه شیشهای بریزیم. این ورقه شیشهای با لایه نازکی از سیلیکا اندود شده است. انتهای این ورقه را در ظرفی قرار میدهیم که حاوی حلال آلی مناسبی باشد. به کمک نیروی «مویینگی» (Cappillary)، ماده حلال در روی ورقهای شیشهای به سمت بالا حرکت میکند و همانطور که در تصویر مشخص است، اجزای مخلوط حاصل به هنگام حرکت به سمت بالا، در ۳ نقطه با رنگهای مختلف از یکدیگر جدا شدهاند.
کروماتوگرافی ستونی
در حالت دوم که در سمت راست تصویر بالا دیده میشود، از یک ستون شیشهای استفاده شده که از پایین به یک شیر متصل است. این ستون را با سیلیکاژل و حلال آلی پر میکنیم. در مرحله بعد، مخلوط حاصل از واکنش را به آرامی از بالا اضافه و شیر پایین را باز میکنیم تا مخلوط در ستون حرکت کند. همانطور که ملاحظه میکنید، در نهایت، مخلوط حاصل با سه نوار رنگی جدا میشود که میتوان هر کدام را جداگانه جمعآوری کرد.
اصول کروماتوگرافی
در ابتدا بهتر است با عباراتی که در کروماتوگرافی مورد استفاده قرار میگیرند آشنا شویم.
| واژه | تعریف |
| فاز متحرک (حامل) | حلال متحرک در ستون کروماتوگرافی |
| فاز ساکن (جاذب) | مادهای که در ستون، ثابت میماند. |
| «شوینده» (Eluent) | مادهای که وارد ستون کروماتوگرافی میشود. |
| «محصول شویش» (Eluate) | مادهای که در بالون جمعآوری میشود. |
| «شویش» (Elution) | فرآیند شستشوی ترکیب از طریق ستون کروماتوگرافی و به کمک یک حلال مناسب |
| «آنالیت» (Analyte) | مخلوط مورد بررسی یا مخلوطی که اجزای آن باید جداسازی شوند. |
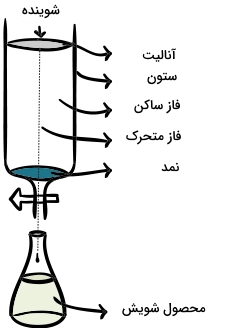
همانطور که در بالا نشان داده شد، آنالیت را در بالای یک بستر سیلیسی قرار میدهیم و به آن زمان میدهیم تا به سیلیس (سیلیکا) بچسبد. در اینجا، سیلیکا نقش فاز ساکن را ایفا میکند. سپس حلال (فاز متحرک) به کمک نیروی جاذبه یا فشار، وادار به حرکت از میان بستر سیلیسی میشود. اجزای مختلف آنالیت، درجات مختلفی از چسبندگی به سیلیس را از خود نشان میدهند.
در نتیجه، این اجزا با سرعتهای متفاوتی از میان فاز ساکن عبور میکنند و به هنگام عبور، از یکدیگر جدا میشوند که این جدایش را به صورت نوارهای رنگی مختلفی میتوان از یکدیگر تشخیص داد. جزئی که به شدت به آنالیز جذب میشود، سرعت حرکت کمتری در مقابل دیگر اجزا خواهد داشت. لازم به ذکر است که از کروماتوگرافی میتوان برای خالصسازی ترکیبات از مقیاس میلیگرم تا گرم استفاده کرد.
قبل از ادامه، بهتر است آزمایشی را انجام دهیم تا قدرت کروماتوگرافی را بهتر نشان دهد.
- در مرحله اول مقداری برگ جمع کنید و در ظرفی آنها را خرد کنید.
- قطرهای از این عصاره برگ را در حدود نیم سانتیمتر بالاتر از لبه کاغذ، روی کاغذ کروماتوگرافی بریزید. کاغذ کروماتوگرافی از سلولوز ساخته شده است و تقریبا قطبی است.
- نوار کاغذی را در شیشهای حاوی استون قرار دهید. مقدار استون باید به گونهای باشد که لبه پایینی کاغذ به خوبی در آن غوطهور شود. بمنظور جلوگیری از تبخیر محلول، روی ظرف را با درب بپوشانید.
- به محلول فرصت دهید تا به کمک نیروی مویینگی، از داخل کاغذ به طرف بالا حرکت کند. زمانی که حلال به نقطه نهایی خود رسید، آن را از داخل شیشه خارج کنید و مشاهدات خود را یادداشت کنید. اجزای مختلف تشکیلدهنده رنگِ برگ از یکدیگر جدا خواهند شد. آیا میدانستید که رنگ یک برگ از ترکیبات متعددی تشکیل شده است؟
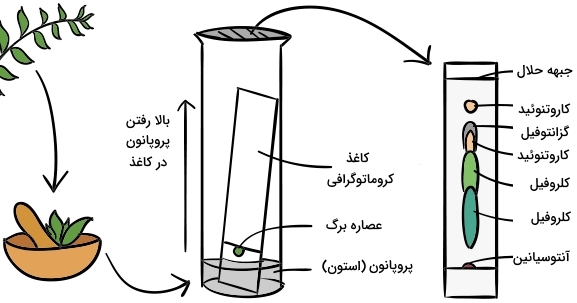
اصول جداسازی ترکیبات مختلف
قدرت چسبندگی اجزای مختلف یک آنالیت در عبور از فاز ساکن، دلیل جدایش این اجزا از یکدیگر به شمار میآید. «میل ترکیبی» (Affinity)، توسط دو خاصیت مولکول موسوم به «جذب» (Adsorption) و «انحلالپذیری» (Solubility)، تعیین میشود.
جذب، خاصیتی است که به نحوه چگونگی چسبندگی اجزای مختلف یک مخلوط به فاز ساکن میپردازد؛ درحالیکه انحلالپذیری، مرتبط با انحلال آن اجزا در فاز متحرک است. هر قدر جذب شدن به فاز ساکن بیشتر باشد، مولکولها در ستون کروماتوگرافی آهستهتر حرکت خواهند کرد. همچنین هر قدر انحلالپذیری در فاز متحرک بیشتر باشد، سرعت مولکول در ستون نیز بیشتر خواهد بود.
در نتیجه برهمکنشهای بالا، مشخص خواهد شد که هر جزء آنالیت، با چه سرعتی در ستون حرکت خواهد کرد. جذب و انحلالپذیری یک مولکول را میتوان با انتخاب صحیح فاز متحرک و ساکن، تغییر داد.
حال این سوال پیش میآید که چرا ترکیبات مختلف، میل ترکیبی مختلفی در رابطه با فاز متحرک و ساکن دارند. در پاسخ به این سوال باید گفت که قطبیت یک ترکیب، این حالت را مشخص میکند. بهتر است این مورد را به کمک یک مثال توضیح دهیم. فرض کنید مخلوطی از دو مولکول A و B داریم. مولکول A، پروتئین و مولکول B، لیپید است. ستون کروماتوگرافی ما نیز شامل سیلیس میشود که در طبیعت خاصیتی قطبی دارد. همچنین، فاز متحرک، هگزان و ناقطبی است. به نظر شما چه اتفاقی خواهد افتاد اگر این ترکیب را در ستون کروماتوگرافی وارد کنیم؟
مولکول A که قطبی است، جذب فاز ساکن قطبی خواهد شد. مولکول B نیز به سادگی در فاز متحرک ناقطبی حل میشود و به سیلیس نمیچسبد. در نتیجه به همراه هگزان، از محلول شسته خواهد شد. زمانی که B خارج شود، فاز متحرک را به یک فاز قطبی همچون «استونیتریل» (Acetonitrile) تغییر میدهیم. با انجام چنین کاری، مولکول A را به جدا شدن از سیلیس و حلشدن در حلال قطبی وادار کردهایم. در نتیجه، مولکول A، به همراه استونیتریل از ستون شسته (شویش) میشود. تصویر زیر، بیانگر موارد بالا است.
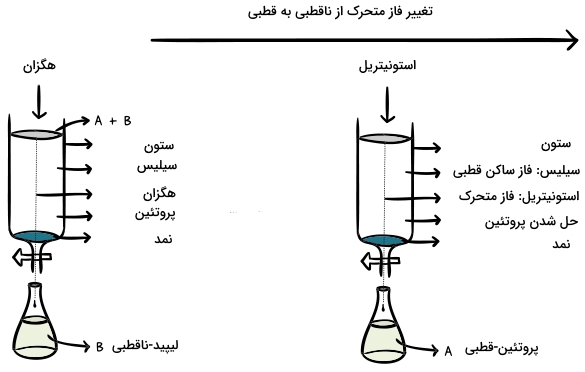
انواع مختلف کروماتوگرافی
در طول این مقاله در خصوص «کروماتوگرافی فاز نرمال» (Normal-phase Chromatography) صحبت میکنیم. این نوع از کروماتوگرافی، حالتی است که در آن، فاز ساکن، قطبی (آبدوست) و فاز متحرک، ناقطبی (آبگریز) باشد. در مواردی برای کاربردهایی خاص، دانشمندان از «کروماتوگرافی فاز معکوس» (Reverse-phase Chromatography) استفاده میکنند که قطبیت فاز ساکن و متحرک، عکس حالت قبل است.
انواع مختلفی از کروماتوگرافی وجود دارد که هر کدام در نوع فاز متحرک و ساکن تفاوت دارند. البته اصل کلی در همه این روشها یکسان است: تمایل اجزای مختلف آنالیت به فازهای ساکن و متحرک، سبب جدایش این اجزا میشوند. همانطور که بالاتر نیز به آن اشاره شد، نوع برهمکنش اجزا با فازهای ساکن و متحرک، بسته به نوع روش کروماتوگرافی ممکن است متفاوت باشد. در جدول زیر، روشهای معمول در کروماتوگرافی آورده شده است:
| روش | فاز ساکن | فاز متحرک | اساس جداسازی |
| کروماتوگرافی کاغذی | جامد (سلولز) | مایع | قطبیت مولکولها |
| کروماتوگرافی لایه نازک | جامد (سیلیس یا آلومینا) | مایع | قطبیت مولکولها |
| کروماتوگرافی مایع | جامد (سیلیس یا آلومینا) | مایع | قطبیت مولکولها |
| کروماتوگرافی اندازه طردی | جامد (دانههای ریزمتخلخل از سیلیس) | مایع | اندازه مولکولها |
| کروماتوگرافی تبادل یونی | جامد (رزین کاتیونی یا آنیونی) | مایع | بار یونی مولکولها |
| کروماتوگرافی میل ترکیبی | جامد (آگارز) | مایع | تمایل ترکیبی مولکول آنالیت به مولکول تثبیتشده در فاز ساکن |
| کروماتوگرافی گاز | مایع یا جامد | گاز | نقطه جوش مولکولها |
کروماتوگرافی تقسیمی
«کروماتوگرافی تقسیمی» (Partition Chromatography) یکی از انواع روشهای جداسازی است که در آن، اجزای مخلوط به دو فاز تقسیم میشوند و فازهای ساکن و متحرک، هردو در یک فاز قرار دارند و بنابراین مولکولها در هر دوفاز پراکنده خواهند شد. کروماتوگرافی تقسیمی را به عنوان روش جداسازی اجزای حلشونده به کمک تقسیم شدن حلشونده بین دو فاز مایع مینامند. البته ما در این آموزش قصد داریم تا با مفاهیم ابتدایی کروماتوگرافی لایه نازک آشنا شویم.
کروماتوگرافی TLC
برای اینکه دوباره مروری کرده باشیم باید اشاره کنیم که «کروماتوگرافی لایه نازک» (Thin Layer Chromatography) که به TLC معروف است، بر روی یک لایه شیشهای اندود شده با سیلیس انجام میشود. در این کروماتوگرافی فاز نرمال، سیلیس به عنوان فاز ساکن و حلال که لایه شیشهای داخل آن قرار میگیرد، به عنوان فاز متحرک عمل میکند. فاز ساکن (سیلیس)، به شدت قطبی است درحالیکه حلال در مقایسه با سیلیس، قطبیت کمتری دارد.
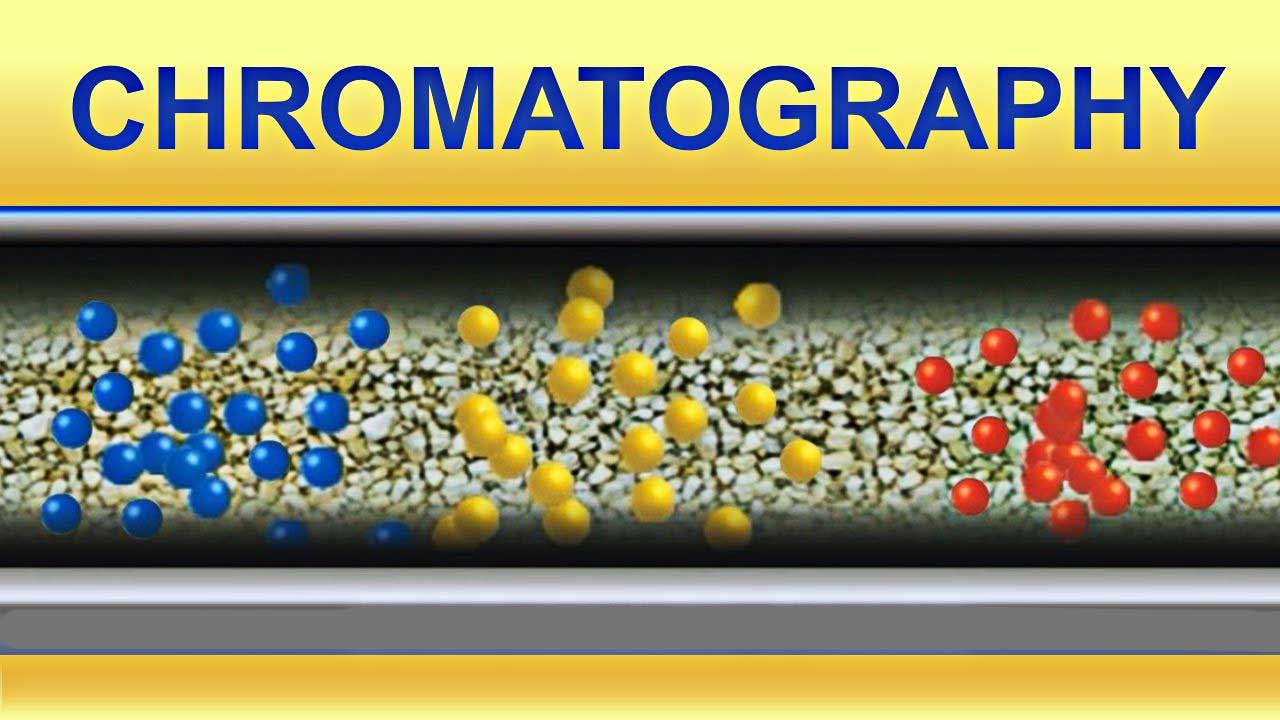
اجزای قطبی آنالیت، با قدرت به سیلیکا میچسبند و در نتیجه، با سرعت کمی در طول لایه شیشهای به طرف بالا حرکت میکنند. اجزای ناقطبی یا اجزایی که کمتر قطبی هستند نیز به دلیل چسبندگی کم به سیلیس، با سرعت بیشتری به همراه حلال در طول لایه شیشهای حرکت خواهند کرد. حال بهتر است دوباره نگاهی به تصویر ابتدای مقاله بیاندازیم:
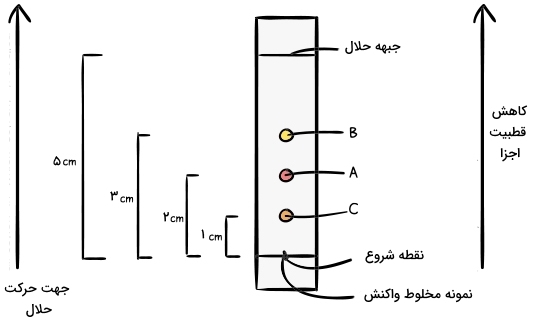
همانطور که در بالا نشان داده شده است، ۳ جزء A، B و C از مخلوط، فاصلههای متفاوتی را در طول لایه TLC طی کردهاند. اندازهگیریها نشان میدهد که جزء C، یک سانتیمتر، جزء A دو سانتیمتر و جزء B، سه سانتیمتر در طول لایه حرکت کردهاند. حلال نیز ۵ سانتیمتر از نقطه شروع تا رسیدن به نقطه پایانی موسوم به «جبهه حلال» (Solvent Front)، حرکت کرده است.
به عنوان یک قانون سرانگشتی میتوان ذکر کرد که جزئی که از همه کمتر بر روی لایه TLC حرکت کرده باشد، بیشترین قطبیت را دارد، چراکه به شدت به سیلیس میچسبد. در مقابل، جزئی که بیشترین مسافت را در طول لایه طی کرده باشد، خاصیت ناقطبی بیشتری دارد و به علت انحلال در فاز متحرک، حرکت آن نیز بیشتر خواهد بود.
تشخیص قطبیت ماده با مشاهده لایه TLC
در نتیجه، کافی است تا به لایه TLC نگاه کنید تا ببینید کدامیک از اجزا قطبیت بیشتری دارند و کدامیک کمتر. البته در کروماتوگرافی لایه نازک، یک پارامتر کمی نیز وجود دارد که به آن «ضریب بازداری» (Retention Factor) میگویند و آن را با نشان میدهند. ضریب (عامل) بازداری را میتوان برای هر جزء، جداگانه حساب کرد و مقدار آن در سنتزهای شیمیایی بسیار پرکاربرد است. مقدار ضریب بازداری را به طور دقیق در مقالات علمی ذکر میکنند تا اگر شخصی از روی مقاله علمی در حال تحقیق باشد بتواند به همان مقادیر دست پیدا کند.
عامل بازداری عبارتست از فاصله طی شده توسط یک جزء مشخص تقسیم بر کل فاصله طی شده توسط حلال. هرقدر مقدار کمتر باشد، ماده مورد نظر قطبیتر است. جدول زیر، فواصل طی شده و میزان عامل بازداری را در خصوص آزمایش بالا نشان میدهد. بر اساس مقادیر ذکر شده، میتوان دریافت که جزء C بیشترین قطبیت و جزء B کمترین قطبیت را دارد.
| جزء | فاصله طی شده توسط اجزا (سانتیمتر) | فاصله طی شده توسط حلال (سانتیمتر) | ضریب بازداری |
| C | 1 | 5 | |
| A | 2 | 5 | |
| B | 3 | 5 |
ستون کروماتوگرافی
ستون کروماتوگرافی، ابزاری است که در کروماتوگرافی از آن استفاده میکنند. پنج روش کروماتوگرافی که در آن از ستون کروماتوگرافی بهره میگیرند عبارتند از:
- گازی
- مایع
- «تبادل یونی» (Ion Exchange)
- «اندازه طردی» (Size Exclusion)
- «کایرال» (Chiral)
در کروماتوگرافی گازی، فاز متحرک، گاز است. ستون کروماتوگرافی در این روش در حدود 1-100 متر طول دارد. در کروماتوگرافی گاز-مایع (GLC)، فاز مایعِ ساکن، با سطح باز ستون لوله مویین یا مواد جامد پرشده داخل ستون پیوند دارد. تطبیق قطبیت آنالیت و فاز ساکن، دانش دقیقی را شامل نمیشود اما این دو باید قطبیت یکسانی داشته باشند. ضخامت فاز ساکن به طور معمول بین 0/1 تا 8 میکرومتر است. هرقدر لایه ضخیمتر باشد، آنالیت فرارتر خواهد بود.
ستون کروماتوگرافی با عملکرد بالا
«ستون کروماتوگرافی با عملکرد بالا» (High Performance Liquid Chromatographic Columns) که به ستونهای HPLC معروف هستند از یک فاز متحرک مایع استفاده میکنند. این نوع از کروماتوگرافی را که با نام کروماتوگرافی مایع نیز میشناسند، از همان اصول کروماتوگرافی گازی استفاده میکند. سه نوع مختلف از ستونهای مایع داریم:
- مایع-مایع: دارای فاز ساکنِ مایع هستند که به سطح ستون یا مواد پرشده جذب شدهاند. پایداری این نوع از ستونها پایین است و به همین سبب، استفاده از آنها رواج ندارد. همچنین، عمل «بخشبندی» (Partitioning) نیز بین دو مایعِ متفاوت در فازهای ساکن و متحرک، رخ خواهد داد.
- مایع-جامد: در این ستون، فاز ساکن، جامد است و آنالیت به فاز ساکن جذب میشود.
- تبادل یونی: در ستون تبادل یونی، فاز ساکن را نوعی رزین تشکیل میدهد و همچنین عمل بخشبندی بین آنالیت و فاز ساکن انجام میشود.
به طور معمول، ستون HPLC شامل یک ستون محافظ نیز هست. این ستون محافظ را جهت افزایش عمر و همچنین محافظت از ستون اصلی (تحلیلی) بکار میبرند که میتواند موجب فیلتر کردن و حذف ریزگردها، آلودگیها و مولکولهای متصل به ستون اصلی شود. این ستون محافظ نیز، فاز ساکنی مشابه با ستون اصلی دارد.
بیشتر ستونهای HPLC معمول از فولاد ضدزنگ ساخته شدهاند اما ستونهایی شامل مواد زیر نیز تهیه و تولید شدهاند:
- شیشه ضخیم
- پلیمری همچون «پلیاتر اترکتون» (Polyetherethelketone)
- ترکیبی از شیشه و فولاد ضدزنگ
- ترکیبی از فولاد ضدزنگ و پلیمر
در ستونهای HPLC، طول ستون تحلیلی معمولا بین ۳ تا ۲۵ سانتیمتر است و قطری در حدود ۱ تا ۵ میلیمتر و موادی که آن را پرمیکنند، قطری در حدود ۱ تا ۵ میکرومتر دارند. در ستونهای مایع، زمانی که قطر مواد پرکننده ستون، کاهش یابد، بازده افزایش پیدا میکند.

ماده پر شده در ستون
ستونهای HPLC به طور معمول از ذرات متخلخل یا «غشایی» (Pellicular) تشکیل شده است. ذرات غشایی از پلیمر یا شیشه ساخته شدهاند. این ذرات، با لایهای یکسان از سیلیس، رزین سنتزی، آلومینا یا سایر رزینهای تبادل یونی احاطه شدهاند. قطر این ذرات بین ۳۰-۴۰ میکرومتر است. البته از ذرات متخلخل استفادههای بیشتری میشود که قطری بین ۳ تا ۱۰ میکرومتر دارند. ذرات متخلخل نیز از سیلیس، رزین سنتزی، آلومینا و دیگر رزینهای تبادل یونی ساخته شدهاند. در بین مواد مختلف، سیلیس بیشترین کاربرد را در بین ذرات متخلخل دارد.
HPLC فاز نرمال و معکوس
به منظور انجام HPLC نرمال، از یک فاز ساکن با خاصیت قطبی و یک فاز متحرک ناقطبی استفاده میشود. در زمان انجام HPLC فاز نرمال، ابتدا ترکیباتی که بیشترین خاصیت ناقطبی را دارند شویش خواهند شد. در فاز معکوس، از یک فاز متحرک قطبی و یک فاز ساکن ناقطبی بهره میگیرند. روش فاز معکوس، معمولترین روش در کروماتوگرفی مایع به شمار میآید. در این روش همچنین میتوان از آب به عنوان فاز متحرک استفاده کرد چراکه مادهای ارزان، غیرسمی و در محدوده پرتو فرابنفش، نامرئی است. در این روش، ابتدا قطبیترین ترکیبات شویش خواهند شد.
ستون کروماتوگرافی تبادل یونی
برای جدا کردن یونها و مولکولهایی که به سادگی یونیزه میشوند، از ستون کروماتوگرافی تبادل یونی بهره میگیرند. جدایش یونها به تمایل آنها به فاز ساکن بستگی دارد که این عمل در نهایت، یک سیستم تبادل یونی را ایجاد میکند. برهمکنش الکترواستاتیک بین آنالیت، فاز متحرک و فاز ساکن موجب جدایش یون در نمونه میشود.
مواد معمول پرکننده در این ستونها شامل آمینها، سولفونیک اسید، «خاک دیاتومه» (Diatomaceous Earth)، رزینهای اتصال عرضی (کراسلینک)، و «استایرین دیوینیل بنزن» (Styrene-Divinylbenzene) موسوم به DVB هستند. از اولین «تبادلگرهای یونی» (Ion Exchangers)، آلومینوسیلیکات (زئولیت) بود که البته کاربرد فراوانی ندارد.
ستون کروماتوگرافی اندازه طردی
این ستون، مولکولها را بر اساس اندازه آنها جداسازی میکند و وزن مولکولی در این روش دخیل نیست. از «غربالهای مولکولی» (Molecular Sieves) به عنوان ماده پرکننده این ستونها بهره میگیرند. غربالهای مولکولی، حفراتی دارند که مولکولهای کوچک وارد آنها میشوند اما مولکولهای بزرگ نمیتوانند وارد شوند. این امر موجب خواهد شد که مولکولهای بزرگتر، با سرعت بیشتری نسبت به مولکولهای کوچکتر، از داخل ستون عبور کنند. از پلیساکارید و سایر پلیمرها و همچنین سیلیس، به عنوان مواد پرکننده استفاده میکنند. اندازه حفرات برای این روش بین 4 تا 200 نانومتر است.

ستونهای کایرال
این نوع از ستونها برای جداسازی انانتیومرها مورد استفاده قرار میگیرند. جداسازی مولکولهای کایرال، مرتبط با مبحث شیمی فضایی (استریو شیمی) است. فاز ساکن این نوع از ستونها، به طور انتخابی با انانتیومرها برهمکنش انجام میدهد. این نوع از ستونها برای جداسازی مخلوطهای راسمیک بسیار مناسب هستند. برخی از فازهای ساکن مورد استفاده در این ستونها برای جداسازی انانتیومرها در جدول زیر آورده شدهاند.
| فاز ساکن | روش مورد استفاده |
| عامل کلاته کننده فلزی | کروماتوگرافی گازی و کروماتوگرافی مایع |
| مشتقات آمینواسید | کروماتوگرافی گازی و کروماتوگرافی مایع |
| پروتئینها | کروماتوگرافی مایع |
| پلیمرها | کروماتوگرافی مایع |
| مشتقات سیکلودکسترین | کروماتوگرافی گازی و کروماتوگرافی مایع |
بازده ستون
هرقدر یک ماده، مدت زمان بیشتری در ستون کروماتوگرافی باشد، پیکهای (قلههای) حاصل از کروماتوگرافی، عریضتر میشوند. برای بهبود جدایش مواد در ستون، میتوان طول ستون را افزایش داد. علاوه بر این، برای افزایش بازدهی ستون، دمای آن باید ثابت باشد. ارتفاع «سینیها» (Plates) و عدد «سینیهای نظری» (Theoretical Plates)، از عوامل تعیین کننده در بازده ستون به شمار میآیند.
بمنظور افزایش بازده ستون، باید عدد سینیها افزایش و ارتفاع آنها کاهش یابند. عدد سینیها را میتوان از رابطههای زیر محاسبه کرد که در این روابط، L، طول ستون و H، ارتفاع هر سینی است:
$$N=5.54left(\dfrac{t_R}{W_{1/2}}\right)^2$$
در رابطه بالا:
- : «زمان بازداری» (Retention Time)
- : عرض پیک (قله)
- : نصف عرض پیک
ارتفاع معادل سینی نظری (HETP) را میتوان از طریق رابطه زیر محاسبه کرد:
همچنین این ارتفاع را میتوان به کمک «رابطه فن-بیمتر» (van-Beemter) محاسبه کرد:
- : عبارت مربوط به «نفوذ اددی» (Eddy Diffusion)
- : عبارت مربوط به «نفوذ طولی» (Longitudinal Diffusion)
- : ضریب انتقال جرم بین فاز ساکن و متحرک
- : سرعت خطی
معادله HETP را معمولا برای توصیف راندمان ستون بکار میبرند. ستونی با راندمان بالا، باید مقدار HETP پایینی داشته باشد. باید به این نکته اشاره کرد که ارتفاع ستونهای کروماتوگرافی گاز، تا ۱۰۰ متر نیز میرسد اما این ارتفاع برای ستونهای کروماتوگرافی مایع در حدود 25 سانتیمتر است.
اگر این مطلب برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای مهندسی شیمی
- آموزش مقدماتی شیمی تجزیه دستگاهی
- فیلتراسیون در شیمی — از صفر تا صد
- محلولها — به زبان ساده
^^








سلام ممنون بابت مطلب کامل شما. موفق باشید
سلام خواستم زوش عملی شو یاد بگیرم
خیلی خوب توضیح داده بودید تشکر