واکنش فریدل کرافتس – به زبان ساده
واکنش فریدل کرافتس به دستهای از واکنشهای شیمیایی میگویند که توسط «شارل فریدل» (Charles Friedel) و «جیمز کرافتس» (James Crafts) در سال ۱۸۷۷ توسعه پیدا کردند تا یک گروه استخلافی (جانشین) به یک حلقه آروماتیکی متصل شود. واکنش فریدل کرافتس دو نوع اصلی به نام واکنش آلکیلاسیون و واکنش آسیلاسیون دارد که هردو در اثر واکنش جانشینی الکتروفیلی آروماتیک اتفاق میافتند.


در تصویر زیر، هر دو نوع واکنش فریدل کرافتس در حلقه بنزنی نمایش داده شده است.

میتوان دریافت که هرکدام از این واکنشها شامل حذف اتم هیدروژن متصل به حلقه آروماتیک به کمک یک الکتروفیل (الکتروندوست) است. در واکنش فریدل کرافتس به طور معمول از آلومینیم تریکلرید () به عنوان کاتالیزور استفاده میشود چراکه در نقش اسید لوویس عمل میکند و در فرآیند سبب ایجاد یک الکتروفیل میشود.
آلکیلاسیون فریدل کرافتس
آلکیلاسیون فریدل کرافتس عبارتست از جایگزینی یک پروتون در حلقه آروماتیک با یک گروه آلکیل. این امر در اثر «حمله الکتروفیلی» (Electrophilic Attack) بر حلقه آروماتیک به کمک یک کربوکاتیون صورت میگیرد.
واکنش آلکیلاسیون فریدل کرافتس روشی برای تولید آلکیلبنزنها با استفاده از آلکیل هالیدها به عنوان واکنشدهنده است. واکنش آلکیلاسیون فریدل کرافتس را در تصویر زیر مشاهده میکنید
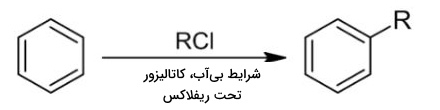
در این واکنش، یک کاتالیزور اسید لوییس همچون یا بکار گرفته میشود تا تشکیل کربوکاتیون را با تسهیل حذف هالوژن، امکانپذیر کند. کربوکاتیون حاصل، پیش از پیشرفت واکنش، دچار بازآرایی میشود.
مکانیسم آلکیلاسیون فریدل کرافتس
مکانیسم واکنش آلکیلاسیون فریدل کرافتس در یک مکانیسم سهمرحلهای انجام میشود:
مرحله اول
یک کاتالیزور (اسید لوییس) همچون با آلکیل هالید وارد واکنش میشود و یک کربوکاتیون الکتروفیل ایجاد میکند.
مرحله دوم
کربوکاتیون با حمله به حلقه آروماتیک، یک کاتیون «سیکلوهگزادینیل» (Cyclohexadienyl) به عنوان ماده واسط تولید میکند. در اثر شکست پیوند دوگانه کربن-کربن، به طور موقت، آروماتیسیته این ترکیب از دست میرود.
مرحله سوم
پروتونگیری از ترکیب واسط سبب تشکیل مجدد پیوند دوگانه کربن-کربن و بازگشت خاصیت آروماتیکی میشود. در ادامه نیز پروتون سبب تشکیل هیدروکلریک اسید و تولید مجدد خواهد شد. در تصویر زیر، این مکانیسم فریدل کرافتس را مشاهده میکنید.

محدودیت های آلکیلاسیون فریدل کرافتس
زمانی که بخواهید زنجیر کربنی با بیش از ۲ اتم کربن اضافه کنید، امکان بازآرایی (نوآرایی) کربوکاتیون وجود دارد. این بازآرایی به دلیل «جابجایی هیدرید» (Hydride Shift) و جابجایی متیل رخ میدهد.از نمونههای این بازآرایی میتوان به واکنش زیر اشاره کرد. از جمله راهحلهای این مشکل، بکارگیری واکنش آسیلاسیون فریدل کرافتس است.

همچنین، واکنش تنها زمانی رخ میدهد که حلقه اضافه شده به گروه استخلافی، غیرفعال نشده باشد. زمانیکه که در واکنش فریدل کرافتس از ترکیبات غیرفعال کننده همچون نیتروبنزن استفاده شود، واکنش انجام نخواهد شد.

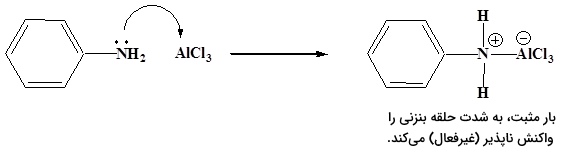
در اثر این اتفاق، واکنش فریدل کرافتس پیشروی نخواهد کرد و حلقه آروماتیک شامل گروههای ، یا خواهد بود. جفتالکترون ناپیوندی بر روی آمینها با اسید لوییس واکنش میدهد. این امر، بار مثبتی را در کنار حلقه بنزنی قرار میدهد که مانع از پیشرفت واکنش فریدل-کرافتس میشود.
در نهایت، آلکیلاسیون فریدل کرافتس میتواند در واکنشهای پلیآلکیلاسیون شرکت کند. در اثر این واکنش، گروه آلکیل الکتروندهنده اضافه میشود و در حقیقت، بیش از یک گروه آلکیل به حلقه آروماتیکی اضافه خواهد شد. برای جلوگیری از این اتفاق باید ترکیب آروماتیک را با مقدار اضافی در واکنش شرکت داد .چنین مشکلی در آسیلاسیون فریدل کرافتس رخ نخواهد داد

آسیلاسیون فریدل کرافتس
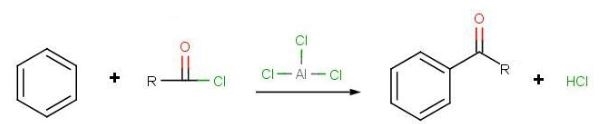
آسیلاسیون فریدل کرافتس شامل افزایش یک گروه «آسیل» (Acyl) به یک حلقه آروماتیک است. به طور معمول، این کار از طریق بکارگیری یک اسید کلرید و یک اسید لوویس همچون خواهد بود. در واکنش آسیلاسیون فریدل کرافتس، حلقه آروماتیک به یک کتون تبدیل میشود. واکنش بین بنزن و آسیل کلرید تحت این شرایط، در تصویر زیر آورده شده است.

در این واکنش، میتوان به جای یک آسیل هالید از اسید انیدرید استفاده کرد. هالوژن مرتبط با آسیل هالید، با اسید لوییس یک کمپلکس تشکیل میدهد و سبب تولید الکتروفیلی به نام یون آسیلیوم میشود. این یون، فرمول عمومی به صورت دارد پایداری آن از طریق رزونانس صورت میگیرد.
مکانیسم آسیلاسیون فریدل کرافتس
مکانیسم آسیلاسیون فریدل-کرافتس شامل چهار مرحله است که در نهایت، واکنشی به شکل زیر خواهد بود.
مرحله اول شامل تشکیل یون آسیلیوم است که در ادامه، با بنزن واکنش میدهد.
در مرحله دوم، یون آسیلیوم به عنوان یک الکتروفیل جدید به حلقه آروماتیکی حمله میکند که در اثر این اتقاق، یک کمپلکس جدید ایجاد خواهد شد.

در مرحله سوم، با خروج پروتون، به طور مجدد در بنزن، خاصیت آروماتیکی خواهیم داشت.

در طول مرحله سوم، به طور مجدد با شرکت در واکنش سبب حذف یک پروتون از حلقه بنزن خواهد شد و امکان بازگشت حلقه به آروماتیسیته را ایجاد میکند. در اثر این اتفاق، ، دوباره برای استفاده مجدد همراه با ، تولید میشود. از همه مهمتر اینکه بخش اول فرآورده نهایی واکنش، یعنی یک کتون، به تولید میرسد. بخش اول این فرآورده، نوعی کمپلکس با آلومینیوم کلرید است که در تصویر زیر نمایش داده شده است.
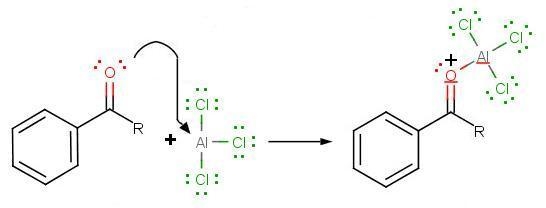
مرحله نهایی، شامل افزایش آب بمنظور تولید فرآورده نهایی به شکل آسیلبنزن خواهد بود.

محدودیت های آسیلاسیون فریدل کرافتس
بر خلاف غلبه بر محدودیتهای آلکیلاسیون فریدل-کرافتس، این واکنش، با محدودیتهایی مواجه است که در ادامه به آن خواهیم پرداخت.
- واکنش آسیلاسیون، تنها کتون تولید میکند زیرا فرمیل کلرید ، زمانیکه تحت شرایط واکنش قرار بگیرد، به و تجزیه میشود.
- اگر ترکیب آروماتیکی، واکنشپذیری کمتری نسبت به مونو هالوبنزن داشته باشد، در این واکنش شرکت نمیکند.
- از آریلآمینها نمیتوان در این واکنشها استفاده کرد چراکه با کاتالیزور اسید لوییس، کمپلکسهایی با شدت واکنشپذیری بسیار کم تشکیل میدهند.
در صورتیکه از آمین یا الکل استفاده کنیم، مکان وقوع آسیلاسیون میتواند در اتمهای نیتروژن یا اکسیژن انجام بگیرد.
تست فریدل کرافتس برای هیدروکربن های آروماتیک
واکنش کلروفرم با ترکیبات آروماتیک به همراه کاتالیزور آلومینیوم کلرید، تریآریل متانها را بدست میدهد که به طور معمول، رنگ روشنی دارند و این روش، به عنوان تست ترکیبات آروماتیک شناخته میشود.













