کلوئید در شیمی چیست؟ – به زبان ساده + مثال و جدول انواع
کلویید یکی از انواع مخلوطهای ناهمگن است که در آن ذراتی به شکل یکنواخت و پایدار پخش شده و معلق هستند. تفاوت این مواد با محلول و مخلوط همگن در اندازه ذرات آنها (بین ۱ تا ۱۰۰۰ نانومتر) است که نسبتا بزرگ هستند. به همین دلیل این ذرات باید توسط عاملهای پایدار کننده در یکدیگر پخش شوند. از انواع کلوئیدها میتوان به شیر، مایونز و ژلاتین اشاره کرد. در این مطلب از مجله فرادرس میآموزیم کلوئید چیست، چه خواصی دارد و انواع آن کدامند.
- میآموزید کلوئید چیست و در دستهبندی کدام مواد قرار میگیرد.
- با خواص کلوئید و اجزای تشکیل دهنده آن آشنا میشوید.
- میتوانید چندین نوع کلوئید با انواع مختلف ماده تشکیلدهنده را تشخیص دهید.
- با اثر تیندال و نقش کلوئید در صابونها آشنا میشوید.
- خواص الکتریکی ذرات کلوئید و کاربرد آنها را میشناسید.
- با تاریخچه کلوئیدها و انواع ژلها آشنا میشوید.


کلوئید چیست؟
کلوئید نوعی مخلوط ناهمگن است که اجزای حلشونده آن اندازهای بین ۱ تا ۱۰۰۰ نانومتر دارند. این ذرات به صورت پایدار و معلق هستند و تهنشین نمیشوند. برای اینکه یک مخلوط در دستهبندی کلوئید قرار بگیرد باید ذراتی داشته باشد که از مولکول بزرگتر بوده و از ذراتی که با چشم دیده میشوند کوچکتر باشد. اگر ذرات مخلوط کوچکتر از مولکول باشد محلول و اگر با چشم دیده شود سوسپانسیون نام میگیرد.
ممکن است در کودکی با گواش و ترکیب کردن آن در آب کار کرده باشید یا با ماسه و آب، مخلوطهایی تهیه کرده باشید. این سوسپانسیونها، مخلوطهایی ناهمگن، با اجزای درشت بودند. همچنین این اجزا، به صورت تودههایی وجود داشتند که با گذشت زمان تهنشین میشدند. در مقابل، زمانی که محلولی تهیه میکنیم، نتیجه، مخلوط همگنی از مولکولها یا یونها است که اجزای آن تهنشین نمیشوند.
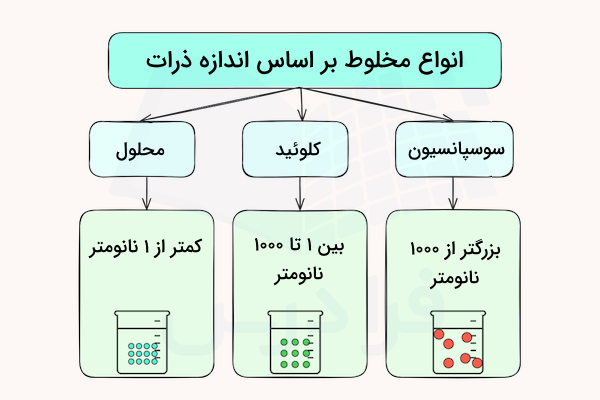
این محلولها رفتاری کاملا متفاوت با سوسپانسیون دارند. یک محلول حتی در صورتی که رنگی باشد، نور را از خود عبور میدهد و شفاف است. در این انواع مواد، مولکولها یا یونها قابل تشخیص و تهنشینی نیستند. گروهی از مخلوطها موسوم به «کلوئید» (Colloids)، خواصی بینابین محلولها و سوسپانسیونها دارند. اجزا در یک کلوئید از بیشتر مولکولهای ساده بزرگترند اما آنقدر بزرگ نیستند که با گذشت زمان تهنشین شوند.

در ادامه خواص کلوئید را نام بردهایم:
- ذرات پایدار و معلق
- اندازه ذرات بین ۱ تا ۱۰۰۰ نانومتر
- پراکندگی نور
- نوعی مخلوط ناهمگن
- اندازه ذرات بین محلول و سوسپانسیون
اجزای کلوئید
همانند تقسیمبندی یک محلول به دو جزء حلشونده و حلال، کلوئیدها نیز بر اساس اجزای تشکیلدهنده دستهبندی میشوند. اجزایی که به طور کلی در مقادیر کم حضور دارند «فاز پخش شونده» (Dispersed Phase)، و فضایی که اجزای فاز پخش شونده در آن پراکنده شدهاند، «فاز پخش کننده» (Dispersion Medium) نام دارد. کلوئيد ها ترکیبی از تمامی حالتهای ماده را شامل میشوند که نمونههایی از آنها در جدول زیر آورده شده است.
| حالت | فاز پخش شونده | فاز پخش کننده | مثال | نام |
| جامد در گاز | جامد | گاز | دود | آیروسول جامد |
| جامد در مایع | جامد | مایع | رنگ، شیر منیزی، نشاسته در آب | سول |
| جامد در جامد | جامد | جامد | برخی سنگهای قیمتی | سول جامد |
| مایع در گاز | مایع | گاز | ابر، مه، افشانه (اسپری) | ایروسول |
| مایع در مایع | مایع | مایع | شیر، مایونز، کره | امولسیون |
| مایع در جامد | مایع | جامد | ژله، ژل، صدف و عقیق | ژل |
| گاز در مایع | گاز | مایع | فوم، کف، خامه زده شده | فوم |
| گاز در جامد | گاز | جامد | سنگ پا | فوم جامد |
تهیه یک سیستم کلوئیدی
دو روش اصلی برای تهیه کلوئیدها وجود دارد:
- پخش کردن اجزای بزرگ یا قطرات کلوئید بوسیله اسپری کردن، آسیاب کردن، مخلوط کردن، تکان دادن و ...
- میعان مولکولهای کوچک حلشده در اجزای بزرگتر کلوئیدی با روشهای تهنشینی، تراکمی یا واکنشهای ردوکس.
روش اول موسوم به «روش پخشی» (Dispersion Method) است. در این روش، اجزای بزرگتر به اجزای کوچکتر خرد میشوند. نمونهای از آن جوهر رنگی است که با پخش کردن اجزای بزرگ یا آسیاب کردن دانههای رنگی بوجود میآید.
روش دوم «روش میعانی» (Condensation Method) نام دارد. این روش در حقیقت، رشد به کمک واحدهای کوچکتر است. به طور مثال، ابرها زمانی تشکیل میشوند که مولکولهای بسیار کوچک آب به صورت میعانی تشکیل شوند. روش «تراکمی»، نام دیگری است که به این دسته از واکنشها نسبت میدهند. این فرآیندها همچنین در موارد آمادهسازی طلا و سیلیکا نیز کاربرد دارند.

برخی جامدات در برخورد با مایعات به طور خود به خودی در مایع پخش میشوند و تشکیل کلوئيد میدهند. ژلاتین، چسب، نشاسته و پودر شیر خشک چنین رفتاری دارند. امولسیونها با تکان دادن یا ترکیب دو مایع امتزاج ناپذیر نیز بوجود میآیند. این عمل موجب قطره قطره شدن یک مایع و تبدیل آن به ذرات کلوئیدی میشود. مرحله بعد شامل پخش شدن قطرات مایع در مایع دیگر است. نمونهای از این مدل را میتوان در آلودگی آب دریاها توسط قطرات نفت بررسی کرد. پاک کردن آلودگی آب دریا توسط قطرات نفت دشوار است چراکه موج دریا امولسیونی از نفت و آب تشکیل میدهد.
عامل امولسیون کننده
در بسیاری از امولسیونها، فاز پخششونده در نهایت به قطرات بزرگی تبدیل و تهنشین (جدا) میشود. در این شرایط، برای پایداری امولسیونها از «امولسیون کننده» (Emulsifying Agent) استفاده میکنند. امولسیون کننده مادهای است که مانع از تبدیل فاز پخش شونده به قطرات بزرگتر میشود.
به طور مثال، استفاده از کمی صابون میتواند نفت و آب دریا را به امولسیون پایدار تبدیل کند. شیر، امولسیونی از آب و کره است که در آن کازئین یا همان پروتئین شیر، نقش امولسیون کننده را دارد. مایونز نیز امولسیونی از روغن و سرکه به همراه زرده تخم مرغ به عنوان عامل امولسیون کننده است.

واکنشهای شیمیایی و تولید کلوئید
در روش میعانی، تجمع مولکولها یا یونها موجب تشکیل ذرات کلوئیدی است. اگر این ذرات بیشتر از اندازه کلوئید ها رشد کنند، تهنشین میشوند که این حالت، دیگر کلوئیدی نیست. به طور مشابه، ابرها با تجمع مولکولهای آب، ذراتی با اندازه کلوئید میسازند. اگر این ذرات به قطرههایی بزرگ تبدیل شوند، یا کریستالهایی از یخ را تشکیل دهند، از حالت کلوئیدی خارج میشوند و به صورت باران، تگرگ یا برف فرو میریزند.
بسیاری از روشهای میعانی، شامل واکنشهای شیمیایی هستند. به عنوان مثال، سوسپانسیون کلوئیدی و قرمزرنگ آهن (III) هیدروکسید از مخلوط کردن آب داغ با محلول غلیظ آهن (III) کلرید بدست میآید:
$$$\mathrm{Fe}^{3+}(s)+3 \mathrm{Cl}^{-}(g)+6 \mathrm{H}_{2} \mathrm{O}(l) \rightarrow \mathrm{Fe}(\mathrm{OH})_{3}(a q)+\mathrm{H}_{3} \mathrm{O}^{+}(a q)+3 \mathrm{Cl}^{-}(a q)$$
در تولید طلا میتوان با استفاده از عوامل کاهنده همچون فرمالدهید، قلع (III) کلرید یا آهن (III) سولفات، سول جامد طلا را تهیه کرد:
برخی از سولهای جامدی که در سال ۱۸۵۷ از این روش تولید شدهاند، همچنان به همان صورت و بدون جدا شدن ذرات کلوئیدی باقی ماندهاند که گواهی بر پایداری طولانی مدت بسیاری از کلوئیدها است.
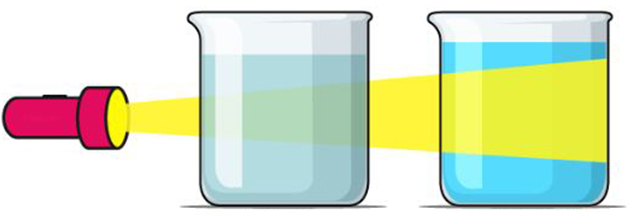
اثر تیندال
در یک کلوئید، اجزا آنقدر بزرگ هستند که سبب پخش شدن نور عبوری از خود شوند. این خاصیت پخشی نور در کلوئیدها به «اثر تیندال» (Tyndall Effect) موسوم است. این خاصیت سبب میشود تا کلوئیدها به صورت تودهای و با رنگ مات باشند.
نمونههایی از کلوئیدها، ابرها هستند. ابرها از قطرات آب با مولکولهایی بزرگ تشکیل شدهاند اما اندازه این مولکولها به قدری نیست که سبب تهنشست آنها شوند.
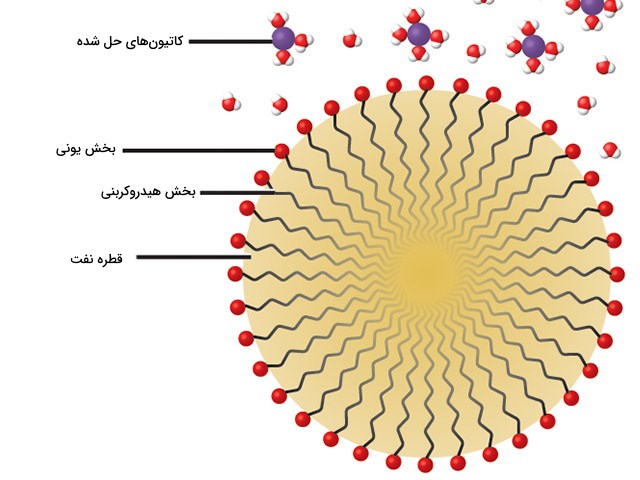
کلوئید و پاککنندگی صابونها
خاصیت کلوئیدی را میتوان در پاککنندگی صابونها نیز جستجو کرد. سر ناقطبی صابون یا «دترجنت» (Detergents) در آلودگیهایی همچون نفت، روغن و گریس حل میشود. در همین زمان، سر قطبی صابون نیز جذب مولکول آب میشود. در نتیجه این امر، صابون به عنوان پلی برای اتصال بین مواد قطبی و ناقطبی عمل میکند. این نوع از مولکولها موسوم به «دوگانه دوست» یا آمفیپاتیک (Apmphiphilic) هستند چراکه همزمان دو خاصیت آبدوست و آبگریز را بروز میدهند. در طی فرآیند ذکر شده، آلودگیها به عنوان ذرات کلوئیدی در آب معلق شده و به سادگی شسته میشوند.
خواص الکتریکی ذرات کلوئید
به طور معمول، ذرات کلوئیدی فاز پخش شونده، دارای بار الکتریکی هستند. به عنوان مثال، ذره کلوئیدی آهن (III) هیدروکسید، تعداد کافی یون هیدروکسید ندارد تا بار مثبت یون آهن (III) را به خوبی جبران کند. در نتیجه هر توده کلوئیدی دارای مقداری بار مثبت و مقادیری یون هیدروکسید است. این امر سبب میشود که عمل پخش شدن ذرات کلوئیدی به لحاظ الکتریکی خنثی باشد.
بسیاری از هیدروکسیدهای فلزی، کلوئیدهایی با بار مثبت هستند در حالیکه بیشتر فلزات و سولفید فلزات در پخش شدن، تشکیل بار منفی میدهند. در حقیقت، تمامی ذرات کلوئیدی موجود در یک سیستم دارای بار یکسان هستند. اگر این امر اتفاق نیوفتد، ذرات با بار ناهمنام یکدیگر را جذب و رسوب میکنند. کربن و گرد و غبار در دوده، خاصیت کلوئیدی دارند. این ذرات همچنین به لحاظ الکتریکی باردار هستند. «فردریک کوترل» (Frederick Cottrell)، شیمیدانی بود که با اختراع دستگاهی، کمک کرد تا این ذرات از یکدیگر جدا شوند.
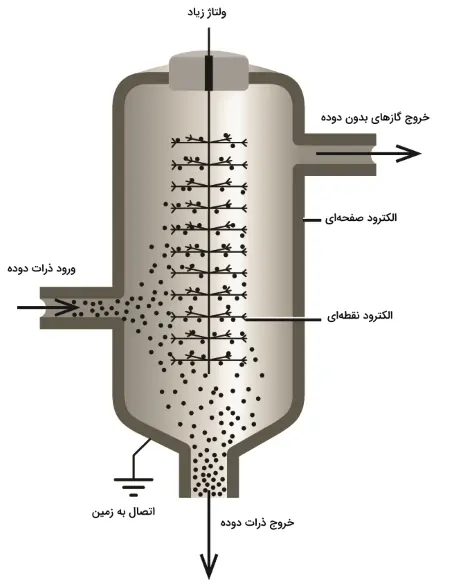
تصفیه هوا به کمک خواص الکتریکی
ذرات باردار دوده، جذب الکترودهایی میشوند که شدیدا باردار هستند. با این کار، ذرات باردار، خنثی و تهنشین میشوند. این روش دارای بیشترین کاربرد در فرآیندهای صنعتی است. از این روش در بازیافت محصولات حاصل از دوده ذوب آهن و کورهها استفاده میشود. همچنین بر این اساس، فیلترهایی یونی نیز برای منازل طراحی شده است تا کیفیت هوای ورودی را افزایش دهند.
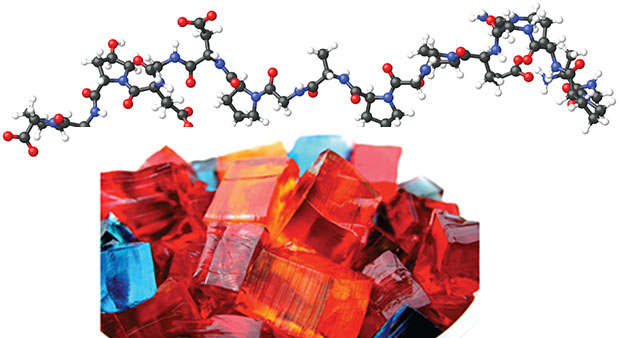
ژلها
ژلاتین و ژله نیز نوعی کلوئید هستند. ژلاتین در دمای پایین بسته (منعقد) میشود و به همراه آن کل جرم محلول که شامل آب نیز هست، با کاهش دما تشکیل مادهای ویسکوز به نام کلوئید میدهد. در این کلوئید، فاز پخش شونده، مایع و فاز پخش کننده جامد است. در حقیقت فیبرهای فاز پخش کننده تشکیل یک شبکه سه بعدی را میدهند که خلخل و فرج آن با مایع پر میشود. از آنجایی که ژلها به روش آبدهی تشکیل میشوند، به آنها هیدراته شده نیز میگویند.
تاریخچه
واژه کلوئید ریشهای یونانی دارد و از دو کلمه «کُلّا» (Kolla) به معنای چسب و «ئیدوس» (Eidos) به معنای شبیه گرفته شده است. این واژه در سال 1861، توسط «توماس گراهام» (Thomas Grraham) برای دستهبندی خواص مخلوطهایی همچون نشاسته در آب و ژلاتین استفاده شد. بسیاری از اجزای کلوئیدی، مجموع هزاران هزار مولکول هستند.
البته این اجزا در برخی موارد همچون پروتئینها و پلیمرها، یک مولکول بسیار بزرگ را تشکیل میدهند. پروتئینها و پلیمرهای سنتز شده، کلوئیدهایی با جرم مولی از چند هزار تا چندین میلیون را شامل میشوند.
اگر این مطلب برای شما مفید بوده است، آموزشهای زیر نیز به شما پیشنهاد میشوند:
- مجموعه آموزشهای دروس شیمی
- مجموعه آموزشهای نرمافزارهای مهندسی شیمی
- آموزش شیمی عمومی
- الکترولیت و هدایت الکتریکی — از صفر تا صد
- استرها — به زبان ساده
^^








با سلام لطفا در خصوص فلزهای کلوئیدی که در ساخت ظروف کاربرد دارند توضیحاتی ارائه نمائید.
با تشکر
با سلام؛
نانوذرات بهبودیافته با پلیمرهای خطی را به عنوان نانوذرات فلزات کلوئیدی میشناسند. این پلیمرهای خطی لایههای محافظ نانوذرات را تشکیل میدهند که کاربردهای مختلفی از جمله در پزشکی و کشف سرطان دارند.
از همراهی شما با مجله فرادرس سپاسگزاریم