عناصر اصلی جدول تناوبی – به زبان ساده
عناصر اصلی جدول تناوبی در بخشهای چپ و راست آن قرار دارند. این عنصرها شامل عناصر بلوک s (گروههای ۱ و ۲) و عناصر بلوک p (گروههای ۱۳ تا ۱۸) هستند. در عناصر بلوک s، اوربیتال s توسط الکترونهای ظرفیت پر میشود و در عناصر بلوک p، اوربیتال p پر میشود. برخی عناصر اصلی جدول تناوبی را عناصر پرکاربرد و فراوان جدول دانسته و برخی دیگر گروههای اصلی جدول تناوبی را سه گروه فلزات، نافلزات و شبهفلزات معرفی میکنند. در این مطلب از مجله فرادرس میآموزیم منظور از عناصر اصلی جدول تناوبی چیست.
- میآموزید عناصر اصلی جدول تناوبی چه عناصری هستند و چه خواصی دارند.
- جدول تناوبی و خواص آن را مرور میکنید.
- با گروههای اصلی و فرعی جدول تناوبی آشنا شده و عناصر آنها را میشناسید.
- میآموزید عناصر جدول تناوبی به چه شکلهایی دستهبندی و مطالعه میشوند.
- دلیل اهمیت عناصر اصلی جدول تناوبی را درک میکنید.
- با کاربردهای عناصر اصلی جدول تناوبی در صنایع مختلف و نقش آنها در زندگی انسان آشنا میشوید.


در ابتدای این مطلب میآموزیم عناصر اصلی جدول تناوبی و مثالهای آنها کدامند. در ادامه، ویژگیهای این عناصر را شناخته و ۸ گروه اصلی جدول تناوبی را معرفی میکنیم. سپس به بررسی گروههای فرعی جدول تناوبی و دستهبندی عناصر جدول تناوبی میپردازیم. در نهایت، اهمیت عناصر اصلی جدول تناوبی را آموخته و کاربردهای آنها را توضیح میدهیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید عناصر اصلی جدول تناوبی چیست.
عناصر اصلی جدول تناوبی
عناصر اصلی جدول تناوبی که با نام «عناصر نماینده» (Representative Elements) نیز شناخته میشوند، عناصری هستند که اوربیتالهای s و p آنها در حال پر شدن است. این عناصر شامل گروههای اول و دوم جدول تناوبی به علاوه عناصر گروه ۱۳ تا ۱۸ هستند. سایر عناصر عناصر فرعی جدول تناوبی نام دارند. عنصرهای فرعی جدول تناوبی شامل فلزات واسطه (فلزات واسطه بیرونی) که اوربیتال d آنها پر میشود و لانتانیدها و اکتینیدها (عناصر واسطه داخلی) هستند که اوربیتالهای f آنها پر میشود.
هر عنصر شیمیایی که به بلوکهای s و p جدول تناوبی تعلق داشته باشد، در شیمی و فیزیک عنصر اصلی نامیده میشود. عناصر بلوک s به دو گروه فلزات قلیایی و فلزات قلیایی خاکی تقسیم میشوند. گروههای ۱۳ تا ۱۸ عناصر بلوک p را تشکیل میدهند که شامل عناصری مانند فلزات پایه، شبهفلزها، نافلزها، هالوژنها و گازهای نجیب هستند.
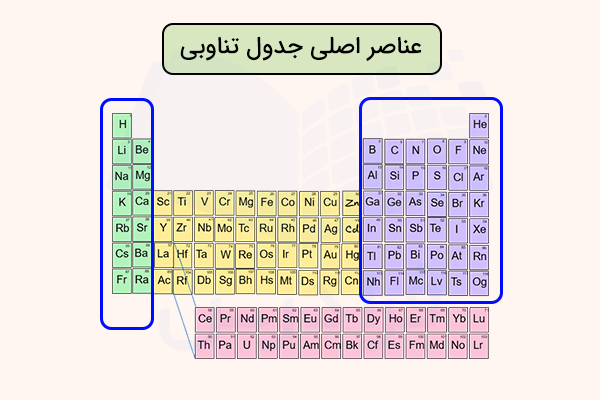
مثال عناصر اصلی جدول تناوبی
هلیوم، لیتیوم، بور، کربن، نیتروژن، اکسیژن، فلوئور و نئون همگی نمونههایی از عناصر اصلی جدول تناوبی هستند. در جدول زیر نام و نماد شیمیایی ۲۰ عنصر اول اصلی جدول تناوبی آورده شده است.
| نام عنصر و نماد شیمیایی | عدد اتمی |
| هیدروژن (H) | ۱ |
| هلیم (He) | ۲ |
| لیتیوم (Li) | ۳ |
| برلیم (Be) | ۴ |
| بور (B) | ۵ |
| کربن (C) | ۶ |
| نیتروژن (N) | ۷ |
| اکسیژن (O) | ۸ |
| فلوئور (F) | ۹ |
| نئون (Ne) | ۱۰ |
| سدیم (Na) | ۱۱ |
| منیزیم (Mg) | ۱۲ |
| آلومینیوم (Al) | ۱۳ |
| سیلیسیم (Si) | ۱۴ |
| فسفر (P) | ۱۵ |
| گوگرد (S) | ۱۶ |
| کلر (Cl) | ۱۷ |
| آرگون (Ar) | ۱۸ |
| پتاسیم (K) | ۱۹ |
| کلسیم (Ca) | ۲۰ |
یادگیری شیمی دهم با فرادرس
برای درک بهتر این موضوع عناصر اصلی جدول تناوبی چیست، ابتدا باید با مفاهیمی چون تاریخچه جدول تناوبی، تشخیص دوره و گروه جدول تناوبی، شعاع اتمی و قانون دورهای عنصرها آشنا شوید. پیشنهاد میکنیم برای درک بهتر این مفاهیم، به مجموعه فیلم آموزش دروس پایه دهم فرادرس، بخش شیمی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مشاهده فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه عناصر اصلی جدول تناوبی دسترسی داشته باشید.
- فیلم آموزش شیمی ۲ پایه یازدهم رشته علوم تجربی و ریاضی و فیزیک فرادرس
- فیلم آموزش شیمی ۲ پایه یازدهم حل سوالات تشریحی امتحانات نهایی فرادرس
- فیلم آموزش شیمی ۳ پایه دوازدهم فرادرس
جدول تناوبی چیست؟
جدول تناوبی عناصر، جدولی است که در آن تمامی عناصر کشف شده به ترتیب افزایش عدد اتمی در ۱۸ گروه و ۷ ردیف مرتب شدهاند. این عناصر بر ترتیب آرایش الکترونی و تعداد الکترونهای ظرفیت موجود در لایه الکترونی آخرشان مرتب شدهاند.
جدول تناوبی امروزه به شکل سادهتری توسط دیمیتری مندلیف (Dmitri Mendeleev) برای اولین بار تدوین شد. سپس جای خالی عناصری که کشف نشده بود توسط سایر دانشمندان تکمیل شد. عناصر در جدول تناوبی به شکلی مرتب شدهاند که عناصر با خواص شیمیایی مشابه در کنار هم قرار بگیرند. برای مثال، تمام فلزات قلیایی (گروه ۱) بسیار واکنشپذیر بوده و یون ۱+ تشکیل میدهند. همه هالوژنها (گروه ۱۷) نیز بسیار واکنشپذیر هستند و یون ۱- تشکیل میدهند.
تعداد عناصر جدول تناوبی
تعداد عناصر جدول تناوبی ۱۱۸ عنصر است که ۹۴ عنصر از آنها به صورت طبیعی وجود دارند و ۲۴ عنصر به صورت آزمایشگاهی سنتز شدهاند. در هر گروه جدول تناوبی، تعداد الکترونهای ظرفیت عناصر با هم برابر است و در هر ردیف جدول تناوبی، تعداد لایههای الکترونی عناصر یکسان است.
اگر تا این قسمت از مطلب را مطالعه کردهاید، با عناصر اصلی جدول تناوبی و خواص آن ها آشنا شدهاید. در ادامه مطلب نیز به بررسی بیشتر این عناصر میپردازیم.
پیشنهاد میکنیم برای دسترسی همیشگی به این نوع مطالب در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همواره به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
نمایش عناصر جدول تناوبی
هر عنصر در جدول تناوبی، با نماد شیمیایی آن، عدد جرمی و عدد اتمی نمایش داده میشود. در برخی از نمایشهای جدول تناوبی، برخی دیگر از خواص عنصر مانند حالت فیزیکی عنصر در دمای اتاق، آرایش الکترونی و نوع عنصر را نیز مشخص میکنند. تصویر زیر، مثالی از نمایش عناصر در جدول تناوبی برای عنصر هیدروژن است.
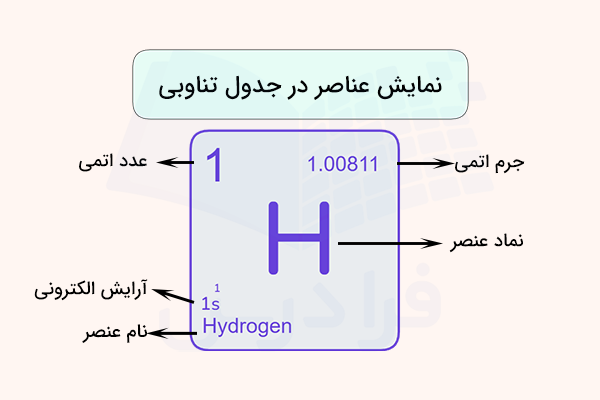
برای درک بهتر جدول تناوبی بهتر است نام فارسی و نام لاتین عناصر جدول تناوبی را بیاموزیم . پیشنهاد میکنیم براییادگیری بهتر نام عناصر، مطلب نام عناصر جدول تناوبی به فارسی مجله فرادرس را مطالعه کنید.
دانلود PDF با کیفیت جدول تناوبی
در ادامه این مطلب، لینکهای دانلود عکس و PDF جدول تناوبی عناصر با کیفیت بالا قرار گرفته است. میتوانید با کلیک بر روی لینکهای زیر فایل PDF جدول تناوبی عناصر و عکس جدول تناوبی عناصر را دانلود کنید.
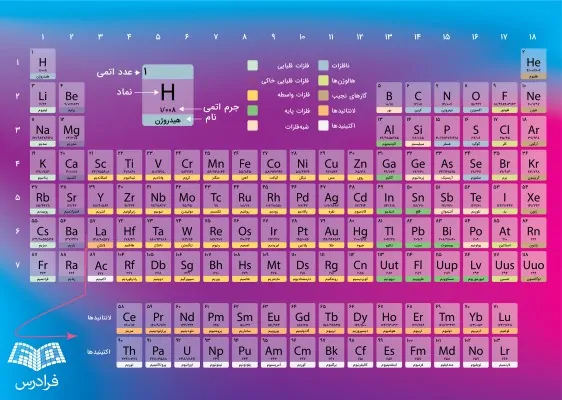
فایل PDF جدول تناوبی فارسی به همراه تقلبنامه جدول تناوبی از لینکهای زیر قابل دانلود هستند. برای دانلود این فایلها، روی آنها کلیک کنید.
-
- دانلود PDF جدول تناوبی عناصر (تقلبنامه جدول تناوبی عناصر)
- دانلود فایل PDF جدول تناوبی فارسی به همراه اسم فارسی عناصر
- دانلود عکس سیاه و سفید جدول تناوبی فارسی برای پرینت سیاه و سفید
ویژگی عناصر اصلی جدول تناوبی
در تقسیمبندی قدیمی جدول تناوبی، عناصر به هشت گروه با زیرگروههای A و B تقسیم میشدند. عناصر زیرگروه A همان عناصر اصلی هستند، در حالی که عناصر زیرگروه B عناصر واسطه را تشکیل میدهند و لانتانیدها و اکتینیدها در ردیفهایی جداگانه در پایین جدول قرار میگیرند.
عناصر اصلی با نام عناصر بلوکهای s و p نیز شناخته میشوند، زیرا در اتمهای آنها اوربیتالهای s و p ترازهای انرژی پر میشوند. این عناصر معمولا لایه ظرفیت کامل ندارند ( بجز گازهای نجیب) و شامل فلزها و نافلزهای واکنشپذیر هستند. رفتار شیمیایی آنها قابل پیشبینی است و از چپ به راست در هر دوره، تعداد الکترونهای ظرفیتی آنها افزایش مییابد تا در انتهای دوره به ظرفیت کامل برسند.
۸ گروه اصلی جدول تناوبی
در سیستمهای قبلی جدول تناوبی، گروههای جدول تناوبی به جای گروه ۱ تا گروه ۱۸ به دو دسته اصلی و فرعی تقسیم میشدهاند. در این دستهبندی، گروه اول و دوم و گروه ۱۳ تا ۱۸، گرووههای اصلی بودهاند. همچنین گروههای ۳ تا ۱۲ ( فلزات واسطه، لانتانیدها و اکتنیدها) گروههای فرعی بودهاند. این دستهبندی گروهها در جدول زیر مشخص شده است.
| نام جدید گروه | نام قدیم گروه به همراه نماد |
| گروه فلزات قلیایی (گروه ۱) | گروه اول اصلی (IA) |
| گروه فلزات قلیایی خاکی (گروه ۲) | گروه دوم اصلی (IIA) |
| گروه بور (گروه ۱۳) | گروه سوم اصلی (IIIA) |
| گروه کربن (گروه ۱۴) | گروه چهارم اصلی (IVA) |
| گروه نیتروژن (گروه ۱۵) | گروه پنجم اصلی (VA) |
| گروه اکسیژن (گروه ۱۶) | گروه ششم اصلی (VIA) |
| هالوژنها (گروه ۱۷) | گروه هفتم اصلی (VIIA) |
| گازهای نجیب (گروه ۱۸) | گروه هشتم اصلی (VIIIA) |
| گروه ۳ | گروه سوم فرعی (IIIB) |
| گروه ۴ | گروه چهارم فرعی (IVB) |
| گروه ۵ | گروه پنجم فرعی (VB) |
| گروه ۶ | گروه ششم فرعی (VIB) |
| گروه ۷ | گروه هفتم فرعی (VIIB) |
| گروه ۸، ۹ و ۱۰ (آهن تا نیکل) | گروه هشتم فرعی (VIIIB) |
| گروه ۱۱ | گروه اول فرعی (IB) |
| گروه ۱۲ | گروه دوم فرعی (IIB) |
همانطور که در بالا مشاهده میکنید، شماره یکان گروههای اصلی و فرعی با سیستم جدید گروهبندی جدول تناوبی مطابقت دارد. گروه هشت و نه و ده جدول تناوبی امروزی، هر سه گروه هشتم فرعی جدول تناوبی به فرم قدیمی را تشکیل میدهند. در ادامه، ویژگیهای هر گروه از گروههای عناصر اصلی جدول تناوبی را به صورت خلاصه بررسی میکنیم.
گروه اول اصلی: فلزات قلیایی
گروه اول عناصر اصلی جدول تناوبی شامل فلزات قلیایی است که لایه ظرفیت آنها شامل ۱ الکترون در زیرلایه s است. این فلزات، به شدت واکنشپذیر هستند و یون کاتیون ۱+ تولید میکنند. به همین دلیل، ترکیبات بسیاری از این عناصر در طبیعت وجود دارد و در صنایع مختلف استفاده میشود. یکی از رایجترین ترکیبات این عناصر، سدیم کلرید است که همان نمک خوراکی مصرفی انسانها است.
این عناصر به دلیل واکنشپذیری بسیار زیاد باید در شرایط اتمسفر خنثی و در شرایط خاص نگهداری شوند. این فلزات، نقطه جوش بالایی دارند و رسانایی خوبی برای گرما و الکتریسیته هستند. آرایش الکترونی عمومی این عناصر اصلی جدول تناوبی به شکل زیر است.
گروه دوم اصلی: فلزات قلیایی خاکی
فلزات قلیایی خاکی در گروه ۲ جدول تناوبی قرار دارند و هنگام واکنش با آب، محلولهایی با خاصیت بازی تولید میکنند. در لایه خارجی این فلزات ۲ الکترون وجود دارد که باعث کامل شدن زیرلایه انرژی s میشود و به همین دلیل، نسبت به فلزات قلیایی از پایداری بیشتری در حالت فلزی برخوردارند. عناصر این گروه هنگام واکنش با نافلزها، با از دست دادن ۲ الکترون خارجی خود، کاتیونی با بار ۲+ تشکیل میدهند و پیوند یونی ایجاد میکنند.
فلزات قلیایی خاکی نسبت به فلزات قلیایی سختتر هستند. سطح آنها جلایی خاکستری مایل به سفید دارد که در مجاورت هوا بهسرعت اکسید شده و کدر میشود. همچنین آلیاژهای این فلزات به دلیل چگالی کم، در ساخت مواد سازهای سبک کاربرد دارند. آرایش الکترونی عمومی این عناصر اصلی جدول تناوبی به شکل زیر است.
گروه سوم اصلی: خانواده بور
گروه سوم اصلی جدول تناوبی، شامل عناصر بور، آلومینیوم، گالیم، اینیدوم، تالیم و نیهونیوم هستند. بجز عنصر شبیهفلز بور، سایر عناصر این گروه، فلز هستند. آرایش الکترونی عمومی این عناصر اصلی جدول تناوبی به شکل زیر است.
گروه چهارم اصلی: خانواده کربن
گروه چهارم اصلی جدول تناوبی، شامل عناصر کربن، سیلیسیم، ژرمانیوم، قلع، سرب و فلروویم است. در این گروه، عنصر کربن نافلز، سیلیسیم و ژرمانیوم شبهفلز و سایر عناصر فلز هستند. آرایش الکترونی این عناصر اصلی جدول تناوبی به شکل زیر است. این عناصر ۴ الکترون در لایه ظرفیت خود دارند.
گروه پنجم اصلی: خانواده نیتروژن
گروه پنجم اصلی جدول تناوبی شامل عناصر نیتروژن، فسفر، آرسنیک، آنتیموان، بیسموت و مسکوویم است. از این عناصر، نیتروژن و فسفر نافلز، آرسنیک و آنتیموان شبهفلز و باقی عناصر فلز هستند. آرایش الکترونی عمومی این عناصر اصلی جدول تناوبی به شکل زیر است و در لایه ظرفیت این عناصر شامل ۵ الکترون است. برخی از عناصر این گروه مانند نیتروژن و فسفر، یون ۳- تشکیل میدهند.
گروه ششم اصلی: خانواده اکسیژن
گروه ششم اصلی جدول تناوبی شامل عناصر اکسیژن، گوگرد، سلنیوم، تلوریم، پولونیم و لیورموریم است. از این عناصر، اکسیژن، گوگرد و سلنیوم نافلز، تلوریم و پولونیوم شبهفلز و لیورموریم فلز است. آرایش الکترونی عمومی عناصر اصلی گروه ششم جدول تناوبی به شکل زیر است.
برخی از عناصر این گروه مانند اکسیژن و گوگرد، یون ۲- تشکیل میدهند.
گروه هفتم اصلی: هالوژن ها
نافلزهای قرارگرفته در گروه ۱۷ «هالوژنها» نام دارند. از نظر شیمیایی، این عناصر بسیار فعال هستند و هرگز بهصورت آزاد در طبیعت یافت نمیشوند. همه هالوژنها در بیرونیترین تراز انرژی خود ۷ الکترون (در زیرلایه p) دارند و تمایل شدیدی به جذب الکترون نشان میدهند تا آرایش پایدار هشتتایی را کامل کنند.
عناصر خانواده هالوژن در هر ۳ حالت ماده دیده میشوند. فلوئور و کلر در دمای اتاق گاز هستند، برم تنها نافلز مایع است و ید بهصورت جامد وجود دارد. آرایش الکترونی عمومی این عناصر اصلی جدول تناوبی به شکل زیر است.
گروه هشتم اصلی: گازهای نجیب
گازهای نجیب گازهایی هستند که در آنها آرایش الکترونی به گونهای است که الکترونها زیرلایههای s و p را (بجز هلیوم) پر کردهاند. یه همین دلیل این عناصر تمایلی به از دست دادن الکترون یا دریافت آن ندارند. به همین دلیل به آنها گازهای نجیب یا گازهای بی اثر گفته میشود.
این عناصر معمولا یون تشکیل نداده و در پیوندهای شیمیایی شرکت نمیکنند. گازهای نجیب عبارتند از:
- هلیوم
- نئون
- آرگون
- کریپتون
- زنون
- رادون
- اوگانسون
آرایش الکترونی عمومی این عناصر اصلی جدول تناوبی به شکل زیر است.
گروههای فرعی جدول تناوبی
گروههای فرعی جدول تناوبی شامل عناصر واسطه و لانتانیدها و اکتینیدها هستند. فلزات واسطه در بخش میانی جدول تناوبی قرار دارند و گروههای ۳ تا ۱۲ را شامل میشوند. لانتایدها و اکتینیدها برای سادگی بیشتر در پایین جدول تناوبی قرار میگیرند. دو فلز لانتان و اکتینیوم در گروه ۳ جدول تناوبی قرار دارند. سایر عناصر این گروه به صورت جداگانه و در پایین این گروه نمایش داده میشوند.
در ادامه خواص گروههای فرعی جدول تناوبی رابررسی میکنیم.
فلزات واسطه
فلزات واسطه رسانای خوبی برای گرما و جریان الکتریکی هستند و خاصیت چکشخواری و مفتولپذیری دارند. بهجز جیوه که مایع است، فلزات واسطه معمولا بهصورت جامدهای سخت با نقطه ذوب و جوش نسبتا بالا وجود دارند. این ناحیه از جدول تناوبی «بلوک d» نامیده میشود، زیرا در این عناصر، الکترونهای ظرفیت، زیرلایه d را پر میکنند.
لانتانیدها و اکتینیدها
لانتانیدها و اکتینیدها با نام فلزات واسطه درونی یا فلزات خاکی کمیاب شناخته میشوند. لانتانیدها فلزهایی با نقطه ذوب نسبتا بالا هستند. آنها در طبیعت بهصورت مخلوط یافت میشوند و به دلیل شباهت زیاد خواصشان، جداسازیشان دشوار است. اکتینیدها همگی پرتوزا هستند. از میان آنها فقط ۳ عنصر بهطور طبیعی یافت میشود و بقیه عناصر مصنوعیاند که به عناصر ترانساورانیومی معروف هستند.
پیشنهاد میکنیم برای درک بهتر خواص این دسته از عناصر، فیلم آموزش لانتانید و اکتینید در جدول تناوبی فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
دستهبندی عناصر جدول تناوبی
عناصر جدول تناوبی بر اساس ویژگیهای مختلف میتوانند به دستهبندیهای مختلفی تقسیم شوند. مهمترین دستهبندی عناصر جدول تناوبی، تقسیم آنها به فلز، نافلز و شبه فلز است. در دستهبندی دیگری، عناصر بر اساس آرایش الکترونی لایه ظرفیت خود، به ۴ دسته s، p، d و f تقسیم میشوند. در ادامه، این دستهبندیها را نام میبریم.
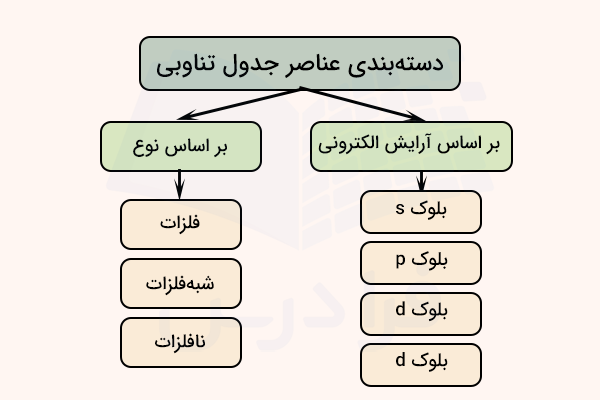
فلز، نافلز و شبه فلز
برخی از دانشمندان، گروههای اصلی جدول تناوبی عناصر را، دستهبندی فلز، نافلز و شبه فلز میدانند. در این دستهبندی، فلزات بر اساس خواص ظاهری و شیمیایی خود به سه دسته فلزات، نافلزات و شبه فلزات تقسیم میشوند. در ادامه، هر یک از این دستهبندیها را توضیح میدهیم.
فلزات جدول تناوبی
بجز عنصر هیدروژن، عناصر موجود در سمت جپ جدول تناوبی، همگی فلز هستند. هیدروژن نیز در فاز جامد میتواند رفتاری مانند فلزات داشته باشد اما در دما اتاق به فرم گاز بوده و این خواص را ندارد به همین دلیل بیشتر به عنوان یک نافلز شناخته میشود.
بخش عمده عناصر جدول تناوبی را فلزات تشکیل میدهند. در ادامه خواص عناصر فلزی را نام میبریم.
- درخشندگی فلزی دارند.
- رسانایی الکتریکی و گرمایی بالا دارند.
- معمولا جامدهای سخت هستند، اما عنصر جیوه مایع است.
- معمولا چکشخوار هستند و قابلیت مفتول شدن دارند.
- بیشتر آنها نقطه ذوب بالایی دارند.
- بهراحتی الکترون از دست میدهند و میل الکترونی پایینی دارند.
- انرژی یونش پایینی دارند.
دو ردیف عنصری که در پایین جدول تناوبی قرار گرفتهاند فلزی هستند. این عناصر شامل فلزات واسطهای به نام لانتانیدها و اکتینیدها (فلزات خاکی کمیاب) هستند. این عناصر در پایین جدول نمایش داده میشوند، زیرا قرار دادن آنها در بدنه اصلی فلزات واسطه باعث میشد شکل جدول نامنظم و غیرمعمول به نظر برسد.
شبه فلرات جدول تناوبی
یک خط زیگزاگ در سمت راست جدول تناوبی، بهنوعی مرزی میان فلزها و نافلزها ایجاد میکند. عناصری که در دو سوی این خط قرار دارند، برخی ویژگیهای فلزها و برخی ویژگیهای نافلزها را نشان میدهند. به این عناصر شبهفلز یا نیمهفلز گفته میشود.
عناصر شبه فلزی شامل عناصر بور، سیلیسیم، ژرمانیوم، آرسنیک، آنتیموان، تلوریم، پلونیم و استاتین هستند. در ادامه برخی از خواص این مود را نام میبریم.
- میتوانند به چند شکل ساختاری متفاوت یا آلوتروپ وجود داشته باشند.
- در شرایط خاص قادر به هدایت جریان الکتریکی هستند و بهعنوان نیمهرسانا شناخته میشوند.
نافلزات جدول تناوبی
عناصر موجود در سمت راست جدول تناوبی، عناصر نافلزی هستند. همچنین، هیدروژن نیز در بسیاری از موارد جزو دسته نافلزات شناخته میشود. در ادامه برخی از خواص عناصر نافلزی را نام میبریم.
- عناصر غیرفلزی، رسانای ضعیفی برای حرارت و الکتریسیته هستند.
- این عناصر معمولا در دمای اتاق در فاز مایع و گاز هستند.
- این عناصر جلای فلزی ندارند.
- این عناصر الکترونگاتیو و دریافت کننده الکترون هستند.
- انرژی یونش این عناصر بالا است.
بلوکهای s و p و d و f
در این دستهبندی، عناصر بر اساس الکترونهای لایه ظرفیتشان دستهبندی میشوند. بر این اساس، الکترون ظرفیت عناصر میتواند در یکی از زیرلایههای s، p، d و f قرار بگیرند. بر این اساس، جدول تناوبی عناصر به ۴ قسمت (بلوک) با مرزهای مشخص تقسیم میشود که به شکل زیر است.
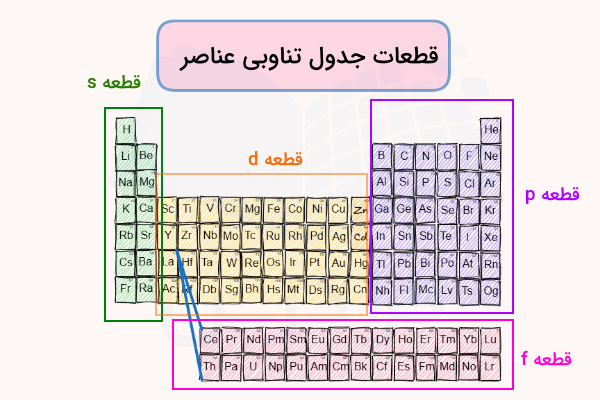
در ادامه ویژگیهای هر قسمت را توضیح میدهیم.
بلوک s
دو گروه اول جدول تناوبی در این قسمت قرار میگیرند. همچنین، عنصر هلیوم با وجود قرار داشتن در دسته گازهای نجیب، جزو قطعه s قرار میگید زیرا دو الکترون در زیرلایه 1s دارد. ویژگی عناصر قطعه s در ادامه نام برده شده است.
-
-
- این عناصر تنها یک حالت اکسایش (۱+ یا ۲+) دارند.
- آرایش الکترونی لایه ظرفیت این عناصر به شکل است.
- تمامی عناصر این قطعه (بجز هلیوم) به شدت واکنشپذیرند.
- این عناصر نرم و با نقطه جوش نسبتا پایین هستند.
- این عناصر (بجز هلیوم) به شدت الکتروپوزتیو هستند و انرژی یونش آنها پایین است.
-
بلوک p
این عناصر گروه سوم تا هشتم اصلی (۱۳ تا ۱۸) جدول تناوبی هستند. در این عناصر، الکترونهای ظرفیت در زیرلایه p قرار دارد. ویژگیهای این عناصر به دلیل گسترده بودن آنها، متفاوت است. در ادامه برخی از ویژگیهای مشترک این عناصر را نام میبریم. این عناصر نیز از عناصر اصلی جدول تناوبی به شمار میآیند.
-
-
- این عناصر میتوانند چندین حالت اکسایش داشته باشند. (۲-، صفر، ۲+، ۴+ و ۶+)
- هلیوم در این دستهبندی قرار نمیگیرد.
- آرایش الکترونی لایه ظرفیت آنها به شکل است.
- این دسته شامل عناصر فلزی، شبه فلزی و نافلزات است.
- این عناصر نسبت به قطعه s الکترونگاتیوتر هستند.
-
بلوک d
بلوک d شامل گروههای فرعی جدول تناوبی (بجز لانتانیدها و اکتنیدها) است. به عبارت دیگر، عناصر قطعه d، فلزات واسطه هستند. این عناصر جزو عناصر فرعی جدول تناوبی بوده و خواص و ویژگیهای متفاوتی دارند. بیشتر آنها رسانای خوب برق و گرما بوده و آرایش الکترونی لایه ظرفیت آنها به شکل است.
بلوک f
بلوک f شامل عناصری است که در آنها الکترونهای لایه ظرفیت، زیرلایه f را پر میکند. این عناصر، منحصرا ردیفهای لاتانیدها و اکتینیدها هستند. آرایش الکترونی این عناصر به شکل است و جزئی از عناصر فرعی جدول تناوبی به شمار میروند.
دلیل اهمیت عناصر اصلی جدول تناوبی
بیشترین عناصر موجود در کیهان، منظومه شمسی و روی زمین، عناصر اصلی و چند فلز واسطه سبک هستند. به همین دلیل، عناصر نماینده اغلب با نام عناصر اصلی شناخته میشوند. عناصر بلوک d به طور سنتی جزو عناصر اصلی در نظر گرفته نمیشوند.
به بیان دیگر، فلزات واسطهای که در بخش میانی جدول تناوبی قرار دارند، همچنین لانتانیدها و اکتینیدهایی که در پایین بدنه اصلی جدول جای گرفتهاند، عناصر اصلی محسوب نمیشوند. برخی دانشمندان نیز هیدروژن را جزو عناصر اصلی به حساب نمیآورند.
کاربردهای عناصر اصلی جدول تناوبی
عناصر اصلی جدول تناوبی در بسیاری از صنایع و تحقیقات علمی استفاده میشوند. این عناصر ترکیبات مختلف و متعددی تشکیل میدهند که اساس زندگی گیاهی و جانوری را در زمین تشکیل دادهاند. در ادامه، برخی از کاربردهای این عناصر را توضیح میدهیم.
فراوانی در زمین و کیهان
عناصر اصلی جدول تناوبی بیشترین فراوانی را در ساخت زمین و کیهان دارند. این عناصر، بهویژه اکسیژن و سیلیکون، حدود ۸۰٪ پوسته زمین را تشکیل میدهند. مانند اکسیژن و سیلیکون، هیدروژن و هلیوم بخش عمدهای از کیهان را تشکیل میدهند.
هیدروژن که گفته میشود در مهبانگ ایجاد شده است، تقریبا ۷۰٪ کیهان را تشکیل میدهد. کربن عنصری ضروری برای تمامی اشکال زندگی روی زمین است.
کاربرد در صنایع
این عناصر اصلی و ترکیبات آنها از مهمترین عناصر از نظر اقتصادی هستند. عنصر لیتیم نقش کلیدی در درمان بیماریهایی مانند اسکیزوفرنی و اختلال دو قطبی دارد. رایجترین کاربرد عنصر سدیم (Na) برای طعم دادن به غذا است. این عنصر در ترکیبی به شکل نمک خوراکی یا کلرید سدیم (NaCl) کشف و عرضه میشود. ساعتهای اتمی از سزیم استفاده میکنند، زیرا قادر است فرکانسهای رزونانس را با دقت اندازهگیری کند.
کاربردهای زیستی
منیزیم یکی از فراوانترین فلزات قلیایی خاکی است و در محیطهای پزشکی بسیار مفید است. منیزیم در آنتیاسیدها، ملینها و نمکهای اپسوم کاربرد دارد. کلسیم حتی فراوانتر از منیزیم روی زمین است و نقش کلیدی در ساختار موجودات زنده مانند استخوانها، دندانها، صدفها و اسکلتهای خارجی دارد.
برخلاف بریلیم که عنصری بسیار شفاف است، باریم توسط پرتوهای ایکس نفوذپذیر نیست و از آن برای مشاهده دستگاه گوارش استفاده میشود.
عناصر فرعی جدول تناوبی
در این مطلب از مجله فرادرس آموختیم مفهوم عناصر اصلی جدول تناوبی چیست. عناصر موجود در قطعههای d و f جدول تناوبی، عناصر فرعی جدول تناوبی به شمار میروند. این عناصر شامل فلزات واسطه، لانتانیدها و اکتینیدها هستند. همچنین برخی از دانشمندان، هیدروژن را نیز جزئی از عناصر اصلی جدول تناوبی در نظر نمیگیرند.








عالی هستین