مولکول آمفی پاتیک چیست؟ – به زبان ساده + خواص و عملکرد
مولکول آمفی پاتیک به مولکولی گفته میشود که هم بخش آبدوست قطبی و هم بخش آبگریز غیرقطبی دارد. از جمله مولکولهای آمفی پاتیک میتوان به فسفولیپیدها، اسیدهای چرب و سورفکتانتها اشاره کرد. در این مطلب از مجله فرادرس میآموزیم مولکول آمفی پاتیک چیست و چه خواص و کاربردهایی دارد.
- میآموزید مولکول آمفی پاتیک چیست و از چه بخشهایی تشکیل شده است.
- با ساختار مولکول آمفی پاتیک و پیوندهای موجود در آن آشنا میشوید.
- می توانید بخش چربیدوست، آب دوست و گروههای باردار را در این مولکولها تشخیص دهید.
- عملکرد مولکول آمفی پاتیک را میآموزید.
- با انواع مولکول آمفی پاتیک از جمله سوفکتانتها آشنا میشوید.
- کاربردهای این نوع مولکول را در صنایع مختلف میشناسید.


در ابتدای این مطلب میآموزیم مولکول آمفی پاتیک چیست. سپس ساختار این مولکولها را بررسی کرده و بخشهای مختلف آن را میآموزیم. در ادامه، با عملکرد این مولکولها آشنا شده و انواع مولکول آمفی پاتیک را یاد میگیریم. در نهایت با کاربردهای این مولکولها آشنا میشویم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید مولکول آمفی پاتیک چیست.
مولکول آمفی پاتیک چیست؟
مولکولهای آمفی پاتیک ترکیبات شیمیایی هستند که هم نواحی قطبی و هم نواحی غیرقطبی دارند و به همین دلیل، هم خاصیت آبدوستی (تمایل به برهمکنش با آب) و هم خاصیت چربیدوستی (تمایل به برهمکنش با چربیها) از خود نشان میدهند. این مولکولها را با نامهای دیگری مانند آمفیفیلیک یا آمفیفیل نیز میشناسند.
واژه آمفیفیل از ریشه یونانی amphis به معنای «هردو» و philia به معنای «دوست داشتن» گرفته شده است. مولکولهای آمفی پاتیک در شیمی و زیستشناسی اهمیت ویژهای دارند. نمونههای شناختهشده آنها شامل کلسترول، مواد شوینده و فسفولیپیدها هستند. در تصویر زیر، قسمتهای چربیدوست و آبدوست مولکول آمفی پاتیک کلسترول مشخص شده است.
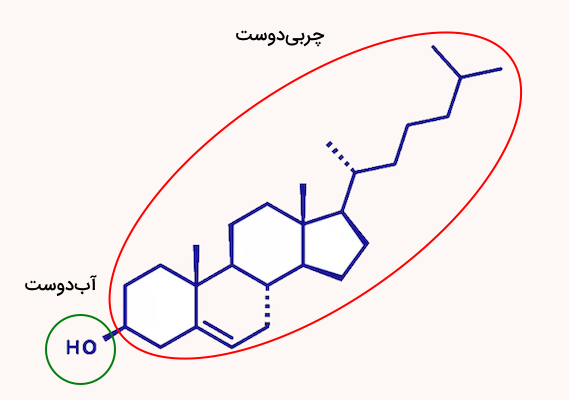
ساختار مولکول آمفی پاتیک
یک مولکول آمفی پاتیک حداقل دارای یک بخش آبدوست و یک بخش چربیدوست است، اما ممکن است چندین بخش آبدوست و چربیدوست نیز داشته باشد. بخش چربیدوست معمولا یک بخش هیدروکربنی است که از اتمهای کربن و هیدروژن تشکیل شده و غیرقطبی و آبگریز است.
بخش آبدوست میتواند دارای بار الکتریکی باشد یا بدون بار باشد. گروههای باردار ممکن است کاتیونی (مثبت) مانند گروه آمونیوم یا آنیونی (منفی) مانند کربوکسیلاتها ، فسفاتها ، سولفاتها و سولفوناتها باشند. گروههای قطبی بدون بار، مانند گروههای الکل، نیز جزو بخشهای آبدوست محسوب میشوند. در ادامه هر یک از این بخشها را بررسی میکنیم.
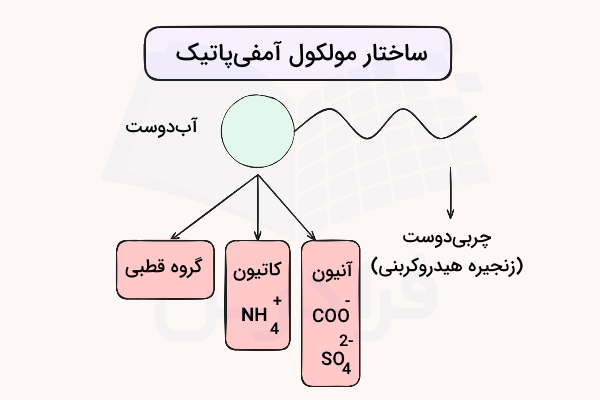
بخش آبدوست
بخش آبدوست مولکولهای آمفی پاتیک میتواند متشکل از گروههای باردار آنیونی یا کاتیونی یا گروههای قطبی خنثی باشد. مولکولهای آبدوست، مولکولهایی هستند که تمایل به آب دارند یا در آب حل میشوند و معمولا ترکیبات یونی یا کووالانسی قطبی هستند.
گروههای باردار
گروههای باردار موجود در مولکولهای آمفی پاتیک، آنیونها یا کاتیونهایی چند اتمی و معدنی هستند. برای مثال، آنیونهای رایج موجود در مولکولهای آمفیپاتیک در ادامه معرفی شده است.
| نام آنیون | فرمول شیمیایی |
| کربوکسیلات | |
| سولفات | |
| سولفونات | |
| فسفات |
همچنین، کاتیونهای چند اتمی مانند آمونیوم با فرمول شیمیایی نیز میتوانند بخش آبدوست مولکولهای آمفی پاتیک را تشکیل دهند.
بخش چربیدوست
گروه چربیدوست مولکول آمفی پاتیک یک بخش هیدروکربنی بزرگ است. این بخش معمولا مانند یک زنجیره هیدروکربنی بلند با فرمول شیمیایی عمومی است که در آن n بزرگتر از ۴ باشد. به دلیل داشتن هر دو بخش چربیدوست و آبدوست، برخی از این ترکیبات هم در آب و هم تا حدی در حلالهای غیرقطبی قابل حل هستند.
وقتی این مولکولها در سیستم دوفازی ناهمگن شامل حلالهای آبی و آلی قرار میگیرند، بین دو فاز تقسیم میشوند و میزان بخشهای آبگریز و آبدوست، میزان توزیع آنها بین فازها را تعیین میکند. پیشنهاد میکنیم برای آشنایی بیشتر با این قسمتهای مولکول آمفی پاتیک، فیلم آموزش مولکول قطبی و غیر قطبی فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
پیوند هیدروژنی
ویژگی آبدوستی یا آبگریزی گروههای اتمی به توانایی آنها در تشکیل پیوند هیدروژنی با مولکولهای آب بستگی دارد. گروههایی که میتوانند با آب پیوند هیدروژنی ایجاد کنند، آبدوست هستند، در حالی که گروههایی که این توانایی را ندارند، آبگریز محسوب میشوند.
اتمهای اکسیژن و نیتروژن به راحتی با مولکولهای آب پیوند هیدروژنی برقرار میکنند، بنابراین هر مولکول آلی که حاوی این اتمها باشد و به زنجیره کربنی متصل شده باشد، بخش آبدوست مولکول است. به عنوان مثال، در مولکول کلسترول، گروه OH که در یک طرف مولکول قرار دارد، آبدوست است و میتواند با آب پیوند هیدروژنی تشکیل دهد، در حالی که حلقههای کربنی که تنها از کربن و هیدروژن ساخته شدهاند، آبگریز هستند و با آب برهمکنش ندارند.
یادگیری شیمی دوازدهم با فرادرس
برای درک بهتر مفهوم و ساختار مولکولهای آمفی پاتیک نیاز است ابتدا با مفاهیمی چون انواع صابون، پاک کنندهها، پاک کنندههای غیرصابونی و دترجنتها آشنا شویم. همچنین، شناخت انواع ترکیبات شیمیایی و انواع هیدروکربنها به ما در درک ساختار این مولکولها کمک میکند. پیشنهاد میکنیم برای درک بهتر این مفاهیم، مجموعه فیلم دروس پایه دوازدهم بخش شیمی فرادرس را مشاهده کنید که با زبانی ساده ولی کاربردی به توضیح آنها میپردازد.
همچنین، با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری درباره آمفی پاتیک دسترسی داشته باشید.
- فیلم آموزش شیمی ۲ پایه یازدهم رشته علوم تجربی و ریاضی و فیزیک فرادرس
- فیلم آموزش شیمی ۱ پایه دهم فرادرس
- فیلم آموزش شیمی ۱ پایه دهم حل سوالات تشریحی امتحانات نهایی فرادرس
عملکرد مولکول آمفی پاتیک
مولکولهای آمفی پاتیک میتوانند تا حدی هم در آب و هم در حلالهای غیرقطبی حل شوند. وقتی این مولکولها در مخلوطی شامل آب و حلالهای آلی قرار میگیرند، بین دو فاز توزیع میشوند. نمونه آشنا این پدیده، عملکرد مایع ظرفشویی است که روغنها و چربیها را از ظروف جدا میکند.
لیپوزومها، میسلها و دولایههای لیپیدی سه شکل رایج مولکولهای آمفی پاتیک در ارگانیسمها هستند. آمفیپاتیکها یکی از مهمترین زنجیرههای جانبی در بسیاری از مولکولهای شیمیایی به شمار میروند که میتوانند ویژگیهای کلی مولکول را تعیین کنند. پیشنهاد میکنیم برای آشنایی بیشتر با این زنجیرهها، مطلب زنجیره جانبی مجله فرادرس را مطالعه کنید.
میسل
زمانی که سر آبدوست مولکولها در تماس با حلال قطبی قرار میگیرد و دمهای آبگریز در مرکز قرار میگیرند، خوشهای از مولکولها شکل میگیرد که به آن میسل گفته میشود. در محلولهای آبی، مولکولهای آمفی پاتیک به صورت خودبهخود میسل تشکیل میدهند. میسل انرژی آزاد کمتری نسبت به مولکولهای آمفی پاتیک آزاد دارد.
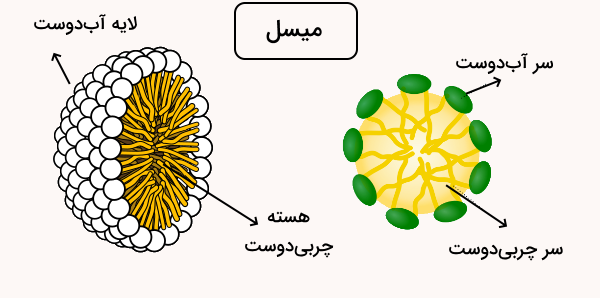
بخش قطبی مولکول (آبدوست) سطح بیرونی میسل را تشکیل داده و با آب در تماس است، در حالی که بخش چربیدوست (آبگریز) از آب محافظت میشود و در داخل میسل قرار میگیرد. هر روغن موجود در مخلوط در داخل میسل محصور میشود و پیوندهای هیدروژنی زنجیرههای هیدروکربنی داخل میسل را پایدار میکنند. شکستن میسل نیازمند صرف انرژی است.
لیپوزوم
مولکولهای آمفی پاتیک همچنین میتوانند لیپوزوم تشکیل دهند. لیپوزومها شامل یک دولایه لیپیدی محصور هستند که به شکل یک کره درمیآیند. بخش قطبی دولایه، محلول آبی را احاطه کرده و با آن در تماس است، در حالی که دمهای آبگریز به سمت یکدیگر قرار میگیرند.
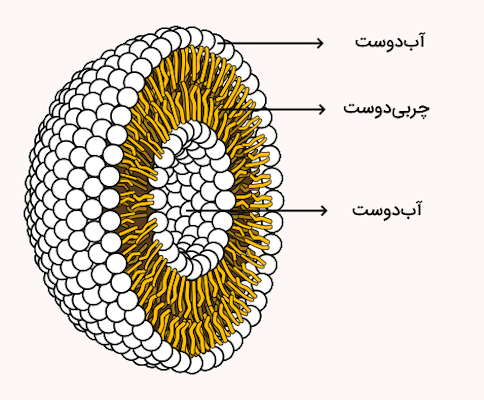
دولایه لیپیدی
دولایه لیپیدی از فسفولیپیدها ساخته شده که هر مولکول دارای سر آبدوست و دم آبگریز است. سرهای آبدوست به سمت بیرون و دمهای آبگریز در مرکز قرار میگیرند و این ساختار عبور مولکولهای غیرقطبی را آسان و عبور مولکولهای قطبی را به کمک پروتئینها ممکن میکند.
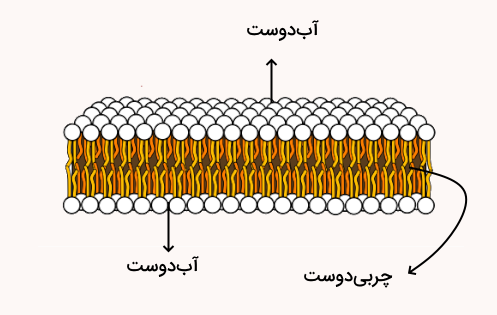
انواع مولکول آمفی پاتیک
مواد شوینده و صابونها نمونههای آشنا از مولکولهای آمفی پاتیک هستند، اما بسیاری از مولکولهای زیستشیمیایی نیز آمفی پاتیک هستند. از جمله این مولکولها میتوان به فسفولیپیدها اشاره کرد که پایه ساختاری غشاهای سلولی را تشکیل میدهند.
کلسترول، گلیکولیپیدها و اسیدهای چرب نیز مولکولهای آمفی پاتیک هستند که در غشاهای سلولی جای میگیرند. اسیدهای صفراوی، آمفیپاتیکهای استروئیدی هستند که در هضم چربیهای غذایی نقش دارند. مولکولهای آمفی پاتیک را میتوان در دستهبندیهای آمفی پولها، بولا آمفیپاتیکها، چربیها و روغنها و سورفکتانتها بررسی کرد.
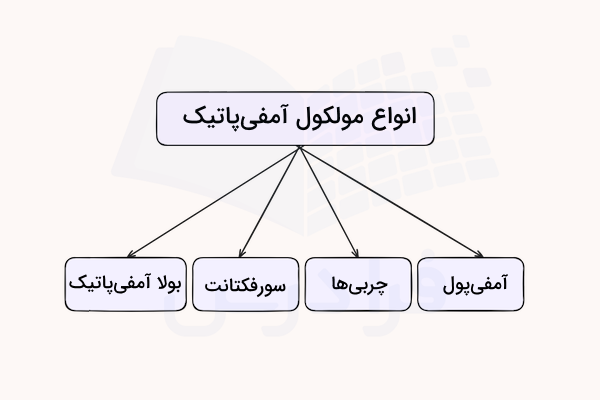
آمفی پول
آمفیپولها، پلیمرهای آمفی فیلیک هستند که بدون نیاز به مواد شوینده، حلپذیری پروتئینهای غشایی را در آب حفظ میکنند.
بولا آمفی پاتیک
مولکولهایی با شکل بیضوی هستند که در هر دو انتهای خود گروههای آبدوست دارند. این مولکولها نسبت به آمفی پاتیکهای با یک سر قطبی، حلالیت بیشتری در آب دارند.
چربیها و روغنها
اسیدهای چرب، چربیها و روغنها نیز از دسته آمفی پاتیکها هستند که در حلالهای آلی حل میشوند اما در آب حل نمیشوند.
سورفکتانت ها
سورفکتانتهای هیدروکربنی که در پاکسازی به کار میروند نیز آمفی پاتیک هستند. از جمله این مواد میتوان به سدیم دودسیل سولفات، ۱- اکتانول، کوکامیدوپروپیل بتائین و بنزالکونیوم کلراید اشاره کرد.
کاربرد مولکولهای آمفی پاتیک
در این مطلب از مجله فرادرس آموختیم مولکول آمفی پاتیک چیست. مولکولهای آمفیپاتیک نقشهای زیستی مهمی ایفا میکنند. آنها جزء اصلی دولایههای لیپیدی هستند که غشاهای سلولی را تشکیل میدهند. در ادامه برخی دیگر از کاربردهای این مولکولها را معرفی میکنیم.

فرآیندهای زیستی
بدن از مولکولهای آمفی پاتیک برای هضم غذا استفاده میکند. این مولکولها در ایمنی نیز اهمیت دارند. برای مثال، پپتیدهای ضد میکروبی آمفیپاتیک دارای خواص ضد قارچی و ضد باکتریایی هستند.
ساخت شوینده ها
رایجترین استفاده تجاری از آمفی پاتیکها در تولید شویندهها و پاککنندهها است. صابونها و مواد شوینده هر دو چربیها را از آب جدا میکنند، اما با سفارشیسازی مواد شوینده با گروههای آبگریز کاتیونی، آنیونی یا بدون بار، دامنه عملکرد آنها در شرایط مختلف گسترش مییابد.
داروسازی
لیپوزومها برای انتقال مواد مغذی یا داروها استفاده میشوند و آمفی پاتیکها در تولید بیحسکنندههای موضعی، عوامل کفزا و سورفکتانتها نیز کاربرد دارند. در داروسازی، از مولکولهای آمفیپاتیک برای افزایش حلشوندگی و در دسترس قرار دادن داروهای آبگریز برای بدن استفاده میشود.
علوم غذایی
مولکولهای آمفی پاتیک مخلوطهای آب و روغن را پایدار میکنند، که معمولا با هم مخلوط نمیشوند. در علوم غذایی، این ویژگی اجازه میدهد امولسیونهای پایدار مانند مایونز یا سس سالاد تولید شود. بخش آبگریز مولکولها با روغن و بخش آبدوست با آب برهمکنش دارد و از جدا شدن روغن جلوگیری میکند. این توانایی باعث بهبود بافت مواد غذایی میشود.