نیتریل چیست؟ – در شیمی آلی و به زبان ساده
نیتریلها گروهی از ترکیبات آلی هستند که از اتصال کربن متصل به پیوند سهگانه با نیتروژن به یک گروه مولکولی متصل شده است. در ساختار مولکولی این ترکیبات، یک گروه سیانو به یک اتم کربن متصل است. این ترکیبات معمولا به صورت مایع یا جامد بیرنگ دیده میشوند و بوی مشخصی دارند. نام دیگر این ترکیبات، ترکیبات سیانو است. این مواد از نظر ساختاری با موادی مانند سیانید، ایزوسیانید، استونیتریل، آکریلونیتریل و مشتقات اسیدهای کربوکسیلیک ارتباط دارند. در این مطلب از مجله فرادرس میآموزیم نیتریل چیست و چه ویژگیهایی دارد.
- میآموزید نیتریل چیست و چه ساختاری دارد.
- با خواص فیزیکی و شیمیایی ترکیبات نیتریل آشنا میشوید.
- با مثالهای نیتریل آشنا میشوید.
- روشهای مختلف تولید ترکیبات نیتریل را میآموزید.
- انواع مختلف روشهای نامگذاری نیتریلها را یاد میگیرید.
- واکنشها، کاربردها و تاریخچه ترکیبات نیتریل را میآموزید.


در ابتدای این مطلب میآموزیم نیتریل چیست. سپس به بررسی ساختار و خواص نیتریل پرداخته و مثالها و روش تولید این ترکیب را میآموزیم. در ادامه، نامگذاری نیتریل را آموخته و واکنشها و کاربردهای آن را توضیح میدهیم. در نهایت روش شناسایی و تاریخچه نیتریل را بررسی خواهیم کرد. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید نیتریل چیست.
نیتریل چیست؟
نیتریل یک ترکیب آلی (گروه عاملی) است که در ساختار خود دارای یک گروه سیانو متصل به یک گروه آلکیل یا آریل است. این گروه از یک اتم کربن با پیوند سهگانه به یک اتم نیتروژن تشکیل شده و به همین دلیل ویژگیهای شیمیایی خاصی به این ترکیبات میدهد. برای مثال، استونیتریل یک نیتریل ساده است که بهعنوان حلال در شیمی آلی استفاده میشود.
نیتریلها بهدلیل انعطافپذیری بالا در شیمی آلی اهمیت زیادی دارند، زیرا میتوان از آنها بهعنوان واسطه در سنتز ترکیبات مختلفی مانند آمینها، اسیدهای کربوکسیلیک و آمیدها استفاده کرد. نیتریلها در بسیاری از ترکیبات کاربردی حضور دارند. برای مثال، متیل سیانوآکریلات که در چسبهای فوری استفاده میشود، و همچنین لاستیک نیتریلی که نوعی پلیمر حاوی گروه نیتریل است و در ساخت دستکشهای آزمایشگاهی و پزشکی بدون لاتکس کاربرد دارد.
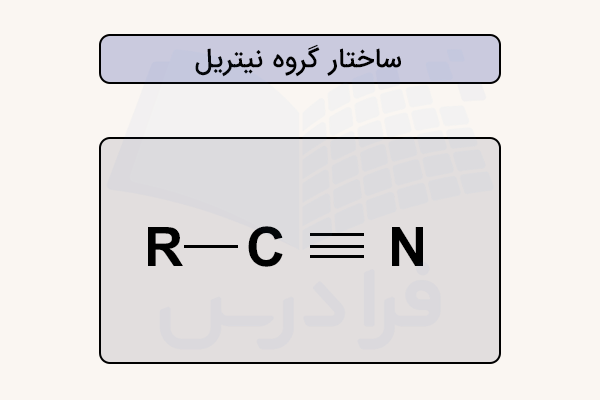
تفاوت سیانید و نیتریل چیست؟
ترکیبات غیرآلی که دارای گروه هستند نیتریل نامیده نمی شوند و به آنها سیانید گفته میشود. با اینکه هر دو دسته میتوانند از نمکهای سیانیدی به دست بیایند، بیشتر نیتریلها در مقایسه با سیانیدها سمیت بسیار کمتری دارند.
نیتریلها ترکیبات آلی هستند، اما سیانیدها میتوانند آلی یا معدنی باشند. در ترکیبات غیرآلی، گروه سیانو به صورت آنیون عمل میکند، در حالی که در نیتریلها به صورت پیوند کووالانسی وجود دارند. مثال نیتریلها استونیتریل و مثال سیانیدها سدیم سیانید و هیدروژن سیانید هستند.
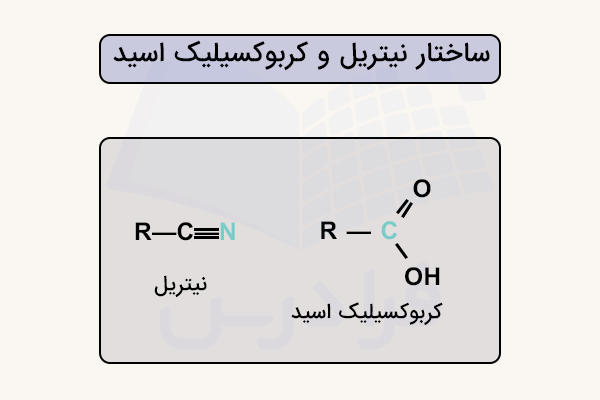
شباهت کربوکسیلیک اسید و نیتریل چیست؟
نیتریلها از نظر ساختاری با اسیدهای کربوکسیلیک شباهت دارند، زیرا در هر دو نوع ترکیب یک اتم کربن وجود دارد که سه پیوند به یک اتم الکترونگاتیو برقرار کرده و همچنین دارای یک پیوند پای هستند. به همین دلیل، برخی از واکنشهای نیتریلها و اسیدهای کربوکسیلیک رفتار مشابهی نشان میدهند.
برای مثال، هر دو دسته ترکیب خاصیت الکتروفیلی دارند و میتوانند در واکنشهای افزایشی هستهدوست شرکت کنند.
یادگیری شیمی آلی با فرادرس
برای درک بهتر این موضوع که نیتریل چیست ابتدا باید با مفاهیمی چون هیدروکربنها، روش نامگذاری هیدروکربنها، شناسایی ترکیبات آلی، انواع طیفسنجی و واکنشهای آلی آشنا شویم. پیشنهاد میکنیم برای درک بهتر این مفاهیم، به مجموعه فیلم آموزش شیمی از دروس دانشگاهی تا کاربردی فرادرس راحعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری درباره نیتریلها دسترسی داشته باشید.
- فیلم آموزش طیف سنجی رزونانس مغناطیسی هسته NMR پیشرفته فرادرس
- فیلم آموزش شیمی آلی ۲ به زبان ساده و گواهینامه فرادرس
- فیلم آموزش مبانی سنتز در شیمی آلی فرادرس
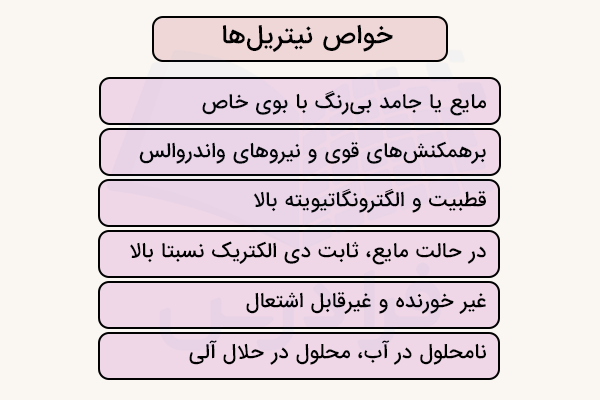
خواص نیتریل چیست؟
نیتریلها معمولا به صورت مایع یا جامد بی رنگ دیده میشوند و بوی مشخصی دارند. در ادامه خواص ترکیبات نیتریل را بررسی میکنیم.
- نیتریلها معمولا بهصورت مایع یا جامد بیرنگ با بوی خاص هستند.
- نقطه جوش آنها معمولا در بازه ۸۲ تا ۱۱۸ درجه سانتی گراد قرار دارد.
- بین مولکولهای آنها برهمکنشهای قوی دوقطبی-دوقطبی و نیروهای واندروالس وجود دارد.
- این ترکیبات قطبیت و الکترونگاتیویته بالایی دارند.
- نیتریلها در آب محلول هستند، اما با افزایش طول زنجیر کربنی، میزان حلالیت آنها کاهش مییابد.
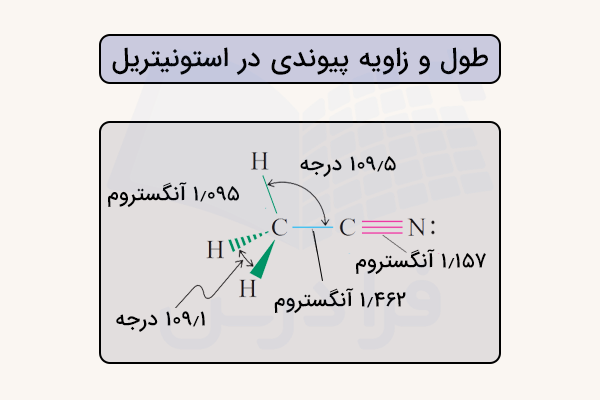
- طول پیوند حدود است.
- در حالت مایع دارای ثابت دی الکتریک نسبتا بالایی هستند.
- غیر خورنده و غیر قابل اشتعال هستند.
- در حلالهای آلی حل میشوند اما در آب نامحلولاند.
ساختار نیتریل چیست؟
ساختار نیتریل شامل حضور پیوند سهگانه بین کربن و نیتروژن است. این پیوند باعث میشود هندسه گروه نیتریل خطی باشد و زاویه پیوندی در اطراف آن ۱۸۰ درجه باشد. از آنجا که نیتروژن الکترونگاتیوتر از کربن است، الکترونها را بیشتر بهسمت خود میکشد و در نتیجه کربن دارای بار جزئی مثبت و نیتروژن دارای بار جزئی منفی میشود. این موضوع نقش مهمی در نحوه واکنشپذیری نیتریلها دارد.
اگر تا این قسمت از مطلب را مطالعه کردهاید با نیتریلها و ساختار و خواص آن آشنا شدهاید. در ادامه مطلب نیز به بررسی بیشتر این ترکیب میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
ساختار خطی گروه سیانو باعث پایداری و در عین حال واکنشپذیری مناسب این ترکیبات میشود. قطبیت بالای پیوند سهگانه به نیتریلها امکان میدهد در برهمکنشهای مختلفی مانند پیوند هیدروژنی و هماهنگی با یونهای فلزی شرکت کنند، که این ویژگیها در بسیاری از واکنشهای شیمیایی اهمیت دارند.
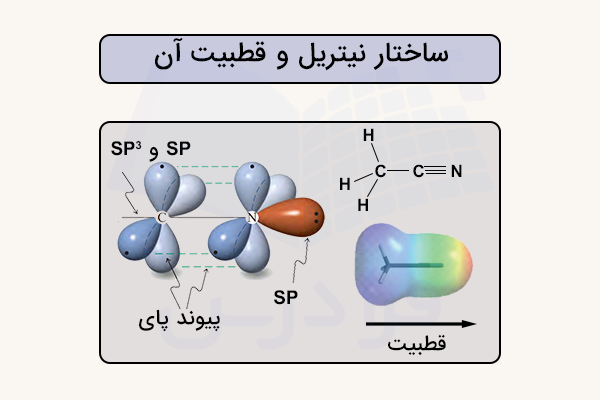
پیوند در ترکیبات نیتریل
ویژگی شاخص نیتریلها، وجود پیوند سهگانه کربن-نیتروژن است. این پیوند مانند پیوند دوگانه، از همپوشانی جانبی اوربیتالهای p در اتمهای مجاور تشکیل میشود. اتمهای کربن و نیتروژن الکترونهای ظرفیتی خود را در اوربیتالهای 2s و 2p دارند و میتوانند این اوربیتالها را به مجموعهای از اوربیتالهای هم انرژی sp، یا تبدیل کنند. طول و زوایای پیوندی استونیتریل در تصویر زیر آورده شده است.
اوربیتالهای معمولا در ترکیبات اشباع دیده میشوند، زیرا یک اتم با این نوع هیبریداسیون میتواند چهار جفت الکترون را در چهار اوربیتال خود جای دهد و به حالت اشباع برسد. اما زمانی که فقط دو اوربیتال پر میشوند، هیبریداسیون به صورت sp انجام میشود و دو اوربیتال sp بهصورت خطی با زاویه ۱۸۰ درجه قرار میگیرند. دو اوربیتال p دیگر بدون تغییر باقی میمانند و نسبت به محور اوربیتالهای sp عمود هستند. همپوشانی سر به سر اوربیتالهای sp پیوند سیگما را ایجاد میکند و همپوشانی جانبی اوربیتالهای p دو پیوند پای میسازد، در نتیجه یک پیوند سهگانه کامل شکل میگیرد.
مثال نیتریل چیست؟
رایجترین نیتریل آلی، استونیتریل است. نیتریلها به دلیل واکنشپذیری مناسب، حلالهای خوبی در بسیاری از کاربردها هستند. استونیتریل کمخطرترین نیتریل محسوب میشود. پلیمرهای نیتریل نیز ترکیباتی رایج هستند. نیتریلهایی که گروه سیانو مستقیما به یک پیوند دوگانه کربن-کربن متصل است، بهراحتی پلیمریزه میشوند. یکی از مهمترین این ترکیبات آکریلونیتریل است که در صنعت پلاستیک کاربرد گسترده دارد.
نیتریل ها در طبیعت
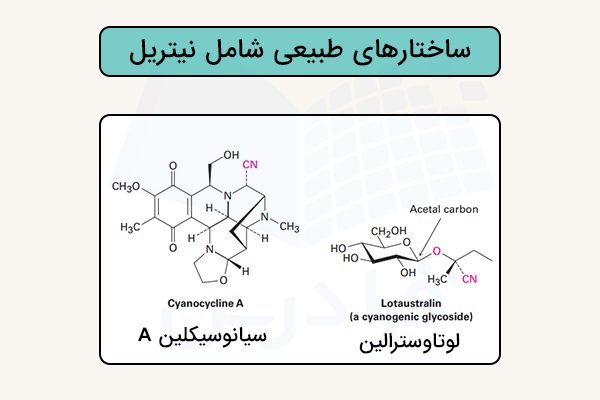
نیتریلها به ندرت در موجودات زنده یافت میشوند، هرچند چند صد نمونه از آنها شناسایی شده است. برای مثال، سیانوسیکلین A از باکتری Streptomyces lavendulae جدا شده و مشخص شده که دارای خواص ضد میکروبی و ضد توموری است. علاوه بر این، بیش از هزار ترکیب با نام گلیکوزیدهای سیانوژنیک شناخته شدهاند که عمدتا منشا گیاهی دارند.
این ترکیبات شامل یک بخش قندی با کربن استالی هستند که یکی از اتمهای اکسیژن آن به کربنی متصل است که گروه نیتریل دارد . در اثر هیدرولیز اسیدی در محیط آبی، این ساختار شکسته شده و سیانوهیدرین تشکیل میشود که در ادامه هیدروژن سیانید آزاد میکند. تصور میشود نقش اصلی این ترکیبات، محافظت از گیاه از طریق مسموم کردن جانورانی است که آن را مصرف میکنند. لوتاوسترالین موجود در گیاه کاساوا نمونهای از این دسته ترکیبات است. این ساختارها در تصویر زیر نمایش داده شدهاند.
روش تولید نیتریل
برخی از ترکیبات نیتریل با استفاده از گرمادهی به کربوکسیلیک اسیدها با آمونیاک در حضور کاتالیزگر تولید میشوند. از این روش برای تولید نیتریلها از چربیها و روغنهای طبیعی استفاده میشود. محصولات به دست آمده به عنوان نرمکننده در لاستیکهای مصنوعی، پلاستیکها و منسوجات کاربرد دارند و همچنین در تولید آمینها به کار میروند.
نیتریلها همچنین با گرم کردن آمیدها در حضور پنتوکسید فسفر تشکیل میشوند. این ترکیبات میتوانند در اثر واکنش با لیتیم آلومینیوم هیدرید به آمینهای نوع اول کاهش یابند یا در حضور اسید یا باز به اسیدهای کربوکسیلیک هیدرولیز شوند. در ادامه روشهای رایج تولید نیتریل را توضیح میدهیم.
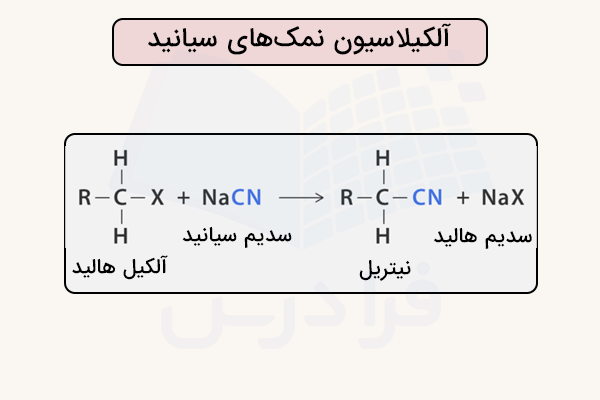
آلکیلاسیون نمکهای سیانید
یکی از روشهای رایج، آلکیلاسیون نمکهای سیانید است. در این روش که نوعی جانشینی نوکلئوفیلی محسوب میشود، یون سیانید جایگزین یون هالید در یک هالید آلکیل میشود. برای این کار، نمکهایی مانند یا با یک هالید آلکیل واکنش میدهند و نیتریل آلکیلی تشکیل میشود. این روش به دلیل سادگی و کارایی بالا بسیار مورد استفاده قرار میگیرد. این روش در تصویر زیر نمایش داده شده است.
این واکنشها از نوع جانشینی نوکلئوفیلی هستند و در آنها از نوکلئوفیلی بودن یون سیانید برای وارد کردن گروه نیتریل استفاده میشود. این واکنش در تصویر زیر نمایش داده شده است.
تولید نیتریل از آلدهید یا کتون
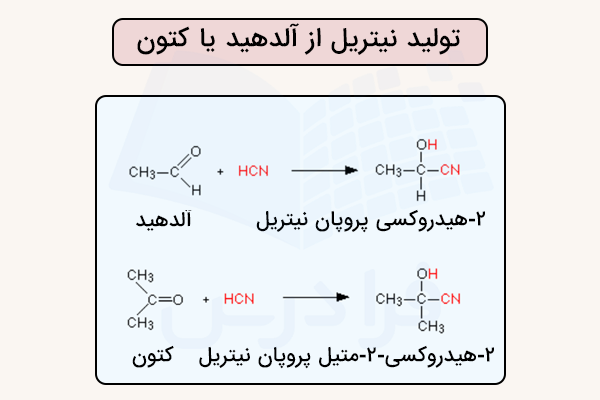
روش دیگر، تشکیل سیانوهیدرین است. این فرایند با یک ترکیب کربونیل مانند آلدهید یا کتون آغاز میشود. با افزودن هیدروژن سیانید یا یون سیانید، ترکیب میانی سیانوهیدرین تشکیل میشود. سپس با حذف آب، گروه نیتریل ایجاد میشود. برای مثال، استون با واکنش داده و سیانوهیدرین مربوطه را تشکیل میدهد که با آبگیری به نیتریل تبدیل میشود. این روش به دلیل استفاده از مواد اولیه در دسترس، اهمیت زیادی دارد.
برای مثال، از واکنش اتانال (یک آلدهید)، ترکیب ۲-هیدروکسی پروپان نیتریل بهدست میآید و از پروپانون (یک کتون)، ۲-هیدروکسی-۲-متیل پروپان نیتریل تشکیل میشود. این روش در تصویر زیر نمایش داده شده است.
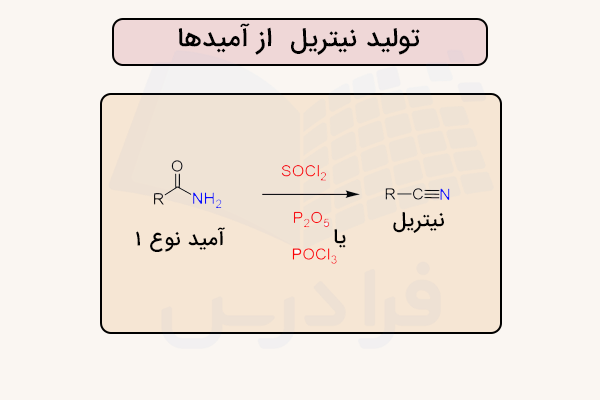
آبگیری از آمیدها
یک روش دیگر برای تولید نیتریلها، آبگیری از آمیدهای نوع اول است. در این فرایند، آمید در حضور عامل آبگیر یا کاتالیزور گرم میشود و با حذف آب، نیتریل حاصل میشود. این روش زمانی کاربرد دارد که ماده اولیه از نوع آمید باشد. این روش در تصویر زیر نمایش داده شده است.
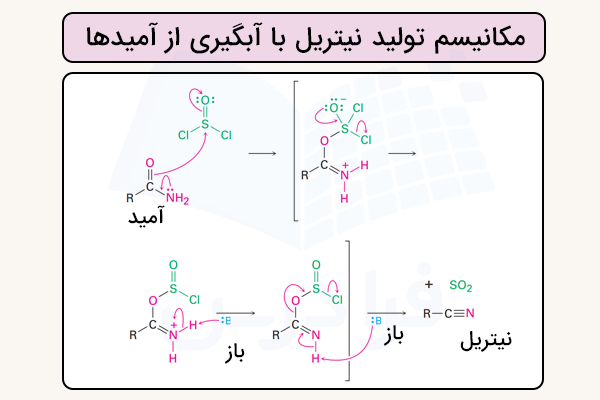
مکانیسم واکنش
آبگیری از ترکیبات آمیدی با استفاده از موادی مانند ، و است. در این فرایند ابتدا اکسیژن گروه کربونیل مورد حمله نوکلئوفیلی قرار میگیرد و سپس به گروه ترککننده مناسب تبدیل میشود و در مراحل بعدی حذف میشود. مرحله نهایی این واکنش برگشتناپذیر است و بهدلیل تشکیل محصولات پایدارتر و اثرات آنتروپی پیش میرود. مکانیزم انجام این واکنش در تصویر زیر نمایش داده شده است.
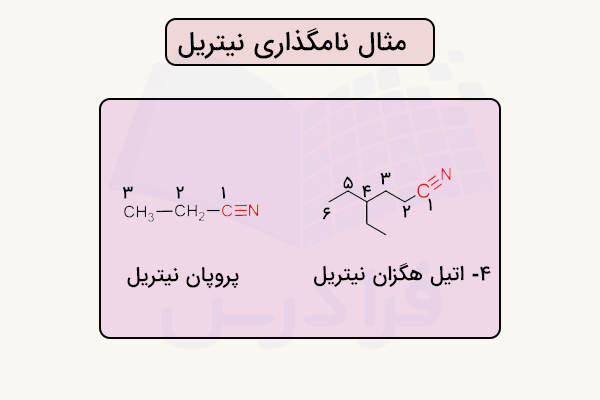
نامگذاری نیتریل
در نیتریلها، گروه عاملی دارای پیوند سهگانه با نام گروه نیتریل یا سیانو شناخته میشود. اگر این گروه اصلیترین گروه عاملی در ترکیب باشد، پسوند «نیتریل» به نام ترکیب پایه اضافه میشود. در این حالت، اتم کربنی که در پیوند سهگانه قرار دارد جزئی از زنجیر اصلی محسوب میشود. برای مثال ، ترکیب بوتیرونیتریل طبق نامگذاری آیوپاک با نام بوتاننیتریل شناخته میشود، زیرا اتم کربن مربوط به گروه نیتریل در زنجیر اصلی در نظر گرفته میشود.
استفاده از پسوند کربونیتریل
در یک شیوه دیگر نامگذاری، میتوان از پسوند «کربونیتریل» استفاده کرد که مشابه نامگذاری اسیدهای کربوکسیلیک است. در این حالت، اتم کربن گروه نیتریل بهعنوان بخشی از زنجیر اصلی در نظر گرفته نمیشود. استفاده از پسوند کربونیتریل زمانی ضروری است که گروه نیتریل به یک حلقه متصل باشد، مانند سیکلوپنتانکربونیتریل، یا زمانی که همه اتمهای کربن در زنجیر اصلی قرار نگیرند. این وضعیت بهطور خاص در ترکیباتی با بیش از دو گروه نیتریل دیده میشود، زیرا این گروهها فقط میتوانند در انتهای زنجیر قرار بگیرند.
استفاده از پیشوند سیانید
اگر گروه نیتریل مهمترین گروه عاملی در مولکول نباشد، از پیشوند سیانو بههمراه شماره موقعیت مناسب استفاده میشود. در این حالت نیز اتم کربن دارای پیوند سهگانه بهعنوان بخشی از زنجیر اصلی در نظر گرفته نمیشود.
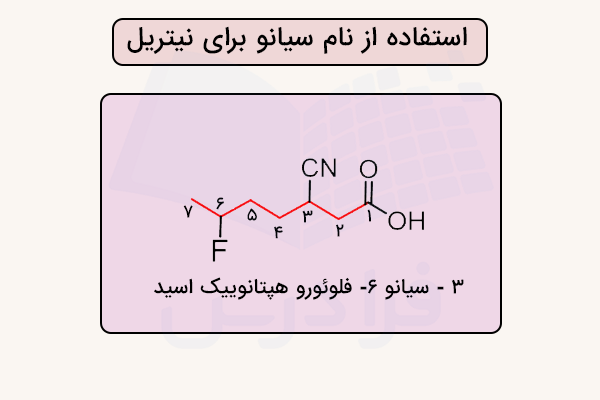
استفاده از نام کربوکسیلیک اسید متناظر
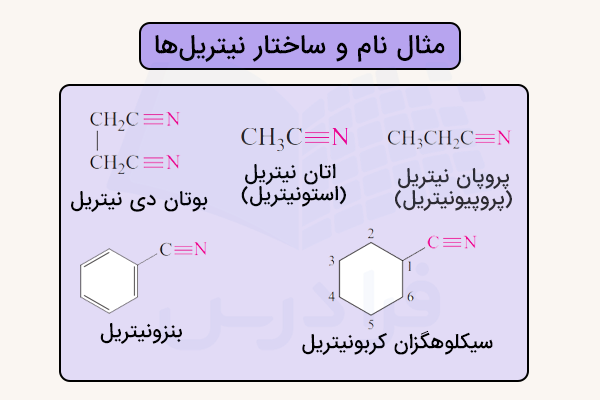
بهدلیل شباهت نیتریلها با اسیدهای کربوکسیلیک از نظر حالت اکسایش کربن، نامهای متداول آنها اغلب از نام اسید کربوکسیلیک متناظر گرفته میشود و پسوند « -و نیتریل» به آن افزوده میشود. برای مثال، اسید بنزوئیک به بنزونیتریل تبدیل میشود. در تصویر زیر ساختار چند نیتریل و نام آنها مشخص شده است.
پیشنهاد میکنیم برای درک بهتر روش نامگذاری کربوکسیلیک اسیدها و سایر هیدروکربنها، مطلب نام گذاری هیدروکربنها را در مجله فرادرس مطاله کنید.
واکنش های نیتریل چیست؟
نیتریلها ترکیباتی واکنشپذیر هستند و بهطور گسترده برای تولید آمینهای نوع اول، اسیدهای کربوکسیلیک و مشتقات آنها استفاده میشوند. گروه نیتریل همانند گروه کربونیل به شدت قطبی است و اتم کربن آن خاصیت الکتروفیلی دارد. به همین دلیل، نیتریلها با نوکلئوفیلها واکنش میدهند.
در ادامه مهمترین واکنشهای ترکیبات نیتریل را توضیح میدهیم.
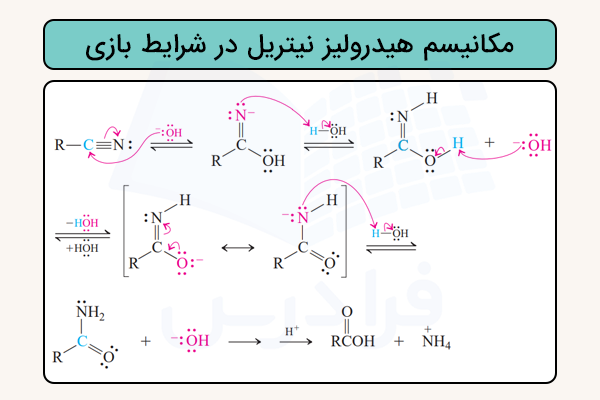
هیدرولیز نیتریل
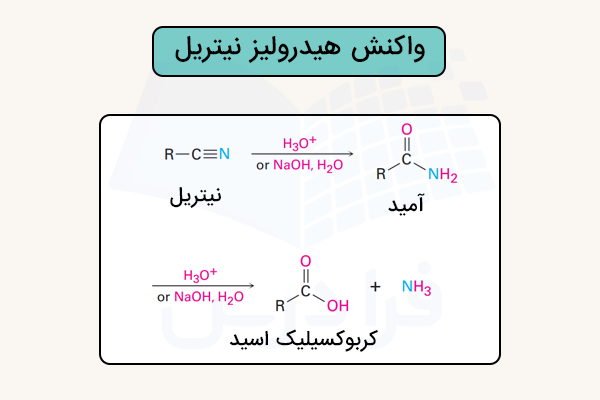
در واکنش هیدرولیز، پیوند سهگانه با آب شکسته شده و اسید کربوکسیلیک یا نمک آن تشکیل میشود. این فرایند معمولا در حضور اسید یا باز قوی انجام میشود. در محیط اسیدی، نیتریل ابتدا پروتونه میشود و سپس مولکول آب به کربن متصل میشود و در نهایت به اسید کربوکسیلیک تبدیل میشود. در محیط بازی، یون هیدروکسید مستقیما به نیتریل حمله کرده و یون کربوکسیلات تشکیل میشود.
این واکنش در تصویر زیر نمایش داده شده است.
مکانیسم
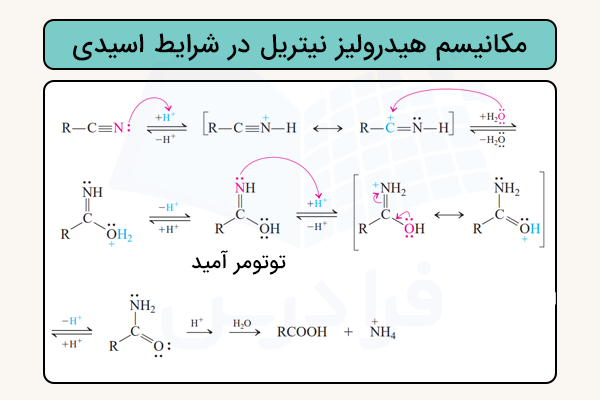
سازوکار این واکنشها از طریق تشکیل حدواسط آمید پیش میرود و شامل مراحل افزایشی - حذفی است. در شرایط اسیدی، ابتدا پروتوندار شدن روی اتم نیتروژن باعث افزایش تمایل مولکول برای حمله نوکلئوفیلی آب میشود. سپس آب به کربن نیتریل حمله میکند و با از دست دادن یک پروتون از اکسیژن، یک حدواسط خنثی تشکیل میشود که در واقع توتومر یک آمید است. در ادامه، پروتوندار شدن دوباره نیتروژن و سپس برداشت پروتون از اکسیژن رخ میدهد و آمید ایجاد میشود. در نهایت، آمید از مسیر معمول افزایشی - حذفی هیدرولیز شده و به اسید کربوکسیلیک تبدیل میشود.
در شرایط بازی، یون هیدروکسید مستقیما به نیتریل حمله میکند و آنیون توتومر آمید تشکیل میشود که روی نیتروژن پروتوندار میشود. سپس پروتون باقیمانده از اکسیژن توسط باز جدا میشود و دوباره پروتوندار شدن نیتروژن رخ میدهد تا آمید حاصل شود. ادامه هیدرولیز آمید نیز طبق سازوکار معمول انجام میگیرد و در نهایت اسید کربوکسیلیک به دست میآید.
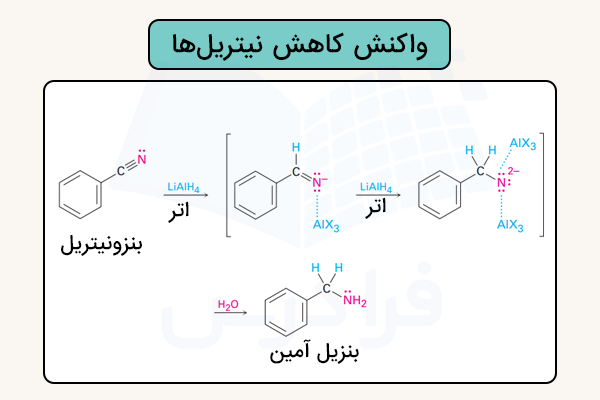
کاهش نیتریل
نیتریلها میتوانند با عوامل کاهندهای مانند یا هیدروژن در حضور کاتالیزور به آمینهای نوع اول تبدیل شوند. در این فرایند، پیوند سهگانه شکسته شده و پیوندهای یگانه جایگزین آن میشوند. سپس با افزودن هیدریدهای بیشتر و در نهایت هیدرولیز، آمین تولید میشود. این واکنش از طریق حمله نوکلئوفیلی یون هیدرید به پیوند قطبی آغاز میشود و یک آنیون ایمینی به وجود میآورد. این حدواسط همچنان دارای پیوند کربن-نیتروژن است، بنابراین یک حمله نوکلئوفیلی دوم توسط هیدرید انجام میشود و یک دیآنیون تشکیل میشود.
در نهایت، با افزودن آب در مرحله هیدرولیز، دیآنیون پروتوندار شده و آمین نهایی حاصل میشود. سازوکار این واکنش برای ترکیب بنزونیتریل در تصویر زیر نمایش داده شده است.
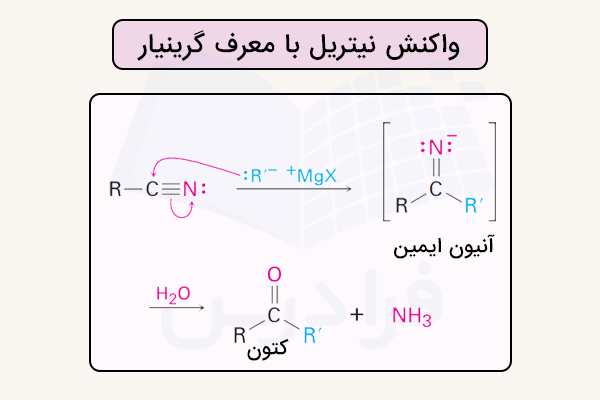
واکنش با ترکیبات آلی فلزی
ترکیبات آلیفلزی مانند واکنشگرهای گرینیار که شامل یک گروه آلکیل یا آریل متصل به منیزیم هالید هستند، میتوانند به کربن گروه نیتریل اضافه شوند و یک پیوند جدید کربن-کربن ایجاد کنند. در این واکنش، کربن نیتریل که کمبود الکترون دارد، گونه غنی از الکترون را جذب میکند و یک حدواسط ایمین تشکیل میشود.
این حدواسط میتواند در ادامه هیدرولیز شده یا به ترکیباتی مانند کتونها تبدیل شود. این واکنش برای ساخت مولکولهای پیچیدهتر بسیار مهم است. سازوکار این واکنش در تصویر زیر نمایش داده شده است.
آلکیلاسیون نیتریل
در این واکنش، نیتریلها میتوانند آلکیله شوند و یونهای نیتریلی تشکیل دهند. واکنشهای دیگر شامل واکنشهای افزایشی نوکلئوفیلی و آسیلاسیون فریدل-کرافتس هستند. در واکنش فریدل-کرافتس، یک گروه آلکیل جایگزین هیدروژن روی حلقه آروماتیک میشود. این واکنش با کمک کاتالیزورهای لوئیس مانند یا انجام میشود و از طریق تشکیل کربوکاتیون پیش میرود.
مثال واکنش نیتریل
برای درک بهتر واکنشهایی که در قیمت قبل برای تهیه نیتریل آورده شده است، به سوالات زیر پاسخ دهید.
مثال ۱
چطور میتوان ۲-متیل-۳-پنتانون را از یک نیتریل تهیه کرد؟
پاسخ
در واکنش بین یک معرف گرینیار و یک نیتریل، یک کتون تشکیل میشود که در آن کربن گروه به کربن کربونیل تبدیل میشود. بنابراین باید دو گروه متصل به کربن کربونیل در محصول را شناسایی کرد. یکی از این گروهها از معرف گرینیار و دیگری از نیتریل تامین میشود. این واکنش با استفاده از دو روش زیر امکانپذیر است.
حالت اول
- نیتریل: پروپانونیتریل
- معرف گرینیار: ایزوپروپیلمنیزیم برومید
حالت دوم
- نیتریل: ایزوبوتیرونیتریل
- معرف گرینیار: اتیلمنیزیم برومید
در هر دو حالت، پس از واکنش گرینیار با نیتریل و انجام هیدرولیز اسیدی، کتون مورد نظر یعنی ۲-متیل-۳-پنتانون به دست میآید.
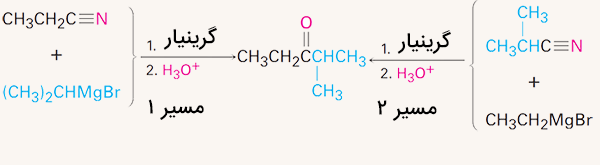
مثال ۲
چطور میتوان ۱-فنیل-۲-بوتانون را از بنزیل برومید تهیه کرد؟ این فرآیند به بیش از یک مرحله نیاز دارد.
پاسخ
ابتدا باید بنزیل برومید را به نیتریل تبدیل کنیم و سپس با استفاده از واکنش گرینیار آن را به کتون مورد نظر برسانیم. مرحله اول شامل تبدیل به نیتریل با سدیم سیانید است. واکنش جانشینی نوکلئوفیلی نوع با سدیم سیانید به شکل زیر است.
مرحله دوم با تشکیل کتون با معرف گرینیار تکمیل میشود. واکنش نیتریل با اتیل منیزیم برومید و سپس هیدرولیز اسیدی به شکل زیر است.
در این مسیر، کربن گروه به کربن کربونیل تبدیل میشود و گروه اتیل از معرف گرینیار به آن متصل میشود، در نتیجه ۱-فنیل-۲-بوتانون به دست میآید.
کاربرد نیتریل چیست؟
نیتریلها کاربردهای گستردهای در صنایع و پزشکی دارند. برای مثال، دستکشهای نیتریل یکی از پراستفادهترین نوع دستکش در آزمایشگاهها و مصارف پزشکی هستند. همچنین، برخی از داروهای درمان سرطان نیز دارای ساختار نیتریل در ترکیب شیمیایی خود هستند. در ادامه برخی از کاربردهای این مواد را معرفی میکنیم.

دستکش نیتریل
دستکشهای نیتریلی از لاستیک نیتریلی ساخته میشوند که از آکریلونیتریل بهدست میآید. این دستکشها در محیطهای پزشکی، آزمایشگاهی و صنعتی بهدلیل مقاومت بالا در برابر مواد شیمیایی، سوراخشدن و ایجاد حساسیت، بسیار پرکاربرد هستند.
لاستیک نیتریل
یکی از رایجترین موارد حضور نیتریلها در مواد مختلف، لاستیک نیتریل است. لاستیک نیتریل یک کوپلیمر مصنوعی از آکریلونیتریل و بوتادین بهشمار میآید. این نوع لاستیک مقاومت بسیار بالایی در برابر مواد شیمیایی دارد و به همین دلیل در تولید دستکشهای محافظ، شیلنگها و انواع آببندها مورد استفاده قرار میگیرد.
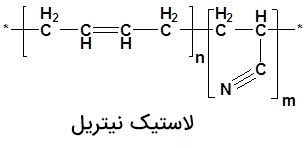
نساجی
الیاف اکریلیک که از پلیآکریلونیتریل تولید میشوند، در تولید لباس، پتو و فرش استفاده میشوند و بهدلیل سبک بودن، گرم بودن و مقاومت در برابر مواد شیمیایی و حشرات مورد توجه قرار دارند.
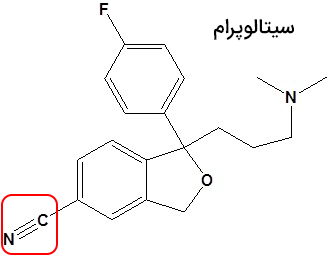
داروسازی
بسیاری از ترکیبات نیتریلی بهعنوان واسطه در تولید داروها استفاده میشوند. این ترکیبات در ساخت داروهایی برای درمان بیماریهایی مانند فشار خون بالا، افسردگی و سرطان نقش دارند. برای مثال، ساختار داروی ضدافسردگی سیتالوپرام در تصویر زیر آورده شده است.
سایر کاربردها
علاوه بر موارد اشاره شده، نیتریلها در بسیاری دیگر از صنایع و ترکیبات حضور دارند و استفاده میشوند. در ادامه برخی از این کاربردها را نام میبریم.
- در تولید دستکشهای نیتریلی، درزگیرها و شیلنگها استفاده میشوند، زیرا در برابر مواد شیمیایی مقاوم هستند.
- در برخی داروها از جمله داروهای مرتبط با دیابت و درمان سرطان پستان کاربرد دارند.
- ترکیبی به نام پریسایازین از مشتقات نیتریل است که بهعنوان داروی ضد روانپریشی در درمان اعتیاد استفاده میشود.
- این ترکیبات در منابع گیاهی و جانوری نیز یافت میشوند.
- در تولید مواد مقاوم در برابر روغن و کاربردهای دما پایین استفاده میشوند.
- در سیستمهای خودرویی، شیلنگهای هیدرولیکی و سامانههای هواپیما کاربرد دارند.
- استفاده در قطعات خودرو، واشرها، سیستمهای سوخت و لولهها
- استفاده در صنایع نفت و گاز و اتصالات و قطعات آببندی
- برای تولید آمینها استفاده میشوند.
شناسایی نیتریل ها
در قسمتهای قبل آموختیم نیتریل چیست و چه واکنشهایی دارد. شناسایی نیتریلها در ترکیبات مختلق با استفاده از طیف سنجی مادون قرمز یا NMR انجام میشود. در ادامه این موارد را توضیح میدهیم. پیشنهاد میکنیم برای آشنایی با سایر روشهای شناسایی ترکیبات آلی، فیلم آموزش شناسایی ترکیبات آلی فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
طیف IR نیتریل
نیتریلها در طیفسنجی فروسرخ، یک جذب قوی و قابل تشخیص مربوط به پیوند در ناحیه حدود ۲۲۵۰ سانتیمتر به توان منفی یک نشان میدهند. این مقدار برای ترکیبات اشباع به طور معمول نزدیک به ۲۲۵۰ سانتیمتر به توان منفی یک است، در حالی که در ترکیبات آروماتیک و مزدوج این جذب در حدود ۲۲۳۰ سانتیمتر به توان منفی یک دیده میشود. از آنجا که تعداد کمی از گروههای عاملی دیگر در این ناحیه جذب دارند، طیفسنجی مادون قرمز ابزار بسیار مناسبی برای شناسایی و تشخیص نیتریلها به شمار میرود.
طیف NMR نیتریل
نیتریلها در NMR کربن-۱۳ در محدوده ۱۱۵ تا ۱۳۰ ppm جذب نشان میدهند. به همین دلیل شناسایی آنها با این روش طیف سنجی (به خصوص در مقایسه با اسیدها) بسیار کاربردی است.
تاریخچه نیتریل
در این مطلب از مجله فرادرس آموختیم نیتریل چیست. نخستین بررسیهای مهم درباره نیتریلها به اواخر قرن هجدهم و اوایل قرن نوزدهم برمیشود. «شله» (Carl Wilhelm Scheele) در ۱۷۸۲ هیدروژن سیانید را سنتز کرد و «گیلوساک» (Joseph Louis Gay-Lussac) در ۱۸۱۱ آن را به صورت خالص تهیه کرد و بعدها در ۱۸۱۵ دیسیان را ساخت. سپس «وهلر» (Friedrich Wöhler) و «لیبیگ» (Justus von Liebig) بنزونیتریل را سنتز کردند و «پلوز» (Théophile-Jules Pelouze) نیز پروپیونیتریل را به دست آورد.
در ۱۸۴۴ «فلینگ» (Hermann Fehling) روش موثری برای تهیه بنزونیتریل ارائه داد و واژه نیتریل را معرفی کرد. در قرن بیستم، درک سازوکار و کاربرد نیتریلها گسترش یافت. «لپورت» (Arthur Lapworth) در ۱۹۰۳ نقش یون سیانید در تشکیل سیانوهیدرینها را نشان داد. از دهه ۱۹۳۰ به بعد، نیتریلها وارد کاربردهای صنعتی مهم شدند. برای مثال، تولید نایلون از آدیپونیتریل و توسعه آکریلونیتریل برای الیاف مصنوعی و سیانوآکریلاتها برای چسبهای فوری از کاربردهای این ماده در قرن اخیر است.












