فلز و نافلز چیست؟ – به زبان ساده
فلزات و نافزات مواد پیرامون ما را تشکیل میدهند. در حقیقت، عناصر را میتوان به فلز و نافلز تقسیم کرد و باید بدانیم که هریک در کدام دسته قرار دارند. فلزات - به طور مثال مس و آلومینیوم - رسانای خوب گرما و الکتریسیته هستند درحالیکه نافلزات - مانند فسفر و گوگرد - خاصیتی عایق دارند. بنابراین، فلز و نافلز را بسته به نوع خواص ماده میتوان از یکدیگر تشخیص داد. در این مطلب از مجله فرادرس میآموزیم فلز و نافلز چیست و ویژگیهای آنها کدام است.
- با فلزات در جدول تناوبی آشنا شده و ویژگیهای آنها را میشناسید.
- میآموزید عناصر نافلزی کدامند و چه خواصی دارند.
- میتوانید تفاوت شبهفلزات را با فلز و نافلز تشخیص دهید.
- خواص فیزیکی و شیمیایی فلز و نافلز را میشناسید.
- با تفاوتهای اصلی فلزات و نافلزات آشنا میشوید.
- کاربرد نافلزات به عنوان سوخت را میشناسید.


فلز چیست؟
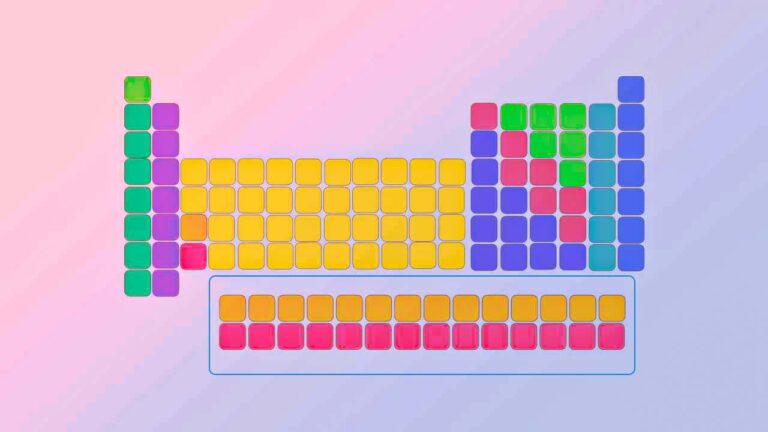
بیشتر عناصر در جدول تناوبی را فلزات تشکیل دادهاند. از جمله عناصر فلزی میتوان به فلزات قلیایی، فلزات قلیایی خاکی، فلزات واسطه و همچنین لانتانیدها و اکتینیدها اشاره کرد. فلز و نافلز در جدول تناوبی به کمک یک خط زیگزاگ از یکدیگر جدا شدهاند. این خط از کربن شروع میشود و تا «رادون» (Radon) ادامه دارد. عناصر بین این دو، فسفر، سلنیوم و ید هستند.
عناصر بالا و همچنین عناصر سمت راست آنها در جدول تناوبی، در دسته نافلزات جای میگیرند. عناصری که در سمت چپ این خط قرار دارند را با نام «شبه فلز» (Metalloid) میشناسند. این عناصر، خواصی ترکیبی از فلز و نافلز را شامل میشوند.

نافلزات، بخش بالایی و سمت راست جدول تناوبی را شامل میشوند. در رابطه با خواص آنها نیز باید گفت که مانند فلزات، براق و چکشخوار نیستند و نمیتوان از آنها برای هدایت جریان الکتریکی استفاده کرد. همین خواص هستند که سبب میشوند تا به راحتی، تفاوت فلز و نافلز را درک کنیم.
اشتراک میان خواص نافلزات از فلزها بسیار کمتر است زیرا خواص فیزیکی و شیمیایی آنها تغییرات بسیار زیادی دارد. برخی نافلزات، جامد و برخی در دمای اتاق، به حالت گاز قرار دارند.

نافلز چیست؟
همانطور که گفته شد، عناصر بسیار کمی در جدول تناوبی به عنوان نافلز شناخته میشوند. این عناصر را در سمت راست جدول تناوبی میتوان مشاهده کرد. عناصر نافلزی شامل گوگرد، کربن، هالوژنها، فسفر، هیدروژن، اکسیژن، سلنیوم، نیتروژن و گازهای نجیب هستند. در جدول تناوبی، نافلزات در سمت چپ هالوژنها و سمت راستِ شبهفلزات قرار دارند.
ویژگی فلز و نافلز
در ادامه این آموزش، به بررسی خواص فلز و نافلز میپردازیم. خواص فلزات و نافلزات را میتوان به طور جداگانه به دو دسته خواص فیزیکی و شیمیایی تقسیم کرد و هریک را به طور مجزا مورد بررسی قرار داد. پیشنهاد می کنیم برای درک بهتر این ویژگیها، فیلم آموزش تفاوت عناصر فلزی، نافلزی و شبه فلزی در جدول تناوبی فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
خواص فیزیکی فلز
در فهرست زیر، برخی از خواص فیزیکی فلزات آورده شده است.
لازم به ذکر است، به غیر از جیوه، تمامی فلزات در دمای اتاق به حالت جامد قرار دارند.

خواص شیمیایی فلز
برخی از خواص شیمیایی فلزات در زیر، فهرست شدهاند:
- به راحتی دچار خوردگی میشوند.
- میتوانند الکترون از دست بدهند.
- اکسیدهای بازی تشکیل میدهند.
- الکترونگاتیوی پایینی دارند.
- عوامل کاهنده مناسبی به شمار میآیند.
خواص فیزیکی نافلز
خواص فیزیکی نافلزات در فهرست زیر آورده شده است:
- هادی ضعیف الکتریسیته و حرارت هستند.
- چکشخوار نیستند.
- جامدهایی شکننده هستند.
- در دمای اتاق به حالتهای مختلف جامد، مایع و گاز وجود دارند.
- در برخی موارد، موادی شفاف را تشکیل میدهند.
خواص شیمیایی نافلز
در ادامه بررسی فلز و نافلز به خواص شیمیایی نافلزات اشاره میکنیم که این خواص در زیر آورده شدهاند:
- تعداد الکترونها در لایه خارجی به طور معمول بین ۴-۸ الکترون است.
- به راحتی الکترون جذب میکنند و از دست میدهند.
- در تماس با اکسیژن، اکسیدهای اسیدی تولید میکنند.
- عناصری با الکترونگاتیوی بالا (خاصیت نافلزی) به شمار میآیند.
- عوامل اکسنده مناسبی هستند.
فلز و نافلز آلوتروپهای مختلفی را تشکیل میدهند که شکل و خواص متفاوتی دارند. از جمله آلوتروپها میتوان به الماس و گرافیت اشاره کرد و همچنین در مثالی دیگر باید گفت عنصر آهن دارای دو آلوتروپ «آستنیت» (Austenite) و «فریت» (Ferrite) است.
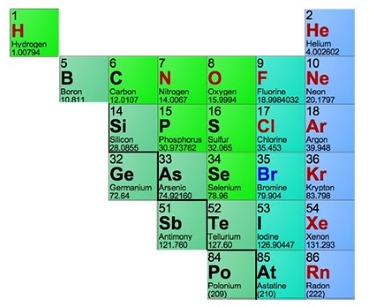
تفاوت فلز و نافلز
برای اینکه درک بهتری از تفاوتهای فلزات و نافلزات داشته باشیم، این تفاوتها در زیر به صورت جدول آورده شدهاند:
| فلزات | نافلزات |
| به غیر از جیوه، در دمای اتاق به شکل جامد وجود دارند. | در هر سه حالت جامد و مایع و گاز دیده میشوند. |
| به غیر از سدیم، بسیار سخت هستند. | به غیر از الماس، موادی نرم هستند. |
| خاصیت چکشخواری و تورقپذیری دارند. | در حالت جامد، خاصیت شکنندگی دارند و به قطعات کوچکتری خرد میشوند. |
| براق هستند. | به غیر از ید، هیچکدام شفاف نیستند. |
| الکترونگاتیوی آنها پایین است. | الکترونگاتیوی بالایی دارند. |
| چگالی بالایی دارند. | نسبت به فلزات، چگالی کمتری دارند. |
سوالات متداول در زمینه فلز و نافلز
حال که تا اینجای کار با فلزات و نافلزات آشنا شدیم، ممکن است سوالاتی در ذهن شما پیش بیاید که در ادامه، به بررسی برخی از سوالات متداول در زمینه فلز و نافلز میپردازیم.
نافلز را تعریف کنید و چند نمونه نافلز را نام ببرید؟
نافلز به عنصری شیمیایی میگویند که شامل هیچ خاصیت فلزی نباشد. از نمونههای نافلزات میتوان به هیدروژن، هلیوم، اکسیژن، نیتروژن، فلوئور، نئون و ... اشاره کرد.
فلز را تعریف کنید و چند نمونه فلز را نام ببرید؟
بسیاری از عناصر شیمیایی را میتوان در دسته فلزات قرار داد که در گروههای مختلفی از جدول تناوبی قرار دارند. تقریبا تمامی فلزات، رسانای خوب جریان الکتریکی و حرارت هستند و به راحتی میتوان آنها را شکل داد.
کدام نافلز برای ادامه حیات، ضروری است؟
اکسیژن، نافلزی است که برای ادامه حیات انسان ضروری است و بدون آن، حیات انسانها و بسیاری از موجودات، امکانپذیر نیست.
کدام نافلز به عنوان سوخت بکار میرود؟
سوختی که در موشکها مورد استفاده قرار میگیرد، هیدروژن مایع است. مخازن مجزایی از هیدروژن و اکسیژن وجود دارند که در ترکیب با یکدیگر، انرژی مورد نیاز موشک را تامین میکنند.
آزمون فلز و نافلز
۱. کدام ویژگی برای تفکیک فلزات از نافلزات به کار میرود؟
داشتن رنگ سفید براق
قابلیت حل شدن در آب
دارا بودن رسانایی الکتریکی
قابلیت ترکیب با اکسیژن
ویژگی «دارا بودن رسانایی الکتریکی» مشخصه اصلی فلزات است که آنها را از نافلزات متمایز میکند. فلزها معمولا جریان برق را به خوبی عبور میدهند، ولی نافلزها عایق هستند. موارد مانند «قابلیت ترکیب با اکسیژن» میتواند هم برای فلز و هم نافلز رخ دهد، «داشتن رنگ سفید براق» ویژگی عمومی فلزها نیست و «قابلیت حل شدن در آب» برای هر دو گروه الزامی نیست و نشانهای برای تشخیص آنها نیست.
۲. کدام ویژگی موجب شده فلزها نسبت به نافلزها برای رسانایی الکتریکی مناسبتر باشند؟
نافلزها به طور معمول در برابر برق واکنش شیمیایی میدهند.
فلزها به خوبی گرما و برق را عبور میدهند.
نافلزها رسانای عالی گرما هستند.
فلزها به راحتی در آب حل میشوند.
فلزات رسانای عالی جریان برق هستند. در حالی که نافلزها بیشتر خاصیت عایق دارند و نمیتوانند به خوبی برق را از خود عبور دهند.
۳. برای ساخت سیم برق، انتخاب عناصر کدام گروه مناسبتر است و چرا؟
نافلزات به دلیل نرم بودن
نافلزات به دلیل عایق بودن
فلزات به دلیل شکننده بودن
فلزات به دلیل رسانایی بالا
فلزها به طور طبیعی رسانای خوب جریان برق هستند و به همین سبب برای ساخت سیم برق بسیار مناسباند.








چرا میگیم عنصر نافلز مانند کلر و گوگرد نیز مولکول هستند اگر عنصر هستند پس نباید مولکول باشند؟ لطفا این موضوع را توضیح دهید
با سلام؛
برای پاسخ به این سوال ابتدا باید مفهوم عنصر و مولکول را به خوبی بیاموزیم. عناصر، اتمهایی تکی هستند که به صورت مجزا مطالعه و بررسی میشوند. گوگرد با نماد شیمیایی S و کلر با نماد شیمیایی Cl، عناصری هستند که به ترتیب در گروههای ۱۶ و ۱۷ جدول تناوبی قرار دارند. این عناصر مولکولهایی چند اتمی تشکیل میدهند. مولکول این عناصر از ترکیب دو یا چند عنصر یکسانِ متصل تشکیل میشود و نام این مولکولها مشابه نام عناصر آنها است. بنابراین وقتی از مولکول کلر حرف میزنیم، منظور مولکول دو اتمی کلر با فرمول شیمیایی Cl2 است. به همین ترتیب، «مولکول گوگرد» به مولکول چند اتمی S8 اشاره دارد. پیشنهاد میکنیم برای درک بهتر این مفاهیم، مطلب عنصر مولکولی مجله فرادرس را مطالعه فرمایید.
با تشکر از همراهی شما با مجله فرادرس
باسلام لطفا عکسی از جدول قرار بدهید که فلزات نافلزات و شبه فلزات رو از هم تفکید شده نشان بده ممنون مطلبتون عالی بود
سلام
مچکرم از داده های بسیار عالی تون خیلی برام کاربردی و مفید بود🌸
سلام
چون ذرات سازنده فلزات فقط اتم ها هستن
ولی نافلزات رو مولکول ها تشکیل داده اند
مولکول از تشکیل دویا چند اتم به وجود می اید
سلام. چرا نافلزات ساختار مولکولی دارن و فلزات ساختار اتمی؟
خوبه اطلاعاتتون ممنون
با سلام؛
خوشحالیم که مطالعه این مطلب برای شما مفید بوده است.
با تشکر
نوشتین به جز ید هیچکدوم شفاف نیستن ولی الماس یه نافلز شفافه
سلام فلز فعال تر است یا نافلز؟
با سلام؛
از حسن توجه شما سپاسگزاریم. در موارد بسیاری، الماس به صورت شفاف وجود دارد اما الماسی که تراشکاری شده نباشد، به طور معمول به صورت سنگی نیمهکدر دیده میشود و موسوم به «الماس خام» (Raw Diamond) یا «Uncut Diamond» است.
با تشکر