خواص ترمودینامیک سیالات – به زبان ساده
خواص ترمودینامیکی سیالات نقش اساسی در توصیف وضعیت و رفتار آنها در شرایط مختلف را دارند. این خواص در کنار میدان سرعت، امکان تحلیل دقیق جریان، انتقال انرژی و تغییرات حالت را فراهم میکنند. این خواص شامل کمیتهایی مانند فشار، دما، چگالی، انرژی درونی، آنتالپی، آنتروپی، گرمای ویژه، گرانروی و رسانندگی گرمایی هستند. این کمیتها پایهی بسیاری از تحلیلهای مهندسی بوده و در طراحی و بررسی سیستمهای مرتبط با سیالات اهمیت ویژهای دارند. در این مطلب از مجله فرادرس میآموزیم خواص ترمودینامیک سیالات چیست.
- میآموزید خواص ترمودینامیکی سیالات چیست و شامل چه کمیتهایی است.
- اهمیت خواص ترمودینامیکی سیالات و انواع کمیتهای ترمودینامیکی را میشناسید.
- با مفهوم فشار و دما در سیالات آشنا میشوید.
- چگالی در سیالات را شناخته و با اثر دما و فشار بر آن آشنا میشوید.
- روابط و معادله حالت را برای گازها و مایعات بررسی میکنید.
- با گرانروی و رسانندگی گرمایی سیالات آشنا میشوید.


در ابتدای این مطلب مفهوم خواص ترمودینامیکی سیالات را بررسی کرده و آنها را معرفی میکنیم. سپس به بررسی کمیتهای اصلی مانند فشار، دما و چگالی پرداخته و در ادامه خواص انرژی و گرمایی از جمله انرژی درونی، آنتالپی و آنتروپی را توضیح میدهیم. پس از آن، روابط حالت در سیالات (برای گازها و مایعات) بررسی شده و در نهایت خواص انتقالی مهم شامل گرانروی و رسانندگی گرمایی را میآموزیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید خواص ترمودینامیکی سیالات چیست.
خواص ترمودینامیکی سیالات چیست؟
در مکانیک سیالات، با اینکه میدان سرعت مهمترین ویژگی جریان است، اما این کمیت بهتنهایی کافی نیست و همواره در کنار خواص ترمودینامیکی بررسی میشود. این خواص به ما کمک میکنند رفتار فیزیکی سیال را بهتر درک کنیم و بتوانیم تحلیل دقیقتری از جریان ارائه دهیم. در واقع، بدون در نظر گرفتن این کمیتها، توصیف کامل یک جریان امکانپذیر نیست.
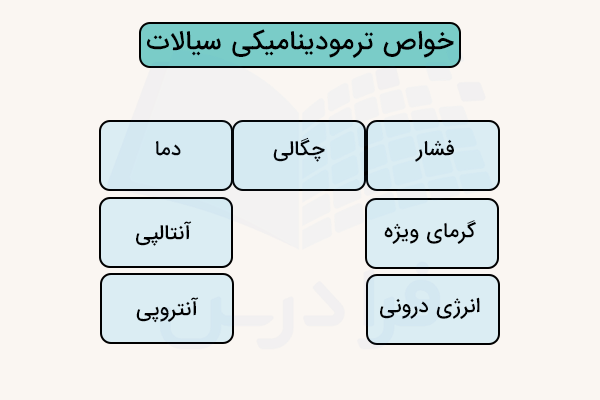
خواص ترمودینامیکی سیالات کمیتهایی هستند که در ادامه نام برده شدهاند.
- فشار
- چگالی
- دما
- انرژی درونی
- آنتالپی
- آنتروپی
- گرمای ویژه (در حجم یا فشر ثابت)
این موارد، خواص واقعی ترمودینامیکی هستند که به حالت سیال بستگی دارند. برای مثال، در یک ماده تکفاز مانند آب یا اکسیژن، دانستن دو خاصیت مستقل مانند فشار و دما کافی است تا بقیه خواص مشخص شوند. علاوه بر خواص ترمودینامیکی، خواص انتقالی مرتبط با ترمودینامیک سیال مانند ضریب گرانروی و رسانندگی گرمایی، در تحلیل جریان اهمیت دارند. این خواص در ادامه نام برده شدهاند.
- ضریب گرانروی
- رسانندگی گرمایی (رسانایی حرارتی)
در این مطلب این موارد را بررسی کرده و توضیح میدهیم.
اهمیت خواص ترمودینامیکی سیالات
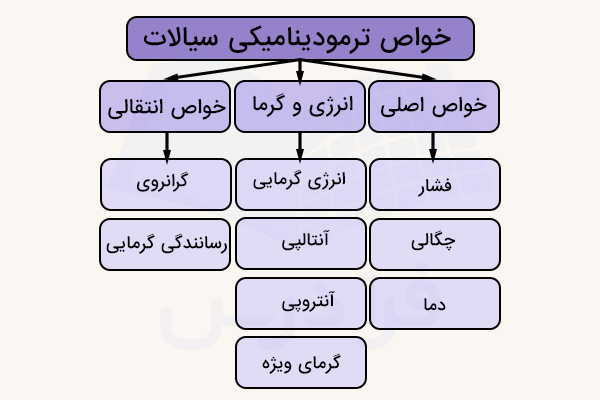
دما، فشار و چگالی، سه کمیت اصلی ترمودینامیکی هستند که برای بررسی میدان جریان در آنالیز جریان سیال استفاده میشوند. چهار خاصیت ترمودینامیکی دیگر سیالات که در حضور کار، گرما و سایر صورتهای انرژی استفاده و بررسی میشوند، عبارتند از
- انرژی درونی
- آنتالپی
- آنتروپی
- گرمای ویژه (ظرفیت گرمایی ویژه)
همچنین، اثرات اصطکاک و هدایت گرمایی به دو خاصیت انتقالی وابسته هستند. این دو کمیت ضریب گرانروی و رسانندگی گرمایی هستند.
اگر تا این قسمت از مطلب را مطالعه کردهاید، با انواع خواص ترمودینامیکی سیالات آشنا شدهاید. در ادامه این مطلب نیز به بررسی بیشتر این خواص میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
کمیت های اصلی ترمودینامیکی
سه خاصیت بنیادی که در تقریبا تمام مسائل جریان حضور دارند، فشار، چگالی و دما هستند. این سه کمیت بهطور مستقیم وضعیت سیال را مشخص میکنند و معمولا به عنوان متغیرهای پایه در تحلیلها به کار میروند. این کمیتها همواره همراه با میدان سرعت در نظر گرفته میشوند و تغییرات آنها نقش مهمی در رفتار جریان، مانند انبساط، تراکم و انتقال انرژی دارد.
خواص انرژی و گرمایی
در بررسیهایی که شامل کار، گرما و انرژی هستند، خواص دیگری نیز اهمیت پیدا میکنند. از جمله این خواص میتوان به انرژی درونی، آنتالپی، آنتروپی و گرماهای ویژه اشاره کرد. آنتالپی به صورت زیر تعریف میشود:
در این رابطه، کمیت نشاندهنده آنتالپی ویژه و بیانگر مجموع انرژیهای موجود در سیال به ازای واحد جرم است، انرژی درونی ویژه و نشاندهنده انرژی ذخیرهشده درون سیال است، فشار سیال را نشان میدهد و چگالی سیال است که جرم در واحد حجم را بیان میکند. این کمیتها در تحلیلهای ترمودینامیکی پیشرفتهتر، مانند موازنه انرژی و بررسی فرایندهای حرارتی، نقش اساسی دارند و نشاندهنده نحوه ذخیره و انتقال انرژی در سیال هستند.
خواص انتقالی
علاوه بر خواص تعادلی، برخی ویژگیها به نحوه انتقال تکانه و گرما در سیال مربوط میشوند. مهمترین این خواص شامل گرانروی و رسانندگی گرمایی هستند. این کمیتها تعیین میکنند که سیال تا چه حد در برابر جاری شدن مقاومت دارد و گرما با چه سرعتی در آن منتقل میشود، بنابراین در پدیدههایی مانند اصطکاک، لایه مرزی و انتقال حرارت اهمیت زیادی دارند.
یادگیری مکانیک سیالات با فرادرس
برای درک بهتر مفهوم و کاربرد خواص ترمودینامیکی سیالات، نیاز است ابتدا با مفاهیمی چون فشار، وسیکوزیته، اثر مویینگی، سیالات نیوتونی و غیرنیوتونی، کشش سطحی و اصل بقای جرم آشنا شوید. پیشنهاد میکنیم برای یادگیری این مفاهیم و مطالب، به مجموعه فیلم آموزش مکانیک سیالات فرادرس مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مشاهده فیلمهای آموزش فرادرس که لینک آنها در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه خواص ترمودینامیکی سیالات دسترسی داشته باشید.
- فیلم آموزش دینامیک سیالات محاسباتی CFD 1 و گواهینامه فرادرس
- فیلم آموزش مکانیک سیالات دوفازی جامع و کاربردی فرادرس
- فیلم آموزش مکانیک سیالات پیشرفته و گواهینامه فرادرس
مفهوم خواص ترمودینامیکی
خواص ترمودینامیکی وضعیت یک سیستم را توصیف میکنند. سیستم به مجموعهای از ماده گفته میشود که هویت مشخصی دارد و با محیط اطراف خود برهمکنش میکند. در مکانیک سیالات، این سیستم معمولا یک المان بسیار کوچک از سیال در نظر گرفته میشود. در این حالت، خواص به صورت پیوسته در فضا و زمان تعریف میشوند. برای مثال در مورد چگالی، میتوان چگالی را در محورهای مختصات یا در زمان مشخصی درنظر گرفت.
این کار باعث میشود بتوانیم از معادلات ریاضی برای توصیف دقیق رفتار سیال استفاده کنیم. نکته مهم این است که ترمودینامیک معمولا با سیستمهای ساکن سروکار دارد، در حالی که سیالات اغلب در حال حرکت و تغییر هستند. با این حال، این خواص همچنان در جریان سیال معنا دارند. دلیل آن این است که در مقیاس مولکولی، برخوردهای بسیار زیادی در فاصلههای بسیار کوچک رخ میدهد و سیال به سرعت به حالت تعادل نزدیک میشود. بنابراین میتوان فرض کرد که این خواص در هر نقطه از سیال تعریف شده و از قوانین ترمودینامیک تعادلی پیروی میکنند.
فشار در سیالات
یکی از مهمترین خواص ترمودینامیکی سیالات، فشار است. فشار به تنش فشاری در یک نقطه از سیال ساکن گفته میشود. پس از سرعت، فشار سیالات مهمترین کمیت در مکانیک سیالات است. اختلاف یا گرادیان فشار معمولا عامل اصلی حرکت سیال، بهویژه در لولهها و مجاری، محسوب میشود.
در جریانهای کمسرعت، مقدار دقیق فشار اهمیت کمتری دارد، اما در سرعتهای بالا، بهویژه در گازها، فشار نقش بسیار تعیینکنندهای پیدا میکند. برای بسیاری از مسائل، فشار مرجع برابر با یک اتمسفر در نظر گرفته میشود.
کاهش بیش از حد فشار در مایعات نیز میتواند منجر به تشکیل حبابهای بخار شود که پدیدهای مهم در مهندسی به شمار میآید.
دما در سیالات
دما یکی از مهمترین خواص ترمودینامیکی سیالات است و به سطح انرژی درونی آن مربوط میشود. هرچه دمای یک سیال بیشتر باشد، به طور کلی انرژی جنبشی مولکولهای آن نیز بیشتر است. در جریانهای پرسرعت، بهویژه در گازها، دما میتواند تغییرات قابلتوجهی داشته باشد و نقش مهمی در رفتار جریان ایفا کند.
در بسیاری از کاربردهای مهندسی، از مقیاسهای سلسیوس یا فارنهایت استفاده میشود، اما در تحلیلهای دقیقتر باید از مقیاسهای مطلق استفاده کرد. این موارد در ادامه آورده شدهاند.
کمیت نشاندهنده دمای مطلق در مقیاس رانکین است، دما را در مقیاس فارنهایت بیان میکند و عدد ثابت مقدار اختلاف مبدا این دو مقیاس دمایی را نشان میدهد.
چگالی در سیالات
چگالی که با نماد نشان داده میشود، برابر جرم واحد حجم سیال است. این کمیت یکی از مهمترین پارامترها در تحلیل جریان محسوب میشود. چگالی در گازها بسیار متغیر است و با افزایش فشار، تقریبا به صورت متناسب افزایش مییابد. اما در مایعات، چگالی تقریبا ثابت است.
برای مثال، چگالی آب که حدود است، حتی با افزایش زیاد فشار تنها مقدار کمی تغییر میکند. به همین دلیل، بیشتر جریانهای مایع را میتوان به صورت تراکمناپذیر در نظر گرفت. به طور کلی، چگالی مایعات حدود هزار برابر بیشتر از گازها در فشار اتمسفری است.
برای مثال، چگالی جیوه مایع و هیدروژن گازی در ادامه آورده شده است.
- جیوه:
- هیدروژن:
این اختلاف بسیار زیاد نشان میدهد که رفتار سیالات مختلف میتواند تفاوت چشمگیری داشته باشد. این تفاوتها معمولا با استفاده از تحلیل ابعادی بررسی و مقایسه میشوند.
اثر دما و فشار بر چگالی
چگالی مایعات با تغییر دما و فشار کمی تغییر میکند. به طور کلی، با افزایش دما، چگالی اندکی کاهش مییابد و با افزایش فشار، مقدار آن کمی افزایش پیدا میکند. اگر اثر دما نادیده گرفته شود، میتوان رابطهای تجربی بین فشار و چگالی نوشت:
در این رابطه، B و n پارامترهای بدون بعد هستند که مقدار آنها به نوع سیال و دما بستگی دارد. برای مثال، برای آب، به طور تقریبی و است. این رابطه نشان میدهد که حتی با تغییرات قابلتوجه فشار، تغییر چگالی مایعات همچنان محدود باقی میماند.
وزن مخصوص
وزن مخصوص با نماد گاما () نشان داده میشود و برابر وزن واحد حجم سیال است. این کمیت بهطور مستقیم به چگالی وابسته است و از رابطه زیر بهدست میآید:
در این رابطه که در آن g شتاب گرانش است. واحد وزن مخصوص، نیوتن بر متر مکعب یا پوند بر فوت مکعب است. مقدار شتاب گرانش در شرایط معمول زمین برابر است با:
برای مثال، وزن مخصوص هوا و آب در دمای ۲۰ درجه سلسیوس و فشار یک اتمسفر به صورت زیر است:
هوا:
آب:
وزن مخصوص بهویژه در مسائل مربوط به فشار هیدروستاتیکی اهمیت زیادی دارد، زیرا مستقیما در محاسبه نیروی ناشی از وزن سیال وارد میشود.
چگالی نسبی
چگالی نسبی یا SG نسبت چگالی یک سیال به چگالی یک سیال مرجع است. برای مایعات، مرجع معمولا آب در دمای ۴ درجه سلسیوس و برای گازها، هوا در نظر گرفته میشود. برای مثال، چگالی نسبی جیوه به صورت زیر است.
انرژی درونی در سیالات
در ترمودینامیک، انرژی موجود در یک ماده معمولا به صورت انرژی درونی در نظر گرفته میشود که ناشی از حرکت و برهمکنش مولکولها است. اما در مکانیک سیالات، دو نوع انرژی دیگر نیز اهمیت پیدا میکنند. این دو نوع انرژی، انرژی پتانسیل که به موقعیت سیال در میدان گرانشی بستگی دارد و انرژی جنبشی که به سرعت حرکت سیال وابسته است هستند. انرژی پتانسیل برابر کاری است که برای انتقال جرم از مبدا به یک موقعیت مشخص در برابر گرانش لازم است. انرژی جنبشی نیز برابر کاری است که برای رساندن جسم از حالت سکون به سرعت V نیاز است.
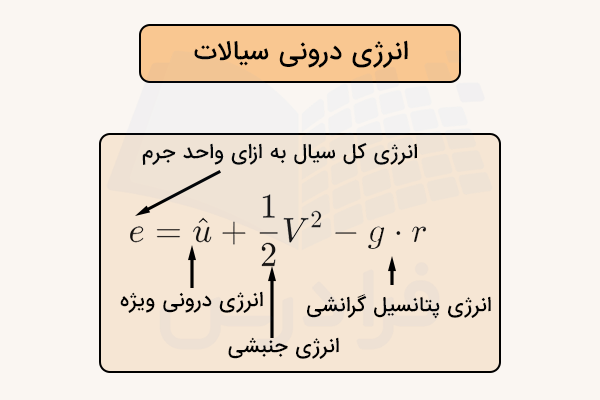
در نتیجه، انرژی درونی کل سیال به ازای واحد جرم به صورت زیر بیان میشود:
در این رابطه، کمیت نشاندهنده انرژی کل سیال به ازای واحد جرم است، انرژی درونی ویژه و بیانگر انرژی ذخیرهشده درون سیال است، سرعت سیال است که جمله انرژی جنبشی به ازای واحد جرم را نشان میدهد، شتاب گرانش است و ارتفاع یا فاصله از مرجع بوده که جمله انرژی پتانسیل گرانشی به ازای واحد جرم را بیان میکند.
اگر محور z را رو به بالا در نظر بگیریم، رابطه سادهتر میشود و به شکل زیر درمیآید:
در این رابطه، انرژی درونی تابعی از دما و فشار است، در حالی که انرژیهای جنبشی و پتانسیل به حرکت و موقعیت وابستهاند.
انرژی درونی گازها
در گازهای کامل، انرژی درونی تنها به دما وابسته است. این رابطه به شکل زیر نمایش داده میشود.
در نتیجه، گرمای ویژه در حجم ثابت نیز تابعی از دما خواهد بود. این رابطه به شکل زیر نوشته میشود.
این رابطه نشان میدهد که تغییرات انرژی درونی مستقیما با تغییرات دما مرتبط است و این موضوع در تحلیلهای حرارتی اهمیت زیادی دارد.
روابط حالت سیالات
خواص ترمودینامیکی یک سیال به یکدیگر وابستهاند و این وابستگیها از طریق توابع حالت بیان میشوند. این روابط برای هر ماده متفاوت هستند. در ادامه این روابط را برای گازها و مایعات بررسی میکنیم.
روابط حالت گازها
هوا مخلوطی از گازهاست، اما در بازه دمایی معمول میتوان آن را بهصورت یک ماده خالص در نظر گرفت. بیشتر گازهای معمول مانند هوا، اکسیژن و نیتروژن در شرایط عادی رفتار نزدیک به گاز ایدهآل دارند. اما برخی سیالات مانند بخار آب، بهویژه در شرایط نزدیک به نقطه بحرانی، از این مدل پیروی نمیکنند. در دماهای بالا و فشارهای پایین، بسیاری از گازها از قانون گاز کامل پیروی میکنند. این رابطه برای سیالات در دمای بالا و فشار پایین به شکل زیر نوشته میشود.
در این رابطه، R ثابت گاز است و از رابطه زیر بهدست میآید:
همچنین میتوان آن را از ثابت جهانی گازها و جرم مولی بهدست آورد:
روابط حالت برای مایعات
برخلاف گازها، برای مایعات یک رابطه ساده و عمومی مانند قانون گاز کامل وجود ندارد. دلیل این موضوع رفتار متفاوت مایعات است، زیرا آنها تقریبا تراکمناپذیر هستند و تغییرات حجم آنها در اثر فشار بسیار ناچیز است. به همین دلیل، تحلیل مایعات معمولا با فرضهای سادهتری انجام میشود.
در بسیاری از مسائل مهندسی، میتوان مایعات را با تقریبهای زیر توصیف کرد:
این روابط نشان میدهند که چگالی مایعات تقریبا ثابت است و گرماهای ویژه آنها نیز تغییر چندانی نمیکند. به همین دلیل، تحلیل جریان مایعات نسبت به گازها سادهتر است.
آنتالپی در سیالات
در گازهای کامل، همانطور که انرژی درونی فقط به دما وابسته است، آنتالپی نیز تنها تابعی از دما خواهد بود. آنتالپی از رابطه زیر تعریف میشود.
در این رابطه، کمیت نشاندهنده آنتالپی ویژه است، انرژی درونی ویژه است، فشار سیال را نشان میدهد، چگالی سیال است، ثابت گاز ویژه است و دمای مطلق را بیان میکند. همچنین گرمای ویژه در فشار ثابت نیز فقط به دما وابسته است. این روابط در ادامه نوشته شدهاند.
کمیت گرمای ویژه در فشار ثابت است، آنتالپی ویژه است، دمای مطلق است و نماد نشان میدهد که مشتقگیری در فشار ثابت انجام میشود. همچنین، کمیت تغییرات آنتالپی ویژه را نشان میدهد، گرمای ویژه در فشار ثابت بهعنوان تابعی از دما است و تغییرات دما را بیان میکند.
این روابط نشان میدهند که در گازهای ایدهآل، تغییرات انرژی حرارتی بهطور مستقیم با دما مرتبط است و وابستگی به فشار یا حجم بهصورت غیرمستقیم از طریق دما بیان میشود. پیشنهاد میکنیم برای درک بهتر این کمیت در سیالات و ترمودینامیک، مطلب بررسی تغییرات آنتالپی در ترمودینامیک مجله فرادرس را مطالعه کنید.
آنتروپی در سیالات
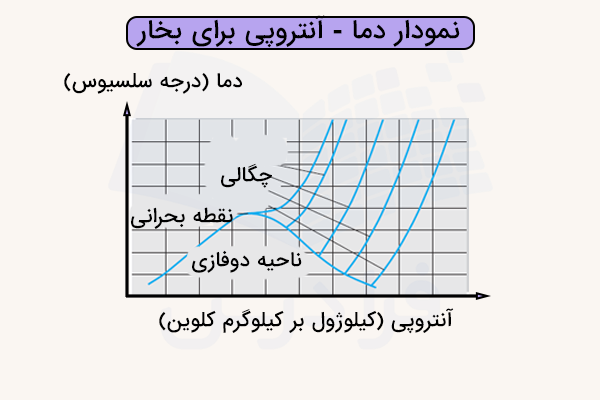
در نمودار دما - آنتروپی، محور عمودی نشاندهنده دما و محور افقی نشاندهنده آنتروپی ویژه است و با افزایش معمولا سیستم گرما دریافت میکند و مقدار سطح این تغییر را مشخص میکند. در نواحی تکفاز مانند بخار فوقداغ، افزایش با افزایش همراه است و رابطهای مستقیم دارند، اما در ناحیه دوفازی، آنتروپی تغییر میکند در حالیکه دما تقریبا ثابت میماند که بیانگر تغییر فاز است و در نزدیکی نقطه بحرانی نیز رفتار این دو کمیت پیچیدهتر و غیرخطیتر میشود.
این نمودار در تصویر زیر نمایش داده شده است.
ضریب گرانروی سیالات
گرانروی یکی از مهمترین خواص انتقالی سیالات است که نشاندهنده مقاومت سیال در برابر تغییر شکل و جاری شدن است. این خاصیت در واقع ناشی از اصطکاک داخلی بین لایههای مختلف سیال است. در یک سیال نیوتنی، تنش برشی متناسب با نرخ تغییر سرعت است. رابطه تنش برشی و ضریب گرانروی سیال به شکل زیر تعریف میشود.
در این رباطه تنش برشی، ضریب گرانروی و گرادیان سرعت سیال است. هرچه مقدار بیشتری داشته باشد، سیال غلظت بیشتری داشته و سختتر جاری میشود. در مقابل، سیالاتی با گرانروی کم (مثل هوا یا آب) راحتتر حرکت میکنند.
اگر یک لایه سیال را در نظر بگیریم که تحت یک تنش برشی قرار دارد، این تنش باعث میشود لایهها نسبت به هم جابهجا شوند.
گرانروی سینماتیکی
یک کمیت مهم دیگر، گرانروی سینماتیکی است که از رابطه زیر بهدست میآید.
این رابطه با استفاده از عدد رینولدز به دست میآید. پارامتر اصلی که رفتار لزج تمام سیالات نیوتنی را به هم مرتبط میکند، عدد بدون بعد رینولدز است.
رابطه گرانروی و خواص ترمودینامیکی سیال
گرانروی سیالات به شدت به دما وابسته است. در مایعات، با افزایش دما گرانروی کاهش یافته و با کاهش دما افزایش مییابد. همچنین، در گازها با افزایش دما، گرانروی افزایش یافته و با کاهش دما کاهش مییابد. ضریب گرانروی نقش بسیار مهمی در تشکیل لایه مرزی، افت فشار در لولهها و جریانهای آرام و آشفته دارد.
رسانندگی گرمایی سیالات
رسانندگی گرمایی نشاندهنده توانایی سیال در انتقال گرما از طریق هدایت است. این خاصیت مشخص میکند که انرژی حرارتی با چه سرعتی در داخل سیال منتشر میشود. قانون اصلی حاکم بر هدایت گرما، قانون فوریه است. این قانون به شکل زیر تعریف میشود.
در این رابطه، q شار حرارتی، k ضریب رسانندگی گرمایی و گرادیان دما است. علامت منفی در این رابطه مشخص میکند که گرما همواره از ناحیه با دمای بالاتر به ناحیه با دمای پایینتر منتقل میشود.
رسانندگی گرمایی حالات ماده
رسانندگی گرمایی با توحه به حالت ماده و ساختار شیمیایی ماده میتواند متفاوت باشد. برای مثال، فلزات رسانندگی گرمایی بالا، مایعات رسانندگی گرمایی متوسط و گازها رسانندگی گرمایی پایینی دارند. در سيالات رسانندگی گرمایی معمولا نسبت به جامدات کمتر است اما این خاصیت در حضور جریان و جابجایی سیال میتواند افزایش یافته و تقویت شود.
جمعبندی
در این مطلب از مجله فرادرس، خواص ترمودینامیکی سیالات و نقش آنها در توصیف وضعیت و رفتار سیال را بررسی کردیم. فشار، دما و چگالی بهعنوان کمیتهای پایه، بیانگر حالت لحظهای سیال و اساس تحلیلهای مکانیک سیالات هستند و تغییرات آنها تصویر دقیقی از رفتار جریان ارائه میدهد.
همچنین، انرژی درونی، آنتالپی، آنتروپی و گرمای ویژه بهعنوان خواص مرتبط با انرژی و فرایندهای ترمودینامیکی مطرح میشوند که نقش مهمی در تحلیل انتقال و تبدیل انرژی در سیال دارند. روابط حالت نیز بهعنوان ارتباطدهنده میان این خواص، امکان توصیف منسجم و یکپارچه رفتار سیال را در شرایط مختلف فراهم میکنند.












