پوزیترون چیست؟ – توضیح و تعریف به زبان ساده
«پوزیترون» (Positron) از نظر بار و جرم دقیقا مشابه الکترون است، فقط علامت بار پوزیترون برخلاف الکترون مثبت است. به همین علت، پوزیترون را پادذره الکترون مینامند. میدانیم تمام مواد اطراف ما از اتمها ساخته شدهاند. ساختار اتم دارای دو بخش مهم به نام هسته و ابر الکترونی دور آن است. اگر وارد دنیای «زیراتمی» (Subatomic) و عجیب هسته شویم، با ذراتی به نام پوزیترون آشنا میشویم. در این مطلب از مجله فرادرس با تمرکز روی فرآیندهای مختلف درون هسته، ابتدا یاد میگیریم که پوزیترون چیست.
- با ویژگیهای ذره پوزیترون مانند نماد، بار و جرم آن آشنا میشوید.
- میآموزید پوزیترون چگونه از طریق واپاشی بتای مثبت در هسته ایجاد میشود.
- فرآیندهای تولید پوزیترون مانند تولید زوج و واپاشی میون را میآموزید.
- میآموزید فرآیندهای واپاشی هستهای و سه نوع ذره پرتوزا کداماند.
- کاربرد پوزیترون در تصویربرداری پزشکی (PET) را یاد میگیرید.
- با تاریخچه کشف این ذره بنیادی آشنا میشوید.


سپس با توضیح انواع فرآیندهای «واپاشی» (Decay)، به بیان ویژگیهای پوزیترون، نحوه تولید این ذره، کاربرد آن در پزشکی و تفاوتهای این ذره با ذراتی مانند ذرات «آلفا» (Alpha)، ذرات «بتا» (Beta)، پرتوهای «گاما» (Gamma)، الکترون، پروتون و نوترون خواهیم پرداخت.
پوزیترون چیست؟
پوزیترون یک ذره زیراتمی با بار مثبت است که دارای جرم، اسپین، اندازه و مقدار باری برابر با جرم، اسپین، اندازه و مقدار بار الکترون است. بنابراین پوزیترون پادذره الکترون است. تابش پوزیترون در فرآیندی به نام واپاشی بتای مثبت از یک هسته ناپایدار یا رادیواکتیو اتفاق میافتد. روشهای دیگر تولید پوزیترون، فرآیند «تولید زوج» (Pair Production) و واپاشی «ميون» (Muon) است. همچنین پوزیترون میتواند در فرآیندی به نام «نابودی» (Annihilation)، بهسرعت با الکترون واکنش دهد و پرتوهای گاما را تولید کند.
در بیشتر اتمها، تعداد نوترونهای هسته از تعداد پروتونها بیشتر است. این مسئله باعث میشود چنین هستهای ناپایدار باشد و از طریق یک واپاشی رادیواکتیو یا پرتوزا تجزیه شود. در این فرآیند، ذراتی از هسته گسیل میشوند و هسته اولیه با تبدیل به یک هسته جدید به پایداری نسبی خواهد رسید. ذراتی که در این واپاشیها گسیل میشوند عبارتاند از ذرات آلفا، ذرات بتا، پوزیترون و پرتوهای گاما. در بخشهای بعدی این فرآیندها را توضیح خواهیم داد و یاد میگیریم پوزیترون چه تفاوتی با این ذرات دارد و در چه شرایطی گسیل میشود.

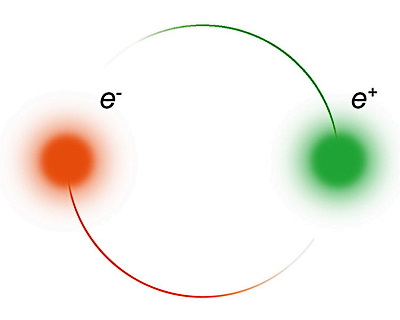
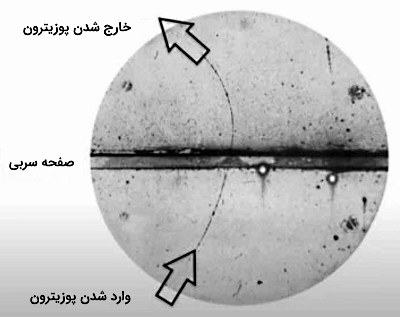
همانطور که گفتیم، پوزیترون، پادذره الکترون یا پادالکترون است. اگر با مفهوم تقارن در طبیعت آشنا باشید، تقارن به این معنا است که برای هر ذرهای، یک پادذره در طبیعت وجود دارد. تصویر بالا این مفهوم را بهخوبی نمایش داده است. در این تصویر در کنار ردپای الکترون، ردپای ذره سبک دیگری کاملا شبیه به الکترون مشاهده میشود که در جهتی متناظر با یک بار مثبت منحرف شده است. این ذره پوزیترون است که مسیر آن با رنگ متفاوتی نشان داده شده است. پادالکترون بودن پوزیترون، در این تصویر برای اولین بار مشاهده شد.
نماد پوزیترون
از آنجا که پوزیترون همان الکترون مثبت یا پادالکترون است، با نماد e+ نمایش داده میشود. از طرفی با توجه به اینکه پوزیترون از واکنشهای واپاشی بتای مثبت گسیل میشود، به شکل یعنی بتای مثبت نیز نشان داده میشود.
بار پوزیترون
همانطور که گفتیم بار پوزیترون از نظر علامت مثبت است، در حالی که علامت بار الکترون منفی است. ولی از نظر اندازه، بار پوزیترون کاملا با اندازه بار الکترون یعنی ۱e برابر است. میدانیم e نماد بار یک الکترون است که برابر است با که در آن C نماد کولن واحد بار الکتریکی است. پس اندازه بار پوزیترون هم برابر است با .
جرم پوزیترون
اگر بخواهیم بدانیم جرم پوزیترون چیست، برمیگردیم به شباهت آن با الکترون. جرم پوزیترون با جرم الکترون یعنی کاملا برابر است. میدانیم kg واحد استاندارد جرم در سیستم SI است. البته در مباحث مربوط به هسته، معمولا جرم برحسب واحدی به نام «یکای جرم اتمی» (Atomic Mass Unit) یا amu بیان میشود که در بخشهای بعدی از این واحد نیز استفاده کردهایم.
یادگیری پوزیترون با فرادرس برای دانشآموزان
در بخش قبل، تا حدودی متوجه شدیم پوزیترون چیست و چه تفاوتی با الکترون دارد. اگر دانشآموز هستید و به یادگیری مباحث مربوط به اتم و هسته علاقهمندید، پیشنهاد میکنیم این فیلمهای آموزشی تهیه شده در فرادرس را بهترتیب مشاهده کنید:
- فیلم آموزش علوم تجربی هشتم بخش شیمی فرادرس
- فیلم آموزش شیمی پایه دهم فرادرس
- فیلم آموزش شیمی دهم حل سوالات امتحانات نهایی فرادرس
- فیلم آموزش فیزیک پایه دوازدهم فرادرس
- فیلم آموزش فیزیک دوازدهم مرور و حل تمرین فرادرس
- فیلم آموزش فیزیک دوازدهم نکته و حل تست کنکور فرادرس
هسته چیست؟
برای اینکه یاد بگیریم پوزیترون چیست، پیش از هر چیز باید به هسته اتم مراجعه کنیم و آن را خوب بشناسیم، چون همه چیز از هسته شروع میشود. هسته یک اتم شامل دو ذره به نام پروتون (p) و نوترون(n) است. پروتون دارای بار مثبت است، در حالی که نوترون ذرهای بدون بار یا خنثی است. چنانچه دانش آموز هستید و قصد دارید مباحث مربوط به اتم و هسته آن را از پایه یاد بگیرید، بهتر است با مشاهده فیلم آموزشی علوم تجربی پایه هشتم بخش شیمی فرادرس که لینک آن در ادامه قرار داده شده است یادگیری خود را آغاز کنید:
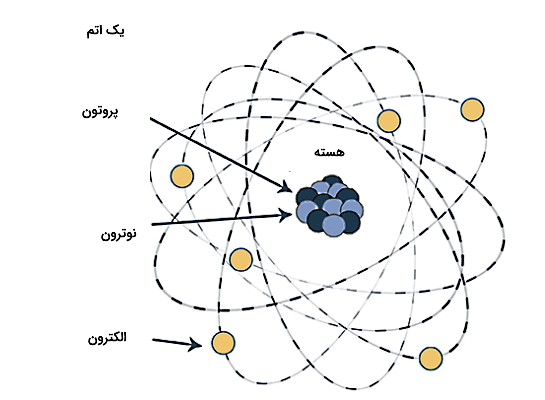
همچنین به هر ذره درون هسته اتم، فرقی ندارد پروتون یا نوترون، نوکلئون هم گفته میشود. اگر تمایل دارید در مورد ذرهای به نام نوکلئون اطلاعات بیشتری بهدست آورید، میتوانید مطلب «نوکلئون چیست؟ – به زبان ساده» از مجله فرادرس را مطالعه کنید. با اینکه اتم در مقایسه با هسته خیلی بزرگتر است، اما بیشتر جرم اتم در هسته آن قرار دارد. بهعبارت دیگر، هسته اتم بخش سنگین اما بسیار کوچکی در مرکز اتم را اشغال کرده است.
عدد اتمی و عدد جرمی چیست؟
یکی از پارامترهایی که ویژگیهای یک اتم را بهخوبی به ما معرفی میکند، «عدد اتمی» (Atomic Number) آن است. عدد اتمی یک عنصر که با Z نشان داده میشود، برابر است با تعداد پروتونهای هسته اتم و بهصورت یک زیرنویس قبل از نماد شیمیایی عنصر نمایش داده میشود. برای مثال، عدد اتمی عنصر «اورانیوم» (Uranium) که برابر با ۹۲ است و نماد شیمیایی آن (U) به شکل زیر نوشته میشوند:
پارامتر مهم بعدی «عدد جرمی» (Mass Number) یک عنصر است که با A نشان داده میشود. عدد جرمی اتم برابر است با مجموع تعداد پروتونها و نوترونهای هسته اتم. تعریف عدد جرمی بهصورت تعداد نوکلئونهای هسته اتم نیز معادل است. عدد جرمی را با یک بالانویس قبل از نماد شیمیایی عنصر نشان میدهند. برای مثال، عدد جرمی عنصر اورانیوم ۲۳۸ است و کنار نماد شیمیایی و عدد اتمی آن به صورت زیر نوشته میشود:
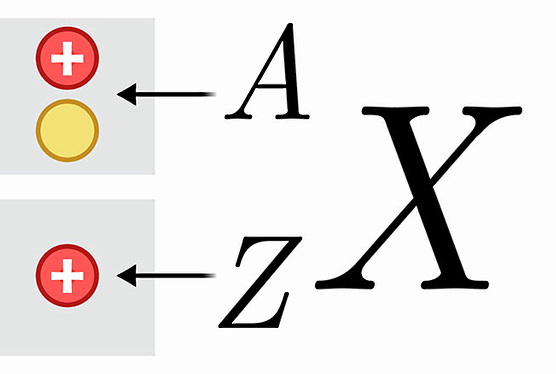
برای اینکه بتوانیم فرآیندهای واپاشی هستهای را در قالب معادلات استانداردی نشان دهیم، نیازمند استفاده از قواعد خاصی هستیم. دو طرف یک معادله هستهای مانند هر معادله شیمیایی دیگری باید در تعادل باشند. این تعادل در یک معادله هستهای به این صورت است که باید مجموع عددهای جرمی و عددهای اتمی دو طرف معادله با هم برابر باشند.
نیروی هستهای چیست؟
در ادامه برای اینکه بهتر متوجه شویم پوزیترون چیست، در این بخش مفاهیم مهم فیزیک هستهای را توضیح میدهیم. اگر توجه خود را روی هسته اتم متمرکز کنیم، احتمالا این سوال پیش میآید که اگر هسته حاوی ذراتی با بار مثبت (p) و ذراتی بدون بار (n) است، چطور از هم نمیپاشد؟ از فیزیک الکتریسیته و قانون کولن، میدانیم ذراتی با بار همنام یکدیگر را دفع میکنند. پس پروتونهای داخل هسته باید با توجه به علامت بار و فاصله خیلی نزدیکی که نسبت به هم دارند، نیروی دافعه خیلی بالایی به هم وارد کنند.
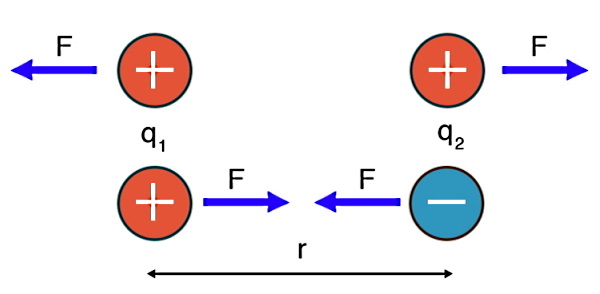
از طرفی اگر چنین چیزی واقعا اتفاق بیفتد، تمام هستههای اتمهای مواد اطراف ما باید از هم بپاشند و اساسا چیزی به نام ماده نخواهیم داشت. پس چه چیزی مانع از هم پاشیدن هسته میشود؟ پاسخ این سوال نیروی هستهای است. نیروی هستهای نوعی نیروی جاذبه بین نوکلئونهای درون هسته است که با نیروی دافعه الکتروستاتیکی بین پروتونها مقابله میکند و باعث میشود هسته پایدار بماند.
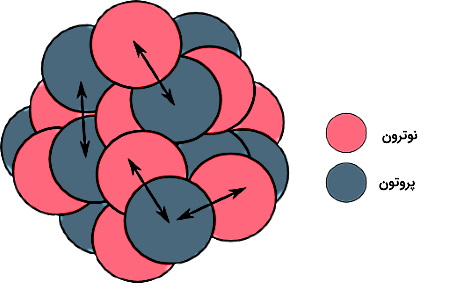
نیروی هستهای کوتاهبرد است، یعنی در فواصل خیلی خیلی کوتاهی مانند ابعاد هسته اتم عمل میکند. همچنین مقدار نیروی هستهای بین یک پروتون و یک نوترون با مقدار نیروی بین دو پروتون یا دو نوترون یکسان است. بهعبارت دیگر، اندازه این نیرو از بار نوکلئون و اینکه پروتون است یا نوترون، مستقل است.
رادیواکتیویته یا پرتوزایی چیست؟
تا اینجا توضیح دادیم که پوزیترون چیست و برای پایداری هسته لازم است نیروی الکتروستاتیکی بین پرتونها با نیروی هستهای بین نوکلئونها در تعادل باشد. اگر تعداد پروتونهای داخل هسته زیاد شود، برای پایدار ماندن هسته لازم است هسته تعداد نوترونهای خود را افزایش دهد. چنین هستههایی معمولا ناپایدار هستند.
در اینجا یکی دیگر از مفاهیم مهم فیزیک هستهای مطرح میشود که «پرتوزایی» (Radioactivity) نام دارد و اولین بار توسط دانشمند فرانسوی به نام «هانری بکرل» (Henri Becquerel) در سال ۱۸۹۶ کشف شد. مطالعات آقای بکرل به همراه سایر دانشمندان از جمله «ماری کوری» (Marie Curie) و «پیر کوری» (Pierre Curie) نشان داد که هسته ناپایدار برخی از عناصر بهصورت کاملا خودبهخودی به یک هسته جدید تبدیل میشود و ذرات جدیدی نیز در این فرآیند تولید میشوند.

هسته اولیه ناپایدار را «هسته مادر» و هسته ثانویه که طی این فرآیند تولید شده و نسبتا پایدارتر است را «هسته دختر» مینامند. این دانشمندان متوجه شدند که بعضی از ذرات تولید شده در این فرآیند، دارای بار مثبت یا منفی بودند. اما برخی دیگر با اینکه انرژی خیلی بالایی هم نشان دادند، اما بهنظر میرسید بدون بار یا خنثی باشند.
به این ترتیب این ذرات در سه گروه ذرات آلفا، ذرات بتا و پرتوهای گاما طبقهبندی شدند. خصوصیات این سه گروه از ذرات، در جدول زیر بهصورت خلاصه جهت مقایسه بهتر آورده شده است:
| نام ذره نماد | جرم (amu) - انرژی - بار (e: بار الکترون) | نماد |
| ذره آلفا یا هسته هلیوم (Z=2 و A=4) | نسبتا سنگین (4 amu) - پایین - 2e+ | یا |
| ذره بتا یا الکترون (Z=-1 و A=0) | سبک (0.0005 amu) - بالا - 1e- | یا |
| پرتو گاما یا تابش الکترومغناطیس (Z=0 و A=0) | خیلی خیلی سبک - خیلی بالا - خنثی |
یکی دیگر از مشاهدات تعجببرانگیز و جالب در مورد عناصر رادیواکتیو یا پرتوزا این بود که با گسیل ذرات توسط این عناصر، ماهیت آنها نیز به آهستگی تغییر میکند. برای مثال زمانی که طبق شکل زیر یک هسته رادیواکتیو یک ذره آلفا را گسیل میکند، انرژیای حدود ۴ amu که معادل دو پروتون است، از دست میدهد.
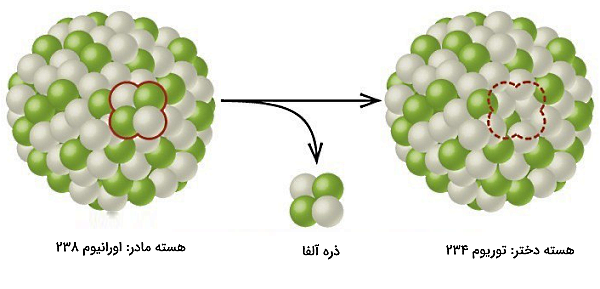
از طرفی میدانیم که تعداد پروتونهای هسته در یک اتم نشاندهنده مشخصه و خواص یک عنصر است، بنابراین عدد اتمی این عنصر با از دست دادن دو پروتون کاهش یافته است. به عبارتی، عدد اتمی یک عنصر رادیواکتیو با از دست دادن یک ذره آلفا دو واحد کم خواهد شد. بنابراین یک عنصر رادیواکتیو مثل اورانیوم () با از دست دادن یک ذره آلفا، به عنصر جدیدی به نام توریوم () تبدیل خواهد شد.
در مورد ایجاد یک ذره بتا یا همان الکترون از یک هسته رادیواکتیو، در واقع باید تجزیه یک نوترون اتفاق بیفتد. فرض کنید در مقیاس خیلی خیلی کوچک، یک نوترون شامل یک پروتون با بار مثبت است که به الکترونی با بار منفی وابسته است. با واپاشی نوترون و گسیل یک ذره بتا، یک پروتون تازه تشکیل میشود که خصوصیات عنصر موردنظر را عوض خواهد کرد.
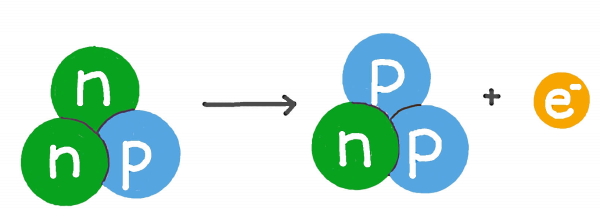
در حال حاضر با اینکه میدانیم «واپاشی هستهای« (Radioactive Decay) یک فرآیند کاملا پیچیده است، اما همچنان اصول و الگوهایی که حدود ۱۰۰ سال پیش برای این فرآیند بنا نهاده شدند، برقراراند. مثلا هنوز سه گروه ذرهای که طی یک فرآیند واپاشی هستهای تولید میشوند، ذرات آلفا یا بتا یا پرتوهای گاما هستند. بر همین اساس، سه نوع واپاشی هستهای مهم به نام واپاشی آلفا، واپاشی بتا و واپاشی گاما داریم که در بخشهای بعدی آنها را کامل توضیح خواهیم داد.
نیمه عمر چیست؟
یک خاصیت مهم عناصر رادیواکتیو، «نیمهعمر یا نیمعمر» (Half-Life) آنها است. گسیل ذرات رادیواکتیو از عناصری مانند ، با یک نرخ ثابت و مشخص برای هر عنصر انجام میشود. نرخ واپاشی یک عنصر رادیواکتیو، با اندازهگیری نیمهعمر آن مشخص میشود. نیمهعمر برابر است با مدت زمانی که طول میکشد تا نصف اتمهای رادیواکتیو واپاشی کنند و با تابش یک ذره، عنصر جدیدی تشکیل شود. نیمهعمر عناصر مختلف گستره متفاوتی دارد، از بیلیون سال تا چند میکروثانیه.
سازوکار نیمهعمر به این صورت است: فرض کنید طبق شکل زیر ۱ gr از یک عنصر رادیواکتیو را در ابتدا در اختیار داریم. با گذشت یک نیمهعمر، ۰٫۵ gr از آن باقی میماند. پس از دو نیمهعمر، نصف ۰٫۵ grاز عنصر واپاشی شده است و تنها ۰٫۲۵ gr از عنصر باقی مانده است. پس از سه نیمهعمر، ۰٫۱۲۵ gr باقی خواهد ماند و به همین ترتیب مقدار عنصر اولیه کمتر میشود.
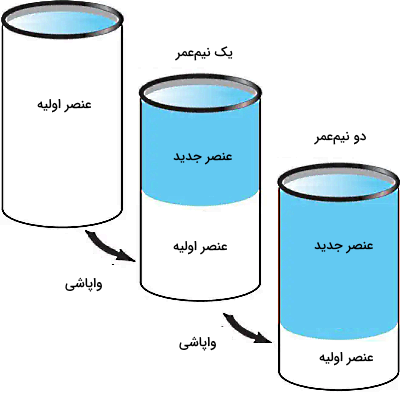
این توضیحات را میتوانیم در قالب یک فرمول ارائه کنیم:
در این فرمول I نشاندهنده جرم اولیه عنصر رادیواکتیو و R بیانگر جرم باقی مانده از این عنصر است.
واپاشی یا تابش هسته
در بخش قبل آموختیم که پوزیترون چیست و گفتیم ذرات آلفا، بتا و پروتوهای گاما در فرآیندهای واپاشی هسته تولید میشوند. در این بخش میخواهیم انواع فرآیندهای واپاشی را بررسی کنیم. سه واپاشی مهم شامل تابش آلفا، تابش بتای منفی و تابش گاما هستند که در ادامه توضیح داده میشوند.
واپاشی آلفا (تابش آلفا)
واپاشی هستهای که در آن یک هسته سنگین با تابش ذره آلفا به عنصر جدید دیگری تبدیل شود، واپاشی آلفا یا تابش آلفا نام دارد. اگر هسته مادر را با نماد کلی نشان دهیم، هسته دختر و ذره آلفا در سمت دیگر معادله واپاشی به شکل زیر خواهند بود:
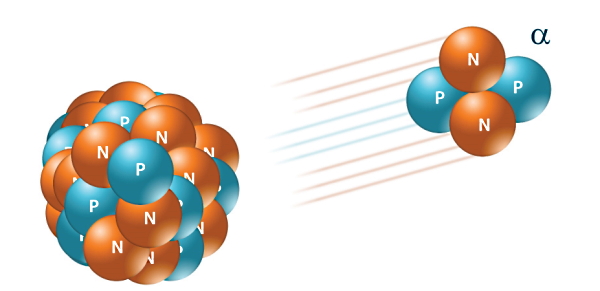
همانطور که از معادله مشخص است، هسته دختر با نماد کاملا متفاوتی از X یعنی با Y نمایش داده شده است، چون این هسته مربوط به عنصر دیگری است و مشخصه هسته مادر را دیگر ندارد. تعییرات عدد جرمی و عدد اتمی کاملا بیانگر تغییرات هسته مادر است.
برای مثال اگر بخواهیم از دست دادن یک ذره آلفا در را در قالب یک معادله هستهای نشان دهیم، باید اورانیوم را در سمت واکنشدهنده معادله (سمت چپ) بهعنوان هسته مادر و ذره آلفا و «توریوم» (Thorium) تولید شده را در بخش محصول تولید شده در فرآیند (سمت راست) قرار دهیم:
دقت شود چون ذره آلفا معادل هسته اتم «هلیوم» (Helium) است، با در معادلات هستهای نشان داده میشود. همچنین نماد شیمیایی عنصر هلیوم He و نماد شیمیایی عنصر توریم Th است. در معادله بالا با اورانیوم ۲۳۸ شروع کردیم، بنابراین در سمت محصولات تولید شده واپاشی لازم است مجموع جرم برابر شود با چهار واحد جرم برای ذره آلفا از دست داده شده و توریوم ۲۳۴.
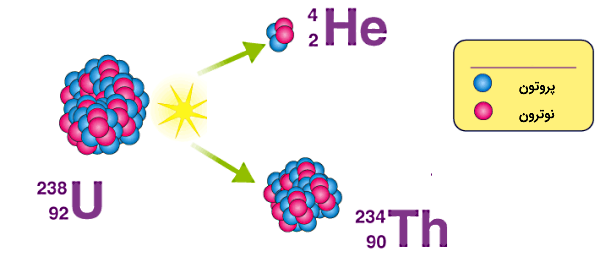
نکته دیگری که این واکنش واپاشی بیان میکند این است که عنصر اورانیوم با از دست دادن دو پروتون، به عنصر جدیدی به نام توریوم تبدیل شده است. همچنین در معادله بالا میتوانیم به جای استفاده از نماد اتمی هلیوم برای ذره آلفا، از نماد نیز استفاده کنیم.
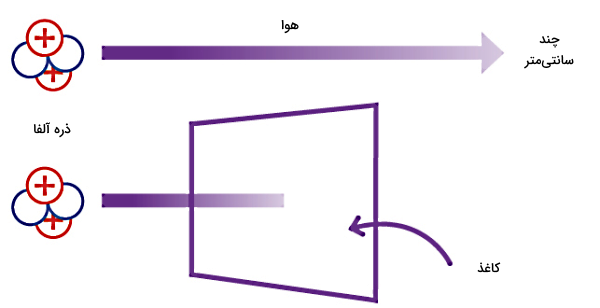
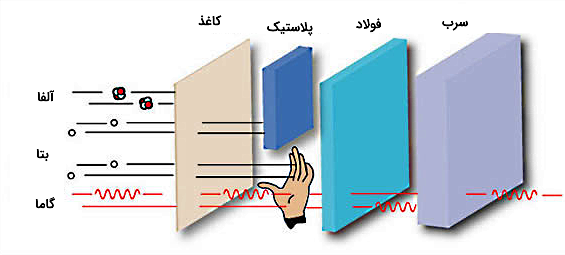
همانطور که در تصویر بالا مشخص است، تابش آلفا حدود چند سانتیمتر میتواند در هوا با سرعت کمی حرکت کند و در نهایت توسط یک تکه کاغذ، قابل متوقف شدن است. بنابراین این ذرات خیلی راحت جذب میشوند، عبور کمی دارند و کوتاهبرداند. همچنین تابش آلفا بهعنوان یک یونیزه کننده (Ionizing) گزینه خوبی محسوب میشود. چون ابعاد این ذره به گونهای است که تمایل دارد با ذرات دیگر برخورد کند. در نتیجه ذره آلفا میتواند با جداسازی الکترون از ساختار اتم، آن را به یون تبدیل کند.
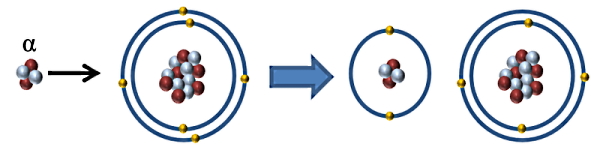
علت دیگری که باعث میشود ذرات آلفا یونیزه کنندهای قوی باشند، این است که بار این ذرات ۲+ است. پس دوست دارند الکترون جذب کنند. در شکل بالا یک ذره آلفا در برخورد با یک اتم خنثی، دو الکترون از اتم جدا کرده است. بنابراین اتم به یک یون دو بار مثبت تبدیل شده است.
واپاشی بتا (تابش بتا)
مهمترین مبحثی که در فهم پوزیترون چیست به ما کمک میکند، واپاشی بتا است. واپاشی یا تابش بتا، در واقع به تولید ذره بتای منفی اشاره دارد. در بخشهای بعد خواهیم دید که تابش پوزیترون همان تابش بتای مثبت است. پس لازم است تفاوت این دو نوع تابش در این دو بخش را خوب متوجه شویم. واپاشی بتا اولین واکنش پرتوزایی بود که توسط بکرل مشاهده شد. این نوع واپاشی در هستههای زیادی اتفاق میافتد و بسیار متداول است.
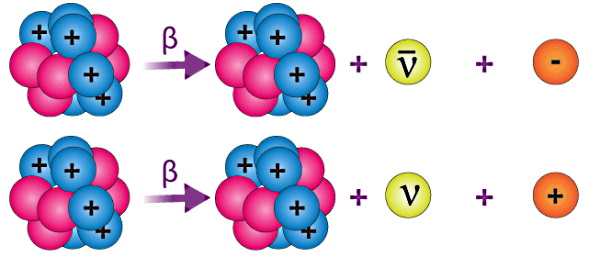
اگر در هسته عنصری نوترون زیاد وجود داشته باشد، یکی از این نوترونها میتواند به یک پروتون و یک الکترون تبدیل شود. مرسوم است گفته شود در چنین واکنشی یک ضدنوترون تولید شده است. بنابراین الکترونی که در این واپاشی تولید میشود، از الکترونهای دور هسته اتم نیست، بلکه از تجزیه نوترون حاصل شده است. با در نظر گرفتن هسته مادر بهصورت و هسته دختر بهصورت ، واپاشی بتای منفی رابطه کلی زیر را دارد:
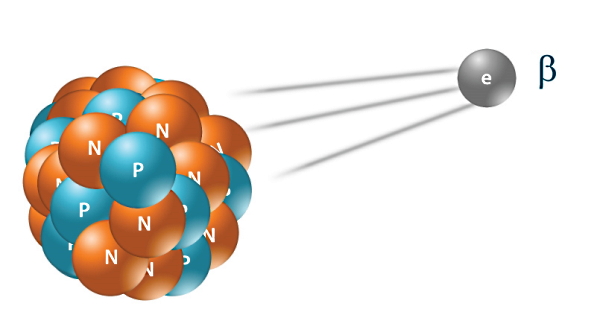
بنابراین با تجزیه نوترون، الکترون تولید شده با سرعت بالایی از هسته خارج میشود ولی پروتون در هسته باقی میماند. این الکترون، ذره بتای منفی نامیده میشود. معادله هستهای که تجزیه نوترون را بیان میکند، بهصورت زیر است:
- نوترون:
- پروتون:
- ذره بتا که در اینجا همان الکترون تولید شده است:
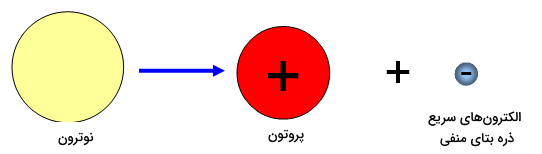
گفتیم که باید در معادلات هستهای تعادل دو طرف معادله برقرار باشد. بنابراین لازم است عدد اتمی ذره بتا ۱- باشد تا مجموع دو عدد اتمی در سمت راست معادله با عدد اتمی در سمت چپ یعنی صفر برابر شود. دقت شود با اینکه نوترون میتواند به یک پروتون و یک الکترون تجزیه شود، اما در حقیقت پروتونی داخل خود ندارد و عدد اتمی آن صفر است. عدد جرمی ذره بتا هم باید صفر باشد تا تعادل معادله از این نظر نیز درست باشد.
پس زمانی که یک هسته ذره بتا از دست میدهد، تعداد نوترونهای آن یکی کمتر خواهد شد، در حالی که عدد جرمی آن تغییری نکرده است. چون این نوترون به پروتون تبدیل میشود و عدد جرمی پروتون مانند نوترون برابر با یک است. اما با تبدیل نوترون به پروتون، عدد اتمی عنصر تغییر خواهد کرد و یک واحد به آن افزوده خواهد شد. برای مثال واپاشی بتای زیر را در نظر بگیرید که در آن توریوم ۲۳۴ با از دست دادن یک ذره بتا، به پروتکتینیم ۲۳۴ تبدیل میشود:
پس در این معادله هم مشخص است که با از دست دادن یک ذره بتا یا در یک واپاشی بتا، عدد جرمی عنصر واکنشدهنده تغییری نمیکند ولی عدد اتمی آن یک واحد افزایش مییابد.
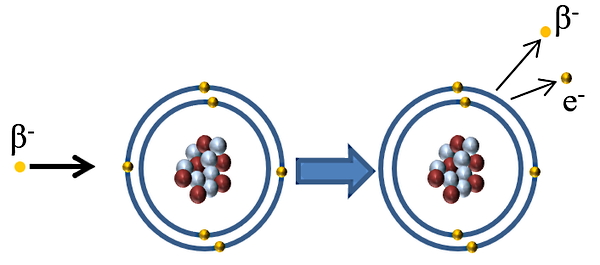
ویژگیهای تابش بتا بین ویژگیهای تابش آلفا و گاما قرار میگیرد. قدرت یونیزه کرن تابش بتا از تابش آلفا کمتر است. در واقع با برخورد یک ذره بتای منفی به یک اتم، یکی از الکترونهای لایه بیرونی اتم میتواند از اتم خارج شود. در نتیجه قابلیت یونیزه کردن اتم برای این ذره در حد ضعیفتری نسبت به ذره آلفا وجود دارد. جرم ذرات بتا خیلی خیلی کم است و با توجه به سایز کمتری که نسبت به ذرات آلفا دارند، قدرت نفوذ بیشتری در مواد دارند. تابش بتا در هوا تا چند متر میتواند حرکت کند و توسط صفحه آلومینیومی با ضخامت ۵ mm قابل متوقف شدن است.
تابش گاما
پس از اینکه یاد گرفتیم پوزیترون چیست و واپاشی ذرات آلفا و بتا به چه صورت هستند، در این بخش با واپاشی یا تابش گاما آشنا میشویم. گاهی اتم دارای انرژی اضافی است و با تابش پرتوهایی به نام پرتو گاما، این انرژی اضافی خود را از دست میدهد. معمولا تابش گاما پس از یک واپاشی آلفا یا بتا اتفاق میافتد. در واقع، هسته پس از این دو نوع واکنش در حالت برانگیخته است و با گسیل فوتونهای پرانرژی گاما به حالت پایه خود میرسد. اگر هسته برانگیخته را با علامت ستاره نشان دهیم، واپاشی بتا آن را به حالت پایه میرساند، بدون اینکه اعداد اتمی و جرمی عوض شوند:
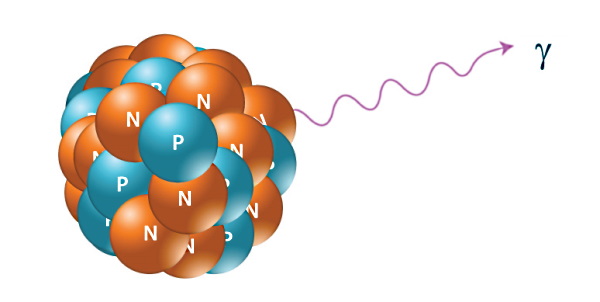
پرتوهای گاما بخشی از طیف الکترومغناطیس هستند، بنابراین دارای مشخصههایی مانند طولموج و فرکانس هستند. طولموج پروتوهای گاما خیلی کوتاه است، در نتیجه فرکانس و انرژی خیلی بالایی دارند. پس تابش گاما فقط یک فوتون انرژی است، یعنی در تابش گاما ذرهای تولید نمیشود. پس نه باری وجود دارد و نه جرمی و عدد جرمی و عدد اتمی تابش گاما هر دو صفر هستند.
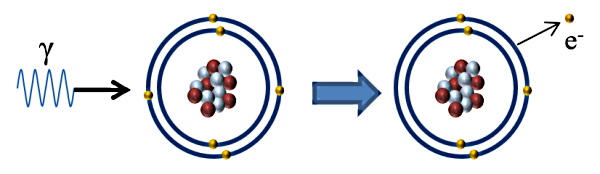
قدرت یونیزه کردن این پرتوها کم است، چون این پروتوها بیشتر تمایل دارند از درون ماده عبور کنند تا اینکه بخواهند با ذرات درون هسته برخورد یا برهمکنشی داشته باشند. اما طبق شکل بالا یونیزه کردن توسط این پروتوها به این صورت است که با جذب پرتو گاما توسط الکترون یک اتم، الکترون از اتم خارج شده است و در نتیجه اتم به یون تبدیل میشود.
پرتوهای گاما عمق نفوذ بیشتری در مواد نسبت به تابش آلفا یا بتا دارند و حرکت این پرتوها در هوا، فواصل دوربردتری را شامل میشود (حدودا بیشتر از یک کیلومتر). همچنین این پرتوها را با ضخامت کافی از موادی با عدد اتمی بالا مانند سرب یا اورانیوم حتی بهراحتی نمیتوان متوقف کرد. در شکل زیر عمق نفوذ و قدرت تابشهای آلفا، بتا و پرتوهای گاما مقایسه شده است.
تابش پوزیترون (تابش بتای مثبت)
پس از اینکه متوجه شدیم پوزیترون چیست و اساس فرآیندهای واپاشی به چه صورت است، میخواهیم بدانیم ارتباط پوزیترون با این واپاشیها چگونه است. گفتیم جرم پوزیترون همان جرم الکترون است و اندازه بار آن نیز، با اندازه بار الکترون یکسان است. تنها تفاوت این دو ذره در این است که بار پوزیترون مثبت است و بار الکترون منفی. به همین دلیل پوزیترون یک ضدالکترون یا پادالکترون است و بهعنوان مثالی از پادماده یا ضدماده برای الکترون شناخته میشود.
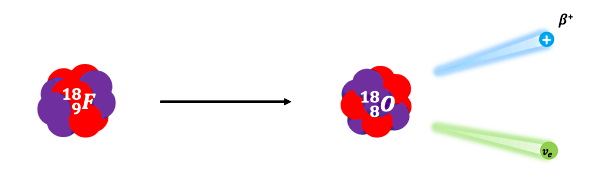
پوزیترونها زمانی تشکیل میشوند که یک پروتون بار مثبت خود را از دست دهد و به یک نوترون و پوزیترون تبدیل شود. این نوترون در هسته باقی میماند ولی پوزیترون با سرعت زیادی از هسته خارج خواهد شد. در واقع تابش پوزیترون زمانی رخ میدهد که هسته تعداد خیلی کمی نوترون داشته باشد. تابش پوزیترون شبیه تابش بتا است، با این تفاوت که تابش پوزیترون را تابش بتای مثبت مینامند. اگر هسته مادر و هسته دختر باشد، واپاشی بتای مثبت با رابطه زیر بیان میشود:
همچنین تابش پوزیترون با معادلهای به شکل زیر نیز نشان داده میشود:
- نوترون:
- پروتون:
- ذره بتا که در اینجا همان پوزیترون تولید شده است:
واقعیت این است که علاوهبر پوزیترون و نوترون، یک «نوترینو» (Neutrino) هم در این فرآیند تولید میشود و با نشان داده میشود. نوترینوها ذرات بسیار کوچک زیراتمی هستند که بهعنوان ذرات نامرئی نیز شناخته میشوند، چرا که معمولا بهندرت با چیز دیگری برهمکنش دارند. مشاهده این ذرات بسیار مشکل است، اما بهوفور در اطراف ما و حتی در بدنمان وجود دارند.
در رابطه بالا، باید تعادل دو طرف معادله از لحاظ برابری مجموع اعداد جرمی و اعداد اتمی برقرار باشد که این مسئله درست است. زمانی که یک عنصر پوزیترون میتاباند، مشخصه آن به عنصری دارای عدد اتمی یک واحد کمتر تغییر خواهد کرد. تابش پوزیترون را میتوانیم زیرمجموعهای از فرآیندهای واپاشی بتا در نظر بگیریم. اما فرق اساسی تابش پوزیترون با یک واپاشی بتا در این است که در واپاشی بتا عدد اتمی عنصر واکنشدهنده یک واحد زیاد میشود، در حالی که در تابش پوزیترون یک واحد از عدد اتمی این عنصر کم میشود. ولی در هر دو واکنش، عدد جرمی عنصر واکنشدهنده با عدد جرمی عنصر تولید شده برابر است.
برای نمونه، در واکنش زیر یک نمونه تابش پوزیترون اتفاق میافتد. در این معادله عنصر «بور» (Boron) با نماد شیمیایی B در هسته خود یک پروتون کمتر از عنصر «کربن» (Carbon) با نماد C دارد. اما جرم تغییری نمیکند، چون پروتون با یک نوترون جایگزین شده است.
تابش بتای مثبت یا پوزیترون محدوده حرکتی کمتری نسبت به تابش بتای منفی در هوا دارد. علت آن است که در اثر برخورد یک پوزیترون با هر الکترونی، نابودی زوج الکترون-پوزیترون اتفاق میافتد و پروتوهای گاما تولید میشوند. توقف تابش پوزیترون مانند تابش بتای منفی با استفاده از صفحات نازکی از فلزات امکانپذیر است.
اگر به جدول بخش «رادیواکتیویته یا پرتوزایی چیست؟» بازگردیم، بهتر است ردیف دیگری برای پوزیترون به آن اضافه کنیم تا تکمیل شود. همچنین پس از یادگیری انواع واپاشی هستهای میتوانیم تغییراتی که در هسته عناصر رادیواکتیو رخ میدهد را درجدول قرار دهیم. پس جدول بخش قبل به این صورت بازنویسی میشود:
| نام ذره | جرم (amu) - انرژی - بار (e: بار الکترون) | نماد |
| ذره آلفا
تابش آلفا عدد اتمی هسته را دو واحد و عدد جرمی آن را چهار واحد کم میکند. | نسبتا سنگین (4 amu) - پایین - 2e+ | |
| ذره بتای منفی
تابش بتا عدد اتمی هسته را یک واحد افزایش میدهد ولی عدد جرمی آن بدون تغییر باقی میماند. | سبک (0.0005 amu) - بالا - 1e- | |
| پوزیترون (Z=+1 و A=0)
تابش پوزیترون عدد اتمی هسته را یک واحد کاهش میدهد ولی عدد جرمی آن بدون تغییر باقی میماند. | سبک (0.0005 amu) - بالا - 1e+ | |
| پرتو گاما
تابش گاما عدد اتمی و عدد جرمی را تغییری نمیدهد. | خیلی خیلی سبک - خیلی بالا - خنثی |
روشهای تولید پوزیترون
فهمیدیم پوزیترون چیست، چه خصوصیاتی دارد و تابش پوزیترون چگونه است. در این بخش میخواهیم ببینیم روشهای تولید پوزیترون کداماند. پوزیترون با سه روش تولید یا گسیل میشود که عبارتاند واپاشی بتای مثبت، تولید زوج و واپاشی میونهای مثبت. در ادامه هر کدام از این سه روش را توضیح خواهیم داد.
تابش پوزیترون
تابش پوزیترون همانطور که گفتیم یک نوع فرآیند واپاشی بتای مثبت از هسته مواد رادیواکتیوی است که تعداد پروتونهای بالا (Proton-rich) و نوترونهای کمی (Neutron-deficient) دارند. در بخش قبل تابش پوزیترون را مفصل توضیح دادهایم.
تولید زوج
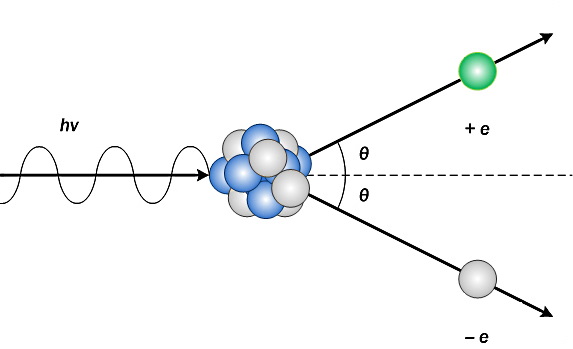
برای اینکه ببینیم پوزیترون چیست، لازم است روشهای بوجود آمدن آن را یاد بگیریم. یکی از این روشها، تولید زوج است. در این فرآیند انرژی پرتوهای گاما به یک زوج الکترون-پوزیترون تبدیل میشود. اساس تولید زوج به این صورت است که یک فوتون دارای انرژی کافی مانند پرتوهای گاما، با هسته اتم یک ماده برهمکنش میکند. در نتیجه انرژی فوتون به یک زوج الکترون-پوزیترون تبدیل میشود.
واپاشی میونها
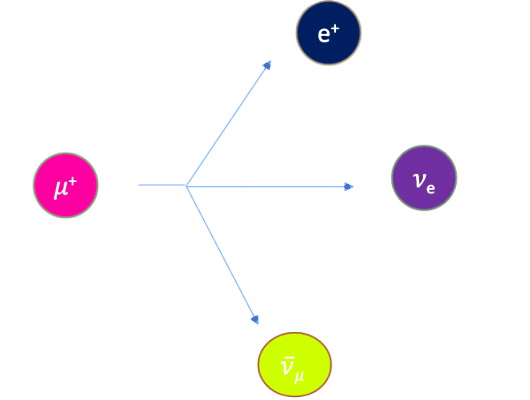
میخواهیم ببینیم روش دیگر تولید پوزیترون چیست. واپاشی ذرات خاصی با طول عمر کوتاه مانند میونها نیز پوزیترون تولید میکند. میونهای مثبت ذرات بنیادی دیگری در طبیعت هستند که با واپاشی خود به دو نوع نوترینو، پوزیترون تولید میکنند. میون با μ نشان داده میشود. در شکل زیر یک میون مثبت که در واقع آنتیمیون است، به پوزیترون و دو نوتیرینو واپاشی کرده است. واپاشی میون منفی، الکترون تولید میکند.
تفاوت پوزیترون با سایر ذرات
در بخشهای گذشته برای اینکه پاسخ مناسب برای «پوزیترون چیست» را پیدا کنیم، خواص این ذره را بیان کردیم و احتمالا تا اینجا متوجه تفاوتهای این ذره با سایر ذرات بهویژه ذرات آلفا و ذرات بتای منفی شدهاید. در این بخش میخواهیم تفاوتهای پوزیترون با بقیه ذرات بنیادی مهم مانند الکترون، پروتون و نوترون را بهصورت جامعتری در یک بخش ارائه کنیم تا بتوانید مقایسه بهتری داشته باشید.
پوزیترون و الکترون
برای فهم بهتر پوزیترون چیست، باید تفاوت این ذره را با سایر ذرات مشابهاش بدانیم. خواص پوزیترون کاملا شبیه خواص الکترون است و تنها اختلافی که در خواص پوزیترون با الکترون وجود دارد، نوع بار است. بار پوزیترون مثبت و بار الکترون منفی است. بنابراین تفاوت پوزیترون و الکترون فقط در علامت بار الکتریکی است. به علت همین شباهت بالا و اختلاف علامت بار، پوزیترون پادذره الکترون محسوب میشود. اگر بخواهیم اختلاف این دو ذره را بهتر متوجه شویم، باید اتم یک ماده و اتم پادمادهاش را با هم مقایسه کنیم. مثلا اتم هیدروژن را در شکل زیر نظر بگیرید.
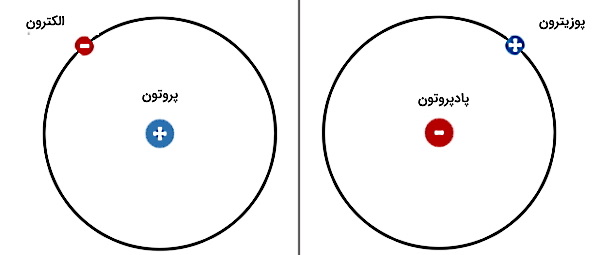
برای هیدروژن پادمادهای به نام پادهیدروژن داریم. اگر اتم این دو ماده را مقایسه کنیم، برای اتم هیدروژن ذرهای که دور هسته میچرخد الکترون است. در حالی که برای اتم پادهیدروژن، ذره در حال چرخش دور هسته پوزیترون است. در جدول زیر بهطور خلاصه، تفاوت و شباهتهای این دو ذره بیان شده است:
| نام ذره | پوزیترون | الکترون |
| اندازه بار برحسب کولن (C) | ||
| علامت بار الکتریکی | مثبت | منفی |
| جرم ذره برحسب کیلوگرم (kg) | ||
| اسپین | ||
| ماهیت | پادذره الکترون | ذره |
| نماد | یا یا | یا یا |
پوزیترون و پروتون
برای فهم دقیقتر اینکه پوزیترون چیست، بهتر است بهصورت دقیقی نیز بدانیم که پروتون چیست. پوزیترون و پروتون هر دو دارای اندازه بار و علامت بار یکسان هستند. بنابراین شاید در نگاه اول، بهنظر برسد که خیلی شبیه هم هستند. تفاوت اساسی این دو ذره در جرم آنها است. جرم پروتون با جرم اتم هیدروژن برابر است و از پوزیترون یا الکترون خیلی سنگینتر است. جدول زیر خلاصهای از خواص این دو ذره را نشان میدهد:
| نام ذره | پوزیترون | پروتون |
| اندازه بار برحسب کولن (C) | ||
| علامت بار الکتریکی | مثبت | مثبت |
| جرم ذره برحسب کیلوگرم (kg) | ||
| اسپین | ||
| ماهیت | پادذره الکترون | ذره |
| نماد | یا |
تفاوت دیگر این دو ذره در این است که پروتون جز ذراتی است که در هسته تمام اتمها وجود دارد. اما پوزیترون ذرهای است که میتواند از یک هسته ناپایدار با تعداد پروتونهای بالا تابش شود. بنابراین ماهیت پوزیترون به عنوان پادذره الکترون با ماهیت پروتون بهعنوان یک ذره کاملا متفاوت است. در شکل بخش قبل که اتم یک ماده با اتم پادمادهاش مقایسه شد، تفاوت پروتون و پوزیترون و جایگاه قرارگیری آنها کاملا مشخص است.
پوزیترون و نوترون
در ادامه یادگیری مبحث پوزیترون چیست، باید بدانیم اختلاف پوزیترون و نوترون بهعنوان یکی دیگر از ذرات مهم داخل هسته، علاوه بر جرم، در اندازه و علامت بار نیز هست. پوزیترون ذرهای بسیار سبکتر از نوترون است. جرم نوترون با پروتون تقریبا یکی است. همچنین پوزیترون دارای بار واحد با علامت مثبت است، در حالی که میدانیم نوترون ذرهای بدون بار یا خنثی است. در جدول زیر خصوصیات این دو ذره مقایسه شده است:
| نام ذره | پوزیترون | نوترون |
| اندازه بار برحسب کولن (C) | ||
| علامت بار الکتریکی | مثبت | خنثی |
| جرم ذره برحسب کیلوگرم (kg) | ||
| اسپین | ||
| ماهیت | پادذره الکترون | ذره |
| نماد | یا |
کاربرد تابش پوزیترون در پزشکی
پس از بررسی جنبههای مختلف، آموختیم که پوزیترون چیست و چه ویژگیهایی دارد. در این بخش کاربرد مهم این ذره در پزشکی را توضیح میدهیم. یکی از معادلات هستهای بیانگر تابش پوزیترون، واکنش زیر است:
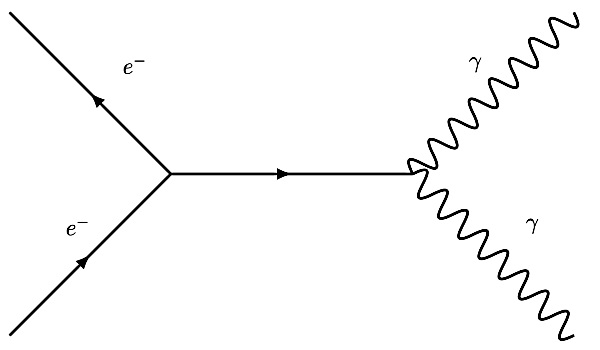
در فرآیند بالا تابش پوزیترون از عنصر «فلوئور» (Fluorine) با نماد F انجام میشود. از این تابش در پزشکی با عنوان «توموگرافی تابش پوزیترون» (Positron Emission Tomography) یا اسکن PET یا پت اسکن جهت تشخیص سلولهای سرطانی استفاده میشود. علت استفاده از پوزیترون در این تکنیک این است که وقتی پوزیترون با یک الکترون برخورد میکند، فورا نابود میشود. این فرآیند همانطور که قبلا هم گفتیم، به نابودی الکترون-پوزیترون یا نابودی ذره-پادذره یا نابودی زوج معروف است. در چنین فرآیندی، دو پرتو گاما با انرژی بالا تولید میشوند.
حالا میخواهیم ببینیم تصویربرداری پت اسکن با توجه به توضیحات بالا چگونه روی بیمار انجام میشود. ابتدا روی بیمار یک تزریق انجام میشود، حاوی مادهای به نام «فلودئوکسی گلوکوز» (Fluorodeoxyglucose) یا FDG که شبیه شکر است. این ماده توسط سلولهای سرطانی، جذب میشود. با جمع شدن FDG در این سلولها، واکنش بالا رخ میدهد و پوزیترون تولید میشود.
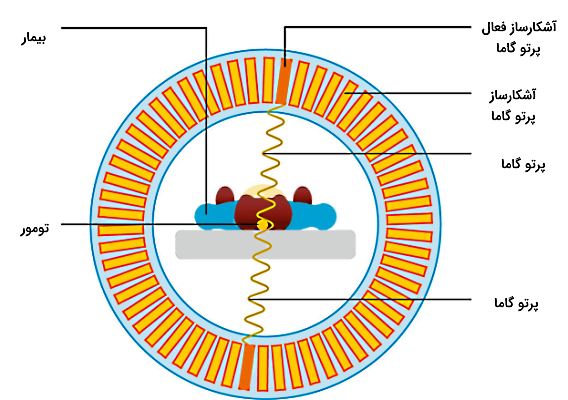
مرحله بعدی، نابودی زوج است که از برخورد پوزیترون با الکترونهای محل تومور انجام میشود. در نتیجه پرتوهای گاما تولید میشوند. بنابراین، آشکارسازی این پرتوها میتواند محل تومور را نشان دهد. پس از گذشت بازه زمانی کوتاهی، تصویربرداری از بیمار توسط ابزارهای مناسبی با قدرت آشکارسازی پرتوهای گاما انجام میشود. همانطور که تصویر مشاهده میکنید، این آشکارسازها بهصورت یک مدار دایرهای دور بیمار قرار دارند تا پرتوهای گامای خروجی حتما آشکار شوند.
چون پرتوهای گاما در فرآیند نابودی زوج در دو جهت مختلف گسیل میشوند، این امکان فراهم است تا کامپیوتر متصل به این سیستم بتواند خطی را رسم کند که دقیقا از نقطه نابودی عبور میکند. در نهایت، با انجام محاسبات دقیقتر، مکان دقیق تابش مشخص میشود.
تاریخچه کشف پوزیترون
پس از اینکه کاملا یاد گرفتیم پوزیترون چیست، در انتها تاریخچه کشف پوزیترون را خیلی مختصر بیان میکنیم. اولین پادذرهای که کشف شد، پوزیترون بود. «کارل دیوید اندرسون» (Carl David Anderson) در سال ۱۹۳۶ حین انجام آزمایشهای خود در مورد اندازهگیری انرژی الکترونهای ناشی از تابش کیهانی توانست پوزیترون را کشف کند و به دنبال آن نیز جایزه نوبل فیزیک را دریافت نمود.

کشف پوزیترون از این جهت دارای اهمیت بود که میتوانست نظریاتی که «پل دیراک» (Paul Dirac) در مورد الکترون داشت را توضیح دهد. دیراک معادله موجی را ارائه کرد که برای آن قواعد کوانتومی بهصورت تقریبی برقرار بود. در واقع طبق توضیحات مکانیک کوانتومی، باید برای الکترون حالتهایی با انرژی منفی در نظر گرفته میشد در حالی که چنین چیزی در آزمایشها مشاهده نمیشد.

در سال ۱۹۳۱، دیراک با این فرض پیش رفت که این حالتهای منفی احتمالا به ذرات جدیدی به نام پادالکترون مربوط هستند. بنابراین دیراک به نوعی وجود چنین ذرهای را پیشبینی کرده بود.
یادگیری پوزیترون با فرادرس برای دانشجویان
پیش از ارائه جمعبندی این مطلب در مورد اینکه پوزیترون چیست، چنانچه دانشجو هستید و تمایل دارید راجعبه ذرات بنیادی و فیزیک هستهای اطلاعات بیشتری کسب کنید، از شما دعوت میکنیم فیلمهای آموزشی زیر در فرادرس را مشاهده کنید:

- فیلم آموزش شیمی عمومی ۱ و ۲ مرور و حل مساله فرادرس
- فیلم آموزش رایگان آشنایی با فیزیک اتمی و هسته ای فرادرس
- فیلم آموزش رایگان واکنش های هسته ای فرادرس
- فیلم آموزش رایگان مقدمات فیزیک ذرات بنیادی فرادرس
- فیلم آموزش فیزیک هستهای ۲ فرادرس
- فیلم آموزش مبانی فیزیک ذرات بنیادی فرادرس
- فیلم آموزش رایگان فیزیک هسته ای پیشرفته فرادرس
- فیلم آموزش رایگان معرفی رشته مهندسی هستهای – دانشگاه، بازار کار و ادامه تحصیل فرادرس
- فیلم آموزش طیف سنجی رزونانس مغناطیسی هسته پیشرفته فرادرس
جمعبندی
در این مطلب از مجله فرادرس یاد گرفتیم پوزیترون چیست و چه تفاوتهایی با ذرات دیگر مانند ذرات آلفا، بتا یا الکترون و پروتون دارد. یک هسته ناپایدار با گسیل ذرات گفته شده طی فرآیندهایی به نام واپاشی پرتوزا، به یک هسته پایدارتر تبدیل خواهد شد.
ذرات آلفا چون شامل دو پروتون و دو نوترون هستند، شبیه هسته یک اتم هلیوماند. ذرات بتای منفی الکترون هستند و پرتوهای پرانرژی، بدون جرم و بار گاما نیز ذره محسوب نمیشوند بلکه فوتوناند. گاهی ذره بتای گسیل شده، دارای بار مثبت است. ذره بتای مثبت، همان پوزیترون است. پوزیترونها دارای جرم ناچیزی هستند و پادذره الکترون یا پادالکتروناند. این ذرات دارای یک بار مثبت هستند. پوزیترون زمانی تشکیل میشود که پروتون به نوترون تبدیل شود. به این ترتیب، اگر هستهای یک پوزیترون تابش کند، عدد اتمی آن یک واحد کم خواهد شد ولی عدد جرمی آن تغییری نمیکند.