آندوسیتوز چیست؟ – درون بری به زبان ساده + تفاوت با اگزوسیتوز
غشای پلاسمایی که مرز بین سلول و محیط خارج آن را میسازد، نیمهتراوا است. یعنی به برخی مولکولهای کوچک و یونها اجازه عبور میدهد ولی سایر مولکولهای کوچک باید از کانالها و پمپهای موجود در آن برای ورود و خروج خود استفاده کنند. با این حال مواد بزرگ نمیتوانند از این کانال و پمپها هم استفاده کنند. برای این مواد روش آندوسیتوز یا درون بری وجود دارد. اندوسیتوز یک فرایند سلولی است که به وسیله آن میتوان مواد خارج سلولی را به همراه بخشی از غشا به داخل سلول آورد. انواع مختلفی از اندوسیتوز بر اساس نوع محموله ورودی به سلول (از هورمونها و مواد مغذی کوچک تا مواد بزرگی مثل باکتریها) وجود دارد. بعد از فرایند اندوسیتوز بخشی از غشا که به داخل سلول وارد شده به غشای پلاسمایی اصلی برمیگردد و بخشی از آن نیز تجزیه میشود. تعادل میان میزان غشای بازگردانده شده و میزان غشای تجزیه شده ساختار غشای پلاسمایی را تعیین میکند. در این مطلب تلاش شده انواع اندوسیتوز و مسیرهای دخیل در آن به طور کامل توضیح داده شود.
- میآموزید که اندوسیتوز چگونه مواد بزرگ را به درون سلول وارد میکند.
- تفاوتهای اصلی آندوسیتوز با اگزوسیتوز و ترنسیتوز را یاد خواهید گرفت.
- انواع مکانیسمهای آندوسیتوز و نقش هر کدام را درک میکنید.
- با نحوه هدفمندسازی و تجزیه محموله در اندوزومها آشنا میشوید.
- نقش آندوسیتوز در بقای سلولی و دفاع ایمنی را خواهید آموخت.
- نقش اختلال در مسیرهای آندوسیتوز در ایجاد بیماری را خواهید آموخت.
آندوسیتوز چیست ؟
واژه «اندوسیتوز» (Endocytosis) یا درون بری اولین بار توسط «ویسکانت دوو» (Christian de Duve) در سال 1963 ارائه شد که از واژه یونانی «éndon» به معنای درون، «kutos» به معنای ظرف توخالی و «osis» به معنای شرایط گرفته شده است. آندوسیتوز فرایندی است که در آن سلول مواد خارج سلولی را با قرار دادن داخل بخشی از غشا و تشکیل وزیکول به داخل سلول میآورد.
اندوسیتوز سلول را قادر میسازد تا مواد مغذی خارج سلول، گیرندههای فعال غشای سلول را به داخل سلول وارد کند. همچنین اندوسیتوز امکان وارونه کردن لیپیدها و پروتئینهای غشایی را نیز فراهم میکند. برخی از سلولهای بدن با اندوسیتوز میتوانند میکروارگانیسمها و سلولهای مرده اطراف سلول را حذف کنند.
مراحل آندوسیتوز
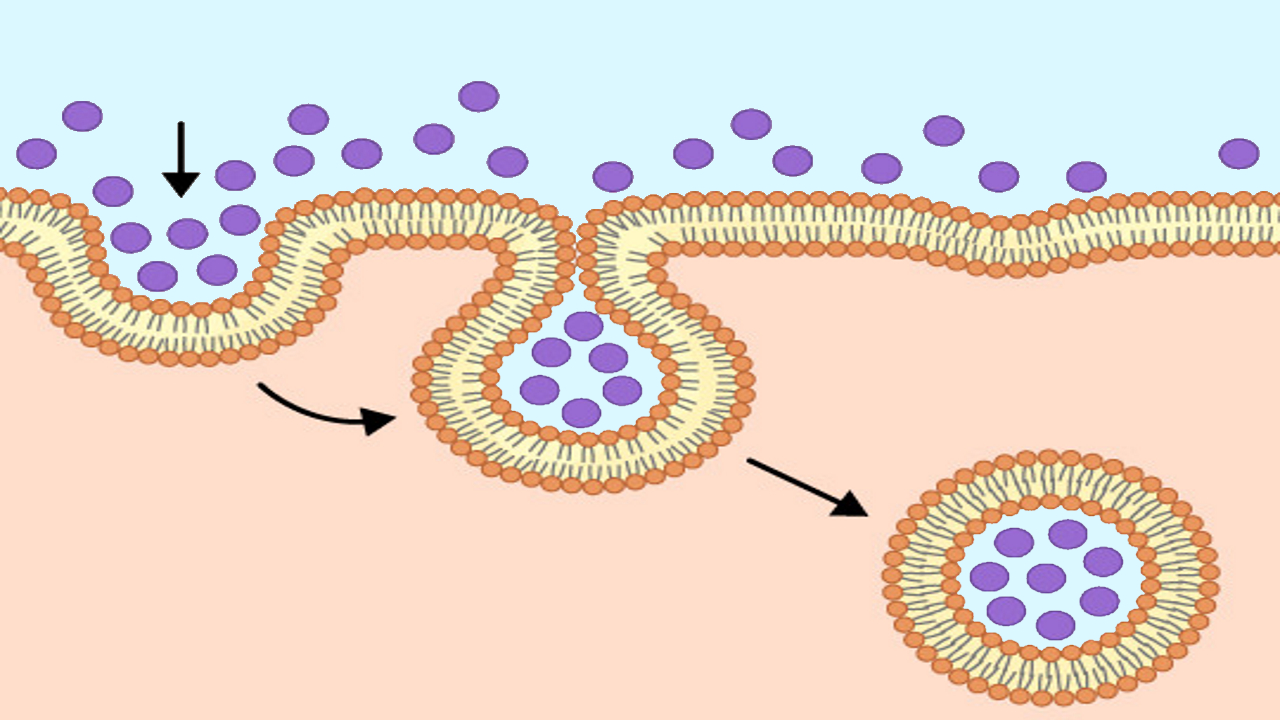
اندوسیتوز به شیوههای مختلفی انجام میشود اما میتوان به طور کلی مراحل زیر را برای آن در نظر گرفت.
- غشای پلاسمایی کمی به داخل میرود و گودال ایجاد میکند.
- مواد خارجی سلولی در این گودال قرار میگیرند.
- لبههای گودال ایجاد شده در غشای پلاسمایی به یکدیگر نزدیک میشوند و کاملا به یکدیگر جوش میخورند.
- مواد خارج سلولی درون غشای پلاسمایی به دام میافتد و به داخل سلول میرود.
تفاوت آندوسیتوز و اگزوسیتوز چیست ؟
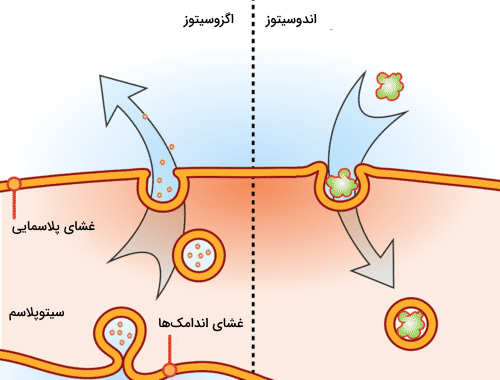
آندوسیتوز و «اگزوسیتوز» (Exocytosis) هر دو روشهایی هستند که برای عبور دادن مواد نسبتا بزرگ از غشا استفاده میشوند. در آندوسیتوز مواد سلولی به داخل سلول وارد میشوند در صورتی که در اگزوسیتوز یا برونرانی مواد به خارج سلول منتقل میشوند. تصویر بالا این تفاوت را به خوبی نشان میدهد.
از اگزوسیتوز برای حذف سموم و مواد زائد داخل سلول، ترمیم غشای سلول و همچنین انتقال مواد برای برقراری ارتباط میان سلولها استفاده میشود. تفاوت اندوسیتوز و اگزوسیتوز در جدول زیر نوشته شده است.
| اندوسیتوز | اگزوسیتوز | |
| تعریف | انتقال ذرات به داخل سلول | انتقال ذرات به خارج سلول |
| عملکرد |
جذب مواد مغذی حذف پاتوژن حذف سلولهای مرده انتقال گیرنده به داخل سلول برعکس کردن پروتئین و لیپیدهای غشا |
حذف سموم و مواد زائد ترمیم غشای سلول ایجاد ارتباط میان سلولها |
| انواع |
فاگوسیتوز پینوسیتوز |
اگزوسیتوز تنظیم شده اگزوسیتوز سازنده |
| مثال | از بین بردن باکتریها توسط گلبولهای سفید | آزاد کردن انتقالدهنده عصبی برای ارسال پیام |
تفاوت اندوسیتوز و ترنسیتوز چیست ؟
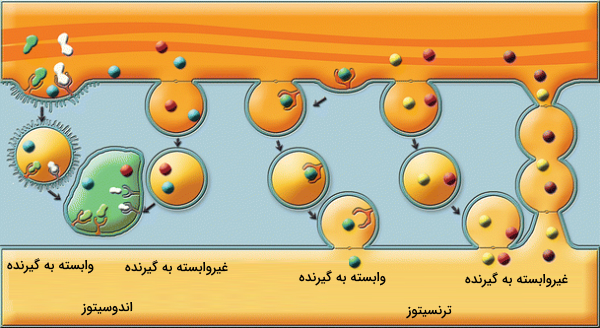
ترنسیتوز ترکیبی از آندوسیتوز (درون بری) و اگزوسیتوز است. در این روش ماکرومولکولهای سطح غشا (سلولهای قطبی) اندوسیتوز میشوند و از طریق وزیکول به داخل سلول میآیند. سپس درون سلول حرکت میکنند و از طریق وزیکول دوباره به قسمت دیگری از غشا متصل میشوند. اما تعریف اندوسیتوز تنها انتقال مواد به داخل سلول از طریق تشکیل وزیکول است.
سلولهای قطبی یا قطبیت سلولی به عدم تقارن در داخل سلولها گفته میشود. این عدم تقارن میتواند در شکل سلول، ساختار یا محل قرار گرفتن اجزای داخل سلولی آن باشد. بیشتر سلولهای اپیتلیال، سلولهای مهاجر و سلولهای در حال تکامل برای انجام فعالیت خود به قطبیت سلول نیاز دارند. در این نوع سلولها معمولا ترنسیتوز انجام میشود.
انواع اندوسیتوز
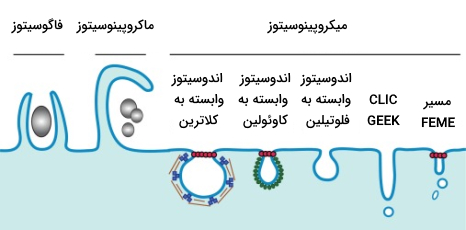
آندوسیتوز یا درون بری را میتوان بر اساس نوع و اندازه محمولهای که به داخل سلول وارد میشود به انواع مختلفی تقسیم کرد. تصویر زیر انواع آندوسیتوز را نشان میدهد.
- «ماکروپینوسیتوز» (Macropinocytosis)
- «آندوسیتوز به واسطه گیرنده» (Receptor-mediated Endocytosis)
- «آندوسیتوز سریع وابسته به اندوفیلین» (Fast Endophilin-mediated Endocytosis | FEME)
- «اندوسیتوز وابسته به فلوتیلین» (Flotillin-associated Endocytosis)
- «اندوسیتوز غیروابسته به کلاترین/ وزیکول غنی از گلیکوفسفاتیدیلینوزیتول» (CLIC/GEEC)
- «کاوئولا» (Caveolae)
- «فاگوسیتوز» (Phagocytosis)
فاگوسیتوز
فاگوسیتوز که به فرایند غذا خوردن سلول معروف است فرایندی است که در آن معمولا ذرات بزرگتر از 500 نانومتر به داخل سلول وارد میشوند. در یوکاریوتهای پست مانند آغازیان از این فرایند برای انتقال مواد غذایی به داخل سلول استفاده میشود. در حالی که در پستانداران، فاگوسیتوز توسط گروه خاصی از سلولها مانند نوتروفیل و ماکروفاژ برای حذف سلولهای مرده و میکروارگانیسمها استفاده میشود.
مراحل فاگوسیتوز
فاگوسیتوز در پنج مرحله انجام میشود که این مراحل به شرح زیر هستند.
- شناسایی: سلول بیگانهخوار یا فاگوسیت آنتیژن یا ذره خارجی را شناسایی میکند و برای انجام فرایند بیگانهخواری به سمت آن حرکت میکند.
- اتصال: سلول فاگوسیت به ذره خارجی اتصال پیدا میکند که در نتیجه آن سودوپودیا اطراف ذره خارجی تشکیل میشود. سودوپودیا بخشی از غشای سلول است که مانند بازو ذره خارجی را احاطه میکند.
- بلع: غشای سودوپودیا از دو طرف به یکدیگر متصل میشوند تا وزیکولی حاوی ذره خارجی ایجاد کنند. به وزیکولی که در این فرایند تشکیل میشود و حاوی ذره خارجی است، فاگوزوم میگویند.
- الحاق: فاگوزوم درون سلول به لیزوزوم متصل میشود و فاگولیزوزوم را تشکیل میدهد. لیزوزوم حاوی آنزیمهایی است که میتواند ذره خارجی را تجزیه کند.
- حذف مواد: مواد زائد ناشی از هضم ذره خارجی توسط وزیکولی به غشا متصل میشوند و به بیرون سلول تخلیه میشوند.
ماکروپینوسیتوز
پینوسیتوز از واژه لاتین «Pino» به معنای نوشیدن گرفته شده است. در این روش انتقال مایعات حاوی مواد خارج سلولی به صورت غیراختصاصی در وزیکولی به داخل سلول فرستاده میشود. در انسان این فرآیند بیشتر در سلولهای پوشاننده روده کوچک اتفاق میافتد و به طور عمده برای جذب قطرات چربی استفاده میشود. وزیکول ها در نهایت با لیزوزوم ترکیب میشوند و در نتیجه محتویات آن هضم میشود. برخلاف فاگوسیتوز و اندوسیتوز وابسته به گیرنده، در این روش مواد به صورت غیراختصاصی وارد سلول میشوند. همچنین این روش نیازی به صرف انرژی ندارد. کشف پینوسیتوز به «وارن لوئیس» (Warren H. Lewis) در سال 1929 نسبت داده شده است.
ظرفیت سلولها برای انجام ماکروپینوسیتوز به نوع مواد نوع سلول بستگی دارد و میتواند به صورت پیوسته یا القایی انجام شود. ماکروفاژها و سلولهای دندریتیک برای بررسی وجود پاتوژنها در محیط خارج سلولی به طور پیوسته و در مقیاس وسیعی ماکروپینوسیتوز انجام میدهند. القای ماکروپینوسیتوز میتواند در اثر طیف وسیعی از محرکها، از جمله گیرندههای خانواده تیروزینکیناز (به عنوان مثال EGFR)، پروتئوگلیکانها یا گیرندههای متصل به پروتئین G اتفاق بیفتد.
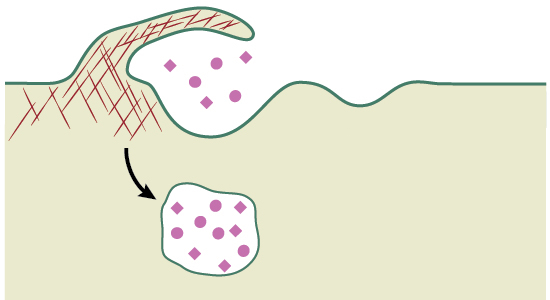
ایجاد ماکروپینوسیتوز در سلول
ایجاد ماکروپینوسیتوز فرایندی وابسته به اکتین است که از طریق فاکتورهای رشدی مانند فاکتور تحریک کننده کلونی (Colony Stimulating Factor | CSF-1)، «فاکتور رشد اپیدرمی» (Epidermal Growth Factor | EGF) و «فاکتور رشد مشتق از پلاکت» (Platelet-derived Growth Factor | PDGF) شروع میشود.
وقتی این لیگاندها به رسپتور خود متصل میشوند، پیام حاصل از تحریک گیرنده منجر به پلیمریزاسیون فیلامنتهای اکتین در غشا میشود. در اثر این اتفاق غشای پلاسمایی به صورت موجی به بیرون چین میخورد و تشکیل لاملیپودا میدهد. بیشتر لاملیپوداهای تشکیل شده دوباره به حالت قبلی برمیگردند ولی بعضی از آنها به سمت داخل خم میشوند و به غشا اتصال مییابند. در اثر این اتفاق وزیکول بزرگی به نام ماکروپینوزوم تشکیل ميشود که حاوی مایع خارج سلول است.
نقش فیزیولوژیک ماکروپینوسیتوز در سلول
بیشتر سلولها در اثر تحریک با فاکتورهای رشد توانایی انجام ماکروپینوسیتوز دارند اما این فرایند در ماکروفاژها و سلولهای دندریتیک به طور مداوم انجام میشود تا سلول بتواند مایع خارج سلولی برای وجود آنتیژنها بررسی کند. از طرفی برخی از ویروسها و باکتریها از این فرصت استفاده میکنند و وارد سلولهای بدن میشوند. نقش فیزیولوژیک ماکروپینوسیتوز را میتوان در فرایندهای زیر مشاهده کرد.
- حرکت سلولها: از آنجایی که ماکروپینوسیتوز با ایجاد موجهایی در سطح سلول شروع میشود، میتواند در فرایندهای دخیل در تحرک سلول مانند کموتاکسی نقش داشته باشد. در کموتاکسی نوتروفیلها، ارتباط بین «جاذب شیمیایی» (Chemoattractant) و گیرندههای کمپلمان باعث تحریک جمع شدن گیرندههای کمپلمان و ورود آنها به سلول توسط ماکروپینوسیتوز میشود.
- ارائه انتیژنها و پاسخ ایمنی: سلولهای ارائه دهنده آنتیژن مانند ماکروفاژ و سلولهای دندریتیک، پیوسته مایع خارج سلولی را برای وجود آنتیژنها ماکروپینوسیتوز میکنند. بعد از ورود آنتیژنها به سلول، پردازش میشوند و پپتیدهای انها روی مولکولهای MHC قرار میگیرد. سپس سلول این مولکولها را در سطح غشای خود قرار میدهد تا سلولهای ایمنی T آنها درک کنند و پاسخ ایمنی مرتبط انجام شود.
- حمله پاتوژنها: بعضی از باکتریها و ویروسها از فرایند ماکروپینوسیتوز استفاده میکنند تا به داخل سلول میزبان راه یابند. برای مثال ویروس Vaccinia با تقلید از اجسام آپوپتوزی باعث ایجاد ماکروپینوسیتوز در سلول میزبان میشوند.
این ویروسها خود را در غشای لیپیدی دولایه سلول میزبان قبلی که آلوده شده به دست این ویروسها قرار میدهند.
در غشای این سلولها به دلیل وجود ویروس، فسفاتیدیل سرین به روی غشا میآید. این ویروسها از این غشا استفاده میکنند و با استفاده از فسفاتیدیل سرین به غشای سلولهای سالم متصل میشوند. سلول سالم فکر میکند که این غشای سلول آپوپتوزی است بنابراین آن را ماکروپینوسیتوز میکند و ویروس از این طریق به سلول سالم دیگری راه پیدا میکند.
اندوسیتوز وابسته کلاترین
در اندوسیتوز وابسته به «کلاترین» (Clathrin-mediated Endocytosis | CME) وزیکولی در اندازهای حدود 100 تا 200 نانومتر تشکیل میشود که در غشای آن پروتئینهای کلاترین وجود دارد. پروتئینهای کلاترین 2٪ از غشای پلاسمایی را دربرمیگیرند و عمر آنها حدود 1 دقیقه در نظر گرفته میشود. بنابراین در هر دقیقه 2٪ از غشا به داخل سلول منتقل میشود.
زنجیرههای سنگین و سبک سه کلاترین کنار هم قرار میگیرند و ساختار «تریسکلیون» (Triskelion) را تشکیل میدهند. تریسکلیونها در کنار هم قرار میگیرند و ساختار مشبکی دور وزیکول ایجاد میکنند. تصویر زیر ساختار مشبک و ترسکلیون را نشان میدهد.
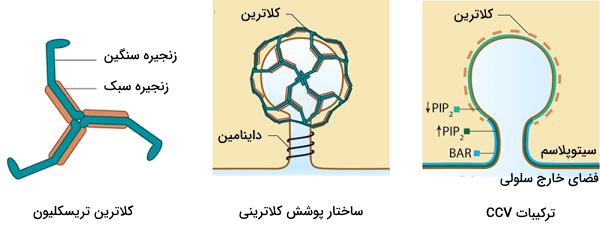
برای اینکه پروتئین کلاترین به غشا متصل شود باید پروتئینهای آداپتور روی غشای پلاسمایی قرار گرفته باشند. یکی از پروتئینهای آداپتوری که کلاترین را به غشا متصل میکند، «کمپلکس پروتئین آداپتور ۲» (Adaptor Protein 2 Complex | AP2) نام دارد. این پروتئین یک «هتروتترامر» (Heterotetramer) است که از دو بخش بزرگ (α و β)، یک بخش متوسط (μ) و یک بخش کوچک (σ) تشکیل شده است.
آهن متصل به گیرنده «ترنسفرسین» (Transferrin) و LDL متصل به گیرنده «لیپوپروتئین چگالی پایین» (Low-density Lipoprotein | LDL) با استفاده از این نوع اندوسیتوز به داخل سلول منتقل میشوند.
از دست دادن عملکرد هر یک از اجزای مرکزی اندوسیتوز وابسته به کلاترین مانند کلاترین، AP2 و دینامین منجر به مرگ جنینی میشود بنابراین جهش شدیدی در آنها دیده نمیشود. با این حال، اختلالات کوچک در این روش اندوسیتوزی با بسیاری از بیماریهای انسانی مانند سرطان، میوپاتی، نوروپاتی، سندرمهای ژنتیکی متابولیک و بیماریهای روانپزشکی و نورودژنراتیو در ارتباط است.
پروتئینهای اداپتور کلاترین
پروتئینهای اداپتور محموله اندوسیتوزی در به گودال پوشیده از کلاترین متصل میکند. دو نوع آداپتور اصلی برای اتصال به کلاترین وجود دارد.
- آداپتورهای کلاسیک: شامل تترامرهای AP1 ،AP2 ،AP3 و AP4 است.
- آداپتورهای جایگزین: معمولا از یک پروتئین (گاهی اوقات همودیمر) تشکیل شده است که محموله را به گودال پوشیده از کلاترین متصل میکند. GGA و اپسین مثالی از آن هستند.
مراحل درون بری وابسته به کلاترین
انجام درون بری با روش وابسته به کلاترین به صورت زیر انجام میشود.
- مولکولی که باید بلعیده شود به گیرنده خاصی روی غشای پلاسمایی متصل میشود و این مجموعه به ناحیهای از غشا حاوی یک گودال پوشیده شده از کلاترین، میرود.
- غشای حاوی کلاترین دور گیرنده و مولکول متصل به آن را دربر میگیرد. برای ایجاد خمیدگی غشا به دور گیرنده پروتئینهایی مانند »اپسین» (Epsin) و «آمفیفیزین» (Amphiphysin) نقش دارند.
- پروتئین «داینامین» (Dynamin) که یک GTPase است با مصرف GTP وزیکول را از غشا جدا میکند و وزیکول تشکیل شده را به داخل سلول میرود.
- وزیکول به اندوزوم داخل سلولی متصل میشود که در نتیجه این اتصال کلاترین از وزیکول اولیه و مولکول از گیرنده جدا میشود. در بیشتر مواقع گیرنده توسط وزیکول دوباره به سطح غشا باز میگردد.
- بعد از جدا شدن کلاترین لیزوزوم به وزیکول متصل میشود و مواد داخل آن را تجزیه میکند.
چگونه کلاترین در برای پوشاندن وزیکول اندوسیتوزی به غشا فراخوانده میشود ؟
اندوسیتوز وابسته به کلاترین در اثر تجمع فسفاتیدیل اینوزیتول 5،4-بیفسفات (Phosphatidylinositol-4,5-bisphosphate | PIP2) القا میشود. تجمع PIP2 در غشا توسط کاتالیز «فسفواینوزیتید» (Phosphoinositide) به وسیله آنزیمهای لیپید کینازی به نام PI4K و PI4P5K و هیدرولیز توسط فسفاتازها انجام میشود.
پروتئینهای آداپتور (AP-2 در پستانداران یا Sla1 در مخمرها) روی PIP2 قرار میگیرند و کمپلکس آداپتور-PIP2 را تشکیل میدهند. این مجموعه توسط پروتئینهای جانبی مانند CLASPs، اکتین و میوزین I تثبیت می شود. پروتئین آداپتور AP-2 هنگامی که میزان محموله اندوسیتوزی یا سطح PIP2 پایین باشد فعالیت خود را مهار میکند. این موضوع فقط در مواقع لزوم باعث تشکیل وزیکول کلاترینی میشود.
اتصال PIP2 و محموله به پروتئین آداپتور AP-2 که به دنبال تجمع PIP2 در غشا اتفاق میافتد، پروتئین آداپتور را فعال میکند و کلاترین به آن اتصال پیدا میکند. به دنبال اتصال کلاترین وزیکول اندوسیتوزی با پوشش کلاترینی تشکیل میشود.
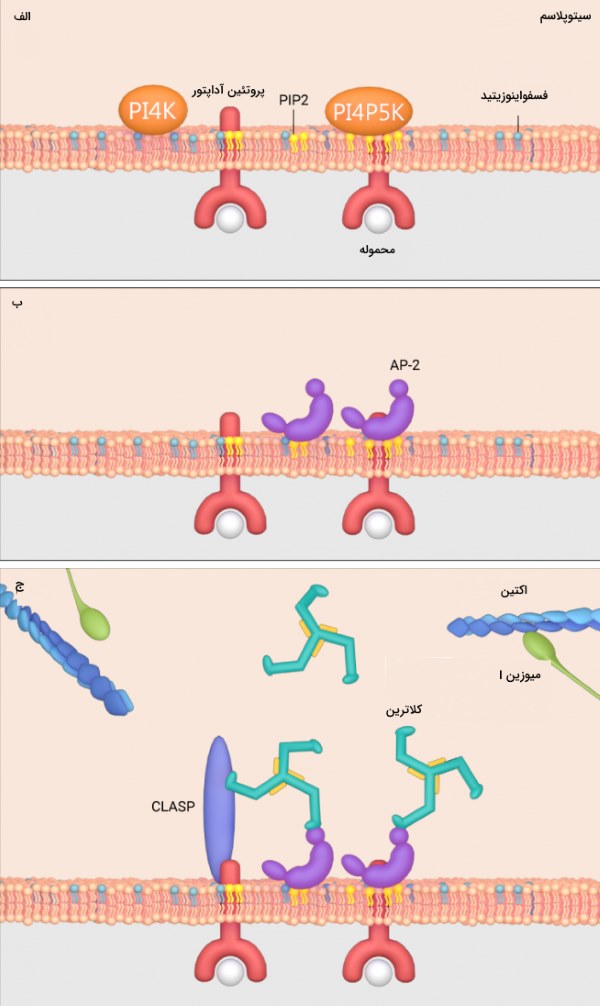
تشکیل گودال پوشیده از کلاترین در غشا چگونه انجام میشود ؟
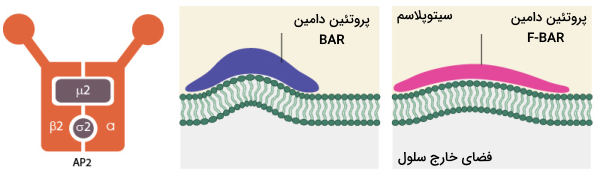
تشکیل «گودال پوشیده از کلاترین» (Clathrin-coated Pits | CCPs) نیازمند پروتئینهای متنوع متصل شونده به پروتئین اکتین مانند خانواده پروتئینی BAR است. این پروتئینها شامل «آمفیفیزین» (Amphiphysin) و «اندوفیلین» (Endophilin) در پستانداران و Rvs161p و Rvs167p در مخمر است. نقش این پروتئین تغییر شکل غشا است به ویژه ایجاد شکل لولهای است.
اتصال این پروتئینها به غشای دارای بار منفی، باعث میشود که غشا شکل دیمر α-هلیکس آمفیپاتیک این پروتئینها را به خود بگیرد و انحنای مقعر پیدا کند (تصویر زیر). پروتئین F-BAR یکی دیگر از اجزای خانواده بزرگ BAR است دامین بزرگتری فراهم می کند که به غشا انحنای مقعر میدهد ولی این انحنا کمتر از پروتئینهای دامین BAR است. پروتئین F-BAR باعث تولید وزیکولهای اندوسیتوزی با شعاع بزرگتر میشود. اعتقاد بر این است که برای تشکیل وزیکول اندوسیتوزی با پوشش کلاترین، پروتئین F-BAR قبل از سایر پروتئینهای دامین BAR به محل اندوسیتوز در غشا میرسند.
در حالی که پروتئنهای خانواده BAR باعث انحنای غشا در محل تشکیل وزیکول اندوسیتوزی میشوند، پروتئینهای آداپتور مثل AP-2، اپسین و AP-180، تریمرهای کلاترین و سایر پروتئین های مورد نیاز برای تشکیل وزیکول را فرا میخوانند.
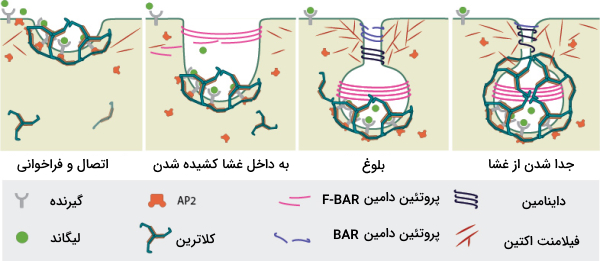
بلوغ وزیکول اندوسیتوزی با پوشش کلاترین چگونه انجام میشود ؟
برای بلوغ وزیکولهای کلاترینی به پروتئینهای مختلفی نیاز است. اکتین، میوزین و WASP همگی نقش مهمی در شکلگیری و استحکام وزیکول کلاترینی دارند. F-اکتین باعث حرکت جانبی گودال پوشیده از کلاترین میشود که به رشد وزیکول کمک میکند.
بعضی از پروتئینها به طور مستقیم روی غشا تاثیر میگذارند در صورتی که بعضی از آنها از طریق پروتئینهای آداپتور نقش خود را ایفا می کنند. یکی از پروتئین های مهم برای تشکیل وزیکول کلاترینی، پروتئین داینامین است. این پروتئین یک GTPase است که باعث جدا شدن وزیکول از غشای پلاسمایی میشود.
داینامین یک GTPase غیرکلاسیک است که تمایل کمی برای اتصال به GTP دارد ولی هیدرولیز آن به GDP را با میزان بالایی انجام میدهد. این ویژگی داینامین این پروتئین را به حسگری برای بلوغ گودال پوشیده از کلاترین به وزیکول کلاترینی تبدیل میکند. قبل از تشکیل گردن وزیکول کلاترینی سرعت بلوغ گودال پایین است اما بعد از تشکیل گردن با هیدرولیز GTP توسط داینامین سرعت بلوغ و تشکیل وزیکول بالا میرود.
در واقع داینامین به عنوان یک حسگر روند پیشرفت تشکیل وزیکول را بررسی میکند و در صورتی که به خوبی انجام نشود از تشکیل وزیکول کلاترینی ممانعت میکند. برای مهار کردن تشکیل وزیکول کلاترینی، داینامین به «آکسیلین» (Auxilin) و Hsc70 متصل میشود که در نتیجه آن تریمرهای کلاترین از وزیکول جدا میشوند.
فاکتورهایی مثل N-WASP ،Arp2/3 و و «کورتاکتین» (Cortactin) نیز به محل تشکیل گودال پوشیده از کلاترین فراخوانده میشوند و به پلیمریزاسیون اکتین برای بلوغ وزیکول کلاترینی کمک میکنند.
چگونه گردن وزیکول اندوسیتوزی با پوشش کلاترین باریکتر میشود ؟
برای جداشدن وزیکول کلاترینی از غشای پلاسمایی PIP2 با آنزیمهای فسفاتازی مانند «سیناپتوجانین» (Synaptojanin 1 | Synj1) دفسفریله میشود. این دفسفریله شدن نه تنها توانایی انتقال سیگنال PIP2 را مهار می کند و تضمین میکند که پروتئینهای آداپتور به طور انتخابی در غشای پلاسما انباشته شوند، بلکه باعث افزایش انحنای غشا برای تشکیل وزیکول شده و همچنین باعث تجزیه پروتئینهای دامین BAR و بسته شدن گردن وزیکول اندوسیتوزی میشود.
Synj1 توسط اندوفیلین 1 فراخوانده میشود. اندوفیلین 1 یکی از پروتئینهای دامین BAR است که دیرتر از سایر پروتئین های آداپتور به محل اندوسیتوزی غشا متصل میشود.
به طور طبیعی PIP2 توسط پروتئینهای دامین BAR از هیدرولیز محافظت میشوند. اما با افزایش میزان انحنای غشا برای تشکیل وزیکول، قدرت اتصال پروتئینهای دامین BAR به PIP2 کاهش مییابد و PIP2 را در مقابل فسفاتازها قرار میدهد. این اتفاق بازخورد مثبت تشکیل میدهد که با افزایش هیدرولیز PIP2 میزان انحنای غشا برای تشکیل وزیکول نیز بیشتر میشود که در نهایت گردن وزیکول باریکتر میشود.
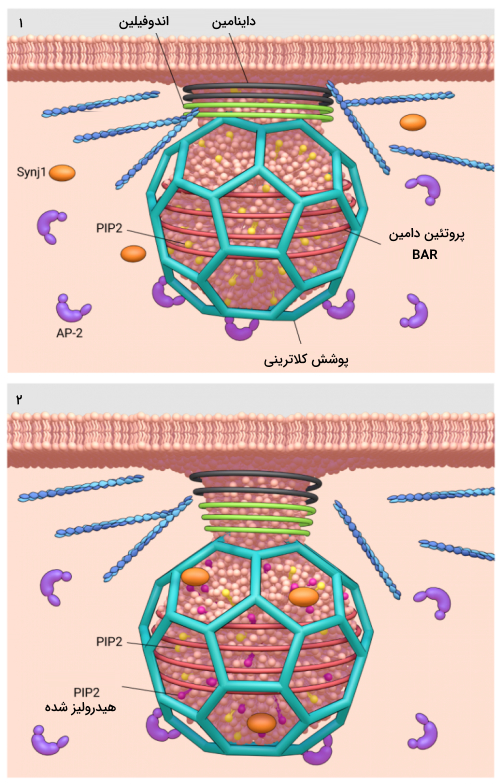
چگونه وزیکول اندوسیتوزی با پوشش کلاترین از غشای پلاسمایی جدا میشود ؟
اعتقاد بر این است که پروتئین داینامین نقش مهمی در جدا شدن وزیکول اندوسیتوزی با پوشش کلاترین از غشای پلاسمایی داشته باشد. پروتئینهای دیگری مثل اندوفیلین و امفیفیزین نیز در تشکیل گردن وزیکول و باریک شدن آن کمک میکنند. در حضور GTP پروتئین داینامین پیچ میخورد و در نتیجه این پیچ خوردن، کشش طولی در گردن وزیکول ایجاد میکند. این انقباض باعث جدا شدن وزیکول از غشا میشود.
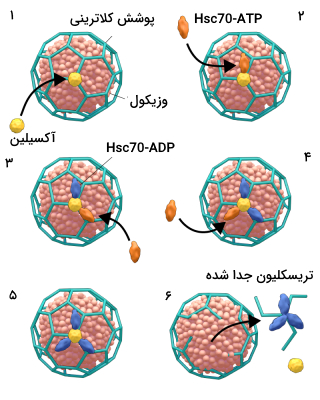
چگونه پوشش کلاترینی از وزیکول اندوسیتوزی جدا میشود ؟
در پستانداران جدا کردن پوشش کلاترینی از وزیکولهای اندوسیتوزی یک واکنش انرژیخواه (نیاز به ATP) است که توسط چاپرون 70 کیلودالتونی «پروتئین وابسته به شوک حرارتی» (Heat Shock Cognate Protein) انجام میشود. علاوه بر این پروتئینها برای جدا کردن هر تریسکلیون کلاترینی به یک مولکول آکسیلین نیز نیاز است.
برای جداشدن پوشش کلاترینی از وزیکول ابتدا یک مولکول اکسیلین به مرکز تریسکلیون متصل میشود. سه مولکول شوک حرارتی هم به آنها اتصال مییابند. با مصرف سه مولکول ATP ترسیکلیون از وزیکول جدا میشود.
مطالعات بیوشیمایی برونتنی انجام شده روی این وزیکولها نشان دادند که این فرایند وابسته به pH است. در pH برابر با 6، چاپرونها به تریسکلیون متصل میشوند و در pH برابر با 7، تریسکلیون از وزیکول کلاترینی جدا میشود.
اندوسیتوز سریع وابسته به اندوفیلین
آندوسیتوز سریع وابسته به «اندوفیلین» (FEME) به تازگی به عنوان یک مسیر مهم برای آندوسیتوز گیرندههای غشایی خاص مطرح شده است که در مسیر پیامرسانی فاکتور رشد و مهاجرت سلولی اهمیت دارد. محمولههای FEME دارای گیرندههای متصل به پروتئین G است که گیرندههای β1-آدرنرژیک، دوپامینرژیک، استیل کولین، گیرندههای IL-2 و گیرندههای فاکتور رشد مثالی از آن هستند.
این نوع آندوسیتوز ویژگیهایی منحصر به فرد دارد که آن را از سایر روشها متمایز می کند.
- تشکیل وزیکولهای این روش نیازی به کلاترین ندارد اما به داینامین احتیاج دارد.
- تشکیل حاملهای اندوسیتوزی با اتصال لیگاند به گیرندههای خاص القا میشود.
آندوسیتوز یا درون بری با روش FEME وقتی اتفاق میافتد که بین دومین SH3 اندوفیلین و گیرندههای مرتبط (به عنوان مثال گیرنده های متصل به پروتئین G) ارتباط مستقیم برقرار شود و یا از طریق پروتئینهای واسطه مانند CIN85 و Cbl (برای EGFR و HGFR) ارتباط غیرمستقیم برقرار شود. دومین BAR اندوفیلین نیز باعث انحنای غشا و تشکیل وزیکول به دور محموله میشود. در نهایت داینامین با مصرف انرژی وزیکول اندوسیتوزی را از غشا جدا میکند و به داخل سلول میفرستد.
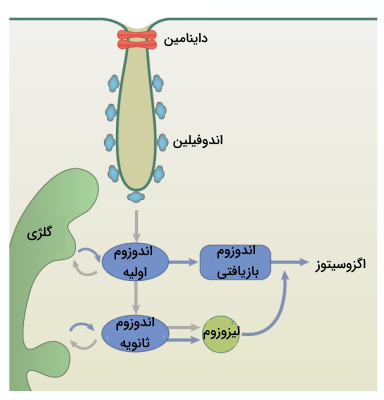
تشکیل وزیکولهای FEME بسیار سریع است (کمتر از 10 ثانیه). این وزیکولها لولهای شکل هستند که 60 تا 80 نانومتر قطر و چند صد نانومتر طول دارند. این روش انتقال مواد در لبه جلویی سلولهای مهاجر انجام میشود و از مسیر پیامرسانی PI3K استفاده میکند. باکتریهایی مانند شیگلا و سم وبا از این روش برای ورود به سلول میزبان بهره میگیرند.
اندوسیتوز وابسته به فلوتیلین
فلوتیلینها پروتئینهایی هستند که در میکرودامینهای خاصی یا در «قایقهای لیپیدی» (Lipid Rafts) غشای پلاسمایی وجود دارند و در اندوسیتوز غیروابسته به کلاترین نقش دارند. فلوتیلینها شوینده های نامحلول هستند که از پروتئین فلوتیلین-1 و فلوتیلین-2 تشکیل شدهاند.
سرهم شدن این پروتئین ها در نقاط خاصی از غشا باعث ایجاد میکرودامینهایی می شود که به داخل سلول جوانه میزنند. پروتئین CD59 و CTxB محمولههایی هستند که با این روش به داخل سلول آندوسیتوز میشوند. تشکیل وزیکولهای اندوسیتوزی با این روش هم میتواند به کمک داینامین و هم بدون داینامین انجام شود.
اندوسیتوز غیر وابسته به کلاترین/ وزیکول غنی از گلیکوفسفاتیدیل اینوزیتول
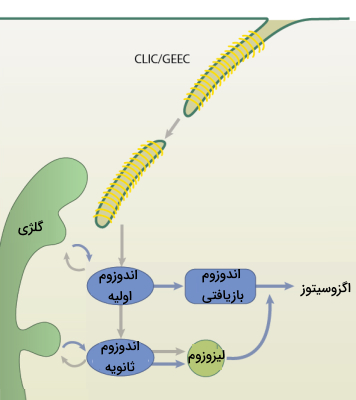
این روش آندوسیتوزی که به اختصار CLIC/GEEC نامیده میشود از کلاترین و داینامین برای تولید وزیکولهای اندوسیتوزی استفاده نمیکند. در واقع در این روش وزیکولهای اولیه لولهایشکل بدون پوشش به نام «حاملهای مستقل از کلاترین» (CLIC) مستقیم از غشای پلاسمایی ساخته میشوند، سپس به وزیکولهای اندوسیتوزی اولیه غنی از «گلیکوفسفاتیدیل اینوزیتول» (GEEC) تبدیل میشوند.
CLIC/GEEC دارای برخی ویژگیهای مشترک با روش FEME است، زیرا هر دو در لبه جلویی سلولهای مهاجر قرار میگیرند و وزیکولهای لولهایشکل ایجاد میکنند. با این حال، بر خلاف روش FEME، که توسط برهمکنشهای خاص بین لیگاند و گیرنده تحریک میشود، آندوسیتوز CLIC/GEEC روشی است که به طور پیوسته در سلولهایی که دارای آن اتفاق میافتد. همچنین نوع محولهای که از این طریق به داخل سلول وارد میشود با محمولههای FEME متفاوت است.
مسیر CLIC/GEEC در جذب پروتئینهای سطحی فراوانی مانند گیرنده «اسیدهیالورونیک» (CD44) و پروتئینهای متصل به گلیکوزیل فسفاتیدیل اینوزیتول نقش دارد و در برخی سلولها نیز باعث جذب مقادیر قابل توجهی مایع و انتقال غشا پلاسمایی به داخل سلول میشود.
این روش توسط ARF1/GBF1، کمپلکس تنظیمی اکتین Arp2/3 و Cdc42 تنظیم میشود و با نوعی پروتئین دامنه BAR، پروتئین IRSp53 و همچنین GRAF1 مرتبط است.
کاوئولا
بعضی از پروتئینها مانند کاوئولین به نقاطی از غشای پلاسمایی اتصال دارند که غنی از گلیکواسفنگولیپید و کلسترول است. اتصال پروتئین کاوئولین به این نقاط گودالی شبیه به فلاسک در اندازهای حدود 50 تا 60 نانومتر به وجود میآورد که کاوئولا نام دارد و در این نقاط درون بری اتفاق میافتد. سه نوع پروتئین کاوئولین وجود دارد.
- کاوئولین 1: در غشای سلولهای غیرعضلانی
- کاوئولین 2: در غشای سلولهای غیرعضلانی
- کاوئولین 3: در غشای سلولهای عضلانی
اندوسیتوز از طریق کاوئولا فرایندی غیروابسته به کلاترین است. تشکیل کاوئولا از طریق پروتئین کاوئولین و همچنین «کاوین» (Cavins) انجام میشود. چهار نوع پروتئین کاوین در پستانداران وجود دارد.
- کاوین 1: نام دیگر آن PTRF است.
- کاوین 2: نام دیگر ان SDPR است.
- کاوین 3: نام دیگر آن PRKCDBP است.
- کاوین 4: اختصاصی سلولهای عضلانی است و نام دیگر آن MURC است.
از طریق اندوسیتوز کاوئولا لیگاندهایی مانند آلبومین، فاکتور حرکتی اتوکرین، «سم کزاز» (Tetanus)، «وبا» (Cholera) و ویروسهایی مانند پولیوما و SV40 وارد سلول میشوند. برای جدا کردن وزیکول پوشیده از کاوئولین نیز به پروتئین داینامین نیاز است.
نقش اسکلت سلولی در اندوسیتوز با استفاده کاوئولا
اسکلت سلولی نقش مهمی در سازماندهی و انتقال کاوئولا دارند. فیبرهای استرس اکتین روی توزیع خطی کاوئولا در غشای پلاسمایی بیشتر سلولها تاثیر میگذارند. فیبرهای استرس تنظیم شده توسط تیروزین کیناز Abl و فرمین mDIA1 نقش مهمی در سازماندهی گودال و همچنین درون بری با استفاده از کاوئولا دارند.
بازیافت کاوئولا را از طریق تثبیت موضعی میکروتوبولها توسط اینتگرین β1 و سیگنالدهی «کیناز متصل به اینتگرین» (Integrin-linked Kinase | ILK) انجام میشود. β1 اینتگرین-ILK پروتئین IQGAP1 را به کار میگیرد و همراه با mDIA1 میکروتوبولها را تثبیت می کند. از این رو، mDIA1 که اکتین و میکروتوبول ها را تنظیم میکند برای درون بری و بازیافت کاوئولا بسیار اهمیت دارد.
کاوئولا میتواند در اثر کشش غشا صاف شوند. به نظر میرسد که این پاسخ حساس مکانیکی کاوئولا علاوه بر فعال کردن پاسخهای پیامرسانی محافظ در پایین دست، از پارگی غشا نیز جلوگیری می کند.
پوتوسیتوز
«پوتوسیتوز» (Pinocytosis) نوعی درون بری وابسته به کاوئولا است که برخلاف سایر روشهای آندوسیتوز، وزیکول انتقال یافته به سلول به جای اتصال به لیزوزوم یا اندامکهای دیگر به درون سیتوزول آزاد میشوند.
تعیین مقصد وزیکول آندوسیتوزی
پس از اینکه محمولهها به شیوه آندوسیتوز وارد سلول شدند با مجموعهای از اندوزومها ترکیب میشوند. این اندوزوم امکان انتقال محمولههای اندوسیتوزی را به محفظههای مجزای غشایی (برای مثال دستگاه گلژی) فراهم میکند. در واقع شبکه اندوزومی محمولههای اندوسیتوزی را جمع آوری و دستهبندی میکند و آنها را به مقصد نهایی میفرستد. در نهایت، محمولهها را میتوان به غشای پلاسمایی بازیافت کرد، از طریق ترافیک رتروگراد به شبکه بخش ترنس دستگاه گلژی فرستاد یا برای تخریب به لیزوزوم دستهبندی کرد.
سه نوع مختلف از اندوزومها وجود دارد.
- «آندوزوم های اولیه» (Early Endosome): پس از این که وزیکول اندوسیتوزی وارد سلول شد به چندین نوع وزیکول دیگر متصل میشود و اندوزوم اولیه را تشکیل میدهد. در درون اندوزومهای اولیه، تصمیم طبقهبندی اولیه محموله اندوسیتوزی گرفته میشود و سرنوشت گیرندههای اندوسیتوز شده تعیین میشود.
اندوزوم های اولیه از شبکهای لوله ای-وزیکولی پویا تشکیل شدهاند بعضی از محمولهها با قرار گرفتن در بخش لولهای اندوزوم اولیه بازیافت میشوند و به غشای سلولی باز میگردند. - «اندوزوم های ثانویه» (Late Endosomes): اندوزومهای اولیه با روشهای مختلفی بالغ می شوند و اندوزوم ثانویه را تشکیل میدهند. یکی از مهمترین اتفاقها اسیدی شدن داخل اندوزوم به دلیل وجود و فعالیت پمپ V-ATPase است.همچنین به دلیل همجوشی هموتیپی آندوزومهای اولیه با یکدیگر معمولا اندوزومهای ثانویه بزرگتر هستند.
بخشی از محمولههای اندوسیتوزی در این مرحله از طریق جوانه زدن از اندوزوم ثانویه به سمت غشای پلاسمایی بازیافت میشوند. اندوزوم ثانویه با از دست دادن پروتئین RAB5A و بدست آوردن پروتئین RAB7A مستعد اتصال به لیزوزوم میشود. - «اندوزوم های بازیافتی» (Recycling Endosome): اندوزوم بازیافتی اندامکی در مسیر اندوسیتی هستند که در آن غشای پلاسمایی (پروتئین و لیپید) به داخل سلول آمده توسط اندوسیتوز برای استفاده مجدد به سطح سلول باز میگردند. بازیافت اندوسیتی راه اصلی سلول برای حفظ اجزای غشای پلاسمایی است.
جدا شدن گیرنده از لیگاند در وزیکول آندوسیتوزی
هنگامی که وزیکولهای اندوسیتوزی وارد سلول میشوند، در اندوزوم اولیه به سمت مقصد نهایی خود دستهبندی میشوند. مرتبسازی اندوزومی اولیه به اسیدی شدن اندوزوم و تفکیک لیگاند بستگی دارد. کمپلکس های لیگاند-گیرنده داخل اندوزوم حساسیت pH متفاوتی برای جدا شدن لیگاند از گیرنده دارند.
به عنوان مثال، گیرندههایی که قرار است به غشای پلاسمای بازیافت شوند، به طور معمول لیگاندهای خود را در pH حدود ۶٫۵ اندوزوم اولیه آزاد میکنند. این امر امکان بازیافت سریع گیرندههایی مانند گیرنده ترانسفرین یا گیرنده LDL را فراهم میکند.
وزیکولهایی که قرار است به قسمت ترنس دستگاه گلژی وارد شوند، لیگاندهای خود را در محدوده pH حدود 5٫۵ اندوزوم ثانویه آزاد میکنند. گیرنده مانوز-6-فسفات مثالی از این نوع است.
وزیکولهای اندوسیتوزی که حاوی گیرندههای پیامرسانی (به عنوان مثال، گیرنده فاکتور رشد اپیدرمی) هستند، اغلب حتی در pH پایین حدود ۴٫۵ نیز به لیگاند خود متصل و فعال باقی میمانند. جدا نشدن لیگاند از گیرنده خود باعث سیگنالدهی مداوم آن میشود تا وقتی که برای تخریب به لیزوزوم فرستاده شوند.
جمعبندی
در این مطلب تلاش کردیم که فرایند اندوسیتوز (درون بری) و مکانیسمهای دخیل در آن توضیح داده شود. به طور خلاصه اندوسیتوز به انتقال مواد خارج سلولی به داخل سلول است. اندوسیتوز میتواند به صورت اختصاصی یا غیراختصاصی انجام شود. اندوسیتوز مواد به داخل سلول با روشهای مختلفی شامل فاگوسیتوز، ماکروپینوسیتوز، FEME، کاوئولا و CLIC/GEEC انجام میشود. سلول از این روشها برای انتقال مواد بزرگی مانند باکتریها، سلولهای مرده، گیرندههای غشایی و غیره استفاده میکند. پس از این که این مواد از طریق وزیکولهای اندوسیتوزی وارد سلول شدند، توسط اندوزومها پردازش میشوند و به محل مورد نظر در سلول میرسند.













عاااالی بود لذت بردم ممنونم برای وقتی که برای نوشتن مطلب گذاشتین.
عالی بود خیلی دنبال این مطالب بودم