پروتون چیست؟ – به زبان ساده
پروتون یکی از سه ذره اصلی است که اتم را تشکیل میدهند. دو جزء دیگر را با نامهای الکترون و نوترون میشناسیم. پروتونها را میتوان در هسته اتم، یعنی ناحیهای چگال در مرکز اتم پیدا کرد. پروتون، بار الکتریکی و جرمی برابر با ۱ واحد جرم اتمی (amu) دارد. این جرم برابر با است. پروتونها به همراه نوترونها، به طور تقریبی، کل جرم یک اتم را تشکیل میدهند.
پروتون با قطر بسیار کوچک متر به طور مستقیم با خورشید به قطر ارتباط دارد. اما منظور از این ارتباط چیست؟ انرژی بسیار زیاد خورشید، ناشی از برهمکنش پروتونها است. در خورشید و سایر ستارگان، پروتونهای اتم هیدروژن، در اثر ترکیب (همجوشی)، هسته اتمهای هلیوم را تشکیل میدهند. چنین واکنشهای همجوشی، مقادیر بسیار زیادی انرژی آزاد میکنند. این واکنشها در دمای بسیار بالا همچون داخل ستارگان بوقوع میپیوندند.


پروتونهای مشابه و عنصرهای متفاوت
تمامی پروتونها با یکدیگر مشابهاند. به طور مثال، پروتونهای هیدروژن به طور دقیق با پروتونهای هلیوم یا سایر عناصر جدول تناوبی مشابه هستند. با این وجود، اتم عنصرهای مختلف، تعداد متفاوتی پروتون دارند. در حقیقت، تعداد پروتون در هر اتم، عدد منحصر به فردی است که با تعداد پروتون در اتم دیگر تفاوت دارد. به طور مثال، اتم هیدروژن تنها یک پروتون دارد درحالیکه اتم هلیوم دارای دو پروتون است.
تعداد پروتونهای یک اتم، میزان بار الکتریکی هسته را مشخص میکنند. هسته اتم همچنین شامل نوترون است اما نوترونها، بار الکتریکی خنثی دارند. به طور مثال، ۱ پروتون موجود در هسته اتم هیدروژن، بار الکتریکی را نتیجه میدهد یا اینکه در اتم هلیوم، بار الکتریکی هسته به دلیل وجود ۲ پروتون، ذکر میشود.
ماهیت پروتونها
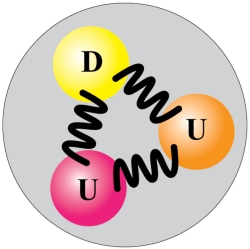
پروتونها از ذرات بنیادی موسوم به «گلوئون» (Gluon) و کوارک تشکیل شدهاند. همانطور که در تصویر زیر مشاهده میکنید، هر پروتون شامل ۳ کوارک (دایرههای رنگی) و ۳ جریان موجی از گلوئون است. دو نوع از کوارکها موسوم به کوارک «بالا» (Up) و کوارک سوم موسوم به کوارک «پایین» (Down) است. این کوارکها به ترتیب با حروف «U» و «D» نشان داده شدهاند.
گلوئونها نیروی بسیار زیاد بین کوارکها را حمل میکنند و سبب پیوند آنها به یکدیگر میشوند. با وجود اینکه پروتونها را در حدود ۱۰۰ سال پیش کشف کردند اما کشف کوارکها و لپتونها محدود به سالهای اخیر است و دانشمندان همچنان در حال بررسی این ذرات بنیادی هستند.
تاریخچه پروتون
مفهوم این ذرات هیدروژنمانند به عنوان اجزای تشکیل دهنده اتمها، از گذشتههای بسیار دور توسعه پیدا کرده است. در اوایل سال 1815، «ویلیام پرووت» (William Prout) بیان کرد که تمامی اتمها، از اتمهای هیدروژن تشکیل شدهاند که به آنها، نام «پروتیل» (Protyle) اختصاص داد.
در سال 1886، دانشمندی آلمانی به نام «اویگن گلدشتاین» (Eugen Goldstein)، با کشف اشعههای آندی نشان داد که این پرتوها، ذراتی با بار مثبت و تولید شده توسط گازها هستند. با این وجود، با توجه به اینکه ذرات گازهای مختلف، نسبت بار به جرم متفاوتی دارند، امکان شناسایی آنها به عنوان یک ذره منفرد وجود نداشت.
به دنبال کشف هسته اتم توسط ارنست رادرفورد در سال 1911، «آنتونیوس وان دن بروک» (Antonius van den Broek) پیشنهاد داد که مکان هر عنصر در جدول تناوبی (عدد اتمی آن)، معادل با بار هسته است. این امر در سال 1913 و با آزمایش طیف اشعه ایکس هنری موزلی، تایید شد.
در سال 1917، رادرفورد ثابت کرد که هسته هیدروژن، شامل هسته دیگری است که نتایج این آزمایش را معادل با کشف پروتون میدانند. این آزمایشات، بعد از این آغاز شد که رادرفورد متوجه شد زمانیکه ذرات آلفا در هوا (نیتروژن) پرتاب شوند، آشکارسازها، علائمی همچون هسته نیتروژن را نشان میدهند. بعد از این مشاهدات، رادرفورد این بار آزمایش دیگری را در نیتروژن خالص انجام داد و مشاهده کرد که اثرات حاصل از آزمایش، بیشتر هستند.
در سال 1919، رادرفورد فرض کرد که ذرات آلفا، در اثر برخورد، یک پروتون را از نیتروژن خارج و آنرا به کربن تبدیل میکنند. بعد از مشاهده تصویر «اتاقک ابر بلاکت» (Blackett's Cloud Chamber) در سال 1925، او متوجه شد که عکس این اتقاق رخ میدهد یعنی بعد از جذب ذره آلفا، یک پروتون خارج میشود و بنابراین، نه کربن، بلکه اکسیژن سنگین خواهیم داشت. و این یعنی Z افزایش پیدا نکرده بلکه کاهش پیدا کرده است. این نتایج با نام «واکنش هستهای» (Nuclear Reaction) گزارش شدند.
رادرفورد میدانست که هیدروژن سبکترین و سادهترین عنصر شناخته شده است و تحت تاثیر نظریه پرووت قرار داشت که بیان میکرد هیدروژن، سنگ بنای تمامی عناصر است. کشف اینکه هسته هیدروژن در تمام هستههای عناصر وجود دارد سبب شد تا رادرفورد، نام ویژهای به عنوان «ذره» (Particle) را برای هسته هیدروژن در نظر بگیرد چراکه او در این فکر بود که هیدروژن تنها دارای یکی از این ذرات است. او برای این ذره بنیادی، نام پروتون را در نظر گرفت. ریشه این نام نیز یونانی و به معنای «اولین» (First) بود.

پایداری پروتون
پروتون آزاد - پروتونی که با هسته یا الکترونها پیوند نداشته باشد - ذرهای پایدار به شمار میآید که تاکنون مشاهده نشده که به طور خودبهخودی به ذرات دیگری شکسته شوند. پروتونهای آزاد در محیطهایی با دما و انرژی بالا یافت میشوند چراکه در این شرایط میتوانند از الکترون، جدا باشند. همچنین، در حالت پلاسما نیز پروتونها وجود دارند. پروتونهای آزاد با انرژی و سرعت بالا، در حدود 90 درصد پرتوهای کیهانی را تشکیل میدهند. علاوه بر این، در برخی از فرآیندهای واپاشی هستهای، پروتونهای آزاد به طور مستقیم گسیل میشوند.
همانطور که گفته شد، واپاشی خودبهخودی پروتونهای آزاد تاکنون مشاهده نشده است و به همین دلیل، پروتونها را به عنوان ذراتی پایدار میشناسند. گرچه برخی مطالعات، عمر پروتون را بین تا سال ذکر کردهاند.
کوارکها و جرم پروتون
در علم «کرومودینامیک کوانتوم» (Quantum Chromodynamics) که نظریه جدید نیروی هستهای به شمار میآید، بیشتر جرم پروتونها و نوترونها به کمک «نسبیت خاص» (Special Relativity) توصیف میشود. جرم پروتون در حدود ۸۰-۱۰۰ برابر بیشتر از مجموع جرم کوارکهای سازنده آن است و برای گلوئنها نیز جرم سکون صفر در نظر گرفته میشود.
انرژی اضافی کوارکها و گلوئنها در ناحیهای با یک پروتون، در مقایسه با انرژی سکون کوارکها به تنهایی در حالت خلا «QCD»، در حدود ۹۹ درصد جرم را تشکیل میدهند. در نتیجه، «جرم سکون» (Rest Mass) پروتون برابر خواهد بود با «جرم نامتغیر» (Invariant Mass) سیستم کوارکها و گلوئنهای متحرک که ذره را میسازند و در چنین سیستمی، حتی انرژی ذرات بدون جرم نیز به عنوان بخشی از جرم سکون سیستم سنجیده میشود.
دو عبارت برای مشخص کردن جرم کوارکهای سازنده پروتون استفاده میشود:
جرم «کوارک جاری» (Current Quark) که بیانگر جرم خود کوارک است و جرم «کوارک اساسی» (Constituent Quark) که شامل جرم کوارک جاری بعلاوه جرم میدان ذرات گلوئن اطراف کوارک است. این جرمها به طور معمول، مقادیر متفاوتی دارند. با وجود اینکه گلوئنها به طور ذاتی، جرمی ندارند اما دارای انرژی هستند. جرم پروتون به طور تقریببی برابر با است که جرم سکون ۳ کوراک آن تنها برابر با خواهد بود و مابقی جرم به گلوئنها اختصاص داده میشود.
شعاع بار در پروتون
مشکلی که در توصیف شعاع اتمی وجود دارد، در بیان شعاع پروتون نیز دیده میشود و آن این است که اتمها و هسته آنها هیچکدام، مرز مشخصی ندارند. با این وجود، هسته را میتوان به صورت کرهای با بار مثبت در نظر گرفت تا بتوان آزمایشهای «پراکندگی الکترون» (Electron Scattering) را توصیف کرد. با توجه به اینکه مرز مشخصی برای هسته وجود ندارد، اگر ناظری را بر روی الکترون در نظر بگیریم، سطح مقطعهای مختلفی از پروتون را میبیند که میانگین آنرا به عنوان سطح مقطع هسته در نظر میگیرند. مقدار پذیرفته شده برای شعاع بار پروتون برابر با 0/8768 فمتومتر ذکر میشود.
فشار داخل پروتون
از آنجایی که پروتونها، از کوارکهای محصور شده توسط گلوئنها تشکیل شدهاند، فشار معادل وارد شده به کوارکها را میتوان تعریف کرد. با این کار، توزیع آنها به عنوان تابعی فاصله از مرکز، به کمک پراکندگی کامپتون الکترونها با انرژی بالا، قابل محاسبه خواهد بود. این میزان فشار، در مرکز هسته به بیشترین مقدار خود میرسد که برابر با ، یعنی بیشتر از فشار داخل یک ستاره نوترونی است.

پروتون در شیمی
مطالبی که تا اینجا مطرح شد، همگی به نوعی با علم فیزیک سروکار داشتند اما در ادامه، به بررسی این ذره در علم شیمی میپردازیم. مفاهیمی همچون عدد اتمی و یون هیدروژن از جمله مباحثی هستند که به بررسی پروتون در شیمی میپردازند.
عدد اتمی
در شیمی، به تعداد پروتون موجود در هسته اتم، عدد اتمی میگویند. این عدد اتمی به نوعی معرف جایگاه و نام یک عنصر شیمیایی در جدول تناوبی است. به طور مثال، عدد اتمی کلر برابر با ۱۷ است که یعنی اتم کلر، ۱۷ پروتون دارد و تمامی اتمها با ۱۷ پروتون، اتم کلر هستند.
خواص شیمیایی هر اتم توسط تعداد الکترونهای آن مشخص میشود که برای اتم خنثی، این مقدار برابر با تعداد پروتونهای آن خواهد بود. به طور مثال، اتم کلر خنثی، ۱۷ الکترون و ۱۷ پروتون دارد درحالیکه آنیون ، دارای ۱۷ پروتون و ۱۸ الکترون، با بار است.
تمامی اتمهای یک عنصر، لزوما با یکدیگر مشابه نیستند و ممکن است در تعداد نوترونها متفاوت باشند که این تفاوت، ایزوتوپهای مختلف یک عنصر را بوجود میآورد. همچنین، انرژیهای این اتمها نیز در صورت تفاوت، «ایزومرهای هستهای» (Nuclear Isomers) را بوجود میآورد. به طور مثال، برای اتم کلر، دو ایزوتوپ با تعداد نوترون ۱۸ و ۲۰ وجود دارد.
یون هیدروژن
عبارت پروتون را در شیمی برای بیان یون هیدروژن استفاده میکنند. با توجه به اینکه هیدروژن، عدد اتمی برابر با ۱ دارد، یک یون هیدروژن، هیچ الکترونی نخواهد داشت و تنها شامل یک هسته با یک پرتون و بدون نوترون (در بیشتر ایزوتوپهای آن) خواهد بود. پروتون، بار مثبتی است که شعاع آن به اندازه شعاع اتم هیدروژن ذکر میشود و به همین دلیل، به لحاظ شیمیایی بسیار واکنشپذیر است.
در نتیجه، پروتون آزاد، در سیستمهای شیمیایی همچون مایعات، عمر بسیار کوتاهی دارد و به سرعت با ابر الکترونی هر مولکولی واکنش میدهد. در محلولهای آبی، در اثر واکنش، یون هیدرونیوم خواهیم داشت که در اثر «حلالپوشی» (Solvation) مولکولهای آب به ترکیباتی همچون و تبدیل میشود.
انتقال در واکنشهای اسید و باز را معمولا با نام انتقال پروتون میشناسند. اسید، دهنده پروتون و باز، پذیرنده پروتون ذکر میشود. به طور مشابه نیز در بیوشیمی از عبارات «پمپ پروتون» (Proton Pump) و «کانال پروتون» (Proton Channel) برای توضیح یونهای آبدار (آبپوشیده) استفاده میشود.
دوتریوم و تریتیوم
به یونی که با حذف الکترون از اتم دوتریوم تولید میشود، به جای پروتون، دوترون میگویند. به طور مشابه نیز، با حذف الکترون از یون تریتیوم، تریتون خواهیم داشت.
رزونانس مغناطیسی هسته (NMR)
همچنین، عبارت پروتون NMR، به مشاهده هسته هیدروژن-۱ (معمولترین ایزوتوپ هیدروژن) در مولکولهای آلی و به کمک رزونانس مغناطیسی هسته (NMR) اشاره دارد.
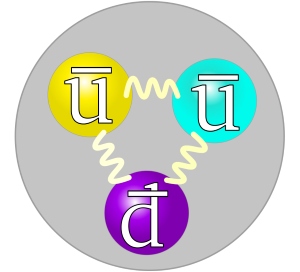
پاد پروتون
«پاد پروتون» (Antiproton)، پاد مادهای از پروتون به شماره میآید که پایداری مناسبی دارد اما عمر آن بسیار کوتاه است و در برخورد با پروتون، انرژی به صورت انفجاری آزاد میشود. برای مطالعه بیشتر پاد ماده میتوانید به مطالب «پاد هیدروژن چیست؟ — به زبان ساده» و «پاد ماده — از صفر تا صد» مراجعه کنید.












دو پروتون در چه فاصله ای نسبت بهم قرار دارند؟