شبکه سارکوپلاسمی چیست؟ – به زبان ساده + ساختار و وظیفه
«شبکه سارکوپلاسمی» (Sarcoplasmic Reticulum | SR)، نوعی تخصص یافته از شبکه آندوپلاسمی است که در سلولهای ماهیچهای دیده میشود. این اندامک غشادار یون کلسیم را مدیریت میکند. این یون برای انقباض و انبساط عضلات ضروری است. با تکیه بر عملکرد این اندامک میزان کلسیم داخل سلولی دههزار بار کمتر از میزان این یون، خارج از غشا سلولی تنظیم میشود. این اختلاف غلظت نشاندهنده این است که با کمترین افزایش در سطح غلظت کلسیم تغییرات چشمگیری در سلول رخ میدهند. در این مطلب یاد میگیریم که شبکه سارکوپلاسمی چیست و سپس به بررسی ساختار و نحوه عملکرد این اندامک سلولی و توبولهای عرضی میپردازیم.
- ساختار شبکه سارکوپلاسمی در ماهیچههای مخطط را یاد میگیرید.
- توبولهای عرضی و نقش آنها را درک میکنید.
- چگونگی شکلگیری شبکه سارکوپلاسمی را میآموزید.
- تفاوت شبکه سارکوپلاسمی در ماهیچه قلبی و اسکلتی را میشناسید.
- نقش جذب، ذخیره و آزادسازی کلسیم توسط شبکه را درک میکنید.
- مکانیسم پایان آزادسازی کلسیم و کمپلکسهای مرتبط را یاد میگیرید.


ساختار شبکه سارکوپلاسمی در ماهیچههای مخطط چیست؟
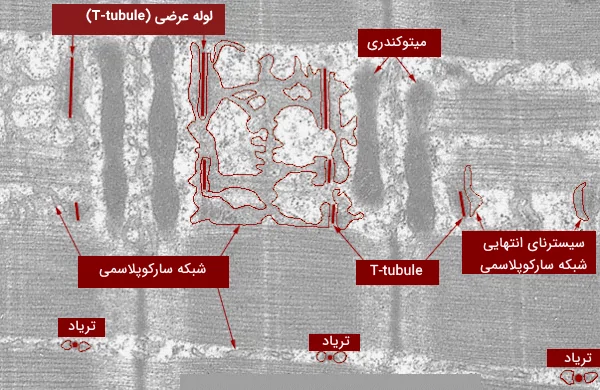
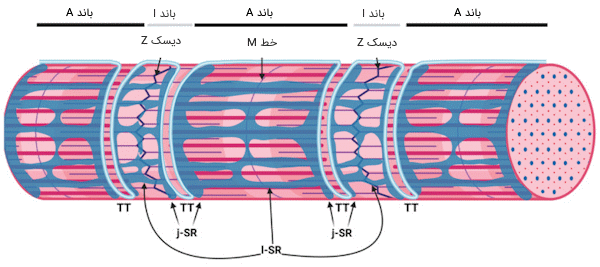
این اندامک سلولی شبکهای از «لولههایی» (Tubules) است که در سطح سلولهای عضلانی گسترده و دور میوفیبریلها پیچیده شدهاند. شبکه سارکوپلاسمی به دو بخش اصلی تقسیم میشود.
- شبکه سارکوپلاسمی طولی (Longitudinal SR):این بخش، از لولههای متعددی تشکیل شده است که به دور هر میوفیبریل میپیچند و یک شبکه را تشکیل میدهند. به بیان دیگر لولههای طولی، موازی با میوفیبریلها گسترش یافتهاند. هر لوله طولی به یک کیسهی طویل شده به نام «سیسترنای انتهایی» (Terminal Cisternae) منتهی میشود. در ماهیچههای اسکلتی پستانداران، بخش طولی SR دور باندهای A و I یک سارکومر را میپوشاند، به این ترتیب بخش اعظم شبکهی سارکوپلاسمی را تشکیل میدهد.
- شبکه سارکوپلاسمی اتصالی (Junctional SR): به محل به هم رسیدن شبکه سارکوپلاسمی و T-توبولها، «شبکه سارکوپلاسمی اتصالی» گفته میشود. این بخش محدود به محل تلاقی «A-band» و «I-band» است.
توبول های عرضی چیست؟
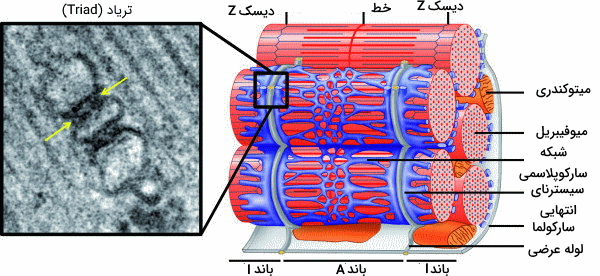
در بخش قبل گفتیم که شبکه سارکوپلاسمی چیست و ساختار آن را در ماهیچههای مخطط بررسی کردیم. اما در ادامه قصد داریم توبولهای عرضی را نیز معرفی کنیم. سلولهای ماهیچهای قلبی و اسکلتی ساختارهایی به نام «لولههای عرضی» (Transverse Tubules) دارند که به آنها «توبولهای T» نیز میگویند. منشا لولههای T، سارکولما (غشای پلاسمایی) است که به شکل لولههای عرضی به سمت مرکز سلول گسترش یافتهاند. ناحیه اتصال T توبولها با SR را با عنوان «ناحیه تریاد» (Triad Region) میشناسیم که از سه بخش تشکیل شده است.
- سیسترنای انتهایی
- لوله T
- سیسترنای انتهایی در سمت دیگر
بنابراین دو کیسهی انتهایی و یک لوله T یک ناحیه تریاد را میسازند. این ناحیه با مهیا کردن شرایط ارتباط بین گیرنده «دیهیدروپریدین» (Dihydropyridine | DHPR) و RyR1، به فیبرهای ماهیچه اسکلتی اجازه میدهد تا «کوپلینگ تحریک-انقباض» (excitation–contraction coupling) در آنها رخ دهد.
شبکه سارکوپلاسمی چگونه شکل می گیرد؟
شبکه سارکوپلاسمی در سلولهای جنینی به این شکلِ تخصصیافته، قابل مشاهده نیست و در طی رشد دستخوش تغییرات میشود. در سلولهای ماهیچهای جنینی، تجمعی نامنظم از غشاها را میبینیم که در حین رشد تبدیل به یک اندامک بسیار دقیق در سلولهای بالغ میشوند. تحقیقات in vivo و in vitro که بر پایه روش ایمونوفلورسانس انجام شدهاند، نشان دهنده فرآیندی تنظیمشده هستند که در حین آن هر دو بخش طولی و اتصالی SR سازماندهی میشوند.
در ابتدا پروتئینهای شبکه سارکوپلاسمی اتصالی مانند RyR و triadin و پروتئینهای لوله T مانند DHPR، خوشههایی مجزا در تمام سلول میسازند. هر خوشه حاوی همان پروتئینهایی است که در یک تریاد کامل میبینیم. این موضوع نشاندهنده این است که مکانیسمهای مسئول در ایجاد و نگهداری این ساختارها از همان مراحل ابتدایی رشد وجود دارند. هنگام جداسازی، این خوشهها با هم یکی میشوند تا جایی که در ناحیه مرزهای A-I از هم متمایز شوند.
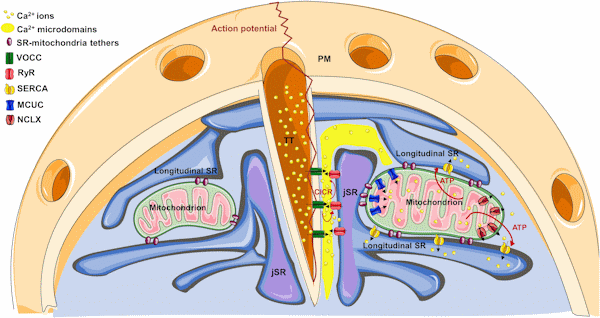
در سلولهای ماهیچه قلبی و اسکلتی تفاوت شبکه سارکوپلاسمی چیست؟
سلولهای عضله قلب همانند سلولهای عضلات اسکلتی از نوع مخطط هستند و وجود شبکه سارکوپلاسمی برای فعالیت آنها اهمیت زیادی دارد. گسترش این اندامک در سلولهای ماهیچه قلبی به اندازه سلولهای ماهیچه اسکلتی نیست. در ماهیچههای اسکلتی T توبولها در هر نقطهی اتصال بین «A-band» و «I-band» دیده میشوند، بنابراین به ازای هر «سارکومر» (یک واحد انقباضی سلول ماهیچه) دو لوله T وجود دارد. اما در ماهیچه قلب برای هر سارکومر فقط یک Tتوبول وجود دارد و آن را در هر «Z-disk» میبینیم. اگر میخواهید آشنایی بهتر و بیشتری با بافتشناسی داشته باشید، میتوانید از فیلم آموزش جامع و کاربردی بافتشناسی عمومی فرادرس استفاده کنید که لینک آن در ادامه آورده شده است.
شبکه سارکوپلاسمی در سلولهای ماهیچه صاف وجود دارد؟
در ماهیچههای صاف، شبکه سارکوپلاسمی در نزدیکی غشای سلولی قرار دارد اما تماسی بین این دو وجود ندارد. در این سلولها بخش نزدیک به غشای سلولی را «محیطی» (peripheral) و قسمتی که از غشا فاصله دارد را «مرکزی» میگوییم. بخش محیطی در هومئوستازی کلسیم، ارتباط با کانالهای یونی غشای پلاسمایی و همچنین قابلیت تحریکپذیری ایفای نقش میکند. عملکرد بخش مرکزی بیشتر به تامین کلسیم مورد نیاز میوفیلامنتها برمیگردد، بنابراین نقش مستقیمی در انقباض دارد.
تفاوت شبکه آندوپلاسمی با شبکه سارکوپلاسمی چیست؟
در سلولهای عضلانی مرز بین شبکه آندوپلاسمی زبر و شبکه آندوپلاسمی صاف مشخص نیست، همچنین مرز این بخشها با شبکه سارکوپلاسمی قابل مشاهده و تمایز نیست. با این حال با بررسیهای آزمایشگاهی و تشخیص حضور پروتئینهای گوناگونی که در بخشهای مختلف شبکه سارکوپلاسمی موجود هستند، شاید بتوان کمی به این مرزبندی نزدیک شد.
شاید برای شما سوال پیش آمده باشد که شبکههای آندوپلاسمی زبر و صاف چیست؟
آندوپلاسمی رتیکولوم بزرگترین اندامک سلولی است که وظایف متفاوتی مانند ذخیره کلسیم، سنتز پروتئین و متابولیسم لیپیدها بر عهده دارد. این شبکه که در همه سلولهای یوکاریوتی دیده میشود، دو بخش اصلی دارد:
- شبکه آندوپلاسمی زبر(خشن): علت نامگذاری این بخش به دلیل ریبوزومهای متصل به غشا آن است. اما چرا ریبوزومها به غشای شبکه آندوپلاسمی زبر میچسبند؟ اگر یک پروتئین، ترشحی یا متعلق به غشای سلولی باشد، ریبوزوم در حین ترجمهی mRNA به غشای شبکه آندوپلاسمی وصل میشود. به این ترتیب رشتهی پلیپپتیدی ساخته شده وارد فضای درونی شبکه آندوپلاسمی شده و تغییرات لازم بر روی آن اعمال میشود.
- شبکه اندوپلاسمی صاف: روی سطح این بخش، ریبوزومها متصل نیستند و به همین دلیل به این صورت نامگذاری شده است. SER مسئول ساخت لیپیدها، استروئیدها و فسفویپیدها و همچنین ذخیره کلسیم است.
البته این موضوع بیشتر در مبحث شبکه آندوپلاسمی بررسی میشود که پیشتر در مجله فرادرس راجع به آن صحبت کردهایم. اگر میخواهید اطلاعات بهتر و بیشتری در رابطه با «شبکه آندوپلاسمی» داشته باشید، پیشنهاد میکنیم، مطلب مربوط به این موضوع را مطالعه کنید.
ارتباط میتوکندری با شبکه سارکوپلاسمی
در سلولها، به جز سلولهای ماهیچهای، میتوکندری و شبکه آندوپلاسمی در هومئوستازی با یکدیگر همکاری میکنند. اخیرا بررسیهای پرتونگاری الکترونی نشان داده است که نقاط خاصی از غشای شبکه آندوپلاسمی زبر و غشای میتوکندری به یکدیگر متصل هستند. به این نقاط اتصال «غشای متصل به میتوکندری» (Mitochondria Associated Membrane | MAMs) میگویند.
غشای این دو اندامک با هم ادغام نمیشود، بلکه با فاصلهای در حدود ۱۰ الی ۲۵ نانومتر در کنار یکدیگر قرار میگیرند. در نقطهی اتصال، تعداد زیادی پروتئین و کمپلکسهای پروتئینی به عنوان متصلکننده شبکه آندوپلاسمی و غشا خارجی میتوکندری حضور دارند. اتصال بین این دو اندامک میتواند همیشگی یا مقطعی باشد.
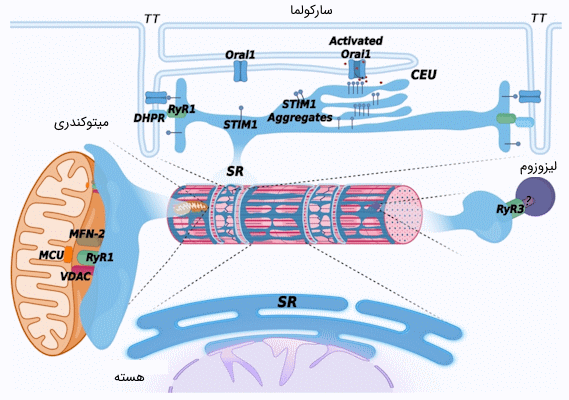
تا اینجا ما ارتباط میتوکندریها و شبکه آندوپلاسمی را بررسی کردیم اما نحوهی قرارگیری میتوکندری کنار شبکه سارکوپلاسمی چیست؟
میتوکندریها در سلولهای ماهیچهای آرایشی کاملا منظم دارند. در اوایل تولد بدون ارتباط ویژهای با SR در اطراف این شبکه پخش هستند. پس از گذشت چند هفته شبکه سارکوپلاسمی و میتوکندری با توجه به میوفیبریلها و یکدیگر، جایگیری میکنند. در ماهیچههای مخطط، میتوکندریها در فضای بین میکروفیبریلها، مجاور تریادها دیده میشوند. البته اتصال بین میتوکندری و بخش طولی شبکه سارکوپلاسمی نیز دیده شده است.
یادگیری زیست شناسی سلولی و مولکولی با فرادرس
حیات یک سلول وابسته به عملکرد درست اجزای مولکولی و اندامکهایش است. در این مطلب ما به بررسی یکی از تخصص یافتهترین اندامکهای سلولی پرداختیم. اما برای تسلط کامل بهتر است یک قدم به عقب برگردیم و سلولها را بشناسیم. سلولهای یوکاریوتی در اندامهای مختلف وظایف متفاوتی را برعهده میگیرند، بنابراین نیاز هر سلول به اندامکهای متناسب با اعمالش، بیشتر است. مثلا سلولهای ماهیچه برای منقبض شدن به شبکه سارکوپلاسمی نیاز دارند در حالی که تعداد بالای لیزوزوم برای ماکروفاژها اهمیت بیشتری دارد.
پس از شناخت انواع سلولها و اندامکهایشان، آشنایی با بافتها و اندامهای مختلف اهمیت پیدا میکند. چنانچه بخواهید این مسیر را شروع کنید و آن را اصولی پیش ببرید، فرادرس در کنار شماست.
فرادرس فیلمهای آموزشی متنوعی را در این حوزه تولید و منتشر کرده که در فهرست زیر به چند مورد اشاره کردهایم.
- فیلم آموزش مبانی و مفاهیم مقدماتی زیست شناسی سلولی و مولکولی در فرادرس
- فیلم آموزش زیست شناسی سلولی در فرادرس
- فیلم آموزش فیزیولوژی جانوری در فرادرس
- فیلم آموزش جامع و کاربردی بافت شناسی عمومی در فرادرس
- فیلم رایگان آموزش سلول و سطوح سازماندهی در فیزیولوژی جانوری ۱
اگر تمایل دارید علاوه بر افزایش دانش سلولی خود در زمینهی ژنتیک، بیوانفورماتیک و روشهای مولکولی آشنا شوید، پیشنهاد میکنیم به صفحه مجموعه فیلمهای آموزش زیستشناسی فرادرس مراجعه کنید.
فعالیت شبکه سارکوپلاسمی
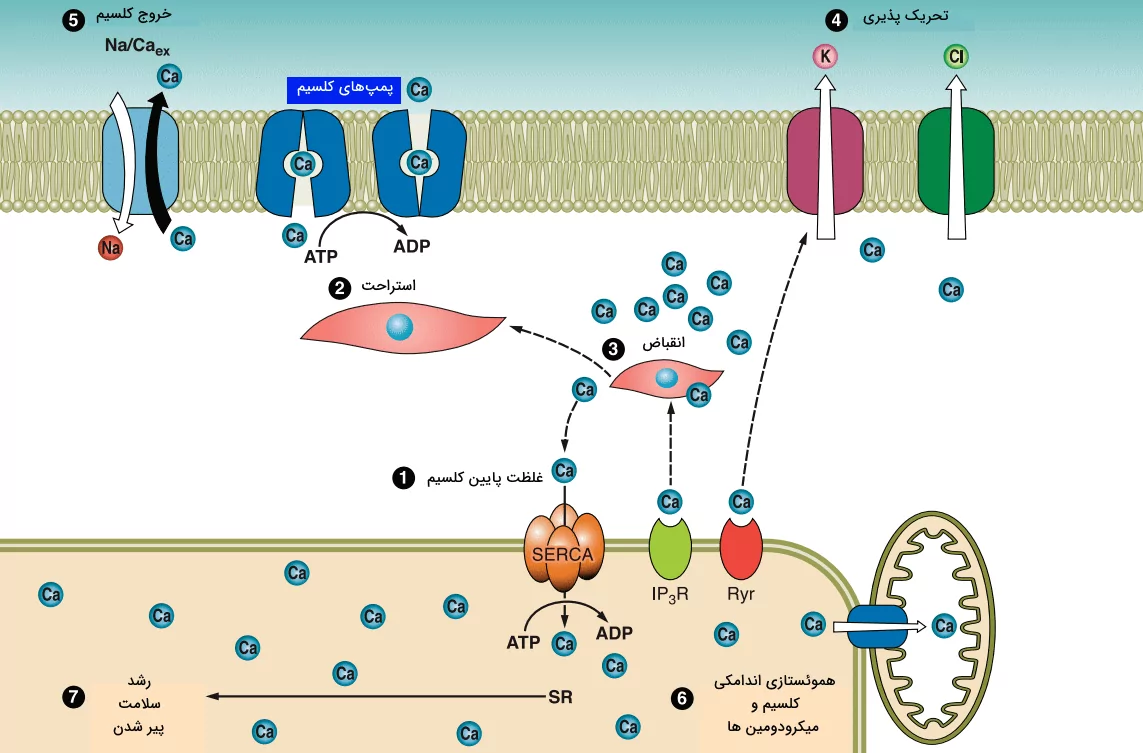
تا اینجا با ساختار این اندامک آشنایی پیدا کردیم. در این بخش به این سوال جواب خواهیم داد که فعالیت شبکه سارکوپلاسمی چیست؟ پاسخ این سوال نقش کلیدی این اندامک در انقباض عضلات را مشخص میکند. در سلولهای ماهیچهای، شبکه سارکوپلاسمی به کنترل غلظت کلسیم درونسلولی میپردازد. این اندامک کلسیم را ذخیره، ترشح و بازجذب میکند تا مراحل انقباض و استراحت ماهیچه را حفظ کند.
جذب کلسیم
در غشای شبکه سارکوپلاسمی تعدادی پمپهای یونی وجود دارند که را بر خلاف شیب غلظت از سارکوپلاسم (سیتوپلاسم در سلولهای ماهیچه) وارد این اندامک میکنند. این فرآیند با صرف انرژی همراه است که از مولکول آدنوزین تری سولفات (ATP) تامین میشود. به این پمپهای کلسیم، «Sarcoplasmic Reticulum ATPase» یا SERCA میگویند.
SERCA از ۱۳ زیرواحد تشکیل شده است که به صورت N ،P ،M1-M10 و A نامگذاری شدهاند. یون کلسیم به زیرواحدهای M1-M10 متصل میشود؛ این زیرواحدها درون غشا قرار دارند. جایگاه اتصال مولکول ATP زیر واحدهای خارج از غشای SR (N، P و A) است.
پمپ زمانی شروع به کار میکند که دو یون کلسیم همراه با یک ATP به سمت سیتوپلاسمیِ این پمپ متصل شوند. در این مرحله ATP به ADP تبدیل شده و یک گروه فسفات آزاد میشود. این فسفات با اتصال به پمپ سبب تغییر شکل فضایی آن میشود که منجر به باز شدن سمت سیتوپلاسمی پمپ میشود. به این ترتیب وارد میشود.
در نهایت سمت سیتوپلاسمی پمپ بسته و سمت شبکه آندوپلاسمی باز میشود تا یون کلسیم وارد فضای درونی SR شود. شماتیکی از این روند در تصویر زیر قابل مشاهده است.
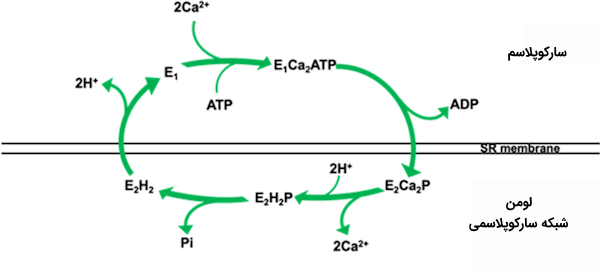
در ماهیچههای قلب، پروتئینی به نام «فسفولامبان» (PLB) وجود دارد که به SERCA متصل شده و تمایل اتصال این پمپ به را کاهش میدهد. بنابراین PLB مانع بازجذب کلسیم به SR است. اما عدم بازجذب کلسیم چه پیامدی دارد؟
باقی ماندن در سیتوپلاسم مانع مرحلهی استراحت ماهیچه میشود و در نهایت میتواند انقباض عضله را نیز کاهش دهد.
مولکولهایی مانند «آدرنالین» و «نورآدرنالین» توانایی این را دارند که از عملکرد PLB جلوگیری کنند. هنگام اتصال این هورمونها به گیرنده موجود در غشا سلولی (Beta-1 Adrenergic Receptor)، مجموعهای از واکنشها انجام میشوند که باعث تولید آنزیمی به نام «پروتئین کیناز A» یا همان PKA میشوند.این آنزیم با اضافه کردن فسفات به PLB در طی فرآیند فسفریلاسیون، مانع اتصال این پروتئین به SERCA میشود تا در نهایت ماهیچه بتواند استراحت کند.
ذخیره کلسیم
در شبکه سارکوپلاسمی، پروتئینی به نام «کلسیکوئسترین» (Calsequestrin) وجود دارد که پروتئین باند شونده به کلسیم است. این پروتئین برای ذخیره کلسیم در حین بازجذب در مرحله استراحت، ضروری است و تجمع آن را در ناحیه اتصالی شبکه سارکوپلاسمی میبینیم. کلسیکوئسترین با اتصال به حدود ۵۰ یون کلسیم ، آزاد در SR را کاهش میدهد.
انواع کلسیکوئسترین
دو نوع کلسی کوئسترین شناسایی شدهاند که در سلولهای متفاوتی وجود دارند.
- CASQ1: کلسیکوئسترین نوع یک را در سلولهای اسکلتی وجود دارد که انقباض سریعی دارند.
- CASQ2: کلسیکوئسترین نوع دو در سلولهای ماهیچه قلبی و سلولهای اسکلتی که سرعت انقباضشان کند است، حضور دارند. به این نوع، کلسیکوئسترین قلبی نیز میگویند.
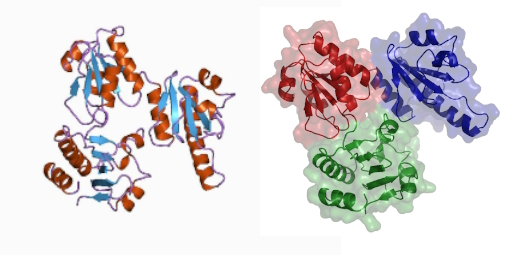
کلسیکوئسترین قلبی نقش مهمی در چرخه قلبی ایفا میکند. جهش در ژن کد کننده این پروتئین باعث آریتمی قلبی و در نهایت مرگ ناگهانی میشود. گمان میشود که CASQ2 در تنظیم زوج تحریک-انقباض قلبی و القای رهاسازی کلسیم توسط کلسیم (Calcium-Induced Calcium Release) در قلب نقش دارد.
آزاد شدن کلسیم
با توجه به نقش بسیار مهم کلسیم در انقباض سلولهای ماهیچهای شاید برای شما سوال باشد که نحوه آزاد شدن کلسیم از شبکه سارکوپلاسمی چیست؟ در این بخش پاسخ این سوال را خواهیم داد.
آزادسازی یون کلسیم از SR در سیسترنای انتهایی و توسط «گیرنده رایانودین» (Ryanodine Receptors) انجام میشود. به این فرآیند «کلسیم اسپارک» (Calcium Spark) گفته میشود. سه دسته رایانودین رسپتور وجود دارد که در نقاط مختلفی از بدن آنها را میبینیم.
- RyR1: بیشتر در سلولهای ماهیچه اسکلتی بیان میشود.
- RyR2: بیشتر در سلولهای ماهیچه قلبی بیان میشود.
- RyR3: این گیرنده بیان گسترهتری دارد، اما به طور ویژه در مغز بیان میشود.
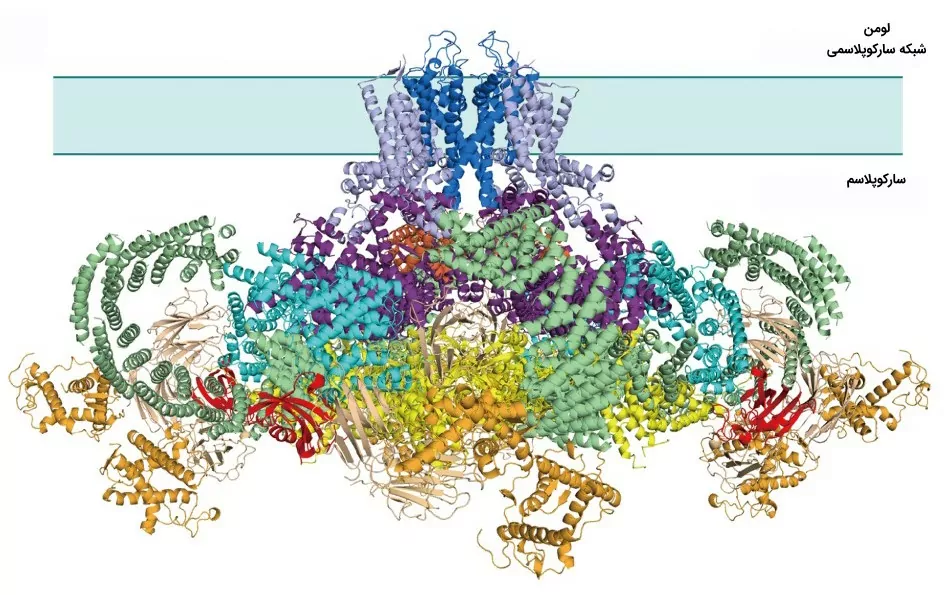
آزاد شدن کلسیم از طریق گیرندههای رایانودین در ماهیچههای مختلف به روشهای متفاوتی انجام میشود. در ماهیچههای قلبی و صاف تحریک الکتریکی (پتانسیل عمل) باعث رها شدن یون کلسیم از طریق کانال DHP میشود. کانالهای DHP را با عنوان «کانال کلسیم نوع L» نیز میشناسند که در غشا سلولی (در ماهیچههای صاف) و غشای توبول T (در ماهیچه قلبی) قرار دارند. به RyR متصل شده و آن را فعال میکند. به این ترتیب، شاهد افزایش کلسیم درون سلول هستیم. در ماهیچه اسکلتی کانال کلسیم نوع L مجاور RyR است. بنابراین فعالسازی این کانال از طریق پتانسیل عمل، مستقیما باعث فعال شدن RyR میشود. در تصویر زیر میتوانید این دو کانال را که مجاور یکدیگر قرار میگیرند ببینید. عملکرد این دو سبب انقباض ماهیچه میشود.
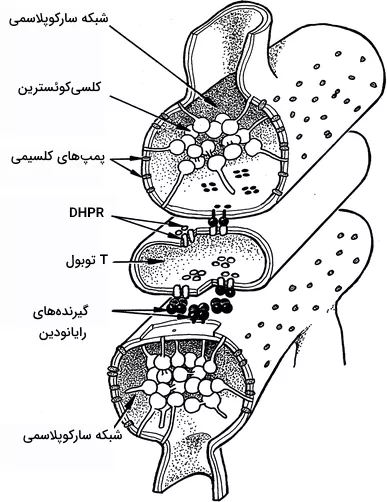
کمپلکس تریادین-جانکتین-رایانودین
«تریادین» (Triadin) و «جانکتین» (Junctin) پروتئینهایی هستند که در غشای SR مجاور RyR قرار دارند. این دو پروتئین باعث لنگر انداختن کلسیکوئسترین به گیرنده رایانودین میشوند. در شرایطی که سطح کلسیم شبکه سارکوپلاسمی از لحاظ فیزیولوژیکی نرمال است، کلسیکوئسترین به RyR، تریادین و جانکتین متصل است و به این ترتیب، RyR بسته میماند. اگر غلظت کلسیم درون SR خیلی پایین بیاید، کلسیمهای کمتری به کلسیکوئسترین متصل خواهند بود. در نتیجه، این پروتئین ظرفیت بیشتری برای اتصال به سه پروتئین نام برده دارد و اتصال محکمتری بین آنها برقرار خواهد شد. در مقابل اگر غلظت کلسیم خیلی بالا رود، ظرفیت کلسیکوئسترین برای اتصال به کمپلکس RyR-triadin-junctin کاهش مییابد و اتصال سستتری به این کمپلکس خواهد داشت. در نتیجه RyR میتواند باز شده و کلسیم را درون سلول آزاد کند.
پروتئین کیناز A که در بخش جذب کلسیم از آن صحبت کردیم، میتواند گیرنده رایانودین را هم فسفریله کند. این فسفریلاسیون موجب حساسیت بیشتر RyR میشود که نتیجه آن افزایش تعداد دفعات باز شدن کانال و بازه زمانی باز ماندن است. به این ترتیب افزایش رهاسازی کلسیم از شبکه سارکوپلاسمی و شدت انقباض را شاهد هستیم.
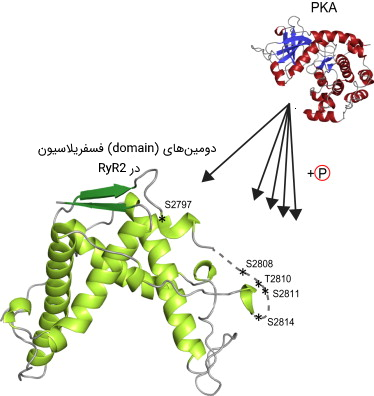
مکانیسم پایان آزادسازی کلسیم از شبکه سارکوپلاسمی چیست؟
مکانیسم پایان آزادسازی کلسیم هنوز به طور کامل شناسایی نشده است. گروهی از محققان باور دارند که گیرندههای رایانودین پس از کلسیم اسپارک غیرفعال میشوند در حالی که گروهی دیگر معتقدند که کاهش کلسیم شبکه سارکوپلاسمی باعث بسته شدن گیرنده میشود.
القای رهاسازی کلسیم توسط کلسیم
«القای رهاسازی کلسیم توسط کلسیم» (Calcium-Induced Calcium Release) یک روند زیستی را توصیف میکند که کلسیم باعث آزاد شدن از مخزنهای درون سلولی این یون ( مانند شبکه آندوپلاسمی و شبکه سارکوپلاسمی) میشود. در ابتدا این پروسه را برای ماهیچههای اسکلتی مطرح کردند، اما در حال حاضر آن را مکانیسم مسئول، در به راه انداختن آزادسازی کلسیم از SR نمیدانند. در عوض به نظر میرسد که CICR برای زوج تحریک-انقباض در ماهیچه قلب ضروری است. امروزه میدانیم که CICR یک مسیر پیامرسانی سلولی است که به صورت گسترده در بسیاری از سلولها مانند سلولهای بتای ترشحکنندهی انسولین در پانکراس، اپیتلیوم و غیره رخ میدهد.
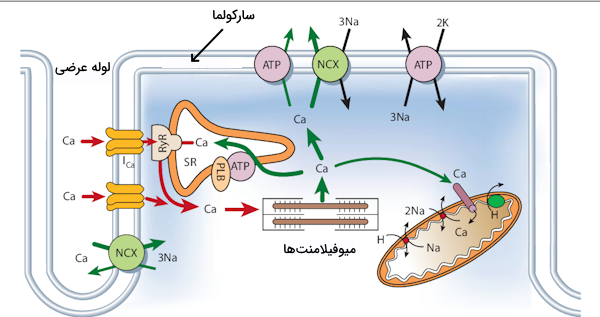
CICR در زوج (کوپلینگ) تحریک-انقباض
«زوج تحریک-انقباض» در میوکاردیوم بر دپلاریزاسیون سارکولما و سپس ورود به منظور رها کردن یون کلسیم از شبکه سارکوپلاسمی، تکیه دارد. زمانی که پتانسیل عمل غشای سلولی را دپلاریزه میکند، کانالهای وابسته به ولتاژ (مانند DHP) فعال میشوند. CICR زمانی شروع میشود که هجوم کلسیم بر گیرنده رایانودین موجود در غشای SR اثر گذاشته باشد. به این ترتیب به درون سارکوپلاسم ترشح میشود.
تاریخچه کشف شبکه سارکوپلاسمی چیست؟
اولین گزارش در مورد حضور سارکوپلاسمی رتیکولوم در سلولهای ماهیچهای با استفاده از میکروسکوپ نوری در سال ۱۹۲۰ توسط «امیلیو وراتی» (Emilio Veratti) ثبت شد. اما برای بیش از ۵۰ سال این اندامک مورد توجه محققان قرار نگرفت تا در دههی ۱۹۶۰ در پی به کارگیری میکروسکوپهای الکترونی شبکه سارکوپلاسمی توسط «پورتر» و «پالاد» ( Porter and Palade) هدف مطالعه قرار گرفت. پس از این کشف مجدد، بیوشیمی، الکتروفیزیولوژی و میکروسکوپهای الکترونی اثر مهم این اندامک را روی انقباض عضلات نشان دادند.

جمعبندی
در این مطلب از مجله فرادرس با ساختار و فعالیت شبکه آندوپلاسمی آشنا شدیم. این اندامک تخصص یافته که در سلولهای ماهیچهای دیده میشود، نقش بسیار مهمی در فرآیند انقباض ماهیچهها دارد. ذخیره، رهاسازی و بازجذب کلسیم توسط سارکوپلاسمی رتیکولوم، مراحل مختلف مدیریت یون کلسیم توسط این اندامک غشادار است.
در سلولهای ماهیچهی مخطط این شبکه را در اطراف سارکومرها میبینیم که ارتباط تنگاتنگی با لولههای عرضی در ناحیه تریاد دارند. لولههای عرضی فرورفتگیهای غشای سلولی هستند و در انتقال سریعتر و موثرتر پتانسیل عمل نقش دارند. در غشای لولههای T گیرندههای مخصوصی وجود دارند که می توانند روی گیرندههای غشای شبکه سارکوپلاسمی اثر بگذارند.
با بررسی این اندامک در ماهیچههای صاف متوجه شدیم که ساختار لولههای عرضی در این دسته از عضلات وجود ندارد. پس در این سلولها، فعالیت شبکه سارکوپلاسمی چیست؟
فعالیت این شبکه در سلولهای ماهیچه صاف همانند دیگر انواع ماهیچههاست. تفاوت اصلی آنها این است که با وجود نقش شبکه سارکوپلاسمی در انقباض سلولها، ارتباطی بین غشای سلولی و غشای شبکه سارکوپلاسمی وجود ندارد.
ارتباط میتوکندری با شبکه سارکوپلاسمی علاوه بر تامین انرژی فعالیتهای سلولی به هومئوستازی کلسیم نیز کمک میکند. این همکاری اندامکی در دیگر سلولها بین میتوکندری و شبکه آندوپلاسمی صورت میگیرد.
فعالیتهای شبکه سارکوپلاسمی را در سه سطح جذب، ذخیره و آزاد کردن کلسیم بررسی کردیم. در مرحلهی جذب کلسیم با ساختار پمپهای یونی غشای شبکه آندوپلاسمی به نام SERCA آشنا شدیم. برای بخش ذخیره کلسیم پروتئین کلسیکوئسترین را معرفی کردیم و در برای آزادسازی کلسیم گیرندههای رایانودین را شناختیم.