بیگانه خوار چیست و چه می کند؟ – به زبان ساده
بسیاری از ما با فاگوسیتوز به عنوان یک رویداد سلولی آشنا شدهایم که در آن سلولهای میزبان مرده، سلولهای میکروبی، اجزای آنها یا سایر اجسام خارجی توسط سلولهای واقعی موسوم به فاگوسیتها یا بیگانه خوار ها بلعیده شده و اغلب از بین میروند. در این مقاله به بررسی تعریف بیگانه خوارها و انواع آنها، فرایند فاگوسیتوز و تفاوتهای آن با اندوسیتوز میپردازیم.
بیگانه خوار چیست؟
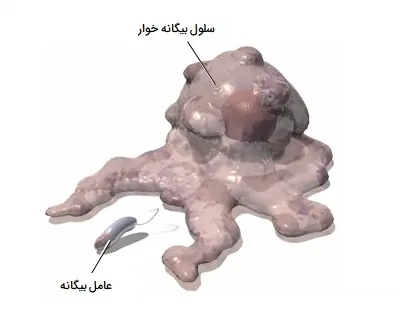
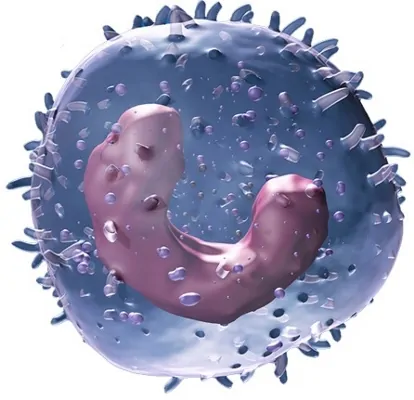
فاگوسیت یا بیگانه خوار نوعی گلبول سفید است که به بدن انسان کمک میکند تا با عفونت مبارزه کرده و سلولهای پیکری مرده یا در حال مرگ را دفع کند. این سلولها توانایی بلع و گاهی هضم ذرات خارجی مانند باکتری، کربن، غبار یا رنگ را دارد. بیگانه خوار ها اجسام خارجی را با گسترش سیتوپلاسم خود به پاهای کاذب خود (پسوندهای سیتوپلاسمی شبیه پا)، احاطه کردن ذره خارجی و تشکیل یک واکوئل میبلعند.
این سلولها به پاتوژنها متصل میشوند و آنها را در یک فاگوزوم وارد میکند که اسیدی شده و با لیزوزومها ترکیب میشود تا محتویات را از بین ببرد. بیگانه خوار ها جزء کلیدی سیستم ایمنی ذاتی هستند. سه گروه اصلی بیگانه خوار ها شامل مونوسیتها و ماکروفاژها، گرانولوسیتها و سلولهای دندریتیک که همگی عملکرد کمی متفاوت در بدن دارند.
بسیاری از گلبولهای سفید و برخی از سایر سلولهای بدن از فاگوسیتوز برای بلعیدن و از بین بردن سلولها استفاده میکنند. سلولهای بیگانه خوار واقعی سلولهای حرفهای مجهز به مولکولهای گیرنده هستند که به سمت مواد شیمیایی خاصی که وجود عفونت را نشان میدهند جذب میشوند. یکی از نقشهای مهم بیگانه خوار ها دفع سلولهایی است که تحت آپوپتوز یا مرگ برنامهریزی شده سلولی قرار گرفتهاند. سلولهای مرده یا در حال مرگ توسط فاگوسیتهای غیراختصاصی دفع میشوند.
سلولها سیگنالهای شیمیایی ارسال میکنند که به بیگانه خوار اجازه میدهد تا از بین رفتن آنها را تشخیص دهد، بنابراین فاگوسیتها میتوانند سلولهای در حال مرگ را با استفاده از فاگوسیتوز بخورند. بیگانه خوار های واقعی نیز از فاگوسیتوز برای دفع باکتریها و سایر میکروبها استفاده میکنند.
فاگوسیتوز یا بیگانه خواری چیست؟
فاگوسیتوز فرآیندی است که در آن یک سلول به بخش خاصی روی سطح سلول مورد نظر متصل میشود و در حالی که اطراف آن را میگیرد، آن را به سمت داخل میکشد. فرآیند بیگانه خواری اغلب زمانی اتفاق میافتد که سلول تلاش میکند چیزی مانند یک ویروس یا یک سلول آلوده را از بین ببرد و این واکنش توسط اغلب سلولهای سیستم ایمنی استفاده میشود. فاگوسیتوز با سایر روشهای اندوسیتوز متفاوت است، زیرا بسیار ویژه بوده و بستگی به این دارد که سلول بتواند از طریق گیرندههای سطح سلولی به مادهای که میخواهد ببلعد بپیوندد. فاگوسیتوز اتفاق نمیافتد مگر اینکه سلول در تماس فیزیکی با ذرهای باشد که قصد بلعیدن آن را دارد.
بیگانه خواری چگونه انجام می شود؟
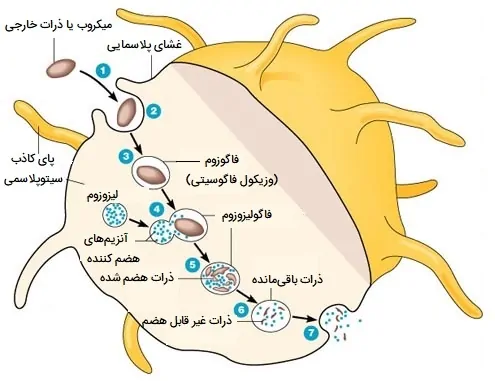
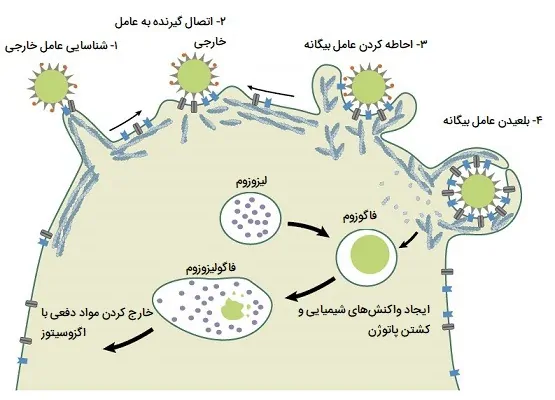
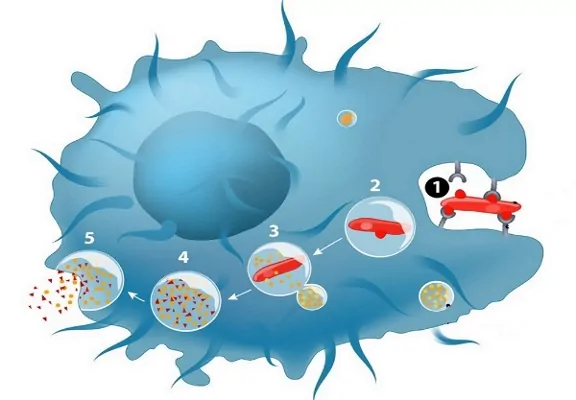
بیگانه خواری فرآیندی است که طی آن سلول بیگانه خوار یک پاتوژن یا بقایای سلولی را میبلعد. این میتواند تقریباً در هر بافتی، اغلب در جریان خون و فضای بین بافتی، همچنین آلوئولهای ریهها و پارانشیم سایر ارگانهای اصلی بدن رخ دهد. فاگوسیتوز معمولی در طی چند مرحله رخ میدهد که در ادامه آنها را توضیح دادهایم.
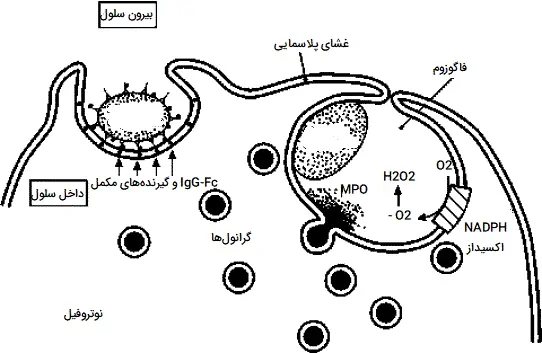
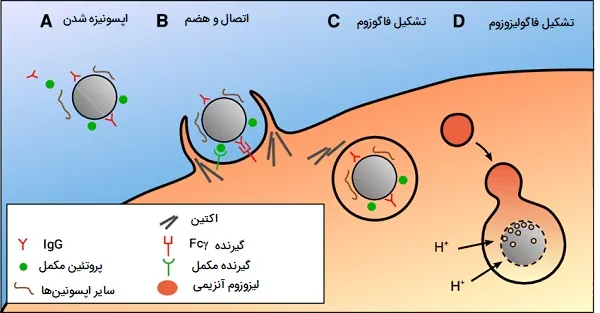
- یک گیرنده روی غشای سلولی بیگانه خوار به یک ذره خارجی مانند یک میکروب بیماریزا یا یک سم متصل میشود. گیرنده Fc به طور معمول گیرنده مورد استفاده است و به آنتیبادیهایی متصل میشود که یک پاتوژن یا سم را اپسونیزه کرده اند. اپسونیزه شدن فرایندی است که در آن از اپسونین (یک نوع آنتیبادی) برای برچسبگذاری پاتوژنها جهت نابودی توسط بیگانه خوار ها استفاده میشود.
- سلول بیگانه خوار سیتوپلاسم پاتوژن متصل شده را از طریق اندوسیتوز احاطه کرده و میبلعد.
- پاتوژن غرق شده در واکوئلی به نام فاگوزوم نگهداری میشود که سپس به لیزوزومهای داخل سلول متصل میشود.
- یک سری واکنشهای شیمیایی به نام انفجار اکسیداتیو رخ میدهد که از گونههای فعال اکسیژن و اکسیداز NADPH برای آسیب رساندن و کشتن پاتوژن از طریق استرس اکسیداتیو استفاده میکند. استرس اکسیداتیو میتواند یک سلول را از طریق آسیب DNA، غشای سلولی یا میتوکندری از بین ببرد.
- بقایای پاتوژن توسط اگزوسیتوز سلول بیگانه خوار دفع میشود.
در گلبول سفید بیگانه خوار تعداد کدام اندامک بیشتر است؟
در سلولهای بیگانه خوار تعداد لیزوزومها که از اجزای سلولی مهم هستند بیشتر است اما علت آن چیست؟ برای پاسخ به این سوال، اولین چیزی که باید بدانید عملکرد لیزوزوم است. لیزوزومها اندامکهای متصل به غشاء هستند که به عنوان معده سلولهای یوکاریوتی عمل میکنند. آنها حاوی حدود پنجاه آنزیم مختلف هستند که انواع مولکولهای بیولوژیکی از جمله پروتئینها، اسیدهای نوکلئیک، لیپیدها و کربوهیدراتها را تجزیه میکنند. سلولها مواد خورده شده توسط سلول را به لیزوزومها منتقل میکنند، این مواد توسط آنزیمها هضم میشوند و مولکولهای هضم شده برای استفاده توسط سلول به داخل سیتوزول منتقل میشوند. هم مواد خارج سلولی که توسط اندوسیتوز وارد سلول میشوند و هم مواد داخل سلولی قدیمی در لیزوزوم تجزیه میشوند.
ما میدانیم که سلولهای بیگانه خوار با بلع ذرات مضر خارجی، باکتریها و سلولهای مرده یا در حال مرگ از بدن محافظت میکنند. اگر وجود لیزوزوم در یک سلول زیاد باشد، به این معنی است که سلول به طور منظم در معرض ورود ذرات خارجی به داخل بدنه سلولی است. این ذرات خارجی میتوانند آنتیژن، ویروس، باکتری و غیره باشند. سلولهای بیگانه خوار اغلب در مبارزه با چنین مواد خارجی نقش دارند. این مواد در چنین سلولهایی به لیزوزومها میروند که در آنجا آنزیمها ذرات را هضم میکنند. از این رو، لیزوزومها در سلولهای فاگوسیتی (بیگانه خوار) غالبتر از غیر فاگوسیتی هستند.
اندوسیتوز چیست؟
اندوسیتوز فرآیندی است که در آن مواد و مایعات از طریق محصور کردن آنها در وزیکولها به داخل سلول وارد میشود. محصور شدن مواد توسط ناحیهای از غشای پلاسمایی صورت میگیرد که با تشکیل یک وزیکول به داخل سلول میچسبد. سه شکل اندوسیتوز عبارتند از فاگوسیتوز، پینوسیتوز و اندوسیتوز با واسطه گیرنده. بنابراین، فاگوسیتوز شامل جذب موادی مانند مواد جامد بزرگ است در حالی که پینوسیتوز بر اساس جذب مایعات همراه با املاح آن است.
تفاوت فاگوسیتوز و اندوسیتوز چیست؟
هم اندوسیتوز و هم فاگوسیتوز دو مکانیسمی هستند که در انتقال مواد به داخل سلول نقش دارند. تفاوت کلیدی بین اندوسیتوز و فاگوسیتوز در این است که اندوسیتوز فرآیند ورود ماده به داخل سلول با تشکیل وزیکولهای غشای سلولی بوده در حالی که فاگوسیتوز فرآیند ورود مواد جامد بزرگ به داخل سلول با تشکیل فاگوزوم است. همانطور که بیان شد اندوسیتوز سه دسته است. در میان این سه دسته فاگوسیتوز و پینوسیتوز دو نوع شایع هستند، بنابراین، فاگوسیتوز نوعی اندوسیتوز است. در طی هر دو مکانیسم، مواد به داخل وزیکولها وارد میشوند. این مواد شامل بقایای سلولی، آنزیمها، سلولهای مرده، پاتوژنها، هورمونها، مواد مغذی و غیره هستند. مکانیسم مخالف اندوسیتوز اگزوسیتوز است که شامل حذف مواد از سلول محصور در وزیکولها میشود.
انواع بیگانه خوار ها
گروههای زیادی از فاگوسیتها در بدن وجود دارد و هر کدام دارای عملکردهای تخصصی متفاوتی هستند که شامل فاگوسیتوز نیز میشود. بیشتر بیگانه خوار ها از سلولهای بنیادی در مغز استخوان مشتق میشوند. انواع اصلی فاگوسیتها مونوسیتها، ماکروفاژها، نوتروفیلها، سلولهای دندریتیک بافتی و ماست سلها هستند. سلولهای دیگر، مانند سلولهای اپیتلیال و فیبروبلاستها نیز ممکن است در فاگوسیتوز شرکت کنند، اما فاقد گیرندههایی برای شناسایی پاتوژنهای اپسونیزه (وچود اپسونین در سطح سلول) شده هستند و در اصل سلولهای سیستم ایمنی نیستند. در ادامه انواع سلولهای بیگانه خوار اصلی و فرعی را بررسی میکنیم.
بیگانه خوارهای اصلی
بیگانه خوار های انسان و سایر مهرهداران آروارهدار بر اساس کارایی که در فاگوسیتوز شرکت میکنند به دو گروه اصلی (حرفهای) و «فرعی» (غیرحرفهای) تقسیم میشوند. فاگوسیتهای حرفهای مونوسیتها، ماکروفاژها، نوتروفیلها، سلولهای دندریتیک بافتی و ماست سلها هستند. یک لیتر خون انسان حاوی حدود شش میلیارد فاگوسیت است. در ادامه انواع سلولهای بیگانه خوار اصلی را بررسی کردهایم.
مونوسیت ها
مونوسیتها نوعی بیگانه خوار هستند که در گردش خون یافت میشوند. آنها در اطراف بدن گردش میکنند و هنگامی که بافتی عفونی یا ملتهب میشود ممکن است جریان خون را ترک کرده و وارد بافت شوند. این سلولها در مغز استخوان رشد میکنند و در خون به بلوغ میرسند. مونوسیتهای بالغ دارای هستههای بزرگ، صاف و لوبدار و سیتوپلاسم فراوانی هستند که حاوی گرانول است، اما از نظر فنی گرانولوسیت در نظر گرفته نمیشوند. مونوسیتها مواد خارجی یا خطرناک را میبلعند و آنتیژن را به سلولهای دیگر سیستم ایمنی بدن ارائه میکنند.
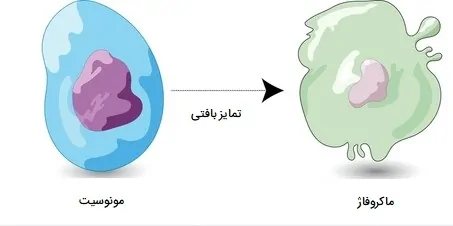
مونوسیتها در بافت به ماکروفاژها متمایز میشوند که جمعیت اصلی فاگوسیتها را در بافتهای طبیعی تشکیل میدهند. مونوسیتها بزرگترین نوع فاگوسیتها هستند که در زیر میکروسکوپ، هستهای به شکل لوبیا دارند. این سلول های بیگانه خوار دو گروه تشکیل میدهند: یک گروه در گردش و یک گروه حاشیهای که در بافتهای دیگر باقی میمانند (تقریباً 70 درصد از آنها در گروه حاشیه بافتی هستند). اکثر مونوسیتها پس از 20 تا 40 ساعت جریان خون را ترک میکنند تا به بافتها و اندامها بروند. در طی این فرآیند، آنها بسته به سیگنالهایی که دریافت میکنند به ماکروفاژها یا سلولهای دندریتیک تمایز مییابند.
ماکروفاژ چیست؟
ماکروفاژها بیگانه خوارهایی هستند که از مونوسیتها مشتق شده و در بافتها یافت میشوند. آنها به عنوان اولین مکانیسم دفاعی در فاگوسیتوز بقایای سلولی، میکروبها و هر ماده خارجی دیگر نقش اساسی دارند. ماکروفاژها میتوانند از مونوسیتها، سلولهای بنیادی گرانولوسیتی یا تقسیم سلولی ماکروفاژهای از قبل موجود، منشأ گرفته باشند. ماکروفاژها گرانول ندارند (دانهدار نیستند)، اما حاوی لیزوزومهای زیادی هستند. آنها در سراسر بدن تقریبا در تمام بافتها و اندامها یافت شده، اما به ندرت در جریان خون یافت میشوند.
ماکروفاژها از طریق تولید اینترلوکین یک (IL-1)، اینترلوکین شش (IL-6) و TNF - آلفا باعث التهاب میشوند. ماکروفاژها به روشهای مختلفی از جمله توسط سلولهای T، سیتوکینهایی مانند IFN - گاما یا ترکیبات مشتق شده از پاتوژن مانند سموم LPS از باکتریها فعال میشوند. در طول التهاب، حدود 72 ساعت پس از پاسخ اولیه برای پاکسازی زبالهها و نوتروفیلهای مرده، این بیگانه خوار ها وارد عمل میشوند. ماکروفاژها ممکن است بسته به محل آنها نامگذاری متفاوتی داشته باشند: میکروگلیا در سیستم عصبی مرکزی وجود دارد و سلولهای کوپفر ماکروفاژهای موجود در کبد هستند.
سلول های دندریتیک یا دارینه ای
عملکرد اصلی سلولهای دندریتیک به عنوان پیوندی بین سیستم ایمنی ذاتی و اکتسابی است. سلولهای دندریتیک سلولهای اختصاصی ارائهدهنده آنتیژن هستند که دارای برآمدگیهای طویلی به نام دندریت یا دارینه هستند، که به بلعیدن میکروبها و سایر مهاجمان کمک میکنند. سلولهای دندریتیک در بافتهایی که با محیط خارجی در تماس هستند، عمدتاً پوست، پوشش داخلی بینی، ریهها، معده و رودهها وجود دارند.
این سلولها به عنوان سلولهای دندریتیک نابالغ در جریان خون حرکت کرده، از طریق بافتها مهاجرت میکنند و به طور مداوم از پاتوژنهایی که از طریق نوعی اندوسیتوز شامل جذب غیر اختصاصی مواد خارج سلولی مانند مولکولهای محلول، آنها را گیر میاندازند نمونهبرداری میکنند. به دنبال فاگوسیتوز، سلول بالغ میشود و به یک اندام لنفاوی محیطی مانند غدد لنفاوی، طحال یا بافت لنفاوی مرتبط با روده مهاجرت میکند تا آنتیژن را به سلول T ارائه کند. سپس سلول T را برای شروع یک پاسخ ایمنی اکتسابی فعال میکند.
سلولهای دندریتیک بالغ سلولهای کمکی T و سلولهای T سیتوتوکسیک را فعال میکنند. سلولهای کمکی T فعالشده با ماکروفاژها و سلولهای B برهمکنش میکنند تا آنها را به نوبه خود فعال کنند. علاوه بر این، سلولهای دندریتیک میتوانند بر نوع پاسخ ایمنی ایجادشده تأثیر بگذارند. هنگامی که آنها به مناطق لنفوئیدی (که در آن سلولهای T نگهداری میشوند) سفر میکنند، میتوانند سلولهای T را فعال کنند، که سپس به سلولهای T سیتوتوکسیک یا سلولهای T کمکی تمایز مییابند. سلولهای دندریتیک را میتوان با وجود برآمدگیهای سیتوپلاسمی متعدد از سطح آنها تشخیص داد، که به آنها نسبت سطح به حجم زیادی میدهد و به تماس نزدیک با چندین سلول کمک میکند. این زائدههای سلولی شبیه به دندریتهای نورونها هستند که نام سلولهای دندریتی را از دندریت سلولهای عصبی گرفتهاند.
ماست سل ها
ماست سلها گیرندههای Toll مانند دارند و با سلولهای دندریتیک، سلولهای B و سلولهای T برای کمک به عملکردهای ایمنی اکتسابی تعامل دارند. ماست سلها مولکولهای MHC کلاس II را بیان میکنند و میتوانند در ارائه آنتیژن شرکت کنند. با این حال، نقش ماستسل در ارائه آنتیژن به خوبی درک نشده است.
ماست سلها میتوانند باکتریهای گرم منفی (مانند سالمونلا) را مصرف کرده و از بین ببرند و آنتیژنهای آنها را پردازش کنند. این سلولهای بیگانه خوار در پردازش پروتئینهای فیمبریال (نوعی پروتئین روی سطح باکتریها که در چسبندگی به بافتها نقش دارند) تخصص دارند. علاوه بر این عملکردها، ماست سلها سیتوکینهایی مانند هیستامین را تولید میکنند که در گرانولهای خود نگهداری میشوند، در هنگام شناسایی یک پاتوژن باعث ایجاد پاسخ التهابی میشود. به دلیل این عملکرد، پاسخهای التهابی آلرژیک زمانی رخ میدهد که ماست سل به آنتیژنی حساس شود که معمولاً به آن واکنش نشان نمیدهد. این یک بخش حیاتی از تخریب میکروبها است زیرا سیتوکینها فاگوسیتهای بیشتری را به محل عفونت جذب میکنند.

نوتروفیل ها
نوتروفیلها به طور معمول در جریان خون یافت میشوند و فراوانترین نوع فاگوسیتها هستند که 50 تا 60 درصد از کل گلبولهای سفید در گردش را تشکیل میدهند. یک لیتر خون انسان حاوی حدود پنج میلیارد نوتروفیل است، که قطر آنها حدود 10 میکرومتر است و تنها حدود پنج روز زنده میمانند. پس از این که آنها سیگنالهای مناسب را دریافت کردند، حدود 30 دقیقه طول میکشد تا خون را ترک کنند و به محل عفونت برسند. نوتروفیلها بیگانه خوار های فعالی هستند و به سرعت مهاجمان پوشیده از آنتیبادیها، مکملها و سلولهای آسیبدیده یا بقایای سلولی را در خود میگیرند. این سلولهای بیگانه خوار به خون باز نمیگردند، تبدیل به سلولهای چرکی شده و میمیرند.
نوتروفیلهای بالغ کوچکتر از مونوسیتها بوده و دارای یک هسته تقسیمبندی شده با چندین بخش هستند. هر بخش توسط رشتههای کروماتین به هم متصل میشود، نوتروفیلها میتوانند 2 تا 5 بخش داشته باشند. این سلولهای بیگانه خوار معمولاً تا زمان بلوغ از مغز استخوان خارج نمیشوند، اما در طول عفونت، پیش سازهای نوتروفیل به نام متامیلوسیت، میلوسیت و پرومیلوسیت آزاد میشوند. گرانولهای درون سلولی نوتروفیل انسانی مدتهاست که به دلیل خاصیت تخریب پروتئین و کشنده بودن برای باکتریها شناخته شدهاند.
این سلولهای بیگانه خوار میتوانند محصولاتی ترشح کنند که مونوسیتها و ماکروفاژها را تحریک کنند. ترشحات نوتروفیل باعث افزایش فاگوسیتوز و تشکیل ترکیبات اکسیژن فعال در کشتن داخل سلولی میشود. ترشحات گرانولهای اولیه نوتروفیلها، انجام فاگوسیتوز باکتریهای پوششدار شده با آنتی بادی IgG را تحریک میکنند. هنگام مواجهه با باکتریها، قارچها یا پلاکتهای فعالشده، ساختارهای کروماتین شبکه مانندی به نام تلههای خارج سلولی نوتروفیل (NETs) تولید میکنند. NET ها که عمدتاً از DNA تشکیل شدهاند، با فرآیندی به نام نتوزیس باعث مرگ میشوند، پس از اینکه پاتوژنها در NET ها به دام افتادند، توسط مکانیسمهای اکسیداتیو و غیر اکسیداتیو کشته میشوند.
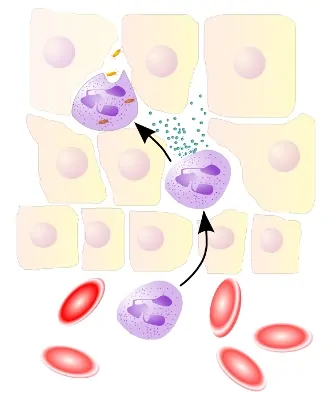
عملکرد سلول های بیگانه خوار اصلی
همه بیگانه خوار ها و به خصوص ماکروفاژها در درجاتی از آمادگی وجود دارند. ماکروفاژها معمولاً در بافتها نسبتاً خفته هستند و به آرامی تکثیر میشوند. در این حالت نیمه استراحت، سلولهای میزبان مرده و سایر بقایای غیر عفونی را پاک میکنند و به ندرت در ارائه آنتیژن شرکت میکنند. دو مرحله اصلی فعالسازی و مهاجرت از بافتها برای بیگانه خوارهای اصلی وجود دارد که در ادامه به هر دو میپردازیم.
فعالسازی
در طول عفونت، بیگانه خوارهای اصلی سیگنالهای شیمیایی که معمولاً اینترفرون گاما است را دریافت میکنند این مرحله تولید مولکولهای MHC II را افزایش میدهد و آنها را برای ارائه آنتیژن آماده میکند. در این حالت، ماکروفاژها ارائه دهنده آنتیژن و قاتلان خوبی هستند. اگر آنها سیگنالی را مستقیماً از مهاجم دریافت کنند، «بیش فعال» (hyperactivated) میشوند، تکثیر متوقف میشوند و روی کشتن تمرکز میکنند. اندازه و سرعت فاگوسیتوز آنها افزایش مییابد و برخی از آنها به اندازهای بزرگ میشوند که تکسلولیهای مهاجم را به طور کامل ببلعند.
مهاجرت
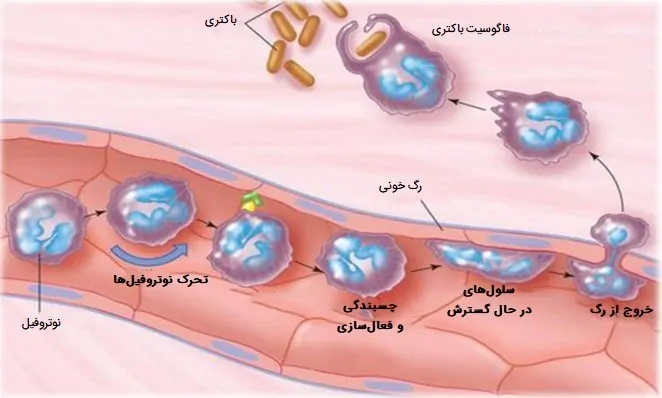
هنگامی که عفونت رخ میدهد، یک سیگنال شیمیایی SOS برای جذب بیگانهخوارهای اصلی به محل ارسال میشود. این سیگنالهای شیمیایی ممکن است شامل پروتئینهایی از باکتریهای مهاجم، پپتیدهای سیستم انعقادی، محصولات مکمل و سیتوکینهایی باشد که توسط ماکروفاژهای واقع در بافت نزدیک محل عفونت منتشر شدهاند. گروه دیگری از جذب کنندههای شیمیایی سیتوکینها هستند که نوتروفیلها و مونوسیتها را از خون جذب میکنند. برای رسیدن به محل عفونت، بیگانه خوار ها جریان خون را ترک کرده و وارد بافتهای آسیبدیده میشوند. سیگنالهای ناشی از عفونت باعث میشود سلولهای اندوتلیال که رگهای خونی را پوشاندهاند، پروتئینی به نام سلکتین بسازند که نوتروفیلها هنگام عبور به آن میچسبند.
سیگنالهای دیگری به نام گشادکنندههای عروق، اتصالات سلولهای اندوتلیال را شل میکند و به بیگانه خوار ها اجازه میدهد از دیواره عبور کنند. کموتاکسی فرآیندی است که طی آن فاگوسیتها بوی سیتوکین را به سمت نقطه آلوده دنبال میکنند. نوتروفیلها از طریق اندامهای پوشیده از سلولهای اپیتلیال به محلهای عفونت میروند و اگرچه مهاجرت بیگانه خوار ها یکی از اجزای مهم مبارزه با عفونت است اما خود میتواند منجر به علائم شبیه به بیماری شود. در طول عفونت، میلیونها نوتروفیل از خون جذب میشوند، اما پس از چند روز میمیرند.
سلول های بیگانه خوار فرعی
سلولهای در حال مرگ و موجودات خارجی توسط سلولهایی غیر از فاگوسیتهای اصلی مصرف میشوند. این سلولها شامل سلولهای اپیتلیال، سلولهای اندوتلیال، فیبروبلاستها و سلولهای مزانشیمی هستند. به دلیل این که تأکید شود وظیفه اصلی این سلولها بیگانه خواری نیست آنها را فاگوسیتهای فرعی نامیدهاند. برای مثال، فیبروبلاستها که میتوانند کلاژن را در فرآیند بازسازی اسکار فاگوسیتوز کنند، برای بلع ذرات خارجی نیز تلاش میکنند.
فاگوسیتهای فرعی از نظر نوع ذرات محدودتر از فاگوسیتهای اصلی هستند. این به دلیل کمبود گیرندههای فاگوسیتیک کارآمد، به ویژه اپسونینها (که آنتیبادیها و مکملهای متصل به مهاجمان توسط سیستم ایمنی هستند) است. علاوه بر این، بیشتر فاگوسیتهای فرعی در پاسخ به فاگوسیتوز، مولکولهای حاوی اکسیژن فعال تولید نمیکنند. در جدول زیر بیگانه خوار های فرعی بافتهای مختلف نشان داده شدهاند.
| مکان اصلی | انواع ظاهری |
| خون، لنف و گرههای لنفی | لنفوسیتها |
| خون، لنف و گرههای لنفی | سلولهای کشنده طبیعی (NK) و لنفوسیتهای دانهدار بزرگ (LGL) |
| خون | ائوزینوفیلها و بازوفیلها |
| پوست | سلولهای اپیتلیال |
| رگهای خونی | سلولهای اندوتلیال |
| بافت پیوندی | فیبروبلاست |
انواع بیگانه خواری
کشتن میکروبها یک عملکرد حیاتی بیگانه خوار ها است که یا در داخل سلول فاگوسیت (کشتن درون سلولی) یا خارج از از آن (کشتن خارج سلولی) انجام میشود. در ادامه انواع روشهایی که توسط سلولهای بیگانه خوار برای از بین بردن عوامل بیگانه استفاده میشود را بررسی میکنیم.
کشتن درون سلولی وابسته به اکسیژن
هنگامی که سلول بیگانه خوار باکتری (یا هر ماده دیگری) را میبلعد، مصرف اکسیژن آن افزایش مییابد. افزایش مصرف اکسیژن در سلول بیگانه خوار که انفجار تنفسی نامیده میشود، مولکولهای فعال حاوی اکسیژن تولید میکند که ضد میکروبی هستند. ترکیبات اکسیژندار هم برای مهاجم و هم برای خود سلول سمی هستند، بنابراین در محفظههای داخل سلول نگهداری میشوند. این روش کشتن میکروبهای مهاجم با استفاده از مولکولهای فعال حاوی اکسیژن به عنوان کشتار درون سلولی وابسته به اکسیژن شناخته میشود که دو نوع از آن وجود دارد.
- نوع اول تولید یک سوپراکسید وابسته به اکسیژن است که یک ماده کشنده باکتری غنی از اکسیژن است. سوپراکسید توسط آنزیمی به نام سوپراکسید دیسموتاز به پراکسید هیدروژن و اکسیژن منفرد تبدیل میشود. سوپراکسیدها همچنین با پراکسید هیدروژن واکنش داده و رادیکالهای هیدروکسیل تولید میکنند که به کشتن میکروب مهاجم کمک میکند.
- نوع دوم شامل استفاده از آنزیم میلوپراکسیداز (MPO) از گرانولهای (دانههای) نوتروفیل است. هنگامی که گرانولها با فاگوزوم ترکیب میشوند، میلوپراکسیداز در فاگولیزوزوم آزاد میشود و این آنزیم از پراکسید هیدروژن و کلر برای ایجاد هیپوکلریت، استفاده میکند.
کشتن درون سلولی مستقل از اکسیژن
بیگانه خوار ها همچنین میتوانند میکروبها را با روشهای مستقل از اکسیژن بکشند، اما این روشها به اندازه روشهای وابسته به اکسیژن موثر نیستند. اولین مورد از پروتئینهای دارای بار الکتریکی استفاده میکند که به غشای باکتری آسیب میزند. نوع دوم از لیزوزیمها استفاده میکند، این آنزیمها دیواره سلولی باکتری را تجزیه میکنند. نوع سوم از لاکتوفرینها استفاده میکند که در گرانولهای نوتروفیل وجود دارد و آهن ضروری را از باکتریها حذف میکند. نوع چهارم از پروتئازها و آنزیمهای هیدرولیتیک استفاده میکند. این آنزیمها برای هضم پروتئینهای باکتریهای تخریبشده استفاده میشوند.
روش کشتن خارج سلولی
اینترفرون گاما (که زمانی فاکتور فعالکننده ماکروفاژ نامیده میشد)، ماکروفاژها را برای تولید اکسید نیتریک تحریک میکند. منبع اینترفرون گاما میتواند سلولهای CD4+) T)، سلولهای CD8+) T)، سلولهای کشنده طبیعی، سلولهای B، سلولهای T کشنده طبیعی، مونوسیتها، ماکروفاژها یا سلولهای دندریتیک باشد. سپس اکسید نیتریک از ماکروفاژ آزاد میشود و به دلیل سمی بودن، میکروبهای نزدیک به ماکروفاژ را از بین میبرد. ماکروفاژهای فعال شده فاکتور نکروز تومور را تولید و ترشح میکنند. این سیتوکین (یک کلاس از مولکولهای سیگنالدهنده) سلولهای سرطانی و سلولهای آلوده به ویروسها را میکشد و به فعال شدن سایر سلولهای سیستم ایمنی کمک میکند.
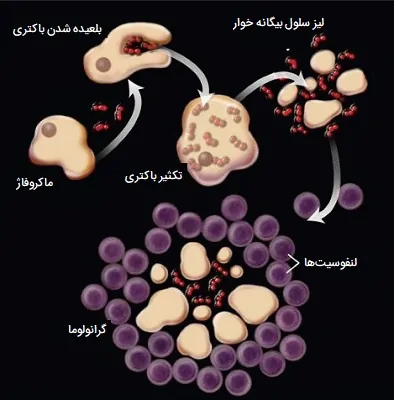
در برخی از بیماریها، به عنوان مثال، بیماری گرانولوماتوز مزمن نادر، کارایی بیگانه خوار ها مختل میشود و عفونتهای باکتریایی مکرر مشکلساز است. در این بیماری یک ناهنجاری وجود دارد که بر عناصر مختلف کشتار وابسته به اکسیژن تأثیر میگذارد. سایر ناهنجاریهای مادرزادی نادر، مانند «سندرم چدیاک هیگاشی» (Chédiak–Higashi syndrome)، نیز با کشتن معیوب میکروبهای بلعیدهشده همراه است.
از بین بردن ویروس ها
ویروسها فقط در داخل سلولها تکثیر میشوند و با استفاده از بسیاری از گیرندههای درگیر در ایمنی وارد میشوند. زمانی که ویروسها وارد سلول میشوند، از ماشینهای بیولوژیکی سلول به نفع خود استفاده میکنند و سلول را مجبور میکنند تا صدها کپی مشابه از ویروس بسازند. اگرچه فاگوسیتها و سایر اجزای سیستم ایمنی ذاتی میتوانند تا حد محدودی ویروسها را کنترل کنند، زمانی که ویروس در داخل سلول قرار گرفت، پاسخهای ایمنی اکتسابی، به ویژه توسط لنفوسیتها، برای دفاع مهمتر هستند. در محلهای عفونت ویروسی، تعداد لنفوسیتها اغلب بسیار بیشتر از سایر سلولهای سیستم ایمنی بوده و در مننژیت ویروسی شایع است. سلولهای آلوده به ویروس که توسط لنفوسیتها کشته شدهاند توسط بیگانه خوار ها از بدن پاک میشوند.
نقش بیگانه خوار ها در آپوپتوز
در جانوران، سلولها به طور مداوم در حال مرگ هستند. تعادل بین تقسیم سلولی و مرگ سلولی تعداد سلولها را در بزرگسالان نسبتاً ثابت نگه میدارد. دو راه مختلف وجود دارد که یک سلول میتواند بمیرد: نکروز یا آپوپتوز. بر خلاف نکروز، که اغلب در نتیجه بیماری یا تروما ایجاد میشود، آپوپتوز یا مرگ برنامهریزی شده سلولی یک عملکرد سالم سلول است. بدن باید هر روز خود را از شر میلیونها سلول مرده یا در حال مرگ خلاص کند و بیگانه خوار ها نقش مهمی در این فرآیند دارند.
سلولهای در حال مرگ که تحت مراحل نهایی آپوپتوز قرار میگیرند مولکولهایی مانند فسفاتیدیل سرین را روی سطح سلول خود برای جذب بیگانه خوار ها به نمایش میگذارند. فسفاتیدیل سرین به طور معمول در سطح سیتوزولی غشای پلاسمایی یافت میشود، اما در طول آپوپتوز توسط پروتئینی به نام اسکرامبلاز به سطح خارج سلولی منتقل میشود. این مولکولها سلول را برای فاگوسیتوز توسط سلولهایی که دارای گیرندههای مناسب مانند ماکروفاژها هستند، مشخص میکنند. حذف سلولهای در حال مرگ توسط بیگانه خوار ها به صورت منظم و بدون ایجاد پاسخ التهابی انجام میشود و عملکرد مهم فاگوسیتها است.
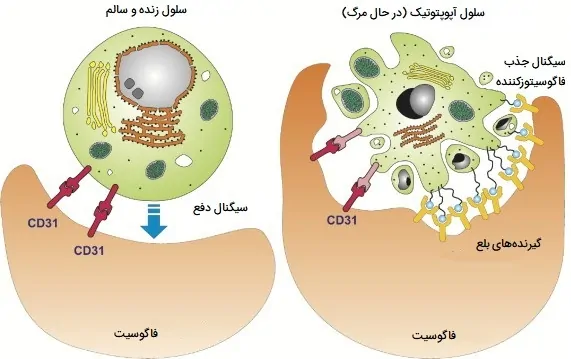
نقش بیگانه خوار ها در ارتباط با سایر سلول ها
بیگانه خوار ها معمولاً به هیچ اندام خاصی متصل نیستند اما در بدن در تعامل با سایر سلولهای فاگوسیتی و غیر فاگوسیتی سیستم ایمنی حرکت میکنند. آنها میتوانند با تولید مواد شیمیایی به نام سیتوکینها با سلولهای دیگر ارتباط برقرار کنند که سایر بیگانه خوار ها را به محل عفونت جذب کرده یا لنفوسیتهای خفته را تحریک میکند. فاگوسیتها بخشی از سیستم ایمنی ذاتی را تشکیل میدهند که جانوران و همچنین انسان، با آن متولد میشوند. سیستم ایمنی ذاتی بسیار موثر اما غیر اختصاصی است زیرا بین انواع مختلف مهاجمان تبعیض قائل نمیشود. از سوی دیگر، سیستم ایمنی اکتسابی مهرهداران آروارهای بسیار تخصصی است و میتواند تقریباً در برابر هر نوع مهاجمی محافظت کند.
سیستم ایمنی اکتسابی به بیگانه خوار ها وابسته نیست، بلکه به لنفوسیتهایی بستگی دارد که پروتئینهای محافظی به نام پادتن (آنتیبادی) تولید میکنند که مهاجمان را برای تخریب برچسبگذاری میکنند و از آلوده کردن سلولها توسط ویروسها جلوگیری میکنند. فاگوسیتها، بهویژه سلولهای دندریتیک و ماکروفاژها، لنفوسیتها را برای تولید آنتیبادی با فرآیند مهمی به نام «ارائه آنتیژن» (antigen presentation) تحریک میکنند.
ارائه آنتی ژن توسط بیگانه خوار ها چگونه است؟
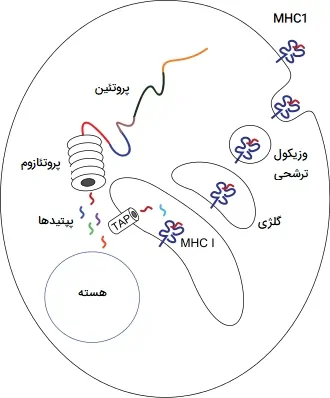
ارائه آنتی ژن فرآیندی است که در آن برخی بیگانه خوار ها بخشهایی از مواد بلعیده شده را به سطح سلولهای خود برمیگردانند و آنها را به سایر سلولهای سیستم ایمنی ارائه میکنند. دو سلول تخصصی ارائهدهنده آنتی ژن وجود دارد: ماکروفاژها و سلولهای دندریتیک. پروتئینهای خارجی (آنتیژنها) پس از بلعیده شدن، در داخل سلولهای دندریتیک و ماکروفاژها به پپتیدها تجزیه میشوند. این پپتیدها سپس به گلیکوپروتئینهای کمپلکس اصلی سازگاری بافتی سلول (MHC) متصل میشوند که پپتیدها را به سطح بیگانه خوار برمیگردانند و در آنجا میتوانند به لنفوسیتها ارائه شوند.
ماکروفاژهای بالغ از محل عفونت دور نمیشوند، اما سلولهای دندریتیک میتوانند به غدد لنفاوی بدن برسند، جایی که میلیونها لنفوسیت وجود دارد. این امر ایمنی را تقویت میکند زیرا لنفوسیتها به آنتیژنهای ارائه شده توسط سلولهای دندریتیک درست همانند پاسخ در محل عفونت اولیه پاسخ میدهند. اما سلولهای دندریتیک همچنین میتوانند لنفوسیتها را در صورت شناسایی اجزای بدن میزبان از بین ببرند یا آرام کنند. این برای جلوگیری از ایجاد واکنشهای خود - ایمنی ضروری است که به این فرآیند «تحمل ایمونولوژیک» (Immunological tolerance) گفته میشود.
تحمل ایمونولوژیک چیست؟
سلولهای دندریتیک همچنین تحمل ایمونولوژیک را تقویت میکنند که بدن را از حمله به سلولهای خودی باز میدارد. اولین نوع تحمل ایمنی بدن، «تحمل مرکزی» (central tolerance) است که در تیموس رخ میدهد، در آنجا سلولهای T که (از طریق گیرنده سلول T خود) به آنتی ژن خود که توسط سلولهای دندریتیک روی مولکولهای MHC ارائه میشوند متصل شده و سلول بیگانه را به شدت به مرگ وادار میکنند. نوع دوم تحمل ایمونولوژیک، «تحمل محیطی» (peripheral tolerance) است که در آن برخی از سلولهای T خود واکنشی به دلایلی از تیموس فرار میکنند که عمدتاً به دلیل عدم بیان برخی آنتیژنهای خود در تیموس است. نوع دیگری از سلول T، سلولهای تنظیمکننده T میتوانند سلولهای T خود واکنشگر را در محیط اطراف تنظیم کنند. هنگامی که تحمل ایمونولوژیک با شکست مواجه میشود، بیماریهای خودایمنی میتوانند به دنبال آن رخ دهند.
گیرنده های سلولی درگیر در فاگوسیتوز
همانطور که گفته شد فاگوسیتوز فرآیندی است که در آن یک سلول به آیتمی که میخواهد روی سطح سلول ببلعد متصل میشود و در حالی که اطراف آن را میگیرد، آن را به سمت داخل میکشد. فرآیند بیگانه خواری اغلب زمانی اتفاق میافتد که سلول تلاش میکند چیزی مانند یک ویروس یا یک سلول آلوده را از بین ببرد و اغلب توسط سلولهای سیستم ایمنی رخ میدهد.
فاگوسیتوز با سایر روشهای اندوسیتوز متفاوت است، زیرا بسیار خاص است و بستگی به این دارد که سلول بتواند از طریق گیرندههای سطح سلولی به مادهای که میخواهد ببلعد بپیوندد. فاگوسیتوز اتفاق نمیافتد مگر اینکه سلول در تماس فیزیکی با ذرهای باشد که قصد بلعیدن آن را دارد. گیرندههای سطح سلولی که برای فاگوسیتوز استفاده میشوند بستگی به نوع سلولی دارد که بیگانه خواری را انجام میدهد. در ادامه آنها را بررسی کردهایم.
گیرنده های اپسونین
گیرندههای اپسونین برای اتصال باکتریها یا سایر ذرات که توسط سیستم ایمنی با آنتیبادیهای ایمونوگلوبولین G (یا IgG) پوشانده شدهاند استفاده میشود. سیستم ایمنی تهدیدات بالقوه را در پوششی از پادتنها قرار میدهد تا سایر سلولها بدانند که چه سلولهایی باید از بین بروند. سیستم ایمنی همچنین میتواند از چیزی به نام «سیستم مکمل» (complement system) استفاده کند که گروهی از پروتئینها است که برای برچسب زدن باکتریها استفاده میشود. سیستم مکمل راه دیگری برای سیستم ایمنی جهت از بین بردن پاتوژنها و تهدیدات میزبان است.
گیرنده های لاشه خوار
گیرندههای لاشه خوار به مولکولهایی که توسط باکتریها تولید میشوند متصل میشوند. بیشتر باکتریها و سایر گونههای سلولی، ماتریکسی از پروتئینهای اطراف خود را به نام ماتریکس خارج سلولی تولید میکنند. این ماتریکس یک راه عالی برای سیستم ایمنی جهت شناسایی ذرات خارجی در بدن است، زیرا سلولهای انسانی ماتریکس پروتئین مشابهی را تولید نمیکنند.
گیرنده های Toll-like
گیرندههای Toll-like، که از یک گیرنده مشابه در مگسهای میوه که توسط ژن Toll رمزگذاری شده است نام گرفتهاند و به مولکولهای خاصی که توسط باکتریها تولید میشوند، متصل میشوند. گیرندههای Toll-like بخش مهمی از سیستم ایمنی ذاتی هستند زیرا پس از اتصال به یک پاتوژن باکتریایی، باکتریهای خاص را شناسایی کرده و پاسخ ایمنی را فعال میکنند. انواع مختلفی از گیرندههای Toll-like تولید شده توسط بدن وجود دارد که همگی مولکولهای مختلفی را به هم متصل میکنند.
پادتن ها
برخی از سلولهای ایمنی آنتیبادیهایی (پادتنهایی) می سازند که میتوانند به آنتیژنهای خاص متصل شوند. این فرآیندی مشابه نحوه تشخیص و شناسایی نوع باکتری میزبان توسط گیرندههای Toll-like است. آنتیژنها مولکولهایی هستند که مانند یک «کارت تماس» پاتوژن عمل میکنند، زیرا به سیستم ایمنی کمک میکنند تا بداند با چه تهدیدی باید مبارزه کند.
سلول های بیگانه خوار و سیستم رتیکولواندوتلیال
سیستم رتیکولواندوتلیال (The Reticuloendothelial System) که به اختصار RES نیز گفته میشود، یک جمعیت ناهمگن از سلولهای فاگوسیتوز در بافتهای ثابت سیستمیک است که نقش مهمی در پاکسازی ذرات و مواد محلول در گردش خون و بافتها دارد و بخشی از سیستم ایمنی را تشکیل میدهد. موادی که پاک میشوند عبارتند از کمپلکسهای ایمنی، باکتریها، سموم و آنتیژنهای اگزوژن (بیرونی). RES شامل سلولهای بیگانه خواری است که در بافت همبند مشبک، عمدتاً مونوسیتها و ماکروفاژها قرار دارند. از آنجایی که فاگوسیتوز نقش اصلی آنها است، «سیستم بیگانه خواری تکهستهای» (Mononuclear Phagocytic System) یا MPS به عنوان نام جایگزین پیشنهاد شده است.
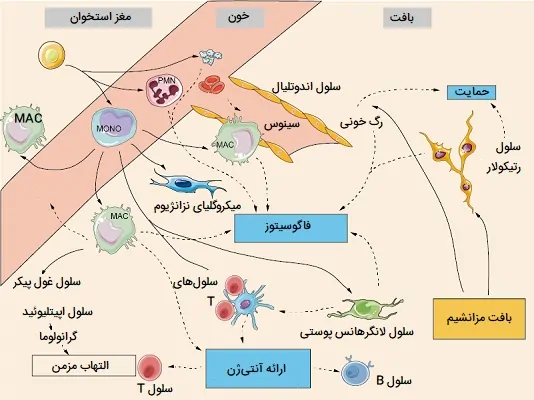
تمایز اساسی بین آن سلولهای فاگوسیتی که از مغز استخوان مشتق شدهاند (آبی در شکل زیر) و سلولهای اندوتلیال و شبکهای که به صورت محلی از خود بافتها تشکیل شدهاند (زرد) وجود دارد. سلولهای رتیکولار و اندوتلیال چندان بیگانه خوار نیستند و عملکرد آنها تا حدی ساختاری بوده و به ترتیب در حفظ یکپارچگی بافت لنفاوی و عروق خونی نقش دارند. سلولهای MPS اکنون بهعنوان موارد اصلی برای فاز «تشخیص» و «پاکسازی» پاسخ ایمنی اکتسابی شناخته میشوند.
ماکروفاژها و سلولهای دندریتیک بهعنوان نگهبانهای بافتی عمل میکنند و به عفونت و آسیب بافتی از طریق گیرندههای ذاتی پاسخ میدهند و از طریق ارائه آنتیژن و آزادسازی سیتوکینهای قدرتمند، زنگ خطر را برای ایمنی اکتسابی سیگنال میدهند. هنگامی که یک پاسخ ایمنی اختصاصی ایجاد شد، یکی از نقشهای اصلی آنتیبادی ترویج و تقویت فاگوسیتوز است، در حالی که لنفوسیتهای T برای فعال کردن فعالیت میکروبکشی ماکروفاژها عمل میکنند. در ادامه وظایف انواع سلولها و بخشهای مختلف سیستم رتیکولواندوتلیال را بررسی میکنیم.
- سلول اندوتلیال: پوشش داخلی رگهای خونی، قادر به جذب رنگ و غیره است، اما واقعا بیگانه خوار نیست. سلولهای اندوتلیال عبور لکوسیتها را از خون به بافتها هدایت میکنند و میتوانند به جای ماکروفاژها، سیتوکینها را تولید کنند و به آنها پاسخ دهند. آنها همچنین میتوانند تحت برخی شرایط آنتیژن را مستقیماً به سلولهای T ارائه دهند.
- سلول رتیکولار: سلول پشتیبان یا استرومایی اصلی اندامهای لنفاوی که معمولاً با رشتههای رتیکولین کلاژن مانند مرتبط است و به راحتی از فیبروبلاستها یا سایر سلولهای شاخه دار یا دندریتیک تشخیص داده نمیشود، به همین دلیل سردرگمی زیادی وجود دارد.
- مزانژیوم: سلولهای مزانژیال ماکروفاژهای تخصصی هستند که در کلیه یافت میشوند، جایی که مواد رسوبشده در آن، بهویژه کمپلکسهای آنتیژن و آنتیبادی را فاگوسیتوز میکنند.
- استئوکلاست: یک ماکروفاژ بزرگ چند هستهای که مسئول جذب و شکل دادن به استخوان و غضروف است. این توسط سیتوکینهایی مانند TNF-α و IL-1 تنظیم شده و تصور میشود که در بیماریهای دژنراتیو مفاصل مانند آرتریت روماتوئید نقش دارد.
- سلولهای دندریتیک: سلول لانگرهانس با فاگوسیت ضعیف اپیدرم و سلولهای تا حدودی مشابه در بافتهای دیگر از طریق عروق لنفاوی یا خون به غدد لنفاوی و طحال (جایی که آنها عوامل اصلی تحریک سلولهای T هستند) مهاجرت میکنند. سلولهای T آنتیژنهای خارجی را در ارتباط با آنتیژنهای سطح سلولی که توسط MHC کدگذاری شدهاند، شناسایی میکنند، منطقهای ژنتیکی که مستقیماً در انواع پاسخهای ایمنی درگیر است. پیشساز سلول دندریتیک از مغز استخوان میآید. سلولهای دندریتیک فولیکولی جداگانهای برای ارائه آنتیژن به سلولهای B وجود دارد که در به دام انداختن کمپلکسهای آنتیژن - آنتیبادی تخصص دارند. آنها در نواحی سلولهای B بافت لنفاوی یافت میشوند، اما یکی از معدود سلولهای سیستم ایمنی هستند که از مغز استخوان مشتق نشدهاند و منشا فیبروبلاست دارند.
- سلولهای کوپفر: ماکروفاژهای تخصصی که در کبد یافت میشوند و گلبولهای قرمز در حال مرگ یا آسیبدیده و سایر مواد را از گردش خون خارج میکنند. آنها بخش عمدهای از سلولهای بیگانه خوار بدن را تشکیل میدهند.
- لنفوسیتهای T و B: اغلب در تماس نزدیک با سلولهای دندریتیک یافت میشوند. این احتمالاً جایی است که ارائه آنتیژن و همکاری سلولهای T - B انجام میشود.
- سلولهای بنیادی: سلولهای بنیادی مغز استخوان که همه سلولهای موجود در خون را ایجاد میکنند.
- پلاکتهای خون: اگرچه عمدتاً در لخته شدن نقش دارند، اما میتوانند کمپلکسهای آنتیژن - آنتیبادی را فاگوسیتوز کنند و همچنین میتوانند برخی از سیتوکینها مانند فاکتور رشد بتا (TGF-β) ترشح کنند.
- RBC: کمپلکسهای آنتیژن - آنتی بادی که دارای کمپلمان متصل هستند میتوانند از طریق گیرنده CR1 به گلبولهای قرمز خون متصل شوند که سپس گلبول قرمز این کمپلکسها را برای حذف توسط ماکروفاژها به کبد منتقل میکند.
- PMN (Polymorphonuclear leucocyte): لکوسیت پلیمورفونوکلئر، سلول فاگوسیتیک اصلی خون است، با این حال، به طور معمول به عنوان بخشی از سیستم بیگانه خواری تکهستهای در نظر گرفته نمیشود.
- MONO: مونوسیتی که در مغز استخوان تشکیل میشود و از طریق خون به بافتها میرود و در آنجا به یک ماکروفاژ بالغ میشود. برخی از مونوسیتها در سطح رگهای خونی گشت میزنند، احتمالاً در ترمیم محلهای آسیب یا عفونت نقش دارند.
- MAC: ماکروفاژ، فاگوسیت بافتی ساکن و با عمر طولانی هستند. ماکروفاژها ممکن است در بافتها آزاد باشند یا در دیوارههای سینوسهای خون ثابت باشند، جایی که خون را برای ذرات، گلبولهای قرمز و غیره کنترل میکنند. ماکروفاژها در آلوئولهای ریه (ماکروفاژهای آلوئولی) مسئول حفظ این کیسههای هوای حیاتی از ذرات و میکروبها هستند. ماکروفاژها (و پلیمورفها) این توانایی ارزشمند را دارند که نه تنها ماده خارجی، بلکه آنتیبادی یا مکمل متصل به آن را نیز تشخیص دهند، که فاگوسیتوز را بسیار افزایش میدهد. علیرغم نقش مهم آنها در دفاع میزبان، فعال شدن بیش از حد ماکروفاژها و به ویژه توانایی آنها در تولید سطوح بالایی از واسطههای اکسیژن فعال و سیتوکین التهابی TNF-α به طور فزایندهای به عنوان نقش مهمی در طیف گستردهای از شرایط التهابی مزمن، از جمله بیماریهای رایج مانند آرتریت روماتوئید، پسوریازیس، بیماری آلزایمر و تصلب شرایین شناخته میشود.
- سمیت سلولی با واسطه آنتیبادی (ADCC): مونوسیتها، ماکروفاژها و گرانولوسیتها میتوانند سلولهای هدف را با فرآیندی شبیه به سلولهای T سیتوتوکسیک CD8 بکشند، اما با واسطهی یک برهمکنش با واسطه آنتیبادی (ADCC) انجام میشود.
- سینوس: کانالهای پرپیچ و خم در کبد، طحال و غیره که خون از طریق آن به وریدها میرسد و به ماکروفاژهای پوششی اجازه میدهد تا سلولهای آسیبدیده یا پوشیده شده با آنتیبادی و سایر ذرات را از بین ببرند. این فرآیند به قدری مؤثر است که به عنوان مثال، یک تزریق بزرگ ذرات کربن را میتوان در عرض چند دقیقه از خون خارج کرد و کبد و طحال را به وضوح سیاه کند.
- میکروگلیا: سلولهای بیگانه خوار مغز که در آسیب بافتی منجر به بیماری آلزایمر و مولتیپل اسکلروزیس نقش دارند. برخلاف سایر ماکروفاژهای بافتی، میکروگلیا ممکن است از یک سلول پیشساز ویژهای مشتق شود که قبل از تولد وارد مغز شده و در داخل مغز تقسیم میشود.
- لیزوزیم: آنزیم مهم ضد باکتریایی است که توسط ماکروفاژها در خون ترشح میشود. ماکروفاژها همچنین سایر عوامل هومورال ذاتی مانند اینترفرون و بسیاری از اجزای مکمل، عوامل سیتوتوکسیک و غیره را تولید میکنند.
- سلول غول پیکر، سلول اپیتلیوئید: سلولهای مشتق از ماکروفاژها معمولا در محلهای التهاب مزمن یافت میشوند. با ادغام در یک توده جامد یا گرانولوم، آنها را موضعی کرده و مواد محرک یا غیرقابل هضم را جدا میکنند. با این حال، گرانولومها با انسداد راههای هوایی و ایجاد خونریزی داخلی، نقش عمدهای در بیماری (مثلاً سل) دارند.